一种合成三氟乙氧基烯碘类化合物的方法
(一)技术领域
[0001]
本发明涉及一种合成三氟乙氧基烯碘类化合物的方法。
(二)
背景技术:[0002]
乙烯类化合物广泛存在于大自然界,是一种重要的工业原料,是合成纤维,合成橡胶,合成塑料,合成乙醇的基本化工原料,也用于制造氯乙烯、苯乙烯、环氧乙烷、醋酸、乙醛、乙醇和炸药等。乙烯的生产量是衡量一个国家石油化工发展水平的重要标志。官能化的烯烃在有机合成方面有着巨大的应用,通过预先引入特殊官能团,实现预官能化,从而实现产物的官能团修饰。而含氟化合物由于氟原子的引入,会极大的改变化合物的空间性,电性,亲脂性,因此含氟类的化合物在制药、兽医、农药化学和材料化学科学中发挥着至关重要的作用。所以在药物的研发过程中,药物研究者常常会引入一个或者多个氟原子,从而改善药物的活性。也正因为氟元素的独特性,使得科研工作者致力于研究含氟类化合物,掀起了研究有机氟化物的狂潮。而本发明所合成的化合物通过一个简单的方法,将溶剂三氟乙醇引入产物,实现了烯烃的双官能化,可以为后续的研究实现预官能化,同时改变烯烃的电性,有利于活化烯烃的活性。与此同时,在引入三氟乙氧基的同时还成功实现了炔烃的烯碘化。碘元素在有机合成有着重要的应用意义,相比其他卤素,碘的活性更强,能够在更加温和的条件下完成各种经典的c-c键、c-n键偶联。因此向炔烃类化合物中引入碘与三氟乙氧基有着重要的作用,以及合成此类化合物是非常有工业发展意义的。
[0003]
目前,对于炔烃的烯碘化报道比较多,但是在引入碘元素的同时又引入一个具有生物活性的三氟乙氧基的方法到目前为止尚未有人报道过。本发明采用2-腈基二苯乙炔类化合物为底物,以单质碘作为碘源,硝酸银为添加剂,三氟乙醇为溶剂,在50℃温和条件下实现了炔烃的双官能化,成功引入碘元素与三氟乙氧基,得到三氟乙氧基烯碘类化合物。该发明所提及的条件温和,原子经济性高,操作简单,有着非常大的应用前景。
(三)
技术实现要素:[0004]
针对现有技术的不足,本发明提供了一种通用、简便、高效的合成三氟乙氧基烯碘类化合物的方法。
[0005]
本发明的技术方案如下:
[0006]
一种合成三氟乙氧基烯碘类化合物的方法,所述方法为:
[0007]
将底物(i)、碘源、添加剂、溶剂三氟乙醇混合,于30~70℃(优选50℃)下反应2~5h(优选3h),之后反应液经后处理,得到三氟乙氧基烯碘类化合物(ii);
[0008]
所述底物(i)、碘源、添加剂的物质的量之比为1:1~3:0.5~1.5,优选1:2:1;
[0009]
所述溶剂三氟乙醇的体积用量以底物(i)的物质的量计为10~20ml/mmol;
[0010]
所述碘源为碘、n-碘代丁二酰亚胺、i2o5中的一种或两种以上任意比例的混合物;
[0011]
所述添加剂为硝酸银、亚硝酸银、碳酸银中的一种或两种以上任意比例的混合物;
[0012]
所述后处理的方法为:反应结束后,反应液中加入柱层析硅胶(100~200目),减压
蒸除溶剂,进行柱色谱分离,以石油醚与乙酸乙酯体积比5:1的混合液作为洗脱剂洗脱,收集含目标产物的洗脱液,蒸除溶剂并干燥,得到三氟乙氧基烯碘类化合物(ii);
[0013]
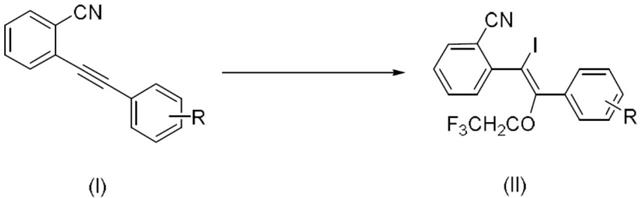
反应式如下:
[0014][0015]
式(i)或式(ii)中,r为氢、叔丁基、溴、氯、三氟甲基、甲氧基或甲酸甲酯基。
[0016]
具体的,优选本发明所述三氟乙氧基烯碘类化合物(ii)为下列化合物之一:
[0017][0018]
与现有技术相比,本发明的有益效果是:
[0019]
(1)安全环保,不产生废气,操作危险性低;
[0020]
(2)底物适应性好,各种取代基都可以实现双官能化;
[0021]
(3)反应条件温和;
[0022]
(4)该反应具有一定的创新性,原子经济性高,更加符合现代绿色化学的理念。
(四)具体实施方式
[0023]
下面结合具体实施例对本发明作进一步详细说明,但本发明的保护范围不限于此:
[0024]
实施例1
[0025][0026]
(e)-2-(1-iodo-2-phenyl-2-(2,2,2-trifluoroethoxy)vinyl)benzonitrile
[0027]
将2-(苯基乙炔基)苄腈(0.3mmol,0.0609g)、碘(0.6mmol,0.1524g)、硝酸银(0.3mmol,0.0507g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在50℃条件下反应3h,反应结束后,在反应液中加入两药匙(0.5g)柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率87%。
[0028]
表征数据:1h nmr(500mhz,cdcl3)δ7.47-7.43(m,2h),7.38-7.36(m,1h),7.30-7.18(m,6h),4.09-3.96(m,2h).
13
c nmr(125mhz,cdcl3)δ157.80,144.34,132.90,132.57,131.70,130.10,129.81,129.67,128.65,128.19,123.04(q,j=277.5hz),117.15,113.20,75.31,66.07(q,j=35hz).
[0029]
实施例2
[0030][0031]
(e)-2-(2-(3-bromophenyl)-1-iodo-2-(2,2,2-trifluoroethoxy)vinyl)benzonitrile
[0032]
将2-((3-溴苯基)乙炔基)苄腈(0.3mmol,0.0843g)、n-碘代丁二酰亚胺(0.6mmol,0.135g)、硝酸银(0.3mmol,0.0507g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在50℃条件下反应3h,反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率57%。
[0033]
表征数据:1h nmr(500mhz,cdcl3)δ7.51-7.48(m,2h),7.43-7.37(m,2h),7.32-7.27(m,2h),7.16-7.11(m,2h),4.13-3.97(m,2h).
13
c nmr(126mhz,cdcl3)δ156.15,143.84,133.03,132.93,132.75,132.37,132.18,131.51,130.17,128.54,128.21,122.92(q,j=277.5hz),122.59,116.98,113.03,77.20,66.27(q,j=35hz).
[0034]
实施例3
[0035][0036]
(e)-2-(2-(3-chlorophenyl)-1-iodo-2-(2,2,2-trifluoroethoxy)vinyl)benzonitrile
[0037]
将2-((3-氯苯基)乙炔基)苄腈(0.3mmol,0.0711g)、i2o5(0.6mmol,0.2004g)、硝酸银(0.3mmol,0.0507g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在50℃条件下反应3h,反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率82%。
[0038]
表征数据:1h nmr(500mhz,cdcl3)δ7.51-7.47(m,2h),7.39-7.37(m,1h),7.30-7.25(m,2h),7.20-7.16(m,2h),7.11-7.09(m,1h),4.13-3.97(m,2h).
13
c nmr(125mhz,
cdcl3)δ156.26,143.88,134.66,133.05,132.75,131.98,131.52,130.04,129.96,129.49,128.54,127.80,122.93(q,j=277.5hz),116.99,113.05,77.13,66.27(q,j=35hz).
[0039]
实施例4
[0040][0041]
(e)-2-(1-iodo-2-(4-methoxyphenyl)-2-(2,2,2-trifluoroethoxy)vinyl)benzonitrile
[0042]
将2-((4-甲氧基苯基)乙炔基)苄腈(0.3mmol,0.0699g)、碘(0.3mmol,0.0762g)、硝酸银(0.3mmol,0.0507g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在50℃条件下反应3h,反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率67%。
[0043]
表征数据:1h nmr(500mhz,cdcl3)δ7.53(d,j=2hz,1h),7.52-7.49(m,2h),7.41-7.39(m,1h),7.30-7.26(m,1h),7.20(dd,j1=8.5hz,j2=2.5hz,1h),6.67(d,j=9hz,1h),4.13-3.96(m,2h),3.84(s,3h).
13
c nmr(125mhz,cdcl3)δ159.01,156.15,144.27,140.67,133.07,132.74,131.72,131.14,128.33,124.02,123.03(q,j=277.5hz),117.14,113.08,110.48,85.70,75.60,66.16(q,j=35hz),56.38
[0044]
实施例5
[0045][0046]
(e)-2-(2-(2,3-dichlorophenyl)-1-iodo-2-(2,2,2-trifluoroethoxy)vinyl)benzonitrile
[0047]
将2-((2,3-二氯苯基)乙炔基)苄腈(0.3mmol,0.081g)、碘(0.9mmol,0.2286g)、硝酸银(0.3mmol,0.0507g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在50℃条件下反应3h,反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率82%。
[0048]
表征数据:1h nmr(500mhz,cdcl3)δ7.69(d,j=8hz,1h),7.66-7.62(m,2h),7.56-7.51(m,2h),7.43-7.39(m,2h),3.91(s,2h).
13
c nmr(126mhz,cdcl3)δ152.55,143.12,135.33,134.20,132.80,132.63,132.46,130.83,130.76,128.54,128.15,122.72(q,j=277.5hz),117.79,112.12,66.44(q,j=35hz).
[0049]
实施例6
[0050][0051]
(e)-2-(2-(4-(tert-butyl)phenyl)-1-iodo-2-(2,2,2-trifluoroethoxy)vinyl)benzonitrile
[0052]
将2-((4-叔丁基苯基)乙炔基)苄腈(0.3mmol,0.0777g)、碘(0.6mmol,0.1524g)、亚硝酸银(0.3mmol,0.0459g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在50℃条件下反应3h,反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率77%。
[0053]
表征数据:1h nmr(500mhz,cdcl3)δ7.54-7.43(m,2h),7.37-7.35(m,1h),7.26-7.23(m,3h),7.16-7.04(m,2h),4.09-3.99(m,2h),1.25(s,9h).
13
c nmr(125mhz,cdcl3)δ157.91,153.10,144.64,132.96,132.55,131.72,129.39,128.11,127.06,125.59,123.15(q,j=277.5hz),117.25,113.40,74.96,66.16(q,j=35hz),34.77,31.05.
[0054]
实施例7
[0055][0056]
(e)-2-(1-iodo-2-(2,2,2-trifluoroethoxy)-2-(4-(trifluoromethyl)phenyl)vinyl)benzonitrile
[0057]
将2-((4-三氟甲基苯基)乙炔基)苄腈(0.3mmol,0.0813g)、碘(0.6mmol,0.1524g)、碳酸银(0.3mmol,0.0501g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在50℃条件下反应3h,反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率67%。
[0058]
表征数据:1h nmr(500mhz,cdcl3)δ7.54-7.49(m,4h),7.42-7.40(m,1h),7.34-7.29(m,3h),4.13-3.95(m,2h).
13
c nmr(125mhz,cdcl3)δ156.27,143.79,133.98,133.15,132.85,131.53,130.03,128.72,125.70(q,j=3.75hz),123.48(q,j=271.25hz),122.90(q,j=277.5hz),116.97,113.04,78.19,66.36(q,j=36.25).
[0059]
实施例8
[0060][0061]
methyl(e)-4-(2-(2-cyanophenyl)-2-iodo-1-(2,2,2-trifluoroethoxy)vinyl)benzoate
[0062]
将4-((2-氰基苯基)乙炔基)苯甲酸甲酯(0.3mmol,0.0783g)、碘(0.6mmol,
0.1524g)、硝酸银(0.15mmol,0.0254g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在50℃条件下反应3h,反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率58%。
[0063]
表征数据:1h nmr(500mhz,cdcl3)δ7.91-7.89(m,2h),7.49-7.46(m,2h),7.39-7.37(m,1h),7.28-7.25(m,3h),4.11-3.97(m,2h),3.89(s,3h).
13
c nmr(126mhz,cdcl3)δ166.06,156.78,143.92,134.67,133.07,132.74,131.59,129.81,129.67,128.56,122.93(q,j=277.5hz),116.99,113.08,77.61,66.32(q,j=36.25hz),52.35.
[0064]
实施例9
[0065][0066]
(e)-2-(1-iodo-2-phenyl-2-(2,2,2-trifluoroethoxy)vinyl)benzonitrile
[0067]
将2-(苯基乙炔基)苄腈(0.3mmol,0.0609g)、碘(0.6mmol,0.1524g)、硝酸银(0.45mmol,0.0762g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在50℃条件下反应3h,反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率80%。
[0068]
表征数据:1h nmr(500mhz,cdcl3)δ7.47-7.43(m,2h),7.38-7.36(m,1h),7.30-7.18(m,6h),4.09-3.96(m,2h).
13
c nmr(125mhz,cdcl3)δ157.80,144.34,132.90,132.57,131.70,130.10,129.81,129.67,128.65,128.19,123.04(q,j=277.5hz),117.15,113.20,75.31,66.07(q,j=35hz).
[0069]
实施例10
[0070][0071]
(e)-2-(2-(3-bromophenyl)-1-iodo-2-(2,2,2-trifluoroethoxy)vinyl)benzonitrile
[0072]
将2-((3-溴苯基)乙炔基)苄腈(0.3mmol,0.0843g)、碘(0.6mmol,0.1524g)、硝酸银(0.3mmol,0.0508g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在30℃条件下反应3h,反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率61%。
[0073]
表征数据:1h nmr(500mhz,cdcl3)δ7.51-7.48(m,2h),7.43-7.37(m,2h),7.32-7.27(m,2h),7.16-7.11(m,2h),4.13-3.97(m,2h).
13
c nmr(126mhz,cdcl3)δ156.15,143.84,133.03,132.93,132.75,132.37,132.18,131.51,130.17,128.54,128.21,122.92(q,j=277.5hz),122.59,116.98,113.03,77.20,66.27(q,j=35hz).
[0074]
实施例11
[0075][0076]
(e)-2-(2-(3-chlorophenyl)-1-iodo-2-(2,2,2-trifluoroethoxy)vinyl)benzonitrile
[0077]
将2-((3-氯苯基)乙炔基)苄腈(0.3mmol,0.0711g)、碘(0.6mmol,0.1524g)、硝酸银(0.3mmol,0.0508g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在70℃条件下反应3h,反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率78%。
[0078]
表征数据:1h nmr(500mhz,cdcl3)δ7.51-7.47(m,2h),7.39-7.37(m,1h),7.30-7.25(m,2h),7.20-7.16(m,2h),7.11-7.09(m,1h),4.13-3.97(m,2h).
13
c nmr(125mhz,cdcl3)δ156.26,143.88,134.66,133.05,132.75,131.98,131.52,130.04,129.96,129.49,128.54,127.80,122.93(q,j=277.5hz),116.99,113.05,77.13,66.27(q,j=35hz).
[0079]
实施例12
[0080][0081]
(e)-2-(1-iodo-2-(4-methoxyphenyl)-2-(2,2,2-trifluoroethoxy)vinyl)benzonitrile
[0082]
将2-((4-甲氧基苯基)乙炔基)苄腈(0.3mmol,0.0699g)、碘(0.6mmol,0.1524g)、硝酸银(0.3mmol,0.0508g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在50℃条件下反应2h,反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率75%。
[0083]
表征数据:1h nmr(500mhz,cdcl3)δ7.53(d,j=2hz,1h),7.52-7.49(m,2h),7.41-7.39(m,1h),7.30-7.26(m,1h),7.20(dd,j1=8.5hz,j2=2.5hz,1h),6.67(d,j=9hz,1h),4.13-3.96(m,2h),3.84(s,3h).
13
c nmr(125mhz,cdcl3)δ159.01,156.15,144.27,140.67,133.07,132.74,131.72,131.14,128.33,124.02,123.03(q,j=277.5hz),117.14,113.08,110.48,85.70,75.60,66.16(q,j=35hz),56.38.
[0084]
实施例13
[0085][0086]
(e)-2-(2-(2,3-dichlorophenyl)-1-iodo-2-(2,2,2-trifluoroethoxy)vinyl)
benzonitrile
[0087]
将2-((2,3-二氯苯基)乙炔基)苄腈(0.3mmol,0.0813g)、碘(0.6mmol,0.1524g)、硝酸银(0.3mmol,0.0508g)加入到15ml封管反应管中,再加入3ml三氟乙醇作溶剂。接着,在50℃条件下反应5h,反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示的产物纯品(以石油醚/乙酸乙酯=5:1作为洗脱剂)。该物质为白色固体,产率86%。
[0088]
表征数据:1h nmr(500mhz,cdcl3)δ7.69(d,j=8hz,1h),7.66-7.62(m,2h),7.56-7.51(m,2h),7.43-7.39(m,2h),3.91(s,2h).
13
c nmr(126mhz,cdcl3)δ152.55,143.12,135.33,134.20,132.80,132.63,132.46,130.83,130.76,128.54,128.15,122.72(q,j=277.5hz),117.79,112.12,66.44(q,j=35hz).
[0089]
同时本发明合成的烯碘类化合物具有如下的应用,其中3a类化合物还是合成克罗米芬(clomid)类药物的中间体。
[0090][0091]
通式步骤:将本发明合成的三氟乙氧基烯碘类化合物(0.5mmol)和四三苯基膦钯(0.025mmol,0.0289g),加入到三颈烧瓶中,抽换氮气3次之后,加入干燥的四氢呋喃5ml,然后滴加加入对甲氧基苯基氯化锌(0.75mmol)溶液,然后回流反应12小时。反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到如结构式所示3a的产物纯品(以石油醚/乙酸乙酯=3:1作为洗脱剂)。
[0092]
具体物质的合成例如:
[0093][0094]
将(e)-2-(1-碘-2-苯基-2-(2,2,2-三氟乙氧基)乙烯基)苄腈(0.5mmol,0.214g)和四三苯基膦钯(0.025mmol,0.0289g),加入到三颈烧瓶中,抽换氮气3次之后,加入干燥的四氢呋喃5ml,然后滴加加入对甲氧基苯基氯化锌(0.75mmol)溶液,然后回流反应12小时。反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到目标产物(以石油醚/乙酸乙酯=3:1作为洗脱剂)。
[0095][0096]
将(e)-2-(1-碘-2-(4-甲氧基苯基)-2-(2,2,2-三氟乙氧基)乙烯基)苄腈(0.5mmol,0.229g)和四三苯基膦钯(0.025mmol,0.0289g),加入到三颈烧瓶中,抽换氮气3次之后,加入干燥的四氢呋喃5ml,然后滴加加入对甲氧基苯基氯化锌(0.75mmol)溶液,然后回流反应12小时。反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到目标产物(以石油醚/乙酸乙酯=3:1作为洗脱剂)。
[0097][0098]
将(e)-2-(1-碘-2-(2,2,2-三氟乙氧基)-2-(4-(三氟甲基)苯基)乙烯基)苄腈(0.5mmol,0.248g)和四三苯基膦钯(0.025mmol,0.0289g),加入到三颈烧瓶中,抽换氮气3次之后,加入干燥的四氢呋喃5ml,然后滴加加入对甲氧基苯基氯化锌(0.75mmol)溶液,然后回流反应12小时。反应结束后,在反应液中加入两药匙柱层析硅胶(100-200目),并通过减压蒸馏除去溶剂,再通过柱色谱分离得到目标产物(以石油醚/乙酸乙酯=3:1作为洗脱剂)。