空气净化器病毒去除率的检测方法与流程
本发明涉及空气净化领域。更具体地说,本发明涉及一种空气净化器病毒去除率的检测方法。
背景技术:
2015年9月15日,gb/t18801-2015《空气净化器》国家标准正式公布。新标准于2016年3月1日正式实施。新标准明确了空气净化器的基本技术指标(核心参数)是“洁净空气量”(简称cadr值)和“累计净化量”(简称ccm值),即空气净化器产品的“净化能力”和“净化能力的持续性”;将空气净化器的噪声限值由低到高划分为4挡;提升了空气净化器针对不同污染物净化能力的能效水平值,分为合格和高效两个等级。
值得注意的是,我国的《空气净化器》标准重点强调了净化水平,而对特定项目(例如,病毒等)缺少具体的检测方法及参数约束。mers病毒(韩国中东呼吸综合征事件)以及sars病毒(中国流感病毒事件)带来的严重健康影响曾引起人类对空气中病毒的恐慌,因此,对空气净化器的要求不能局限在常规细菌去除,实现室内空气病毒的有效灭活才能真正降低健康风险。
技术实现要素:
本发明的一个目的是解决至少上述问题,并提供至少后面将说明的优点。
本发明还有一个目的是提供一种空气净化器病毒去除率的检测方法,具有检测空气净化器除去室内病毒的效果,以判断空气净化器去除病毒性能的强弱。
为了实现根据本发明的这些目的和其它优点,提供了一种空气净化器病毒去除率的检测方法,包括以下步骤:
步骤一、将乙烯基封口膜封住的病毒培养基、微生物采样器放置在空气净化器的试验舱内,消毒,使试验舱达到背景浓度;
步骤二、采用雾化器向试验舱内注入phi-x174接种液,待phi-x174接种液在试验舱内均匀分布;
步骤三、等待40min,运用微生物采样器取样,运行空气净化器,每间隔10min运用微生物采样器取样1次,共取样2次,将取样的病毒在有氧条件下进行培养,检测,计算病毒去除率。
优选的是,步骤一中所述的病毒为大肠杆菌。
优选的是,步骤一中所述的病毒培养基采用双层平板法制备,放置时含有病毒培养基的一侧向上。
优选的是,步骤二中所述的phi-x174接种液的浓度为5×109pfu/ml。
优选的是,步骤二中phi-x174接种液均匀分布采用搅拌扇转动10min。
优选的是,步骤三中所述的培养温度为35±1℃、培养时间为18±2h。
本发明至少包括以下有益效果:本发明提供一种空气净化器病毒去除率的检测方法,可以检测该空气净化器去除浮游病毒的性能,为筛选更优的空气净化器提供检测标准和方法,使空气净化器有效灭活室内空气病毒,为人们提供更好的生活环境。
本发明的其它优点、目标和特征将部分通过下面的说明体现,部分还将通过对本发明的研究和实践而为本领域的技术人员所理解。
附图说明
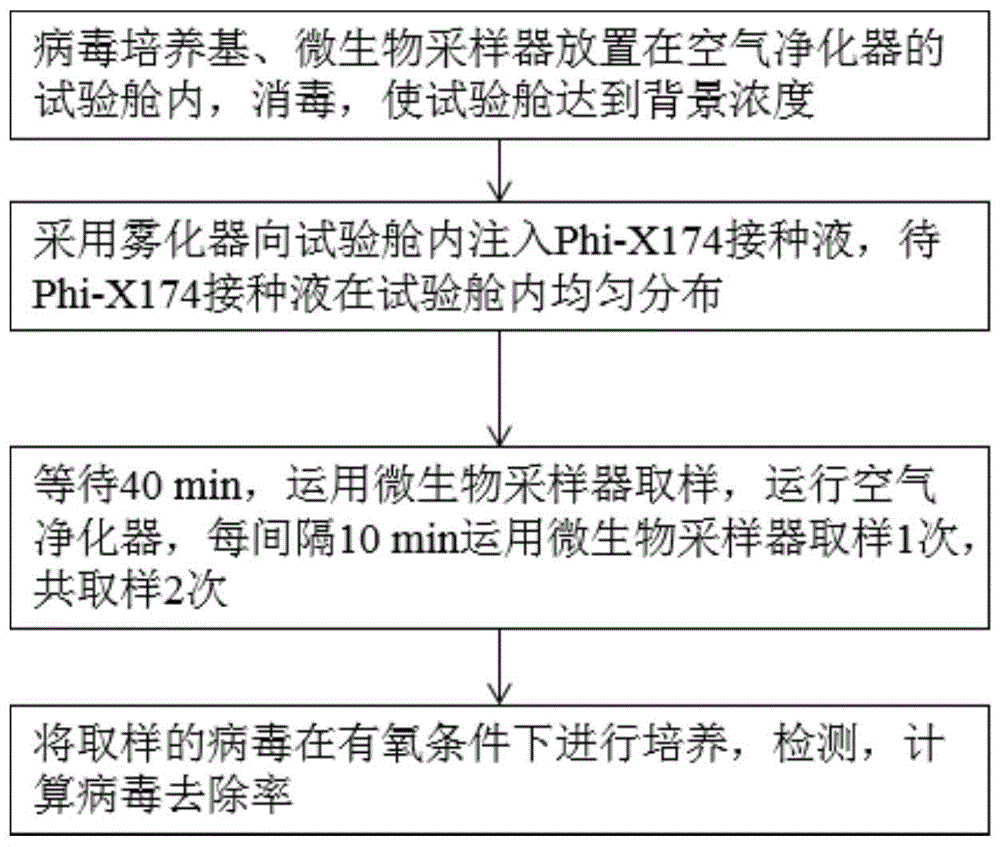
图1为本发明的检测方法的流程示意图;
图2为本发明的测试仪a和测试仪b中病毒自然衰减率;
图3为本发明的浮游病毒(phi-x174)的分布特征;
图4为本发明的病毒自然衰减试验的结果;
图5为本发明的注射病毒后40至60min内病毒的自然衰减率。
具体实施方式
下面结合附图和实施例对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。
需要说明的是,下述实施方案中所述实验方法,如无特殊说明,均为常规方法,所述试剂和材料,如无特殊说明,均可从商业途径获得。
本实施例提供一种空气净化器病毒去除率的检测方法,如图1所示,包括以下步骤:
步骤一、将乙烯基封口膜封住的病毒培养基、微生物采样器放置在空气净化器的试验舱内,微生物采样器为固体撞击式采样器,试验舱参照《gb/t21551.3-2010》和《gb/t18801》设定,空气净化器试验舱体积设定为30m3,试验舱内部的温度和相对湿度分别为23±2℃、湿度为50±5%,消毒,使试验舱达到背景浓度,背景浓度在准备注入测试病毒时测定;
病毒培养基的制备:在试验前应立即制备病毒培养基,为phi-x174生长提供营养物质。将5ml大肠杆菌(e.colic)培养液和5ml上层琼脂混合,然后移到15ml试管中,并确保没有气泡产生,然后倒入5ml下层琼脂,在混合凝固后,倒置,作为病毒培养基;
大肠杆菌(e.colic)培养液的制备:
a)在250ml灭菌的三角瓶中加入10~25mltsb,用接种环接种e.colic,35±1℃、225±25r/min培养12h;
b)将e.colic培养液按1:100的比例接种到100ml的tsb培养基中进行稀释,然后转移到1l三角瓶中,35±1℃、225±25r/min培养12h,得大肠杆菌培养液。
步骤二、将2mlphi-x174接种液采用雾化器向试验舱内注入,运行搅拌扇10min,待phi-x174接种液在试验舱内均匀分布;
phi-x174接种液的制备:
a)将培养的e.colic培养液接种到5~10ml、1.0×(109~1010)pfu/ml的phi-x174中,35±1℃下搅拌1~5h,直到e.colic溶解,吸光度停止减少,表明溶解完成;
b)3000rpm下离心20min,除去e.colic菌体,吸取上清液到无菌的试管,上清液用0.22um的过滤器过滤,取滤液稀释,使其浓度为(5±2)×1010pfu/ml,得phi-x174培养液;
c)用盐溶液将phi-x174培养液10倍稀释,使浓度达到5×109pfu/ml,得phi-x174接种液。
步骤三、步骤二中停止搅拌扇转动后90min内,每10min测量一次自然衰减率,最适起始浓度为100~250pfu,重复测验的结果显示,病毒的浓度在40-60min时最稳定;
因此选择停止搅拌40min后,运用微生物采样器对病毒培养基进行撞击式取样,运行两个撞击器各一次,其中,取样量可根据所注入的病毒的浓度来调节,应至少100l,由于存在无效体积使样本空气的体积存在误差,取样量少于50l将不被记录;
同时运行空气净化器,操作条件:设备运行20min,额定空气流量运行,120cm高度的采样位点,100cm的撞击器距离;
空气净化器运行20min后,也就是搅拌扇停止搅拌60min后,运用微生物采样器每间隔10min进行取样,向两个撞击器中分别加入病毒培养基,运行两个撞击器各一次;
将撞击器中取样的病毒在有氧条件下进行培养,测定菌斑数量,并使用群集数换算表校准,然后计数1m3的pfu值。
计算过程如下:
a)根据初始浓度和最终浓度的平均值,按照如下公式计算自然衰减率bi,以百分比表示;
式中,bi:自然衰减率(%);ci:phi-x174分布稳定i小时候后起始浓度的平均值;ct:在i+20min后phi-x174的最终浓度的平均值。
b)起始浓度的校正值(pfu/m3):
按照如下公式计算起始浓度的校正值sc:
式中,sc:起始浓度的校正值(pfu/m3);bi:自然衰减率(%);pt:设备运行前phi-x174的起始浓度的平均值(pfu/m3)。
c)浮游病毒的去除率(%):
按照如下公式计算浮游病毒的去除率r,用校正的起始浓度平均值(sc)减去最终浓度的平均值,然后除以校正的起始浓度值;
式中,r:浮游病毒的去除率(%);sc:校正的起始浓度平均值(pfu/m3);cf:空气净化器设备运行20min后病毒最终浓度的平均值(pfu/m3)。
d)试验舱的密封性
关于试验舱的密封性,应满足当phi-x174的分布稳定时,自然减少的浓度值在20min后,至少为起始浓度值的80%;
式中:v:试验舱的密封性(%);li:当phi-x174的分布稳定1小时后,phi-x174起始浓度的平均值(pfu/m3);lt:在i+20min后,phi-x174最终浓度的平均值(pfu/m3)。
<试验验证数据及分析>
a)浮游病毒取样方法的对比测试
采用三种微生物取样方法采集浮游病毒,对结果进行对比分析,以验证本标准采用固体撞击法的有效性。固体撞击法、液体撞击发和过滤法三种方法都是在喷洒病毒(phix174)50min钟后,同时启动。在相同条件下取样,发现固体撞击法带来的噬菌斑数量最多,为166pfu,如表1所示。与固体撞击法相比,液体撞击发和过滤法呈现了较小数目的噬菌斑,分别为14pfu和58pfu。以上结果表明:病毒的数量取决于取样的方法。每个培养基中的噬菌斑的数量以固体撞击法最多,其次是液体撞击法和过滤法。固体撞击法的结果是50l的样品以每分钟100l的速度进行了0.5min,液体撞击法是125l的样品以每分钟12.5l的速度进行10min,过滤法是40l的样品以每分钟4l的速度进行了10min。考虑到三种方法取样量和采样时间的差异,因此单位设为培养基的平均噬菌斑数(pfu/培养基)。
表1固体撞击法、液体撞击发和过滤法收集病毒和培养后的培养基噬菌斑数
b)自然衰减率效果和不同测试器的性能分析
进行测试仪a与测试仪b的对比试验,从而验证本标准中检测方法的有效性。在phi-x174病毒喷洒后的40min和60min取样两次,每个测试仪分别重复四次。
空气中病毒自然衰减率结果如表2所示,由表2可知:测试器a的平均自然衰减率是9.50%,低于测试仪b的平均自然衰减率13.07%。测试器a和b的自然衰减率的标准偏差分别是6.27%和4.49%。测试器a的标准偏差略高,如图2所示,图2中n表示自然衰减率(%),a表示菌斑的平均数量,b表示测试仪a的自然衰减率(%),c表示测试仪b的自然衰减率(%)。测试仪a和b在2min内的自然衰减率都低于20%。
为了统计证实两个测试仪的自然衰减率的差异,在假设方差相同的情况下进行了t检验。在0.05显著性水平下的双侧试验结果显示t统计值为2.179。这比2.447的临界值要小。因此,测试仪a和b的对比试验差异不显著。
表2由不同测试器进行病毒取样测试的结果
c)浮游病毒的分布特征
为了确认本标准中试验舱内浮游病毒的分布浓度,进行了不同取样点的比较试验,即试验舱内2个不同位置的病毒浓度进行对比分析。
选取净化完成的2个不同位点的(定义为试验1和2),试验1位于试验舱左侧的撞击器,而试验2定位在右侧。撞击器中的取样培养基位于舱内部的桌面上,保证测试员在试验中不用进入舱内。
注射病毒(phi-x174)10min并运行搅拌风机,分布均匀后,停止搅拌风扇。在等待40min后,取100l的样品,在2个位点用撞击法以10min的间隔测量4次。
在试验1中,平均值和标准差分别为18800pfum3和5302pfu/m3;在试验2中,平均值和标准差分别为16325pfu/m3和5189pfu/m3。两者间平均值的差异为13.16%,标准差的差异为2.13%。结果表明左右两边的病毒的浓度差异不大,进一步证明试验舱内的病毒是均有分布的,结果如图3所示,图3中p表示菌斑形成单位(pfu)每立方米(m3),a表示菌斑总平均数,b表示试验舱左边的菌斑数,c表示试验舱右边的菌斑数。
d)浮游病毒随时间的衰减特征(自然衰减和总衰减测量时间的适用性)
在本标准测试方法中,自然衰减浓度和衰减浓度的测量时间是20min,即病毒注射后的40-60min内。该条件遵循在注入病毒后60min内每间隔10min进行自然减少量的测定试验。图4表明病毒浓度的减少量在注射40min后降低,且病毒浓度稳定,图4中p表示菌斑形成单位(pfu)每立方米(m3),t病毒注入后的时间,单位为min。
为了证实测量时间的有效性,自然衰减率的测定重复6次。病毒注入试验舱后,使用撞击法分别在40min、50min和60min时取样。
试验结果表明在40min和50min间,自然衰减率为8.0%,在50min和60min间为8.1%,在40min和60min间为15.6%,如图5所示,图5中r是自然衰减率(%),a是40-60min的自然衰减率(%),b是40-50min的自然衰减率(%),c是50-60min的的自然衰减率(%)。在所有的情况下自然衰减率少于20%,证明试验舱密封性好。因此,本标准中的测量时间是可行的。
40min和50min的标准方差为4.6%,50min和60min钟的标准方差为3.3%,40min和60min的标准方差最小为2.5%。这意味着此标准方法(40-60min,长20min)中指定的测量时间是有效的。
尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节和这里示出与描述的图例。
- 还没有人留言评论。精彩留言会获得点赞!