一种超声介导丝素蛋白复合胶原水凝胶及其制备方法与流程
本发明涉及水凝胶领域,特别是涉及一种超声介导丝素蛋白复合胶原水凝胶及其制备方法。
背景技术:
水凝胶是由聚合物链形成的,在高分子间空隙保留水分的具有三维网络结构的凝胶。它可以良好模拟细胞外基质的水环境,并为细胞的粘附、增殖和分化提供类似天然外基质的微环境,是组织损伤再生、修复和重建的一种理想材料,因此被广泛应用于生物医学领域,如医用敷料、软骨组织修复、细胞移植、药物递送和组织工程支架等。但目前用于组织修复的水凝胶产品仍面临许多问题,其中力学性能不足及体内降解速率与新生组织再生速率不匹配等问题尤为突出。
胶原蛋白水凝胶属于天然蛋白材料,不仅具有良好的生物相容性和生物降解性,更重要的是具有优异的生物活性,加上其成分与细胞外基质成分相同或同源,所以还具有很多能够被细胞识别和粘附的位点,可为细胞提供了较为接近自然状态的表面。胶原蛋白的纤维自组装能力较强,在适宜的温度和ph条件下易形成凝胶,可以为细胞的粘附、增殖和分化提供优越的微环境。但是因胶原蛋白在提取时容易造成组分不稳定和纯度不高的问题,单纯的胶原水凝胶普遍存在力学性能不足、体内降解时间较短等问题,尤其是胶原水凝胶负载细胞后在培养过程中易产生体积剧烈收缩进而影响细胞的营养供给和生物学行为等,难以满足组织工程快速发展的需求。大量科研工作者致力于通过化学交联改性来提高胶原水凝胶的力学强度并取得了一定效果,但交联剂的引入和残留势必会降低材料的生物相容性和给细胞造成一定的毒副作用,不能同时兼具优异的生物相容性、适宜的机械强度及降解性和特定的细胞和分子响应性等特点。因此,通过直接复合其他高分子材料和物理交联方式将是解决上述瓶颈问题的重要途经。
我国是丝绸大国,蚕丝素蛋白不仅廉价易得,而且安全无毒,素有“纤维皇后”的美誉。研究表明其与胶原蛋白有同等的体内、外生物相容性,另外还兼具力学强度高、可控生物降解和自发或在外界条件促进下(如超声波、ph或交联剂等)向稳定β-sheet结晶构象转变,形成物理交联水凝胶的特性。这些特性能较好的弥补胶原蛋白的不足,为我们设计和制备复合水凝胶材料提供了新的思路。目前,国内外对丝素蛋白的应用研究已从传统的纺织领域快速拓展到细胞工程、组织工程、药物缓释、精准医疗、植入式医疗器械、常温稳定疫苗、3d生物打印等领域,并已取得的一系列的研究成果。当然,作为组织工程支架,单纯丝素蛋白水凝胶虽然具有良好的细胞亲和性,但是其也存在柔韧性差,易脆,结构和性能可调范围较窄等不足之处,极大的限制了其应用范围。
当前,关于超声介导丝素蛋白复合胶原蛋白水凝胶鲜有报道,胶原和丝素蛋白溶液直接混合后极易发生相分离现象仍是困扰科研人员创新的掣肘。因此,如何及时高效整合资源和发挥两种天然蛋白材料的优势,创造出一种高附加值且能有效弥补单纯胶原或丝素蛋白水凝胶不足之处的新型多功能复合水凝胶以便满足我国新材料及相关产业发展特别是生物医药、组织工程等方面巨大需求,这已成为组织工程领域研究的热点和亟待解决的问题。
技术实现要素:
本发明主要解决的技术问题是提供一种超声介导丝素蛋白复合胶原水凝胶,生物相容性和力学性能优异,细胞培养过程中体积收缩变化小。
为解决上述技术问题,本发明采用的一个技术方案是:
提供一种超声介导丝素复合胶原水凝胶,包括丝素蛋白和胶原蛋白;所述超声介导丝素复合胶原水凝胶,所述丝素蛋白的质量体积浓度为0.01%~50%,所述胶原蛋白的质量体积浓度为0.01%~50%;进一步地,所述丝素蛋白:胶原蛋白的质量比为99:1~1:99。
进一步地,所述胶原蛋白为i型胶原蛋白,优选牛源i型胶原蛋白。
在本发明中,所述丝素蛋白是通过桑蚕丝、柞蚕丝、天蚕丝、樟蚕丝、柳蚕丝中的一种或几种经脱胶后得到,但不限于上述蚕丝品种,其它可制备丝素蛋白的蚕丝产品均可适用于本发明。
本发明还提供了上述超声介导丝素复合胶原水凝胶的制备方法,包括如下内容:将丝素蛋白溶液超声处理后与胶原蛋白溶液混合得混合溶液,孵育混合溶液使其凝胶化即得。
进一步地,所述胶原蛋白溶液的质量体积浓度为0.01%~50%。
所述质量体积浓度(w/v)为单位体积(ml)混合物中某组分的质量(g)浓度,即混合物中某组分的质量(g)与混合物体积(ml)的比值。
进一步地,所述胶原蛋白溶液的ph值为3~10。
进一步地,所述丝素蛋白溶液的质量体积浓度为0.01%~50%。
进一步地,所述丝素蛋白溶液的ph值为3~10。
进一步地,所述丝素蛋白溶液与胶原蛋白溶液混合的质量比为99:1~1:99。
进一步地,所述超声处理的条件为:超声功率为5~3000瓦特,超声功率比:1%~100%,时间为1秒~2小时,温度为0~60℃。
进一步地,所述孵育的条件为:温度为0~60℃,时间为0~2小时。
在本发明的具体实施方式中,所述丝素蛋白溶液是将脱胶蚕丝溶解在溶剂中,经透析得到;进一步地,所述溶剂选自cacl2/c2h5oh/h2o三元溶液、libr水溶液、cacl2水溶液中的一种或几种;进一步地,所述cacl2/c2h5oh/h2o三元溶液中cacl2:c2h5oh:h2o的摩尔比为1:2:8,所述libr水溶液的浓度为9.3mol/l,所述cacl2水溶液的质量体积浓度为10%~100%;更进一步地,所述透析的截留分子量为1000~12000da。
进一步地,所述胶原蛋白溶液是将胶原蛋白溶于醋酸溶液、盐酸溶液或去离子水中,调节ph值即得。调节ph值可使用盐酸、醋酸、氢氧化钠溶液等常见的可调节ph值的试剂。
本发明中胶原蛋白溶液和丝素蛋白溶液不限于上述方法,凡是通过本领域内已知的方法制备的胶原蛋白溶液和丝素蛋白溶液均可适用于本发明中。
本发明的有益效果是:
(1)本发明超声介导丝素蛋白复合胶原水凝胶,采用ⅰ型胶原蛋白和丝素蛋白作原料,两者都是天然可再生蛋白材料,来源广泛,廉价易得。
(2)本发明与传统单纯胶原蛋白自组装交联制备的凝胶相比,复合水凝胶体内、外抗酶解能力显著提高,降解速度减慢,延长了其在组织修复时填充作用的时间,提高了材料的有效性。
(3)本发明与单纯丝素蛋白水凝胶相比,胶原蛋白的加入,显著增加了材料的吸水性、柔韧性及填充效果。
(4)本发明超声介导丝素蛋白复合胶原水凝胶不会发生相分离现象,制备方法高效快捷,全程采用物理混合且不添加任何化学交联剂,操作简单且条件温和,无需复杂的设施设备,节能环保,成本低廉,易于产业化和推广应用。
(5)本发明超声介导丝素蛋白复合胶原水凝胶与人体细胞外基质具有相似的机械和结构性能,具有良好的含水率和渗透性,可为细胞的粘附、铺展和生长提供一个优越的微环境。同时还能有效解决单一胶原水凝胶培养细胞过程中因水凝胶剧烈收缩而对细胞产生的负面影响的问题,本发明水凝胶材料在组织工程再生修复领域具有广泛的应用前景。
(6)本发明超声介导丝素蛋白复合胶原水凝胶具有良好的互穿网络结构(ipn结构),力学性能优异,丝素蛋白牢固镶嵌于胶原蛋白纤维结构上,胶原蛋白纤维结构得以保持,整个水凝胶的结构扎实稳固。该复合水凝胶既兼具单纯胶原和丝素蛋白水凝胶的优点,又能弥补两者存在的缺陷,而且还能较好支持骨髓间充质干细胞的粘附、增殖和生长,可为材料诱导干细胞定向分化提供一种新型的三维培养模型。
附图说明
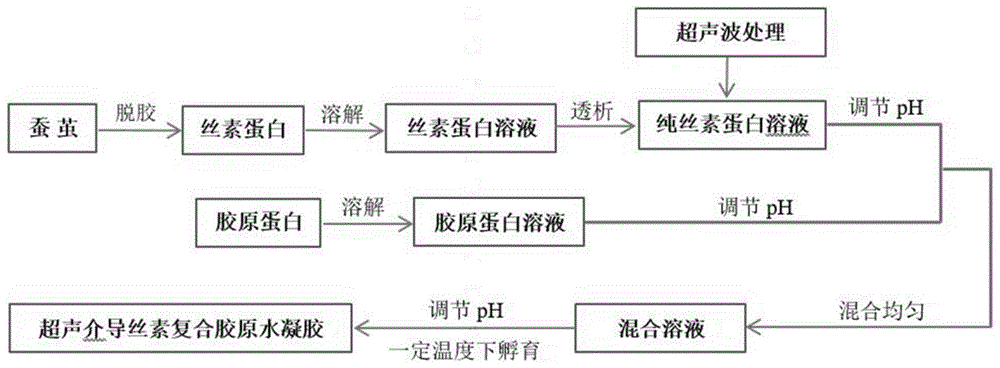
图1是本发明超声介导丝素蛋白复合胶原水凝胶制备工艺流程图;
图2是实施例1超声介导丝素蛋白复合胶原水凝胶的扫描电镜图;
图3是bmscs在实施例1的超声介导丝素蛋白复合胶原水凝胶粘附生长的激光共聚焦图;
图4是bmscs在实施例1的超声介导丝素蛋白复合胶原水凝胶粘附生长的扫描电镜图;
图5是bmscs在实施例1的col、col+sf(ns)和col+sf(s)三组水凝胶材料力学性能比较;
图6是实施例1制备的超声介导丝素蛋白复合胶原水凝胶对比丝素复合胶原水凝胶和胶原水凝胶培养bmscs初期和第一天水凝胶体积变化情况;
图7是实施例1制备的超声介导丝素蛋白复合胶原水凝胶对比丝素复合胶原水凝胶和胶原水凝胶培养bmscs前三天水凝胶体积变化情况。
具体实施方式
下面结合附图对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明实施例中所用的胶原蛋白均为牛源i型胶原蛋白。
实施例1超声介导丝素蛋白复合胶原水凝胶的制备
(1)将0.45g胶原蛋白在2~8℃下完全溶解于1m100ml醋酸溶液中,调节ph值为7.0,获得均匀的胶原蛋白溶液待用。
(2)将10g脱胶蚕丝溶解于cacl2/c2h5oh/h2o(n=1:2:8)三元溶液中,于75±2℃下溶解4h,溶解完全后用截留分子量为3500da透析袋在去离子水中透析3天,获得浓度为5%(w/v)的丝素蛋白溶液,用去离子水稀释至浓度为3%(w/v)备用;
(3)量取步骤(2)制备的5%丝素蛋白溶液50ml,用超声功率为1000瓦特,超声功率比为40%及常温条件下超声处理丝素蛋白溶液1min,然后置于2~8℃下待用;
(4)从(1)和(3)中依次量取20ml胶原蛋白溶液与10ml丝素蛋白溶液进行充分混合均匀形成混合液并调节ph为7.0,接着将混合溶液倒入圆柱形容器中,置于37℃条件下孵育30min使其凝胶化,获得超声介导丝素蛋白复合胶原水凝胶。
通过扫描电镜观察本实施例制备的超声介导丝素蛋白复合胶原水凝胶,见图2。从图2可知,该复合水凝胶具有良好的互穿网络结构(ipn结构),丝素蛋白牢固镶嵌于胶原蛋白纤维结构上,与人体细胞外基质具有相似的结构性能。
实施例2超声介导丝素蛋白复合胶原水凝胶的制备
(1)将1g胶原蛋白在2~8℃下完全溶解于0.3m200ml醋酸溶液中,调节ph值为5.0,获得均匀的胶原蛋白溶液待用。
(2)将10g脱胶蚕丝溶解于9.3mlibr溶液中,于60±5℃下溶解4h,溶解完全后用截留分子量为1000da透析袋在去离子水中透析3天,获得浓度为3%(w/v)的丝素蛋白溶液并调节ph到5待用;
(3)量取步骤(2)制备的3%丝素蛋白溶液30ml,用超声功率为500瓦特,超声功率比为60%及常温条件下处理丝素蛋白溶液10秒,然后置于2~8℃下待用;
(4)从(1)和(3)中依次量取30ml胶原蛋白溶液与10ml丝素蛋白溶液进行充分混合均匀形成混合液并调节ph为7.2,接着将混合溶液倒入圆柱形容器中,置于37℃条件下孵育20min使其凝胶化,获得超声介导丝素蛋白复合胶原水凝胶。
实施例3超声介导丝素蛋白复合胶原水凝胶的制备
(1)将8g胶原蛋白在2~8℃下完全溶解于0.3m200ml醋酸溶液中,调节ph值为5.0,获得均匀的胶原蛋白溶液待用。
(2)将15g脱胶蚕丝溶解于40%cacl2溶液中,于98±2℃下溶解4h,溶解完全后用截留分子量为12000da透析袋在去离子水中透析3天,获得浓度为8%(w/v)的丝素蛋白溶液并调节ph到5待用;
(3)量取步骤(2)制备的8%丝素蛋白溶液50ml,用超声功率为500瓦特,超声功率比为60%及冰浴条件下处理丝素蛋白溶液30秒,然后置于2~8℃下待用;
(4)从(1)和(3)中依次量取10ml胶原蛋白溶液与10ml丝素蛋白溶液进行充分混合均匀形成混合液,调节ph为7.0,接着将混合溶液倒入圆柱形容器中,置于37℃条件下孵育5min使其凝胶化,获得超声介导丝素蛋白复合胶原水凝胶。
实施例4超声介导丝素蛋白复合胶原水凝胶的制备
(1)将1g胶原蛋白在2~8℃下完全溶解于1m200ml盐酸溶液中,调节ph值为7.0,获得均匀的胶原蛋白溶液待用。
(2)将10g脱胶蚕丝溶解于9.3mlibr溶液中,于60±5℃下溶解4h,溶解完全后用截留分子量为8000da透析袋在去离子水中透析3天,获得浓度为5%(w/v)的丝素蛋白溶液并调节ph到7.0待用;
(3)量取步骤(2)制备的5%丝素蛋白溶液60ml,用超声功率为2000瓦特,超声功率比为30%及常温条件下处理丝素蛋白溶液5秒,然后置于2~8℃下待用;
(4)从(1)和(3)中依次量取30ml胶原蛋白溶液与10ml丝素蛋白溶液进行充分混合均匀形成混合液并调节ph为7.0,接着将混合溶液倒入圆柱形容器中,置于37℃条件下孵育30min使其凝胶化,获得超声介导丝素蛋白复合胶原水凝胶。
实施例5超声介导丝素蛋白复合胶原水凝胶的制备
(1)将10g胶原蛋白在2~8℃下完全溶解于2m200ml盐酸溶液中,调节ph值为7.0,获得均匀的胶原蛋白溶液待用。
(2)将30g脱胶蚕丝溶解于9.3mlibr溶液中,于60±5℃下溶解4h,溶解完全后用截留分子量为3500da透析袋在去离子水中透析3天,获得浓度为5%(w/v)的丝素蛋白溶液并调节ph到7.0待用;
(3)量取步骤(2)制备的5%丝素蛋白溶液60ml,用超声功率为500瓦特,超声功率比为80%及冰浴条件下处理丝素蛋白溶液15秒,然后置于2~8℃下待用;
(4)从(1)和(3)中依次量取30ml胶原蛋白溶液与20ml丝素蛋白溶液进行充分混合均匀形成混合液并调节ph为7.2,接着将混合溶液倒入圆柱形容器中,置于37℃条件下孵育15min使其凝胶化,获得超声介导丝素蛋白复合胶原水凝胶。
实施例6超声介导丝素蛋白复合胶原水凝胶的制备
(1)将10g胶原蛋白在2~8℃下完全溶解于0.5m200ml盐酸溶液中,调节ph值为5.0,获得均匀的胶原蛋白溶液待用。
(2)将10g脱胶蚕丝溶解于9.3mlibr溶液中,于60±5℃下溶解4h,溶解完全后用截留分子量为12000da透析袋在去离子水中透析3天,获得浓度为5%(w/v)的丝素蛋白溶液并调节ph到5.0待用;
(3)量取步骤(2)制备的5%丝素蛋白溶液50ml,用超声功率为1000瓦特,超声功率比为10%及常温条件下处理丝素蛋白溶液3分钟,然后置于2~8℃下待用;
(4)从(1)和(3)中依次量取30ml胶原蛋白溶液与30ml丝素蛋白溶液进行充分混合均匀形成混合液并调节ph为7.0,接着将混合溶液倒入圆柱形容器中,置于37℃条件下孵育5min使其凝胶化,获得超声介导丝素蛋白复合胶原水凝胶。
实施例7超声介导丝素蛋白复合胶原水凝胶的制备
(1)将0.03g胶原蛋白在2~8℃下完全溶解于1m100ml醋酸溶液中,调节ph值为10.0,获得均匀的胶原蛋白溶液待用。
(2)将50g脱胶蚕丝溶解于cacl2/c2h5oh/h2o(n=1:2:8)三元溶液中,于75±2℃下溶解4h,溶解完全后用截留分子量为3500da透析袋在去离子水中透析3天,调节溶液ph值为3.0,获得浓度为50%(w/v)的丝素蛋白溶液;
(3)量取步骤(2)制备的50%丝素蛋白溶液10ml,用超声功率为1000瓦特,超声功率比为40%及常温条件下处理丝素蛋白溶液1min,然后置于2~8℃下待用;
(4)从(1)和(3)中依次量取20ml胶原蛋白溶液与1ml丝素蛋白溶液进行充分混合均匀形成混合液并调节ph为7.0,接着将混合溶液倒入圆柱形容器中,置于37℃条件下孵育30min使其凝胶化,获得超声介导丝素蛋白复合胶原水凝胶。
实施例8超声介导丝素蛋白复合胶原水凝胶的制备
(1)将50g胶原蛋白在2~8℃下完全溶解于1m100ml醋酸溶液中,调节ph值为3.0,获得均匀的胶原蛋白溶液待用。
(2)将10g脱胶蚕丝溶解于9.3mlibr溶液中,于60±5℃下溶解4h,溶解完全后用截留分子量3500透析袋在去离子水中透析3天,获得浓度为5%(w/v)的丝素蛋白溶液,用去离子水稀释至浓度为0.03%(w/v)并调节ph到5.0备用;
(3)量取步骤(2)制备的0.03%丝素蛋白溶液50ml,用超声功率为1000瓦特,超声功率比为10%及冰浴条件下处理丝素蛋白溶液3分钟,然后置于2~8℃下待用;
(4)从(1)和(3)中依次量取1ml胶原蛋白溶液与20ml丝素蛋白溶液进行充分混合均匀形成混合液并调节ph为7.0,接着将混合溶液倒入圆柱形容器中,置于37℃条件下孵育5min使其凝胶化,获得超声介导丝素蛋白复合胶原水凝胶。
实施例9超声介导丝素蛋白复合胶原水凝胶的制备
(1)将46g胶原蛋白在2~8℃下完全溶解于1m100ml醋酸溶液中,调节ph值为7.0,获得均匀的胶原蛋白溶液待用。
(2)将45g脱胶蚕丝溶解于cacl2/c2h5oh/h2o(n=1:2:8)三元溶液中,于75±2℃下溶解4h,溶解完全后用截留分子量3500透析袋在去离子水中透析3天,调节溶液ph值为10.0,获得浓度为45%(w/v)的丝素蛋白溶液;
(3)量取步骤(2)制备的50%丝素蛋白溶液100ml,用超声功率为1000瓦特,超声功率比为40%及常温条件下处理丝素蛋白溶液1min,然后置于2~8℃下待用;
(4)从(1)和(3)中依次量取0.2ml胶原蛋白溶液与20ml丝素蛋白溶液进行充分混合均匀形成混合液并调节ph为7.0,接着将混合溶液倒入圆柱形容器中,置于37℃条件下孵育30min使其凝胶化,获得超声介导丝素蛋白复合胶原水凝胶。
实施例10
分别制备col、col+sf(ns)和col+sf(s)三组水凝胶材料进行性能试验。col组为胶原水凝胶,是只采用胶原蛋白的水凝胶;col+sf(ns)组为丝素与胶原复合水凝胶,是丝素蛋白不进行超声处理直接复合与胶原蛋白复合的水凝胶;col+sf(s)组为本发明超声介导丝素蛋白复合胶原水凝胶。
col组:将胶原蛋白浓度为3mg/ml的胶原蛋白溶液调节ph为7.0,倒入圆柱形容器中,置于37℃条件下孵育30min使其凝胶化,得到胶原水凝胶。
col+sf(ns)组:制备方法参考实施例1,区别在于:无步骤(3)的超声处理步骤;胶原蛋白浓度为3mg/ml,丝素蛋白浓度10mg/ml;胶原蛋白和丝素蛋白质量比为3:5,得到丝素与胶原复合水凝胶。
col+sf(s)组:实施例1制备的本发明超声介导丝素蛋白复合胶原水凝胶。
参照现有技术的方法对三组材料进行力学性能测试:
将col、col+sf(ns)和col+sf(s)三组水凝胶材料置于动态力学测试仪(dma)的测试台上,于室温下以5mn的预加应力,20μm的振幅和105%的动态静态力之比的参数,测试水凝胶在1hz的压缩频率下的储能模量。
测试结果如图5所示,在胶原浓度保持不变的情况下,丝素蛋白的引入会增加水凝胶的储能模量,col+sf(ns)组>col组,特别是当丝素蛋白溶液经超声波处理后与胶原蛋白溶液复合组水凝胶(col+sf(s))的储能模量较col+sf(ns)组高,与col组有显著性差异,这间接说明了col+sf(s)组水凝胶材料力学强度比col和col+sf(ns)组好,说明col+sf(s)组水凝胶材料在抵抗细胞介导的材料收缩上体现出明显优势(图6和图7结果也可说明此点)。
参照现有技术的方法对三组材料进行bmscs(兔源)的包裹培养,三组材料包裹的bmscs密度均为500万/ml,观察现象。
由图3~4可知,bmscs可以在本发明的超声介导丝素蛋白复合胶原水凝胶内很好的粘附、增殖和生长,并保持其高活力。
由图6、图7可明显的看出,随着对bmscs培养的时间的增长,col组和col+sf(ns)组的水凝胶材料均出现了明显的收缩,而本发明超声介导丝素蛋白复合胶原水凝胶即col+sf(s)组在培养细胞的过程中,体积变化较小,培养到第3天时,col、col+sf(ns)和col+sf(s)三组材料的直径依次分别减少了88.0%、88.5%和12.3%。
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
- 还没有人留言评论。精彩留言会获得点赞!