抗TSPAN8单克隆抗体及其用途的制作方法
本发明涉及生物医药领域,具体涉及全人源的抗tspan8单克隆抗体及其用途。
背景技术:
tetraspanins又称作四次跨膜蛋白超家族(tm4sf),由33个家族成员组成,包括tspan8、与分化(cd)相关的cd63、cd37、cd53、cd81和cd9等。tetraspanins家族共同特征是具有四个高度保守的膜跨域,在多种细胞功能中发挥重要生物学调控。
肿瘤的侵袭转移和耐药是导致临床治疗失败、患者死亡的主要原因。肿瘤微环境(tumormicroenvironment,tme)中,四次跨膜蛋白tspan8促进肿瘤细胞上皮间质转化(epithelialmesenchymaltransition,emt)及干性(stemness)增强的分子调控机制及关键分子靶点。越来越多的证据表明,tspan8促进肿瘤细胞迁移,侵袭和转移在多种类型的人类癌症,包括卵巢癌和胃癌结肠直肠癌、肝癌、胰腺癌、神经胶质瘤等。
单克隆抗体药物具有靶向性强、特异性高和毒副作用低等特点。以四次跨膜蛋白tspan8为靶标的单克隆抗体可以特异性与tspan8发生特异性结合,从而介导抗肿瘤治疗效果。
全人源抗体是治疗性抗体发展的主要方向,抗体库技术的出现为人源抗体的制备筛选提供了良好的技术平台。抗体库技术绕过了以往单抗研制过程中必须的杂交瘤过程,甚至不需要经过免疫过程即可获得各种抗体基因以及抗体分子片段。噬菌体抗体库是最早出现也是目前应用最广泛的抗体库。噬菌体抗体库根据抗体基因的来源分为免疫库和非免疫库,非免疫库又天然库、半合成库和全合成库。噬菌体抗体库的筛选模拟了抗体亲和力成熟的过程,将抗原包在固相介质上,加入待筛选的噬菌体抗体库,通过数轮“吸附-洗涤-洗脱-扩增”的过程淘选到亲和力特异的抗体。
目前,国内尚且缺乏具有高亲和力的抗肿瘤效果的抗tspan8的全人源抗体。
技术实现要素:
本发明的目的是针对tspan8的胞外段序列作为抗原,从全人源组合天然抗体库中筛选出抗tspan8的单克隆抗体或其片段,该抗体具有高亲和力、且能抑制乳腺癌细胞系的增值和迁移,具有抗肿瘤效果。
为了达到上述目的,本发明提供了一种抗tspan8的单克隆抗体及其应用。
本发明的第一方面,提供了一种抗体的重链可变区,编码所述抗体的重链可变区的核酸序列如seqidno:1所示或其同源性序列。
本发明的第二方面,提供一种抗体的轻链可变区,编码所述抗体的轻链可变区的核酸序列如seqidno:2所示或其同源性序列。
较佳地,所述抗体包括:单链抗体、双链抗体。
较佳地,所述抗体为单克隆抗体。
较佳地,所述抗体为特异性抗tspan8蛋白的单克隆抗体。
较佳地,所述抗体还包含选自igg1或igg4亚型的重链恒定区和包含选自kappa的轻链恒定区。
本发明的第三方面,提供一种编码上述的重链可变区和/或轻链可变区的多核苷酸。
本发明的第四方面,提供一种载体,其包含如第三方面所述的多核苷酸。
本发明的第五方面,提供一种遗传工程化的宿主细胞,其包含如第四方面所述的载体。
本发明取得如下有益效果:
本发明针对tspan8蛋白功能区的胞外段序列作为抗原筛选获得一个特异性针对tspan8蛋白功能区的抑制型单克隆抗体(ts04-igg),本发明提供的抗tspan8的单克隆抗体(ts04-igg)具有高亲和力,特异性强,稳定性好,且具有抑制乳腺癌细胞系的增殖和迁移能力,且可以抑制肿瘤的生长。
附图说明
图1为实施例中tspan8-lel-fc融合蛋白的sds-page分析。
图2为实施例中基于差异富集的组合抗体库筛选结果。
图3为实施例中噬菌体单克隆elisa鉴定结果。
图4为实施例中抗体表达纯化的sds-page分析。
图5为实施例中ts01-igg至ts08-igg和tspan8-lel-fc的相互作用力分析。
图6为实施例中ts03-igg至ts05-igg的细胞膜共定位研究。
图7为实施例中ts04-igg梯度浓度下与tspan8-lel-fc的亲和力分析。
图8a为ts04-igg的表观结合亲和力分析。
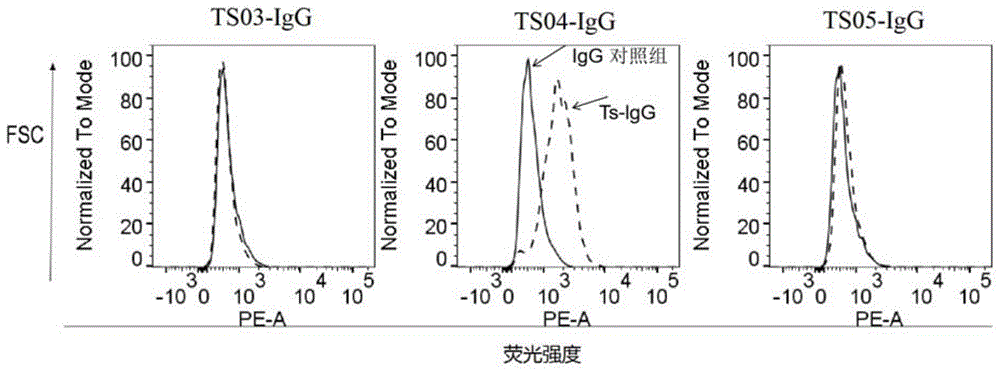
图8b为流式细胞术方法检测ts04-igg与细胞表明的结合能力。
图9为ts04-igg的熔点曲线。
图10a为ts04-igg体外抑制乳腺癌细胞的迁移能力结果图。
图10b为ts04-igg体外抑制乳腺癌细胞的迁移能力统计图。
图11a为本实施例中单克隆抗体抑制mcf-10a细胞的增值能力结果图。
图11b为本实施例中单克隆抗体抑制mda-mb-231细胞的增值能力统计图。
图12a为ts04-igg在小鼠乳腺癌异种移植模型中活体成像。
图12b为ts04-igg抑制肿瘤生长能力分析。
具体实施方式
本发明提供了一种抗tspan8的单克隆抗体及其应用。
如本文所用,术语“可变”表示抗体中可变区的某些部分在序列上有所不同,它形成了各种特定抗体对其特定抗原的结合和特异性。然而,可变性并不均匀地分布在整个抗体可变区中。它集中于轻链和重链可变区中称为互补决定区(cdr)或超变区中的三个片段中。可变区中较保守的部分称为构架区(fr)。天然重链和轻链的可变区中各自包含四个fr区,它们大致上呈β-折叠构型,由形成连接环的三个cdr相连,在某些情况下可形成部分β折叠结构。每条链中的cdr通过fr区紧密地靠在一起并与另一链的cdr一起形成了抗体的抗原结合部位。恒定区不直接参与抗体与抗原的结合,但是它们表现出不同的效应功能,例如参与抗体的依赖于抗体的细胞毒性。
如本文所用,术语“单克隆抗体(单抗)”指从一类基本均一的群体获得的抗体,即该群体中包含的单个抗体是相同的,除少数可能存在的天然发生的突变外。单克隆抗体高特异性地针对单个抗原位点。而且,与常规多克隆抗体制剂(通常是具有针对不同决定簇的不同抗体)不同,各单克隆抗体是针对抗原上的单个决定簇。除了它们的特异性外,单克隆抗体的好处还在于它们是通过杂交瘤培养来合成的,不会被其它免疫球蛋白污染。修饰语“单克隆”表示了抗体的特性,是从基本均一的抗体群中获得的,这不应被解释成需要用任何特殊方法来生产抗体。
如本文所用,术语“可变区”与“互补决定区(complementaritydeterminingregion,cdr)”可互换使用。
一般,抗体的抗原结合特性可由位于重链和轻链可变区的3个特定的区域来描述,称为可变区域(cdr),将该段间隔成4个框架区域(fr),4个fr的氨基酸序列相对比较保守,不直接参与结合反应。这些cdr形成环状结构,通过其间的fr形成的β折叠在空间结构上相互靠近,重链上的cdr和相应轻链上的cdr构成了抗体的抗原结合位点。可以通过比较同类型的抗体的氨基酸序列来确定是哪些氨基酸构成了fr或cdr区域。本发明抗体的重链和/或轻链的可变区特别令人感兴趣,因为它们中至少部分涉及结合抗原。因此,本发明包括那些具有带cdr的单克隆抗体轻链和重链可变区的分子,只要其cdr与此处鉴定的cdr具有90%以上(较佳地95%以上,最佳地98%以上)的同源性,即同源性序列。
本发明抗体指具有tspan8蛋白结合活性的、包括上述cdr区的多肽。该术语还包括具有与本发明抗体相同功能的、包含上述cdr区的多肽的变异形式。这些变异形式包括(但并不限于):一个或多个(通常为1-50个,较佳地1-30个,更佳地1-20个,最佳地1-10个)氨基酸的缺失、插入和/或取代,以及在c末端和/或n末端添加一个或数个(通常为20个以内,较佳地为10个以内,更佳地为5个以内)氨基酸。例如,在本领域中,用性能相近或相似的氨基酸进行取代时,通常不会改变蛋白质的功能。又比如,在c末端和/或n末端添加一个或数个氨基酸通常也不会改变蛋白质的功能。该术语还包括本发明抗体的活性片段和活性衍生物。
该多肽的变异形式包括:同源序列、保守性变异体、等位变异体、天然突变体、诱导突变体、在高或低的严紧度条件下能与本发明抗体的编码dna杂交的dna所编码的蛋白、以及利用抗本发明抗体的抗血清获得的多肽或蛋白。
在本发明中,“保守性变异体”指与本发明抗体的氨基酸序列相比,有至多10个,较佳地至多8个,更佳地至多5个,最佳地至多3个氨基酸被性质相似或相近的氨基酸所替换而形成多肽。
本发明还提供了编码上述抗体或其片段或其融合蛋白的多核苷酸分子。本发明的多核苷酸可以是dna形式或rna形式。dna形式包括cdna、基因组dna或人工合成的dna。dna可以是单链的或是双链的。dna可以是编码链或非编码链。其编码区序列可以与seqidno.:1、2所示的编码区序列相同或者是简并的变异体。如本文所用,“简并的变异体”在本发明中是指编码具有与本发明的多肽相同的氨基酸序列,但与seqidno.:1、2所示的编码区序列有差别的核酸序列。
本发明的抗体的核苷酸全长序列或其片段通常可以用pcr扩增法、重组法或人工合成的方法获得。一种可行的方法是用人工合成的方法来合成有关序列,尤其是片段长度较短时。通常,通过先合成多个小片段,然后再进行连接可获得序列很长的片段。此外,还可将重链的编码序列和表达标签融合在一起,形成融合蛋白。
一旦获得了有关的序列,就可以用重组法来大批量地获得有关序列。这通常是将其克隆入载体,再转入细胞,然后通过常规方法从增殖后的宿主细胞中分离得到有关序列。本发明所涉及的生物分子(核酸、蛋白等)包括以分离的形式存在的生物分子。目前,已经可以完全通过化学合成来得到编码本发明蛋白(或其片段,或其衍生物)的dna序列。然后可将该dna序列引入本领域中已知的各种现有的dna分子(或如载体)和细胞中。此外,还可通过化学合成将突变引入本发明蛋白序列中。
本发明还涉及包含上述的适当dna序列以及适当启动子或者控制序列的载体。这些载体可以用于转化适当的宿主细胞,以使其能够表达蛋白质。
宿主细胞可以是原核细胞,如细菌细胞;或是低等真核细胞,如酵母细胞;或是高等真核细胞,如哺乳动物细胞。代表性例子有:大肠杆菌,链霉菌属;鼠伤寒沙门氏菌的细菌细胞;真菌细胞如酵母;果蝇s2或sf9的昆虫细胞;cho、cos7、293细胞的动物细胞等。
本发明中,流式细胞术的原理:在一定的压力下,鞘液带着细胞通过喷嘴中心进入到流式照射室,在流式照射室的分析点,激光照射到细胞发生散射和折射,发射出散射光(包括前向散射光和侧向散射光);同时细胞所携带的荧光素被激光激发并发射出荧光。前向散射光(forwardscatter,fsc)和侧向散射光(sidescatter,ssc)检测器把散射光转变成电信号。而荧光则被聚光器收集,不同颜色的荧光被双色反光镜转向不同的光电倍增检测器,把荧光信号也转变成电信号。这些电信号再经过数据化处理后输入电脑并储存,即可对细胞进行分析或分选。
本发明中,“nc”代表阴性,“nc-igg”代表阴性对照组。
实施例
一种抗tspan8的单克隆抗体的获得方法,在本实施例中选用igg1亚型的重链恒定区和包含kappa的轻链恒定区,简述包括如下步骤:
s1:利用基因重组技术将编码tspan8胞外段的基因序列(tspan8-lel),c-末端fc-标签克隆到pfuse表达载体中,构建人的tspan8-lel-fc片段,并在hek293f细胞中表达获得tspan8-lel-fc融合蛋白;
s2:以tspan8-lel-fc融合蛋白为抗原,通过三轮抗体库的富集筛选,从全人源的scfv噬菌体库中获得八个亲和力较高的scfv序列,分别命名为tsc01-tsc08。
s3:将上述八个阳性scfv序列,即tsc01-tsc08,克隆到真核表达载体,转染hek293f细胞后表达并纯化,获得抗tspan8单克隆抗体的全抗,并命名为ts01-igg至ts08-igg。
s4:通过elisa、spr、流式细胞技术及熔点试验筛选出高稳定性,高亲和力的抗tspan8的单克隆抗体ts04-igg。
s5:通过transwell迁移实验、cck8增殖试验验证ts04-igg抑制乳腺癌细胞系(mda-mb-231)的增殖和迁移能力。通过小鼠异种移植模型,发现ts04-igg在小鼠体内可以抑制肿瘤的生长。
具体来说,本发明提供的一种抗tspan8的单克隆抗体的获得方法的制备方法如下步骤:
1.抗原蛋白(tspan8-lel-fc)的制备;
利用基因重组技术将编码tspan8胞外段的基因序列(氨基酸110-205;称为tspan8-lel序列),c-末端fc-标签克隆到pfuse表达载体(pfusefc2;invivogen)中,构建人的tspan8-lel-fc片段。
然后在hek293f细胞中转染培养4天以表达异源重组蛋白质。离心后,收集分泌到培养基中的tspan8-lel-fc重组蛋白,在kta蛋白纯化仪(gehealthcare)上,对蛋白ahp柱(#17'3-03;gehealthcare),使用具有柠檬酸盐的缓冲液(ph3.4)洗脱,得到纯化的融合蛋白。
然后将纯化的融合蛋白浓缩至7.82mg/ml,并储存在ph7.4的pbs缓冲液中。如图1所示,第1泳道、第2泳道为未变性的tspan8-lel-fc融合蛋白,第3泳道为蛋白maker,第4泳道、第5泳道为变性的tspan8-lel-fc融合蛋白,通过sds-page分析,判断tspan8-lel-fc融合蛋白纯度>90%,将tspan8-lel-fc融合蛋白在-80℃保存。
2.基于差异富集的组合抗体库筛选
将tspan8-lel-fc融合蛋白稀释至10ug/ml,以100μl/孔包被96孔酶标板并于4℃过夜,随后加入50g/l脱脂奶粉封闭液于4℃封闭过夜,以50μl/孔加入组合人单克隆scfv抗体天然噬菌体文库(1011多样性),进行多轮亲和富集固定在蛋白a包被的磁珠上,37℃孵育2h,洗去没有结合的噬菌体抗体,用甘氨酸-盐酸(ph2.2)洗脱已结合的噬菌体,将洗脱液感染对数生长期的xl1-blue,并用vcsml3辅助噬菌体超感染,经30℃过夜培养,扩增阳性噬菌体克隆,并进行下一轮筛选。共进行3轮(round3)筛选。计算每一轮筛选的洗脱与投入克隆的比例,观察筛选的富集程度。
结果如图2所示,以fc片段为阴性对照组,tspan8-fc01至tspan8-fc13单克隆中,405nm处的吸光值大于1的单克隆序列有12个,说明所述单克隆序列得到了特异性富集。
3.phageelisa和dna测序鉴定
将第3轮筛选后获得的阳性噬菌体克隆感染xl1-blue感受态,直接涂布于含100ug/ml的氨苄青霉素的固定培养基,37℃培养过夜,次日挑单克隆菌落分别置于lb培养基中,加入vcsml3辅助噬菌体超感染制备单克隆噬菌体抗体。离心后把含噬菌体抗体的上清液进行单克隆elisa鉴定。
所述单克隆elisa鉴定方法,以50μl/孔加2ng/m浓度的tspan8-lel-fc抗原包被96孔酶标板,每个单克隆设有3个复孔,室温孵育2h,洗涤后加入hrp标记抗m13二抗室温孵育1h,然后pbst洗涤8次后加入50μlhrp底物2,2'-azinobis(3-乙基苯并噻唑啉-6-磺酸)-二铵盐溶液(#11684302001;roche)加入每个孔中。室温下避光孵育20分钟后,每孔加入50mol/l的h2s04终止反应,于405nm测吸光度。
如图3所示,405nm处吸光值大于0.85的阳性单克隆有八个,即获得八个亲和力较高的scfv序列(阳性),分别命名为tsc01-tsc08(其中,基因测序得到tsc04的重链可变区如seqidno:1所示的核酸序列,tsc04的轻链可变区如seqidno:2所示的核酸序列)。
4.单克隆抗体的表达和纯化
将上述特异性最佳的三个阳性scfv(tsc03-tsc05)的基因序列的轻链区域和重链区域,分别克隆到具有完整恒定重链结构域和完整恒定轻链结构域的质粒中,构建重链载体和轻链载体。然后同时将等摩尔重链载体和轻链载体,共转染到hek293f后继续表达培养4天,获得全人源的igg。将细胞培养基离心后,使用hitrap纯化分泌到培养基中的全长igg抗体。在kta蛋白纯化仪(gehealthcare)上,对蛋白ahp柱(#17'3-03;gehealthcare),使用具有柠檬酸盐的缓冲液(ph3.4)洗脱,纯化得到获得抗tspan8单克隆抗体的全抗,并命名为ts01-igg至ts08-igg。然后将八个抗tspan8单克隆抗体的全抗均浓缩至1mg/ml,并储存在ph7.4的pbs缓冲液中。
如图4所示,通过sds-page分析,第1,2,3泳道分别为未变性的ts04-igg、ts05-igg、ts06-igg,第4泳道为蛋白marker,第5,6,7泳道分别为变性的ts04-igg、ts05-igg、ts06-igg,且ts04-igg、ts05-igg、ts06-igg的纯度均大于90%,,并在-20℃保存。
5.单克隆抗体与tspan8-lel-fc之间的相互作用
在流式细胞术结合实验中,收集高表达tspan8乳腺癌细胞株(mda-mb-231)并重悬于冰冷的facs缓冲液(pbs,0.05%bsa,2mmedta)中。然后将等量的mda-mb-231细胞(每管50,000个细胞)与50nm的ts01-igg至ts08-igg在4℃温育20分钟,用1ml冰冷的facs缓冲液洗涤,旋转,并重悬于100μl冰中。含有识别人fc1:800体积稀释alexa555-耦联二抗的冷facs缓冲液。在4℃温育15分钟后,将细胞洗涤两次并重悬于facs缓冲液中,然后将它们分选并在流式细胞仪(lsrfortessatmx-20;bd)上分析以确定抗体的相对结合水平,记alexa555的平均荧光强度并进行分析。如图5所示,相比对照组,ts03-igg、ts04-igg、ts05-igg处理后平均荧光强度增强了,说明ts03-igg、ts04-igg、ts05-igg均能与细胞膜表面的tspan8有结合。
6.细胞膜共定位研究
将表达tspan8-gfp的293t细胞以2×105个/ml的浓度接种到已铺好盖玻片24孔板上进行细胞爬片。培养24小时后,将细胞在4%多聚甲醛中固定,并在封闭溶液(含有5%小牛血清的pbs溶液)中孵育30分钟。将得到的细胞分别与2μg/ml的ts03-igg、ts04-igg、ts05-igg在4℃下孵育过夜,然后进行三次pbs洗涤,每次5分钟,并与alexa555-缀合的山羊抗人二抗(lifetechnology)一起温育。在另外三次pbs洗涤各5分钟后,细胞核用dapi染色(#10236276001;roche)。并在激光扫描共聚焦显微镜(sp8)上进行定位分析,在1,024×1,024像素的ccd-ccd相机上收集图像。如图6所示,使用sp8专业软件进行数据采集和分析,图中相对阴性对照组及ts03-igg和ts05-igg,只有ts04-igg与膜上面tspan8-gfp有共定位,说明是ts04-igg是与细胞表面直接结合的。
7.抗原结合力分析
spr-结合研究在biacoret200(gehealthcare)上进行。抗原能与生物传感器芯片cm5系列s(gehealthcare)的表面的胺偶联。将重组蛋白tspan8-lel-fc固定在芯片表面上。用含有25mmhepes,500mmnacl,0.05%edta和0.05%ddm的运行缓冲液(ph7.4)按照0,3.125,6.25,12.5,25,50,100nm的浓度梯度稀释的抗体ts04-igg。测量结合/解离的动力学作为spr信号共振单位的变化,使用具有单循环动力学模型的biacoret200评估软件计算表观结合常数km值。
如图7所示,为ts04-igg在梯度浓度下(0,3.125,6.25,12.5,25,50,100nm)与抗原的亲和力分析。
8.细胞膜结合力分析
将等量的mda-mb-231细胞(每管50,000个细胞)与梯度稀释的抗体的ts04-igg(0,6.25,12.5,25,50,100nm)在4℃温育20分钟,用1ml冰冷的facs缓冲液洗涤,旋转,并重悬于100μl冰中。用含有识别人fc按照1:800体积稀释alexa555-耦联二抗的冷facs缓冲液,在4℃温育15分钟后,将细胞洗涤两次并重悬于facs缓冲液中,然后将它们分选并在流式细胞仪(lsrfortessatmx-20;bd)上分析以确定抗体的相对结合水平。记alexa555的平均荧光强度并进行分析,并计算抗体的表观结合亲和力。
如图8a和图8b所示,为流式细胞术方法检测ts04-igg与细胞表明的结合能力,相比阴性对照组,随着不同浓度的ts04-igg抗体(0,6.25,12.5,25,50,100nm)处理后结合的荧光强度增加,且计算得到ts04-igg抗体表观结合亲和力ts04-igg的ic50=22.95nm,hillslop=2.738。ic
9.熔点检测
50nm的ts04-igg填装进毛细管,并安装在温度计精确位置、再固定在b形管中心位置,加热升温测定,最终得到熔点曲线,如图9所示,图中是ts04-igg熔点曲线,测得tm=78.2℃,该熔点大于37℃(人体的正常体温),说明该抗体的稳定性较高。
10.细胞迁移侵袭试验(transwell)
乳腺癌上皮细胞mda-mb-231在不含血清的dmem/f12(3:1)培养基内饥饿12h,胰酶消化后用含0.1%fbsdmem/f12培养基重悬细胞,按1.0×105个/100μl加入上室,各组分别含50nm的ts03-igg、50nm的ts04-igg、50nm的ts05-igg。下室加入600l含的10%fbsdmem/f12培养基,以pbs作为ts-igg的空白对照,常规培养24h。用4%多聚甲醛常温固定细胞30min,并棉签拭去上室内细胞,把膜风干,0.1%结晶紫染色10~30min;显微镜下计数迁移细胞,计算迁移率。
如图10a所示,为ts04-igg体外抑制乳腺癌细胞的迁移能力结果图,如图10b所示,为ts04-igg体外抑制乳腺癌细胞的迁移能力统计图,图中相比用阴性对照,用ts03-igg、ts04-igg、ts05-igg处理后,肿瘤细胞迁移能力均减弱,其中ts04-igg效果最佳(p<0.05,n=3),ts04-igg具有体外抑制乳腺癌细胞的迁移能力。
11.cck8检测细胞增殖
取状态良好、处于增殖期的mda-mb-231,mcf-10a,4175细胞进行实验。细胞常规消化、离心,计数。每种细胞浓度均调整到1000个细胞每100μl培养基,取4个96孔平底板,分别做0h、24h、48h、72h、的时间梯度。将细胞接种到96孔板中,每种细胞做5-6个复孔,每个孔中加100μl培养基。加好细胞后,放入37℃培养箱中培养,细胞接种后24小时待贴壁,然后每孔分布加入50nm的ts03-igg、50nm的ts04-igg、50nm的ts05-igg,并加入10μl10%浓度的cck8试剂,轻轻拍打混匀。于37℃孵育2小时。测定450nm处吸光度值(od值),并测620nm处吸光度,此为培养基测吸光度基底值,实际值则为od450-od620。5组复孔od值中,除去一个最大值和一个最小值,剩余3组结果取平均值为实际od值。将4天的od值做折线图,统计分析两组细胞之间增殖能力差异。
如图11a和图11b所示,分析结果示:ts03-igg、ts04-igg、ts05-igg对于低表达的tspan8的乳腺囊性上皮细胞mcf-10a细胞的生长均没有明显影响;ts03-igg、ts04-igg、ts05-igg能抑制高表达tspan8的乳腺癌上皮细胞mda-mb-231的生长,,其中ts04-igg对肿瘤细胞的生长抑制作用最明显。
12.小鼠试验
向balb/c(n=5/组)雌裸鼠皮下注射5×106个的人肿瘤细胞系(mda-mb-231)构建小鼠异种移植模型。每3天观察一次小鼠生命状态,并测量瘤子大小,大约2周瘤子体积大小达到180mm3,将小鼠随机化分组,并以此为第一天给药进行治疗。分别在第1,3,7,14和21天尾静脉注射ts04-igg(0,1,10,20mg/kg)进行给药治疗,曲妥珠单抗(抗her2)联合ts04-igg用药,每周20mg/kg,pbs作为阴性对照给药,首次给予双倍的剂量治疗增加药物负荷,每次给药前测量瘤子长径a和短径b,根据公式v=a*b2计算肿瘤体积大小,并分析得到瘤子生长曲线,观察再给药1周以后,ts04-igg能抑制瘤子的生长,并且呈给药浓度依赖,抑制作用最强的给药浓度是10mg/kg,增大给药浓度20mg/kg并没有明显增强抑制作用,在给药治疗后的28天时给小鼠腹腔注射显影剂进行体内成像,得到瘤子分布情况。
如图12a和图12b所示,在小鼠乳腺癌异种移植模型,相对阴性对照组,,ts04-igg处理组能抑制瘤子的生长,并且呈给药浓度依赖,抑制作用最强的给药浓度是10mg/kg,增大给药浓度20mg/kg并没有明显增强抑制作用,说明,ts04-igg体内给药浓度10mg/kg可以达到最佳抑制肿瘤的生长的能力(p<0.05,n=5)。
本实施例所使用的实验动物、主要试剂及所使用到的溶液来源:
1)在本实施例中所使用的实验动物与饲养所有动物研究均按照上海仁济医院动物伦理委员会提供的指南。将mda-mb-231细胞皮下接种于5周龄雌性裸鼠中上海实验动物中心。每4天次测量和监测肿瘤大小,其结果表示为平均值±sem。肿瘤组织是在实验结束时收集,称重并拍照。对于遗传治疗方法,20只荷瘤裸鼠随机分为4组,每组5只进行尾静脉注射不同浓度梯度的(0,1,10,20mg/kg)全抗ts-igg。每3天打一次。
2)本实施例所使用的主要试剂与仪器:
dmem/f12培养基(gibco);胎牛血清(gibco);双抗(gibco);35mm培养皿(nest);25mm细胞爬片(nest);磷酸盐缓冲液/pbs(博士德);荧光共聚焦显微镜(leica);35mm细胞培养皿(corning公司);倒置显微镜(leica);流式分析仪器(lsrfortessatmx-20;bd);抗体纯化仪器
3)本实施例所使用的溶液的配制:
细胞培养液:dmem/f12培养基+10%胎牛血清+1%双抗(体积分数);
spr运行buffer:25mmhepes,500mmnacl,0.05%edta,0.05%ddm。
实施例总结:
本实施例在噬菌体展示技术和全人源组合抗体库技术的基础上,利用基因重组技术,针对tspan8蛋白功能区的胞外段序列作为抗原筛选,获得一个特异性针对tspan8蛋白功能区的抑制型单克隆抗体ts04-igg,并通过elisa、spr、流式检测技术及熔点试验,验证了ts04-igg的亲和性、稳定性。并在体外通过transwell迁移实验以及cck8增殖试验验证了ts04-igg抑制乳腺癌细胞系(mda-mb-231)的增殖和迁移能力。进一步通过小鼠异种移植模型,发现ts04-igg体内可以抑制肿瘤的生长。
综上所述,本发明提供的针对tspan8蛋白功能区的抑制型单克隆抗体ts04-igg,具有高亲和力,特异性强,稳定性好,且具有抑制乳腺癌细胞系的增殖和迁移能力,对肿瘤具有明显的抑制作用,能用于治疗或预防具有tspan8介导促进肿瘤细胞上皮间质转化(epithelialmesenchymaltransition,emt)及干性(stemness)增强的分子调控机制及关键分子靶点的疾病。
尽管本发明的内容已经通过上述优选实施例作了详细介绍,但应当认识到上述的描述不应被认为是对本发明的限制。在本领域技术人员阅读了上述内容后,对于本发明的多种修改和替代都将是显而易见的。因此,本发明的保护范围应由所附的权利要求来限定。
序列表
<110>上海市第一人民医院
<120>抗tspan8单克隆抗体及其用途
<160>2
<170>siposequencelisting1.0
<210>1
<211>354
<212>dna
<213>人工序列(artificialsequence)
<400>1
caggagtccggcccaggacgggtgaagccttcggagaccctgtccctcacttgcactgtc60
tctggtgggtccgtcagcagtggtagccactactggagctggatccggcagcccccaggg120
aagggactggagtggattggatatatctattacagtgggaccaccaactacaacccctcc180
ctgaagagtcgagtcaccatatcaggagacaggtccaggaatcagttctccctgaagttg240
acctctgtgaccgctgcggacacggccgtgtattattgtgcgaccctccggtggagagat300
gtcttcaattcagggccccactggggccaggggaccacggtcaccgtctcctca354
<210>2
<211>321
<212>dna
<213>人工序列(artificialsequence)
<400>2
gaaattgtgttgacgcagtctccagccaccctatctttgtctccagggcaaagagccacc60
ctctcctgcagggccagtcagagtgtgaggaccttcttagcctggtacctacagaaacct120
ggccaggctcccaggctcctcatctatgatacatccaccagggccactggcatcccagac180
aggttcagtggcagtgggtctgggacagacttcactctcaccgtcagcagactggagcct240
gaagattttgcagtgtattactgtcagctgtatggcagctcgctgtgcacttttggccag300
gggaccaaggtggagatcaaa321
- 还没有人留言评论。精彩留言会获得点赞!