一种制备拉替拉韦钾晶型3的方法与流程
1.本发明属于药物化学技术领域,具体涉及一种制备拉替拉韦钾晶型3的方法。
背景技术:
2.拉替拉韦钾(raltegravir potassium)化学名称为n-(2-(4-(4-氟苄基氨基甲酰基)-5-羟基-1-甲基-6-氧代-1,6-二氢嘧啶-2-基)丙-2-基)-5-甲基-1,3,4-恶二唑-2-甲酰胺钾盐,商品名为isentress,由美国merck公司研发,于2007年10月获fda批准上市,是世界上第一个应用于临床的hiv整合酶抑制剂,用于治疗获得性免疫缺陷综合征(hiv)。
[0003][0004]
专利wo03035077中公布拉替拉韦化合物并公开其合成方法。
[0005]
专利wo2006060730公布拉替拉韦钾的晶型1、晶型2和晶型3三种晶型。其中,晶型1晶型为无水物,x射线粉末衍射显示其2θ值在5.9
°
、12.5
°
、20.0
°
、20.6
°
和25.6
°
有特征峰,差示扫描量热曲线显示具有279℃的吸热峰;晶型2为水合晶体钾盐形式,x射线粉末衍射显示其2θ值在7.9
°
、13.8
°
、15.7
°
、24.5
°
和31.5
°
有特征峰,差示扫描量热曲线显示具有146℃,239℃两个宽吸热峰和276℃一个尖锐的吸收峰;晶型3晶型也为拉替拉韦钾的无水物形式,x射线粉末衍射显示其2θ值在7.4
°
、7.8
°
、12.3
°
、21.6
°
和64.7
°
有特征峰,差示扫描量热曲线显示具有284℃的单个吸热峰。
[0006]
本专利中制备晶型3晶型需要在-78℃条件下先得到无定型钾盐,然后在乙醇溶剂中结晶得到。反应条件苛刻,操作复杂,不易工业化。
[0007]
专利wo2017001996报道拉替拉韦钾晶型3的制备方法,按照此专利方法实施,得到的拉替拉韦钾产品中降解杂质e(结构如下)超过产品质量限度,不易精制,且得到的产品中为少量含有晶型1晶型的混晶。
[0008][0009]
专利wo2018051239也报道了拉替拉韦钾晶型3的制备方法,此方法中使用酮类溶剂。众所周知,酮类溶剂碱性条件下反应容易产生亚异丙基丙酮杂质,此杂质为基因毒杂质,在产品中限度难以控制。
[0010]
拉替拉韦钾的晶型1和晶型3形式均为无水物晶型,专利wo2018051239实验数据表明,晶型3具有很好的化学稳定性和晶型稳定性,同时通过溶解度实验发现,晶型3较晶型1
有更好的水溶性,是拉替拉韦钾制剂开发的良好选择。因此,开发稳定的,操作简单的,产品质量满足原料药质量标准要求的,可工业化实施的晶型3的制备工艺,可为拉替拉韦钾制剂形式的开发提供更多的选择,满足产品市场需求。
技术实现要素:
[0011]
现有拉替拉韦钾晶型3的制备方法要么反应条件苛刻,生产过程不易实施,要么容易产生降解杂质,产品质量不能满足要求,要么增加基因毒杂质的产生,产品中难以控制,因此急需开发晶型3的新的制备方法,以满足现有市场对于拉替拉韦钾各种制剂形式开发的需求。
[0012]
本发明提供一种稳定的,操作简单的,产品质量满足原料药质量标准要求的,可工业化实施的拉替拉韦钾晶型3形式的新的制备方法。
[0013]
本发明的一方面在于提供一种拉替拉韦钾晶型3的制备新方法,其特征在于,所述方法包含以下步骤
[0014]
(1)将拉替拉韦悬浮于无水乙醇中,控制体系温度在10℃以下;
[0015]
(2)准备氢氧化钾的无水乙醇溶液,溶清待用;
[0016]
(3)将步骤2中制备的氢氧化钾乙醇溶液滴加到拉替拉韦乙醇悬浮液中,滴加完毕后,升温反应体系至20~30℃,保温搅拌;
[0017]
(4)抽滤,烘干,得拉替拉韦钾晶型3形式固体。
[0018]
其中步骤4中所得固体,纯度不低于99.6%,单一杂质不高于0.10%。
[0019]
在另一优选例中,步骤(2)中氢氧化钾的与拉替拉韦摩尔比为0.95~1.05:1。
[0020]
本发明的优点在于:提供了一种拉替拉韦钾晶型3的新的制备方法,此制备方法操作简单,生产条件易于控制;避免原工艺中可能产生基因毒杂质的风险;通过反应温度精确控制,减少降解杂质的产生,而且能很好实现粉体粒度的控制,避免混晶的产生,同时降低抽滤难度,便于工业化实施。
[0021]
应理解,在本发明范围内,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅在此不再一一赘述。
附图说明
[0022]
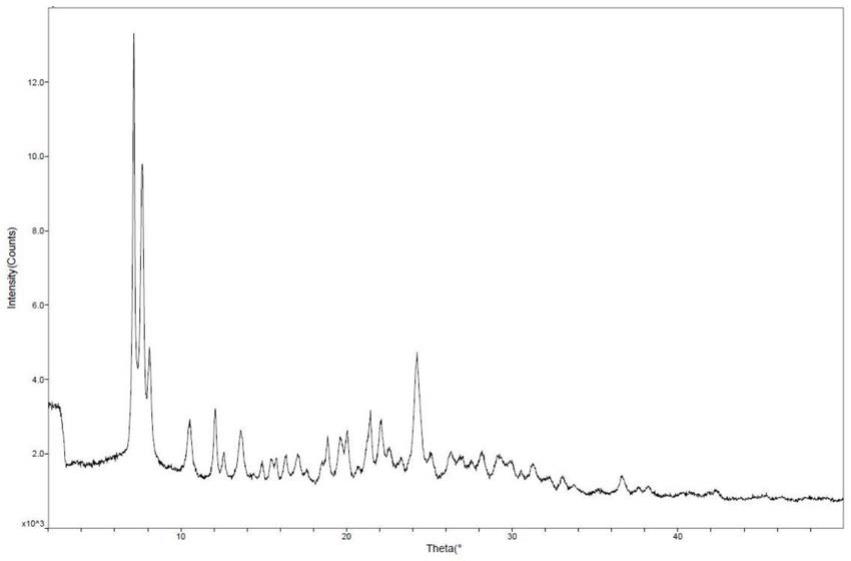
图1显示了拉替拉韦钾晶型3的x-射线粉末衍射图谱(xrpd);
[0023]
图2显示了拉替拉韦钾晶型3差示扫描量热分析谱图(dsc)。
具体实施方式
[0024]
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数是重量百分比和重量份数。
[0025]
以下实施例中所用的实验材料和试剂如无特别说明均可从市售渠道获得。
[0026]
x-射线粉末衍射(xrpd):
[0027]
x-射线粉末衍射仪器:brucker d8 advance x-射线粉末衍射仪;x-射线粉末衍射的参数如下:铜靶在室温条件下扫描。
[0028]
电压:40千伏特(kv)
[0029]
电流:40毫安培(ma)
[0030]
扫描模式:连续
[0031]
扫描范围:2.0~50.0度
[0032]
步长:0.020
°
[0033]
每步测量时间:0.1秒
[0034]
差式扫描量热分析(dsc):
[0035]
差示扫描量热(dsc)仪器:ta q2000型。
[0036]
差示扫描量热(dsc)分析方法参数如下:
[0037]
温度范围:25~250℃
[0038]
扫描速度:10℃/分钟
[0039]
保护气体:氮气,50毫升/分钟
[0040]
实施例1
[0041]
将331.5g氢氧化钾以及12l无水乙醇加入到反应瓶中,氩气环境下机械搅拌溶清待用。
[0042]
将2.5kg拉替拉韦游离酸及12.5l的无水乙醇加入到30l反应釜中,搅拌,控制体系温度不高于10℃。
[0043]
将制备的氢氧化钾乙醇溶液滴加到拉替拉韦游离酸的乙醇溶液中,滴加完毕后,将反应体系升温至20~25℃。保温搅拌1~2小时,抽滤,无水乙醇洗涤滤饼1~2次,将得到的湿品于40~45℃条件下减压干燥至恒重,得拉替拉韦钾晶型3形式固体,其xrd谱图如图1所示,dsc谱图如图2所示(重量收率103.1%,纯度99.8%)。
[0044]
实施例2
[0045]
将331.5g氢氧化钾以及12l无水乙醇加入到反应瓶中,氩气环境下机械搅拌溶清待用。
[0046]
将2.5kg拉替拉韦游离酸及12.5l的无水乙醇加入到30l的反应釜中,搅拌,控制体系温度不高于10℃。
[0047]
将制备的氢氧化钾乙醇溶液滴加到拉替拉韦游离酸的乙醇溶液中,滴加完毕后,将反应体系升温至20~25℃。保温搅拌1~2小时,抽滤,无水乙醇洗涤滤饼1~2次,将得到的湿品于40~45℃条件下减压干燥至恒重,得拉替拉韦钾晶型3形式固体,其xrd谱图如图1所示,dsc谱图如图2所示(重量收率100.3%,纯度99.7%)。
[0048]
实施例3
[0049]
将337.6g氢氧化钾以及12l无水乙醇加入到反应瓶中,氩气环境下机械搅拌溶清待用。
[0050]
将2.5kg拉替拉韦游离酸及12.5l的无水乙醇加入到30l的反应釜中,搅拌,控制体系温度不高于10℃。
[0051]
将制备的氢氧化钾乙醇溶液滴加到拉替拉韦游离酸的乙醇溶液中,滴加完毕后,将反应体系升温至20~25℃。保温搅拌1~2小时,抽滤,无水乙醇洗涤滤饼1~2次,将得到
的湿品于40~45℃条件下减压干燥至恒重,得拉替拉韦钾晶型3形式固体,其xrd谱图如图1所示,dsc谱图如图2所示(重量收率104.5%,纯度99.8%)。
[0052]
实施例4
[0053]
将337.6g氢氧化钾以及12l无水乙醇加入反应瓶中,氩气环境下机械搅拌溶清待用。
[0054]
将2.5kg拉替拉韦游离酸及12.5l的无水乙醇加入到30l的反应釜中,搅拌,控制体系温度不高于10℃。
[0055]
将制备的氢氧化钾乙醇溶液滴加到拉替拉韦游离酸的乙醇溶液中,滴加完毕后,将反应体系升温至20~25℃。保温搅拌1~2小时,抽滤,无水乙醇洗涤滤饼1~2次,将得到的湿品于40~45℃条件下减压干燥至恒重,得拉替拉韦钾晶型3形式固体,其xrd谱图如图1所示,dsc谱图如图2所示(重量收率103.5%,纯度99.6%)。
[0056]
对比实施例1
[0057]
将331.5g氢氧化钾以及12l无水乙醇加入到反应瓶中,氩气环境下机械搅拌溶清待用。
[0058]
将2.5kg拉替拉韦游离酸及12.5l的无水乙醇加入到30l的反应釜中,搅拌,控制体系温度15~20℃。
[0059]
将制备的氢氧化钾乙醇溶液滴加到拉替拉韦游离酸的乙醇溶液中,滴加完毕后,将反应体系快速升温至20~25℃。保温搅拌1~2小时,抽滤,抽滤速度慢,滤饼粘稠。
[0060]
对比实施例2
[0061]
将331.5g氢氧化钾以及12l无水乙醇加入反应瓶中,氩气环境下机械搅拌溶清待用。
[0062]
将2.5kg拉替拉韦游离酸及12.5l的无水乙醇加入到30l的反应釜中,搅拌,控制体系温度20~25℃。
[0063]
将制备的氢氧化钾乙醇溶液滴加到拉替拉韦游离酸的乙醇溶液中,滴加完毕后,保温搅拌1~2小时,未过滤,晶浆粘稠,抽滤困难。
[0064]
本发明制备方法得到的拉替拉韦晶型3的影响因素实验结果如下:
[0065]
(1)放置条件:40℃,75
±
5%rh
[0066]
放置时间化学纯度杂质情况晶型稳定性0m99.807%单一杂质≤0.10%form 31m99.767%单一杂质≤0.10%稳定2m99.669%单一杂质≤0.10%稳定3m99.76%单一杂质≤0.10%稳定6m99.7489%单一杂质≤0.10%稳定
[0067]
(2)放置条件:25℃,60
±
5%rh
[0068]
放置时间化学纯度杂质情况晶型稳定性0m99.9067%单一杂质≤0.10%form 33m99.9645%单一杂质≤0.10%稳定6m99.7274%单一杂质≤0.10%稳定15m99.6623%单一杂质≤0.10%稳定
18m99.3821%单一杂质≤0.10%稳定
[0069]
在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1