定量检测样品中乙型肝炎病毒RNA的方法及其系统与流程
本发明涉及分子生物学
技术领域:
,特别涉及一种定量检测样品中乙型肝炎病毒rna的方法及其系统。
背景技术:
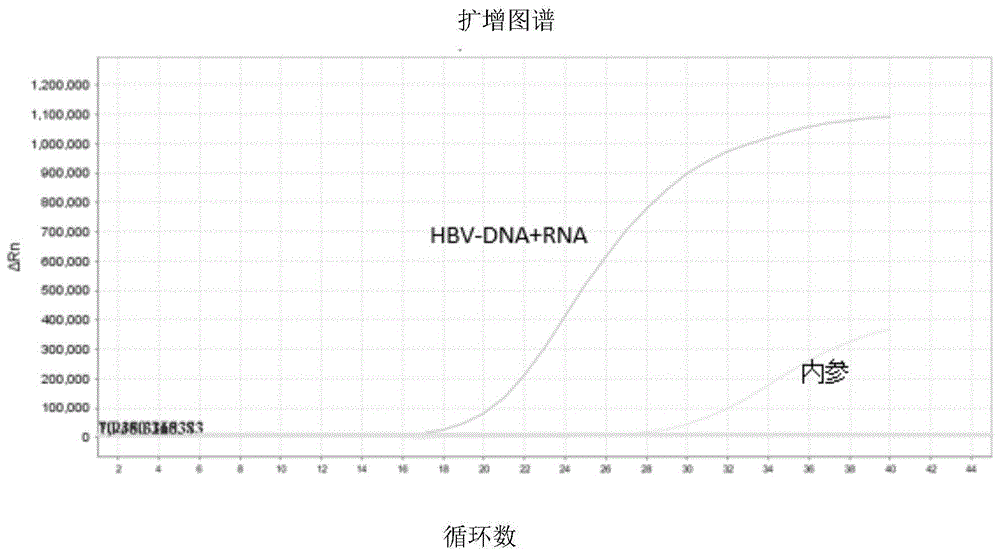
:乙型肝炎病毒(hepatitisbvirus,hbv)属嗜肝dna病毒科,基因组长约3.2kb,为部分双链环状dna(relaxedcirculardna,rcdna)。hbvdna长链为负链,位置和长度相对固定。短链为正链,其长度可变,约为负链的50%~80%。乙型肝炎病毒(hbv)感染是一个严重的公共卫生问题,世界卫生组织报告全球约有20亿人感染过hbv,其中3-4亿人为慢性hbv感染。在我国肝硬化和肝癌患者中,由hbv感染引起的比例分别高达60%和80%以上。现有的治疗药物主要为核苷酸类似物,虽然能够有效抑制病毒,但是存在长期用药、病毒耐药、病毒载量反弹等问题。根据hbv的复制感染机制,慢乙肝难以治愈和引起停药后病毒学反弹的主要原因是存在于感染肝细胞核内的病毒复制模板-hbv共价闭合环状dna(cccdna)难以清除。目前的停药指标主要有三种。一是血清hbvdna低于检测下限作为停药的治疗终点,但研究发现该指标并不能客观反映cccdna的转录活跃状态,有很大的病毒学反弹和疾病复发风险;二是临床上以血清hbv表面抗原(hbsag)转阴作为临床治愈的指标,结果也不尽如人意,因为除了完整的dane颗粒,hbsag还有另外两种存在形式,数量远超dane颗粒,且随着hbv病毒核酸长期存在于肝细胞内,hbv核酸片段能够整合到宿主基因组中,也能转录翻译产生hbsag,会使多数慢乙肝患者面临着终生用药。三是cccdna的清除,这是最理想的停药指标,但由于cccdna存在于感染的肝细胞内,只能通过肝组织活检来判断病毒的清除和安全停药,这在临床实践中并不适用。临床在治疗慢性乙肝过程中,常采用监测患者血清/血浆中hbvdna的量来反应抗病毒治疗的疗效,但因为目前常用抗病毒药物“核苷(酸)类药物”主要作用于hbvdna的合成阻断,血液中的hbvdna水平经过一段时间抗病毒治疗后迅速下降并消失。但由于cccdna的持续存在,且其转录活性不受影响,血液中仍存在hbvrna。前期研究者也揭示血清hbvpgrna的水平可反映患者肝细胞内cccdna存在和转录活性状态。所以,血液中hbvdna和rna均为hbvcccdna存在和复制的标志,血液中hbv总核酸(hbvdna+rna)的定量检测显得尤为重要。但目前市场上仅有针对hbvdna定量检测的试剂,暂无hbvrna的定量检测试剂,且国际或国内均无hbvrna定量的相关标准物质,给hbvrna准确定量带来困扰。本发明通过定量hbvdna的量来计算患者血液中hbvrna的量,简单、方便。技术实现要素:在一种实施方式中,本发明提供一种定量检测样品中乙型肝炎病毒rna的方法,所述方法通过直接定量样品中乙型肝炎病毒dna的量来定量所述样品中乙型肝炎病毒rna的量。在一种实施方式中,通过pcr方法和乙型肝炎病毒dna定量标准品的定量标准曲线来定量所述乙型肝炎病毒dna的量。在一种实施方式中,所述方法包括以下步骤:步骤1:提取所述样品中乙型肝炎病毒的核酸dna和rna;步骤2:针对乙型肝炎病毒dna和rna序列的共同保守区域设计特异性上、下游引物和探针;步骤3:用所述引物和探针分别配制含逆转录酶的荧光pcr试剂和不含逆转录酶的荧光pcr试剂,用pcr方法检测所述样品中乙型肝炎病毒的核酸dna和rna,其中用不含逆转录酶的荧光pcr试剂检测乙型肝炎病毒dna时设置标准曲线对样品中乙型肝炎病毒dna进行标定;和步骤4:根据以下公式计算样品中的乙型肝炎病毒rna量:根据以下公式计算样品中的乙型肝炎病毒rna量:其中ctrna+dna为含逆转录酶的荧光pcr试剂扩增ct值,ctdna为不含逆转录酶的荧光pcr试剂扩增ct值,qdna为样品中标定的乙型肝炎病毒dna浓度,qrna为样品中的乙型肝炎病毒rna的浓度。在一种实施方式中,所述步骤3中的pcr方法是rt-pcr方法,即在pcr扩增之前,包含一步逆转录酶扩增过程。在一种实施方式中,步骤1中乙型肝炎病毒的dna和rna的提取是dna和rna同时提取。在一种实施方式中,所述上、下游引物的tm值55℃~65℃,gc含量40%-60%;和所述探针的tm值65℃~75℃,gc含量40%-70%。在一种实施方式中,所述步骤2中的上游引物为seqidno:1:gaggctgtaggcataaattgg;下游引物为seqidno:2:acagcttggaggcttgaacagt;和所述探针序列为seqidno:3:tgttcaccagcaccatgcaactttttc。在一种实施方式中本发明提供在上述方法中使用的系统,所述系统包括:a.提取乙型肝炎病毒的dna和rna的提取试剂盒;b.用于扩增乙型肝炎病毒的rna的含逆转录酶的荧光pcr扩增体系和用于扩增乙型肝炎病毒的dna的不含逆转录酶的荧光pcr扩增体系;和c.用于乙型肝炎病毒的dna定量的标准品。在一种实施方式中,所述系统还包括阳性质控品、阴性质控品和内参质控。在一种实施方式中,本发明提供上述系统在乙肝指导用药中的应用。本发明的主要优点如下:1、检测hbvdna和rna的灵敏度高达5iu/ml;2、检测范围广,可以有效检出乙肝各基因型,包括a、b、c、d、e、f、h基因型;3、本发明检测体系对其他病原体或人基因组无非特异扩增,特异性好;4、在没有hbvrna标准物质的情况下,通过直接定量hbvdna的量来定量hbvrna的量,简单、方便;5、同时检测样品中hbv的总核酸dna和rna,检测灵敏度提高,避免因药物治疗过程对dna或rna的抑制而导致的假阴性;6、同时对样品中的hbvdna和hbvrna进行准确定量检测,为患者抗病毒治疗方案及是否停药提供有效的数据支持。附图说明为了更清楚地说明本申请实施例中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本申请中记载的一些实施例,对于本领域普通技术人员来说,在不付出创造性劳动的前提下,还可以根据这些附图获得其它的附图。图1表示含逆转录酶的荧光pcr反应液检测样品中hbvdna和rna总核酸(fam通道)和内标(vic通道)扩增曲线图;图2表示不含逆转录酶的荧光pcr反应液检测样品中hbvdna(fam通道)和内内标(vic通道)的扩增曲线图;图3表示不含逆转录酶的荧光pcr反应液检测4个工作标准品的扩增曲线图;图4表示不含逆转录酶的荧光pcr反应液检测4个工作标准品的标准曲线图;图5表示本发明计算hbvrna浓度与ddpcr定量浓度的相关性。具体实施方式为了使本领域
技术领域:
人员更好地理解本申请中的技术方案,下面将结合实施例对本发明作进一步说明,显然,所描述的实施例仅仅是本申请一部分实施例,而不是全部的实施例。基于本申请中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其它实施例,都应当属于本申请保护的范围。下述实施例中,如无特殊说明,均为本领域常规方法。以下实施例中,所用的材料,如无特殊说明,均为本领域常规生化试剂公司买得到的。在下列实施例中均使用病毒dna/rna提取试剂盒制备样品dna和rna。实施例1:本发明定量检测样品中hbvrna1.引物探针设计实施例分析了hbv不同型别(a-h)的dna和rna序列,找出保守区域设计上、下游引物及探针,相关参数为:引物:tm值55.0℃-60.0℃,gc值40.0%-60.0%;上游引物序列:gaggctgtaggcataaattgg(seqidno:1)下游引物序列:acagcttggaggcttgaacagt(seqidno:2)探针:tm值65.0℃-75.0℃,gc值40%-70%,对探针进行5’端fam标记,3’端bhq1标记。探针序列:fam-tgttcaccagcaccatgcaactttttc-bhq1(seqidno:3)2.荧光pcr反应体系a)含逆转录酶的荧光pcr反应体系(以下简rna+dna反应液)b)不含逆转录酶的荧光pcr反应体系(以下简称dna反应液)3.荧光pcr反应程序:50℃15分钟、95℃10分钟;5个循环:95℃15秒,55℃45秒;40个循环:95℃15秒,55℃45秒(收集荧光)。4.结果分析a).设置扩增曲线的基线和阈值线在合适的位置;b).分别统计“rna+dna反应液”和“dna反应液”检测的ct值,分别记为ct(rna+dna)和ctdna;c).在对应的反应孔输入hbvdna工作标准品的浓度,分析得出各样品hbvdna浓度,记为qdna。d).将ct(rna+dna)、ctdna、qdna值带入以下公式,计算得出hbvrna的浓度。5.实验结果同一份样品在2种不同反应体系中的扩增曲线图分别见图1和图2;本发明表示不含逆转录酶的荧光pcr反应液检测4个工作标准品的扩增曲线图如图3所示;不含逆转录酶的荧光pcr反应液检测4个工作标准品的标准曲线图如图4所示。样品检测rna+dna的ct值小于单检测hbvdna的ct值,即样品中hbvrna+dna的浓度大于dna浓度,说明hbv总核酸(dna+rna)的量高于dna的量。rna+dna反应液和dna反应液检测各样品的统计结果见表1。表1.两组反应体系扩增样本中hbv效率比较样品编号ct(rna+dna)ctdnadna定量计算hbvrna量13026.5927.591.78e+041.78e+0413311.6822.564.97e+059.36e+0813721.0122.295.95e+058.50e+0514515.9123.183.29e+055.04e+0714624.9926.643.32e+047.10e+0425-2118.2220.252.29e+067.06e+0626-2420.4321.191.23e+068.53e+0526-6316.1917.51.42e+072.10e+0726-0216.317.461.45e+071.79e+0727-6517.2418.298.42e+069.01e+06实施例2:本发明检测hbvrna的准确性为了比较本发明定量检测hbvrna的准确性,采用ddpcr进行对比。1.ddpcr引物探针设计针对hbvrna设计保守上、下游引物及探针(参考中国专利201810682313.8):上游引物序列:ggaggctgtaggcataaattggtc(seqidno4);下游引物序列:atcgtcgtcgtaggctgctc(seqidno5)逆转录引物序列:atcgtcgtcgtaggctgctctttttttttttttttgw(seqidno6)探针:5'-fam-cctactgttcaagcctccaagctgtg-bhq1-3'(seqidno7)2.ddpcr反应体系ddpcr反应体系如下:试剂1人份buffermix4.81μl引物mix2.6μl酶mix0.59μl模板6.5μl总体积14.5μl将ddpcr反应液通过3dchiploader转移至芯片,覆盖immersionfluid,于proflextm仪器反应。3.ddpcr反应程序:50℃15分钟、95℃10分钟;5个循环:95℃15秒,55℃45秒;40个循环:95℃15秒,55℃45秒(收集荧光);60℃2min,10℃∞4.实验结果通过本发明方法计算所得hbvrna浓度与ddpcr绝对定量的hbvrna浓度相差不大,10份样品检测hbvrna浓度的log10对数值相关性r2为0.9865(图5),说明计算所得hbvrna浓度准确。表2.本发明方法定量检测hbvrna浓度与ddpcr定量浓度的比较样品编号计算hbvrna量ddpcr定量结果1301.78e+042.51e+041339.36e+087.32e+081378.50e+058.66e+051455.04e+074.19e+071467.10e+046.47e+0425-217.06e+068.51e+0626-248.53e+057.99e+0526-632.10e+071.52e+0726-021.79e+074.58e+0727-659.01e+067.53e+06应该理解到披露的本发明不仅仅限于描述的特定的方法、方案和物质,因为这些均可变化。还应理解这里所用的术语仅仅是为了描述特定的实施方式方案的目的,而不是意欲限制本发明的范围,本发明的范围仅受限于所附的权利要求。本领域的技术人员还将认识到,或者能够确认使用不超过常规实验,在本文中所述的本发明的具体的实施方案的许多等价物。这些等价物也包含在所附的权利要求中。序列表<110>江苏宏微特斯医药科技有限公司<120>定量检测样品中乙型肝炎病毒rna的方法及其系统<160>7<170>siposequencelisting1.0<210>1<211>21<212>dna<213>人工序列(artificialsequence)<400>1gaggctgtaggcataaattgg21<210>2<211>22<212>dna<213>人工序列(artificialsequence)<400>2acagcttggaggcttgaacagt22<210>3<211>27<212>dna<213>人工序列(artificialsequence)<400>3tgttcaccagcaccatgcaactttttc27<210>4<211>24<212>dna<213>人工序列(artificialsequence)<400>4ggaggctgtaggcataaattggtc24<210>5<211>20<212>dna<213>人工序列(artificialsequence)<400>5atcgtcgtcgtaggctgctc20<210>6<211>37<212>dna<213>人工序列(artificialsequence)<400>6atcgtcgtcgtaggctgctctttttttttttttttgw37<210>7<211>26<212>dna<213>人工序列(artificialsequence)<400>7cctactgttcaagcctccaagctgtg26当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1