一种用于实时荧光定量核酸扩增检测的装置、系统及方法与流程
本发明涉及核酸扩增检测技术领域,特别是一种用于实时荧光定量核酸扩增检测的装置、系统及方法。
背景技术:
聚合酶链反应(pcr)是一种在分子生物学中广泛使用的技术,通过模拟生物体内dna复制条件,利用dna聚合酶反应,特异性扩增某一dna片段。pcr技术对于人类诊断中的基因测序,分子克隆和基因突变分析是必不可少的。pcr反应过程通常涉及变性,退火,延伸三个步骤,这些步骤需要对反应体系进行变温,控温操作来实现。pcr仪或热循环仪通过在循环程序中调节温度,用于核酸样本的扩增和检测。根据规模,复杂性和应用需求,自pcr仪问世以来的几十年中,pcr仪的机械技术不断进步;设备的安全性,热块可靠性和总体设计规格都不断得到更新和发展,同时涌现了多种pcr设备。例如定量pcr(qpcr)提供了基于参考标准的定量数据;数字pcr(dpcr)提供了无标准的高灵敏度定量分析;数字液滴pcr(ddpcr)使用了大量的样品分区来生成高通量数据。其中,结合微流体技术的定量pcr设备可实现快速核酸扩增和高通量检测,是目前pcr设备发展的前沿。
微流体芯片是一组微通道,这些通道被蚀刻或模制到特定材料上(玻璃,硅或聚二甲基硅氧烷等聚合物)。形成微流控芯片的微通道连接在一起,以实现混合,泵送,分选或控制生化环境等所需的功能。在生物医学领域,通过微流体技术将多种医学测试集成在单个芯片上,可实现芯片实验室(laboratoriesonachip)的愿景。此外,微流体技术的应用可使昂贵试剂的消耗减少,简化复杂的工作流程,提高其具有固有的临床价值。
定量pcr(qpcr)具有出色的检测阈值,信号分析响应和动态范围。然而,复杂的控温程序与单一的进样方式仍旧是制约qpcr装置发展与更新的核心问题。大多数商业上可用的实时qpcr平台仍需频繁的控温操作,这增加了核酸扩增与检测的消耗时间,降低了反应效率。而在传统qpcr设备运行过程中,多个样品必须批次反应,统一检测,同时结束,这令传统qpcr设备难以实现单个或不同批次样品的灵活安排,从而不能成为真正的高通量检测。
技术实现要素:
本发明的主要目的是提供一种用于实时荧光定量核酸扩增检测的装置、系统及方法,对核酸扩增检测尤其是其控温操作进行优化,实现快速灵活控制的核酸扩增与检测,简化操作的同时降低时间和物料成本,提高检测效率。
为实现上述目的,本发明采用以下技术方案:
一种用于实时荧光定量核酸扩增检测的装置,包括微流控单元、进样单元、温控单元以及驱动单元,所述微流控单元上设置有一条或多条并行的环形流道,所述环形流道具有进液口和出液口,所述进样单元设置于所述环形流道的进液口,用于向所述环形流道内进样,所述温控单元与所述微流控单元相配合设置,用于对所述环形流道进行分段控温,所述驱动单元与所述微流控单元相配合设置,用于驱动所述环形流道内的微流体运动,所述环形流道的至少一段为透明材质,以便进行荧光检测,其中,所述温控单元经配置以使所述环形流道的不同流段具有不同的预定温度,所述微流体通过在所述环形流道内不同温度的流段的移动,实现变温操作。
进一步地:
所述温控单元包括对应覆盖于所述环形流道的三个不同流段外的三块温控板,通过控制各温控板实施所述分段控温,对应于微流体内核酸变性、退火、延伸的不同需求设定不同温度,在所述温控板上或在所述温控板之间设置有对应于所述环形流道的透明段的荧光检测槽,优选地,所述透明段和所述荧光检测槽设置在所述环形流道的起点处,以检测每一个流动循环结束后的微流体荧光值。
各温控板为扇形,所述三块温控板形成为对应于所述环形流道的环形结构。
所述进样单元包括微流体发生器和进样泵,所述微流体发生器通过进样泵连接所述环形流道的进液口,含有样品的pcr反应液和磁流体输入所述微流体发生器,在所述微流体发生器内,磁流体液滴包裹在所述样品的外层而形成带磁性的微流体液滴,并通过所述进样泵将所述微流体液滴泵入所述环形流道中,优选地,还包括设置在所述出液口的排液泵。
所述驱动单元为气压驱动、低速离心力驱动、机械力驱动或磁力驱动。
所述驱动单元包括气泵和设置在所述环形流道上与所述气泵相连的气孔。
所述驱动单元包括设置在所述环形流道的圆周中心的转轴以及与所述转轴相连并径向延伸到所述环形流道上方的转臂,所述转臂为带磁性的转臂或在所述转臂上设置有磁力装置,所述微流体经改性后带磁性。
一种微流体实时荧光定量核酸扩增检测系统,包括所述的用于实时荧光定量核酸扩增检测的装置和用于对所述环形流道内的样品进行实时荧光核酸扩增检测的检测单元,所述检测单元包括荧光检测器,优选地,所述荧光检测器包括激发光源、成像系统以及ccd相机。
一种微流体实时荧光定量核酸扩增检测方法,使用所述的微流体实时荧光定量核酸扩增检测系统进行实时荧光定量核酸扩增检测,所述方法包括如下步骤:
通过所述温控单元对所述微流控单元的环形流道的不同流段加热至所需温度;
通过所述进样单元将待测微流体输入所述环形流道;
通过所述驱动单元驱动所述微流体沿所述环形流道按照设定的循环数进行单向循环流动,每个循环经过不同温度的流段,对所述微流体内反应液实现程序变温,进行扩增反应,并通过所述检测单元进行实时荧光定量核酸扩增检测。
进一步地,所述方法还包括:在设定的循环周期结束后将所述微流体从所述环形流道内排出,通过所述进样单元向所述环形流道内泵入清洗液进行流道清洗。
本发明具有如下有益效果:
本发明提供了一种用于实时荧光定量核酸扩增检测的装置、系统及方法,本发明的装置能够实现对核酸扩增检测仪变温程序的优化和简化,显著减少升降温操作造成的时间与能量损耗,实现快速、高通量、灵活控制的核酸扩增与检测操作。操作者只需将待测样品加入微流控单元的环形流道中,本装置即可自动进行扩增与检测步骤。本装置的自动化操作中,利用温控单元,优选为覆盖环形流道的多个温控板,改变同一环形流道内的不同流段的温度,通过驱动单元的驱动微流体在同一环形流道内移动,较佳为匀速移动,经过不同温度的流道段,实现程序变温操作。微流体可通过在同一环形流道的单向循环移动,实现多个程序变温的循环周期,并可对每一个循环结束后的微流体荧光值进行检测。
藉由上述方案,本发明相对于现有技术至少具有以下优点:
1.本装置为自动化程度高,人员的操作大大简化。
2.核酸在该设备中进行扩增反应时,不需频繁升降温操作。
3.本装置可令反应中的核酸得到快速,无缝衔接的温度切换,增强反应效率。
4.利用微流体技术,可减少反应体系体积,并可在同一流道添加多批样品,以实现高通量检测。
5.可在已有样品在流道反应中的情况下随时进样,实时检测。
6.单位样品进行扩增反应所需时间比传统qpcr仪至少缩小约3mins。
总之,本发明能够实现耗时短、高通量、可控性强的核酸扩增和检测,对比传统qpcr仪大大缩小了反应时间,从而快速得到多种目标物检测结果;本发明微流体实时荧光定量核酸扩增检测系统可以替代传统非微流控qpcr仪,广泛地适用于核酸分子诊断,并降低时间和物料成本,简化人为操作,进而提高检测效率。
附图说明
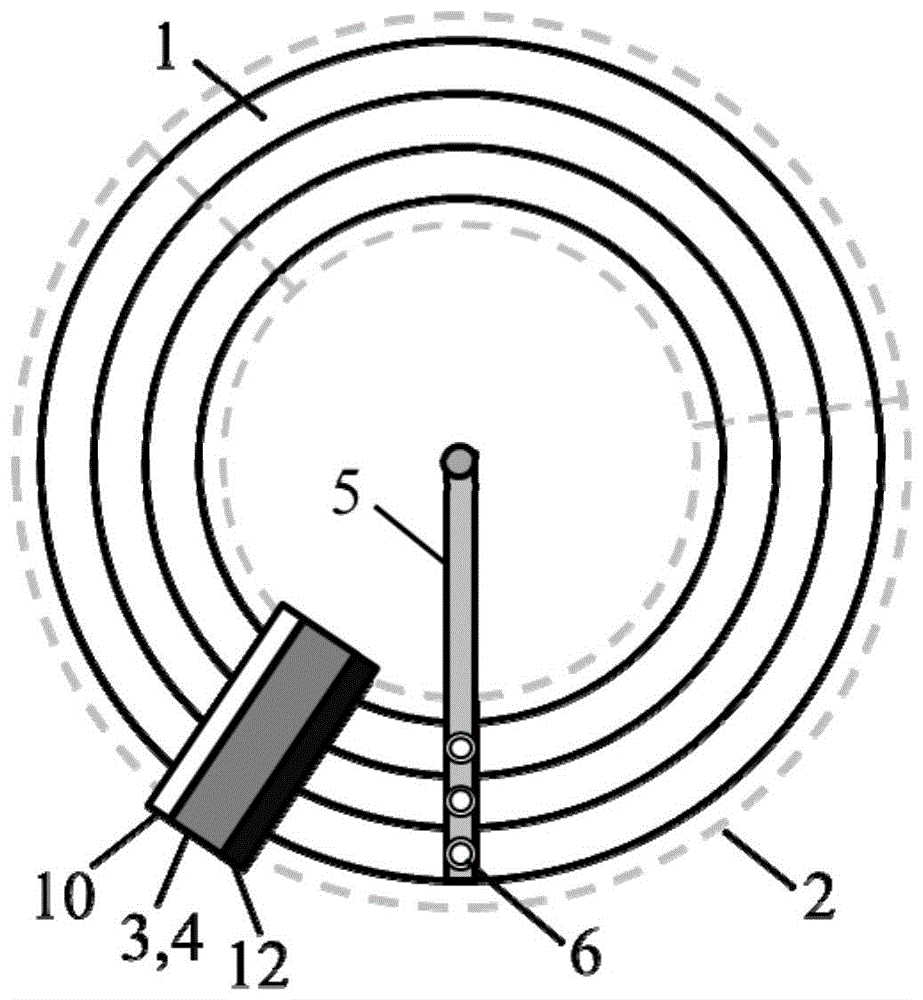
图1为本发明一种实施例的实时荧光定量核酸扩增检测系统的整体示意图。
图2为本发明一种实施例中的温控板示意图。
图3为本发明一种实施例中的微流体发生器与进样泵示意图。
图4为本发明一种实施例中的驱动单元的转轴示意图。
具体实施方式
以下对本发明的实施方式作详细说明。应该强调的是,下述说明仅仅是示例性的,而不是为了限制本发明的范围及其应用。
需要说明的是,当元件被称为“固定于”或“设置于”另一个元件,它可以直接在另一个元件上或者间接在该另一个元件上。当一个元件被称为是“连接于”另一个元件,它可以是直接连接到另一个元件或间接连接至该另一个元件上。另外,连接既可以是用于固定作用也可以是用于电路/信号连通作用。
需要理解的是,术语“长度”、“宽度”、“上”、“下”、“前”、“后”、“左”、“右”、“竖直”、“水平”、“顶”、“底”“内”、“外”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本发明实施例和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本发明的限制。
此外,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多该特征。在本发明实施例的描述中,“多个”的含义是两个或两个以上,除非另有明确具体的限定。
图1为本发明一种实施例的微流体实时荧光定量核酸扩增检测系统的整体示意图。本发明实施例提出一种用于实时荧光定量核酸扩增检测的装置,包括微流控单元、进样单元、温控单元2以及驱动单元5,所述微流控单元上设置有一条或多条并行的环形流道1,所述环形流道1具有进液口和出液口,所述进样单元设置于所述环形流道1的进液口,用于向所述环形流道1内进样,所述温控单元2与所述微流控单元相配合设置,用于对所述环形流道1进行分段控温,所述驱动单元5与所述微流控单元相配合设置,用于驱动所述环形流道1内的微流体运动,所述环形流道1的至少一段为透明材质,以便进行荧光检测,其中,所述温控单元2经配置以使所述环形流道1的不同流段具有不同的预定温度,所述微流体通过在所述环形流道1内不同温度的流段的移动,实现变温操作。
进行检测时,所述驱动单元5可驱动微流体在同一环形流道1内不同温度的流道段匀速移动,实现程序变温操作。微流体通过在同一环形流道1的单向循环移动,可实现多个程序变温的循环周期。
图2为本发明一种实施例中的温控板示意图。在优选的实施例中,所述温控单元2包括对应覆盖于所述环形流道1的三个不同流段外的三块温控板,通过控制各温控板实施所述分段控温,对应于微流体内核酸变性、退火、延伸的不同需求设定不同温度,在所述温控板上或在所述温控板之间设置有对应于所述环形流道1的透明段的荧光检测槽11,优选地,所述透明段和所述荧光检测槽11设置在所述环形流道1的起点处,以检测每一个流动循环结束后的微流体荧光值。优选地,各温控板为扇形,所述三块温控板形成为对应于所述环形流道1的环形结构。
图3为本发明一种实施例中的微流体发生器与进样泵示意图。在优选的实施例中,所述进样单元包括微流体发生器3和进样泵4,所述微流体发生器3通过进样泵4连接所述环形流道1的进液口,含有样品7的pcr反应液和磁流体输入所述微流体发生器3,在所述微流体发生器3内,磁流体液滴8包裹在所述样品7的外层而形成带磁性的微流体液滴6,并通过所述进样泵4将所述微流体液滴6泵入所述环形流道1中,优选地,还包括设置在所述出液口的排液泵12。
所述pcr反应液可含扩增模板、酶、引物、镁离子和反应缓冲剂,如图3所示,可将需要扩增检测的样品7通过排枪加入到微流体发生器3中。磁流体液滴8经过微流体发生器3包裹在样品7外层,形成带磁性的微流体液滴6。带磁性的微流体液滴6通过进样泵4泵入环形微流体流道1中后,在驱动单元5的驱动下开始循环匀速移动。
在不同的实施例中,所述驱动单元5可以为气压驱动、低速离心力驱动、机械力驱动或磁力驱动等。
在一个实施例中,所述驱动单元5包括气泵和设置在所述环形流道1上与所述气泵相连的气孔。
参见图1和图4,在一个实施例中,所述驱动单元5包括设置在所述环形流道1的圆周中心的转轴以及与所述转轴相连并径向延伸到所述环形流道1上方的转臂,所述转臂为带磁性的转臂,或是在所述转臂上设置有磁力装置9,所述微流体经改性后带磁性,从而可随所述转臂的转动而被磁力装置9驱动以沿着所述环形流道1移动。转轴连接驱动源,如电机。
参阅图1,本发明的实施例还提供一种微流体实时荧光定量核酸扩增检测系统,包括前述任一实施例的用于实时荧光定量核酸扩增检测的装置和用于对该装置的环形流道1内的样品进行实时荧光核酸扩增检测的检测单元,所述检测单元包括荧光检测器10,优选地,所述荧光检测器10包括激发光源、成像系统以及ccd相机。核酸检测基于实时荧光核酸扩增检测技术(rt-qpcr)。
本发明的实施例还提供一种微流体实时荧光定量核酸扩增检测方法,使用所述的微流体实时荧光定量核酸扩增检测系统进行实时荧光定量核酸扩增检测,所述方法包括如下步骤:
通过所述温控单元2对所述微流控单元的环形流道1的不同流段加热至所需温度;
通过所述进样单元将待测微流体输入所述环形流道1;
通过所述驱动单元5驱动所述微流体沿所述环形流道1按照设定的循环数进行单向循环流动,每个循环经过不同温度的流段,对所述微流体内反应液实现程序变温,进行扩增反应,并通过所述检测单元进行实时荧光定量核酸扩增检测。
进一步地,所述方法还包括:在设定的循环周期结束后将所述微流体从所述环形流道1内排出,通过所述进样单元向所述环形流道1内泵入清洗液进行流道清洗。
以下结合附图进一步描述本发明的具体实施例。
如图1所示实施例的微流体实时荧光定量核酸扩增检测系统,包括微流控单元、进样单元(本实施例兼作为清洗单元)、温控单元2、驱动单元5以及检测单元。微流控单元上设置有闭环流通的环形流道1,用于微流体在流道内移动并发生扩增反应。进样单元设置于环形流道1一端,涉及微流体发生器3,进样泵4,排液泵12等外部单元。温控单元2中设置三块变温板,覆盖于微流体环形流道1上,用于流道的分段控温;驱动单元5与微流控单元匹配,可利用微流体磁性、重量或表面张力等特性通过转轴驱动微流体运动;检测单元为荧光检测系统,置于微流控单元外部,可包括激发光源、ccd相机等。
其中,温控单元2利用多块温控板覆盖微流体环形流道1的方式改变同一环形流道1内不同流段的温度。微流体通过在同一环形流道1内不同温度的流道段匀速移动,实现程序变温操作。微流体通过在同一环形流道1的单向循环移动,实现多个程序变温的循环周期。温控板上或在所述温控板之间对应所述环形流道1的起点和透明段设置荧光检测槽11,以检测每一个循环结束后的微流体荧光值。所述环形流道1至少设置其中一段为透明材质,以便进行荧光检测。
其中,以外部预混好模板、酶、引物、镁离子的pcr混合反应液为主体,通过微流体发生器3包裹成带有特殊属性的微流体,所述特殊属性包括磁化,表面改性,特殊材料包裹等。所述微流体形成后通过进样泵4进入环状微流体流道,通过驱动系统在环形流道1内进行单向循环运动。所述驱动系统对微流体的驱动力通过磁力、气压、旋转力或机械力等实现。
其中,该流道为密闭的环形闭合流道,可设置为单个或多个流道并行。所述环形流道1上置单个或并排进样孔,供进样泵4往流道内泵入微流体。
其中,根据所设计的微流体特质,不限于某一种微流体驱动方法,可以采用低速离心、外加压力、磁力驱动等多种方式,优选高通量流体驱动方法。例如,若使用气压驱动微流体,所述驱动单元5包括气泵,所述环形流道1设置相应气孔。
优选地,使用磁力驱动微流体,所述驱动单元5包括转轴和带磁性的转臂,所述微流体液滴6经改性具有磁性。
其中,根据所述微流体内pcr反应液所需的反应条件,驱动微流体在所述环形流道1内匀速流动。若所述环形流道1并联进样或同一流道多次进样,微流体驱动系统将保持环形流道1内所有微流体匀速流动。
其中,可根据微流体内核酸变性、退火、延伸的不同需求设定不同温度,设置至少三块不同温度的控温板覆盖于所述环形微流体流道。
其中,所述荧光检测系统可包括但不限于激发光源、滤光片、ccd相机、图像成像系统。所述荧光检测系统可置于环形微流体流道一侧,实时检测流道内微流体荧光信号,并传输数据生成图像。
其中,微流控单元、进样单元以及驱动单元5所用的材料不限于采用聚氯乙烯(pvc),聚乙烯(pe)、聚丙烯(pp)、聚苯乙烯(ps)、聚碳酸酯(pc)、abs等常见的医用塑料或玻璃制品。
利用如图1所示实施例的微流体实时荧光定量核酸扩增检测装置进行核酸扩增检测的方法可包括如下步骤:
(1)使用注射枪从外部将预混好的pcr反应液注入所述微流体生成器;同时所述控温板开始加热至所需温度;
(2)所述微流体生成器生成带有特殊属性的含pcr混合反应液的微流体,通过进样泵4泵入所述环形微流体流道;
(3)在所述微流体驱动系统的驱动下,微流体开始沿流道进行单向循环流动。因微流体经过不同温度的流道,微流体内反应液实现了程序变温,开始进行扩增反应,同时所述荧光检测系统开始工作;
(4)微流体在所述环形流道1内按照设定的循环数循环运动,仪器内软件开始工作,将检测到的信号传输至处理器并将其可视化。
(5)通过操控软件的计时或计数算法,在适当的循环周期结束后将微流体排出,待全部微流体排出后可通过进样泵4泵入清洗液进行流道清洗。
检测实例
按照待扩增检测样品7制作成磁性微流体,实施例利用磁力装置9驱动微流体进行操作。但本发明并不局限于此实施例。
本实施例将已经预混好的pcr反应液,内含扩增模板,酶,引物,镁离子和反应缓冲剂,如图3中所示,将需要扩增检测的样品7通过排枪加入到微流体发生器3中。磁流体液滴8经过微流体发生器包裹在样品7外层,形成带磁性的微流体液滴6。微流体液滴6通过进样泵4泵入微流体环形流道1中开始循环匀速移动。根据实验需求,以pcr反应需程序变温:以94℃变性---50℃退火---72℃延伸为例。预先将温控板中a,b,c三个模块段加热至a:94℃,b:50℃,c:72℃。微流体液滴6泵入温控板中的a段起始,同时驱动单元5开始工作,通过磁力装置9带动流道内微流体液滴6开始匀速运动,如图1所示。由外部操控软件操控,令驱动单元5控制微流体液滴6以设定好的时间匀速依次走完a、b、c三段,即完成一个循环。一个循环结束后,使用荧光检测器10透过检测槽11检测微流体6的荧光值并上传数据至分析软件。然后微流体液滴6重新进入a段,开始第二轮循环。如此循环往复,经历40个循环后,扩增与检测反应全部结束,操控软件分析得到荧光增量图。此时将启动排液泵12将结束反应的微流体排出。若环形微流道内所有微流体均已排出,将启动进样泵3泵入清洗液清洗所有流道。本实例还可实现在有多个微流体在流道内反应时,在并联流道实时添加新样品检测,不影响当前正在扩增检测的微流体。如可设置多个微流体驱动转轴,假设其中某微流体驱动转轴上已有的微流体反应结束并排出后,空出磁力装置9。其时即可添加新的微流体液滴6,开展新的扩增反应。
本发明的背景部分可以包含关于本发明的问题或环境的背景信息,而不一定是描述现有技术。因此,在背景技术部分中包含的内容并不是申请人对现有技术的承认。
以上内容是结合具体/优选的实施方式对本发明所作的进一步详细说明,不能认定本发明的具体实施只局限于这些说明。对于本发明所属技术领域的普通技术人员来说,在不脱离本发明构思的前提下,其还可以对这些已描述的实施方式做出若干替代或变型,而这些替代或变型方式都应当视为属于本发明的保护范围。在本说明书的描述中,参考术语“一种实施例”、“一些实施例”、“优选实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。尽管已经详细描述了本发明的实施例及其优点,但应当理解,在不脱离专利申请的保护范围的情况下,可以在本文中进行各种改变、替换和变更。
- 还没有人留言评论。精彩留言会获得点赞!