用于最小化条形码交换的方法和系统与流程
用于最小化条形码交换的方法和系统
1.交叉引用
2.本申请要求提交于2018年8月3日的美国临时专利申请62/714,476的权益,所述申请以引用方式全文并入本文。
背景技术:
3.可以出于各种目的,例如鉴定样品内的部分的类型,对样品进行处理。样品可以是生物样品。可以例如检测疾病(例如癌症)或鉴定特定物质,对生物样品进行处理。存在各种用于处理样品的方法,例如聚合酶链式反应(pcr)和测序。
4.可以在各种反应环境内,例如分区内,对生物样品进行处理。分区可以是孔或液滴。液滴或孔可用于以使得能够分配生物样品并单独处理的方式来处理生物样品。例如,此类液滴可以与其他液滴流体分离,从而使得能够精确控制液滴中的相应环境。
5.分区中的生物样品可以经受各种过程,例如化学过程或物理过程。分区中的样品可以经受加热或冷却,或化学反应,例如以获得可以定性或定量处理的物质。
6.某些应用可能受益于对从更大的群体中获得的单细胞中获得的物质的扩增或测序。在一些情况下,单个目标细胞可能非常罕见。因此,需要允许对来自单个目标细胞的核酸进行测序的样品制备技术。
技术实现要素:
7.在一方面,本文提供了一种用于核酸处理的方法,所述方法包括:(a)在多个分区中,使用来自多个核酸条形码分子的核酸条形码分子和多个核酸分子来生成多个条形码化核酸分子;(b)从所述多个分区回收所述多个条形码化核酸分子,以产生包含所述多个核酸条形码分子和所述多个核酸条形码分子的剩余部分的混合物;(c)在(b)之后,使所述混合物经受足以将阻断寡核苷酸偶联至所述多个核酸条形码分子的所述剩余部分的条件,其中所述阻断寡核苷酸包含:(i)互补区,所述互补区包含与所述多个核酸条形码分子的所述剩余部分中的序列至少75%互补的序列;和(ii)3’阻断基。
8.在一些实施方案中,所述3’阻断基被配置成防止所述剩余部分与核酸分子连接。在一些实施方案中,所述3’阻断基被配置成当与靶核酸分子杂交时防止所述引物序列延伸。在一些实施方案中,所述多个分区是多个液滴。在一些实施方案中,所述多个分区是多个孔。在一些实施方案中,所述阻断寡核苷酸从5’到3’包含第一茎序列、环序列、与所述第一茎序列至少75%互补的第二茎序列,和所述互补区。在一些实施方案中,所述3’阻断基在所述阻断寡核苷酸的3’端。在一些实施方案中,所述3’阻断基是2
’‑3’‑
二脱氧胞嘧啶(ddc)、2
’‑5’
连接的核苷、3’c3间隔子、氨基修饰的c6、反向脱氧胸苷(dt)、3’氨基修饰的核苷酸或3’磷酸基。在一些实施方案中,所述2
’‑5’
连接的核苷是3
’‑
脱氧胸苷(3
’‑
dt)、3
’‑
脱氧胞苷(3
’‑
dc)、3
’‑
脱氧腺苷(3
’‑
da)或3
’‑
脱氧鸟苷(3
’‑
dg)。在一些实施方案中,将所述阻断寡核苷酸连接至所述剩余部分。在一些实施方案中,所述阻断寡核苷酸包含5’磷酸基。
9.在另一方面,本文公开了一种组合物,所述组合物包含:核酸分子,所述核酸分子
从5’到3’包含:(a)第一区域,所述第一区域包含条形码序列和引物序列;以及(b)第二区域,所述第二区域包含(i)与所述引物序列互补的序列;和(ii)3’阻断基。在一些实施方案中,所述3’阻断基在所述阻断寡核苷酸的3’端。在一些实施方案中,所述3’阻断基是2
’‑3’‑
二脱氧胞嘧啶(ddc)、2
’‑5’
连接的核苷、3’c3间隔子、氨基修饰的c6、反向脱氧胸苷(dt)、3’氨基修饰的核苷酸或3’磷酸基。在一些实施方案中,所述2
’‑5’
连接的核苷是3
’‑
脱氧胸苷(3
’‑
dt)、3
’‑
脱氧胞苷(3
’‑
dc)、3
’‑
脱氧腺苷(3
’‑
da)或3
’‑
脱氧鸟苷(3
’‑
dg)。在一些实施方案中,所述第二区域从5’到3’包含:第一茎序列、环序列、与所述第一茎序列至少75%互补的第二茎序列、与所述引物序列互补的所述序列,和所述3’阻断基。
10.在另一方面,本文公开了一种用于核酸处理的方法,所述方法包括:(a)提供反应混合物,所述反应混合物包含:(i)模板核酸分子;(ii)rnase酶;和(iii)多个核酸条形码分子,其中所述多个核酸条形码分子中的每个核酸条形码分子包含:(a)共同条形码序列;(b)能够与靶核酸杂交的序列;(c)至少一个核糖核苷酸;和(d)3’阻断基;(b)使所述反应混合物经受足以使所述模板核酸分子与所述多个核酸条形码分子中的核酸条形码分子杂交的条件;(c)使所述反应混合物经受足以使所述rnase酶降解所述核糖核苷酸从而释放所述3’阻断基的条件;以及(d)使用所述模板核酸分子和所述核酸条形码分子来生成条形码化模板核酸分子。在一些实施方案中,所述3’阻断基被配置成防止所述剩余部分与核酸分子连接。在一些实施方案中,所述3’阻断基被配置成当与靶核酸分子杂交时防止所述引物序列延伸。在一些实施方案中,所述共同条形码序列在所述至少一个核糖核苷酸和所述3’阻断基的5’。在一些实施方案中,所述3’阻断基在所述多个核酸条形码分子的3’端。在一些实施方案中,所述3’阻断基是2
’‑3’‑
二脱氧胞嘧啶(ddc)、2
’‑5’
连接的核苷、3’c3间隔子、氨基修饰的c6、反向脱氧胸苷(dt)、3’氨基修饰的核苷酸或3’磷酸基。在一些实施方案中,所述2
’‑5’
连接的核苷是3
’‑
脱氧胸苷(3
’‑
dt)、3
’‑
脱氧胞苷(3
’‑
dc)、3
’‑
脱氧腺苷(3
’‑
da)或3
’‑
脱氧鸟苷(3
’‑
dg)。在一些实施方案中,所述方法还包括将所述反应混合物共同分配到分区中。在一些实施方案中,所述分区是孔。在一些实施方案中,所述分区是乳液中的水性液滴。在一些实施方案中,所述多个核酸条形码分子附接至珠粒。在一些实施方案中,所述多个核酸条形码分子可释放地附接至所述珠粒。在一些实施方案中,所述珠粒是凝胶珠粒。在一些实施方案中,所述凝胶珠粒是可降解凝胶珠粒。在一些实施方案中,所述可降解凝胶珠粒可通过化学刺激来降解。在一些实施方案中,所述化学刺激是还原剂。在一些实施方案中,所述反应混合物包含还原剂。在一些实施方案中,所述rnase酶是rnase h2酶。在一些实施方案中,通过引物延伸生成所述条形码化模板核酸分子。在一些实施方案中,通过核酸扩增生成所述条形码化模板核酸分子。在一些实施方案中,通过连接生成所述条形码化模板核酸分子。在一些实施方案中,在(b)之前,将衔接子序列添加至所述模板核酸分子,并且其中能够与所述靶核酸杂交的所述序列与所述衔接子序列的至少一部分互补。在一些实施方案中,通过转座酶将所述衔接子序列添加至所述模板核酸分子。在一些实施方案中,所述衔接子序列包含测序引物序列,并且其中能够与所述靶核酸杂交的所述序列与所述测序引物序列互补。
11.在另一方面,本文描述了一种部分双链核酸条形码分子,所述部分双链核酸条形码分子包含(a)第一链,所述第一链包含(i)引物退火序列的互补序列和(ii)条形码序列;以及(b)第二链,所述第二链包含(i)5’突出端和(ii)无碱基位点,其中所述第一链和所述
第二链彼此退火。
12.在一些实施方案中,所述无碱基位点在所述5’突出端中。在一些实施方案中,所述无碱基位点位于与所述第一链的3’末端处的碱基退火的所述第二链的碱基的5’的至少3个碱基位置。在一些实施方案中,所述无碱基位点位于与所述第一链的所述3’末端处的碱基退火的所述第二链的碱基的5’的3、4、5、6、7或8个碱基位置。在一些实施方案中,所述无碱基位点在所述第二链中的某个位置,其中如果在所述位置处存在碱基,则所述第一链的3’末端处的碱基将退火。在一些实施方案中,所述第二链包含所述引物退火序列。在一些实施方案中,所述部分双链核酸条形码分子附接至珠粒。在一些实施方案中,所述珠粒是凝胶珠粒。
13.在另一方面,本文公开了一种部分双链核酸条形码分子,所述部分双链核酸条形码分子包含(a)第一链,所述第一链包含(i)引物退火序列的互补序列和(ii)条形码序列;以及(b)第二链,所述第二链包含(i)dna,(ii)5’突出端和(iii)非经典碱基,其中所述第一链和所述第二链彼此退火。
14.在一些实施方案中,所述非经典碱基在所述5’突出端中。在一些实施方案中,所述非经典碱基位于与所述第一链的3’末端处的碱基退火的所述第二链的碱基的5’的至少3个碱基。在一些实施方案中,所述非经典碱基位于与所述第一链的所述3’末端处的碱基退火的所述第二链的碱基的5’的3、4、5、6、7或8个碱基。在一些实施方案中,所述非经典碱基与所述第一链的所述3’末端处的碱基退火。在一些实施方案中,所述非经典碱基包括尿嘧啶。在一些实施方案中,所述第二链包含所述引物退火序列。在一些实施方案中,所述部分双链核酸条形码分子附接至珠粒。在一些实施方案中,所述珠粒是凝胶珠粒。
15.在另一方面,本文提供了一种部分双链核酸条形码分子,所述部分双链核酸条形码分子包含(a)第一链,所述第一链包含(i)引物退火序列的互补序列和(ii)条形码序列;以及(b)第二链,所述第二链包含5’突出端,其中所述第一链和所述第二链彼此退火,并且其中所述第二链被配置成防止聚合酶使用所有的所述5’突出端作为模板来合成链。
16.在一些实施方案中,所述部分双链核酸条形码分子附接至珠粒。在一些实施方案中,所述珠粒是凝胶珠粒。
17.在另一方面,本文提供了一种部分双链核酸条形码分子,所述部分双链核酸条形码分子包含(a)第一链,所述第一链包含(i)引物退火序列的互补序列和(ii)条形码序列;以及(b)第二链,所述第二链包含5’突出端和3’末端,所述3’末端包含防止所述第二链的所述3’末端通过酶延伸的阻断物,其中所述第一链和所述第二链彼此退火。
18.在一些实施方案中,所述阻断物包括c3间隔子、2
’‑3’‑
二脱氧胞嘧啶(ddc)、反向dt、氨基或磷酸酯。在一些实施方案中,所述部分双链核酸条形码分子附接至珠粒。在一些实施方案中,所述珠粒是凝胶珠粒。
19.在一方面,本文提供了一种生成包含无碱基位点的部分双链核酸条形码分子的方法,所述方法包括:(a)提供部分双链核酸条形码分子,所述部分双链核酸条形码分子包含(i)第一链,所述第一链包含(a)引物退火序列的互补序列和(b)条形码序列;和(ii)第二链,所述第二链包含(a)dna,(b)5’突出端和(c)非经典碱基,其中所述第一链和所述第二链彼此退火;以及(b)用剂处理所述部分双链dna,从而在所述非经典碱基的位置处生成无碱基位点。
20.在一些实施方案中,所述非经典碱基是尿嘧啶。在一些实施方案中,所述剂是尿嘧啶
‑
dna
‑
糖基化酶(udg)。在一些实施方案中,所述第二链包含所述引物退火序列。
21.在另一方面,本文提供了一种用于核酸处理的方法,所述方法包括:在多个分区中,使用多个核酸分子中的核酸分子和部分双链核酸条形码分子来生成多个条形码化核酸分子。
22.在一些实施方案中,所述生成包括将所述多个核酸分子中的核酸分子连接至所述部分双链核酸条形码分子。在一些实施方案中,所述连接包括将所述多个核酸分子中的所述核酸分子连接至所述部分双链核酸条形码分子的所述第一链的3’末端。在一些实施方案中,所述多个分区是多个液滴。在一些实施方案中,所述多个分区是多个孔。在一些实施方案中,所述核酸分子是标记片段化的核酸分子。
23.在一些实施方案中,在所述多个分区中的每个分区中,所述部分双链核酸条形码分子的所述条形码序列是唯一的,并且所述引物退火序列的所述互补序列是共同的。
24.在另一方面,本文提供了一种核酸处理的方法,所述方法包括:(a)在多个分区中,(i)将部分双链核酸条形码分子的第二链的5’突出端与核酸分子退火,其中所述部分双链核酸条形码分子的第一链包含(a)共同引物退火序列的互补序列和(b)唯一条形码序列;以及(i)将所述部分双链核酸条形码分子连接至所述核酸分子,从而生成条形码化核酸分子;(a)从所述多个分区汇集所述条形码化核酸分子;(b)使用与所述共同引物退火序列退火的引物扩增所述条形码化核酸分子,其中在所述扩增后所述条形码化核酸分子的条形码交换率小于50%。
25.在一些实施方案中,所述条形码交换率小于10%。在一些实施方案中,所述条形码交换率小于1%。在一些实施方案中,将所述部分双链核酸条形码分子偶联至珠粒。在一些实施方案中,所述珠粒是凝胶珠粒。在一些实施方案中,所述多个分区是多个液滴。在一些实施方案中,所述多个分区是多个孔。在一些实施方案中,所述核酸分子是标记片段化的核酸。
26.在一些实施方案中,本文公开了用于核酸处理的方法,所述方法包括:(a)在多个分区中,使用来自多个核酸条形码分子的核酸条形码分子和多个核酸分子来生成多个条形码化核酸分子;(b)从所述多个分区回收所述多个条形码化核酸分子,以产生包含所述多个核酸条形码分子和所述多个核酸条形码分子的剩余部分的混合物;(c)在(b)之后,使所述混合物经受足以将阻断寡核苷酸偶联至所述多个核酸条形码分子的所述剩余部分的条件,其中所述阻断寡核苷酸包含:(i)互补区,所述互补区包含与所述多个核酸条形码分子的所述剩余部分中的序列至少75%互补的序列;和(ii)3’阻断基。
27.在一些实施方案中,所述3’阻断基被配置成防止所述剩余部分与核酸分子连接。在一些实施方案中,所述3’阻断基被配置成当与靶核酸分子杂交时防止所述引物序列延伸。在一些实施方案中,所述多个分区是多个液滴。在一些实施方案中,所述多个分区是多个孔。
28.在一些实施方案中,所述阻断寡核苷酸从5’到3’包含第一茎序列、环序列、与所述第一茎序列至少75%互补的第二茎序列,和所述互补区。在一些实施方案中,所述3’阻断基在所述阻断寡核苷酸的3’端。在一些实施方案中,所述3’阻断基是2
’‑3’‑
二脱氧胞嘧啶(ddc)、2
’‑5’
连接的核苷、3’c3间隔子、氨基修饰的c6、反向脱氧胸苷(dt)、3’氨基修饰的核
苷酸或3’磷酸基。在一些实施方案中,所述2
’‑5’
连接的核苷是3
’‑
脱氧胸苷(3
’‑
dt)、3
’‑
脱氧胞苷(3
’‑
dc)、3
’‑
脱氧腺苷(3
’‑
da)或3
’‑
脱氧鸟苷(3
’‑
dg)。在一些实施方案中,将所述阻断寡核苷酸连接至所述剩余部分。在一些实施方案中,所述阻断寡核苷酸包含5’磷酸基。
29.在一些实施方案中,本文还公开了一种组合物,所述组合物包含:核酸分子,所述核酸分子从5’到3’包含:(a)第一区域,所述第一区域包含条形码序列和引物序列;以及(b)第二区域,所述第二区域包含(i)与所述引物序列互补的序列;和(ii)3’阻断基。在一些实施方案中,所述3’阻断基在所述阻断寡核苷酸的3’端。在一些实施方案中,所述3’阻断基是2
’‑3’‑
二脱氧胞嘧啶(ddc)、2
’‑5’
连接的核苷、3’c3间隔子、氨基修饰的c6、反向脱氧胸苷(dt)、3’氨基修饰的核苷酸或3’磷酸基。在一些实施方案中,所述第二区域从5’到3’包含:第一茎序列、环序列、与所述第一茎序列至少75%互补的第二茎序列、与所述引物序列互补的所述序列,和所述3’阻断基。
30.在一些实施方案中,本文还公开了用于核酸处理的方法,所述方法包括:(a)提供反应混合物,所述反应混合物包含:(i)模板核酸分子;(ii)rnase酶;和(iii)多个核酸条形码分子,其中所述多个核酸条形码分子中的每个核酸条形码分子包含:(a)共同条形码序列;(b)能够与靶核酸杂交的序列;(c)至少一个核糖核苷酸;和(d)3’阻断基;(b)使所述反应混合物经受足以使所述模板核酸分子与所述多个核酸条形码分子中的核酸条形码分子杂交的条件;(c)使所述反应混合物经受足以使所述rnase酶降解所述核糖核苷酸从而释放所述3’阻断基的条件;以及(d)使用所述模板核酸分子和所述核酸条形码分子来生成条形码化模板核酸分子。
31.在一些实施方案中,所述3’阻断基被配置成防止所述剩余部分与核酸分子连接。在一些实施方案中,所述3’阻断基被配置成当与靶核酸分子杂交时防止所述引物序列延伸。在一些实施方案中,所述条形码序列在所述至少一个核糖核苷酸和所述3’阻断基的5’。
32.在一些实施方案中,所述3’阻断基在所述多个核酸条形码分子的3’端。在一些实施方案中,所述3’阻断基是2
’‑3’‑
二脱氧胞嘧啶(ddc)、2
’‑5’
连接的核苷、3’c3间隔子、氨基修饰的c6、反向脱氧胸苷(dt)、3’氨基修饰的核苷酸或3’磷酸基。在一些实施方案中,所述2
’‑5’
连接的核苷是3
’‑
脱氧胸苷(3
’‑
dt)、3
’‑
脱氧胞苷(3
’‑
dc)、3
’‑
脱氧腺苷(3
’‑
da)或3
’‑
脱氧鸟苷(3
’‑
dg)。
33.在一些实施方案中,用于核酸处理的方法还包括将反应混合物共同分配到分区中。在一些实施方案中,所述分区是孔。在一些实施方案中,所述分区是乳液中的水性液滴。
34.在一些实施方案中,所述多个核酸条形码分子附接至珠粒。在一些实施方案中,所述多个核酸条形码分子可释放地附接至所述珠粒。在一些实施方案中,所述珠粒是凝胶珠粒。在一些实施方案中,所述凝胶珠粒是可降解凝胶珠粒。在一些实施方案中,所述可降解凝胶珠粒可通过化学刺激来降解。在一些实施方案中,所述化学刺激是还原剂。在一些实施方案中,所述反应混合物包含还原剂。
35.在一些实施方案中,所述rnase酶是rnase h2酶。在一些实施方案中,通过引物延伸生成所述条形码化模板核酸分子。在一些实施方案中,通过核酸扩增、延伸或合成生成所述条形码化模板核酸。在一些实施方案中,通过连接生成所述条形码化模板核酸分子。
36.在一些实施方案中,用于核酸处理的方法还包括在(b)之前将衔接子序列添加至所述模板核酸分子,其中所述衔接子序列能够与所述靶核酸杂交,与所述衔接子序列的至
少一部分互补。在一些实施方案中,通过转座酶将所述衔接子序列添加至所述模板核酸分子。在一些实施方案中,所述衔接子序列包含测序引物序列,其中能够与所述靶核酸杂交的所述序列与所述测序引物序列互补。
37.本领域的技术人员从以下详细描述将显而易见本公开的额外方面和优点,其中仅仅展示和描述本公开的例示性实施方案。正如将认识到的那样,本公开能够具有其他不同的实施方案,并且其若干细节能够在各种明显的方面进行修改,都不脱离本公开。因此,图式和描述本质上应视为说明性而非限制性的。
38.以引用的方式并入
39.本说明书中所提及的所有公布、专利和专利申请都以引用的方式并入本文中,其引用程度如同特别且个别地指示每篇个别公布、专利或专利申请以引用的方式并入一般。在以引用的方式并入的公布和专利或专利申请与本说明书中所含的公开内容矛盾的程度上,本说明书意图取代和/或优先于任何这类矛盾材料。
附图说明
40.本发明的新颖特征在随附申请专利范围中详细地阐述。通过参考阐述其中利用本发明的原理的例示性实施方案的以下详细描述和如下附图(本文中又称为“图”),将更好地了解本发明的特征和优点,在附图中:
41.图1示出了用于分配单独的生物颗粒的微流体通道结构的一个实例。
42.图2示出了用于将携带条形码的珠粒递送至液滴的微流体通道结构的一个实例。
43.图3示出了用于将生物颗粒和试剂共同分配的微流体通道结构的一个实例。
44.图4示出了用于将珠粒受控分配到离散液滴中的微流体通道结构的一个实例。
45.图5示出了用于增加液滴生成通过量的微流体通道结构的一个实例。
46.图6示出了用于增加液滴生成通过量的微流体通道结构的另一实例。
47.图7a示出了具有用于进行受控分配的几何特征的微流体通道结构的另一实例的横截面视图。图7b示出了图7a的通道结构的透视图。
48.图8说明了携带条形码的珠粒的一个实例。
49.图9示出了一种计算机系统,其被编程或以其他方式配置成实施本文提供的方法。
50.图10a示出了用于tn5介导的染色质标记片段化反应的示例性二衔接子转座酶
‑
核酸复合物。图10b示出了使用基于连接或基于线性扩增的条形码缀合方法进行的对标记片段化的核dna的基于分区的条形码化。
51.图11示出了示例性的基于线性扩增的条形码化方案,其示出了分区内的条形码和衔接子序列附接,以及在本体中进行的其他处理步骤。
52.图12a示出了代表性条形码交换反应的示意图。图12b示出了在基于连接的条形码缀合之后用于条形码交换的机制的示意图。
53.图13a至图13c说明了防止条形码交换的代表性发夹帽的设计。
54.图14a至图14c说明了示例性的含有3’阻断基的含核糖核苷酸的条形码分子。图14a示出了含核糖核苷酸的条形码分子的示例性序列。图14b说明了与附接至固体支持物的含核糖核苷酸的条形码分子结合的衔接子侧接模板核酸。图14c说明了核糖核苷酸和3’阻断基的rnase h2依赖性裂解,从而促进了衔接子侧接的模板核酸分子的条形码化。
55.图15a和图15b示出了使用阻断寡核苷酸的扩增反应的代表性结果。
56.图16示出了显示使用阻断寡核苷酸的条形码交换百分比的代表性数据。
57.图17示出了处理分区中的核酸分子的方法的示意图。
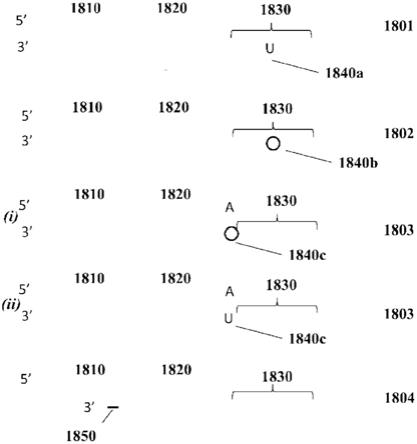
58.图18a至图18d示出了可防止条形码延伸的核酸条形码分子的示例性设计的示意图。
59.图19示出了显示使用包含非经典碱基例如尿嘧啶的核酸分子的条形码匹配百分比的代表性数据。
60.图20示出了显示使用包含非经典碱基例如尿嘧啶或无碱基位点的核酸分子防止延伸的代表性数据。
具体实施方式
61.虽然本文已经展示和描述了本发明的多种实施方案,但是本领域的技术人员显而易见这类实施方案仅仅是为了举例而提供。在不偏离本发明的情况下本领域技术人员现将进行各种改变、变化和取代。应了解,可以采用本文所述的本发明的实施方案的多个替换方案。
62.在值被称作范围的情况下,应了解,这类公开内容包括这类范围内的所有可能的子范围的公开,以及在这类范围内的具体数值,不管是否明确说明具体数值或具体子范围。
63.如本文所用,术语“条形码”通常是指传达或能够传达关于分析物的信息的标记或标识符。条形码可以是分析物的一部分。条形码可以与分析物无关。条形码可以是除分析物的内源特征(例如分析物的尺寸或末端序列)外附连至分析物(例如核酸分子)的标签或标签的组合。条形码可以是唯一的。条形码可以具有多种不同的格式。例如,条形码可以包括:多核苷酸条形码;随机的核酸和/或氨基酸序列;和合成的核酸和/或氨基酸序列。条形码可以用可逆的或不可逆的方式附连至分析物。条形码可以例如在样品测序之前、期间和/或之后加入至脱氧核糖核酸(dna)或核糖核酸(rna)样品的片段。条形码可允许鉴定和/或量化单独测序读段。
64.如本文所用,术语“实时”可以指少于约1秒,十分之一秒、百分之一秒、毫秒或更少的响应时间。响应时间可以大于1秒。在一些情况下,实时可指同时或基本上同时处理、检测或鉴定。
65.如本文所用,术语“受试者”通常是指动物,例如哺乳动物(例如人)或鸟禽(例如鸟),或其他生物体,例如植物。例如,受试者可以是脊椎动物、哺乳动物、啮齿动物(例如小鼠)、灵长类动物、猿或人。动物可以包括(但不限于)农畜、运动动物和宠物。受试者可以是健康或无症状的个体、患病或怀疑患病(例如癌症)或易患病之个体、和/或需要治疗或怀疑需要治疗的个体。受试者可以是患者。受试者可以是微生物(microorganism或microbe)(例如细菌、真菌、古菌、病毒)。
66.如本文所用,术语“基因组”通常是指来自受试者的基因组信息,其可以是例如受试者遗传信息的至少一部分或全部。基因组可以呈dna或rna编码。基因组可以包含编码区(例如编码蛋白质的区域)以及非编码区。基因组可以包括生物体中在一起的所有染色体的序列。例如,人类基因组通常具有总共46条染色体。这些在一起的所有染色体的序列可以组成人类基因组。
67.术语“适配子”、“衔接子”和“标签”可以同义使用。适配子或标签可通过任何方法偶联至待“标记”的多核苷酸序列,所述方法包括连接、杂交或其他方法。
68.如本文所用,术语“测序”通常是指用于确定一个或多个多核苷酸中的核苷酸碱基序列的方法和技术。多核苷酸可以是例如核酸分子,例如脱氧核糖核酸(dna)或核糖核酸(rna),包括它们的变体或衍生物(例如单链dna)。测序可以通过现用多种系统进行,例如不限于pacific biosciencesoxford或life technologies(ion)的测序系统。可替代地或此外,可以使用核酸扩增、聚合酶链式反应(pcr)(例如数字pcr、定量pcr或实时pcr)或等温扩增。此类系统可以提供与受试者(例如人类)的遗传信息相对应的多个原始遗传数据,如通过系统从受试者提供的样品产生。在一些实例中,此类系统提供测序读段(本文中也称为“读段”)。读段可以包括与已经进行测序的核酸分子序列相对应的一串核酸碱基。在一些情形下,本文提供的系统和方法可以与蛋白质组学信息一起使用。
69.如本文所用,术语“珠粒”通常是指颗粒。珠粒可以是固体或半固体颗粒。珠粒可以是凝胶珠粒。凝胶珠粒可以包括聚合物基质(例如由聚合或交联形成的基质)。聚合物基质可以包括一种或多种聚合物(例如具有不同官能团或重复单元的聚合物)。聚合物基质中的聚合物可以随机排列,例如在无规共聚物中,和/或具有有序结构,例如在嵌段共聚物中。交联可以经由共价、离子或感应相互作用或物理缠结。珠粒可以是大分子。珠粒可以由结合在一起的核酸分子形成。该珠粒可以通过分子(例如,大分子)例如单体或聚合物的共价或非共价组装形成。此类聚合物或单体可以是天然的或合成的。此类聚合物或单体可以是或包括例如核酸分子(例如dna或rna)。珠粒可以由聚合材料形成。珠粒可以是磁性或无磁性的。珠粒可以是刚性的。珠粒可以是柔性和/或可压缩的。珠粒可以是可破裂或可溶解的。珠粒可以是用包含一种或多种聚合物的涂层覆盖的固体颗粒(例如基于金属的颗粒,包括但不限于氧化铁、金或银)。此类涂层可以是可破裂或可溶解的。
70.如本文所用,术语“样品”通常是指受试者的生物样品。生物样品可以包含许多大分子,例如细胞大分子。样品可以是细胞样品。样品可以是细胞系或细胞培养物样品。样品可以包括一种或多种细胞。样品可以包括一种或多种微生物。生物样品可以是核酸样品或蛋白质样品。生物样品也可以是碳水化合物样品或脂质样品。生物样品可以源自另一样品。样品可以是组织样品,例如活检物、芯活检物、针吸出物或细针吸出物。样品可以是流体样品,例如血液样品、尿液样品或唾液样品。样品可以是皮肤样品。样品可以是颊拭子。样品可以是血浆或血清样品。样品可以是无细胞的或无细胞样品。无细胞的样品可以包括胞外多核苷酸。胞外多核苷酸可以从可以选自由以下组成的组的身体样品分离:血液、血浆、血清、尿液、唾液、黏膜排泄物、痰液、粪便和眼泪。
71.如本文所用,术语“生物颗粒”通常是指源自生物样品的离散的生物系统。生物颗粒可以是大分子。生物颗粒可以是小分子。生物颗粒可以是病毒。生物颗粒可以是细胞或细胞的衍生物。生物颗粒可以是细胞器。生物颗粒可以是来自细胞群体的稀少细胞。生物颗粒可以是任何类型的细胞,包括不限于原核细胞、真核细胞、细菌、真菌、植物、哺乳动物或其他动物细胞类型、支原体、正常组织细胞、肿瘤细胞或任何其他细胞类型,无论源自单细胞还是多细胞生物体。生物颗粒可以是细胞的成分。生物颗粒可以是或可以包括dna、rna、细胞器、蛋白质或它们的任何组合。生物颗粒可以是或可包括染色体或基因组的其他部分。生
物颗粒可以是或可以包括包含细胞或来自细胞(例如细胞珠粒)的一种或多种成分,例如来自细胞的dna、rna、细胞器、蛋白质或它们的任何组合的基质(例如凝胶或聚合物基质)。生物颗粒可以从受试者的组织获得。生物颗粒可以是硬化细胞。这种硬化细胞可以包括或可以不包括细胞壁或细胞膜。生物颗粒可以包括细胞的一种或多种成分,但可以不包括细胞的其他成分。此类成分的一个实例是细胞核或细胞器。细胞可以是活细胞。活细胞能够被培养,例如当装入凝胶或聚合物基质中时培养,或当包含凝胶或聚合物基质时培养。
72.如本文所用,术语“大分子成分”通常是指生物颗粒内所含或来自生物颗粒的大分子。大分子成分可以包含核酸。在一些情况下,生物颗粒可以是大分子。大分子成分可以包含dna。大分子成分可以包含rna。rna可以是编码或非编码的。rna可以是例如信使rna(mrna)、核糖体rna(rrna)或转运rna(trna)。rna可以是转录物。rna可以是长度小于200个核酸碱基的小rna,或长度大于200个核酸碱基的大rna。小rna可以包括5.8s核糖体rna(rrna)、5s rrna、转运rna(trna)、微型rna(mirna)、小干扰rna(sirna)、小核仁rna (snorna)、piwi相互作用rna(pirna)、源自trna的小rna(tsrna)和源自小rdna的rna(srrna)。rna可以是双链rna或单链rna。rna可以是环形rna。大分子成分可以包含蛋白质。大分子成分可以包含肽。大分子成分可以包含多肽。
73.如本文所用,术语“分子标签”通常是指能够结合于大分子成分的分子。分子标签可以在高亲和力下结合于大分子成分。分子标签可以在高特异性下结合于大分子成分。分子标签可以包含核苷酸序列。分子标签可以包含核酸序列。核酸序列可以是分子标签的至少一部分或全部。分子标签可以是核酸分子或可以是核酸分子的一部分。分子标签可以是寡核苷酸或多肽。分子标签可以包含dna适体。分子标签可以是或包含引物。分子标签可以是或包含蛋白质。分子标签可以包含多肽。分子标签可以是条形码。
74.如本文所用,术语“分区”通常是指可适于容纳一种或多种物质或进行一种或多种反应的空间或体积。分区可以是物理隔室,例如液滴或孔。分区可以将空间或体积与另一个空间或体积分隔开。液滴可以是在与第一相不可混溶的第二相(例如油)中的第一相(例如水相)。液滴可以是在不与第一相相分开的第二相中的第一相,例如在水相中的胶囊或脂质体。分区可以包含一个或多个其他(内部)分区。在一些情况下,分区可以是虚拟隔室,它可以通过标志(例如标志文库)跨越多个和/或偏远的物理隔室界定和鉴定。例如,物理隔室可以包含多个虚拟隔室。
75.用于样品划分的系统和方法
76.在一方面,本文所述的系统和方法提供一个或多个颗粒(例如生物颗粒、生物颗粒的大分子成分、珠粒、试剂等)划分、沉积或分配至离散的隔室或分区(本文中可交换地称为分区),其中每个分区维持其自身的内容物与其他分区的内容物分开。分区可以是乳液中的液滴。分区可以包括一个或多个其他分区。
77.分区可以包括一个或多个颗粒。分区可以包括一种或多种类型的颗粒。例如,本公开的分区可以包含一个或多个生物颗粒和/或其大分子成分。分区可以包含一个或多个凝胶珠粒。分区可以包含一个或多个细胞珠粒。分区可以包括单个凝胶珠粒、单个细胞珠粒,或单个细胞珠粒和单个凝胶珠粒两者。分区可以包括一种或多种试剂。可替代地,分区可以是未被占用的。例如,分区可以不包含珠粒。细胞珠粒可以是例如经由含有生物颗粒的液滴与能够聚合或胶凝的前体的聚合而包裹在凝胶或聚合物基体内的生物颗粒和/或其大分子
成分中的一种或多种。可以在液滴产生之前、之后或同时例如经由微囊(例如珠粒)将唯一标识符(例如条形码)注射到液滴中,如本文其他地方所描述。微流体通道网络(例如,在芯片上)可用于产生如本文所述的分区。在单独的生物颗粒的分配中还可以采用替代机制,包括多孔膜,细胞的水性混合物通过多孔膜挤出成非水性流体。
78.分区可以在流体流中流动。分区可以包含例如微泡,所述微泡具有环绕内部流体中心或核心的外部屏障。在一些情况下,分区可以包括能够将材料夹带和/或保留在其基质内的多孔基质。分区可以是第一相在第二相内的液滴,其中第一相和第二相不可混溶。例如,分区可以是水性流体在非水性连续相(例如油相)内的液滴。在另一实例中,分区可以是非水性流体在水相内的液滴。在一些实例中,分区可以以油包水乳液或水包油乳液的形式提供。多种不同的容器例如描述于美国专利申请公布第2014/0155295号中,所述申请出于所有目的以引用方式整体并入本文。用于在非水性或油状连续相中产生稳定液滴的乳液体系描述于例如美国专利申请公布第2010/0105112号中,所述申请出于所有目的以引用方式整体并入本文。
79.在乳液中的液滴的情况下,在一个非限制性实例中,将单独的颗粒分配到离散分区可以通过将水性流体中流动的颗粒流引入到流动的非水性流体流中,使得在两股流的接点处产生液滴来实现。可以调节流体特性(例如流体流速、流体粘度等)、颗粒特性(例如体积分数、粒度、颗粒浓度等)、微流体架构(例如通道几何形状等)以及其他参数以控制所得分区的占用率(例如,每个分区的生物颗粒数量、每个分区的珠粒数量等)。例如,可以通过提供一定颗粒浓度和/或流速的水流来控制分区占用率。为了产生单个生物颗粒分区,可以选择不混溶流体的相对流速,使得所述分区可以每个分区含少于一个生物颗粒,以便确保被占用的那些分区主要被单个地占用。在一些情况下,多个分区中的分区至多可以含有一个生物颗粒(例如,珠粒、dna、细胞或细胞物质)。在一些实施方案中,可以选择或调节各种参数(例如流体特性、颗粒特性、微流体结构等),使得大部分分区被占用,例如,仅允许一小部分分区未被占用。可以控制流量和通道架构以确保给定量的单个已占用分区,低于某一水平的未已占用分区和/或低于某一水平被多个占用的分区。
80.图1示出了用于分配单独的生物颗粒的微流体通道结构100的一个实例。通道结构100可以包括在通道接点110处连通的通道区段102、104、106和108。在操作中,包括悬浮生物颗粒(或细胞)114的第一水性流体112可以沿通道区段102转运到接点110处,而与水性流体112不可混溶的第二流体116从通道区段104和106中的每一个递送至接点110处以产生第一水性流体112的离散液滴118、120,第一水性流体流入通道区段108中,并且从接点110处流走。通道区段108可以与出口储槽流体联接,可以将离散液滴储存和/或收获在出口储槽中。生成的离散液滴可以包括单独的生物颗粒114(例如液滴118)。生成的离散液滴可以包括多于一个的单独生物颗粒114(在图1中未示出)。离散液滴可以不含生物颗粒114(例如液滴120)。每个离散分区可以保持其自身内容物(例如,单独的生物颗粒114)与其他分区的内容物分离。
81.第二流体116可以包含油,例如含氟油,所述油包括用于稳定所得液滴,例如抑制所得液滴118、120的后续聚结的含氟表面活化剂。特别有用的分配流体和含氟表面活性剂的实例描述于例如美国专利申请公布第2010/0105112号中,所述申请出于所有目的以引用方式整体并入本文。
82.正如将认识到的,本文所述的通道区段可以联接至各种不同的流体源或接收部件中的任何一个,包括储槽、管道、歧管或其他系统的流体部件。正如将认识到的,微流体通道结构100可以具有其他几何结构。例如,微流体通道结构可以具有多于一个通道接点。例如,微流体通道结构可以具有2、3、4或5个通道区段,每个通道区段都携带有颗粒(例如,生物颗粒、细胞珠粒和/或凝胶珠粒),这些通道区段在通道接点处会合。可以引导流体经由一个或多个流体流动单元沿一个或多个通道或储槽流动。流体流动单元可以包括压缩机(例如,提供正压)、泵(例如,提供负压)、致动器等,以控制流体的流量。流体还可以或以其他方式通过施加的压力差、离心力、电动泵送、真空、毛细管流或重力流等来控制。
83.生成的液滴可以包括两个子集的液滴:(1)已占用液滴118,其含有一个或多个生物颗粒114,以及(2)未占用液滴120,其不含任何生物颗粒114。已占用液滴118可以包括单个地占用的液滴(具有一个生物颗粒)和多个地占用的液滴(具有多于一个生物颗粒)。如本文其他地方所述,在一些情况下,大多数已占用分区中每个已占用分区可以包括不超过一个生物颗粒,并且生成的一些分区可未被占用(未被任何生物颗粒占用)。然而,在一些情况下,一些已占用分区可以包括多于一个生物颗粒。在一些情况下,可以控制分配过程,使得少于约25%的已占用分区含有多于一个生物颗粒,并且在许多情况下,少于约20%的已占用分区具有多于一个生物颗粒,而在一些情况下,少于约10%或甚至少于约5%的已占用分区的每个分区包括多于一个生物颗粒。
84.在一些情况下,可能希望最小化过度数量空分区的产生,例如以降低成本和/或提高效率。虽然这种最小化可以通过在分配接点110处提供足够数量的生物颗粒(例如,生物颗粒114)来实现,以便确保至少一个生物颗粒包封在分区中,但是泊松分布(poissonian distribution)可以预期地增加包括多个生物颗粒的分区的数量。因此,在要获得单个地占用的分区的情况下,所生成的分区中至多约95%、90%、85%、80%、75%、70%、65%、60%、55%、50%、45%、40%、35%、30%、25%、20%、15%、10%、5%或更少可未被占用。
85.在一些情况下,可以控制生物颗粒(例如,在通道区段102中)或引导到分配接点中(例如,在通道区段104、106中)的其他流体中的一种或多种的流量,使得在许多情况下,所生成的分区中不超过约50%、所生成的分区中不超过约25%或所生成的分区中不超过约10%未被占用。可以控制这些流量,以呈现单个占用分区的非泊松分布,同时提供较低水平的未占用分区。可以实现上述未占用分区的范围,同时仍提供上述任何单个占用率。例如,在许多情况下,本文所述的系统和方法的使用可以产生所得分区,所得分区具有小于约25%、小于约20%、小于约15%、小于约10%的多个占用率,并且在许多情况下,小于约5%,而未占用分区小于约50%、小于约40%、小于约30%、小于约20%、小于约10%、小于约5%或更少。
86.正如将认识到的,上述占用率也适用于包括生物颗粒和额外试剂两者的分区,包括但不限于携带有条形码化核酸分子(例如,寡核苷酸)的微囊或珠粒(例如,凝胶珠粒)(相对于图2描述)。已占用分区(例如,至少约10%、20%、30%、40%、50%、60%、70%、80%、90%、95%或99%的已占用分区)可以包括包含条形码化核酸分子的微囊(例如,珠粒)和生物颗粒两者。
87.在另一方面,除了或替代基于液滴的分配,生物颗粒可以包封在微囊内,该微囊包括外壳、层或多孔基质,其中夹带了一个或多个单独的生物颗粒或小群生物颗粒。微囊可以
包括其他试剂。生物颗粒的包封可以通过多种方法进行。此类方法可以将含有生物颗粒的水性流体与聚合物前体材料组合,在向聚合物前体施加特定的刺激时该聚合物前体材料能够形成凝胶或其他固体或半固体基质。此类刺激可以包括例如热刺激(例如,加热或冷却)、光刺激(例如,通过光固化)、化学刺激(例如,通过交联、前体的聚合引发(例如,通过添加的引发剂))、机械刺激或它们的组合。
88.包含生物颗粒的微囊的包封可以通过多种方法进行。例如,可以使用气刀液滴或气溶胶发生器将前体流体的液滴分配到胶凝溶液中,以便形成包括单独的生物颗粒或小群生物颗粒的微囊。同样,可以使用基于膜的包封系统来生成包含如本文所述的包封生物颗粒的微囊。如本文所述,本公开的微流体系统,例如图1中所示的微流体系统,可以容易地用于包封细胞。具体来说,并且参考图1,包含(i)生物颗粒114和(ii)聚合物前体材料(未示出)的水性流体112流入通道接点110中,在那里水性流体通过非水流体流116而分配成液滴118、120。在包封方法的情况下,非水性流体116还可以包括引发剂(未示出)以引起聚合物前体的聚合和/或交联以形成包括所夹带的生物颗粒的微囊。聚合物前体/引发剂对的实例包括美国专利申请公布第2014/0378345号中描述的那些,所述申请出于所有目的以引用方式整体并入本文。
89.例如,在聚合物前体材料包括线性聚合物材料(例如线性聚丙烯酰胺、peg或其他线性聚合物材料)的情况下,活化剂可以包括交联剂或活化所形成的液滴内的交联剂的化学物质。同样,对于包含可聚合单体的聚合物前体,活化剂可以包含聚合引发剂。例如,在某些情况下,在聚合物前体包含丙烯酰胺单体与n,n
’‑
双
‑
(丙烯酰基)胱胺(bac)共聚单体的混合物的情况下,可以在通道区段104和106中的第二流体流116内提供例如四乙基亚甲基二胺(temed)之类的试剂,该试剂可以引发丙烯酰胺和bac共聚成交联的聚合物网络或水凝胶。
90.在第二流体流116与第一流体流112在接点110处接触后,在液滴形成期间,temed可以从第二流体116扩散到包含线性聚丙烯酰胺的水性流体112中,这样将活化液滴118、120内的聚丙烯酰胺的交联,从而导致形成凝胶(例如,水凝胶)微囊,作为夹带有细胞114的固体或半固体珠粒或颗粒。尽管在聚丙烯酰胺包封方面进行了描述,但是在本文所述的方法和组合物的背景下也可以采用其他"可活化"包封组合物。例如,藻酸盐液滴的形成,随后暴露于二价金属离子(例如,ca
2+
离子),可用作使用所述方法的包封方法。同样,琼脂糖液滴也可以通过基于温度的胶凝作用(例如,在冷却时,等等)转化成胶囊。
91.在一些情况下,包封的生物颗粒可以选择性地从微囊中释放出来,例如随着时间的推移或在施加特定刺激时,充分降解微囊,以允许生物颗粒(例如,细胞)或它的其他内容物降从微囊中释放出来,例如释放到分区(例如,液滴)中。例如,在上述聚丙烯酰胺聚合物的情况下,微囊的降解可通过引入适当的还原剂例如dtt等来裂解使聚合物基质交联的二硫键而实现。参见,例如,美国专利申请公布第2014/0378345号,所述申请出于所有目的以引用方式整体并入本文。
92.可以使生物颗粒经受足以使前体聚合或胶凝的其他条件。足以使前体聚合或胶凝的条件可以包括暴露于加热、冷却、电磁辐射和/或光。足以使前体聚合或胶凝的条件可以包括足以使前体聚合或胶凝的任何条件。聚合或胶凝之后,可在生物颗粒周围形成聚合物或凝胶。聚合物或凝胶可以是化学或生化试剂可扩散性渗透的。聚合物或凝胶可以是生物
颗粒的大分子成分不可扩散性渗透的。以这种方式,聚合物或凝胶可以起到允许生物颗粒经受化学或生化操作的作用,同时将大分子成分在空间上限制到由聚合物或凝胶限定的液滴区域中。聚合物或凝胶可以包括以下的一种或多种:二硫化物交联的聚丙烯酰胺、琼脂糖、藻酸盐、聚乙烯醇、聚乙二醇(peg)
‑
二丙烯酸酯、peg
‑
丙烯酸酯、peg
‑
硫醇、peg
‑
叠氮化物、peg
‑
炔、其他丙烯酸酯、壳聚糖、透明质酸、胶原、纤维蛋白、明胶或弹性蛋白。聚合物或凝胶可以包含任何其他聚合物或凝胶。
93.可以将聚合物或凝胶官能化为与目标分析物,例如核酸、蛋白质、碳水化合物、脂质或其他分析物结合。聚合物或凝胶可以通过被动机制聚合或胶凝。聚合物或凝胶在碱性条件或高温下可以稳定。聚合物或凝胶可具有与珠粒的机械特性相似的机械特性。例如,聚合物或凝胶可以具有与珠粒相似的大小。聚合物或凝胶可具有与珠粒相似的机械强度(例如,拉伸强度)。聚合物或凝胶的密度可低于油。聚合物或凝胶的密度可以大致类似于缓冲剂的密度。聚合物或凝胶可具有可调的孔径。可以选择孔径以例如保留变性的核酸。可以选择孔径以保持对外源化学物质(例如氢氧化钠(naoh))和/或内源化学物质(例如抑制剂)的扩散渗透性。聚合物或凝胶可以是生物相容的。聚合物或凝胶可以维持或增强细胞活力。聚合物或凝胶可以是生物化学相容的。聚合物或凝胶可以通过热、化学、酶和/或光学方式聚合和/或解聚。
94.聚合物可以包含经二硫连键交联的聚(丙烯酰胺
‑
共
‑
丙烯酸)。聚合物的制备可以包括两步反应。在第一活化步骤中,可将聚(丙烯酰胺
‑
共
‑
丙烯酸)暴露于酰化剂,以将羧酸转化为酯。例如,可将聚(丙烯酰胺
‑
共
‑
丙烯酸)暴露于4
‑
(4,6
‑
二甲氧基
‑
1,3,5
‑
三嗪
‑2‑
基)
‑4‑
甲基吗啉盐酸盐(dmtmm)。可将聚丙烯酰胺
‑
共
‑
丙烯酸暴露于4
‑
(4,6
‑
二甲氧基
‑
1,3,5
‑
三嗪
‑2‑
基)
‑4‑
甲基吗啉的其他盐。在第二交联步骤中,可将第一步中形成的酯暴露于二硫化物交联剂。例如,可以将酯暴露于胱胺(2,2'
‑
二硫代双(乙胺))。在这两个步骤之后,生物颗粒可被通过二硫桥连接在一起的聚丙烯酰胺链包围。以这种方式,可以将生物颗粒封闭在凝胶或基质(例如,聚合物基质)内部或包含该凝胶或基质,以形成“细胞珠粒”。细胞珠粒可以含有生物颗粒(例如,细胞)或生物颗粒的大分子成分(例如,rna、dna、蛋白质等)。细胞珠可包括单个细胞或多个细胞,或单个细胞或多个细胞的衍生物。例如在裂解和洗涤细胞后,可以将来自细胞裂解物的抑制组分洗掉,并且大分子成分可以结合为细胞珠粒。本文公开的系统和方法可适用于含有生物颗粒的细胞珠粒(和/或液滴和其他分区)和含有生物颗粒的大分子成分的细胞珠粒(和/或液滴或其他分区)两者。
95.与基于液滴分配的生物颗粒相比,包封的生物颗粒可以提供更易储存和更便携的某些潜在优点。此外,在一些情况下,可能希望在分析之前允许生物颗粒孵育一段选定的时间,例如,以便表征在存在或不存在不同刺激的情况下此类生物颗粒随时间的变化。在此类情况下,包封可允许比在乳液液滴中分配更长的孵育,但是在一些情况下,液滴分区的生物颗粒也可以孵育不同的时间段,例如至少10秒、至少30秒、至少1分钟、至少5分钟、至少10分钟、至少30分钟、至少1小时、至少2小时、至少5小时或至少10小时或更多时间。生物颗粒的包封可以构成生物颗粒的分区,其他试剂被共同分配到生物颗粒中。可替代地或另外,包封的生物颗粒可以容易地沉积到如上所述的其他分区(例如,液滴)中。
96.珠粒
97.分区可以包含一个或多个唯一标识符,例如条形码。条形码可以预先、随后或同时
递送到容纳划分或分配的生物颗粒的分区中。例如,条形码可以在液滴生成之前、之后或与之同时注入到液滴中。将条形码递送至特定分区允许随后将单独生物颗粒的特征归属于特定分区。条形码可以例如在核酸分子(例如,寡核苷酸)上,通过任何适合机制递送至分区。条形码化核酸分子可通过微囊递送至分区。在一些情况下,微囊可以包含珠粒。下面更详细地描述珠粒。
98.在一些情况下,条形码化核酸分子可以最初与微囊缔合,然后从微囊中释放出来。条形码化核酸分子的释放可以是被动的(例如,通过扩散出微囊)。另外地或可替代地,从微囊中释放可以在施加允许条形码化核酸分子从微胶囊中解离或释放的刺激时。此类刺激可以破坏微囊,这是一种使条形码化核酸分子偶联至微囊或处于微囊内或两者的相互作用。此类刺激可以包括,例如热刺激、光刺激、化学刺激(例如,ph的变化或还原剂的使用)、机械刺激、辐射刺激、生物刺激(例如酶)或它们的任何组合。
99.图2示出了用于将携带条形码的珠粒递送至液滴的微流体通道结构200的一个实例。通道结构200可以包括在通道接点210处连通的通道区段201、202、204、206和208。在操作中,通道区段201可以将包括多个珠粒214(例如,含核酸分子、寡核苷酸、分子标签)的水性流体212沿通道区段201转运至接点210处。所述多个珠粒214可以来源于珠粒悬浮液。例如,通道区段201可以连接至包含珠粒214的水性悬浮液的储槽。通道区段202可以将包括多个生物颗粒216的水性流体212沿通道区段202转运至接点210处。所述多个生物颗粒216可以来源于生物颗粒的悬浮液。例如,通道区段202可以连接至包含生物颗粒216的水性悬浮液的储槽。在一些情况下,第一通道区段201或第二通道区段202或两个区段中的水性流体212可以包括一种或多种试剂,如下面进一步详述的。可以将与水性流体212不可混溶的第二流体218(例如,油)从通道区段204和206中的每一个递送至接点210处。在来自通道区段201和202中的每一个的水性流体212与来自通道区段204和206中的每一个的第二流体218在通道接点210处会合时,水性流体212可以在第二流体218中分配为离散液滴220并且沿通道区段208从接点210处流走。通道区段208可以将离散液滴递送到与通道区段208流体联接的出口储槽,可以将离散液滴收获在出口储槽中。
100.作为替代,通道区段201和202可以在接点210上游的另一接点处会合。在此接点处,珠粒和生物颗粒可以形成混合物,沿另一通道将混合物引导至接点210处,以得到液滴220。所述混合物可以以交替的方式提供珠粒和生物颗粒,使得例如液滴包含单个珠粒和单个生物颗粒。
101.珠粒、生物颗粒和液滴可以以基本上规则的流动曲线(例如,以规则的流速)沿通道流动。此类规则的流动曲线可以容许液滴包括单个珠粒和单个生物颗粒。此类规则的流动曲线可以容许液滴具有大于5%、10%、20%、30%、40%、50%、60%、70%、80%、90%或95%的占用率(例如,具有珠粒和生物颗粒的液滴)。在例如美国专利公布第2015/0292988号中提供了此类常规流动模式和可用于提供此类常规流动模式的装置,所述专利以引用方式整体并入本文。
102.第二流体218可以包含油,例如含氟油,所述油包括用于稳定所得液滴,例如抑制所得液滴220的后续聚结的含氟表面活化剂。
103.生成的离散液滴可以包括单独的生物颗粒216。生成的离散液滴可以包括携带条形码或其他试剂的珠粒214。生成的离散液滴可以包括单独的生物颗粒和携带条形码的珠
粒(例如液滴220)两者。在一些情况下,离散液滴可以包括多于一个单独的生物颗粒或不包括生物颗粒。在一些情况下,离散液滴可以包括多于一个珠粒或不包括珠粒。离散液滴可以未被占用(例如,无珠粒、无生物颗粒)。
104.有利地,将生物颗粒和携带条形码的珠粒分配的离散液滴可以有效地允许将条形码归属于分区内生物颗粒的大分子成分。分区的内容物可保持与其他分区的内容物离散。
105.正如将认识到的,本文所述的通道区段可以联接至各种不同的流体源或接收部件中的任何一个,包括储槽、管道、歧管或其他系统的流体部件。正如将认识到的,微流体通道结构200可以具有其他几何结构。例如,微流体通道结构可以具有多于一个的通道接点。例如,微流体通道结构可以具有2、3、4或5个通道区段,每个通道区段都携带有珠粒,这些通道区段在通道接点处会合。可以引导流体经由一个或多个流体流动单元沿一个或多个通道或储槽流动。流体流动单元可以包括压缩机(例如,提供正压)、泵(例如,提供负压)、致动器等,以控制流体的流量。流体还可以或以其他方式通过施加的压力差、离心力、电动泵送、真空、毛细管流或重力流等来控制。
106.珠粒可以是多孔的、无孔的、固体、半固体、半流体、流体和/或它们的组合。在一些情况下,珠粒可以是可溶解的、可破裂的和/或可降解的。在一些情况下,珠粒可以不是可降解的。在一些情况下,珠粒可以是凝胶珠粒。凝胶珠粒可以是水凝胶珠粒。凝胶珠粒可由分子前体例如聚合物或单体物质形成。半固体珠粒可以是脂质体珠粒。固体珠粒可以包含金属,包括氧化铁、金和银。在一些情况下,珠粒可以是二氧化硅珠粒。在一些情况下,珠粒可以是刚性的。在其他情况下,珠粒可以是柔性的和/或可压缩性的。
107.珠粒可以具有任何适合形状。珠粒形状的实例包括但不限于球形、非球形、椭圆形、长方形、无定形、圆形、圆柱形及其变型。
108.珠粒可以具有均一的大小或非均一的大小。在一些情况下,珠粒的直径可以为至少约10纳米(nm)、100nm、500nm、1微米(μm)、5μm、10μm、20μm、30μm、40μm、50μm、60μm、70μm、80μm、90μm、100μm、250μm、500μm、1mm或更大。在一些情况下,珠粒的直径可以小于约10nm、100nm、500nm、1μm、5μm、10μm、20μm、30μm、40μm、50μm、60μm、70μm、80μm、90μm、100μm、250μm、500μm、1mm或更小。在一些情况下,珠粒的直径可以在约40
‑
75μm、30
‑
75μm、20
‑
75μm、40
‑
85μm、40
‑
95μm、20
‑
100μm、10
‑
100μm、1
‑
100μm、20
‑
250μm或20
‑
500μm的范围内。
109.在某些方面,珠粒可以作为具有相对单分散的粒度分布的珠粒群体或多个珠粒提供。在可能希望在分区内提供相对一致量的试剂的情况下,保持相对一致的珠粒特征(例如大小)可以有助于总体一致性。具体来说,本文所述的珠粒可具有这样的粒度分布,所述粒度分布在其横截面尺寸上的变异系数小于50%、小于40%、小于30%、小于20%,并且在一些情况下小于15%、小于10%、小于5%或更小。
110.珠粒可以包含天然材料和/或合成材料。例如,珠粒可以包含天然聚合物、合成聚合物或天然聚合物和合成聚合物两者。天然聚合物的实例包括蛋白质和糖,例如脱氧核糖核酸、橡胶、纤维素、淀粉(例如直链淀粉、支链淀粉)、蛋白质、酶、多糖、丝、聚羟基烷基酸酯、壳聚糖、葡聚糖、胶原蛋白、卡拉胶、卵叶车前子、阿拉伯胶、琼脂、明胶、虫胶、梧桐胶、黄原胶、玉米糖胶、瓜尔胶、刺梧桐胶、琼脂糖、海藻酸、海藻酸盐或它们的天然聚合物。合成聚合物的实例包括丙烯酸类、尼龙、硅酮、氨纶、粘胶人造丝、聚羧酸、聚乙酸乙烯酯、聚丙烯酰胺、聚丙烯酸酯、聚乙二醇、聚氨酯、聚乳酸、二氧化硅、聚苯乙烯、聚丙烯腈、聚丁二烯、聚碳
酸酯、聚乙烯、聚对苯二甲酸乙二醇酯、聚(氯三氟乙烯)、聚(环氧乙烷)、聚(对苯二甲酸乙二醇酯)、聚乙烯、聚异丁烯、聚(甲基丙烯酸甲酯)、聚(氧化亚甲基)、聚甲醛、聚丙烯、聚苯乙烯、聚(四氟乙烯)、聚(乙酸乙烯酯)、聚(乙烯醇)、聚(氯乙烯)、聚(偏二氯乙烯)、聚(偏二氟乙烯)、聚(氟乙烯)和/或它们的组合(例如,共聚物)。珠粒也可由除聚合物之外的材料(包括脂质、胶束、陶瓷、玻璃
‑
陶瓷、复合材料、金属、其他无机材料等)形成。
111.在一些情况下,珠粒可以含有分子前体(例如,单体或聚合物),其可以通过分子前体的聚合而形成聚合物网络。在一些情况下,前体可以是已经聚合的物质,其能够经由例如化学交联进行进一步聚合。在一些情况下,前体可以包含丙烯酰胺或甲基丙烯酰胺单体、低聚物或聚合物中的一种或多种。在一些情况下,珠粒可以包含预聚物,其是能够进一步聚合的低聚物。例如,可以使用预聚物制备的聚氨酯珠粒。在一些情况下,珠粒可以含有可进一步聚合在一起的单独聚合物。在一些情况下,可通过不同前体的聚合而产生珠粒,使得它们包含混合的聚合物、共聚物和/或嵌段共聚物。在一些情况下,珠粒可以包含在聚合物前体(例如,单体、低聚物、线性聚合物)、核酸分子(例如,寡核苷酸)、引物和其他实体之间的共价键或离子键。在一些情况下,共价键可以是碳
‑
碳键、硫醚键或碳
‑
杂原子键。
112.交联可以是永久性的或可逆性的,这取决于所用的特定交联剂。可逆性交联可以允许聚合物在适当的条件下线性化或解离。在一些情况下,可逆性交联也可以允许与珠粒表面结合的材料的可逆性附接。在一些情况下,交联剂可以形成二硫连键。在一些情况下,形成二硫连键的化学交联剂可以是胱胺或修饰的胱胺。
113.在一些情况下,可以在分子前体单元(例如,单体、低聚物或线性聚合物)或掺入珠粒中的前体与核酸分子(例如,寡核苷酸)之间形成二硫连键。胱胺(包括修饰的胱胺)例如是一种包含二硫键的有机试剂,可以用作珠粒的单独的单体或聚合物前体之间的交联剂。聚丙烯酰胺可以在胱胺或包含胱胺的物质(例如,修饰的胱胺)的存在下聚合,以产生包含二硫连键的聚丙烯酰胺凝胶珠粒(例如,包含可化学还原的交联剂的可化学降解的珠粒)。当珠粒暴露于还原剂时,二硫连键可容许珠粒降解(或溶解)。
114.在一些情况下,壳聚糖(一种线性多糖聚合物)可通过亲水链与戊二醛交联形成珠粒。壳聚糖聚合物的交联可通过受热、压力、ph值变化和/或辐射引发的化学反应来实现。
115.在一些情况下,珠粒可以包含丙烯酰胺基(acrydite)部分,其在某些方面可用于将一个或多个核酸分子(例如,条形码序列、条形码化核酸分子、带条形码的寡核苷酸、引物或其他寡核苷酸)附接至珠粒。在一些情况下,丙烯酰胺基部分可以指由丙烯酰胺基与一种或多种物质的反应,例如聚合反应期间丙烯酰胺基与其他单体和交联剂的反应而产生的丙烯酰胺基类似物。可以对丙烯酰胺基部分进行修饰以与待附接的物质形成化学键,所述物质例如核酸分子(例如,条形码序列、条形码化核酸分子、带条形码的寡核苷酸、引物或其他寡核苷酸)。丙烯酰胺基部分可以用能够形成二硫键的硫醇基团修饰或者可以用已经包含二硫键的基团修饰。硫醇或二硫化物(通过二硫化物交换)可以用作要附接的物质的锚定点,或者可以将丙烯酰胺基部分的另一部分用于附接。在一些情况下,附接可以是可逆性的,使得当二硫键被破坏时(例如,在还原剂的存在下),所附接的物质从珠粒释放。在其他情况下,丙烯酰胺基部分可以包含可用于附接的反应性羟基。
116.用于附接核酸分子(例如,寡核苷酸)的珠粒的官能化可以通过多种不同的方法实现,所述不同的方法包括聚合物内化学基团的活化、聚合物结构中活性或可活化官能团的
掺入或在珠粒产生中在预聚物或单体阶段的附接。
117.例如,聚合形成珠粒的前体(例如,单体、交联剂)可以包含丙烯酰胺基部分,使得当珠粒生成时,该珠粒也包含丙烯酰胺基部分。可以将丙烯酰胺基部分附接至核酸分子(例如,寡核苷酸),该核酸分子可以包括引物序列(例如,用于扩增靶核酸的引物、随机引物、信使rna的引物序列)和/或一个或多个条形码序列。所述一个以上的条形码序列可以包括对于偶联至给定珠粒的所有核酸分子相同的序列和/或在偶联至给定珠粒的所有核酸分子中不同的序列。核酸分子可以掺入到珠粒中。
118.在一些情况下,核酸分子可以包含功能序列,例如,用于附接至测序流动池的功能序列,例如,用于测序的p5序列。在一些情况下,核酸分子或其衍生物(例如,由核酸分子产生的寡核苷酸或多核苷酸)可以包含另一功能序列,例如,用于附接至测序流动池以进行illumina测序的p7序列。在一些情况下,核酸分子可以包含条形码序列。在一些情况下,引物还可以包含唯一分子标识符(umi)。在一些情况下,引物可以包含用于illumina测序的r1引物序列。在一些情况下,引物可以包含用于illumina测序的r2引物序列。此类核酸分子(例如,寡核苷酸、多核苷酸等)及其用途的实例,如可与本公开的组合物、装置、方法和系统一起使用的,提供于美国专利公布第2014/0378345和2015/0376609号(其各自以引用方式整体并入本文)中。
119.图8说明了携带条形码的珠粒的一个实例。核酸分子802,例如寡核苷酸,可以通过可释放连键806例如二硫化物连接子,偶联至珠粒804。同一珠粒804可以与一个或多个其他核酸分子818、820偶联(例如,经由可释放连键)。核酸分子802可以是条形码或包含条形码。如本文其他地方所述,条形码的结构可以包含许多序列元件。核酸分子802可以包含可用于后续处理的功能序列808。例如,功能序列808可以包括以下的一种或多种:测序仪特异性的流动池附接序列(例如,用于测序系统的p5序列)测序引物序列(例如,用于测序系统的r1序列)。核酸分子802可以包含对样品(例如,dna、rna、蛋白质等)进行条形码化的条形码序列810。在一些情况下,条形码序列810可以是珠粒特异性的,使得条形码序列810为偶联至相同珠粒804的所有核酸分子(例如,包括核酸分子802)所共有。可替代地或另外,条形码序列810可以是分区特异性的,使得条形码序列810为偶联至分配到同一分区中的一个或多个珠粒的所有核酸分子所共有。核酸分子802可以包含特异性引物序列812,例如mrna特异性引物序列(例如,聚t序列)、靶向引物序列和/或随机引物序列。核酸分子802可以包含锚定序列814以确保特异性引物序列812在序列末端(例如,mrna的序列末端)杂交。例如,锚定序列814可以包括随机的短核苷酸序列,例如1
‑
聚体、2
‑
聚体、3
‑
聚体或更长的序列,其可以确保聚t区段更有可能在mrna的聚a尾的序列末端杂交。
120.核酸分子802可以包含唯一分子标识序列816(例如,唯一分子标识符(umi))。在一些情况下,唯一分子标识序列816可以包含约5至约8个核苷酸。可替代地,唯一分子标识序列816可以包含少于约5个或多于约8个核苷酸。唯一分子标识序列816可以是在偶联至单个珠粒(例如,珠粒804)的单独核酸分子(例如,802、818、820等)间不同的唯一序列。在一些情况下,唯一分子标识序列816可以是随机序列(例如,随机n
‑
聚体序列)。例如,umi可以提供被捕获的起始mrna分子的唯一标识符,以便允许定量原始表达的rna的数量。正如将认识到的,图8示出了偶联至珠粒804的表面的核酸分子802、818、820,单独的珠粒可以偶联至任意
数量的单独核酸分子,例如从一到几十到成千上万个或甚至数百万个单独核酸分子。单独核酸分子的相应条形码可以包括在偶联至同一珠粒的不同单独核酸分子之间的共有序列区段或相对共有序列区段(例如,808、810、812等)和可变或唯一序列区段(例如,816)两者。
121.在操作时,生物颗粒(例如,细胞、dna、rna等)可以连同带条形码化珠粒804一起共同分配。条形码化核酸分子802、818、820可以从分区中的珠粒804中释放。举例而言,在分析样品rna的情况下,其中一个释放的核酸分子(例如,802)的聚t区段(例如,812)可以与mrna分子的聚a尾杂交。逆转录可产生mrna的cdna转录物,但是该转录物包括核酸分子802的序列区段808、810、816中的每一个。因为核酸分子802包含锚定序列814,所以将更有可能与mrna的聚a尾的序列末端杂交并引发逆转录。在任何给定分区中,单独mrna分子的cdna转录物可以包括共有条形码序列区段810。然而,由给定分区内的不同mrna分子产生的转录物可在唯一分子标识序列812区段(例如,umi区段)处不同。有利地,甚至在给定分区的内容物的任何后续扩增之后,不同umi的数量可以指示来源于给定分区并因此来源于生物颗粒(例如,细胞)的mrna的量。如上所述,可以对转录物进行扩增、纯化和测序以鉴定mrna的cdna转录物的序列,以及对条形码区段和umi区段进行测序。虽然描述了聚t引物序列,但是其他靶向或随机引物序列也可以用于引发逆转录反应。同样,尽管描述为将带条形码的寡核苷酸释放到分区中,但是在一些情况下,与珠粒(例如,凝胶珠粒)结合的核酸分子可用于杂交和捕获珠粒固相上的mrna,例如,以便促进rna与其他细胞内容物的分离。
122.在一些情况下,可以将包含具有反应性或能够被活化以使其变为反应性的官能团的前体与其他前体聚合以生成包含活化或可活化的官能团的凝胶珠粒。然后官能团可用于将另外的物质(例如,二硫化物连接子、引物、其他寡核苷酸等)附接至凝胶珠粒。例如,一些包含羧酸(cooh)基团的前体可以与其他前体共聚以形成也包含cooh官能团的凝胶珠粒。在一些情况下,丙烯酸(包含游离cooh基团的物质)、丙烯酰胺和双(丙烯酰基)胱胺可以共聚在一起以产生包含游离cooh基团的凝胶珠粒。凝胶珠粒的cooh基团可以被活化(例如,经由1
‑
乙基
‑3‑
(3
‑
二甲基氨基丙基)碳二亚胺(edc)和n
‑
羟基琥珀酰亚胺(nhs)或4
‑
(4,6
‑
二甲氧基
‑
1,3,5
‑
三嗪
‑2‑
基)
‑4‑
甲基吗啉盐酸盐(dmtmm)),使得它们具有反应性(例如,当使用edc/nhs或dmtmm活化时,对胺官能团具有反应性)。然后,活化的cooh基团可以与包含待连接到珠粒上的部分的适当物质(例如,包含胺官能团的物质,其中羧酸基团经活化以与胺官能团具有反应性)反应。
123.在其聚合物网络中包含二硫连键的珠粒可用另外的物质,通过将一些二硫连键还原成游离硫醇而官能化。二硫连键可以通过例如还原剂(例如,dtt、tcep等)的作用而还原,以产生游离硫醇基团,而珠粒不会溶解。然后,珠粒的游离硫醇可以与物质或包含另一二硫键的物质的游离硫醇反应(例如,通过硫醇
‑
二硫化物交换),使得该物质可以与珠粒连接(例如,通过产生的二硫键)。在一些情况下,珠粒的游离硫醇可与任何其他适合基团反应。例如,珠粒的游离硫醇可与包含丙烯酰胺基部分的物质反应。珠粒的游离硫醇基团可以通过迈克尔加成化学与丙烯酰胺基反应,使得包含丙烯酰胺基的物质与珠粒连接。在一些情况下,可以通过包含硫醇封端剂(例如n
‑
乙基马来酰胺或碘乙酸)来防止不受控制的反应。
124.珠粒中二硫连键的活化可以控制,使得仅少量的二硫连键被活化。例如,可以通过控制用于生成游离硫醇基团的还原剂的浓度和/或用于在珠粒聚合中形成二硫键的试剂的浓度来进行控制。在一些情况下,低浓度(例如,还原剂分子:凝胶珠粒比率小于或等于约1:
100,000,000,000、小于或等于约1:10,000,000,000、小于或等于约1:1,000,000,000、小于或等于约1:100,000,000、小于或等于约1:10,000,000、小于或等于约1:1,000,000、小于或等于约1:100,000、小于或等于约1:10,000)还原剂可用于还原。控制还原为游离硫醇的二硫连键的数量可对确保官能化期间的珠粒结构完整性有用。在一些情况下,光学活性剂例如荧光染料可通过珠粒的游离硫醇基团与珠粒偶联,并用于定量珠粒中存在的游离硫醇的数量和/或跟踪珠粒。
125.在一些情况下,在凝胶珠粒形成后向凝胶珠粒添加部分可能是有利的。例如,在凝胶珠粒形成之后添加寡核苷酸(例如,带条形码的寡核苷酸)可以避免链转移终止期间物质的损失,该损失可在聚合过程中发生。而且,较小的前体(例如,不包含侧链基团和所连接的部分的单体或交联剂)可用于聚合,并且可以由于粘性效应,最小限度地阻碍其生长链端。在一些情况下,在凝胶珠粒合成之后的功能化可以使要负载潜在损伤因子(例如,自由基)和/或化学环境的物质(例如,寡核苷酸)的暴露最小化。在一些情况下,所产生的凝胶可具有上临界溶解温度(ucst),其可容许珠粒受温度驱动溶胀和坍塌。此类功能性可以有助于寡核苷酸(例如,引物)在随后用寡核苷酸对珠粒进行功能化期间渗入珠粒中。产生后的功能化也可用于控制珠粒中物质的负载比,使得例如负载比的可变性最小化。物质负载也可以在分批工艺中进行,使得多个珠粒可以在单一批次中受物质功能化。
126.注入或以其他方式引入到分区中的珠粒可以包含可释放地、可裂解地或可逆性地附接的条形码。注入或以其他方式引入到分区中的珠粒可以包含可活化的条形码。注入或以其他方式引入到分区中的珠粒可以是可降解的、可破裂的或可溶解的珠粒。
127.条形码可以可释放地、可裂解地或可逆性地附接至珠粒,使得条形码可以通过条形码分子和珠粒之间的连键的裂解而释放或可释放,或通过基础珠粒本身的降解而释放,从而允许条形码被其他试剂接近或可接近,或两者。在非限制性实例中,裂解可通过以下方式实现:二硫键的还原、限制酶的使用、光活化裂解或通过其他类型的刺激(例如化学、热、ph、酶刺激等)进行的裂解和/或反应,例如本文其他地方所述的。可释放的条形码有时可以称为是可活化的,因为它们一旦释放就可用于反应。因此,例如,可活化的条形码可以通过使条形码从珠粒(或本文所述的其他合适类型的分区)中释放而活化。在所述方法和系统的上下文中还设想了其他可活化构造。
128.除了珠粒与缔合分子之间的可裂解连键外,或作为珠粒与缔合分子之间的可裂解连键的替代,所述缔合分子例如为含有核酸分子的条形码(例如,带条形码的寡核苷酸),珠粒可以是自发地或在暴露于一种或多种刺激(例如,温度变化、ph变化、暴露于特定化学物质或相、暴露于光、还原剂等)时可降解的、可破裂的或可溶解的。在一些情况下,珠粒可以是可溶解的,使得当暴露于特定化学物质或环境变化,例如温度变化或ph变化时,珠粒的材料组分被溶解。在一些情况下,凝胶珠粒可在高温和/或碱性条件下降解或溶解。在一些情况下,珠粒可以是可热降解的,使得当珠粒暴露于适当的温度变化(例如,热)时,珠粒降解。与物质(例如,核酸分子,例如,带条形码的寡核苷酸)结合的珠粒的降解或溶解可引起物质从珠粒中释放。
129.正如从上述公开内容中可以认识到的,珠粒的降解可以指在有或没有结构性降解物理珠粒本身的情况下,所结合或夹带的物质从珠粒上解离。例如,珠粒的降解可涉及通过本文其他地方描述的一种或多种物质和/或方法裂解可裂解的连键。在另一个实例中,夹带
的物质可以通过由于例如改变化学环境而产生的渗透压差从珠粒中释放。举例来说,由于渗透压差引起的珠粒孔径的改变通常可以在珠粒本身没有结构降解的情况下发生。在一些情况下,由于珠粒的渗透溶胀而引起的孔径增加可容许珠粒内夹带的物质释放。在其他情况下,珠粒的渗透收缩可使珠粒由于孔径收缩而更好地保留夹带的物质。
130.可以将可降解珠粒引入到分区,例如乳液液滴或孔中,使得当施加适当的刺激时,珠粒在分区内降解并且任何缔合的物质(例如,寡核苷酸)都在液滴内释放。游离物质(例如,寡核苷酸、核酸分子)可以与分区内所含的其他试剂相互作用。例如,包含胱胺并通过二硫键与条形码序列连接的聚丙烯酰胺珠粒可以与还原剂在油包水乳液的液滴内组合。在液滴内,还原剂可断裂各种二硫键,导致珠粒降解并且条形码序列释放到液滴的内部水性环境中。在另一个实例中,在碱性溶液中加热包含珠粒结合的条形码序列的液滴也可导致珠粒降解并且附接的条形码序列释放到液滴的内部水性环境中。
131.任意合适数量的分子标签分子(例如,引物、带条形码的寡核苷酸)都可以与珠粒缔合,使得从珠粒中释放后,分区中存在预定浓度的分子标签分子(例如,引物,例如带条形码的寡核苷酸)。可以选择此类预定浓度以促进在分区内产生测序文库的某些反应,例如扩增。在一些情况下,引物的预定浓度可以通过产生带有核酸分子(例如,寡核苷酸)的珠粒的过程来限制。
132.在一些情况下,珠粒可以非共价负载有一种或多种试剂。例如,通过使珠粒经受足以使珠粒溶胀的条件,允许有足够的时间使试剂扩散到珠粒的内部,以及使珠粒经受足以使珠粒去溶胀的条件,可以使珠粒非共价地负载。珠粒的溶胀可通过例如将珠粒置于热力学上有利的溶剂中,使珠粒经受更高或更低的温度,使珠粒经受更高或更低的离子浓度和/或使珠粒经受电场来完成。珠粒的溶胀可以通过各种溶胀方法完成。珠粒的去溶胀可通过例如转移热力学上有利的溶剂中的珠粒,使珠粒经受更低的温度或高温,使珠粒经受更低或更高的离子浓度和/或将珠粒从电场中移除来完成。珠粒的去溶胀可以通过各种去溶胀方法完成。转移珠粒可引起珠粒中的孔隙收缩。然后收缩可阻碍珠粒内的试剂从珠粒内部扩散出来。所述阻碍可能是由于试剂与珠粒内部之间的空间相互作用产生的。转移可以用微流体方式来完成。例如,可以通过将珠粒从一个共流溶剂流移动到不同的共流溶剂流来实现转移。珠粒的可溶胀性和/或孔径可通过改变珠粒的聚合物组成来调节。
133.在一些情况下,与前体连接的丙烯酰胺基部分,与前体连接的另一物质,或前体本身可以包含不稳定键,例如化学敏感键、热敏键或光敏键,例如二硫键、uv敏感键等。一旦丙烯酰胺基部分或包含不稳定键的其他部分掺入到珠粒中,则珠粒也可以包含不稳定键。不稳定键可以例如用于将物质(例如,条形码、引物等)可逆性地连接(例如,共价连接)到珠粒上。在一些情况下,热不稳定键可以包括基于核酸杂交的附接,例如,其中寡核苷酸与附接至珠粒的互补序列杂交,使得杂交体的热解链使寡核苷酸(例如含条形码的序列)从珠粒或微囊中释放。
134.向凝胶珠粒添加多种类型的不稳定键可导致生成能够响应各种刺激的珠粒。每种类型的不稳定键可能对相关刺激(例如,化学刺激、光、温度、酶等)敏感,使得可以通过施加适当的刺激来控制经由每种不稳定键附接至珠粒的物质的释放。此类功能性可用于物质从凝胶珠粒的控释中。在一些情况下,包含不稳定键的另一种物质可以在凝胶珠粒形成之后通过例如如上所述的凝胶珠的活化官能团与凝胶珠粒连接。正如将认识到的,可释放地、可
裂解地或可逆性地附接至本文所述的珠粒的条形码包括通过条形码分子和珠粒之间的连键的裂解而释放的条形码,或通过基础珠粒本身的降解而释放,从而允许条形码被其他试剂接近或可接近的条形码,或两者。
135.如本文所述的可释放的条形码有时可以称为可活化,因为它们一旦释放,就可用于反应。因此,例如,可活化的条形码可以通过使条形码从珠粒(或本文所述的其他合适类型的分区)中释放而活化。在所述方法和系统的上下文中还设想了其他可活化构造。
136.除了可热裂解的键、二硫键和uv敏感键之外,可偶联至前体或珠粒的不稳定键的其他非限制性实例包括酯连键(例如,可被酸、碱或羟胺裂解)、邻二醇连键(例如,可经由高碘酸钠裂解)、diels
‑
alder连键(例如,可经由热裂解)、砜连键(例如,可经由碱裂解)、甲硅烷基醚连键(例如,可经由酸裂解)、糖苷连键(例如,可经由淀粉酶裂解)、肽连键(例如,可经由蛋白酶裂解)或磷酸二酯连键(例如,可经由核酸酶(例如,dnase)裂解)。键可通过其他靶向核酸分子的酶,例如限制酶(例如,限制性内切核酸酶)裂解,如下面进一步描述的。
137.可在珠粒产生期间(例如,在前体聚合期间)将物质包封在珠粒中。此类物质可以参与或可以不参与聚合。此类物质可以进入聚合反应混合物中,使得在珠粒形成后,产生的珠粒包含所述物质。在一些情况下,可以在形成之后将此类物质添加到凝胶珠粒中。此类物质可以包括例如核酸分子(例如,寡核苷酸),用于核酸扩增反应的试剂(例如,引物、聚合酶、dntp、辅因子(例如,离子辅因子)、缓冲剂)(包括本文所述的那些),用于酶促反应的试剂(例如,酶、辅因子、底物、缓冲剂),用于核酸修饰反应(例如聚合、连接或消化)的试剂,和/或用于一个或多个测序平台的模板制备(例如,标签化)的试剂(例如,用于的)。此类物质可以包括本文所述的一种或多种酶,包括但不限于聚合酶、逆转录酶、限制酶(例如,内切核酸酶)、转座酶、连接酶、蛋白酶k、dnase等。此类物质可以包括本文其他地方描述的一种或多种试剂(例如,裂解剂、抑制剂、灭活剂、螯合剂、刺激物)。此类物质的捕集可以通过在前体聚合期间产生的聚合物网络密度、对凝胶珠粒内离子电荷的控制(例如,通过与聚合物质连接的离子物质)或通过其他物质的释放来控制。可以在珠粒降解时和/或通过施加能够使物质从珠粒中释放的刺激,使包封的物质从珠粒中释放。可替代地或另外,可以在分区形成期间或之后,将物质分配在分区(例如,液滴)中。此类物质可以包括但不限于以上提到的也可以包封在珠粒中的物质。
138.可降解珠粒可以包含一种或多种具有不稳定键的物质,使得当珠粒/物质暴露于适当的刺激时,键断裂并且珠粒降解。不稳定键可以是化学键(例如,共价键、离子键)或者可以是另一种类型的物理相互作用(例如,范德华相互作用、偶极
‑
偶极相互作用等)。在一些情况下,用于产生珠粒的交联剂可以包含不稳定键。暴露于适当条件时,不稳定键可断裂并且珠粒降解。例如,将包含胱胺交联剂的聚丙烯酰胺凝胶珠粒暴露于还原剂时,胱胺的二硫键可断裂并且珠粒降解。
139.与不降解的珠粒相比,当对珠粒施加适当的刺激时,可降解珠粒可以用于更快速地使附接的物质(例如,核酸分子、条形码序列、引物等)从珠粒释放。例如,对于与多孔珠粒的内表面结合的物质,或在包封的物质的情况下,在珠粒降解时,所述物质在溶液中可具有更大的迁移率和与其他物质的可接近性。在一些情况下,物质还可以经由可降解连接子(例如,二硫化物连接子)与可降解珠粒连接。可降解连接子可与可降解珠粒响应于相同的刺激,或者两种可降解物质可响应于不同的刺激。例如,条形码序列可以通过二硫键与包含胱
胺的聚丙烯酰胺珠粒连接。带条形码的珠粒暴露于还原剂时,珠粒会降解并且在条形码序列与珠粒之间的二硫连键以及珠粒中的胱胺的二硫连键都断裂时,条形码序列被释放。
140.正如将从上述公开内容中认识到的,当称为珠粒的降解时,在如以上提到的许多情况下,所述降解可以指在有或没有结构性降解物理珠粒本身的情况下,所结合或夹带的物质从珠粒上解离。例如,夹带的物质可以通过由于例如改变化学环境而产生的渗透压差从珠粒中释放。举例来说,由于渗透压差引起的珠粒孔径的改变通常可以在珠粒本身没有结构降解的情况下发生。在一些情况下,由于珠粒的渗透溶胀而引起的孔径增加可容许珠粒内夹带的物质释放。在其他情况下,珠粒的渗透收缩可使珠粒由于孔径收缩而更好地保留夹带的物质。
141.在提供可降解珠粒的情况下,避免在给定时间之前将此类珠粒暴露于引起此类降解的一种或多种刺激可能是有益的,例如,以避免珠粒过早降解以及由此类降解引起的问题,包括例如不良的流动特征和聚集。举例来说,在珠粒包含可还原的交联基团,例如二硫基团的情况下,将期望避免使此类珠粒与还原剂例如dtt或其他二硫化物裂解试剂接触。在此类情况下,将在一些情况下提供不含还原剂(例如dtt)的对本文所述珠粒的处理。因为在商业酶制剂中常常会提供还原剂,所以可能期望在处理本文所述的珠粒时提供不含还原剂(或不含dtt)的酶制剂。此类酶的实例包括例如聚合酶制剂、逆转录酶制剂、连接酶制剂以及许多可用于处理本文所述的珠粒的其他酶制剂。术语“不含还原剂”或“不含dtt”的制剂可以指具有小于约1/10、小于约1/50或甚至小于约1/100下限的用于降解珠粒的此类材料的制剂。例如,对于dtt,不含还原剂的制剂可以具有小于约0.01毫摩尔(mm)、0.005mm、0.001mm dtt、0.0005mm dtt,或甚至小于约0.0001mm dtt。在许多情况下,dtt的量是不可检测的。
142.许多化学触发剂可以用于触发珠粒的降解。这些化学变化的实例可以包括但不限于ph介导的珠粒内组分完整性的改变、珠粒组分通过交联键断裂进行的降解和珠粒组分的解聚。
143.在一些实施方案中,珠粒可由包含可降解的化学交联剂例如bac或胱胺的材料形成。此类可降解交联剂的降解可以通过许多机制完成。在一些实例中,可以使珠粒与可以诱导氧化、还原或其他化学变化的化学降解剂接触。例如,化学降解剂可以是还原剂,例如二硫苏糖醇(dtt)。还原剂的其他实例可以包括β
‑
巯基乙醇、(2s)
‑2‑
氨基
‑
1,4
‑
二巯基丁烷(二硫代丁胺或dtba)、三(2
‑
羧乙基)膦(tcep)或它们的组合。还原剂可以降解在形成珠粒的凝胶前体之间形成的二硫键,并且因此可以降解珠粒。在其他情况下,溶液ph的变化,例如ph的增加,可触发珠粒的降解。在其他情况下,暴露于水溶液例如水,可触发水解降解,并且因此可以触发珠粒的降解。在一些情况下,刺激的任何组合可以触发珠粒的降解。例如,ph的变化可以使化学试剂(例如,dtt)成为有效的还原剂。
144.在施加热刺激时,还可诱导珠粒释放其内容物。温度的变化可引起珠粒的各种变化。例如,热量可以引起固体珠粒液化。热量的变化可引起珠粒熔融,使得珠粒的一部分降解。在其他情况下,热量可以增加珠粒组分的内部压力,使得珠粒破裂或爆裂。热量也可作用于用作构造珠粒的材料的热敏聚合物。
145.任何适合试剂都可以降解珠粒。在一些实施方案中,可以使用温度或ph的变化来降解珠粒中的热敏或ph敏感键。在一些实施方案中,可以使用化学降解剂通过氧化、还原或
其他化学变化来降解珠粒中的化学键。例如,化学降解剂可以是还原剂,例如dtt,其中dtt可以降解在交联剂与凝胶前体之间形成的二硫键,从而降解珠粒。在一些实施方案中,可以添加还原剂以降解珠粒,这可以引起或可以不引起珠粒释放其内容物。还原剂的实例可以包括二硫苏糖醇(dtt)、β
‑
巯基乙醇、(2s)
‑2‑
氨基
‑
1,4
‑
二巯基丁烷(二硫代丁胺或dtba)、三(2
‑
羧乙基)膦(tcep)或它们的组合。还原剂可以以0.1mm、0.5mm、1mm、5mm、10mm的浓度存在。还原剂可以以至少约0.1mm、0.5mm、1mm、5mm、10mm或高于10mm的浓度存在。还原剂可以以至多约10mm、5mm、1mm、0.5mm、0.1mm或更低的浓度存在。
146.任意合适数量的分子标签分子(例如,引物、带条形码的寡核苷酸)都可以与珠粒缔合,使得从珠粒中释放后,分区中存在预定浓度的分子标签分子(例如,引物,例如带条形码的寡核苷酸)。可以选择此类预定浓度以促进在分区内产生测序文库的某些反应,例如扩增。在一些情况下,引物的预定浓度可以通过产生带有寡核苷酸的珠粒的过程来限制。
147.尽管图1和图2已经根据提供基本上单个占用的分区进行了描述,但是在上面,在某些情况下,可能期望提供多个占用的分区,例如,在单个分区内含有两个、三个、四个或更多个包含条形码化核酸分子(例如,寡核苷酸)的细胞和/或微囊(例如,珠粒)。因此,如上所述,可以控制含有生物颗粒和/或珠粒的流体和分配流体的流动特征,以提供此类多个占用的分区。具体来说,可以控制流动参数以提供大于约50%的分区、大于约75%,并且在某些情况下大于约80%、90%、95%或更高百分比的给定占用率。
148.在一些情况下,可以使用其他微囊将其他试剂递送到分区。在此类情况下,可能有利的是将不同的珠粒从不同的珠粒源(例如,含有不同的相关试剂)通过通入共用通道或液滴生成接点(例如,接点210)的不同通道入口引入到此类共用通道或液滴生成接点中。在此类情况下,可以控制不同珠粒流入通道或接点的流量和频率,以提供一定比率的来自每个来源的微囊,同时确保进入分区的此类珠粒与给定数量的生物颗粒的给定配对或组合(例如,每个分区一个生物颗粒和一个珠粒)。
149.本文所述的分区可以包含小体积,例如小于约10微升(l)、5l、1l、900皮升(pl)、800pl、700pl、600pl、500pl、400pl、300pl、200pl、100pl、50pl、20pl、10pl、1pl、500纳升(nl)、100nl、50nl或更小。
150.例如,在基于液滴的分区的情况下,液滴的总体积可小于约1000pl、900pl、800pl、700pl、600pl、500pl、400pl、300pl、200pl、100pl、50pl、20pl、10pl、1pl或更小。在与微囊共同分配的情况下,将认识到在分区内的样品流体体积,例如包括共同分配的生物颗粒和/或珠粒,可以小于上述体积的约90%、小于上述体积的约80%、小于上述体积的约70%、小于上述体积的约60%、小于上述体积的约50%、小于上述体积的约40%、小于上述体积的约30%、小于上述体积的约20%或小于上述体积的约10%。
151.如本文其他地方所述,将物质分配可以产生一群或多个分区。在此类情况下,可以产生或以其他方式提供任意合适数量的分区。例如,可产生或以其他方式提供至少约1,000个分区、至少约5,000个分区、至少约10,000个分区、至少约50,000个分区、至少约100,000个分区、至少约500,000个分区、至少约1,000,000个分区、至少约5,000,000个分区、至少约10,000,000个分区、至少约50,000,000个分区、至少约100,000,000个分区、至少约500,000,000个分区、至少约1,000,000,000个分区或更多个分区。而且,所述多个分区可以包括未占用分区(例如,空分区)和已占用分区。
152.试剂
153.根据某些方面,可以将生物颗粒连同裂解试剂一起分配,以便释放分区内生物颗粒的内容物。在此类情况下,可以在将生物颗粒引入到分配接点/液滴生成区(例如接点210)中的同时或就在之前,例如通过通道接点上游的一个或多个另外的通道,使裂解剂与生物颗粒悬浮液接触。根据其他方面,另外或可替代地,生物颗粒可以连同其他试剂一起分区,正如下面将进一步描述的那样。
154.图3示出了用于将生物颗粒和试剂共同分配的微流体通道结构300的一个实例。通道结构300可以包括通道区段301、302、304、306和308。通道区段301和302在第一通道接点309处连通。通道区段302、304、306和308在第二通道接点310处连通。
155.在示例性操作中,通道区段301可以将包括多个生物颗粒314的水性流体312沿通道区段301转运至接点310处。作为替代或补充,通道区段301还可以转运珠粒(例如,凝胶珠粒)。珠粒可以包含条形码分子。
156.例如,通道区段301可以连接至包含生物颗粒314的水性悬浮液的储槽。在第二接点310上游并且就在到达第二接点之前,通道区段301可在第一接点309处遇到通道区段302。通道区段302可以将悬浮在含水流体312中的多个试剂315(例如,裂解剂)沿通道区段302转运到第一汇合点309中。例如,通道区段302可以连接至包含试剂315的储槽。在第一接点309之后,通道区段301中的水性流体312可以将生物颗粒314与试剂315两者携带到第二接点310处。在一些情况下,通道区段301中的水性流体312可以包括一种或多种试剂,所述试剂可以与试剂315相同或不同。可以将与水性流体312不可混溶的第二流体316(例如,油)从通道区段304和306中的每一个递送至第二接点310处。在来自通道区段301的水性流体312与来自通道区段304和306中的每一个的第二流体316在第二通道接点310处会合时,水性流体312可以在第二流体316中分配为离散液滴318并且沿通道区段308从第二接点310处流走。通道区段308可以将离散液滴318递送到与通道区段308流体联接的出口储槽,可以将离散液滴收获在出口储槽中。
157.第二流体316可以包含油,例如含氟油,所述油包括用于稳定所得液滴,例如抑制所得液滴318的后续聚结的含氟表面活化剂。
158.生成的离散液滴可以包括单独的生物颗粒314和/或一种或多种试剂315。在一些情况下,生成的离散液滴可以包括携带条形码的珠粒(未示出),例如经由本文其他地方所述的其他微流体。在一些情况下,离散液滴可以未被占用(例如,无试剂、无生物颗粒)。
159.有益地,当裂解试剂和生物颗粒共同分配时,裂解试剂可以促进分区内生物颗粒的内容物的释放。分区中释放的内容物可保持与其他分区的内容物离散。
160.正如将认识到的,本文所述的通道区段可以联接至各种不同的流体源或接收部件中的任何一个,包括储槽、管道、歧管或其他系统的流体部件。正如将认识到的,微流体通道结构300可以具有其他几何结构。例如,微流体通道结构可以具有两个以上的通道接点。例如,微流体通道结构可以具有2、3、4、5个通道区段或更多,每个通道区段携带相同或不同类型的珠粒、试剂和/或生物颗粒,这些通道区段在通道接点处会合。可以控制每个通道区段中的流体流动以控制将不同元素分配到液滴中。可以引导流体经由一个或多个流体流动单元沿一个或多个通道或储槽流动。流体流动单元可以包括压缩机(例如,提供正压)、泵(例如,提供负压)、致动器等,以控制流体的流量。流体还可以或以其他方式通过施加的压力
差、离心力、电动泵送、真空、毛细管流或重力流等来控制。
161.裂解剂的实例包括生物活性试剂,例如用于裂解不同细胞类型(例如革兰氏阳性或阴性细菌、植物、酵母、哺乳动物等)的裂解酶,例如溶菌酶、无色肽酶、溶葡球菌酶、唇形酶(labiase)、立枯丝核菌裂解酶(kitalase)、溶细胞酶,和多种其他可从例如sigma
‑
aldrich,inc.(st louis,mo)获得的裂解酶,以及其他可商购获得的裂解酶。其他裂解剂可以另外或可替代地与生物颗粒共同分配,以引起生物颗粒的内容物释放到分区中。例如,在一些情况下,基于表面活性剂的裂解溶液可以用于裂解细胞,但是这些对于基于乳液的体系可能是不太期望的,其中表面活性剂可干扰稳定的乳液。在一些情况下,裂解溶液可以包含非离子表面活性剂,例如tritonx
‑
100和tween 20。在一些情况下,裂解溶液可以包含离子表面活性剂,例如像十二烷基肌氨酸钠和十二烷基硫酸钠(sds)。在某些情况下也可以使用电穿孔、热、声或机械细胞破坏,例如,非基于乳液的分配,例如可以作为液滴分配的补充或代替的生物颗粒包封,其中包封物的任何孔径都足够小以在细胞破裂后保留给定大小的核酸片段。
162.作为与上述生物颗粒共同分配的裂解剂的替代或补充,其他试剂也可与生物颗粒共同分配,包括例如dnase和rnase灭活剂或抑制剂(例如蛋白酶k)、螯合剂(例如edta),以及用于消除或以其他方式降低不同细胞裂解物组分的负面活性或对核酸后续处理的影响的其他试剂。另外,在包封的生物颗粒的情况下,可将生物颗粒暴露于适当的刺激下以使生物颗粒或其内容物从共同分配的微囊中释放。例如,在一些情况下,化学刺激可以连同包封的生物颗粒一起共同分配,以允许微囊降解以及细胞或其内容物释放到更大的分区中。在一些情况下,这种刺激可以与本文其他地方描述的用于核酸分子(例如,寡核苷酸)从它们各自的微囊(例如,珠粒)释放的刺激相同。在替代方面中,这可以是不同且不重叠的刺激,以便允许包封的生物颗粒在与核酸分子释放到分区中不同的时间释放到同一分区中。
163.其他试剂也可以与生物颗粒共同分配,例如用于使生物颗粒的dna片段化的内切核酸酶,用于扩增生物颗粒的核酸片段并将条形码分子标签附接至扩增片段的dna聚合酶和dntp。其他酶可共同分配,包括但不限于聚合酶、转座酶、连接酶、蛋白酶k、dnase等。另外的试剂还可以包括逆转录酶,包括具有末端转移酶活性的酶、引物和寡核苷酸、以及可以用于模板转换的转换寡核苷酸(在本文中也称为“转换oligo”或“模板转换寡核苷酸”)。在一些情况下,模板切换可用于增加cdna的长度。在一些情况下,模板切换可用于将预定核酸序列附加到cdna上。在模板切换的实例中,可由模板例如细胞mrna的逆转录产生cdna,其中具有末端转移酶活性的逆转录酶可以以模板非依赖性方式向cdna添加附加核苷酸,例如聚c。切换寡核苷酸可以包括与附加核苷酸例如聚g互补的序列。cdna上的附加核苷酸(例如,聚c)可以与切换寡核苷酸上的附加核苷酸(例如,聚g)杂交,由此切换寡核苷酸可以被逆转录酶用作模板以进一步延伸cdna。模板切换寡核苷酸可以包含杂交区和模板区。杂交区可以包含能够与靶标杂交的任何序列。在一些情况下,如先前所述,杂交区包含一系列g碱基以与cdna分子的3’末端处突出的c碱基互补。所述系列的g碱基可以包括1个g碱基、2个g碱基、3个g碱基、4个g碱基、5个g碱基或多于5个g碱基。模板序列可以包含待掺入cdna中的任何序列。在一些情况中,模板区包含至少1个(例如,至少2、3、4、5个或更多个)标签序列和/或功能序列。切换寡聚物可以包含脱氧核糖核酸;核糖核酸;经修饰的核酸,包括2
‑
氨基嘌呤、2,6
‑
二氨基嘌呤(2
‑
氨基
‑
da)、反向dt、5
‑
甲基dc、2
’‑
脱氧肌苷、超级t(5
‑
羟基丁酰
‑2’‑
脱氧
尿苷)、超级g(8
‑
氮杂
‑7‑
脱氮鸟苷)、锁核酸(lna)、解锁核酸(una,例如una
‑
a、una
‑
u、una
‑
c、una
‑
g)、异
‑
dg、异
‑
dc、2’氟碱基(例如,氟c、氟u、氟a和氟g)或任何组合。
164.在一些情况下,切换寡核苷酸的长度可为至少约2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112、113、114、115、116、117、118、119、120、121、122、123、124、125、126、127、128、129、130、131、132、133、134、135、136、137、138、139、140、141、142、143、144、145、146、147、148、149、150、151、152、153、154、155、156、157、158、159、160、161、162、163、164、165、166、167、168、169、170、171、172、173、174、175、176、177、178、179、180、181、182、183、184、185、186、187、188、189、190、191、192、193、194、195、196、197、198、199、200、201、202、203、204、205、206、207、208、209、210、211、212、213、214、215、216、217、218、219、220、221、222、223、224、225、226、227、228、229、230、231、232、233、234、235、236、237、238、239、240、241、242、243、244、245、246、247、248、249或250个核苷酸或更长。
165.在一些情况下,切换寡核苷酸的长度可为至多约2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112、113、114、115、116、117、118、119、120、121、122、123、124、125、126、127、128、129、130、131、132、133、134、135、136、137、138、139、140、141、142、143、144、145、146、147、148、149、150、151、152、153、154、155、156、157、158、159、160、161、162、163、164、165、166、167、168、169、170、171、172、173、174、175、176、177、178、179、180、181、182、183、184、185、186、187、188、189、190、191、192、193、194、195、196、197、198、199、200、201、202、203、204、205、206、207、208、209、210、211、212、213、214、215、216、217、218、219、220、221、222、223、224、225、226、227、228、229、230、231、232、233、234、235、236、237、238、239、240、241、242、243、244、245、246、247、248、249或250个核苷酸。
166.一旦细胞的内容物释放到它们各自的分区中,其中所含的大分子组分(例如,生物颗粒的大分子成分,例如rna、dna或蛋白质)就可以在分区内被进一步处理。根据本文所述的方法和系统,可以为单独的生物颗粒的大分子组分内容物提供唯一标识符,使得在表征那些大分子组分时,可以将其归属为源自相同的一个或多个生物颗粒。通过将唯一标识符特异性地分配给单独的生物颗粒或多组生物颗粒来提供将特征归属于单独生物颗粒或多组生物颗粒的能力。唯一标识符(例如,为核酸条形码形式)可以分配给单独的生物颗粒或生物颗粒群体或与之缔合,以便用唯一标识符标注或标记生物颗粒的大分子组分(并因此,标注或标记其特征)。然后,可以使用这些唯一标识符将生物颗粒的组分和特征归属于单独的生物颗粒或一组生物颗粒。
167.在一些方面中,这是通过将单独的生物颗粒或多组生物颗粒组与唯一标识符共同分配来进行的,例如上文所述(参考图2)。在一些方面,唯一标识符以核酸分子(例如,寡核
苷酸)的形式提供,所述核酸分子包含可以与单独的生物颗粒的核酸内容物,或与生物颗粒的其他组分,并且尤其是与那些核酸的片段附接或以其他方式缔合的核酸条形码序列。分配核酸分子,使得在给定分区中的核酸分子之间,其中所含的核酸条形码序列相同,但是在不同分区之间,核酸分子可以并且确实具有不同的条形码序列,或者在给定分析中的所有分区中至少呈现出大量不同的条形码序列。在一些方面,仅一个核酸条形码序列可以与给定分区缔合,但是在一些情况下,可以存在两个或更多个不同的条形码序列。
168.在核酸分子(例如,寡核苷酸)的序列内,核酸条形码序列可以包括约6至约20个核苷酸。核酸条形码序列可以包括约6至约20、30、40、50、60、70、80、90、100个或更多个核苷酸。在一些情况下,条形码序列的长度可为约6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个核苷酸或更长。在一些情况下,条形码序列的长度可为至少约6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个核苷酸或更长。在一些情况下,条形码序列的长度可为至多约6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个核苷酸或更短。这些核苷酸可以是完全连续的,即处于单一的相邻核苷酸段中,或者它们可以分离成由1个或更多个核苷酸隔开的两个或更多个分离的子序列。在一些情况下,分离的条形码子序列的长度可以为约4至约16个核苷酸。在一些情况下,条形码序列的长度可为约4、5、6、7、8、9、10、11、12、13、14、15、16个核苷酸或更长。在一些情况下,条形码序列的长度可为至少约4、5、6、7、8、9、10、11、12、13、14、15、16个核苷酸或更长。在一些情况下,条形码序列的长度可为至多约4、5、6、7、8、9、10、11、12、13、14、15、16个核苷酸或更短。
169.共同分配的核酸分子还可以包含可用于处理来自于共同分配的生物颗粒生物颗粒的核酸的其他功能序列。这些序列包括例如,用于扩增来自于分区内单独的生物颗粒生物颗粒的基因组dna,同时附接相关条形码序列的靶向或随机/通用扩增引物序列,测序引物或引物识别位点,杂交或探测序列(例如用于鉴定序列的存在或用于下拉带条形码的核酸),或许多其他潜在功能序列中的任一种。也可以采用将寡核苷酸共同分配的其他机制,包括例如两个或更多个液滴的聚结,其中一个液滴含有寡核苷酸,或将寡核苷酸微分配到分区(例如微流体系统内的液滴)中。
170.在一个实例中,提供了微囊,例如珠粒,其各自包括大量可释放地附接至珠粒的上述条形码化核酸分子(例如,带条形码的寡核苷酸),其中附接至特定珠粒的所有核酸分子都将包括相同的核酸条形码序列,但其中在所使用的珠粒群体中呈现出大量不同的条形码序列。在一些实施方案中,水凝胶珠粒(例如,包含聚丙烯酰胺聚合物基质)用作固相支持体和将核酸分子递送至分区中的媒介物,因为它们能够携带大量核酸分子,并且可以被配置成如本文其他地方所述,暴露于特定刺激时,释放核酸分子。在一些情况下,所述珠粒群体提供多样化条形码序列文库,该文库包括至少约1,000个不同的条形码序列、至少约5,000个不同的条形码序列、至少约10,000个不同的条形码序列、至少约50,000个不同的条形码序列、至少约100,000个不同的条形码序列、至少约1,000,000个不同的条形码序列、至少约5,000,000个不同的条形码序列或至少约10,000,000个不同的条形码序列或更多。另外,可以为每个珠粒提供大量附接的核酸(例如,寡核苷酸)分子。具体来说,单独的珠粒上的核酸分子中包括条形码序列的分子数量可以为至少约1,000个核酸分子、至少约5,000个核酸分子、至少约10,000个核酸分子、至少约50,000个核酸分子、至少约100,000个核酸分子、至少约500,000个核酸、至少约1,000,000个核酸分子、至少约5,000,000个核酸分子、至少约10,
000,000个核酸分子、至少约50,000,000个核酸分子、至少约100,000,000个核酸分子、至少约250,000,000个核酸分子并且在一些情况下为至少约10亿个核酸分子或更多。给定珠粒的核酸分子可以包括相同的(或共同的)条形码序列、不同的条形码序列,或两者的组合。给定珠粒的核酸分子可以包括多个集合的核酸分子。给定集合的核酸分子可以包括相同的条形码序列。所述相同的条形码序列可以与另一集合的核酸分子的条形码序列不同。
171.而且,分配珠粒群体时,所得珠粒群体也可以包括多样化条形码文库,该文库包括至少约1,000个不同的条形码序列、至少约5,000个不同的条形码序列、至少约10,000个不同的条形码序列、至少约50,000个不同的条形码序列、至少约100,000个不同的条形码序列、至少约1,000,000个不同的条形码序列、至少约5,000,000个不同的条形码序列或至少约10,000,000个不同的条形码序列。另外,该群体的每个分区可以包括至少约1,000个核酸分子、至少约5,000个核酸分子、至少约10,000个核酸分子、至少约50,000个核酸分子、至少约100,000个核酸分子、至少约500,000个核酸、至少约1,000,000个核酸分子、至少约5,000,000个核酸分子、至少约10,000,000个核酸分子、至少约50,000,000个核酸分子、至少约100,000,000个核酸分子、至少约250,000,000个核酸分子并且在一些情况下包括至少约10亿个核酸分子。
172.在一些情况下,可能期望在给定分区内掺入多个不同的条形码,无论是附接至分区内的单个珠粒还是多个珠粒。例如,在一些情况下,混合但已知的条形码序列集合可在后续处理中提供更大的标识保证,例如,通过向给定分区提供条形码的更强寻址或归属,作为来自给定分区的输出的重复或独立确认。
173.核酸分子(例如,寡核苷酸)在向珠粒施加特定刺激时可从珠粒释放。在一些情况下,所述刺激可以是光刺激,例如通过裂解光不稳定性连键释放核酸分子。在其他情况下,可以使用热刺激,其中珠粒环境温度的升高将导致连键的断裂或核酸分子从珠粒的另外释放。在其他情况下,可以使用化学刺激,其裂解核酸分子与珠粒的连键,或以其他方式导致核酸分子从珠粒释放。在一种情况下,此类组合物包括上述用于包封生物颗粒的聚丙烯酰胺基质,并且可以通过暴露于还原剂(例如dtt)而降解,以释放所附接的核酸分子。
174.在一些方面,提供了用于进行受控分配的系统和方法。可以通过调节通道结构(例如,微流体通道结构)中的某些几何特征来控制液滴大小。例如,可以调节通道的扩展角、宽度和/或长度以控制液滴大小。
175.图4示出了用于将珠粒受控分配到离散液滴中的微流体通道结构的一个实例。通道结构400可以包括在通道接点406(或交叉点)处与储槽404连通的通道区段402。储槽404可以是腔室。如本文所用,任何对“储槽”的提及,也可以指“腔室”。在操作时,包括悬浮珠粒412的水性流体408可以沿通道区段402转运到接点406处,以与储槽404中与水性流体408不可混溶的第二流体410会合,以产生流入储槽404中的水性流体408的液滴416、418。在水性流体408和第二流体410会合的接点406处,可以基于例如接点406处的流体动力、两股流体408、410的流速、流体特性以及通道结构400的某些几何参数(例如,w、h0、α等)的因素而形成液滴。可以通过将水性流体408从通道区段402连续注射通过接点406而将多个液滴收集在储槽404中。
176.生成的离散液滴可以包括珠粒(例如,如同在已占用液滴416中)。可替代地,生成的离散液滴可以包括多于一个珠粒。可替代地,生成的离散液滴可以不包括任何珠粒(例
如,如同在未占用液滴418中)。在一些情况下,生成的离散液滴可以含有一个或多个生物颗粒,如本文其他地方所述。在一些情况下,生成的离散液滴可以包含一种或多种试剂,如本文其他地方所述。
177.在一些情况下,水性流体408可以具有浓度或频率基本上均一的珠粒412。可以从单独的通道(图4中未示出)将珠粒412引入到通道区段402中。可以通过控制将珠粒412引入到通道区段402中的频率和/或通道区段402和单独的通道中流体的相对流速来控制通道区段402中的珠粒412的频率。在一些情况下,可以从多个不同的通道将珠粒引入到通道区段402中,并因此而控制频率。
178.在一些情况下,通道区段402中的水性流体408可以包含生物颗粒(例如,参考图1和图2中描述的)。在一些情况下,水性流体408可以具有浓度或频率基本上均一的生物颗粒。如同珠粒一样,可以从单独的通道将生物颗粒引入到通道区段402中。可以通过控制将生物颗粒引入到通道区段402中的频率和/或通道区段402和单独的通道中流体的相对流速来控制通道区段402中的水性流体408中的生物颗粒的频率或浓度。在一些情况下,可以从多个不同的通道将生物颗粒引入到通道区段402中,并因此而控制频率。在一些情况下,第一单独通道可以将珠粒引入到通道区段402中并且第二单独通道可以将生物颗粒引入到其中。引入珠粒的第一单独通道可以在引入生物颗粒的第二单独通道的上游或下游。
179.第二流体410可以包含油,例如含氟油,所述油包括用于稳定所得液滴,例如抑制所得液滴的后续聚结的含氟表面活化剂。
180.在一些情况下,第二流体410可以不经受和/或不被引导流入和流出储槽404。例如,第二流体410在储槽404中可以是基本上静止的。在一些情况下,第二流体410可以经受在储槽404内流动,但不会流入和流出储槽404,例如通过向储槽404施加压力和/或受到接点406处的水性流体408的来流影响时。可替代地,第二流体410可以经受和/或被引导流入或流出储槽404。例如,储槽404可以是将第二流体410从上游引导至下游,从而转运生成的液滴的通道。
181.在接点406处或附近的通道结构400可以具有至少部分地决定了由通道结构400形成的液滴大小的某些几何特征。通道区段402在接点406处或附近可以具有高度h0和宽度w。举例来说,通道区段402可以包括矩形横截面,该矩形横截面通向具有更宽的横截面(例如在宽度或直径方面)的储槽404。可替代地,通道区段402的横截面可以是其他形状,例如圆形、梯形、多边形或任何其他形状。在接点406处的储槽404的顶壁和底壁可以呈扩展角α倾斜。扩展角α使舌部(在液滴形成之前,水性流体408从接点406处离开通道区段402并且进入储槽404的部分)长度增加并且促进中间形成的液滴的曲率减小。液滴大小随着扩展角增大而减小。所得液滴的半径r
d
可以通过以下针对前述几何参数h0、w和α的方程式来预测:
[0182][0183]
举例来说,对于w=21μm、h=21μm和α=3
°
的通道结构来说,预测的液滴大小为121μm。在另一个实例中,对于w=25μm、h=25μm和α=5
°
的通道结构来说,预测的液滴大小为123μm。在另一个实例中,对于w=28μm、h=28μm和α=7
°
的通道结构来说,预测的液滴大小为124μm。
[0184]
在一些情况下,扩展角α可以在约0.5
°
至约4
°
、约0.1
°
至约10
°
或约0
°
至约90
°
的范
围之间。例如,扩展角可以为至少约0.01
°
、0.1
°
、0.2
°
、0.3
°
、0.4
°
、0.5
°
、0.6
°
、0.7
°
、0.8
°
、0.9
°
、1
°
、2
°
、3
°
、4
°
、5
°
、6
°
、7
°
、8
°
、9
°
、10
°
、15
°
、20
°
、25
°
、30
°
、35
°
、40
°
、45
°
、50
°
、55
°
、60
°
、65
°
、70
°
、75
°
、80
°
、85
°
或更大。在一些情况下,扩展角可以为至多约89
°
、88
°
、87
°
、86
°
、85
°
、84
°
、83
°
、82
°
、81
°
、80
°
、75
°
、70
°
、65
°
、60
°
、55
°
、50
°
、45
°
、40
°
、35
°
、30
°
、25
°
、20
°
、15
°
、10
°
、9
°
、8
°
、7
°
、6
°
、5
°
、4
°
、3
°
、2
°
、1
°
、0.1
°
、0.01
°
或更小。在一些情况下,宽度w可以在约100微米(μm)至约500μm的范围之间。在一些情况下,宽度w可以在约10μm至约200μm的范围之间。可替代地,宽度可以小于约10μm。可替代地,宽度可以大于约500μm。在一些情况下,进入接点406的水性流体408的流速可以在约0.04微升(μl)/分钟(min)至约40μl/min之间。在一些情况下,进入接点406的水性流体408的流速可以在约0.01微升(μl)/分钟(min)至约100μl/min之间。可替代地,进入接点406的水性流体408的流速可以小于约0.01μl/min。可替代地,进入接点406的水性流体408的流速可以大于约40μl/min,例如45μl/min、50μl/min、55μl/min、60μl/min、65μl/min、70μl/min、75μl/min、80μl/min、85μl/min、90μl/min、95μl/min、100μl/min、110μl/min、120μl/min、130μl/min、140μl/min、150μl/min或更高。在更低的流速下,例如大约小于或等于10微升/分钟的流速下,液滴半径可以不依赖于进入接点406的水性流体408的流速。
[0185]
在一些情况下,生成的至少约50%的液滴可以具有均一大小。在一些情况下,生成的至少约55%、60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或更多的液滴可以具有均一大小。可替代地,生成的少于约50%的液滴可以具有均一大小。
[0186]
可以通过增加生成点,例如增加水性流体408通道区段(例如,通道区段402)与储槽404之间的接点(例如,接点406)的数量来增加液滴生成的通过量。可替代地或另外,可以通过增加通道区段402中的水性流体408的流速来增加液滴生成的通过量。
[0187]
图5示出了用于增加液滴生成通过量的微流体通道结构的一个实例。微流体通道结构500可以包括多个通道区段502和一个储槽504。所述多个通道区段502中的每一个均可与储槽504流体连通。通道结构500可以在所述多个通道区段502与储槽504之间包括多个通道接点506。每个通道接点都可以是液滴生成点。图4中来自通道结构400的通道区段402以及对其部件的任何描述可对应于通道结构500中的所述多个通道区段502中的给定通道区段以及对其相应部件的任何描述。来自通道结构400的储槽404以及对其部件的任何描述可对应于来自通道结构500的储槽504以及对其相应部件的任何描述。
[0188]
所述多个通道区段502中的每个通道区段均可以包括含有悬浮珠粒512的水性流体508。储槽504可以包括与水性流体508不可混溶的第二流体510。在一些情况下,第二流体510可以不经受和/或不被引导流入和流出储槽504。例如,第二流体510在储槽504中可以是基本上静止的。在一些情况下,第二流体510可以经受在储槽504内流动,但不会流入和流出储槽504,例如通过向储槽504施加压力和/或受到接点处的水性流体508的来流影响时。可替代地,第二流体510可以经受和/或被引导流入或流出储槽504。例如,储槽504可以是将第二流体510从上游引导至下游,从而转运生成的液滴的通道。
[0189]
在操作时,包括悬浮珠粒512的水性流体508可以沿所述多个通道区段502转运到所述多个接点506处,以与储槽504中的第二流体510会合以产生液滴516、518。可以从每个通道区段,在与储槽504的每个相应接点处形成液滴。在水性流体508和第二流体510会合的接点处,可以基于例如接点处的流体动力、两股流体508、510的流速、流体特性以及如本文
其他地方所述的通道结构500的某些几何参数(例如,w、h0、α等)的因素而形成液滴。可以通过将水性流体508从所述多个通道区段502连续注射通过所述多个接点506而将多个液滴收集在储槽504中。用通道结构500的平行通道构造,通过量可以显著增加。例如,具有五个包含水性流体508的入口通道区段的通道结构生成液滴的频率可以是具有一个入口通道区段的通道结构的五倍,条件是通道区段中的流体流速基本上相同。不同入口通道区段中的流体流速可以基本上相同或者可以基本上不相同。通道结构可以具有与实际和储槽大小所允许的一样多的平行通道区段。例如,通道结构可以具有至少约2、3、4、5、6、7、8、9、10、20、30、40、50、60、70、80、90、100、150、500、250、300、350、400、450、500、600、700、800、900、1000、1500、5000个或更多个平行的或基本上平行的通道区段。
[0190]
几何参数w、h0和α,对于所述多个通道区段502中的每个通道区段来说可以是均一的或者可以不是均一的。例如,每个通道区段在其各自与储槽504的通道接点处或附近,可以具有相同或不同的宽度。例如,每个通道区段在其各自与储槽504的通道接点处或附近,可以具有相同或不同的高度。在另一个实例中,储槽504在与所述多个通道区段502的不同通道接点处可以具有相同或不同的扩展角。当几何参数均一时,有益地,即使通过量增加,也可以将液滴大小控制为均一的。在一些情况下,当期望具有不同的液滴大小分布时,所述多个通道区段502的几何参数可相应地变化。
[0191]
在一些情况下,生成的至少约50%的液滴可以具有均一大小。在一些情况下,生成的至少约55%、60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或更多的液滴可以具有均一大小。可替代地,生成的少于约50%的液滴可以具有均一大小。
[0192]
图6示出了用于增加液滴生成通过量的微流体通道结构的另一实例。微流体通道结构600可以包括多个通道区段602,其大致呈圆形排列在储槽604的外周。所述多个通道区段602中的每一个均可与储槽604流体连通。通道结构600可以在所述多个通道区段602与储槽604之间包括多个通道接点606。每个通道接点都可以是液滴生成点。图2中来自通道结构400的通道区段402以及对其部件的任何描述可对应于通道结构600中的所述多个通道区段602中的给定通道区段以及对其相应部件的任何描述。来自通道结构400的储槽404以及对其部件的任何描述可对应于来自通道结构600的储槽604以及对其相应部件的任何描述。
[0193]
所述多个通道区段602中的每个通道区段均可以包括含有悬浮珠粒612的水性流体608。储槽604可以包括与水性流体608不可混溶的第二流体610。在一些情况下,第二流体610可以不经受和/或不被引导流入和流出储槽604。例如,第二流体610在储槽604中可以是基本上静止的。在一些情况下,第二流体610可以经受在储槽604内流动,但不会流入和流出储槽604,例如通过向储槽604施加压力和/或受到接点处的水性流体608的来流影响时。可替代地,第二流体610可以经受和/或被引导流入或流出储槽604。例如,储槽604可以是将第二流体610从上游引导至下游,从而转运生成的液滴的通道。
[0194]
在操作时,包括悬浮珠粒612的水性流体608可以沿所述多个通道区段602转运到所述多个接点606处,以与储槽604中的第二流体610会合以产生多个液滴616。可以从每个通道区段,在与储槽604的每个相应接点处形成液滴。在水性流体608和第二流体610会合的接点处,可以基于例如接点处的流体动力、两股流体608、610的流速、流体特性以及如本文其他地方所述的通道结构600的某些几何参数(例如,通道区段602的宽度和高度,储槽604的扩展角等)的因素而形成液滴。可以通过将水性流体608从所述多个通道区段602连续注
射通过所述多个接点606而将多个液滴收集在储槽604中。用通道结构600基本上平行的通道构造,通过量可以显著增加。通道结构可以具有与实际和储槽大小所允许的一样多的基本上平行的通道区段。例如,通道结构可以具有至少约2、3、4、5、6、7、8、9、10、20、30、40、50、60、70、80、90、100、150、200、250、300、350、400、450、500、600、700、800、900、1000、1500、5000个或更多个平行的或基本上平行的通道区段。所述多个通道区段可以例如围绕储槽的边缘或外周基本上均匀地间隔开。可替代地,所述多个通道区段的间隔可以是不均匀的。
[0195]
储槽604可以在每个通道接点处或附近具有扩展角α(在图6中未示出)。所述多个通道区段602中的每个通道区段都可以在通道接点处或附近具有宽度w和高度h0。几何参数w、h0和α,对于所述多个通道区段602中的每个通道区段来说可以是均一的或者可以不是均一的。例如,每个通道区段在其各自与储槽604的通道接点处或附近,可以具有相同或不同的宽度。例如,每个通道区段在其各自与储槽604的通道接点处或附近,可以具有相同或不同的高度。
[0196]
储槽604在与所述多个通道区段602的不同通道接点处可以具有相同或不同的扩展角。例如,圆形储槽(如图6中所示)可以具有圆锥形、圆顶状或半球形顶板(例如,顶壁)以便在所述多个通道连接子606处或附近为每个通道区段602提供相同或基本上相同的扩展角。当几何参数均一时,有益地,即使通过量增加,也可以将所得液滴大小控制为均一的。在一些情况下,当期望具有不同的液滴大小分布时,所述多个通道区段602的几何参数可相应地变化。
[0197]
在一些情况下,生成的至少约50%的液滴可以具有均一大小。在一些情况下,生成的至少约55%、60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或更多的液滴可以具有均一大小。可替代地,生成的少于约50%的液滴可以具有均一大小。注入液滴中的珠粒和/或生物颗粒可以具有或可以不具有均一大小。
[0198]
图7a示出了具有用于进行受控分配的几何特征的微流体通道结构的另一实例的横截面视图。通道结构700可以包括在通道接点706(或交叉点)处与储槽704连通的通道区段702。在一些情况下,通道结构700及其部件中的一个或多个与通道结构100及其部件中的一个或多个相对应。图7b示出了图7a的通道结构700的透视图。
[0199]
包括多个颗粒716的水性流体712可以沿通道区段702转运到接点706处以会合与储槽704中水性流体712不混溶的第二流体714(例如,油等),以产生流入储槽704的水性流体712的液滴720。在水性流体712和第二流体714相遇的接点706处,可以基于例如接点706处的流体动力、两股流体712、714的流动速率、流体特性以及通道结构700的某些几何参数(例如,δh等)的因素而形成液滴。可以通过将水性流体712从通道区段702连续注射通过接点706而将多个液滴收集在储槽704中。
[0200]
生成的离散液滴可以包含所述多个颗粒716中的一个或多个颗粒。如本文其他地方所述,颗粒可以是任何颗粒,例如珠粒、细胞珠粒、凝胶珠粒、生物颗粒的大分子成分或其他颗粒。可替代地,生成的离散液滴可以不包括任何珠粒。
[0201]
在一些情况下,水性流体712可以具有浓度或频率基本上均一的颗粒716。如本文其他地方所述(例如,参考图4),可以从单独的通道(图7中未示出)将颗粒716(例如,珠粒)引入到通道区段702中。可以通过控制将颗粒716引入到通道区段702中的频率和/或通道区段702和单独的通道中流体的相对流速来控制通道区段702中的颗粒716的频率。在一些情
况下,可以从多个不同的通道将颗粒716引入到通道区段702中,并因此而控制频率。在一些情况下,不同颗粒经由单独的通道引入。例如,第一单独通道可以将珠粒引入到通道区段702中并且第二单独通道可以将生物颗粒生物颗粒引入到其中。引入珠粒的第一单独通道可以在引入生物颗粒的第二单独通道的上游或下游。
[0202]
在一些情况下,第二流体714可以不经受和/或不被引导流入和流出储槽704。例如,第二流体714在储槽704中可以是基本上静止的。在一些情况下,第二流体714可以经受在储槽704内流动,但不会流入和流出储槽704,例如通过向储槽704施加压力和/或受到接点706处的水性流体712的来流影响时。可替代地,第二流体714可以经受和/或被引导流入或流出储槽704。例如,储槽704可以是将第二流体714从上游引导至下游,从而转运生成的液滴的通道。
[0203]
在接点706处或附近的通道结构700可以具有至少部分地决定了由通道结构700形成的液滴大小和/或形状的某些几何特征。通道区段702可以具有第一横截面高度h1,储槽704可以具有第二横截面高度h2。第一横截面高度h1和第二横截面高度h2可以不同,使得在接点706处,存在高度差δh。第二横截面高度h2可以大于第一横截面高度h1。在一些情况下,之后储槽可以逐渐增加横截面高度,例如离接点706越远。在一些情况下,在接点706处,储槽的横截面高度可以根据扩展角β而增大。高度差δh和/或扩展角β可以使舌部(在液滴形成之前,水性流体712从接点706处离开通道区段702并且进入储槽704的部分)长度增加并且促进中间形成的液滴的曲率减小。例如,液滴大小可以随高度差增大和/或扩展角增大而减小。
[0204]
高度差δh可为至少约1μm。可替代地,高度差可为至少约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、60、70、80、90、100、200、300、400、500μm或更大。可替代地,高度差可为至多约500、400、300、200、100、90、80、70、60、50、45、40、35、30、25、20、19、18、17、16、15、14、13、12、11、10、9、8、7、6、5、4、3、2、1μm或更小。在一些情况下,扩展角β可以在约0.5
°
至约4
°
、约0.1
°
至约10
°
或约0
°
至约90
°
的范围之间。例如,扩展角可以为至少约0.01
°
、0.1
°
、0.2
°
、0.3
°
、0.4
°
、0.5
°
、0.6
°
、0.7
°
、0.8
°
、0.9
°
、1
°
、2
°
、3
°
、4
°
、5
°
、6
°
、7
°
、8
°
、9
°
、10
°
、15
°
、20
°
、25
°
、30
°
、35
°
、40
°
、45
°
、50
°
、55
°
、60
°
、65
°
、70
°
、75
°
、80
°
、85
°
或更大。在一些情况下,扩展角可以为至多约89
°
、88
°
、87
°
、86
°
、85
°
、84
°
、83
°
、82
°
、81
°
、80
°
、75
°
、70
°
、65
°
、60
°
、55
°
、50
°
、45
°
、40
°
、35
°
、30
°
、25
°
、20
°
、15
°
、10
°
、9
°
、8
°
、7
°
、6
°
、5
°
、4
°
、3
°
、2
°
、1
°
、0.1
°
、0.01
°
或更小。
[0205]
在一些情况下,进入接点706的水性流体712的流速可以在约0.04微升(μl)/分钟(min)至约40μl/min之间。在一些情况下,进入接点706的水性流体712的流速可以在约0.01微升(μl)/分钟(min)至约100μl/min之间。可替代地,进入接点706的水性流体712的流速可以小于约0.01μl/min。可替代地,进入接点706的水性流体712的流速可以大于约40μl/min,例如45μl/min、50μl/min、55μl/min、60μl/min、65μl/min、70μl/min、75μl/min、80μl/min、85μl/min、90μl/min、95μl/min、100μl/min、110μl/min、120μl/min、130μl/min、140μl/min、150μl/min或更高。在更低的流速下,例如大约小于或等于10微升/分钟的流速下,液滴半径可以不依赖于进入接点706的水性流体712的流速。第二流体714在储槽704中可以是基本上静止的。可替代地,第二流体714可以是流动的,例如以上文针对水性流动712描述的流速流动。
[0206]
在一些情况下,生成的至少约50%的液滴可以具有均一大小。在一些情况下,生成的至少约55%、60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或更多的液滴可以具有均一大小。可替代地,生成的少于约50%的液滴可以具有均一大小。
[0207]
虽然图7a和7b说明了在接点706处突变(例如,阶跃增加)的高度差δh,但是高度差也可以逐渐增加(例如,从约0μm到最大高度差)。可替代地,高度差可以从最大高度差逐渐减小(例如,渐缩)。如本文所用,高度差的逐渐增加或减小可指高度差的连续递增或递减,其中高度轮廓的任何一个差异区段与高度轮廓的紧邻差异区段之间的角度大于90
°
。例如,在接点706处,通道的底壁和储槽的底壁可以呈大于90
°
的角度会合。可替代地或另外,通道的顶壁(例如,顶板)和储槽的顶壁(例如,顶板)可以呈大于90
°
的角度会合。逐渐增加或减小可以是线性的或非线性的(例如,指数的、正弦的等)。可替代地或另外,高度差可以线性地或非线性地可变地增加和/或减小。虽然图7a和7b说明了为线性的扩展储槽横截面高度(例如,恒定的扩展角β),但是横截面高度可以非线性地扩展。例如,储槽可以至少部分地由具有可变扩展角的圆顶状(例如,半球形)形状限定。横截面高度可以以任何形状扩展。
[0208]
例如,如上所述或本文其他地方所述的通道网络可与适当的流体部件流体联接。例如,入口通道区段与它们要输送到通道连接子的适当材料来源流体联接。这些来源可以包括各种不同的流体部件中的任何一种,从限定在微流体装置的主体结构中或连接到微流体装置的主体结构的简单储槽到从装置外来源、歧管、流体流动单元(例如,致动器、泵、压缩机)等输送流体的流体导管。同样,出口通道区段(例如,通道区段208、储槽604等)可以与用于已分配的细胞的接收容器或导管流体联接以进行后续处理。同样,这可以是限定在微流体装置的主体中的储槽,或者它可以是用于将已分配的细胞输送至后续的操作、仪器或部件的流体导管。
[0209]
本文所述的方法和系统可用于大大增加细胞应用和/或接收基于液滴的输入的应用的效率。例如,在分选已占用的细胞和/或适当大小的细胞之后,可以进行的后续操作可以包括产生扩增产物、纯化(例如,通过固相可逆固定(spri))、进一步处理(例如,剪切、连接功能序列及后续扩增(例如,通过pcr))。这些操作可以在本体中(例如,在分区外)进行。在分区是乳液中的液滴的情况下,可以破坏乳液,并且合并液滴的内容物用于另外的操作。可以与带条形码化珠粒一起共同分配的其他试剂可以包括阻断核糖体rna(rrna)的寡核苷酸和消化来自细胞的基因组dna的核酸酶。可替代地,rrna去除剂可应用于另外的处理操作中。通过此类方法产生的构建体的构型可以帮助最小化(或避免)对测序期间的聚t序列和/或多核苷酸序列的5’末端的测序。可以对扩增产物,例如第一扩增产物和/或第二扩增产物进行测序以进行序列分析。在一些情况下,可以使用测序用部分发夹扩增(phase)方法进行扩增。
[0210]
多种应用需要评估生物颗粒群体内不同生物颗粒或生物体类型的存在和定量,包括例如微生物组分析和表征、环境测试、食品安全测试、流行病学分析(例如,在跟踪污染中)等。
[0211]
条形码交换
[0212]
在一些实施方案中,本文公开了用于核酸处理的方法,所述方法包括:(a)在多个分区中,使用来自多个核酸条形码分子的核酸条形码分子和多个核酸分子(例如,源自细胞)来生成多个条形码化核酸分子;(b)从所述多个分区回收所述多个条形码化核酸分子,
以产生包含所述多个核酸条形码分子和所述多个核酸条形码分子的剩余部分的混合物;(c)在(b)之后,使所述混合物经受足以将阻断寡核苷酸偶联至所述多个核酸条形码分子的所述剩余部分的条件,其中所述阻断寡核苷酸包含:(i)互补区,所述互补区包含与所述多个核酸条形码分子的所述剩余部分中的序列至少75%互补的序列;和(ii)3’阻断基。
[0213]
在一些实施方案中,本文所公开的用于核酸处理的方法包括单细胞的利用高通量测序的转座酶可接近性染色质测定(atac
‑
seq)。用于单细胞atac
‑
seq的示例性方法可见于例如美国专利公开号20180340169中,所述专利整体以引用方式并入本文。
[0214]
在atac
‑
seq方法中,使用加载有含转座子末端序列的核酸分子的转座酶分子(例如,tn5转座酶)的转座酶核酸复合物对来自细胞或细胞核的含基因组dna的染色质进行标记和片段化(标记片段化的,也称为标记片段化(tagmentation))。在一些情况下,含转座子末端序列的核酸分子还包含衔接子序列(例如,测序引物序列,例如illumina r1或r2测序引物序列)。参见,例如,图10a。标记的核酸分子(例如,染色质中的基因组dna)也可包含转座子末端序列(例如,图11中的1105)。在一些实施方案中,衔接子序列用作用于基于扩增或连接的条形码化方案的杂交位点,以将条形码序列附接至衔接子侧接的模板核酸片段(参见,例如,美国专利公开号20180340169,所述专利整体以引用方式并入本文)。在一些情况下,含条形码的寡核苷酸分子包含另外的功能序列(例如,illumina p5或p7序列或其互补序列)。在标记片段化之后,可对衔接子侧接的核酸分子进行缺口填充反应(例如,图11中的过程1170)以促进后续处理步骤(例如,图11中的基于线性扩增的条形码化方案1180,且如本文进一步所述)。核酸反应,例如线性扩增,可重复一次或多次,如图11的过程1190中所例示的。在一些情况下,缺口填充反应1170在分区中发生。缺口填充反应1170也可在分区外(例如,在本体中)发生。
[0215]
在一些实施方案中,基于线性扩增的条形码缀合用于条形码标记片段化的衔接子侧接的模板dna(参见,例如,图10b)。在一些实施方案中,基于线性扩增的条形码缀合方案包括分区内条形码附接以及在本体中进行的其他处理步骤(参见,例如,图11)。在一些情况下,线性扩增在分区(例如,液滴乳液)中发生。在一些实例中,线性扩增在分区中发生,其中核酸条形码分子偶联至固相支持体。在一些情况下,固相支持体是珠粒。在一些实施方案中,固相支持体是凝胶珠粒。在一些情况下,核酸条形码分子可释放地附接至固相支持体。在一些实施方案中,固相支持体是玻璃或石英表面。在一些实施方案中,固相支持体可形成分区或孔。核酸条形码分子可包含衔接子序列(例如,illumina p5序列,例如1110)、条形码序列(例如,1120)和引物序列(例如,测序引物序列1130和1130b,例如illumina r1或r2测序引物序列或与r1或r2序列互补的序列)。另外或可替代地,条形码分子可包含功能序列,例如间隔子序列、唯一分子标识符、结合序列、限制位点等的任何组合或变型。在一些实施方案中,通过将核酸条形码分子与衔接子侧接的模板核酸片段上的互补区(例如,r1衔接子序列)退火来生成条形码化的衔接子侧接的模板核酸片段,将所述模板核酸片段使用聚合酶在线性扩增(例如,1180和1190)反应中扩增,如图11所示。
[0216]
在一些实施方案中,基于连接的条形码缀合用于对标记片段化的核酸分子,例如标记片段化的衔接子侧接的模板dna进行条形码化(参见,例如,图10b、图17和美国专利公开号20180340169(其以引用方式整体并入本文))。可以是部分双链核酸条形码分子(例如,1701)可包含衔接子序列(例如,引物退火序列或功能序列,例如1110、1210、1310、1710和
1810所示的illumina p5序列)、条形码序列(例如,1120、1320、1720、1820)和引物序列(例如,测序引物序列,例如illumina r1或r2测序引物序列或与r1或r2序列互补的序列,例如1130、1230、1330和1730)。标记片段化的核酸分子还可包含转座子末端序列(例如,1705)或其互补序列。另外或替代地,核酸条形码分子(例如,1701)可包含功能序列,例如间隔子序列、唯一分子标识符、结合序列、限制位点等或其互补序列的任何组合或变型。核酸条形码分子1701可以与标记片段化的衔接子侧接的模板dna 1707缔合(例如,通过杂交)。在一些情况下,核酸条形码分子1701上的一个或多个序列(例如,1730)可以是突出序列(例如5’突出端),并且可以与标记片段化的衔接子侧接的模板dna上的一个或多个序列互补且能够与所述一个或多个序列退火。在一些情况下,标记片段化的衔接子侧接的模板dna可以在例如过程1750中用酶(例如,t4多核苷酸激酶)处理,以使5’末端磷酸化。然后可使用酶(例如,连接酶(例如t4 dna连接酶))将核酸条形码分子1701连接至标记片段化的衔接子侧接的模板dna,以生成条形码化核酸分子,例如条形码化的衔接子侧接的模板核酸片段。在一些实例中,核酸条形码分子偶联至固相支持体。在一些情况下,固相支持体是珠粒。在一些实施方案中,固相支持体是如本文其他地方所述的凝胶珠粒。在一些情况下,核酸条形码分子可释放地附接至固相支持体。
[0217]
在一些实施方案中,在条形码化反应之后,将条形码化的衔接子侧接的模板核酸片段从分区中取出(例如,将液滴乳液破碎或破坏),在一些情况下进行纯化,并在本体中合并在一起以用于样品标志聚合酶链式反应(si
‑
pcr,例如1195、1795),例如图11、图17所示。在一些情况下,使条形码化的衔接子侧接的模板核酸片段经受足以进行缺口填充的条件(例如,过程1770)。缺口填充可例如使用酶,例如聚合酶和/或连接酶发生。在一些情况下,si
‑
pcr(例如1195、1795)包括一个或多个pcr反应,用于将另外的序列(例如,p7或样品标志序列(例如,i7))添加至条形码化的衔接子侧接的核酸片段,准备这些片段以进行高通量测序(例如,illumina测序)。在一些情况下,可将线性扩增过程中未掺入的过量核酸条形码分子从分区转移到本体si
‑
pcr反应中。在这些情况下,在本体si
‑
pcr过程中,过量的条形码分子可引发模板核酸片段,导致pcr产物含有与亲本模板分子不同的条形码序列(此过程称为“条形码交换”或“条形码交换反应”)。
[0218]
条形码交换反应的代表性实例示于图12a中。将条形码化的衔接子侧接的模板核酸分子1202从分区中取出并在本体si
‑
pcr反应中合并后,本体混合物包含条形码化片段,每个条形码化片段均具有特定的条形码序列,所述条形码序列指示并关联条形码化片段由单细胞产生。如图12a示出了包括条形码序列1220a的代表性的条形码化的衔接子侧接的模板核酸分子1202。衔接子侧接的模板核酸分子1202还可包含衔接子序列1210(例如,p5序列)、测序引物序列1230和1230b(例如,r1或r2序列)和/或转座子末端序列1205,或其任何互补序列。分区中(例如图11中所示的线性扩增引物)遗留过量核酸条形码分子1201b(其可能包含不同的条形码序列1220b),可能导致si
‑
pcr过程中发生不期望的引发和扩增,进而导致条形码交换。例如,图12a示出了包含条形码序列1220b的示例性遗留核酸条形码分子。在si
‑
pcr期间,包含条形码序列1220b的此条形码分子1201b可杂交并扩增含1220a的片段以产生含1220b的模板核酸分子,从而将1220a条形码序列交换为1220b条形码序列。因为1220a条形码指示特定的单细胞,所以交换的条形码会造成浪费和不准确的数据,从而干扰有效单细胞分析。
[0219]
条形码交换反应的示例性机制示于图12b中。将条形码化的衔接子侧接的模板核酸分子从分区中取出并在本体si
‑
pcr反应中合并后,可扩增任何剩余的未结合核酸条形码分子(例如1201b)。在一些情况下,核酸条形码分子1201b可以是部分双链的并且可进行缺口填充反应1270(例如,在扩增1280(例如,线性扩增或si
‑
pcr)之前,使用酶[例如,聚合酶]利用底部链中的r1序列作为模板来延伸核酸条形码分子1201b的顶部链的3’末端)。核酸条形码分子1201b还可包含衔接子序列1210(例如p5序列,衔接子序列可与例如1110、1310、1410和1810基本上类似),以及测序引物序列1230(其可与例如1130、1330、1430和1830或其互补序列基本上类似)。在扩增反应1280(例如线性扩增或si
‑
pcr)期间,核酸条形码分子1201b中的一部分(例如,其中一条链)可能参与条形码交换反应。例如,如图12a所示,包含条形码序列1220b的条形码分子1201b可(例如,经由衔接子序列1230的序列互补性)与包含条形码序列1220a的衔接子侧接的模板核酸分子1202杂交。然后,扩增反应可导致将1220a条形码序列交换为1220b条形码序列。另外,可扩增核酸条形码分子1201b的一部分(例如,其中一条链),从而产生额外的双链核酸条形码分子。如本文所述,在核酸扩增期间,这些额外的核酸条形码分子也可能参与条形码交换反应,并造成浪费和不准确的数据。
[0220]
在一些实施方案中,可通过在二乙氨基乙基纤维素(deae)膜上经由尺寸依赖性纯化去除过量的条形码化引物来防止或减少条形码交换。在一些实施方案中,可通过使用固相可逆固定化(spri)去除过量的条形码化引物来防止或减少条形码交换。然而,在一些情况下,在文库扩增之前执行的此类纯化步骤可能导致测序文库中唯一分子丢失,从而降低文库复杂性。
[0221]
在一些实施方案中,本公开提供了用于最小化条形码交换的方法。在一些实施方案中,本公开提供了使用含有不能被聚合酶延伸的3’端化学阻断物的寡核苷酸来最小化条形码交换的方法。
[0222]
用于最小化条形码交换的发夹帽分子
[0223]
在一些实施方案中,本文公开了用于核酸处理的方法,所述方法包括:(a)在多个分区中,使用来自多个核酸条形码分子的核酸条形码分子和多个核酸分子来生成多个条形码化核酸分子;(b)从所述多个分区回收所述多个条形码化核酸分子,以产生包含所述多个核酸条形码分子和所述多个核酸条形码分子的剩余部分的混合物;(c)在(b)之后,使所述混合物经受足以将阻断寡核苷酸偶联至所述多个核酸条形码分子的所述剩余部分的条件,其中所述阻断寡核苷酸包含:(i)互补区,所述互补区包含与所述多个核酸条形码分子的所述剩余部分中的序列至少75%互补的序列;和(ii)3’阻断基。
[0224]
在一些实例中,所述多个分区是多个液滴。在一些实例中,所述多个分区是多个孔。
[0225]
在一些实施方案中,本公开的阻断寡核苷酸从5’到3’包含第一茎序列、环序列、与第一茎序列至少75%互补的第二茎序列以及与核酸条形码分子的剩余部分中的序列至少75%互补的序列。在一些实施方案中,第二茎序列与第一茎序列75%、76%、77%、78%、79%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%互补。在一些实施方案中,第二茎序列包含与第一茎序列75%、76%、77%、78%、79%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%互补的区域。
例如,在一些情况下,第一茎序列包含(1)与第二茎序列至少75%互补的一个或多个区域,和(2)与第二茎序列不互补的一个或多个内部环。在一些实施方案中,第二茎序列包含(1)与第一茎序列至少75%互补的一个或多个区域,和(2)与第一茎序列不互补的一个或多个内部环。在一些实施方案中,阻断寡核苷酸包含与所述多个核酸条形码分子的剩余部分中的序列75%、76%、77%、78%、79%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%互补的序列。
[0226]
图13a示出了代表性的剩余(即,自分区遗留)核酸条形码分子1301,其中1310代表衔接子序列(例如,p5序列),1320代表条形码序列,并且1330代表引物序列(例如,r1测序引物序列)。图13b示出了代表性的阻断寡核苷酸1302,其中1340代表5’磷酸基,1350代表第一茎序列,1360代表环序列,1370代表与第一茎序列互补的第二茎序列,1380代表与核酸条形码分子的剩余部分中的序列(1330)互补的序列,并且1390代表防止经聚合酶延伸和/或连接的3’阻断基。图13c示出了代表性的加帽条形码分子1303,其中阻断寡核苷酸1302已经连接至剩余的核酸条形码分子1301。为了有助于连接过程,阻断寡核苷酸序列1380与互补序列1330杂交,而3’阻断基1390则防止加帽条形码分子1303参与条形码交换反应。
[0227]
阻断寡核苷酸的第一茎序列和/或第二茎序列的序列和长度可改变,其中所述序列保持其互补区并与其自身形成发夹结构。在一些实施方案中,阻断寡核苷酸由于其发夹结构而被称为发夹帽,因此在本文中使用时,阻断寡核苷酸和发夹帽可互换使用。在一些情况下,阻断寡核苷酸不形成发夹结构。在一些情况下,阻断寡核苷酸与另一寡核苷酸二聚,其中该二聚体有效地阻止遗留的条形码分子在si
‑
pcr期间用于条形码交换。
[0228]
在一些实施方案中,阻断寡核苷酸的环的序列可改变。在一些情况下,阻断寡核苷酸的环的大小可增加。在一些情况下,阻断寡核苷酸的环的大小可减小。在一些实施方案中,亲和柄附接至阻断寡核苷酸(例如,在环序列中),其中亲和柄用于纯化阻断寡核苷酸和/或连接的加发夹帽的条形码分子。在一些情况下,亲和柄是生物素基团,但是可包含任何合适的亲和柄以促进阻断寡核苷酸或其衍生物的纯化。
[0229]
在一些实施方案中,3’阻断基被配置成防止剩余部分与核酸分子连接。在一些情况下,3’阻断基被配置成当与靶核酸分子杂交时防止引物序列延伸。在一些实施方案中,3’阻断基在阻断寡核苷酸的3’端。在一些实施方案中,3’阻断基是2
’‑3’‑
二脱氧胞嘧啶(ddc)。在一些实施方案中,3’阻断基是2
’‑5’
连接的核苷。在一些实施方案中,3’阻断基是3’c3间隔子。在一些实施方案中,3’阻断基是氨基修饰的c6。在一些实施方案中,3’阻断基是反向脱氧胸苷(dt)。在一些实施方案中,3’阻断基是3’氨基修饰的核苷酸。在一些实施方案中,3’阻断基是3’磷酸基。在一些实施方案中,3’阻断基是2
’‑5’
连接的核苷,其中2
’‑5’
连接的核苷是3
’‑
脱氧胸苷(3
’‑
dt)。在一些情况下,2
’‑5’
连接的核苷是3
’‑
脱氧胞苷(3
’‑
dc)。在一些情况下,2
’‑5’
连接的核苷是3
’‑
脱氧腺苷(3
’‑
da)。在一些情况下,2
’‑5’
连接的核苷是3
’‑
脱氧鸟苷(3
’‑
dg)。
[0230]
在一些实施方案中,本文公开了组合物,所述组合物从5’到3’包含:(a)第一区域,所述第一区域包含条形码序列和引物序列;以及(b)第二区域,所述第二区域包含(i)与引物序列互补的序列;和(ii)3’阻断基。代表性的组合物示于图13b中。在一些实施方案中,与引物序列互补的序列与引物序列75%、76%、77%、78%、79%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、
99%、100%互补。
[0231]
在一些实施方案中,本文所公开的组合物的3’阻断基在阻断寡核苷酸的3’端。在一些实施方案中,本文所公开的组合物的3’阻断基是2
’‑3’‑
二脱氧胞嘧啶(ddc)。在一些实施方案中,本文所公开的组合物的3’阻断基是2
’‑5’
连接的核苷。在一些实施方案中,本文所公开的组合物的3’阻断基是3’c3间隔子。在一些实施方案中,本文所公开的组合物的3’阻断基是氨基修饰的c6。在一些实施方案中,本文所公开的组合物的3’阻断基是反向脱氧胸苷(dt)。在一些实施方案中,本文所公开的组合物的3’阻断基是3’氨基修饰的核苷酸。在一些实施方案中,本文所公开的组合物的3’阻断基是3’磷酸基。在一些实施方案中,本文所公开的组合物的3’阻断基是2
’‑5’
连接的核苷,其中2
’‑5’
连接的核苷是3
’‑
脱氧胸苷(3
’‑
dt)。在一些情况下,本文所公开的组合物的2
’‑5’
连接的核苷是3
’‑
脱氧胞苷(3
’‑
dc)。在一些情况下,本文所公开的组合物的2
’‑5’
连接的核苷是3
’‑
脱氧腺苷(3
’‑
da)。在一些情况下,本文所公开的组合物的2
’‑5’
连接的核苷是3
’‑
脱氧鸟苷(3
’‑
dg)。
[0232]
在一些实施方案中,本公开的组合物的第二区域从5’到3’包含:第一茎序列,环序列,与第一茎序列至少75%互补的第二茎序列,与引物序列互补的序列,和3’阻断基(图13b)。在一些实施方案中,本文所公开的组合物的第二茎序列与第一茎序列75%、76%、77%、78%、79%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%、100%互补。
[0233]
本文所公开的阻断寡核苷酸也可用于防止多种基于核酸的反应中的不想要的相互作用。例如,本文所公开的阻断寡核苷酸可用于阻止,抑制或以其他方式改变pcr反应的速率(例如,在以下情况下:(1)纯化步骤无法执行或不理想,或(2)为了最小化样品中由一种或多种特异性引物或引物组引发的pcr反应)。
[0234]
使用rnase最小化条形码交换
[0235]
在一些实施方案中,本文公开了用于核酸处理的方法,所述方法包括:(a)提供反应混合物,所述反应混合物包含:(i)模板核酸分子;(ii)rnase酶;和(iii)多个核酸条形码分子,其中所述多个核酸条形码分子中的每个核酸条形码分子包含:(a)共同条形码序列;(b)能够与靶核酸杂交的序列;(c)至少一个核糖核苷酸;和(d)3’阻断基;(b)使所述反应混合物经受足以使所述模板核酸分子与所述多个核酸条形码分子中的核酸条形码分子杂交的条件;(c)使所述反应混合物经受足以使所述rnase酶降解所述核糖核苷酸从而释放所述3’阻断基的条件;以及(d)使用所述模板核酸分子和所述核酸条形码分子来生成条形码化模板核酸分子(图14a至图14c)。
[0236]
在一些实施方案中,3’阻断基被配置成防止剩余部分与核酸分子连接。在一些情况下,3’阻断基被配置成当与靶核酸分子杂交时防止引物序列延伸。在一些情况下,条形码序列在至少一个核糖核苷酸和3’阻断基的5’,且不是从核酸条形码分子中释放出来的。
[0237]
在一些实施方案中,3’阻断基在所述多个核酸条形码分子的3’端。在一些情况下,3’阻断基是2
’‑3’‑
二脱氧胞嘧啶(ddc)。在一些情况下,3’阻断基是2
’‑5’
连接的核苷。在一些情况下,3’阻断基是3’c3间隔子。在一些情况下,3’阻断基是氨基修饰的c6,即反向脱氧胸苷(dt)。在一些情况下,3’阻断基是3’氨基修饰的核苷酸。在一些情况下,3’阻断基是3’磷酸基。在一些情况下,3’阻断基是2
’‑5’
连接的核苷,其中2
’‑5’
连接的核苷是3
’‑
脱氧胸苷(3
’‑
dt)。在一些实施方案中,2
’‑5’
连接的核苷是3
’‑
脱氧胞苷(3
’‑
dc)。在一些实施方案
中,2
’‑5’
连接的核苷是3
’‑
脱氧腺苷(3
’‑
da)。在一些实施方案中,2
’‑5’
连接的核苷是3
’‑
脱氧鸟苷(3
’‑
dg)。在一些实施方案中,3’阻断基不能通过聚合酶延伸。
[0238]
在一些实施方案中,本公开的方法还包括将反应混合物共同分配到分区中。在一些情况下,分区是孔。在一些情况下,分区是乳液中的水性液滴。
[0239]
在一些实施方案中,所述多个核酸条形码分子附接至固相支持体。在一些情况下,固相支持体是珠粒。在一些情况下,所述多个核酸条形码分子可释放地附接至珠粒。在一些情况下,珠粒是凝胶珠粒。在一些实例中,珠粒是凝胶珠粒。在一些实施方案中,凝胶珠粒是可降解凝胶珠粒。在一些情况下,可降解凝胶珠可通过化学刺激来降解。在一些实施方案中,化学刺激是还原剂。在一些实施方案中,反应混合物包含还原剂。
[0240]
在一些实施方案中,将附接至固相支持体(例如,珠粒或凝胶珠粒)的多个核酸条形码分子修饰为含有核糖核苷酸。在一些情况下,核糖核苷酸是3’阻断基上游大约4至8个核苷酸。在一些实施方案中,核糖核苷酸是3’阻断基上游大约4、5、6、7、8或更多个核苷酸。含有3’阻断基的示例性的含核糖核苷酸的条形码分子示于图14a至图14c中。特征1410代表衔接子序列,其中在一些情况下,衔接子序列是illumina p5序列。特征1420代表条形码序列。特征1430代表引物序列,其中在一些情况下,引物序列是测序引物序列,例如illumina r1测序引物序列。特征1440代表转座子末端序列,其中在一些情况下,转座子末端序列是14bp的镶嵌元件。特征1450代表核糖核苷酸。特征1460代表3’阻断基,其中在一些情况下,3’阻断基是c3间隔子。特征1430和1440被配置成分别与衔接子侧接模板核酸分子中的特征1470和1480互补,其中特征1490代表模板核酸序列,特征1400和1405分别代表转座子末端序列和衔接子序列(例如,illumina r2序列)。
[0241]
在一些实施方案中,在本文所公开的方法中,rnase酶不能裂解含单链核糖核苷酸的条形码分子。在一些实施方案中,一旦模板核酸分子与核酸条形码分子杂交形成包含核糖核苷酸的至少部分双链的区域,则rnase酶裂解核糖核苷酸,从而释放3’阻断基。在一些实施方案中,rnase酶是rnase h2酶。在一些实施方案中,rnase h2酶是热稳定的。在一些实施方案中,rnase h2酶不裂解单链rna。在一些实施方案中,rnase h2酶裂解rna:dna双链体中的rna。在一些实施方案中,热稳定的rnase h2酶使3’阻断基释放。在一些实例中,热稳定的rnase h2酶使3’阻断基释放,如图14c所示。
[0242]
在一些实施方案中,本文所公开的用于核酸处理的方法包括向模板核酸分子添加衔接子序列,之后与本文所述的核酸条形码分子杂交并进行条形码化。在一些情况下,衔接子序列能够与核酸条形码分子上的序列杂交(图14b)。在一些实施方案中,通过转座酶(例如,通过标记片段化反应)将衔接子序列添加至模板核酸分子。在一些实施方案中,衔接子序列包含测序引物序列。在一些情况下,将引物序列与包含核糖核苷酸和3’阻断基的核酸条形码分子中的互补序列退火,其中3’阻断基通过rnase酶裂解核糖核苷酸而释放(图14c)。rnase裂解阻断基之后,衔接子侧接的模板核酸分子通过例如核酸延伸反应而条形码化。
[0243]
在一些实施方案中,所述多个核酸条形码分子能够与模板退火,但是直到3’阻断基被rnase酶裂解才生成延伸产物。
[0244]
在一些实施方案中,在线性扩增后,纯化dna并去除rnase。在一些情况下,剩余的核酸条形码分子可在si
‑
pcr期间与模板dna退火,但由于3’阻断基而不会引发dna聚合酶,
由此最小化条形码交换。
[0245]
在连接条形码化中最小化条形码交换
[0246]
在一些实施方案中,本文公开了用于核酸处理的方法,所述方法包括:在多个分区中,使用来自多个核酸条形码分子的核酸条形码分子和多个核酸分子(例如,来自或源自细胞),以生成多个条形码化核酸分子,其中所述核酸条形码分子包含防止核酸扩增、合成和/或延伸的序列、位点或区域。核酸条形码分子可以是部分双链的(例如,包含单链突出端),并且可另外包含一个或多个功能序列,例如引物序列、引物退火序列、条形码序列、唯一分子标志或这些序列中任一者的互补序列,以及可防止核酸条形码分子(例如,经由从模板链合成核酸分子的酶)扩增和/或延伸的位点、序列或区域(例如,无碱基位点、非经典碱基、3’阻断部分等)。在一些情况下,核酸条形码分子可包含5’突出序列。在一些情况下,5’突出序列可包含无碱基位点或非经典碱基(例如,尿嘧啶)。无碱基位点或非经典碱基(例如,尿嘧啶)可沿突出序列的5’方向位于任何数目的碱基位置(例如,3、4、5、6、7或8个碱基位置)。在一些情况下,使用3’阻断部分。
[0247]
在一些情况下,多个分区是多个液滴(例如,液滴乳剂)。在一些情况下,多个分区是多个孔(例如,微孔阵列)。
[0248]
在一些实施方案中,防止扩增和/或延伸的序列包含无碱基位点。在一些实施方案中,防止扩增和/或延伸的序列包含非经典碱基,例如尿嘧啶。在一些实施方案中,防止扩增和/或延伸的序列包含3’阻断物,例如3’延伸阻断剂。
[0249]
在一些实施方案中,通过将所述多个部分双链核酸条形码分子连接至所述多个核酸分子来生成多个条形码化核酸分子。
[0250]
在一些实施方案中,基于连接的条形码缀合用于对标记片段化的衔接子侧接的模板dna进行条形码化(参见,例如,图10b、图17和美国专利公开号20180340169(其以引用方式整体并入本文))。在一些情况下,核酸条形码分子包含部分双链区域。如本文所用,在一些情况下,术语“核酸条形码分子”可指部分双链条形码核酸分子。条形码核酸分子可包含衔接子序列(例如,illumina p5序列或其互补序列)、条形码序列和引物序列(例如,测序引物序列,例如illumina r1或r2测序引物序列或其互补序列)。另外或替代地,条形码分子可包含功能序列,例如间隔子序列(如本文其他地方所述)、唯一分子标识符、结合序列、限制位点等的任何组合或变型。核酸条形码分子可与标记片段化的衔接子侧接的模板dna缔合(例如,经由杂交)。在一些情况下,核酸条形码分子上的一个或多个序列(例如,5’突出端)可以与标记片段化的衔接子侧接的模板dna上的一个或多个序列互补并且/或者能够与所述一个或多个序列退火。在一些情况下,标记片段化的衔接子侧接的模板dna可以用酶(例如,t4多核苷酸激酶)处理,以使5’末端磷酸化。然后可使用酶(例如,连接酶(例如t4 dna连接酶))将核酸条形码分子连接至标记片段化的衔接子侧接的模板dna,以生成条形码化核酸分子。在一些实例中,核酸条形码分子偶联至固相支持体。在一些情况下,固相支持体是珠粒。在一些实施方案中,固相支持体是如本文其他地方所述的凝胶珠粒。在一些情况下,如本文其他地方所述,核酸条形码分子可释放地连接至固相支持体。
[0251]
图18a示意性地示出了示例性核酸条形码分子1801,其可防止核酸条形码分子1801的下游扩增和/或延伸(例如,聚合酶从突出序列或模板链合成链)。核酸条形码分子可以是部分双链的(例如,包含单链突出端)。核酸条形码分子1801可包含衔接子序列1810(例
如,p5序列)、条形码序列1820和引物序列1830(例如,r1测序引物序列)或这些序列中任一者的互补序列。核酸条形码分子1801的引物序列1830(例如,r1序列)或其互补序列可以是单链突出序列(例如5’突出端),并且可至少部分地与衔接子侧接模板核酸片段的序列互补并且/或者能够与所述序列退火,并且可包含防止扩增和/或延伸的碱基对、位点或序列1840a(例如,非经典碱基(例如,如图18a所示的尿嘧啶)、氧化碱基对、间隔子(例如,c3间隔子)或甲基化碱基对)。在使用尿嘧啶的情况下,可将尿嘧啶置于序列1830中的任何位置,例如置于双链接点之后的位置1、2、3、4、5、6、7、8、9等。在一些情况下,可用酶例如尿嘧啶
‑
dna
‑
糖基化酶处理包含尿嘧啶的核酸条形码分子,以生成无碱基位点1840b。在一些实施方案中,无碱基位点(也称为四氢呋喃(thf)位点或嘌呤/嘧啶基(ap)位点)是通过寡核苷酸引物的化学合成而生成的。在一些实施方案中,化学合成的无碱基位点可包含双脱氧四氢呋喃、1
’‑
核四氢呋喃或2
’‑
核四氢呋喃(也称为无碱基ii位点)。图18b示意性地示出了另一示例性核酸条形码分子1802,其可防止核酸条形码分子1802的下游扩增和/或延伸。核酸条形码分子可以是部分双链的。核酸条形码分子1802可包含衔接子序列1810(例如,p5序列)、条形码序列1820和引物序列1830(例如,r1测序引物序列)或这些序列中任一者的互补序列。引物序列1830(例如,r1序列)或其互补序列可以是至少部分地与衔接子侧接模板核酸片段的序列互补和/或能够与所述序列退火的单链突出序列(例如,5’突出端),并且可包含防止扩增和/或延伸的序列、位点或区域,例如无碱基位点1840b。无碱基位点1840b可置于序列1830中的任何位置,例如置于双链接点之后的位置1、2、3、4、5、6、7、8、9等。图18c示意性地示出了示例性核酸条形码分子1803,其可防止核酸条形码分子1803的下游扩增和/或延伸。核酸条形码分子可以是部分双链的。核酸条形码分子1803可包含衔接子序列1810(例如,p5序列)、条形码序列1820和引物序列1830(例如,r1测序引物序列)或这些序列中任一者的互补序列。核酸条形码分子1803的引物序列1830或其互补序列可以是突出序列(例如,5’突出端),并且可至少部分地与衔接子侧接模板核酸片段的序列互补,并且可包含防止扩增和/或延伸的序列、位点或区域,例如无碱基位点1840c(图i)或非经典碱基(例如,尿嘧啶,图ii)。尿嘧啶或无碱基位点1840c可置于双链接点处(例如,置于互补[底部]链上的条形码序列1820的至少[3’末端]碱基位置[用“a”表示]处)。图18d示意性地示出了另一示例性核酸条形码分子1804,其可防止核酸条形码分子1804的下游扩增和/或延伸。核酸条形码分子可以是部分双链的。核酸条形码分子1804可包含衔接子序列1810(例如,p5序列)、条形码序列1820和引物序列1830(例如,r1测序引物序列)或这些序列中任一者的互补序列。核酸条形码分子1804的引物序列1830或其互补序列可以是突出序列(例如,5’突出端),并且可至少部分地与衔接子侧接模板核酸片段的序列互补。核酸条形码分子1804的一条链(例如,底部链)可包含防止扩增和/或延伸的序列,例如可阻止延伸的3’阻断基1850。3’延伸阻断剂可以是3’c3间隔子、双脱氧核苷酸、反向核苷酸、氨基或磷酸基等。
[0252]
在一些实施方案中,本文所公开的组合物的3’阻断基在阻断寡核苷酸的3’端。在一些实施方案中,本文所公开的组合物的3’阻断基是2
’‑3’‑
二脱氧胞嘧啶(ddc)。在一些实施方案中,本文所公开的组合物的3’阻断基是2
’‑5’
连接的核苷。在一些实施方案中,本文所公开的组合物的3’阻断基是3’c3间隔子。在一些实施方案中,本文所公开的组合物的3’阻断基是氨基修饰的c6。在一些实施方案中,本文所公开的组合物的3’阻断基是反向脱氧胸苷(dt)。在一些实施方案中,本文所公开的组合物的3’阻断基是3’氨基修饰的核苷酸。在
一些实施方案中,本文所公开的组合物的3’阻断基是3’磷酸基。在一些实施方案中,本文所公开的组合物的3’阻断基是2
’‑5’
连接的核苷,其中2
’‑5’
连接的核苷是3
’‑
脱氧胸苷(3
’‑
dt)。在一些情况下,本文所公开的组合物的2
’‑5’
连接的核苷是3
’‑
脱氧胞苷(3
’‑
dc)。在一些情况下,本文所公开的组合物的2
’‑5’
连接的核苷是3
’‑
脱氧腺苷(3
’‑
da)。在一些情况下,本文所公开的组合物的2
’‑5’
连接的核苷是3
’‑
脱氧鸟苷(3
’‑
dg)。
[0253]
本文所公开的阻断寡核苷酸也可用于防止多种基于核酸的反应中的不想要的相互作用。例如,本文所公开的阻断寡核苷酸可用于阻止,抑制或以其他方式改变pcr反应的速率(例如,在以下情况下:(1)纯化步骤无法执行或不理想,或(2)为了最小化样品中由一种或多种特异性引物或引物组引发的pcr反应)。在一些情况下,阻断寡核苷酸防止核酸延伸或连接。
[0254]
包含防止扩增和/或延伸的序列的条形码分子可用于防止条形码交换反应,例如,图12b所示的那些。例如,将条形码化的衔接子侧接的模板核酸分子从分区中取出并在本体样品标志pcr(si
‑
pcr)反应中合并后,任何剩余的未掺入的核酸条形码分子都可能会发生不期望的扩增反应(例如,本文所述的条形码交换反应)。然而,包含防止扩增和/或延伸的序列的核酸条形码分子的一部分(例如,一条链)可能不会被扩增,因此额外/遗留双链条形码分子的生成被最小化。由于额外的条形码分子可能会与用于衔接子侧接模板核酸分子或其产物的si
‑
pcr的引物竞争并导致高条形码交换率,因此使用包含防止扩增和/或延伸的序列的条形码分子的方法可显著减少条形码交换(参见,例如,图20)。
[0255]
计算机系统
[0256]
本公开提供被编程用于实施本公开的方法的计算机系统。图9示出一种计算机系统901,其被编程或以其它方式配置用于例如:(i)控制微流体系统(例如,流体流动);(ii)将被占用的液滴与未被占用的液滴分类;(iii)使液滴聚合;(iv)进行测序应用;(v)生成和维持dna或cdna片段的文库;和/或(vi)分析可接近染色质的区域。计算机系统901可调控本公开的各个方面,例如,调控微流体结构中的一个或多个通道中的流体流速,调控聚合应用单元,调控本文所述某些反应的条件。计算机系统901可以是用户的电子设备或相对于该电子设备远程定位的计算机系统。该电子设备可以是移动电子设备。
[0257]
计算机系统901包括中央处理单元(cpu,本文中又称为“处理器”和“计算机处理器”)905,它可以是单核或多核处理器,或用于并行处理的多个处理器。计算机系统901还包括存储器或存储位置910(例如随机存取存储器、只读存储器、快闪存储器)、电子存储单元915(例如硬盘)、用于与一个或多个其他系统通信的通信接口920(例如网络适配器)和外围设备925,例如高速缓冲存储器、其他存储器、数据存储和/或电子显示适配器。存储器910、存储单元915、接口920和外围设备925与cpu 905通过通信总线(实线),例如母板通信。存储单元915可以是用于存储数据的存储单元(或数据储存库)。计算机系统901可以借助于通信接口920与计算机网络(“网络”)930可操作地耦合。网络930可以是因特网、内网和/或外网或与因特网通信的内网和/或外网。网络930在一些情况下是无线电通信和/或数据网络。网络930可以包括一个或多个计算机服务器,所述计算机服务器可以实现分布式计算,例如云计算。网络930,在一些情况下借助于计算机系统901,可以实现对等网络,对等网络可以使设备能够与计算机系统901耦合以起到客户端或服务器的作用。
[0258]
cpu 905可以执行一系列机器可读的指令,所述指令可以体现在程序或软件中。所
述指令可以存储在存储位置,例如存储器910中。可以将指令引导到cpu 905,随后可编程或以其他方式配置cpu 905以实现本公开的方法。通过cpu 905执行的操作的实例可以包括获取指令、解码、执行和回写。
[0259]
cpu 905可以是电路、例如集成电路的一部分。系统901的一个或多个其他组件可以包括在电路中。在一些情况下,电路是专用集成电路(asic)。
[0260]
存储单元915可以存储文件夹,例如驱动器、程序库和保存的程序。存储单元915可以存储用户数据,例如用户偏好和用户程序。在一些情况下,计算机系统901可以包括一个或多个另外的数据存储单元,所述数据存储单元在计算机系统901以外,例如位于远程服务器上,所述远程服务器通过内网或因特网与计算机系统901通信。
[0261]
计算机系统901可以与一个或多个远程计算机系统通过网络930通信。例如,计算机系统901可以与用户(例如,操作人员)的远程计算机系统通信。远程计算机系统的实例包括个人计算机(例如便携式pc)、触屏平板或平板pc(例如ipad、galaxy tab)、电话、智能手机(例如iphone、安卓启动装置、)或个人数字助理。用户可以经由网络930进入计算机系统901。
[0262]
如本文所述的方法可以借助于计算机系统901的电子存储位置上,例如存储器910或电子存储单元915上存储的机器(例如,计算机处理器)可执行代码实施。机器可执行或机器可读代码可以呈软件形式提供。使用期间,代码可由处理器905执行。在一些情况下,可以从存储单元915检索代码,并且将其存储在存储器910上以供处理器905进行就绪访问。在一些情况下,可排除电子存储单元915,并且将机器可执行指令存储在存储器910上。
[0263]
代码可以预编译和配置以用于具有被调适成执行所述代码的处理器的机器,或可以在运行时间期间编译。代码可以呈编程语言提供,所述编程语言经过选择,以使代码能够以预编译或如所编译的方式执行。
[0264]
本文提供的系统和方法的各方面,例如计算机系统901,可以在编程中体现。这项技术的各个方面可以被认为是“产品”或“制品”,通常呈在一种机器可读介质上携带或体现的机器(或处理器)可执行代码和/或相关数据的形式。机器可执行代码可以存储在电子存储单元,例如存储器(例如,只读存储器、随机存取存储器、闪速存储器)或硬盘上。“存储”型介质可以包括计算机、处理器等的任何或所有有形存储器,或其相关模块,例如各种半导体存储器、磁带驱动器、磁盘驱动器等,这些模块可以在任何时候为软件编程提供非暂时性存储。软件整体或部分有时可以通过因特网或各种其他电信网通信。这类通信例如能够将软件从一个计算机或处理器装载至另一个计算机或处理器,例如从管理服务器或主机装载至应用服务器的计算机平台。因此,可以负载软件元件的另一类型介质包括光波、电波和电磁波,例如跨越本地设备之间的物理接口使用,通过有线和光学固定网络和经各种空中链路。携带这类波的物理元件,例如有线或无线链路、光链路等,也可以被认为是负载软件的介质。如本文所用,除非局限于非暂时性有形“存储”介质,否则例如计算机或机器“可读介质”的术语是指参与提供指令给处理器来执行的任何介质。
[0265]
因此,例如计算机可执行代码的机器可读介质可以采取许多形式,包括但不限于有形存储介质、载波介质或人工传输介质。非易失性存储介质包括例如光盘或磁盘,例如图式中所示的任何计算机中的任一存储装置等,例如可以用于实施数据库等。易失性存储介
质包括动态存储器,例如这类计算机平台的主存储器。有形传输介质包括同轴电缆;铜丝和光纤,包括包含计算机系统内的母线的电线。载波传输介质可以采取电信号或电磁信号的形式,或声波或光波的形式,例如在射频(rf)和红外线(ir)数据通信期间产生的那些形式。因此,计算机可读介质的常见形式包括例如:软盘、软磁盘、硬盘、磁带、任何其他磁性介质、cd
‑
rom、dvd或dvd
‑
rom、任何其他光学介质、穿孔纸带、具有孔图案的任何其他物理存储介质、ram、rom、prom和eprom、flash
‑
eprom、任何其他存储芯片或存储卡、载波输送数据或指令、输送这类载波的电缆或链路或计算机可以从中读取编程代码和/或数据的任何其他介质。计算机可读介质的这些形式中的许多可能参与将一系列或多个系列的一个或多个指令携带至处理器进行执行。
[0266]
计算机系统901可包括电子显示器935或与所述电子显示器通信,所述电子显示器包括用户界面(ui)940,所述用户界面用于提供例如测序分析的结果,将测序读段与发生条形码交换的区域相关联等。ui的实例包括但不限于图形用户界面(gui)和基于网络的用户界面。
[0267]
本公开的方法和系统可以借助于一种或多种算法实施。算法可以在由中央处理器905执行时通过软件来实现。该算法可例如执行测序反应,将测序读段与条形码交换发生相关联等。
[0268]
本公开的装置、系统、组合物和方法可以用于各种应用,例如处理来自单细胞的单个分析物(例如rna、dna或蛋白质)或多种分析物(例如dna和rna、dna和蛋白质、rna和蛋白质或rna、dna和蛋白质)。例如,生物颗粒(例如,细胞或细胞珠粒)被分配在分区(例如,液滴)中,并将来自生物颗粒的多种分析物处理以供后续处理。多种分析物可以来自所述单细胞。这能够对细胞进行例如同时的蛋白质组学、转录物组和基因组分析。
[0269]
虽然本文已经展示和描述了本发明的优选实施方案,但是本领域的技术人员显而易见这类实施方案仅仅是为了举例而提供。不意图本发明受本说明书内所提供的特定实例限制。虽然本发明已经参考前述说明书进行了描述,但是对本文的实施方案的描述和说明并不意在以限制性意义进行解释。在不偏离本发明的情况下本领域技术人员现将进行各种变型、变化和替换。此外,应了解本发明的所有方面不限于本文阐述的取决于各种条件和变量的具体描述、配置或相对比例。应了解,可以采用本文所述的本发明的实施方案的多个替换方案实施本发明。因此,预期本发明还将涵盖任何此类替换方案、修改、改变或等效方案。意图以下权利要求书界定本发明的范围,并且因此涵盖在这些权利要求书范围内的方法和结构和它们的等效物。
[0270]
实施例
[0271]
实施例1.在分区中通过线性扩增使用本体标记片段化和条形码化生成条形码化核酸片段
[0272]
以基本上维持天然染色质组织的方式从目标细胞群体中的细胞中大批收获细胞核。或者,将细胞透化,使转座酶
‑
核酸复合物进入细胞核。在一些情况下,如本文其他地方所述,可将细胞掺入细胞珠粒中。然后在转座酶
‑
核酸复合物的存在下孵育透化的细胞核(或透化的细胞)以生成衔接子侧接的核酸片段(例如,基因组dna的,例如染色质中的基因组dna的)。
[0273]
然后将包含衔接子侧接的模板核酸片段的细胞核(或细胞)分配到多个分区(例
如,多个液滴或多个孔)中,以使至少一些分区包含(1)单个细胞核(或细胞),其包含衔接子侧接的模板核酸片段;和(2)多个单链条形码寡核苷酸分子,其包含转座子末端序列(me)、read1序列(r1)或其一部分、条形码序列(bc)和p5衔接子序列(p5)。在一些实施方案中,将单链条形码寡核苷酸分子附接至凝胶珠粒并进行分配,以使至少一些分区包含(1)单个细胞核(或细胞),其包含衔接子侧接的模板核酸片段;和(2)单个凝胶珠粒。除了前述组分之外,在一些实施方案中,所述多个分区还包含促进下述反应的试剂(例如,酶和缓冲剂)。
[0274]
然后使含单个细胞核的分区经受条件以使衔接子侧接的模板核酸片段从细胞核释放。在释放衔接子侧接的模板核酸片段之后,用合适的酶填充转座反应的缺口。在某些实施方案中,在条形码寡核苷酸附接至凝胶珠粒的情况下,使分区经受条件以使条形码寡核苷酸分子从凝胶珠粒释放(例如,例如使用还原剂例如dtt使凝胶珠粒解聚)。然后,使用单链条形码寡核苷酸分子作为引物,对填充缺口的衔接子侧接的模板核酸片段进行线性扩增反应,以产生条形码化的衔接子侧接的模板核酸片段。参见图11。
[0275]
然后使条形码化的衔接子侧接的模板核酸片段从分区释放,并在本体样品标志聚合酶链反应(si
‑
pcr)中进行处理,以完成文库制备用于下一代高通量测序(例如,以添加样品标志(si)序列(例如,i7)和/或其他衔接子序列(例如,p7))。在一些情况下,在本体处理(例如,si
‑
pcr)之前,将本公开的阻断寡核苷酸连接至条形码化的衔接子侧接的模板核酸片段以防止条形码交换,如图12a所示。在一些实施例中,在本体处理(即,si
‑
pcr)之前,使用来自本公开的含有3’阻断基的含核糖核苷酸的条形码分子来防止条形码交换,如图14所示。然后根据合适的下一代测序方案(例如,illumina测序)对完整构建的文库进行测序。
[0276]
实施例2.在分区中通过线性扩增使用标记片段化和条形码化生成条形码化核酸片段
[0277]
将来自目标细胞群体的细胞(或来自目标细胞群体中的细胞的完整细胞核)分配到多个分区中,或掺入细胞珠粒中并进行分配,以使至少一些分区包含(1)包含模板核酸的单个细胞(或单个细胞核),或单个细胞珠粒;和(2)多个单链条形码寡核苷酸分子,其包含转座子末端序列(me)、read1序列(r1)、条形码序列(bc)和p5衔接子序列(p5)。在一些实施方案中,将单链条形码寡核苷酸分子附接至凝胶珠粒并进行分配,以使至少一些分区包含(1)单个细胞(或单个细胞核)和(2)单个凝胶珠粒。除了前述组分之外,在一些实施方案中,所述多个分区还包含促进下述反应的试剂(例如,酶和缓冲剂)。
[0278]
分配到多个分区中后,将单个细胞(或细胞核)裂解,以基本上维持天然染色质组织的方式释放模板基因组dna。在某些实施方案中,在条形码寡核苷酸附接至凝胶珠粒的情况下,使分区经受条件以使条形码寡核苷酸分子从凝胶珠粒释放(例如,例如使用还原剂例如dtt使凝胶珠粒解聚)。然后使分区经受条件以生成转座酶
‑
核酸复合物。或者,在一些实施方案中,将多个预先形成的转座酶
‑
核酸复合物分配到多个分区中。然后使分区经受条件,使得转座酶
‑
核酸复合物将第一衔接子序列和第二衔接子序列整合到模板核酸中以产生双链的衔接子侧接的模板核酸片段。因为转座酶
‑
核酸复合物只能作用于无核小体的dna,所以衔接子侧接的模板核酸片段代表单个细胞中可接近染色质的全基因组区域。或者,在一些实施方案中,在完整细胞核中进行标记片段化反应,并且使细胞核裂解以释放双链的衔接子侧接的模板核酸片段。
[0279]
然后一般如实施例1中所述对样品进行处理。标记片段化后,用合适的缺口填充酶
填充转作反应所产生的缺口。然后使用单链条形码寡核苷酸分子作为引物,对填充缺口的衔接子侧接的模板核酸片段进行线性扩增反应,以产生条形码化的衔接子侧接的模板核酸片段。
[0280]
然后使条形码化的衔接子侧接的模板核酸片段从分区释放,并进行本体处理,以完成文库制备用于下一代高通量测序(例如,以添加样品标志(si)序列(例如,i7)和/或其他衔接子序列(例如,p7))。在一些情况下,在本体处理(反应(例如,si
‑
pcr))之前,将本公开的阻断寡核苷酸连接至条形码化的衔接子侧接的模板核酸片段以防止条形码交换,如图12a所示。在一些实施例中,在本体处理(即,si
‑
pcr)之前,使用来自本公开的含有3’阻断基的含核糖核苷酸的条形码分子来防止条形码交换,如图14所示。然后根据合适的下一代测序方案(例如,illumina测序)对完整构建的文库进行测序。
[0281]
实施例3.发夹帽防止经由pcr扩增
[0282]
测试了本公开的阻断寡核苷酸,以确定它们是否可成功地阻断聚合酶链反应(pcr)。生成与本文所公开的衔接子侧接的模板核酸分子类似的dna片段(参见图11)并使用与衔接子侧接的核酸分子中的r1和r2序列互补的引物进行扩增(参见图15a)。在pcr之前,将样品在存在阻断寡核苷酸(“+h”)或不存在阻断寡核苷酸(
“‑
h”)下,且在存在dna连接酶(“+l”)或不存在dna连接酶(
“‑
l”)下孵育。在pcr之后,将反应物清理并在生物分析仪上运行以定量dna(图15b)。如图15b所示,当不包括阻断寡核苷酸(
“‑
h”)时,容易检测到pcr产物,如图中蓝色和红色峰所指示的。然而,当包括阻断寡核苷酸时,即使不存在dna连接酶,pcr产物也显著减少,如图15b上的图中绿色和青色线中不存在峰所指示的。总体而言,这些结果证实本公开的阻断寡核苷酸可抑制pcr反应并起到减少条形码交换反应的作用。此外,如由包括阻断寡核苷酸但不包括dna连接酶的反应所示,阻断寡核苷酸与引物序列的杂交可能足以抑制pcr,因此阻断寡核苷酸与引物的连接可能不是严格必要的。
[0283]
实施例4.发夹帽减少条形码交换
[0284]
测试了本公开的阻断寡核苷酸,以确定它们是否可成功地减少si
‑
pcr反应期间条形码化的衔接子侧接的模板核酸片段上的条形码交换。为此,在线性扩增后,将外源条形码核酸分子(含有与用于对模板核酸片段进行条形码化的条形码序列不同的条形码序列)掺入si
‑
pcr反应中(一般参见图11)。这样,外源条形码序列存在于最终文库中的唯一方法是通过本文所述的条形码交换事件。在线性扩增后,si
‑
pcr反应设置为使用恒定浓度的外源条形码和两种不同浓度的阻断寡核苷酸(“hp
”‑
15nm和500nm)和dna连接酶(“+连接酶”)。阴性对照反应设置为不使用阻断寡核苷酸(“0nm hp”),也不使用dna连接酶(
“‑
连接酶”)。然后对最终文库产物进行测序,并计算出含有外源条形码的读段的分数。结果显示,条形码交换的频率下降了约50%,并且似乎与所利用的阻断寡核苷酸的浓度无关(图16)。
[0285]
实施例5.在分区中通过连接使用本体标记片段化和条形码化生成条形码化核酸片段
[0286]
以基本上维持天然染色质组织的方式从目标细胞群体中的细胞中大批收获细胞核。或者,将细胞透化,使转座酶
‑
核酸复合物进入细胞核。如本文其他地方所述,可将细胞掺入细胞珠粒中。然后在转座酶
‑
核酸复合物的存在下孵育透化的细胞核(或透化的细胞)以生成衔接子侧接的核酸片段(例如,基因组dna的,例如染色质中的基因组dna的)。
[0287]
然后将包含衔接子侧接的模板核酸片段的细胞核(或细胞或细胞珠粒)分配到多
个分区(例如,多个液滴或多个孔)中,以使至少一些分区包含(1)单个细胞核(或细胞或细胞珠粒),其包含衔接子侧接的模板核酸片段;和(2)多个部分双链核酸条形码分子,其包含转座子末端序列、read1序列(r1)或其一部分、条形码序列(bc)和p5衔接子序列(p5)。在一些实施方案中,将部分双链核酸条形码分子附接至凝胶珠粒并进行分配,以使至少一些分区包含(1)单个细胞核(或细胞或细胞珠粒),其包含衔接子侧接模板核酸片段和(2)单个凝胶珠粒。除了前述组分之外,在一些实施方案中,所述多个分区还包含促进下述反应的试剂(例如,酶和缓冲剂)。
[0288]
然后使含单个细胞核的分区经受条件以使衔接子侧接的模板核酸片段从细胞核释放。在释放衔接子侧接的模板核酸片段之后,用酶例如t4多核苷酸激酶处理5’末端,以使衔接子侧接的模板核酸片段的5’末端磷酸化。在某些实施方案中,在条形码寡核苷酸附接至凝胶珠粒的情况下,使分区经受条件以使核酸条形码分子从凝胶珠粒释放(例如,例如使用还原剂例如dtt使凝胶珠粒解聚)。条形码寡核苷酸分子可以是部分双链的,并且可与5
’‑
磷酸化的衔接子侧接的模板核酸片段缔合(例如,退火)。然后可使用酶例如连接酶(例如t4 dna连接酶)将条形码寡核苷酸分子连接至5
’‑
磷酸化的衔接子侧接的模板核酸片段,以生成条形码化核酸分子。参见,例如,图17。然后将分区破损或破坏,并使条形码化核酸分子经受足以填补由标记片段化引入的缺口以及添加其他序列例如p7序列和i7序列的条件(例如,经受si
‑
pcr用于文库制备和测序)。
[0289]
实施例6.在部分双链条形码分子中放置尿嘧啶可防止条形码交换。
[0290]
为了测试条形码交换,将包含尿嘧啶或无碱基位点的部分双链核酸条形码分子(例如,如图18a至图18c所示)掺入条形码文库中,并确定条形码匹配的量(条形码对应性)。简而言之,用以下各项进行pcr反应:(1)外来的部分双链条形码分子;(2)4个dna模板中的一个,每个模板具有以下结构p5
‑
bc
‑
r1
‑
插入物
‑
r2
‑
p7,并且除条形码外具有相同的序列(参见表1;条形码序列以粗体显示,插入物带下划线)。在pcr之后,将反应产物纯化,测序,并确定与原始4个条形码相关的读段的数目作为条形码匹配百分比(图19)。阴性对照反应不包含掺入的外来条形码,而阳性对照则包含掺入的条形码,所述掺入的条形码不包含任何尿嘧啶或无碱基位点。对于某些反应,掺入的条形码分子在选定位置包含尿嘧啶或无碱基位点。将尿嘧啶或无碱基部分置于条形码分子的单链部分的多个位置(例如,包含5’突出序列的底部链上的r1引物序列内的各个位置)处并用尿嘧啶
‑
dna
‑
糖基化酶(udg)处理以生成无碱基位点。尿嘧啶位于距包含5’突出序列的链上的双链接点3、4、5、6、7、8或9个碱基(沿5’方向)。
[0291]
如图19所示,针对每一测试条件将条形码对应性的百分比绘制为条形图。无碱基(“ab”)位于距接点位置5(在包含5’突出序列的链上沿5’方向)处使得条形码对应性为约99%。类似地,尿嘧啶位于距接点位置5、6、7或8(在包含5’突出序列的链上沿5’方向)处,随后进行udg处理,使得条形码对应性大于95%(位置5、6和7处为99.6%,位置8处为97.5%)。同样,尿嘧啶或无碱基位点位于距双链接点3或4个核苷酸(在包含5’突出序列的链上沿5’方向),随后进行udg处理,产生高条形码对应性(数据未示出)。然而,尿嘧啶位于距双链接点9个碱基(在包含5’突出序列的链上沿5’方向),使得条形码交换的程度更高(62.5%的条形码匹配)。总体而言,这些结果证实,使用本文所述的方法,在本公开的核酸条形码分子的5’突出序列中掺入尿嘧啶,然后进行udg处理或掺入无碱基位点,可减少条形码交换反应。
[0292]
表1.掺入反应中使用的序列。
[0293]
[0294][0295]
实施例7.在条形码分子中掺入防止扩增的序列可防止延伸。
[0296]
测试了防止核酸条形码分子中的扩增的序列的掺入以确定这种方法是否可成功地防止核酸条形码分子的延伸。使用包含尿嘧啶部分或无碱基位点的部分双链核酸分子(例如,如图18a所示)作为条形码分子。尿嘧啶部分位于双链接点后5个碱基。使包含尿嘧啶的核酸条形码分子,包含无碱基位点的核酸条形码分子,包含经udg处理的尿嘧啶(并因此包含无碱基位点)的核酸条形码分子进行延伸反应。该测定如下进行:将5
’‑
fam标记的(荧光素)顶部链和含有对照/尿嘧啶/无碱基位点的底部链(参见表2)彼此退火,并与聚合酶(nebnext high fidelity 2x pcr主混合物)一起在72℃下孵育5分钟。然后将反应用edta猝灭,并加载到毛细管电泳仪上进行分析。在一些组中,在延伸之前,对包含尿嘧啶的核酸条形码分子进行尿嘧啶
‑
dna
‑
糖基化酶(udg)处理以生成无碱基位点。图20示出了来自这种实验的示例性数据。在图20中示出了毛细管电泳的色谱图。沿x轴为核酸分子的大小(以碱基对为单位),而y轴描绘了的荧光信号强度(以au(吸光度单位)为单位)。可看出,阳性对照2007a(“延伸的对照
”‑
无尿嘧啶或无碱基位点,如2007b示意性示出)核酸分子被延伸并产生了一个可检测的峰,该峰对应于长度为约53个核苷酸的延伸的分子。相比之下,阴性对照2001a(“未延伸的对照”,如2001b示意性示出)产生了一个可检测的峰,该峰对应于长度为约38个核苷酸的未延伸的分子。进行延伸的尿嘧啶未经udg处理组2003a(如2003b示意性地示出)具有与未延伸的对照组2001a相似的长度。延伸后,尿嘧啶/经udg处理组2009a(示意
性地示于2009b中)和无碱基组2005a(示意性地示于2005b中)均产生可检测到的峰,该峰对应于长度为约43个核苷酸的分子(双链接点后5个核苷酸的尿嘧啶或无碱基位点)。尽管未示出,但在双链接点处或双链接点后的位置1或2处包含尿嘧啶或无碱基位点也可有效抑制延伸。总体而言,这些结果证实在核酸条形码分子中掺入尿嘧啶或无碱基位点可抑制核酸分子的延伸,并隐隐减少不想要的条形码交换事件。
[0297]
表2.延伸反应中使用的序列。
[0298]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1