包含糖原合酶激酶-3(GSK3)编码区的重组的具有复制能力的病毒和杀伤异常细胞的方法与流程
糖原合酶激酶-3(gsk3)是一种多功能酶,其参与多种细胞过程,例如细胞增殖、凋亡、神经功能、新陈代谢、胚胎发育和胰岛素信号传导(1,2)。存在这种蛋白质的两种已知的同种型;gsk3-α和gsk3-β。酶通过在不同残基中的磷酸化而经历活化或失活。这两种同种型具有相似的结构,但细胞功能不同,并且由不同的基因编码(3)。
蛋白质活化和失活的一种方式是通过酪氨酸(y)和丝氨酸(s)残基的翻译后磷酸化发生的。gsk3-α和gsk3-β被认为在非刺激的静止细胞中是有活性的。两种同种型也能够自动磷酸化gsk3-α中的y279残基和gsk3-β中的y216。已知在这些位置的磷酸化增加了蛋白质的催化活性。gsk3-α的s21和gsk3-β的s9的磷酸化可以灭活相应的蛋白质;这些磷酸化的残基阻断底物结合位点,从而可以抑制gsk3功能(4,5)。
gsk3的失调与不同的疾病有关。值得注意的是神经退行性病症、糖尿病和癌症中的一些(1,2)。其过表达及其在肿瘤促进或阻抑中的意义已有报道;但可能依赖于细胞类型和磷酸化状态(6-8)。
已经在几种类型的肿瘤中描述了gsk3的过表达,其中它可以充当促进存活、细胞生长和血管生成的肿瘤促进剂(9,10)。gsk3被认为是多形性胶质母细胞瘤、胰腺癌、结肠直肠癌、肾癌、白血病和卵巢癌中的癌症促进剂(5)。
在许多癌症类型中已经报道了gsk3-β的失活。gsk3-β被认为是皮肤癌、乳腺癌、口腔癌和肺癌中的肿瘤抑制剂(5,11-13)。
产生具有组成型活性的gsk3-β的一种方式是将在第9位的丝氨酸取代为丙氨酸(s9a-gsk3-β),这防止在该位置形成可以使蛋白质失活的磷酸化丝氨酸。几个组已经设计了抑制gsk3-β在已知gsk3是原致癌的(pro-tumorigenic)那些癌症中的活性的小分子(14-16)。
近年来,具有复制能力的腺病毒作为癌症治疗中的溶瘤剂吸引了新的兴趣。当前的方法使用腺病毒基因组中的修饰,与正常细胞相比,其促进肿瘤细胞中优先的病毒复制。在这方面,腺病毒突变体“onyx-015”和delta24腺病毒可以充当原型。onyx-015病毒在编码e1b55kda蛋白质的区域中具有缺失。结果,病毒不能下调有效病毒复制所必需的p53活性。delta24病毒在病毒e1a基因中携带缺失,所述缺失涵盖负责结合rb蛋白的区域。rb的结合对于含rb的细胞中的有效复制是必需的。
本发明是第一个其中gsk3用于促进腺病毒的复制和/或其溶瘤特性。这在本发明中用于例如促进感染的肿瘤细胞的杀伤和癌症的治疗。
发明概述
本发明提供了重组的具有复制能力的腺病毒,其在所述腺病毒的基因组中包含与表达控制序列可操作地连接的糖原合酶激酶-3(gsk3)蛋白的编码序列。
还提供了治疗个体中的癌症的方法,其包括向有需要的个体施用本发明的腺病毒。
进一步提供了本发明的腺病毒,其用于治疗患有癌症的个体。
进一步提供了杀伤癌细胞的方法,其包括向包含所述癌细胞的肿瘤提供本发明的腺病毒。
还提供了用于提高重组的具有复制能力的腺病毒在容纳性细胞中的复制速率的方法,其包括向所述腺病毒的基因组提供与表达控制序列可操作地连接的gsk3蛋白的编码序列,用于在所述细胞中表达所述编码序列。
进一步提供了用于增加溶瘤性重组的具有复制能力的腺病毒的溶瘤特性的方法,其包括向所述腺病毒的基因组提供与表达控制序列可操作地连接的gsk3蛋白的编码序列,用于表达所述编码序列。
在另一个方面,提供了增加重组的具有复制能力的腺病毒在肿瘤中的复制速率和扩散的方法,所述方法包括向溶瘤腺病毒提供与表达控制序列可操作地连接的gsk3蛋白的编码序列,用于在所述肿瘤的细胞中表达所述编码序列。
还提供了gsk3蛋白的编码序列用于提高重组腺病毒的复制速率的用途,所述gsk3蛋白的编码序列与表达控制序列可操作地连接,用于提高所述重组腺病毒的复制速率。
进一步提供了包含本发明的腺病毒与另外的药物,优选癌症药物的组合。
本发明还提供了治疗方法或用于治疗的本发明的腺病毒,其中所述治疗还包括同时或依次施用放射疗法、抗体疗法、化学疗法、细胞疗法、免疫疗法或者其它抗癌干预或治疗。
发明详述
gsk3-α也以例如糖原合酶激酶3α、丝氨酸/苏氨酸-蛋白激酶gsk3a、gsk3α和糖原合酶激酶-3α的名称为人所知。gsk3α的参考序列可以在以下登录号找到:hgnc:4616;entrezgene:2931;ensembl:ensg00000105723;omim:606784或uniprotkb:p49840。gsk3-β也以例如糖原合酶激酶3β、丝氨酸/苏氨酸-蛋白激酶gsk3b、gsk3β、糖原合酶激酶-3β和gsk3β同种型的名称为人所知。gsk3β的参考序列可以在以下登录号找到:hgnc:4617;entrezgene:2932;ensembl:ensg00000082701;omim:605004和uniprotkb:p49841。给予参考序列仅用于鉴定基因。这并不意味着该基因必须具有与数据库中针对相应登录代码所指示的完全相同的序列。基因名称涵盖了序列的天然和重组变体。
本文所述的腺病毒编码的gsk3蛋白优选是gsk3-β蛋白。gsk3蛋白优选是具有组成型活性的突变蛋白。在这方面,gsk3蛋白优选是gsk3-β蛋白,其中第9位的丝氨酸残基被另一个氨基酸残基,优选丙氨酸残基取代。
gsk3的编码序列通常包含该基因的cdna。cdna通常比基因组序列短,在重组病毒中优选较短的序列。另一方面,细胞中的表达通常通过一个或多个内含子的存在而增强。这种内含子可以是gsk3基因的天然内含子。优选地,内含子是人工内含子,优选地被引入包含编码区的mrna前体(pre-mrna)的5'-非编码区中。
编码区优选与表达控制序列如启动子可操作地连接。启动子通常与增强子序列连接。启动子和增强子的组合有时统称为启动子。启动子是在肿瘤细胞中有活性的启动子。优选的启动子是cmv启动子、sv40启动子或管家基因启动子例如pgk启动子。表达控制序列也可以是内源性病毒启动子,例如腺病毒血清型5的内源性主要晚期启动子(mlp)。在这种情况下,编码序列可以例如通过与插入的剪接受体位点的选择性剪接可操作地连接到mlp,所述剪接受体位点类似于腺病毒血清型40长纤突(fiber)基因的剪接受体位点(carette等人,jgenemed.2005aug;7(8):1053-62)。
本发明提供了重组病毒,其包含含有与启动子可操作地连接的gsk3-β编码区的核酸分子。重组病毒优选是腺病毒(ad)、单纯疱疹病毒(hsv)、牛痘病毒、脊髓灰质炎病毒、呼肠孤病毒、水疱性口炎病毒(vsv)、塞姆利基森林病毒、塞内卡病毒(senecavirus)或马拉巴病毒(marabavirus)。该病毒优选是具有复制能力的病毒。具有复制能力的病毒,例如本文所述的重组的具有复制能力的腺病毒,可以在癌细胞中复制并裂解癌细胞。在本发明的上下文中的具有复制能力是指具有在容纳性细胞中复制的所有必需机构的病毒。使用腺病毒作为实例进一步例示复制能力。同样的原理适用于其它病毒。具有复制能力的腺病毒不需要包装细胞中另外的腺病毒蛋白的辅助。例如,e1缺失的复制缺陷型腺病毒需要反式提供e1蛋白以进行有效复制的互补细胞。许多具有复制能力的腺病毒在癌细胞中比在正常细胞中更有效地复制。对这种病毒的兴趣随着被修饰以增强癌细胞中优先复制的第一批重组腺病毒而增加。修饰包括对病毒基因组的修饰,使得腺病毒在正常细胞中而不是在癌细胞中有效复制所必需的一个或多个部分已经被修饰、去除或以其它方式工程化而不在正常细胞中表达。优先在癌细胞中复制的腺病毒也称为“溶瘤腺病毒”。本文所用的溶瘤腺病毒意指与非癌细胞相比优先杀伤癌细胞的腺病毒。在优选的实施方案中,本文所述的具有复制能力的腺病毒在病毒基因组中包含修饰,该修饰使得腺病毒能够在肿瘤细胞中优先复制。该修饰优选是病毒基因组中的突变。突变优选在e1a区域、e1b区域、e4-区域或者其一种或多种的组合中。许多溶瘤腺病毒在一个或多个这些区域中包含突变。根据本发明的腺病毒优选在e1a区域携带突变,优选涵盖e1a的cr2结构域的至少一部分,优选涵盖e1a的氨基酸122-129(ltcheagf)的缺失。这种缺失被称为delta-24缺失。具有指示的e1a-δ24突变的e1a的实例从seqidno:5的第1551位至第2512位指示。本文所用的术语“基因”或“区域”包括基因表达所需的完整基因组区域,包括例如增强子区域、启动子区域和内含子外显子序列。另一种能够在肿瘤细胞中优先复制的突变是消除蛋白质e1b-55k或至少其表达。e1b-55k使p53失活以在感染的细胞中诱导进入细胞周期的s期并防止细胞凋亡。e1b-55k突变的腺病毒被称为onyx-015。这种病毒已被用于治疗p53缺陷的肿瘤。具有前面提到的delta-24突变的腺病毒以不同的方式在肿瘤中实现选择性复制。delta-24突变影响e1a的保守区2(cr2)。该e1a区域介导与视网膜母细胞瘤(rb)家族的蛋白质的结合。prb蛋白阻断细胞周期的go/g1期向s期的转变,与e2f一起形成复合转录抑制剂。当e1a与prb结合时,prb-e2f复合物的e2f转录因子被释放,并且e2f充当负责移至s期的基因和病毒基因例如e2的转录激活因子。因此,e2f的释放是腺病毒复制的关键步骤。在肿瘤细胞中,细胞周期失控,因为prb不存在或通过过度磷酸化而失活,并且e2f是游离的。在这些细胞中,现在不需要通过e1a失活prb。因此,cr2突变的腺病毒在其中e2f游离的细胞例如许多癌细胞中繁殖,并且在具有功能性prb的正常细胞中复制效率低得多。
优先复制也可以通过用肿瘤选择性启动子替换病毒启动子来实现。在该实施方案中,修饰包括e1a或e1b的组织或细胞类型特异性表达的启动子。一个实例是其中e1a启动子被另一个启动子替换的修饰。已经将各种启动子用于该作用,例如甲胎蛋白启动子、前列腺特异性抗原(psa)启动子、激肽释放酶启动子、粘蛋白1启动子或骨钙蛋白启动子。这种腺病毒在(特别是)肿瘤细胞中更有效地复制,但由于替换启动子的不完全关闭,在正常细胞中也有一些复制。现今存在重组腺病毒,其中一个以上的早期区域启动子已被肿瘤细胞选择性启动子替换。各种病毒基因的调控可以用针对每种病毒基因的不同启动子进行,例如针对e1a的e2f1启动子和针对e4的端粒酶启动子。在这种情况下,两个启动子必须以合适的水平表达以允许病毒复制,使得溶瘤效力保留在许多肿瘤细胞中。可选地,两种病毒基因可以由相同的启动子调控,例如在溶瘤腺病毒onyx411中,其中e1a和e4由e2f1启动子调控。
在一些实施方案中,优先复制是通过用肿瘤选择性启动子替换用于复制必需病毒基因的病毒启动子来实现的。本发明的具体实施方案包括溶瘤腺病毒载体,其复制通过用e2f(例如e2f1)应答性启动子替换全部或部分e1a启动子而通过选择性表达腺病毒e1蛋白,优选e1a蛋白而被限制于具有失控p16/rb途径的细胞。在优选的实施方案中,e1a基因与e2f1启动子可操作地连接。优先复制也可以通过组合一种或多种用于实现选择性的不同手段来实现。优选的组合是调控具有delta-24突变的e1a基因的e2f1启动子(majem等人,cancergenether.2006jul;13(7):696-705以及alonso等人,cancerres.2007sep1;67(17):8255-63)。
在另一个方面,修饰包括在e3-区域中的核酸序列的突变或整个e3-区域的缺失。e3-区域的突变可以增强具有复制能力的腺病毒的溶瘤作用。一种这样的突变是e3-19k的内质网滞留结构域中的突变。已知e3-19k蛋白调控细胞膜上mhc-i的存在。该蛋白的一种功能涉及与mhc-i的结合,另一种功能涉及e3-19蛋白和与其结合的mhc-i在内质网中的滞留。e3-19k在细胞中的表达防止mhc-i向质膜的运送以及与mhc-i相关的抗原的呈递。因此,e3-19k的表达与对腺病毒感染的细胞的免疫应答降低相关。另一方面,发现e3-19k中防止其滞留在内质网中的突变可以增加腺病毒的溶瘤潜能。在一个实施方案中,本发明的腺病毒包含修饰的e3-区域。修饰可以是e3-区域的一个或多个部分或者全部的缺失。在一个实施方案中,修饰包括e3-19k蛋白的突变,其防止e3-19k在内质网中滞留。特别地,e3-19k的羧基末端结构域被消除或修饰以防止e3-19k在内质网中的滞留并引起其运送至质膜。复制并且含有e3-19k的这种特定突变的腺病毒被更有效地从感染的细胞中释放出来。这种较高的释放引起较高的溶瘤作用。这种增强的溶瘤作用可用于治疗癌症。e3-19k中的优选突变描述于wo2008/110579中,将其通过引用并入本文。合适的e3-突变在其中通过seqidno:1、2、4和5描述和例示。序列在本文中被重申为seqidno:1、2、3和4。本发明的复制型腺病毒优选表达带有具有seqidno4的羧基末端尾部的e3-19k。在本发明的另一个实施方案中,复制型腺病毒至少包含核苷酸序列seqidno:1、seqidno:5和seqidno:6。在一个实施方案中,本发明的复制型腺病毒表达带有具有seqidno:2的羧基末端尾部的e3-19k;并且在纤突蛋白中具有rgd基序的插入(由seqidno:6的第1648位至第1656位限定);以及赋予所述腺病毒在肿瘤细胞中的选择性复制的调控区,所述调控区由dm1绝缘子(由seqidno:5的第367位至第1095位限定)、e2f1启动子的片段(由seqidno:5的第1282位至第1545位限定)、ccacckozak序列(由seqidno:5的第1546位至第1550位限定)和腺病毒e1a-δ24突变基因(由seqidno:5的第1551位至第2512位限定)组成。本发明的另一个目的是在e3-19k的内质网滞留结构域中包含突变的复制型腺病毒,该突变防止e3-19k在内质网中滞留,其中所述腺病毒包含核苷酸序列seqidno:1。在本发明的另一个方面,所述复制型腺病毒表达带有具有seqidno:2的羧基末端尾部的e3-19k。在一个实施方案中,复制型腺病毒是如dong,w等人(2014,humangenetherapy25:897-904)所述的orca-10。gsk3β编码区优选作为cdna插入,如图5或图6所示。gsk3β优选是具有组成型活性的gsk3β。具有组成型活性的gsk3β优选是gsk3β,其中第9位的丝氨酸残基被另一个氨基酸残基替换。gsk3β突变体优选是s9a突变体,其中s是丝氨酸,a是丙氨酸。
根据本发明的腺病毒可以包含以下修饰:增加其复制潜能,诸如例如e3区域的保留(suzuki等人,clin.cancerres.8(2002):3348-3359)或e1b-19k基因的缺失(sauthoff等人,hum.genether.11(2000):379-388),或者增加对某种类型细胞的复制选择性,包括但不限于促进早期区域基因在癌细胞中选择性表达的修饰,或者降低或增强免疫原性(即,当引入动物体内时它们诱导免疫应答的潜能),诸如例如e1b区域的保留(wang等人,naturebiotechnol.21(2003):1328-1335)。
肿瘤疗法是基于选择性杀伤肿瘤细胞的药物和治疗。这种治疗的目的是尽可能多地保留正常的“健康”细胞。肿瘤细胞可能由于尤其由病毒的内部复制所引起的致细胞病变效应,由于另外引入的基因的表达,对肿瘤细胞的免疫应答和/或其它原因(例如但不限于与病毒相关的另外的毒素)而死亡。肿瘤的溶解被称为溶瘤。在肿瘤中选择性复制的腺病毒被称为溶瘤腺病毒。溶瘤腺病毒是具有复制能力的腺病毒,其已经被开发用于在癌细胞中优先复制。当病毒在所述癌细胞中的复制比在来源于与癌细胞来源相同的细胞类型的健康细胞中的复制快20%,优选30%、40%、50%、80%,更优选100%时,复制对于癌细胞是优选的。
本发明还提供了用于治疗个体中癌症的方法,其包括向有需要的个体施用重组的具有复制能力的腺病毒,所述腺病毒在其基因组中包含与表达控制序列可操作地连接的糖原合酶激酶-3(gsk3)蛋白的编码序列。
术语“癌症”是指恶性原发性和/或转移性癌症。癌症的实例包括但不限于癌;肉瘤、淋巴瘤、白血病、黑色素瘤或骨髓瘤。癌症优选是骨癌,脑癌,眼癌,乳腺癌,皮肤癌例如黑色素瘤,头颈鳞状细胞癌(hnscc),膀胱癌,肺癌,输尿管癌,尿道癌,甲状腺癌,甲状旁腺癌,唾液腺癌,肾癌,前列腺癌,生殖系统癌(包括宫颈癌、卵巢癌和睾丸癌),子宫内膜癌,血液/血液系统癌症或者胃肠组织中的癌症例如结肠癌。在优选的实施方案中,所述癌症是前列腺癌、皮肤癌、肺癌或胰腺癌。宿主细胞优选是癌细胞。癌细胞优选是恶性原发性和/或转移性癌细胞。癌症细胞(cancercell)可以是癌细胞(carcinomacell);肉瘤细胞、淋巴瘤细胞、白血病细胞、黑色素瘤细胞或骨髓瘤细胞。癌细胞也可以是骨癌细胞、脑癌细胞、眼癌细胞、乳腺癌细胞、皮肤癌细胞例如黑色素瘤细胞、或hnscc细胞、膀胱癌细胞、肺癌细胞、输尿管癌细胞、尿道癌细胞、甲状腺癌细胞、甲状旁腺癌细胞、唾液腺癌细胞、肾癌细胞、前列腺癌细胞、生殖系统癌细胞(包括卵巢癌细胞和睾丸癌细胞)、子宫内膜癌细胞、血液/血液系统癌细胞或者胃肠组织中的癌细胞。肿瘤通常包括癌细胞和支持细胞,例如基质细胞、血管细胞、血液和/或免疫细胞。术语“癌细胞”是指癌性细胞而不是支持细胞。具有复制能力的腺病毒也可以在支持细胞中感染和复制。术语“肿瘤”和“癌症”在本文中可互换使用。
癌细胞优选是不表达或不过表达gsk3的癌细胞。不表达或不过表达的gsk3优选是gsk3β。
优选地,本发明的腺病毒中的gsk编码区包含具有组成型活性的gsk3。具有组成型活性的gsk3优选是在gsk3α的位置s21或gsk3β的位置s9具有活化突变的突变体。活化突变优选是在指示位置用丙氨酸残基的密码子替换丝氨酸残基(分别在第21位或第9位)的密码子。
本发明还提供了用于提高重组的具有复制能力的腺病毒在容纳性细胞中的复制速率的方法,其包括向所述腺病毒的基因组提供与表达控制序列可操作地连接的gsk3蛋白的编码序列,用于在所述细胞中表达所述编码序列。复制速率的度量是腺病毒感染细胞表现出致细胞病变效应(cpe)所花费的时间。复制速率也可以通过测量感染后某一时间产生的感染性颗粒的数量来测量。复制速率通常相对于另一种腺病毒进行评估。当两种不同的病毒在其它情况相同的情况下并行测试时,显示产生的感染性病毒颗粒数量最快增加或cpe最快诱导的病毒具有更高的复制速率。如果细胞支持如本文所述的具有复制能力的腺病毒的复制,则它是容纳性细胞。
本发明还提供了用于增加溶瘤性重组的具有复制能力的腺病毒的溶瘤特性的方法,其包括向所述腺病毒的基因组提供与表达控制序列可操作地连接的gsk3蛋白的编码序列,用于表达所述编码序列。
本发明还提供了增加重组的具有复制能力的腺病毒在肿瘤中的复制速率和扩散的方法,所述方法包括向溶瘤腺病毒提供与表达控制序列可操作地连接的gsk3蛋白的编码序列,用于在所述肿瘤的细胞中表达所述编码序列。
本文所述的腺病毒可以具有一个或多个用于其它转基因的编码区。合适的其它转基因的实例是il2、gm-csf和tnf-α。其它合适的转基因在本文别处描述。
人类腺病毒目前可以细分为7种(a至g)和57种不同的(血清)型。
不同的血清型目前分类如下:
-种类a:血清型12、18、31;
-种类b:血清型3、7、11、14、16、21、34、35、50、55;
-种类c:血清型1、2、5、6、57;
-种类d:血清型8-10、13、15、17、19、20、22-30、32、33、36-39、42-49、51、53、54、56;
-种类e:血清型4;
-种类f:血清型40、41;以及
-种类g:血清型52
本发明的腺病毒优选是b、c或d腺病毒,优选b或c腺病毒。腺病毒优选是种类c腺病毒。腺病毒优选是血清型1、2、3、5、6、7、8、9、10、11、13、14、15、16、17、19、20、21、22-30、32、33、34、35、36-39、42-49、50、51、53、54、55、56或57的腺病毒。在优选的实施方案中,腺病毒是血清型1、2、3、5、6、7、11、14、16、21、34、35、50、55或57的腺病毒。腺病毒优选是血清型1、2、5、6或57的腺病毒,优选血清型2或5的腺病毒。不难产生含有来自一种腺病毒血清型的一部分和来自另一血清型的另一部分的嵌合腺病毒。已知含有相同种类的血清型部分的嵌合腺病毒,例如嵌合血清型2和5病毒。也考虑含有一种血清型的早期基因和另一种血清型的晚期基因的嵌合病毒。含有嵌合腺病毒蛋白的腺病毒也是已知的。例如,murakami等人(2010,prostatevol70(4):pp362-376)中描述了嵌合腺病毒纤突蛋白,其中腺病毒-5病毒的纤突轴(fibershaft)和knob结构域被来自腺病毒-3、腺病毒-11或腺病毒-35的相应结构域遗传替换。与腺病毒-5相比时,这些特定的嵌合腺病毒具有修饰的靶细胞向性。
所述腺病毒优选是基于腺病毒血清型5的病毒、基于腺病毒血清型24的病毒、基于腺病毒血清型35的病毒、或基于腺病毒血清型51的病毒、或嵌合腺病毒,例如通过用血清型35的纤突的一部分替换血清型5的纤突的一部分,基于血清型5以及血清型35的向性。所述腺病毒还可以提供治疗性转基因的表达,例如优选p53、肿瘤抗原,或分泌的蛋白,例如生长因子、细胞因子或趋化因子。所述腺病毒是具有复制能力的,特别是溶瘤的。所述腺病毒是用于在人类和灵长类动物细胞中感染和复制的人类或灵长类动物腺病毒。所述腺病毒是另一种哺乳动物腺病毒,例如分别用于狗细胞或马细胞的感染和复制的犬科动物或马科动物腺病毒。
根据本发明的优选的腺病毒是人类腺病毒,优选血清型5的人类腺病毒。
具有复制能力的腺病毒可以在动物体内的许多不同细胞中复制,条件是它们衍生自具有正确物种向性的腺病毒,并且所述细胞表达所述腺病毒的表面受体。如本领域技术人员已知的,重组腺病毒(包括具有复制能力的腺病毒)的特异性细胞表面识别可以通过假型化或靶向来改变。
本发明还提供了根据本发明的腺病毒,其用作药物。本发明还提供了根据本发明的腺病毒,其用作用于治疗癌症的药物。根据腺病毒学和腺病毒载体领域中的标准方法繁殖腺病毒。优选的繁殖方法是感染允许腺病毒复制的合适的细胞系。用于产生腺病毒的方法的一个实例还可以包括当它们显示细胞病变效应时收集细胞的步骤,所述细胞病变效应指示病毒的产生和细胞的冻融以产生细胞提取物。可以使用标准技术从细胞提取物中纯化病毒,例如在氯化铯梯度上显带和例如针对磷酸盐-缓冲盐水-10%甘油的透析。cscl的替代物是vivapure病毒纯化试剂盒(sartorius)。透析和/或纯化的病毒可以等分并储存在-80℃。根据标准方案进行噬斑形成腺病毒颗粒和单位的数量的定量。含有10%甘油的盐水磷酸盐缓冲液是用于储存腺病毒的标准制剂。
可以将腺病毒施用至动物或人体以体内感染细胞。施用可以通过几种途径进行,包括但不限于局部注射到肿瘤或肿瘤所处的体腔中,注射到血液循环中,吸入和施加到某一身体区域的表面。感染后,具有复制能力的腺病毒可以复制并扩散至其它细胞,条件是感染的细胞支持所述重组腺病毒的复制。因此,具有复制能力的腺病毒可以用于再感染新细胞以进一步繁殖和扩增所述具有复制能力的腺病毒。
优选将腺病毒配制到用于保存可以直接施用至有机体的病毒颗粒的水性或溶液介质中。制剂优选包含药学上可接受的盐和赋形剂,诸如例如人类血清白蛋白、糖(例如蔗糖和甘露糖醇)和/或表面活性剂(诸如例如以伯羟基为末端的双官能嵌段共聚物表面活性剂(pluronicf68tm)。
在一个实施方案中,根据本发明的具有复制能力的腺病毒还可以包含一个或多个表达盒,所述表达盒介导一种或多种小的或非蛋白编码rna分子例如mirna或shrna的表达。小的或非蛋白编码rna分子可以对细胞中p53途径的p53拮抗剂和/或抑制剂或其组合具有特异性。
先前,我们发现,通过恢复感染的癌细胞中的p53功能,可以加速腺病毒后代从所述癌细胞中的溶瘤和释放(vanbeusechem等人,cancerres.62(2002):6165-6171;wo03/057892,在此通过引用并入)。所述p53功能的恢复通过在所述癌细胞中表达恢复因子,即p53依赖性凋亡途径的功能因子来完成,关于所述功能在所述癌细胞中不表达或不充分表达,其中所述恢复因子优选包含蛋白质(wo03/057892)。因此,所述恢复因子是p53依赖性凋亡途径的必需阳性成分。
p53的正常功能的丧失与对程序性细胞死亡、体外细胞转化和体内癌症的发展的抵抗力有关。在约50%的人类癌症中,编码p53的基因通过缺失或突变是非功能性的(levine等人,nature351(1991):453-456;hollstein等人,science253(1991):49-53;chang等人,j.clin.oncol.13(1995):1009-1022)。在许多其它确实表达野生型p53蛋白的50%的癌细胞中,p53的功能仍然受到p53拮抗剂作用的阻碍。p53拮抗剂的一个实例是mdm2。肿瘤抑制蛋白p14arf的丧失或mdm2蛋白的过表达可以通过结合mdm2蛋白和随后的降解而导致p53的功能性失活。另外,即使p53的功能本身是完整的,p53依赖性细胞死亡也可能由于作用于p53下游的p53途径的抗凋亡蛋白,例如抗凋亡bcl-2及iap家族成员和bi-1的过表达而受到阻碍。另一个实例是p73deltan,其与p53竞争结合p53应答性启动子,从而拮抗p53依赖性细胞死亡(kartasheva等人,oncogene21(2002):4715-4727)。在细胞中对p53途径的一种或多种p53拮抗剂和/或抑制剂或其组合具有特异性的一种或多种rnai介导分子的表达将增强包含功能性p53的靶细胞中的溶原活性。
所述p53途径的拮抗剂和/或抑制剂优选地选自synoviolin、mdm2、pirh2、cop1、bruce、hpv-e6、疱疹病毒-8lana、parc、致死蛋白(mortalin)、plk-1、bi-1、p73deltan、bcl-2、bcl-xl、bcl-w、bfl-1、brag-1、mcl-1、ciap1、ciap2、ciap3、xiap和存活素。表达盒还包含在所述宿主细胞中起作用的一个或多个表达控制序列,例如与一个或多个rnai介导的分子可操作地连接的增强子/启动子和终止子。作为替代方案,p53途径的一种或多种p53拮抗剂和/或抑制剂或其组合的表达与控制元件可操作地连接,所述控制元件介导编码在减少宿主细胞中靶基因的表达中起作用的沉默因子的至少一种dna序列的表达。已经发现癌细胞可以含有p53途径的一种以上的p53拮抗剂和/或抑制剂。当通过针对p53途径的那些p53拮抗剂和/或抑制剂中的至少两种的rnai提供此类细胞时,它们被更有效地裂解。
在另一个实施方案中,根据本发明的具有复制能力的腺病毒还包含与在宿主细胞中起作用的一个或多个表达控制元件可操作地连接的dna序列,该dna序列编码在恢复宿主细胞中p53依赖性凋亡途径中起作用的至少一种恢复因子。所述恢复因子优选地选自bcl-2家族的促凋亡死亡基因,例如bax、bak、bad、bid、bik、bim、bok、blk、hrk、puma、noxa和bcl-xs(miyashita和reed,cell80(1995):293-299;han等人,genesdev.10(1996):461-477;zoernig等人,biochim.biophys.acta1551(2001):f1-f37)和/或p53、或其功能部分或衍生物。在恢复p53依赖性凋亡途径中起作用的优选的恢复因子是p53。
具有复制能力的腺病毒还可以包含编码沉默因子的dna序列,所述沉默因子在降低癌细胞中pot1的表达和/或活性中起作用。沉默因子优选是反义rna,例如rnai或剪接调节寡核苷酸。本领域技术人员能够设计合适的基于rna的沉默因子以降低癌细胞中pot1的表达。在pot1的情况下,优选的是癌症和/或癌细胞是前列腺癌。进一步优选的是,前列腺癌的治疗还包括照射所述癌症。
病毒载体是复制缺陷的并且需要包装细胞来提供互补基因以允许复制。
本文所用的腺病毒基因组意指编码与腺病毒的功能/生命周期相关的结构蛋白和元件的dna序列。
如本文所定义的具有复制能力的腺病毒是包含要在宿主细胞发挥复制功能的作为宿主细胞基因组的一部分的腺病毒,其中复制依赖于与宿主细胞的内源性细胞机构组合的病毒提供的复制功能。因此,宿主细胞的基因组不需要具有病毒复制所必需的外源序列编码因子。术语“内源的”在这方面意指病毒复制所必需的细胞机构(因此包括编码序列)是天然存在的机构,例如不是通过人工操作技术引入细胞中。后者被定义为“外源的”。如所定义的,复制功能是病毒在宿主细胞中复制所必需的由病毒编码的因子,例如蛋白质,并且在本文中也称为病毒复制因子。重要的是要注意这些因子由病毒基因组编码并且不需要外源因子补充。因此,复制依赖于病毒中缺失但被引入宿主细胞中的一种或多种复制功能的病毒被定义为复制缺陷的,因此不是本发明的一部分。所要求保护的本发明涉及具有复制能力的病毒,即其中编码病毒复制因子的病毒基因存在于病毒基因组上,所述病毒复制因子对于调节病毒在宿主细胞中的复制是必需的。宿主细胞通常是癌细胞或癌症样细胞。
为了清楚和简明的目的,描述特征在本文被描述为相同或单独实施方案的一部分,然而,应理解,本发明的范围可以包括具有所描述的所有或一些特征的组合的实施方案。
附图简述
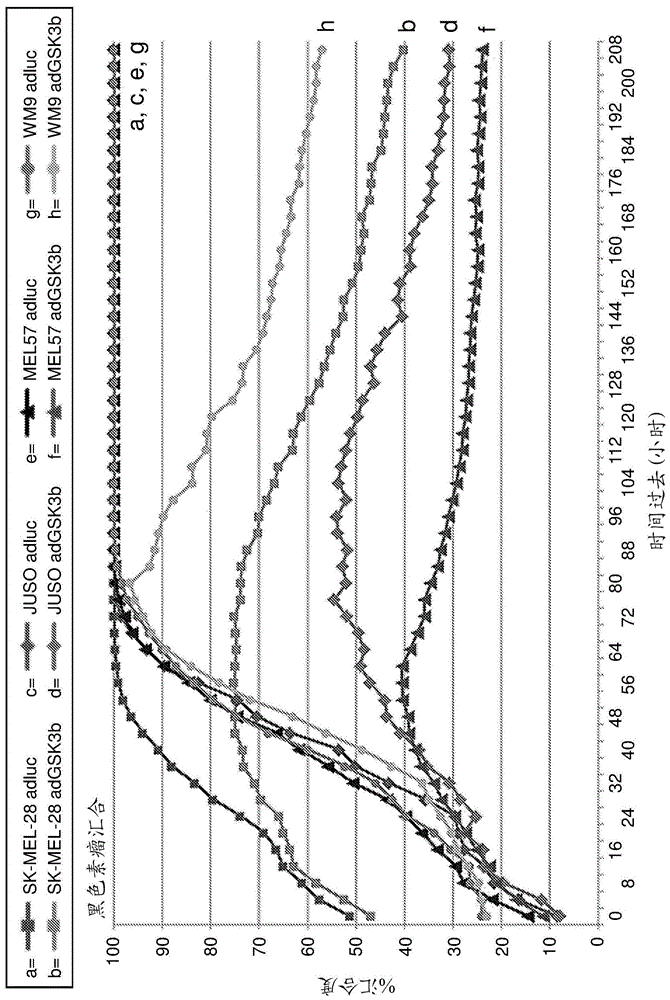
图1:表达gsk3-β的腺病毒在体外抑制人类癌细胞的生长,但在体外不抑制原代非恶性人类细胞的生长。图1a:表达gsk3-β的腺病毒在体外抑制癌细胞增殖。表达gsk3-β的腺病毒(adgsk3b)抑制4种黑色素瘤细胞系(sk-mel-28、juso、mel57和wm9)的生长。使用表达荧光素酶的腺病毒(adluc)作为对照。感染细胞,然后培养8天;通过incucyte每4小时拍摄孔的照片。图1b:gsk3-β表达不影响正常原代成纤维细胞的生长。表达gsk3-β的腺病毒不抑制未转化的原代人类成纤维细胞的生长。作为对照,取癌细胞系juso,其生长被抑制。图1c:在用ad.luc或ad.ca.gsk3-β感染之后第6天原代成纤维细胞的照片。
图2:通过用ad.ca.gsk3-β转导诱导不同黑色素瘤细胞系的细胞凋亡。图2a:用ad.ca.gsk3-β感染的癌细胞在第1天明显受到影响,更圆的表型指示细胞死亡的开始。在第3天,半胱天冬酶3/7阳性细胞(绿色)的数量增加。在第6天,具有ad.ca.gsk3b的癌细胞对于凋亡标志物大部分是阳性的,而用对照病毒转导的癌细胞几乎没有显示任何凋亡细胞。sk-mel-28细胞系数据作为实例示出。图2b:在不同时间点不同黑色素瘤细胞系的相对凋亡,比较用ad.luc对比用ad.ca.gsk3-β转导的细胞的效果。ad.ca.gsk3-β比ad.luc更早地诱导凋亡,证明了用表达具有组成型活性形式的gsk3-β的腺病毒感染黑色素瘤细胞的溶瘤作用。
图3:表达gsk3-β的腺病毒在原发性黑色素瘤肿瘤悬液中选择性诱导癌细胞杀伤。
图4:gsk3-β的表达增强腺病毒复制。
图4a显示了未感染的911细胞及其生长动力学,在第3天达到汇合。图4b显示了用1moi的ad.luc感染的911细胞,其在第3天半(感染后84小时)具有完全细胞病变效应(cpe)。表达gsk3-β的腺病毒(ad.ca-gsk3-β)在感染后第1天具有完全的cpe(图4c)。
图5:dong等人所述的编码orca-10病毒的dna构建体的示意图(2014,humangenetherapy25:897-904)、包含在cmv启动子控制下的gsk3βs9a编码区的同源重组构建体的示意图以及包含具有在cmv启动子控制下的gsk3βs9a编码区的orca-10病毒的重组构建体的示意图。
图6:dong等人所述的编码orca-10病毒的dna构建体的示意图(2014,humangenetherapy25:897-904)、包含在sv40启动子控制下的gsk3βs9a编码区的同源重组构建体的示意图以及包含具有在sv40启动子控制下的gsk3βs9a编码区的orca-10病毒的重组构建体的示意图。
图7:dong等人所述的编码orca-10病毒的dna构建体的示意图(2014,humangenetherapy25:897-904)、包含在cmv启动子控制下的rluc编码区(荧光素酶编码区)的同源重组构建体的示意图以及包含具有在提及的cmv启动子控制下的rluc编码区的orca-10病毒的重组构建体的示意图。
实施例
在附图和实施例中,使用不同的名称来指示相同的病毒。具有gsk3-βs9a编码区的腺病毒被称为adgsk3b;ad.ca.gsk3-β;ad.ca.gsk3-β;和ad.ca.gsk3-βs9a等。具有参照荧光素酶编码区的腺病毒称为ad.luc;ad.luc和ad.luc等。
实施例1:表达gsk3-β的腺病毒在体外抑制人类癌细胞的生长,但不抑制原代非恶性人类细胞的生长。
为了评价表达gsk3-β的腺病毒对癌细胞和非恶性细胞的作用,我们培养了4种不同的黑色素瘤细胞系(sk-mel-28、juso、mel57和wm9)和从健康皮肤新分离的皮肤来源的原代成纤维细胞(fibro)。
将细胞在完全rpmi培养基(补充有10%热灭活的fcs(hyclone)、100iu/ml青霉素钠、100μg/ml链霉素,2mml-谷氨酰胺和50μmβ-巯基乙醇的rpmihepes和l-谷氨酰胺培养基(lonza))中培养。将细胞(sk-mel-28、juso、mel57、wm9或fibro)接种在96孔板中(每孔10000个细胞)。铺板后24小时,用500感染复数(moi)的ad.luc(ad5luc1,(ref17)krasnykh等人.j.ofvirology,75(2001):4176-4183)或ad.ca.gsk3-β(kim等人.(ref18)j.ofbio.chemistry,277(2002):41888–41896)感染细胞。将细胞在37℃和5%co2下在incucytezoom(essenbioscience)中孵育,然后培养8天。通过incucytezoom每4小时拍摄一次孔的照片。使用incucytezoom软件分析孔,通过软件应用汇合遮罩(confluencemask)以获得在不同测量时间点下每孔的汇合百分比。使用graphpadprism(graphpad)将汇合度数据绘制在图上。
通过使用adeno-x快速滴定试剂盒(bdclontech)滴定911细胞上的病毒来测定病毒的感染性滴度。500moi是指使用adeno-x快速滴定试剂盒通过病毒滴定测定的500个感染性病毒颗粒/个细胞。
结果显示,用表达gsk3-β的病毒感染的癌细胞生长受到抑制,并且在感染后3-4天之后细胞数量开始减少,表明细胞死亡(图1a)。相比之下,表达荧光素酶的病毒不抑制癌细胞的生长,并且孔在约4天时汇合。如图1b和1c所示,这是一种特异性的抗癌作用,因为原代人类成纤维细胞未被ad.ca.gsk3-β感染抑制生长。
总之,这些数据显示腺病毒实施的具有组成型活性形式的gsk-β的表达杀伤癌细胞,而它对原代成纤维细胞没有显示任何影响。
实施例2:通过ad.ca.gsk3-β转导诱导人类黑色素瘤细胞系的凋亡。
为了证明ad.ca.gsk3-β能够诱导癌细胞杀伤,将10.000个黑色素瘤细胞(sk-mel-28、juso、mel57或wm9)在完全rpmi培养基中铺板于96孔板中。铺板后24小时,按照制造商的程序,用500moi的ad.luc或ad.ca.gsk3-β以及1:1000fitc半胱天冬酶3/7试剂(incucyte)感染细胞。将细胞在37℃和5%co2下在incucytezoom中孵育8天。通过incucyte每4小时拍摄孔的照片。使用incucytezoom软件分析数据,通过软件应用汇合和绿色汇合遮罩以分别获得每孔的汇合百分比和孔中绿色信号的百分比。通过将绿色遮罩值除以在不同时间点的汇合值来确定凋亡细胞的分数。
在6天的时间内,与ad.luc感染的培养物相比,在ad.ca.gsk3-β感染的培养物中半胱天冬酶3/7阳性细胞(凋亡细胞)的百分比增加得更快(图2a和b)。在第1天,与对照病毒(ad.luc)相比,当用ad.ca.gsk3-β感染时,对sk-mel-28细胞的形态有明显的影响(图2a)。在第3天,在含有ad.ca.gsk3-β(用绿色标记表示)的培养物中可以观察到几种半胱天冬酶3/7阳性染色细胞。在第6天,用ad.ca.gsk3-β转导的sk-mel-28对于凋亡标志物大部分是阳性的,而用对照病毒转导的癌细胞几乎没有显示任何凋亡细胞。
这些数据显示腺病毒实施的具有组成型活性形式的gsk3-β的表达促进癌细胞的凋亡。
实施例3:表达gsk3-β的腺病毒在转移性黑色素瘤肿瘤悬液中诱导选择性癌细胞杀伤。
为了证明腺病毒递送的gsk3-β的抗肿瘤作用,用ad.luc或ad.ca.gsk3-β感染转移性黑色素瘤肿瘤细胞悬液。
从黑色素瘤患者获得活的肿瘤组织。然后用解剖刀切碎样品,并在含有0.1%dna酶i型和0.14%胶原酶i型(sigmachemical)的hbss(whittakerbioproducts)中解离。然后,将单细胞悬液用10%dmso以每毫升1.5至2千万个细胞的等分试样在受控速率冷冻器中冷冻,并储存在液氮中直至使用。
解冻黑色素瘤细胞悬液,将1.200.000个转移性黑色素瘤肿瘤细胞在完全rpmi培养基中培养在6孔板中,4小时后用500moi的ad.luc或ad.ca.gsk3-β感染。然后将细胞在37℃和5%co2下孵育5天。5天之后,收获样品(以1560rpm离心5分钟),用补充有0.1%牛血清白蛋白(bsa)和0.02%叠氮化钠的pbs以及含0.1%bsa的pbs(facs缓冲液)洗涤,并以1560rpm离心5分钟。接着,去除上清液,在约50微升上清液中留下细胞沉淀。将细胞重悬于剩余的上清液中,并在4℃下对表面标志物cd45(af700,biolegend)和mcsp(apc,miltenyibiotec)染色30分钟。孵育之后,通过用facs缓冲液洗涤去除过量的抗体。通过流式细胞仪fortessa(bdbioscience)和kaluza分析软件(beckman)分析样品。
该分析的结果显示在图3中。将细胞用cd45标志物染色,以区分肿瘤微环境中的黑色素瘤细胞和健康免疫细胞。免疫细胞(以紫色设门)是cd45阳性的,而肿瘤细胞是阴性的。另外,为了真正区分癌细胞和非免疫健康细胞(例如成纤维细胞),加入了mcsp标志物。mcsp是已知的黑色素瘤标志物,因此,黑色素瘤细胞将是mcsp+cd45-细胞(以橙色设门)。然而,重要的是注意到mcsp-cd45-细胞级分(以蓝色设门)可以包含非免疫健康细胞,但也许还包含一些不表达mcsp标志物的黑色素瘤细胞(不是所有黑色素瘤细胞对于相同标志物都是阳性的,并且在这方面存在供体可变性)。
当用ad.ca.gsk3-β转导黑色素瘤细胞悬液时,5天之后黑色素瘤细胞的相对百分比是1.72%。相比之下,在ad.luc感染的黑色素瘤悬液中,存活的黑色素瘤细胞的相对百分比是21.65%。此外,免疫细胞似乎不受ad.ca.gsk3-β存在的影响,在ad.luc的情况下,存活率是50.77%,在ad.ca.gsk3-β的情况下,存活率是64.29%,进一步证明了ad.ca.gsk3-β的肿瘤特异性。其它细胞(cd45-mcsp-,大多数是健康的非免疫细胞,如成纤维细胞)也不受用编码具有组成型活性的gsk3-β的腺病毒转导的影响。
结果显示利用具有组成型活性的gsk3-β的腺病毒递送以诱导特异性癌细胞杀伤的潜力。
实施例4:gsk3-β的表达增强腺病毒复制。
ad.ca.gsk3-β和ad.luc是复制缺陷型腺病毒载体。为了验证具有组成型活性的gsk3-β在具有复制能力的腺病毒的情况中的作用,进行了在911细胞(补充复制缺陷型腺病毒用于腺病毒复制的细胞系)中的实验(图4)。在911细胞(补充腺病毒复制的细胞系)中扩增复制缺陷型ad.luc或ad.ca.gsk3-β。将911细胞(fallauxfj等人.humgenether.,(1992):215-22)在完全rpmi中培养。在第1天,将911细胞铺板在96孔板(10000个细胞/孔)中,6小时后用moi1的ad.luc或ad.ca.gsk3-β感染。作为阴性感染对照,使用未感染的911细胞。将细胞在37℃和5%co2下在incucytezoom中孵育,并随后孵育5天。通过incucyte以不同的间隔拍摄孔的照片。结果显示ad.luc在感染后约3天诱导可见的cpe(细胞病变效应)(图4b),而表达gsk3-β的病毒(ad.ca.gsk3-β)在第1天已经显示cpe(图4c),表明gsk3-β和具有复制能力的腺病毒的协同细胞毒性效应。在该实验中使用的moi是每个细胞1个感染性病毒颗粒(1moi)。因此,很可能不是所有的细胞都被来自接种物的病毒颗粒感染。与ad.ca.gsk3-β感染的细胞中缺乏细胞增殖一起,这表明具有组成型活性的gsk3-β的存在加速病毒复制或病毒释放,这是溶瘤病毒疗法的期望特征。
实施例5:构建表达gsk3-β的具有复制能力的腺病毒的方法。
在腺病毒基因组的e4与右侧itr之间含有gsk3b的具有复制能力的腺病毒可以如下进行不同的克隆步骤。制备携带gsk3b表达盒的腺病毒穿梭载体。在第二步中,将该穿梭载体线性化并与全长线性化腺病毒dna(例如orca-010;即,具有e1aδ24、t1突变和纤突rgd插入的溶瘤腺病毒)重组。gsk3-βdna序列将在c-末端区域含有第9位的丝氨酸至丙氨酸的突变和ha(血凝素)标签序列。
gsk3-β表达盒
gsk3-β表达盒含有以下序列。通过dna合成(geneartgenesynthesis,thermofisherscientific)产生表达盒。使用ecori限制位点将表达盒克隆到pmk克隆载体(thermofisherscientific)中。
cmv-gsk3-βha-pa
ecori位点
gaattc-
spei位点
actagt–
cmv增强子
gacattgattattgacagttattaatagtaatcaattacggggtcattagttcatagcccatatatggagttccgcgttacataacttacggtaaatggcccgcctggctgaccgcccaacgacccccgcccattgacgtcaataatgacgtatgttcccatagtaacgccaatagggactttccattgacgtcaatgggtggactatttacggtaaactgcccacttggcagtacatcaagtgtatcatatgccaagtacgccccctattgacgtcaatgacggtaaatggcccgcctggcattatgcccagtacatgaccttatgggactttcctacttggcagtacatctacgtattagtcatcgctattaccatg-
cmv启动子
gtgatgcggttttggcagtacatcaatgggcgtggatagcggtttgactcacggggatttccaagtctccaccccattgacgtcaatgggagtttgttttggcaccaaaatcaacgggactttccaaaatgtcgtaacaactccgccccattgacgcaaatgggcggtaggcgtgtacggtgggaggtctatataagcagagct-
含i-ceui限制位点的序列
cgtaactataacggtcctaaggtagcgaaa-
ha标记的gsk3β序列(以斜体和下划线表示的ha-标签序列)
polya
tggatccagacatgataagatacattgatgagtttggacaaaccacaactagaatgcagtgaaaaaaatgctttatttgtgaaatttgtgatgctattgctttatttgtaaccattataagctgcaataaacaagttaacaacaacaattgcattcattttatgtttcaggttcagggggaggtgtgggaggttttttaaagcaagtaaaacctctacaaatgtgatatggctgat-
spei位点
actagt
ecori位点
gaattc-
携带gsk3-β表达盒构建体的穿梭载体
作为穿梭载体骨架,将使用pendk/spel载体(由dr.r.alemany,institutcatalad'oncologia,barcelona,spain提供)。通过kpni消化载体ptg3602(chartier等人,j.virol,70(1996):4805-4810)和再连接包含ad5图谱单元0-7和93-100的载体片段以产生pendk来制备pendk/spel。通过定点诱变将ad5核苷酸35813从a改变为t将spei位点引入pendk以产生pendk/spei。pendk/spei携带两个ad5itr侧翼的paci限制位点。
使用spei限制位点将通过dna合成产生的gsk3-β表达盒克隆到pendk/spei中,得到pendk/spei-gsk3β。正确的pendk/spei-gsk3-β克隆可以通过使用载体中存在的不同限制酶(例如i-ceui独特的限制位点)进行限制分析来鉴定。
重组产生携带gsk3-β的全长腺病毒基因组
用kpni使质粒pendk/spei-gsk3β线性化。线性化的质粒可以在细菌(例如bj5183)或酵母(例如yph857)中与全长的具有复制能力的腺病毒dna(例如orca-010)重组。
全长腺病毒dna可以从腺病毒颗粒中分离,或者可选地可以通过限制酶消化从携带全长腺病毒dna插入物的质粒中释放。
同源重组产生具有全长腺病毒基因组的质粒,其中gsk3-β表达盒插入e4区与右侧itr之间。应注意,根据该方法,任何具有复制能力的腺病毒都可以用于插入gsk3b表达盒中,包括具有另外修饰的重组腺病毒,诸如例如e3缺失的、增强的肿瘤选择性或溶瘤潜能,改变的向性或转基因插入。然而,优选的是所述全长的具有复制能力的腺病毒基因组在其基因组中不包括paci限制位点。
病毒产生
随后通过paci消化将具有插入的gsk3b表达盒的具有复制能力的腺病毒基因组从质粒中释放出来。使用例如lipofectamine试剂将该dna转染到在补充有10%fbs(hyclone)和100u/mlpen/strep的杜尔伯克氏改良伊格尔培养基(dulbecco’smodifiedeaglemedium)中培养的人类细胞,例如a549中。根据本领域已知的标准细胞培养和病毒学方法,分离、进一步繁殖和纯化根据本发明的所得的重组的具有复制能力的腺病毒。
实施例6:构建表达gsk3-β的具有复制能力的腺病毒的方法。
类似于实施例5,其中gsk3-β表达盒具有以下序列。
sv40-gsk3-βha-pa
ecori位点
gaattc-
spei位点
actagt–
sv40启动子
ggtgtggaaagtccccaggctccccagcaggcagaagtatgcaaagcatgcatctcaattagtcagcaaccaggtgtggaaagtccccaggctccccagcaggcagaagtatgcaaagcatgcatctcaattagtcagcaaccatagtcccgcccctaactccgcccatcccgcccctaactccgcccagttccgcccattctccgccccatggctgactaattttttttatttatgcagaggccgaggccgcctcggcctctgagctattccagaagtagtgaggaggcttttttggaggcctaggcttttgcaaa–
含有i-ceui限制位点的序列
cgtaactataacggtcctaaggtagcgaaa-
ha标记的gsk3β序列(以斜体和下划线表示的ha-标签序列)
polya
tggatccagacatgataagatacattgatgagtttggacaaaccacaactagaatgcagtgaaaaaaatgctttatttgtgaaatttgtgatgctattgctttatttgtaaccattataagctgcaataaacaagttaacaacaacaattgcattcattttatgtttcaggttcagggggaggtgtgggaggttttttaaagcaagtaaaacctctacaaatgtgatatggctgat-
spei位点
actagt
ecori位点
gaattc-
实施例7:构建表达荧光素酶的具有复制能力的腺病毒的方法。
作为对照,可以制备条件性表达具有复制能力的溶瘤腺病毒的荧光素酶。方法类似于实施例5或6,其中表达盒中的dna合成的ha标记的gsk3-β序列已经被以下荧光素酶序列替换。
海肾荧光素酶序列
atgacttcgaaagtttatgatccagaacaaaggaaacggatgataactggtccgcagtggtgggccagatgtaaacaaatgaatgttcttgattcatttattaattattatgattcagaaaaacatgcagaaaatgctgttatttttttacatggtaacgcggcctcttcttatttatggcgacatgttgtgccacatattgagccagtagcgcggtgtattataccagaccttattggtatgggcaaatcaggcaaatctggtaatggttcttataggttacttgatcattacaaatatcttactgcatggtttgaacttcttaatttaccaaagaagatcatttttgtcggccatgattggggtgcttgtttggcattttattatagctatgagcatcaagataagatcaaagcaatagttcacgctgaaagtgtagtagatgtgattgaatcatgggatgaatggcctgatattgaagaagatattgcgttgatcaaatctgaagaaggagaaaaaatggttttggagaataacttcttcgtggaaaccatgttgccatcaaaaatcatgagaaagttagaaccagaagaatttgcagcatatcttgaaccattcaaagagaaaggtgaagttcgtcgtccaacattatcatggcctcgtgaaatcccgttagtaaaaggtggtaaacctgacgttgtacaaattgttaggaattataatgcttatctacgtgcaagtgatgatttaccaaaaatgtttattgaatcggacccaggattcttttccaatgctattgttgaaggtgccaagaagtttcctaatactgaatttgtcaaagtaaaaggtcttcatttttcgcaagaagatgcacctgatgaaatgggaaaatatatcaaatcgttcgttgagcgagttctcaaaaatgaacaataa
实施例8:评价表达gsk3-β的具有复制能力的腺病毒的溶瘤效力的方法。
将实施例5和6中产生的表达gsk3-β的具有复制能力的腺病毒的溶瘤效力与其相关对照(基于启动子),即实施例7中产生的表达荧光素酶的具有复制能力的腺病毒进行比较。可选地,也可以使用在cmv或sv40启动子下表达荧光素酶的其它已经条件性可用的具有复制能力的全长腺病毒。
为了比较不同病毒的溶瘤效力,将进行人类癌细胞系的细胞毒性测定。不同的癌细胞系可以用于测定(例如hep3b、a549、u2os、hct116、sk-mel-28、um-scc-22a、lncap、np9、du-145、um-scc-11b、um-scc-14c、pc-3、vu1131、mda-mb-231和/或fadu)。细胞毒性测定将使用实施例5、6和7中产生的病毒根据dong等人(humangenetherapy25(2014):897–904)进行。
这项工作部分地由欧盟地平线2020研究与创新计划(europeanunionhorizon2020researchandinnovationprogramme),玛丽·居里(marie-sklodowska-curie)基金号643130资助。
引用的文献
1.beurele,griecosf,jopers.2015.glycogensynthasekinase-3(gsk-3):regulation,actions,anddiseases.pharmacolther148:114-31
2.domotot,pykoiv,furutat,miyashitak,ueharam,shimasakit,nakadam,minamotot.2016.glycogensynthasekinase-3betaisapivotalmediatorofcancerinvasionandresistancetotherapy.cancersci107:1363-72
3.stamosjl,chuml,enosmd,shahn,weiswi.2014.structuralbasisofgsk-3inhibitionbyn-terminalphosphorylationandbythewntreceptorlrp6.elife3:e01998
4.goca,al-huseinb,katsanevask,steinbacha,louu,sabbinenih,deremerdl,somanathpr.2014.targetingsrc-mediatedtyr216phosphorylationandactivationofgsk-3inprostatecancercellsinhibitprostatecancerprogressioninvitroandinvivo.oncotarget5:775-87
5.naginis,sophiaj,mishrar.2018.glycogensynthasekinases:moonlightingproteinswiththeranosticpotentialincancer.semincancerbiol
6.lich,liucw,tsaich,pengyj,yangyh,liaopl,leecc,chengyw,kangjj.2017.cytoplasmicarylhydrocarbonreceptorregulatesglycogensynthasekinase3beta,acceleratesvimentindegradation,andsuppressesepithelial-mesenchymaltransitioninnon-smallcelllungcancercells.archtoxicol91:2165-78
7.pramanikkk,singhak,alamm,kashyapt,mishrap,pandaak,deyrk,ranaa,naginis,mishrar.2016.reversion-inducingcysteine-richproteinwithkazalmotifsanditsregulationbyglycogensynthasekinase3signalinginoralcancer.tumourbiol37:15253-64
8.yul,lix,lih,chenh,liuh.2016.rab11asustainsgsk-3beta/wnt/beta-cateninsignalingtoenhancecancerprogressioninpancreaticcancer.tumourbiol37:13821-9
9.furutat,sabith,dongy,miyashitak,kinoshitam,uchiyaman,hayashiy,minamotot,nakadam.2017.biologicalbasisandclinicalstudyofglycogensynthasekinase-3beta-targetedtherapybydrugrepositioningforglioblastoma.oncotarget8:22811-24
10.garceag,mansonmm,nealcp,pattendencj,suttoncd,dennisonar,berrydp.2007.glycogensynthasekinase-3beta;anewtargetinpancreaticcancer?currcancerdrugtargets7:209-15
11.mac,wangj,gaoy,gaotw,cheng,bowerka,odetallahm,dingm,kez,luoj.2007.theroleofglycogensynthasekinase3betainthetransformationofepidermalcells.cancerres67:7756-64
12.faragom,dominguezi,landesman-bollage,xux,rosnera,cardiffrd,seldindc.2005.kinase-inactiveglycogensynthasekinase3betapromoteswntsignalingandmammarytumorigenesis.cancerres65:5792-801
13.mishrar,naginis,ranaa.2015.expressionandinactivationofglycogensynthasekinase3alpha/betaandtheirassociationwiththeexpressionofcyclind1andp53inoralsquamouscellcarcinomaprogression.molcancer14:20
14.zhouw,wangl,gousm,wangtl,zhangm,liut,wangcy.2012.shrnasilencingglycogensynthasekinase-3betainhibitstumorgrowthandangiogenesisinpancreaticcancer.cancerlett316:178-86
15.shakooria,maiw,miyashitak,yasumotok,takahashiy,ooia,kawakamik,minamotot.2007.inhibitionofgsk-3betaactivityattenuatesproliferationofhumancoloncancercellsinrodents.cancersci98:1388-93
16.kingwellk.2018.flippingtheswitchforselectivegsk-3inhibition.naturereviewsdrugdiscovery17:314
17.krasnykhv.,belousovan.,korokhovn.,mikheevag.,curield.t.genetictargetingofanadenovirusvectorviareplacementofthefiberproteinwiththephaget4fibritin.j.ofvirology.,75:4176-4183,2001.
18.kimh.s.,skurkc.,thomass.r.,bialika.,suharat.,kureishiy.,birnbaumm.,keaneyj.f.regulationofangiogenesisbyglycogensynthasekinase-3.j.ofbiologicalchemistry,277:41888–41896,2002.
一些序列
序列表
<110>奥尔卡治疗有限公司(orcatherapeuticsb.v.)
<120>包含糖原合酶激酶-3(gsk3)编码区的重组的具有复制能力的病毒和杀伤异常细胞的方法
<130>p120105pc00
<150>ep18192104.0
<151>2018-08-31
<160>16
<170>patentinversion3.5
<210>1
<211>484
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>人类腺病毒血清型5的蛋白e3-19k的编码区的突变体
<400>1
atgattaggtacataatcctaggtttactcacccttgcgtcagcccacggtaccacccaa60
aaggtggattttaaggagccagcctgtaatgttacattcgcagctgaagctaatgagtgc120
accactcttataaaatgcaccacagaacatgaaaagctgcttattcgccacaaaaacaaa180
attggcaagtatgctgtttatgctatttggcagccaggtgacactacagagtataatgtt240
acagttttccagggtaaaagtcataaaacttttatgtatacttttccattttatgaaatg300
tgcgacattaccatgtacatgagcaaacagtataagttgtggcccccacaaaattgtgtg360
gaaaacactggcactttctgctgcactgctatgctaattacagtgctcgctttggtctgt420
accctactctatattaaatacaaaaagcagacgcagctttattgaggaaaagaaaatgcc480
ttaa484
<210>2
<211>7
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>人类腺病毒5型的蛋白e3-19k的突变的羧基末端片段的片段
<400>2
lyslysglnthrglnleutyr
15
<210>3
<211>483
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>人类腺病毒5型的蛋白e3-19k的编码区的突变体
<400>3
atgattaggtacataatcctaggtttactcacccttgcgtcagcccacggtaccacccaa60
aaggtggattttaaggagccagcctgtaatgttacattcgcagctgaagctaatgagtgc120
accactcttataaaatgcaccacagaacatgaaaagctgcttattcgccacaaaaacaaa180
attggcaagtatgctgtttatgctatttggcagccaggtgacactacagagtataatgtt240
acagttttccagggtaaaagtcataaaacttttatgtatacttttccattttatgaaatg300
tgcgacattaccatgtacatgagcaaacagtataagttgtggcccccacaaaattgtgtg360
gaaaacactggcactttctgctgcactgctatgctaattacagtgctcgctttggtctgt420
accctactctatattaaatacaaaagcagacgcagctttattgaggaaagcagcatgcct480
taa483
<210>4
<211>13
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>人类腺病毒5型的蛋白e3-19k的突变的羧基末端片段的片段
<400>4
lysserargargserproilegluglusersermetpro
1510
<210>5
<211>2512
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>具有调控区dm1绝缘子(从第367位至第1095位);e2f1启动子的片段(从第1282位至第1545位);
ccacckozak序列(从第1546位至第1550位);和e1a-24基因(从第1551位至第2512位)的序列
<400>5
catcatcaattataccttccattttggattgaagccaatatgataatgagggggtggagt60
ttgtgacgtggcgcggggcgtgggaacggggcgggtgacgtagtagtgtggcggaagtgt120
gatgttgcaagtgtggcggaacacatgtaagcgacggatgtggcaaaagtgacgtttttg180
gtgtgcgccggtgtacacaggaagtgacaattttcgcgcggttttaggcggatgttgtag240
taaatttgggcgtaaccgagtaagatttggccattttcgcgggaaaactgaataagagga300
agtgaaatctgaataattttgtgttactcatagcgcgtaatctctagcatcgatgtcgag360
gatccctcgagaccctgaaactgtcttcgactccggggccccgttggaagactgagtgcc420
cggggcacggcacagaagccgcgcccaccgcctgccagttcacaaccgctccgagcgtgg480
gtctccgcccagctccagtcctgtgatccgggcccgccccctagcggccggggagggagg540
ggccgggtccgcggccggcgaacggggctcgaagggtccttgtagccgggaatgctgctg600
ctgctgctggggggatcacagaccatttctttctttcggccaggctgaggccctgacgtg660
gatgggcaaactgcaggcctgggaaggcagcaagccgggccgtccgtgttccatcctcca720
cgcacccccacctatcgttggttcgcaaagtgcaaagctttcttgtgcatgacgccctgc780
tctggggagcgtctggcgcgatctctgcctgcttactcgggaaatttgcttttgccaaac840
ccgctttttcggggatcccgcgcccccctcctcacttgcgctgctctcggagccccagcc900
ggctccgcccgcttcggcggtttggatatttattgacctcgtcctccgactcgctgacag960
gctacaggacccccaacaaccccaatccacgttttggatgcactgagaccccgacattcc1020
tcggtatttattgtctgtccccacctaggacccccacccccgaccctcgcgaataaaagg1080
ccctccatctgcccctcgagtctagagatggccgcaataaaatatctttattttcattac1140
atctgtgtgttggttttttgtgtgaatcgatagtactaacatacgctctccatcaaaaca1200
aaacgaaacaaaacaaactagcaaaataggctgtccccagtgcaagtgcaggtgccagaa1260
catttctctatcgataggtaccatccggacaaagcctgcgcgcgccccgccccgccattg1320
gccgtaccgccccgcgccgccgccccatctcgcccctcgccgccgggtccggcgcgttaa1380
agccaataggaaccgccgccgttgttcccgtcacggccggggcagccaattgtggcggcg1440
ctcggcggctcgtggctctttcgcggcaaaaaggatttggcgcgtaaaagtggccgggac1500
tttgcaggcagcggcggccgggggcggagcgggatcgagccctcgccaccatgagacata1560
ttatctgccacggaggtgttattaccgaagaaatggccgccagtcttttggaccagctga1620
tcgaagaggtactggctgataatcttccacctcctagccattttgaaccacctacccttc1680
acgaactgtatgatttagacgtgacggcccccgaagatcccaacgaggaggcggtttcgc1740
agatttttcccgactctgtaatgttggcggtgcaggaagggattgacttactcacttttc1800
cgccggcgcccggttctccggagccgcctcacctttcccggcagcccgagcagccggagc1860
agagagccttgggtccggtttctatgccaaaccttgtaccggaggtgatcgatccaccca1920
gtgacgacgaggatgaagagggtgaggagtttgtgttagattatgtggagcaccccgggc1980
acggttgcaggtcttgtcattatcaccggaggaatacgggggacccagatattatgtgtt2040
cgctttgctatatgaggacctgtggcatgtttgtctacagtaagtgaaaattatgggcag2100
tgggtgatagagtggtgggtttggtgtggtaattttttttttaatttttacagttttgtg2160
gtttaaagaattttgtattgtgatttttttaaaaggtcctgtgtctgaacctgagcctga2220
gcccgagccagaaccggagcctgcaagacctacccgccgtcctaaaatggcgcctgctat2280
cctgagacgcccgacatcacctgtgtctagagaatgcaatagtagtacggatagctgtga2340
ctccggtccttctaacacacctcctgagatacacccggtggtcccgctgtgccccattaa2400
accagttgccgtgagagttggtgggcgtcgccaggctgtggaatgtatcgaggacttgct2460
taacgagcctgggcaacctttggacttgagctgtaaacgccccaggccataa2512
<210>6
<211>1773
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>编码包含含有rgd基序(从1648至1656)的肽rgd(从第1639位至第1665位)的插入的人类腺病毒5型(从第1位至第1638位;
以及第1666位至第1773位)的纤突的序列
<400>6
atgaagcgcgcaagaccgtctgaagataccttcaaccccgtgtatccatatgacacggaa60
accggtcctccaactgtgccttttcttactcctccctttgtatcccccaatgggtttcaa120
gagagtccccctggggtactctctttgcgcctatccgaacctctagttacctccaatggc180
atgcttgcgctcaaaatgggcaacggcctctctctggacgaggccggcaaccttacctcc240
caaaatgtaaccactgtgagcccacctctcaaaaaaaccaagtcaaacataaacctggaa300
atatctgcacccctcacagttacctcagaagccctaactgtggctgccgccgcacctcta360
atggtcgcgggcaacacactcaccatgcaatcacaggccccgctaaccgtgcacgactcc420
aaacttagcattgccacccaaggacccctcacagtgtcagaaggaaagctagccctgcaa480
acatcaggccccctcaccaccaccgatagcagtacccttactatcactgcctcaccccct540
ctaactactgccactggtagcttgggcattgacttgaaagagcccatttatacacaaaat600
ggaaaactaggactaaagtacggggctcctttgcatgtaacagacgacctaaacactttg660
accgtagcaactggtccaggtgtgactattaataatacttccttgcaaactaaagttact720
ggagccttgggttttgattcacaaggcaatatgcaacttaatgtagcaggaggactaagg780
attgattctcaaaacagacgccttatacttgatgttagttatccgtttgatgctcaaaac840
caactaaatctaagactaggacagggccctctttttataaactcagcccacaacttggat900
attaactacaacaaaggcctttacttgtttacagcttcaaacaattccaaaaagcttgag960
gttaacctaagcactgccaaggggttgatgtttgacgctacagccatagccattaatgca1020
ggagatgggcttgaatttggttcacctaatgcaccaaacacaaatcccctcaaaacaaaa1080
attggccatggcctagaatttgattcaaacaaggctatggttcctaaactaggaactggc1140
cttagttttgacagcacaggtgccattacagtaggaaacaaaaataatgataagctaact1200
ttgtggaccacaccagctccatctcctaactgtagactaaatgcagagaaagatgctaaa1260
ctcactttggtcttaacaaaatgtggcagtcaaatacttgctacagtttcagttttggct1320
gttaaaggcagtttggctccaatatctggaacagttcaaagtgctcatcttattataaga1380
tttgacgaaaatggagtgctactaaacaattccttcctggacccagaatattggaacttt1440
agaaatggagatcttactgaaggcacagcctatacaaacgctgttggatttatgcctaac1500
ctatcagcttatccaaaatctcacggtaaaactgccaaaagtaacattgtcagtcaagtt1560
tacttaaacggagacaaaactaaacctgtaacactaacgatcacactaaacggtacacag1620
gaaacaggagacacaacttgtgactgccgcggagactgtttctgcccatctgcatactct1680
atgtcattttcatgggactggtctggccacaactacattaatgaaatatttgccacatcc1740
tcttacactttttcatacattgcccaagaataa1773
<210>7
<211>379
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>cmv增强子
<400>7
gacattgattattgacagttattaatagtaatcaattacggggtcattagttcatagccc60
atatatggagttccgcgttacataacttacggtaaatggcccgcctggctgaccgcccaa120
cgacccccgcccattgacgtcaataatgacgtatgttcccatagtaacgccaatagggac180
tttccattgacgtcaatgggtggactatttacggtaaactgcccacttggcagtacatca240
agtgtatcatatgccaagtacgccccctattgacgtcaatgacggtaaatggcccgcctg300
gcattatgcccagtacatgaccttatgggactttcctacttggcagtacatctacgtatt360
agtcatcgctattaccatg379
<210>8
<211>204
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>cmv启动子
<400>8
gtgatgcggttttggcagtacatcaatgggcgtggatagcggtttgactcacggggattt60
ccaagtctccaccccattgacgtcaatgggagtttgttttggcaccaaaatcaacgggac120
tttccaaaatgtcgtaacaactccgccccattgacgcaaatgggcggtaggcgtgtacgg180
tgggaggtctatataagcagagct204
<210>9
<211>30
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>含有i-ceui限制位点的序列
<400>9
cgtaactataacggtcctaaggtagcgaaa30
<210>10
<211>1311
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>ha标记的gsk3β序列
<400>10
atggcagggcggcccagaaccaccgcctttgcggagagctgcaagccggtgcagcagcct60
tcagcttttggcagcatgaaagttagcagagacaaggacggcagcaaggtgacaacagtg120
gtggcaactcctgggcagggtccagacaggccacaagaagtcagctatacagacactaaa180
gtgattggaaatggatcatttggtgtggtatatcaagccaaactttgtgattcaggagaa240
ctggtcgccatcaagaaagtattgcaggacaagagatttaagaatcgagagctccagatc300
atgagaaagctagatcactgtaacatagtccgattgcgttatttcttctactccagtggt360
gagaagaaagatgaggtctatcttaatctggtgctggactatgttccggaaacagtatac420
agagttgccagacactatagtcgagccaaacagacgctccctgtgatttatgtcaagttg480
tatatgtatcagctgttccgaagtttagcctatatccattcctttggaatctgccatcgg540
gatattaaaccgcagaacctcttgttggatcctgatactgctgtattaaaactctgtgac600
tttggaagtgcaaagcagctggtccgaggagaacccaatgtttcgtatatctgttctcgg660
tactatagggcaccagagttgatctttggagccactgattatacctctagtatagatgta720
tggtctgctggctgtgtgttggctgagctgttactaggacaaccaatatttccaggggat780
agtggtgtggatcagttggtagaaataatcaaggtcctgggaactccaacaagggagcaa840
atcagagaaatgaacccaaactacacagaatttaaattccctcaaattaaggcacatcct900
tggactaaggtcttccgaccccgaactccaccggaggcaattgcactgtgtagccgtctg960
ctggagtatacaccaactgcccgactaacaccactggaagcttgtgcacattcatttttt1020
gatgaattacgggacccaaatgtcaaacatccaaatgggcgagacacacctgcactcttc1080
aacttcaccactcaagaactgtcaagtaatccacctctggctaccatccttattcctcct1140
catgctcggattcaagcagctgcttcaacccccacaaatgccacagcagcgtcagatgct1200
aatactggagaccgtggacagaccaataatgctgcttctgcatcagcttccaactccact1260
agctacccatacgatgttccagattacgcaagcttgggtggtcccaactaa1311
<210>11
<211>236
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>polya
<400>11
tggatccagacatgataagatacattgatgagtttggacaaaccacaactagaatgcagt60
gaaaaaaatgctttatttgtgaaatttgtgatgctattgctttatttgtaaccattataa120
gctgcaataaacaagttaacaacaacaattgcattcattttatgtttcaggttcaggggg180
aggtgtgggaggttttttaaagcaagtaaaacctctacaaatgtgatatggctgat236
<210>12
<211>317
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>sv40启动子
<400>12
ggtgtggaaagtccccaggctccccagcaggcagaagtatgcaaagcatgcatctcaatt60
agtcagcaaccaggtgtggaaagtccccaggctccccagcaggcagaagtatgcaaagca120
tgcatctcaattagtcagcaaccatagtcccgcccctaactccgcccatcccgcccctaa180
ctccgcccagttccgcccattctccgccccatggctgactaattttttttatttatgcag240
aggccgaggccgcctcggcctctgagctattccagaagtagtgaggaggcttttttggag300
gcctaggcttttgcaaa317
<210>13
<211>30
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>含有i-ceui限制位点的序列
<400>13
cgtaactataacggtcctaaggtagcgaaa30
<210>14
<211>936
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>海肾荧光素酶序列
<400>14
atgacttcgaaagtttatgatccagaacaaaggaaacggatgataactggtccgcagtgg60
tgggccagatgtaaacaaatgaatgttcttgattcatttattaattattatgattcagaa120
aaacatgcagaaaatgctgttatttttttacatggtaacgcggcctcttcttatttatgg180
cgacatgttgtgccacatattgagccagtagcgcggtgtattataccagaccttattggt240
atgggcaaatcaggcaaatctggtaatggttcttataggttacttgatcattacaaatat300
cttactgcatggtttgaacttcttaatttaccaaagaagatcatttttgtcggccatgat360
tggggtgcttgtttggcattttattatagctatgagcatcaagataagatcaaagcaata420
gttcacgctgaaagtgtagtagatgtgattgaatcatgggatgaatggcctgatattgaa480
gaagatattgcgttgatcaaatctgaagaaggagaaaaaatggttttggagaataacttc540
ttcgtggaaaccatgttgccatcaaaaatcatgagaaagttagaaccagaagaatttgca600
gcatatcttgaaccattcaaagagaaaggtgaagttcgtcgtccaacattatcatggcct660
cgtgaaatcccgttagtaaaaggtggtaaacctgacgttgtacaaattgttaggaattat720
aatgcttatctacgtgcaagtgatgatttaccaaaaatgtttattgaatcggacccagga780
ttcttttccaatgctattgttgaaggtgccaagaagtttcctaatactgaatttgtcaaa840
gtaaaaggtcttcatttttcgcaagaagatgcacctgatgaaatgggaaaatatatcaaa900
tcgttcgttgagcgagttctcaaaaatgaacaataa936
<210>15
<211>936
<212>dna
<213>海桑(renillareniformis)
<400>15
atgacttcgaaagtttatgatccagaacaaaggaaacggatgataactggtccgcagtgg60
tgggccagatgtaaacaaatgaatgttcttgattcatttattaattattatgattcagaa120
aaacatgcagaaaatgctgttatttttttacatggtaacgcggcctcttcttatttatgg180
cgacatgttgtgccacatattgagccagtagcgcggtgtattataccagaccttattggt240
atgggcaaatcaggcaaatctggtaatggttcttataggttacttgatcattacaaatat300
cttactgcatggtttgaacttcttaatttaccaaagaagatcatttttgtcggccatgat360
tggggtgcttgtttggcattttattatagctatgagcatcaagataagatcaaagcaata420
gttcacgctgaaagtgtagtagatgtgattgaatcatgggatgaatggcctgatattgaa480
gaagatattgcgttgatcaaatctgaagaaggagaaaaaatggttttggagaataacttc540
ttcgtggaaaccatgttgccatcaaaaatcatgagaaagttagaaccagaagaatttgca600
gcatatcttgaaccattcaaagagaaaggtgaagttcgtcgtccaacattatcatggcct660
cgtgaaatcccgttagtaaaaggtggtaaacctgacgttgtacaaattgttaggaattat720
aatgcttatctacgtgcaagtgatgatttaccaaaaatgtttattgaatcggacccagga780
ttcttttccaatgctattgttgaaggtgccaagaagtttcctaatactgaatttgtcaaa840
gtaaaaggtcttcatttttcgcaagaagatgcacctgatgaaatgggaaaatatatcaaa900
tcgttcgttgagcgagttctcaaaaatgaacaataa936
<210>16
<211>8
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>e1a的cr2结构域的一部分
<400>16
leuthrcyshisglualaglyphe
15
- 还没有人留言评论。精彩留言会获得点赞!