掩蔽型细胞因子多肽的制作方法
相关申请的交叉引用
本申请要求2018年9月27日提交的62/737,803号美国临时申请、2019年8月16日提交的62/888,276号美国临时申请和2019年8月23日提交的62/891,199号美国临时申请的优先权。上面列出的申请的内容出于所有的目的以全文引用的方式并入本文。
以引用的方式并入序列表
本申请连同电子格式的序列表一起提交。序列表作为2019年9月26日创建的名为737762000940seqlist的文件提供,其大小为1,024.111kb。电子格式的序列表中的信息以全文引用的方式并入。
本发明涉及掩蔽型细胞因子以及有关其使用和制备的方法。
背景技术:
癌症在美国是第二大死亡主要原因,造成的死亡人数超过了接下来的五种主要原因(慢性呼吸系统疾病、中风、意外事故、阿尔茨海默氏病和糖尿病)。尽管特别是在靶向疗法方面已经取得了长足的进步,但在此领域中仍然有大量的工作要做。免疫疗法和作为该领域的一个分支的免疫肿瘤学正在成为治疗恶性肿瘤的可行且令人振奋的治疗选择。具体地,现在认识到癌症的一个标志是免疫逃避,并且大量的努力已经确认了靶标,并开发了针对这些靶标的疗法,以重新激活免疫系统来识别并治疗癌症。
细胞因子疗法是刺激免疫系统以诱导抗肿瘤细胞毒性的有效策略。例如,白介素-2(il-2)的一种重组形式阿地白介素已经被fda批准用于治疗转移性肾细胞癌和黑素瘤。遗憾的是,施用给患者的细胞因子的半衰期通常非常短,因此需要频繁给药。例如,以商标名proleukin销售的阿地白介素的产品标签指出该药物在接受5分钟静脉内(iv)输注的患者中显示具有85分钟的半衰期。此外,施用高剂量的细胞因子可能会通过全身免疫激活引起不利的健康结果,如血管渗漏。这些发现表明需要开发有效靶向肿瘤而没有与全身免疫激活相关的副作用的细胞因子治疗剂。为了解决这种需求,本文提供了掩蔽型细胞因子、其组合物及其使用方法。
本文引用的所有参考文献,包括专利申请、专利公布和科学文献,均以全文引用的方式并入本文,如同指出将每一单独的参考文献具体且单独地以引用的方式并入。
技术实现要素:
公开的发明涉及掩蔽型细胞因子或其功能片段的工程化和用途,在一些实施方案中,所述细胞因子或其功能片段被工程化,以在细胞因子或其功能片段的一个或多个受体结合位点处被掩蔽部分掩蔽。在一些实施方案中,细胞因子被工程化,以通过包括可蛋白水解切割的接头而可以在靶位点处(如在肿瘤微环境中)被蛋白酶激活。在一些实施方案中,可蛋白水解切割的接头将细胞因子与掩蔽部分连接、将细胞因子与半衰期延长结构域连接和/或将掩蔽部分与半衰期延长结构域连接。掩蔽部分阻断、封闭、抑制(例如,降低)或以其它方式阻止(例如,掩蔽)细胞因子的活性或与其同源受体或蛋白质的结合。可切割接头在靶位点处被蛋白水解切割时,细胞因子被激活,使其能够以增加的亲和力与其同源受体或蛋白质结合。
一个实施方案包括掩蔽型细胞因子,所述掩蔽型细胞因子包含掩蔽部分;和细胞因子或其功能片段,其中所述掩蔽部分经由接头与所述细胞因子或其功能片段连接。一方面,掩蔽型细胞因子进一步包含与掩蔽部分或细胞因子或其功能片段连接的半衰期延长结构域。
在一个实施方案中,掩蔽型细胞因子在n至c末端或c至n末端方向上包含:a)掩蔽部分;b)第一接头;c)细胞因子或其功能片段;和d)半衰期延长结构域。在另一实施方案中,掩蔽型细胞因子在n至c末端或c至n末端方向上包含:a)掩蔽部分;b)第一接头;c)细胞因子或其功能片段;d)第二接头;和e)半衰期延长结构域。在另一实施方案中,掩蔽型细胞因子在n至c末端或c至n末端方向上包含:a)细胞因子或其功能片段;b)第一接头;c)掩蔽部分;和d)半衰期延长结构域。
在另一实施方案中,掩蔽型细胞因子在n至c末端或c至n末端方向上包含:a)细胞因子或其功能片段;b)第一接头;c)掩蔽部分;d)第二接头;和e)半衰期延长结构域。
在一个实施方案中,所述细胞因子或其功能片段是il-2多肽或其功能片段或il-15多肽或其功能片段。
在一个实施方案中,掩蔽型细胞因子向il-2或il-15多肽或其功能片段的氨基酸序列中引入一个或多个氨基酸取代。在一个实施方案中,氨基酸取代降低了il-2多肽或其功能片段对cd25(il-2rα)的亲和力。
在一个实施方案中,il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代而产生的氨基酸序列。
在一个实施方案中,半衰期延长结构域是抗体或其片段,并且在一些实施方案中,一个或多个氨基酸取代改变效应子功能。
在一个实施方案中,所述抗体或其片段是片段可结晶结构域(fc结构域)或其片段。
在一个实施方案中,半衰期延长结构域是聚氨基酸序列,如pas多肽或xten多肽。
在一个实施方案中,掩蔽型细胞因子包含第二掩蔽部分,其中第二掩蔽部分经由第二接头与所述细胞因子或其功能片段连接。
在一个实施方案中,掩蔽型细胞因子在n至c末端或c至n末端方向上包含:a)第一掩蔽部分;b)第一接头;c)细胞因子或其功能片段;d)第二接头;e)第二掩蔽部分;和f)半衰期延长结构域。
在一个实施方案中,掩蔽型细胞因子在n至c末端或c至n末端方向上包含:a)第一掩蔽部分;b)第一接头;c)细胞因子或其功能片段;d)第二接头;e)第二掩蔽部分;f)第三接头;和g)半衰期延长结构域。
在一个实施方案中,掩蔽型细胞因子在n至c末端或c至n末端方向上包含:a)第二掩蔽部分;b)第二接头;c)细胞因子或其功能片段;d)第一接头;e)第一掩蔽部分;和f)半衰期延长结构域。
在一个实施方案中,掩蔽型细胞因子在n至c末端或c至n末端方向上包含:a)第二掩蔽部分;b)第二接头;c)细胞因子或其功能片段;d)第一接头;e)第一掩蔽部分;f)第三接头;和g)半衰期延长结构域。
在一个实施方案中,半衰期延长结构域是白蛋白多肽或其功能片段。
在一个实施方案中,所述可切割肽被选自由以下组成的组的一种或多种酶切割:abhd12、adam12、abhd12b、abhd13、abhd17a、adam19、adam20、adam21、adam28、adam30、adam33、adam8、abhd17a、adamdec1、adamts1、adamts10、adamts12、adamts13、adamts14、adamts15、adamts16、adamts17、adamts18、adamts19、adamts2、adamts20、adamts3、adamts4、abhd17b、adamts5、adamts6、adamts7、adamts8、adamts9、adamtsl1、adamtsl2、adamtsl3、abhd17c、adamtsl5、astl、bmp1、cela1、cela2a、cela2b、cela3a、cela3b、adam10、adam15、adam17、adam9、adamts4、ctse、ctsf、adamtsl4、cma1、ctrb1、ctrc、ctso、ctr1、ctsa、ctsw、ctsb、ctsc、ctsd、esp1、ctsg、ctsh、gzma、gzmb、gzmh、ctsk、gzmm、ctsl、ctss、ctsv、ctsz、htra4、klk10、klk11、klk13、klk14、klk2、klk4、dpp4、klk6、klk7、klkb1、ece1、ece2、ecel1、masp2、mep1a、mep1b、elane、fap、gzma、mmp11、gzmk、hgfac、hpn、htra1、mmp11、mmp16、mmp17、mmp19、htra2、mmp20、mmp21、htra3、htra4、kel、mmp23b、mmp24、mmp25、mmp26、mmp27、mmp28、klk5、mmp3、mmp7、mmp8、mmp9、lgmn、lnpep、masp1、pappa、pappa2、pcsk1、napsa、pcsk5、pcsk6、mme、mmp1、mmp10、plat、plau、plg、prss1、prss12、prss2、prss21、prss3、prss33、prss4、prss55、prss57、mmp12、prss8、prss9、prtn3、mmp13、mmp14、st14、tmprss10、tmprss11a、tmprss11d、tmprss11e、tmprss11f、tmprss12、tmprss13、mmp15、tmprss15、mmp2、tmprss2、tmprss3、tmprss4、tmprss5、tmprss6、tmprss7、tmprss9、nrdc、ovch1、pamr1、pcsk3、phex、tinag、tpsab1、tpsd1和tpsg1。
在一个实施方案中,半衰期延长结构域与诸如以下的剂缀合:微管蛋白聚合的抑制剂、dna损伤剂或dna合成抑制剂、类美登素(maytansinoid)、奥瑞他汀(auristatin)、吡咯并苯并二氮杂卓(pbd)二聚体、卡奇霉素、倍癌霉素(duocarmycin)、吲哚啉并苯并二氮杂卓二聚体或依喜替康衍生物dxd。
在一个实施方案中,半衰期延长结构域与免疫刺激剂缀合,所述免疫刺激剂如干扰素基因的刺激物(sting)激动剂,如环二核苷酸(cdn),如cgamp、c-di-amp、c-di-gmp、caimp、c-di-imp或4-(2-氯-6-氟苄基)-n-(呋喃-2-基甲基)-3-氧代-3,4-二氢-2h-苯并[b][1,4]噻嗪-6-甲酰胺或toll样受体(tlr)激动剂,如tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9或tlr10。
在一个实施方案中,掩蔽型细胞因子包含第一半衰期延长结构域和第二半衰期延长结构域,其中掩蔽部分与第一半衰期延长结构域连接,且其中细胞因子或其功能片段与第二半衰期延长结构域连接。
在一个实施方案中,第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰。
一个实施方案包括编码本文所述的掩蔽型细胞因子的核酸。另一实施方案包括包含所述核酸的载体。在另一实施方案中,宿主细胞包含所述核酸。另一实施方案包括一种或多种编码本文所述的掩蔽型细胞因子的核酸。另一实施方案包括包含所述一种或多种核酸的载体。另一实施方案包括包含所述一种或多种核酸的一种或多种载体。
在另一实施方案中提供了制备掩蔽型细胞因子的方法,包括在产生掩蔽型细胞因子的条件下培养宿主细胞。在一个实施方案中,回收由宿主细胞产生的掩蔽型细胞因子。一个实施方案包括通过所公开的方法制备的掩蔽型细胞因子。
在一个实施方案中,提供了包含所公开的掩蔽型细胞因子的组合物。在另一实施方案中,所述组合物进一步包含抗炎剂或抗癌剂,如pd-1抑制剂、egfr抑制剂、her2抑制剂、vegfr抑制剂、ctla-4抑制剂、btla抑制剂、b7h4抑制剂、b7h3抑制剂、csfir抑制剂、hvem抑制剂、cd27抑制剂、kir抑制剂、nkg2a抑制剂、nkg2d激动剂、tweak抑制剂、alk抑制剂、cd52靶向抗体、ccr4靶向抗体、pd-l1抑制剂、kit抑制剂、pdgfr抑制剂、baff抑制剂、hdac抑制剂、vegf配体抑制剂、cd19靶向分子、folr1靶向分子、dll3靶向分子、dkk1靶向分子、muc1靶向分子、muc16靶向分子、psma靶向分子、msln靶向分子、ny-es0-1靶向分子、b7h3靶向分子、b7h4靶向分子、bcma靶向分子、cd29靶向分子、cd151靶向分子、cd123靶向分子、cd33靶向分子、cd37靶向分子、cdh19靶向分子、cea靶向分子、claudin18.2靶向分子、clec12a靶向分子、egfrviii靶向分子、epcam靶向分子、epha2靶向分子、fcrh5靶向分子、flt3靶向分子、gd2靶向分子、磷脂酰肌醇蛋白聚糖3靶向分子、gpa33靶向分子、gprc5d靶向分子、il-23r靶向分子、il-1rap靶向分子、mcsp靶向分子、ron靶向分子、ror1靶向分子、steap2靶向分子、tfr靶向分子、cd166靶向分子、tpbg靶向分子、trop2靶向分子、蛋白酶体抑制剂、abl抑制剂、cd30抑制剂、flt3抑制剂、met抑制剂、ret抑制剂、il-1β抑制剂、mek抑制剂、ros1抑制剂、braf抑制剂、cd38抑制剂、rankl抑制剂、b4galnt1抑制剂、slamf7抑制剂、idh2抑制剂、mtor抑制剂、cd20靶向抗体、btk抑制剂、pi3k抑制剂、flt3抑制剂、parp抑制剂、cdk4抑制剂、cdk6抑制剂、fgfr抑制剂、raf抑制剂、jak1抑制剂、jak2抑制剂、jak3抑制剂、il-6抑制剂、il-17抑制剂、平滑化(smoothened)抑制剂、il-6r抑制剂、bcl2抑制剂、ptch抑制剂、pigf抑制剂、tgfb抑制剂、cd28激动剂、cd3激动剂、cd40激动剂、gitr激动剂、ox40激动剂、vista激动剂、cd137激动剂、lag3抑制剂、tim3抑制剂、tigit抑制剂或il-2r抑制剂。
在一个实施方案中,所述抗炎剂是环氧合酶(cox)抑制剂,如cox-1和/或cox-2抑制剂,如sc-560、fr122047、p6、莫苯唑酸、tfap、氟比洛芬、酮洛芬、塞来昔布、罗非昔布、美洛昔康、吡罗昔康、德拉昔布、帕瑞昔布、伐地昔布、依托昔布、色烯衍生物、色满衍生物、n-(2-环己氧基硝基苯基)甲磺酰胺、帕瑞考昔、罗美昔布、rs57067、t-614、bms-347070、jte-522、s-2474、svt-2016、ct-3、abt-963、sc-58125、尼美舒利、氟舒胺、ns-398、l-745337、rwj-63556、l-784512、达布飞龙、cs-502、las-34475、las-34555、s-33516、双氯芬酸、甲芬那酸、sd-8381、布洛芬、萘普生、酮咯酸、吲哚美辛、阿司匹林、萘普生、托美汀、吡罗昔康或甲氯芬那酸酯。
在一个实施方案中,所述抗炎剂是nf-κb抑制剂,如ikk复合物抑制剂、iκb降解抑制剂、nf-κb核易位抑制剂、p65乙酰化抑制剂、nf-κbdna结合抑制剂、nf-κb反式激活抑制剂或p53诱导抑制剂。
在一个实施方案中,nf-κb抑制剂是tpca-1、nf-κb激活抑制剂vi(bot-64)、bms-345541、氨来占诺、sc-514(gk-01140)、imd-0354、ikk-16、bay-11-7082、mg-115、mg-132、乳胞素、环氧酶素、小白菊内酯、卡非佐米、mln-4924(pevonedistat)、jsh-23咯利普兰、没食子酸、漆树酸、gyy-4137、p-xsc、cv-3988、前列腺素e2(pge2)、ly-294002、渥曼青霉素、美沙拉嗪、奎纳克林或夫拉平度。
一个实施方案包括包含所公开的掩蔽型细胞因子和药学上可接受的载体的药物组合物。
另一实施方案包括包含所公开的掩蔽型细胞因子的试剂盒。
另一实施方案包括治疗或预防受试者的肿瘤性疾病的方法,所述方法包括对受试者施用有效量的所公开的用于治疗疾病或疾患(如肿瘤性疾病,例如癌症)的掩蔽型细胞因子组合物。在一个实施方案中,所述癌症是白血病、淋巴瘤、头颈癌、结肠直肠癌、前列腺癌、胰腺癌、黑素瘤、乳腺癌、成神经细胞瘤、肺癌、卵巢癌、骨癌(例如,骨肉瘤、软骨肉瘤、尤因肉瘤)、膀胱癌、宫颈癌、肝癌、肾癌、皮肤癌、睾丸癌、肾上腺癌、腺样囊性癌、肛门癌、脑癌、导管癌、子宫内膜癌、食道癌、胃癌、口腔癌、甲状腺癌、成视网膜细胞瘤、甲状旁腺癌、垂体癌、胆管癌或子宫癌。在一些实施方案中,所述癌症选自由以下组成的组:淋巴瘤、肉瘤、膀胱癌、骨癌、脑肿瘤、宫颈癌、结肠癌、食道癌、胃癌、头颈癌、肾癌、骨髓瘤、甲状腺癌、白血病、前列腺癌、乳腺癌(例如三阴性、er阳性、er阴性、化疗抗性、赫赛汀抗性、her2阳性、多柔比星抗性、他莫昔芬抗性、导管癌、小叶癌、原发性、转移性)、卵巢癌、胰腺癌、肝癌(例如肝细胞癌)、肺癌(例如非小细胞肺癌、鳞状细胞肺癌、腺癌、大细胞肺癌、小细胞肺癌、类癌、肉瘤)、多形性成胶质细胞瘤、神经胶质瘤、黑素瘤、前列腺癌、去势抵抗性前列腺癌、乳腺癌、三阴性乳腺癌、成胶质细胞瘤、卵巢癌、肺癌、鳞状细胞癌(例如,头、颈或食道)、结肠直肠癌、白血病、急性髓性白血病、淋巴瘤、b细胞淋巴瘤或多发性骨髓瘤。另外的实例包括甲状腺癌、内分泌系统癌、脑癌、乳腺癌、宫颈癌、结肠癌、头颈癌、食道癌、肝癌、肾癌、肺癌、非小细胞肺癌、黑素瘤、间皮瘤、卵巢癌、肉瘤、胃癌、子宫癌或成神经管细胞瘤、霍奇金病、非霍奇金淋巴瘤、多发性骨髓瘤、成神经细胞瘤、神经胶质瘤、多形性成胶质细胞瘤、卵巢癌、横纹肌肉瘤、原发性血小板增多症、原发性巨球蛋白血症、原发性脑肿瘤、癌症、恶性胰腺胰岛瘤、恶性类癌、泌尿系统膀胱癌、癌前皮肤病变、睾丸癌、淋巴瘤、甲状腺癌、成神经细胞瘤、食道癌、生殖泌尿道癌、恶性高钙血症、子宫内膜癌、肾上腺皮质癌、内分泌或外分泌胰腺肿瘤、甲状腺髓样癌(medullarythyroidcancer)、甲状腺髓样癌(medullarythyroidcarcinoma)、黑素瘤、结肠直肠癌、乳头状甲状腺癌、肝细胞癌、乳头佩吉特病、叶状肿瘤、小叶癌、导管癌、胰腺星状细胞癌、肝星状细胞癌或前列腺癌。
另一实施方案包括治疗或预防受试者的炎性或自身免疫性疾病的方法,所述方法包括对受试者施用有效量的所公开的掩蔽型细胞因子组合物,其中所述炎性或自身免疫性疾病选自由以下组成的组:动脉粥样硬化、肥胖症、炎性肠病(ibd)、类风湿性关节炎、过敏性脑炎、银屑病、特应性皮肤病、骨质疏松症、腹膜炎、肝炎、狼疮、乳糜泻、舍格伦综合征、风湿性多肌痛、多发性硬化(ms)、强直性脊柱炎、1型糖尿病、斑秃、血管炎和颞动脉炎、移植物抗宿主病(gvhd)、哮喘、copd、副肿瘤性自身免疫性疾病、软骨炎症、幼年型关节炎、幼年型类风湿性关节炎、少关节幼年型类风湿性关节炎、多关节幼年型类风湿性关节炎、全身发作性幼年型类风湿性关节炎、幼年型强直性脊柱炎、幼年型肠病性关节炎、幼年型反应性关节炎、幼年型赖特尔综合征、sea综合征(血清阴性、接骨点病变、关节病综合征)、幼年型皮肌炎、幼年型银屑病关节炎、幼年型硬皮病、幼年型全身性红斑狼疮、幼年型血管炎、少关节类风湿性关节炎、全身发作性类风湿性关节炎、肠病性关节炎、反应性关节炎、赖特尔综合征、皮肌炎、银屑病关节炎、硬皮病、血管炎、肌炎、多肌炎、皮肌炎、结节性多动脉炎、韦格纳肉芽肿病、动脉炎、风湿性多肌痛、结节病、硬化症、原发性胆汁性硬化、硬化性胆管炎、银屑病、斑块状银屑病、滴状银屑病、反型银屑病、脓疱性银屑病、红皮病性银屑病、皮炎、特应性皮炎、动脉粥样硬化、斯蒂尔病、全身性红斑狼疮(sle)、重症肌无力、克罗恩病、溃疡性结肠炎、乳糜泻、鼻窦炎、具有息肉的鼻窦炎、嗜酸性食管炎、嗜酸性支气管炎、格林-巴利病、甲状腺炎(例如,格雷夫斯病)、阿狄森病、雷诺现象、自身免疫性肝炎、移植排斥、肾损伤、丙型肝炎诱导的血管炎或自发性妊娠丢失。
附图说明
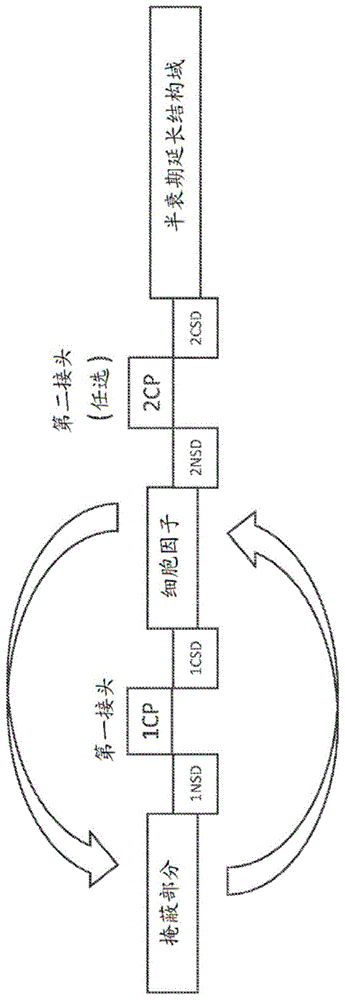
图1a和图1b显示掩蔽型细胞因子的示例性实施方案的结构,所述掩蔽型细胞因子包括掩蔽部分、细胞因子或其功能片段(“细胞因子”)、半衰期延长结构域和第一接头,所述第一接头包括第一可切割肽(“1cp”)、第一n末端间隔区结构域(“1nsd”)和第一c末端间隔区结构域(“1csd”)。这些示例性实施方案还包括第二接头,所述第二接头包括第二可切割肽(“2cp”)、第二n末端间隔区结构域(“2nsd”)和第二c末端间隔区结构域(“2csd”)。如箭头所示,虽然示例性实施方案显示掩蔽部分与第一接头连接,且细胞因子或其功能片段与第一接头和第二接头连接,但掩蔽部分和细胞因子或其功能片段可以互换,使得细胞因子或其功能片段与第一接头连接,且掩蔽部分与第一接头和第二接头连接。图1a显示作为单体的掩蔽型细胞因子的示例性实施方案的结构。图1b显示作为由二硫键形成的同源二聚体的掩蔽型细胞因子的示例性实施方案的结构。
图2a和图2b显示掩蔽型细胞因子的示例性实施方案的结构,所述掩蔽型细胞因子包括第一掩蔽部分(“mask1”)、细胞因子或其功能片段(“细胞因子”)、第二掩蔽部分(“mask2”)、半衰期延长结构域、第一接头和第二接头,所述第一接头包括第一可切割肽(“1cp”)、第一n末端间隔区结构域(“1nsd”)和第一c末端间隔区结构域(“1csd”),所述第二接头包括第二可切割肽(“2cp”)、第二n末端间隔区结构域(“2nsd”)和第二c末端间隔区结构域(“2csd”)。这些示例性实施方案还包括第三接头,所述第三接头包括第三可切割肽(“3cp”)、第三n末端间隔区结构域(“3nsd”)和第三c末端间隔区结构域(“3csd”)。图2a显示作为单体的掩蔽型细胞因子的示例性实施方案的结构。图2b显示作为由二硫键形成的同源二聚体的掩蔽型细胞因子的示例性实施方案的结构。
图3a显示包括掩蔽部分、细胞因子或其功能片段(“细胞因子”)、第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子的示例性实施方案的结构。图3a中所示的示例性实施方案还包括第一接头和第二接头,所述第一接头包括第一可切割肽(“1cp”)、第一n末端间隔区结构域(“1nsd”)和第一c末端间隔区结构域(“1csd”),所述第二接头包括第二可切割肽(“2cp”)、第二n末端间隔区结构域(“2nsd”)和第二c末端间隔区结构域(“2csd”)。示例性第一和第二半衰期延长结构域包括促进第一半衰期延长结构域与第二半衰期延长结构域缔合的“旋钮入孔(knobsintoholes)”修饰,如由第一半衰期延长结构域中的“孔”和第二半衰期延长结构域中的“旋钮”所示。还显示由于二硫键的形成,第一半衰期延长结构域和第二半衰期延长结构域至少部分地缔合。要理解的是,虽然“孔”被描绘为第一半衰期延长结构域的一部分(与掩蔽部分连接),且“旋钮”被描绘为第二半衰期延长结构域的一部分(与细胞因子连接),但“孔”和“旋钮”可以可替代地分别被包括在第二半衰期延长结构域和第一半衰期延长结构域中,从而“孔”是第二半衰期延长结构域的一部分(与细胞因子连接),且“旋钮”是第一半衰期延长结构域的一部分(与掩蔽部分连接)。图3b显示包括掩蔽部分、细胞因子或其功能片段(“细胞因子”)、第一半衰期延长结构域、第二半衰期延长结构域和第三接头的掩蔽型细胞因子的示例性实施方案的结构,所述第三接头包括第三n末端间隔区结构域(“3nsd”)和第三c末端间隔区结构域(“3csd”)。第三接头将第一半衰期延长结构域与第二半衰期延长结构域连接。图3b中所示的示例性实施方案还包括第一接头和第二接头,所述第一接头包括第一可切割肽(“1cp”)、第一n末端间隔区结构域(“1nsd”)和第一c末端间隔区结构域(“1csd”),所述第二接头包括第二可切割肽(“2cp”)、第二n末端间隔区结构域(“2nsd”)和第二c末端间隔区结构域(“2csd”)。
图4显示由二硫键形成的图3a中所示的示例性掩蔽型细胞因子的二聚体。
图5a显示包括第一掩蔽部分(“mask1”)、第一半衰期延长结构域、第二掩蔽部分(“mask2”)、细胞因子或其功能片段(“细胞因子”)和第二半衰期延长结构域的掩蔽型细胞因子的示例性实施方案的结构。图5a中所示的示例性实施方案还包括第一接头、第二接头和第三接头,所述第一接头包括第一可切割肽(“1cp”)、第一n末端间隔区结构域(“1nsd”)和第一c末端间隔区结构域(“1csd”),所述第二接头包括第二可切割肽(“2cp”)、第二n末端间隔区结构域(“2nsd”)和第二c末端间隔区结构域(“2csd”),所述第三接头包括第三可切割肽(“3cp”)、第三n末端间隔区结构域(“3nsd”)和第三c末端间隔区结构域(“3csd”)。要理解的是,虽然“孔”被描绘为第一半衰期延长结构域的一部分(与掩蔽部分连接),且“旋钮”被描绘为第二半衰期延长结构域的一部分(与细胞因子连接),但“孔”和“旋钮”可以可替代地分别被包括在第二半衰期延长结构域和第一半衰期延长结构域中,从而“孔”是第二半衰期延长结构域的一部分(与细胞因子连接),且“旋钮”是第一半衰期延长结构域的一部分(与掩蔽部分连接)。图5b显示包括第一掩蔽部分(“mask1”)、第一半衰期延长结构域、第二掩蔽部分(“mask2”)、细胞因子或其功能片段(“细胞因子”)、第二半衰期延长结构域和第四接头的掩蔽型细胞因子的示例性实施方案的结构,所述第四接头包括第四n末端间隔区结构域(“4nsd”)和第四c末端间隔区结构域(“4csd”)。第四接头将第一半衰期延长结构域与第二半衰期延长结构域连接。图5b中所示的示例性实施方案还包括第一接头、第二接头和第三接头,所述第一接头包括第一可切割肽(“1cp”)、第一n末端间隔区结构域(“1nsd”)和第一c末端间隔区结构域(“1csd”),所述第二接头包括第二可切割肽(“2cp”)、第二n末端间隔区结构域(“2nsd”)和第二c末端间隔区结构域(“2csd”),所述第三接头包括第三可切割肽(“3cp”)、第三n末端间隔区结构域(“3nsd”)和第三c末端间隔区结构域(“3csd”)。如图5a和5b中的箭头所示,虽然示例性实施方案显示第二掩蔽部分与第三接头连接,且细胞因子或其功能片段与第三接头和第二接头连接,但第一掩蔽部分和细胞因子或其功能片段可以互换,使得细胞因子或其功能片段与第三接头连接,且第一掩蔽部分与第三接头和第二接头连接。
图6显示由二硫键形成的图5a中所示的示例性掩蔽型细胞因子的二聚体。
图7a-7e显示如在肿瘤微环境下被蛋白酶切割之前(左)和之后(右)的掩蔽型细胞因子的示例性实施方案。图7a-7d显示掩蔽型il-2细胞因子的示例性实施方案,且图7e显示掩蔽型il-15细胞因子的示例性实施方案。通过蛋白酶切割释放掩蔽部分(例如il-2rβ,如图7a、7b和7d中所示),或释放il-2(图7c),或释放il-15(图7e)。
图8显示在示例性构建体(ak304、ak305、ak307、ak308、ak309、ak310、ak311、ak312、ak313、ak314和ak315)的产生和纯化之后对流通(ft)样品(即,未与蛋白a柱结合的蛋白)和洗脱(e)样品(即,与蛋白a柱结合并从其中洗脱的蛋白)进行的sds-page分析。
图9a-9d显示测试示例性掩蔽型il-2多肽构建体(ak215和ak216)或rhil2对照与cd25-fc结合的spr分析的结果。图9a显示ak215与cd25-fc之间的相互作用,图9b显示ak216与cd25-fc之间的相互作用,且图9c显示重组人il2(rhil2)对照与cd25-fc之间的相互作用。图9d提供汇总针对每种相互作用的缔合常数(ka)、解离常数(kd)、平衡解离常数(kd)以及chi2值和u值获得的数据的表格。
图10a-10d显示测试示例性掩蔽型il-2多肽构建体(ak216和ak218)或rhil2对照与cd122-fc结合的spr分析的结果。图10a显示ak216与cd122-fc之间的相互作用,图10b显示ak218与cd122-fc之间的相互作用,且图10c显示重组人il2(rhil2)对照与cd122-fc之间的相互作用。图10d提供汇总针对每种相互作用的缔合常数(ka)、解离常数(kd)、平衡解离常数(kd)以及chi2值和u值获得的数据的表格。
图11a显示如在肿瘤微环境下被蛋白酶切割之前(左)和之后(右)的掩蔽型细胞因子的示例性实施方案。图11b显示在不存在(左泳道)或存在(右泳道)mmp10蛋白酶的情况下温育的示例性掩蔽型il-2多肽构建体的sds-page分析,其显示了il-2从fc部分中的释放。
图12a-12d显示用构建体ak032、ak035、ak041或作为对照的rhil-2处理的pbmc中的stat5激活(%)。对于nk细胞、cd8+t细胞、效应t细胞(teff)和调控性t细胞(treg)显示了stat5激活(%)的水平,如在与rhil-2(图12a)、ak032(图12b)、ak035(图12c)或ak041(图12d)一起温育之后所测定。
图13a-13c显示用构建体ak081或ak032处理的pbmc中的stat5激活(%)。测试了有和没有之前暴露于mmp10的ak081构建体。还测试了同种型对照以及无il-2阴性对照。对于nk细胞(图13a)、cd8+t细胞(图13c)和cd4+t细胞(图13b)显示了stat5激活(%)的水平。
图14a-14d显示使用构建体ak081和ak111以及包括rhil-2和抗rsv抗体的对照在pbmc中进行stat5激活研究的结果。还测试了无处理的对照。还显示了rhil-2、ak081和ak111处理的ec50(pm)。对于cd4+foxp3+cd25+细胞(图14a)、cd8+细胞(图14b)和cd4+foxp3-cd25-细胞(图14c)显示了stat5激活(%)。图14d提供ak081、ak111构建体以及rhil-2对照的ec50(pm)和倍数变化数据。
图15a-15d显示使用构建体ak167和ak168以及包括rhil-2和抗rsv抗体的对照在pbmc中进行stat5激活研究的结果。还测试了无处理的对照。还显示了rhil-2、ak167和ak168处理的ec50(pm)。对于cd4+foxp3+cd25+细胞(图15a)、cd8+细胞(图15b)和cd4+foxp3-cd25-细胞(图15c)显示了stat5激活(%)。图15d提供ak167和ak168构建体以及rhil-2对照的ec50(pm)和倍数变化数据。
图16a-16d显示用有(+mmp10)或没有先前暴露于mmp10蛋白酶的构建体ak165或ak166或同种型对照或il-2-fc对照处理的pbmc中的stat5激活(%)。如图16a中所示的图例也适用于图16b,且如图16c中所示的图例也适用于图16d。对于cd4+foxp3+t调控细胞(图16a)、cd4+foxp3-t辅助细胞(图16b)、cd8+细胞毒性t细胞(图16c)和cd56+nk细胞(图16d)显示了stat5激活(%)。
图17a-17c显示用有(+mmp10)或没有先前暴露于mmp10蛋白酶的构建体ak109或ak110或同种型对照或il-2-fc对照处理的pbmc中的stat5激活(%)。如图17b中所示的图例也适用于图17a。对于nk细胞(图17a)、cd8细胞(图17b)和cd4细胞(图17c)显示了stat5激活(%)。
图18a-18d显示使用构建体ak211、ak235、ak253、ak306、ak310、ak314和ak316以及rhil-2对照在pbmc中进行stat5激活研究的结果。对于cd3+cd4+foxp3+细胞(图18a)、cd3+cd4+foxp3-细胞(图18b)和cd3+cd8+细胞(图18c)显示了stat5激活(%)。图18d提供每种测试构建体以及rhil-2对照的ec50数据。
图19a-19d显示使用已被蛋白酶激活的构建体ak081、ak167、ak216、ak218、ak219、ak220和ak223以及rhil-2对照在pbmc中进行stat5激活研究的结果。对于cd4+foxp3+cd25+调控性t细胞(图19a)、cd4+foxp3-cd25-细胞(图19b)和cd8+细胞(图19c)显示了stat5激活(%)。图19d提供每种测试构建体以及rhil-2对照的ec50数据。
图20a-20c显示用构建体ak081、ak189、ak190或ak210或抗rsv对照处理的pbmc中的stat5激活(%)。如图20a中所示的图例也适用于图20b和20c。对于调控性t细胞(图20a)、cd4辅助t细胞(图20b)和cd8细胞(图20c)显示了stat5激活(%)。
图21a-21c显示用构建体ak167、ak191、ak192或ak193或抗rsv对照处理的pbmc中的stat5激活(%)。如图21a中所示的图例也适用于图21b和21c。对于调控性t细胞(图21a)、cd4辅助t细胞(图21b)和cd8细胞(图21c)显示了stat5激活(%)。
图22a和22b显示对有(+mmp)或没有之前暴露于激活蛋白酶的示例性掩蔽型il-15多肽构建体ak248或作为对照的rhil-15进行报道子生物测定的结果。图22a显示使用hek-blueil2报道细胞系进行报道子生物测定的结果,且图22b显示用小鼠ctll2细胞系进行il-15生物测定的报道子生物测定的结果。
图23a-23d显示使用构建体ak032、ak081、ak111、ak167或ak168或抗rsv对照在荷瘤小鼠中进行药代动力学研究的结果。图23a提供对测试的每种构建体的结构的简化描绘。图23b通过检测人igg显示血浆中的fc水平(μg/ml),图23c通过检测人cd122显示血浆中的fc-cd122水平(μg/ml),且图23d通过检测人il-2显示血浆中的fc-il2水平(μg/ml)。在检测步骤之前,使用抗人ig作为捕获抗体。
图24a-24d显示使用构建体ak167、ak191ak197、ak203、ak209或ak211或抗rsv对照在荷瘤小鼠中进行药代动力学研究的结果。图24a提供对测试的每种构建体的结构的简化描绘。图24b通过检测人igg显示血浆中的fc水平(μg/ml),图24c通过检测人il-2显示血浆中的fc-il2水平(μg/ml),且图24d通过检测人cd122显示血浆中的fc-cd122水平(μg/ml)。在检测步骤之前,使用抗人ig作为捕获抗体。
图25a-25l显示使用ak032、ak081、ak111、ak167或ak168构建体或抗rsvigg对照测试脾、血液和肿瘤中的cd4、cd8、nk和treg百分比的体内反应的研究的结果。对于脾组织,显示了cd3细胞的%cd8细胞(图25a)、cd3细胞的%cd4(图25b)、cd3-细胞的%nk细胞(图25c)、cd4细胞的%foxp3(图25d)。对于血液,显示了cd3细胞的%cd8细胞(图25e)、cd3细胞的%cd4(图25f)、cd3-细胞的%nk细胞(图25g)、cd4细胞的%foxp3(图25h)。对于肿瘤组织,显示了cd3细胞的%cd8细胞(图25i)、cd3细胞的%cd4(图25j)、cd3-细胞的%nk细胞(图25k)、cd4细胞的%foxp3(图25l)。
图26a-26l显示使用ak167、ak168、ak191、ak197、ak203、ak209或ak211构建体或抗rsvigg对照测试脾、血液和肿瘤中的cd4、cd8、nk和treg百分比的体内反应的研究的结果。对于脾组织,显示了cd3细胞的%cd8细胞(图26a)、cd3细胞的%cd4(图26b)、cd3-细胞的%nk细胞(图26c)、cd4细胞的%foxp3(图26d)。对于血液,显示了cd3细胞的%cd8细胞(图26e)、cd3细胞的%cd4(图26f)、cd3-细胞的%nk细胞(图26g)、cd4细胞的%foxp3(图26h)。对于肿瘤组织,显示了cd3细胞的%cd8细胞(图26i)、cd3细胞的%cd4(图26j)、cd3-细胞的%nk细胞(图26k)、cd4细胞的%foxp3(图26l)。
图27a-27l显示使用ak235、ak191、ak192、ak193、ak210、ak189、ak190或ak211构建体或抗rsvigg对照测试脾、血液和肿瘤中的cd4、cd8、nk和treg百分比的体内反应的研究的结果。对于脾组织,显示了cd3细胞的%cd8细胞(图27a)、cd3细胞的%cd4(图27b)、cd3-细胞的%nk细胞(图27c)、cd4细胞的%foxp3(图27d)。对于血液,显示了cd3细胞的%cd8细胞(图27e)、cd3细胞的%cd4(图27f)、cd3-细胞的%nk细胞(图27g)、cd4细胞的%foxp3(图27h)。对于肿瘤组织,显示了cd3细胞的%cd8细胞(图27i)、cd3细胞的%cd4(图27j)、cd3-细胞的%nk细胞(图27k)、cd4细胞的%foxp3(图27l)。
图28a-28i显示使用ak235、ak191、ak192、ak193、ak210、ak189、ak190或ak211构建体在脾、血液和肿瘤中进行体内t细胞激活的结果。在脾、血液和肿瘤中,t细胞激活被测量为cd8+t细胞(图28a;图28d;图28g)、cd4+t细胞(图28b;图28e;图28h)或foxp3+细胞(图28c;图28f;图28i)中的cd25的平均荧光强度(mfi)。与不可切割的ak211构建体相比,采用单向anova进行统计分析。
图29a-29d显示测试示例性掩蔽型il-2多肽构建体ak168(可切割肽序列:mpydlyhp;seqidno:96)和ak209(可切割肽序列:vplsly;seqidno:135)的体内切割的研究结果。图29e显示对于ak167、ak168和ak209构建体的总水平以及每种构建体的非切割形式的水平的总血浆igg浓度(μg/ml)的药代动力学研究结果。
图30a-30d显示使用示例性掩蔽型il-2多肽构建体ak111或ak168或非掩蔽型il-2多肽构建体ak081或ak167或抗rsv对照来评估血管渗漏的体内研究的结果。图30a显示体重损失的百分比(%),且图30b、30c和30d分别显示肝、肺和脾各自的重量(克)。
图31a和31b显示评估血管渗漏的体内研究的结果,如通过在施用ak081、ak111、ak167或ak168构建体或抗rsv对照之后测量染料向肝和肺组织中渗漏的程度所指示。基于在650nm的吸光度来测量染料向肝(图31a)和肺(图31b)中渗漏的程度。
图32a和32b显示评估血管渗漏的体内研究的结果,如通过在施用ak081、ak111、ak167或ak168构建体或抗rsv对照之后测量单核细胞血管周围侵入肝和肺组织的程度所指示。各自描绘了肝中的单核细胞平均数(图32a)和肺中的单核细胞平均数(图32b)。
图33a和33b显示在用ak032、ak081、ak111、ak167或ak168构建体或抗rsv对照治疗的过程中评估肿瘤体积和体重的同系肿瘤模型研究的结果。图33a显示治疗过程中的肿瘤体积的数据,且图33b显示治疗过程中的体重变化百分比(%)的数据。
具体实施方式
本文提供了细胞因子或其功能片段,在一些实施方案中,所述细胞因子或其功能片段被工程化,以在细胞因子或其功能片段的一个或多个受体结合位点处被掩蔽部分掩蔽。在一些实施方案中,细胞因子被工程化,以通过包括可蛋白水解切割的接头而可以在靶位点处(如在肿瘤微环境中)被蛋白酶激活。在一些实施方案中,可蛋白水解切割的接头将细胞因子与掩蔽部分连接、将细胞因子与半衰期延长结构域连接和/或将掩蔽部分与半衰期延长结构域连接。掩蔽部分阻断、封闭、抑制(例如,降低)或以其它方式阻止(例如,掩蔽)细胞因子的活性或与其同源受体或蛋白质的结合。可切割接头在靶位点处被蛋白水解切割时,细胞因子被激活,使其能够以增加的亲和力与其同源受体或蛋白质结合。
通过使用掩蔽部分,所施用的细胞因子的全身副作用可通过干扰细胞因子的结合能力而降低。例如,高剂量重组il-2(阿地白介素)已被fda批准用于治疗转移性肾细胞癌和黑素瘤,但有相关的严重心血管、肝、肺、胃肠、神经和血液学副作用。临床前研究显示,例如il-2诱发的肺水肿由il-2与肺内皮细胞上的il-2受体(il-2r)的il-2rα(cd25)亚基之间的相互作用引起,并且可通过干扰il-2结合il-2rα的能力而消除il-2介导的肺水肿。参见krieg等人,(2010)pnas,107(26):11906-11911。因此,在细胞因子或其功能片段是il-2多肽的一些实施方案中,使用阻断、封闭、抑制(例如,降低)或以其它方式阻止(例如,掩蔽)il-2细胞因子的活性或与il-2rα结合的掩蔽部分。为了进一步降低掩蔽型il-2多肽的全身作用,掩蔽型il-2多肽可进一步包括阻断、封闭、抑制(例如,降低)或以其它方式阻止(例如,掩蔽)il-2细胞因子的活性或与il-2r的il-2rβ和/或il-2rγ亚基结合的掩蔽部分。类似的策略同样用于其它细胞因子,方式是通过干扰它们结合与引起不利的全身副作用相关的某些蛋白质(例如,受体亚基)的能力。此外,通过使用包括可切割肽的接头掩蔽细胞因子,可以通过在肿瘤微环境下切割可切割肽来恢复通过使用掩蔽部分干扰的结合能力。因此,在一些实施方案中,本文提供的掩蔽型细胞因子被工程化,以通过利用作为癌症的标志之一的高局部浓度的活性蛋白酶来将药理学活性精确地靶向肿瘤微环境。肿瘤微环境的这一特征用于将全身惰性分子转化成局部活性细胞因子。细胞因子在肿瘤微环境下的激活显著降低了可能与对受试者施用活性形式的药物相关的全身毒性。
出于所有的目的,本申请中提到的所有出版物(包括专利文献、科学论文和数据库)以引用的方式全文并入,其程度如同每一单独的出版物单独以引用的方式并入一般。如果本文阐述的定义与以引用的方式并入本文的专利、申请、公布的申请及其它出版物中阐述的定义相反或以其它方式不一致,则本文阐述的定义优先于以引用方式并入本文的定义。
本文所用的章节标题仅用于组织的目的,并不被解释为限制所描述的主题。
i.掩蔽型细胞因子
本文在一些实施方案中提供了掩蔽型细胞因子,其包含(a)掩蔽部分;和(b)细胞因子或其功能片段,其中掩蔽部分经由第一接头与细胞因子或其功能片段连接。在一些实施方案中,掩蔽型细胞因子进一步包含与掩蔽部分或细胞因子或其功能片段连接的半衰期延长结构域。在一些实施方案中,半衰期延长结构域经由第二接头与掩蔽部分或il-2多肽或其功能片段连接。
在一些实施方案中,掩蔽型细胞因子在n至c末端方向上包含:(a)掩蔽部分;(b)第一接头;(c)细胞因子或其功能片段;和(d)半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子在c至n末端方向上包含:(a)掩蔽部分;(b)第一接头;(c)细胞因子或其功能片段;和(d)半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子在n至c末端方向上包含:(a)掩蔽部分;(b)第一接头;(c)细胞因子或其功能片段;(d)第二接头,和(e)半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子在c至n末端方向上包含:(a)掩蔽部分;(b)第一接头;(c)细胞因子或其功能片段;(d)第二接头,和(e)半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子在n至c末端方向上包含:(a)细胞因子或其功能片段;(b)第一接头;(c)掩蔽部分;和(d)半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子在c至n末端方向上包含:(a)细胞因子或其功能片段;(b)第一接头;(c)掩蔽部分;和(d)半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子在n至c末端方向上包含:(a)细胞因子或其功能片段;(b)第一接头;(c)掩蔽部分;(d)第二接头;和(e)半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子在c至n末端方向上包含:(a)细胞因子或其功能片段;(b)第一接头;(c)掩蔽部分;(d)第二接头;和(e)半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子在n至c末端方向上包含:(a)半衰期延长结构域;(b)第一接头;(c)掩蔽部分;(d)第二接头;和(e)细胞因子或其功能片段。在一些实施方案中,掩蔽型细胞因子在n至c末端方向上包含:(a)半衰期延长结构域;(b)细胞因子或其功能片段;(c)第一接头;和(d)掩蔽部分。在一些实施方案中,掩蔽型细胞因子包含与选自由seqidno:585-597、602、610-614、627-636、642和643组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含选自由seqidno:585-597、602、610-614、627-636、642和643组成的组的氨基酸序列。在一些实施方案中,掩蔽型细胞因子是表4或表5中所述的任何示例性构建体,或者是通过修饰表4或表5中所述的任何示例性构建体而产生的变体,如通过将一种或多种另外的组分掺入到根据本文教导的构建体的结构中。
本文在一些实施方案中还提供了掩蔽型细胞因子,其包含(a)第一掩蔽部分;(b)细胞因子或其功能片段,其中第一掩蔽部分经由第一接头与细胞因子或其功能片段连接;和(c)第二掩蔽部分,其中第二掩蔽部分经由第二接头与细胞因子或其功能片段连接。在一些实施方案中,掩蔽型细胞因子进一步包含与第一掩蔽部分或第二掩蔽部分连接的半衰期延长结构域。在一些实施方案中,半衰期延长结构域经由第三接头与第一掩蔽部分或第二掩蔽部分连接。
本文在一些实施方案中还提供了掩蔽型细胞因子,其包含(a)第一掩蔽部分,其中第一掩蔽部分与第一半衰期延长结构域连接;(b)细胞因子或其功能片段,其中细胞因子或其功能片段与第二半衰期延长结构域连接;和(c)第二掩蔽部分,其中第二掩蔽部分与第一掩蔽部分连接。在一些实施方案中,第一掩蔽部分经由第一接头与第一半衰期延长结构域连接。在一些实施方案中,第二掩蔽部分经由第二接头与第一掩蔽部分连接。在一些实施方案中,细胞因子或其功能片段经由第三接头与第二半衰期延长结构域连接。在一些实施方案中,第一接头包含可切割肽。在一些实施方案中,第二接头包含可切割肽。在一些实施方案中,第三接头包含可切割肽。
在一些实施方案中,掩蔽型细胞因子在n至c末端方向上包含:(a)第一掩蔽部分;(b)第一接头;(c)细胞因子或其功能片段;(d)第二接头;(e)第二掩蔽部分;和(f)半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子在c至n末端方向上包含:(a)第一掩蔽部分;(b)第一接头;(c)细胞因子或其功能片段;(d)第二接头;(e)第二掩蔽部分;和(f)半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子在n至c末端方向上包含:(a)第一掩蔽部分;(b)第一接头;(c)细胞因子或其功能片段;(d)第二接头;(e)第二掩蔽部分;(f)第三接头;和(g)半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子在c至n末端方向上包含:(a)第一掩蔽部分;(b)第一接头;(c)细胞因子或其功能片段;(d)第二接头;(e)第二掩蔽部分;(f)第三接头;和(g)半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子在n至c末端方向上包含:(a)半衰期延长结构域;(b)第一接头;(c)第一掩蔽部分;(d)第二接头;(e)细胞因子或其功能片段;(f)第三接头;和(g)第二掩蔽部分。在一些实施方案中,掩蔽型细胞因子包含选自由seqidno:567和598-601组成的组的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与选自由seqidno:567和598-601组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,掩蔽型细胞因子是表6或表7中所述的任何示例性构建体,或者是通过修饰表6或表7中所述的任何示例性构建体而产生的变体,如通过将一种或多种另外的组分掺入到根据本文教导的构建体的结构中。
本文在一些实施方案中还提供了掩蔽型细胞因子,其包含(a)第一半衰期延长结构域和第二半衰期延长结构域;(b)掩蔽部分;和(c)细胞因子或其功能片段,其中掩蔽部分与第一半衰期延长结构域连接,细胞因子或其功能片段与第二半衰期延长结构域连接,且第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰。在一些实施方案中,掩蔽部分经由第一接头与第一半衰期延长结构域连接,和/或细胞因子或其功能片段经由第二接头与第二半衰期延长结构域连接。在一些实施方案中,第一半衰期延长结构域任选通过第三接头与第二半衰期延长结构域连接。在一些实施方案中,掩蔽型细胞因子包含(a)包含seqidno:155的氨基酸序列的第一半衰期延长结构域和包含seqidno:156的氨基酸序列的第二半衰期延长结构域;(b)包含seqidno:261的氨基酸序列的掩蔽部分;和(c)包含seqidno:3的氨基酸序列的细胞因子或其功能片段,其中掩蔽部分经由包含seqidno:28的氨基酸序列的第一接头与第一半衰期延长结构域连接,细胞因子或其功能片段经由包含seqidno:811的氨基酸序列的第二接头与第二半衰期延长结构域连接,第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰,且掩蔽型细胞因子包含seqidno:266和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含(a)包含seqidno:155的氨基酸序列的第一半衰期延长结构域和包含seqidno:156的氨基酸序列的第二半衰期延长结构域;(b)包含seqidno:261的氨基酸序列的掩蔽部分;和(c)包含seqidno:260的氨基酸序列的细胞因子或其功能片段,其中掩蔽部分经由包含seqidno:28的氨基酸序列的第一接头与第一半衰期延长结构域连接,细胞因子或其功能片段经由包含seqidno:262的氨基酸序列的第二接头与第二半衰期延长结构域连接,第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰,且掩蔽型细胞因子包含seqidno:266和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含seqidno:266的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含seqidno:267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含seqidno:266和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:266的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:266的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含(a)包含seqidno:155的氨基酸序列的第一半衰期延长结构域和包含seqidno:156的氨基酸序列的第二半衰期延长结构域;(b)包含seqidno:261的氨基酸序列的掩蔽部分;和(c)包含seqidno:3的氨基酸序列的细胞因子或其功能片段,其中掩蔽部分经由包含seqidno:28的氨基酸序列的第一接头与第一半衰期延长结构域连接,细胞因子或其功能片段经由包含seqidno:807的氨基酸序列的第二接头与第二半衰期延长结构域连接,第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰,且掩蔽型细胞因子包含seqidno:679和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含(a)包含seqidno:156的氨基酸序列的第一半衰期延长结构域和包含seqidno:155的氨基酸序列的第二半衰期延长结构域;(b)包含seqidno:261的氨基酸序列的掩蔽部分;和(c)包含seqidno:3的氨基酸序列的细胞因子或其功能片段,其中掩蔽部分经由包含seqidno:28的氨基酸序列的第一接头与第一半衰期延长结构域连接,细胞因子或其功能片段经由包含seqidno:807的氨基酸序列的第二接头与第二半衰期延长结构域连接,第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰,且掩蔽型细胞因子包含seqidno:679和267的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含(a)包含seqidno:155的氨基酸序列的第一半衰期延长结构域和包含seqidno:156的氨基酸序列的第二半衰期延长结构域;(b)包含seqidno:261的氨基酸序列的掩蔽部分;和(c)包含seqidno:3的氨基酸序列的细胞因子或其功能片段,其中掩蔽部分经由第一接头与第一半衰期延长结构域连接,细胞因子或其功能片段经由第二接头与第二半衰期延长结构域连接,第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰,其中第一接头和/或第二接头包含可切割肽。在一些实施方案中,掩蔽型细胞因子包含(a)包含seqidno:156的氨基酸序列的第一半衰期延长结构域和包含seqidno:155的氨基酸序列的第二半衰期延长结构域;(b)包含seqidno:261的氨基酸序列的掩蔽部分;和(c)包含seqidno:3的氨基酸序列的细胞因子或其功能片段,其中掩蔽部分经由第一接头与第一半衰期延长结构域连接,细胞因子或其功能片段经由第二接头与第二半衰期延长结构域连接,第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰,其中第一接头和/或第二接头包含可切割肽。
在一些实施方案中,掩蔽型细胞因子包含(a)包含seqidno:155的氨基酸序列的第一半衰期延长结构域和包含seqidno:156的氨基酸序列的第二半衰期延长结构域;(b)包含seqidno:261的氨基酸序列的掩蔽部分;和(c)包含seqidno:1的氨基酸序列的细胞因子或其功能片段,其中掩蔽部分经由包含seqidno:28的氨基酸序列的第一接头与第一半衰期延长结构域连接,细胞因子或其功能片段经由包含seqidno:812的氨基酸序列的第二接头与第二半衰期延长结构域连接,第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰,且掩蔽型细胞因子包含seqidno:689和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含(a)包含seqidno:156的氨基酸序列的第一半衰期延长结构域和包含seqidno:155的氨基酸序列的第二半衰期延长结构域;(b)包含seqidno:261的氨基酸序列的掩蔽部分;和(c)包含seqidno:1的氨基酸序列的细胞因子或其功能片段,其中掩蔽部分经由包含seqidno:28的氨基酸序列的第一接头与第一半衰期延长结构域连接,细胞因子或其功能片段经由包含seqidno:812的氨基酸序列的第二接头与第二半衰期延长结构域连接,第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰,且掩蔽型细胞因子包含seqidno:689和267的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含(a)包含seqidno:155的氨基酸序列的第一半衰期延长结构域和包含seqidno:156的氨基酸序列的第二半衰期延长结构域;(b)包含seqidno:261的氨基酸序列的掩蔽部分;和(c)包含seqidno:1的氨基酸序列的细胞因子或其功能片段,其中掩蔽部分经由第一接头与第一半衰期延长结构域连接,细胞因子或其功能片段经由第二接头与第二半衰期延长结构域连接,第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰,其中第一接头和/或第二接头包含可切割肽。在一些实施方案中,掩蔽型细胞因子包含(a)包含seqidno:156的氨基酸序列的第一半衰期延长结构域和包含seqidno:155的氨基酸序列的第二半衰期延长结构域;(b)包含seqidno:261的氨基酸序列的掩蔽部分;和(c)包含seqidno:1的氨基酸序列的细胞因子或其功能片段,其中掩蔽部分经由第一接头与第一半衰期延长结构域连接,细胞因子或其功能片段经由第二接头与第二半衰期延长结构域连接,第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰,其中第一接头和/或第二接头包含可切割肽。
在一些实施方案中,掩蔽型细胞因子包含seqidno:562和563的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:562的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:563的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:608和603的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:608的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:603的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:604和603的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:604的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:603的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:605和603的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:605的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:603的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:606和603的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:606的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:603的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:615和617的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:615的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:617的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:618和620的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:618的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:620的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:621和623的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:621的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:623的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:624和626的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:624的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:626的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:608和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:608的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:663和664的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:663的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:664的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:665和666的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:665的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:666的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:667和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:667的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:669和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:669的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:670和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:670的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:672和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:672的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:673和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:673的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:674和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:674的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:675和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:675的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:676和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:676的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:677和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:677的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:678和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:678的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:679和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:679的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:680和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:680的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:681和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:681的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:682和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:682的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:683和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:683的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:684和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:684的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:685和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:685的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:686和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:686的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:687和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:687的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:688和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:688的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:689和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:689的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:690和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:690的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:266和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:266的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:692和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:692的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:693和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:693的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:694和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:694的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:695和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:695的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:696和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:696的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:697和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:697的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:698和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:698的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:699和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:699的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:700和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:700的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:701和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:701的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:702和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:702的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:703和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:703的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:704和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:704的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:705和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:705的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:706和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:706的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:707和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:707的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:708和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:708的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:709和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:709的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:710和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:710的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:711和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:711的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:712和667的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:712的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:667的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:713和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:713的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:714和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:714的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:716和699的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:716的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:699的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:717和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:717的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:718和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:718的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:719和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:719的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:720和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:720的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:722和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:722的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:723和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:723的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:726和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:720的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:728和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:728的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:729和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:729的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:730和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:730的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:731和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:731的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:732和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:732的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:733和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:733的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:734和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:734的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:735和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:735的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:736和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:736的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:737和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:737的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:738和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:738的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:739和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:739的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:740和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:740的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:741和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:741的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:742和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:742的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:743和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:743的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:744和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:744的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:745和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:745的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:746和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:746的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:674和828的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:674的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:828的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:674和829的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:674的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:829的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:726和830的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:726的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:830的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:726和829的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:726的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:829的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:747和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:747的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:715和267的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:715的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:267的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:715和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:715的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:748和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:748的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:749和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:749的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:750和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:750的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:751和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:751的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:752和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:752的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:753和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:753的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:754和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:754的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:758和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:758的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:759和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:759的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:760和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:760的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含seqidno:761和671的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:761的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且包含与seqidno:671的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子是如表8-11中的任一者中所述的示例性掩蔽型细胞因子构建体,或者是通过修饰表8-11中所述的任何示例性构建体产生的变体,如通过将一种或多种另外的组分掺入到根据本文教导的构建体的结构中。
本文在一些实施方案中还提供了掩蔽型细胞因子,其包含(a)第一半衰期延长结构域和第二半衰期延长结构域;(b)第一掩蔽部分和第二掩蔽部分;以及(c)细胞因子或其功能片段,其中第一掩蔽部分与第一半衰期延长结构域连接,第二掩蔽部分与细胞因子或其功能片段连接,第二掩蔽部分或细胞因子或其功能片段与第二半衰期延长结构域连接,且第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰。在一些实施方案中,第一掩蔽部分经由第一接头与第一半衰期延长结构域连接,和/或第二掩蔽部分或细胞因子或其功能片段经由第二接头与第二半衰期延长结构域连接。在一些实施方案中,第二掩蔽部分经由第三接头与细胞因子或其功能片段连接。在一些实施方案中,第一半衰期延长结构域任选通过第四接头与第二半衰期延长结构域连接。在一些实施方案中,掩蔽型细胞因子包含seqidno:755和616的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含seqidno:756和616的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含seqidno:757和616的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:755的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列和与seqidno:616的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:756的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列和与seqidno:616的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与seqidno:757的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列和与seqidno:616的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含选自由seqidno:265-267、556-720、722、723、726、728-761和828-830组成的组的氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含选自由seqidno:265-267、556-720、722、723、726、728-761和828-830组成的组的两个不同氨基酸序列。在一些实施方案中,掩蔽型细胞因子包含与表4-11中所述的任何示例性构建体相关的氨基酸序列。
下文更详细地讨论本文提供的掩蔽型细胞因子的每种组分。
a.细胞因子
本文提供了细胞因子或其功能片段。所述细胞因子或其功能片段可以是任何细胞因子、任何细胞因子的任何功能片段或任何细胞因子的任何天然或非天然变体。细胞因子是在细胞信号传导中,特别是在免疫系统的细胞中起作用的小多肽。细胞因子的实例可包括趋化因子、干扰素、白介素、淋巴因子和肿瘤坏死因子。
细胞因子可以按多种方式进行分类,如基于它们的三维结构。实例包括β-三叶形折叠类、短链四螺旋束类和长链四螺旋束类。
β-三叶形折叠类包括以三个βββ-环-β单元(总共12条β链)为特征的细胞因子,所述单元形成具有筒的发夹帽的筒结构。β-三叶形折叠类中的细胞因子的实例包括il-1α、il-1β、il-1受体拮抗剂(il-1ra)、il-18、il-33、il-36α、il-36β、il-36γ、il-36受体拮抗剂(il-36ra)、il-37和il-38。
短链和长链四螺旋束类的特征在于具有以独特的上-上-下-下拓扑取向的四个两亲性螺旋的单体螺旋束。短链四螺旋束类的特征在于螺旋较短,如长度为10-20个氨基酸残基的那些,而长链四螺旋束类的特征在于螺旋较长,如长度为20-30个氨基酸残基的那些。短链四螺旋束类中的细胞因子的实例包括il-2、il-3、il-4、il-5、il-7、il-9、il-13、il-15、il-21、粒细胞-巨噬细胞集落刺激因子(gm-csf)和巨噬细胞集落刺激因子(m-csf)。长链四螺旋束类中的细胞因子的实例包括il-6、il-11、il-12、生长激素(gh)、促红细胞生成素(epo)、促乳素(prl)、白血病抑制因子(lif)、制瘤素(osm)和促血小板生成素(tpo)。
与为单体的短链和长链四螺旋束类相反,一些细胞因子是同源二聚的。二聚细胞因子的实例包括il-10和ifn-γ(伽玛)。
一些细胞因子被分类为异源二聚的。异源二聚细胞因子的实例包括il-12和il-23。
一些细胞因子如il-15也通过与膜结合细胞因子受体结合并由其呈递而发挥作用。
在一些实施方案中,细胞因子或其功能片段是il-2,或者是il-2的功能片段或变体。在一些实施方案中,细胞因子或其功能片段是il-15,或者是il-15的功能片段或变体。在一些实施方案中,细胞因子或其功能片段选自由il-2、il-10、il-12、il-15、il-18、干扰素(ifn)-α(阿尔法)、ifn-β(贝塔)和ifn-γ(伽玛)组成的组。在一些实施方案中,细胞因子或其功能片段是il-2、il-10、il-12、il-15、il-18、ifn-α(阿尔法)、ifn-β(贝塔)或ifn-γ(伽玛)的功能片段或变体。
在一些实施方案中,细胞因子或其功能片段选自由il-1α、il-1β、il-1受体拮抗剂(il-1ra)、il-18、il-33、il-36α、il-36β、il-36γ、il-36受体拮抗剂(il-36ra)、il-37和il-38组成的组。
在一些实施方案中,细胞因子或其功能片段选自由以下组成的组:il-2、il-3、il-4、il-5、il-7、il-9、il-13、il-15、il-21、粒细胞-巨噬细胞集落刺激因子(gm-csf)、巨噬细胞集落刺激因子(m-csf)、il-6、il-11、il-12、生长激素(gh)、促红细胞生成素(epo)、促乳素(prl)、白血病抑制因子(lif)、制瘤素(osm)和促血小板生成素(tpo)。
在一些实施方案中,细胞因子或其功能片段选自由以下组成的组:cxcl1、cxcl2、cxcl3、cxcl4、cxcl5、cxcl6、cxcl7、cxcl8、cxcl9、cxcl10、cxcl11、cxcl12、cxcl13、cxcl14、cxcl15、cxcl16、ccl1e、ccl2、ccl3、ccl3l1、ccl4、ccl5、ccl6、ccl7、ccl8、ccl9/10、ccl11、ccl12、ccl13、ccl14、ccl15、ccl16、ccl17、ccl18、ccl19、ccl20、ccl21、ccl22、ccl23、ccl24、ccl25、ccl26、ccl27、ccl28、cx3cl1、xcl1和xcl2。在一些实施方案中,细胞因子或其功能片段是cxcl1、cxcl2、cxcl3、cxcl4、cxcl5、cxcl6、cxcl7、cxcl8、cxcl9、cxcl10、cxcl11、cxcl12、cxcl13、cxcl14、cxcl15、cxcl16、ccl1e、ccl2、ccl3、ccl3l1、ccl4、ccl5、ccl6、ccl7、ccl8、ccl9/10、ccl11、ccl12、ccl13、ccl14、ccl15、ccl16、ccl17、ccl18、ccl19、ccl20、ccl21、ccl22、ccl23、ccl24、ccl25、ccl26、ccl27、ccl28、cx3cl1、xcl1或xcl2的功能片段或变体。
在一些实施方案中,细胞因子或其功能片段选自由ifn-α(阿尔法)、ifn-β(贝塔)、ifn-γ(伽玛)、ifn-ε(艾普斯龙)、ifn-κ(卡帕)、
在一些实施方案中,细胞因子或其功能片段选自由以下组成的组:il-1、il-2、il-3、il-4、il-5、il-6、il-7、il-8、il-9、il-10、il-11、il-12、il-13、il-14、il-15、il-16、il-17、il-18、il-19、il-20、il-21、il-22、il-23、il-24、il-25、il-26、il-27、il-28a、il-28b、il-29、il-30、il-31、il-32、il-33、il-34、il-35、il-36和il-37。在一些实施方案中,细胞因子或其功能片段是il-1、il-2、il-3、il-4、il-5、il-6、il-7、il-8、il-9、il-10、il-11、il-12、il-13、il-14、il-15、il-16、il-17a、il-17c、il-17d、il-17f、il-17a/f、il-18、il-19、il-20、il-21、il-22、il-23、il-24、il-25、il-26、il-27、il-28a、il-28b、il-29、il-30、il-31、il-32、il-33、il-34、il-35、il-36或il-37的功能片段或变体。
在一些实施方案中,细胞因子或其功能片段选自由以下组成的组:粒细胞-巨噬细胞集落刺激因子(gm-csf)、巨噬细胞集落刺激因子(m-csf)、肿瘤坏死因子α(tnf-α)、转化生长因子β(tgf-β)、ifn-γ(伽玛)、il-2、il-3、il-4、il-5、il-6、il-7、il-8和il-12。在一些实施方案中,细胞因子或其功能片段是粒细胞-巨噬细胞集落刺激因子(gm-csf)、巨噬细胞集落刺激因子(m-csf)、肿瘤坏死因子α(tnf-α)、转化生长因子β(tgf-β)、ifn-γ(伽玛)、il-2、il-3、il-4、il-5、il-6、il-7、il-8或il-12的功能片段或变体。
在一些实施方案中,细胞因子或其功能片段选自由以下组成的组:tnf-α(阿尔法)、tnf-β(贝塔)、tnf-γ(伽玛)、cd252、cd154、cd178、cd70、cd153、4-1bb-l、trail、rankl、apo3l、cd256、cd257、cd258、tl1、aitrl和eda1。在一些实施方案中,细胞因子或其功能片段是tnf-α(阿尔法)、tnf-β(贝塔)、tnf-γ(伽玛)、cd252、cd154、cd178、cd70、cd153、4-1bb-l、trail、rankl、apo3l、cd256、cd257、cd258、tl1、aitrl和eda1的功能片段或变体。
所述细胞因子或其功能片段包含氨基末端和羧基末端。在一些实施方案中,半衰期延长结构域与细胞因子或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,掩蔽部分与细胞因子或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,接头与细胞因子或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,接头的可切割肽与细胞因子或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,接头的n末端间隔区结构域或c末端间隔区结构域与细胞因子或其功能片段的氨基末端或羧基末端连接。
下面详细提供il-2多肽或其功能片段和il-15多肽或其功能片段形式的细胞因子或其功能片段的示例性实施方案。
1.il-2多肽
在一些实施方案中,细胞因子或其功能片段是il-2多肽或其功能片段。在真核细胞中,il-2作为153个氨基酸的前体多肽被合成,其然后通过移除氨基酸残基1-20被加工成成熟il-2。这产生由133个氨基酸(氨基酸残基21-153)组成的成熟形式的il-2,其以成熟的活性形式被分泌。
在一些实施方案中,il-2多肽或其功能片段是能够与白介素-2受体(il-2r)或其组分(例如,il-2rα链)结合或以其它方式表现出对白介素-2受体(il-2r)或其组分(例如,il-2rα链)的亲和力的任何天然存在的白介素-2(il-2)蛋白或其修饰变体。在一些实施方案中,il-2多肽或其功能片段是由seqidno:159的氨基酸残基21-153组成的成熟形式的il-2。在一些实施方案中,il-2多肽或其功能片段包含seqidno:160的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含选自由seqidno:1-8和260组成的组的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含seqidno:260的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含选自由seqidno:1-8、160、230、243-251、260、775-792和813-822组成的组的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含与选自由seqidno:1-8、160、243-251、260、775-792和813-822组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含seqidno:230的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含与seqidno:230的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含seqidno:3的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含与seqidno:3的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,il-2多肽或其功能片段包含通过对选自由seqidno:1-8、160、230、243-251、260、775-792和813-822组成的组的氨基酸序列进行至少一个氨基酸修饰而产生的氨基酸序列。至少一个氨基酸修饰中的每一者可以是任何氨基酸修饰,如取代、插入或缺失。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、230、243-251、260、775-792和813-822中的任一者的氨基酸序列中的至少1个、至少2个、至少3个、至少4个、至少5个、至少6个、至少7个、至少8个、至少9个或至少10个氨基酸取代产生的氨基酸序列。在一些实施方案中,il-2肽或其功能片段包含在氨基酸残基125处包含丝氨酸(s)、甘氨酸(g)或丙氨酸(a)残基的氨基酸序列。在一些实施方案中,il-2肽或其功能片段包含在氨基酸残基3处包含丙氨酸(a)残基的氨基酸序列。例如,在一些实施方案中,il-2肽或其功能片段包含通过向选自由seqidno:1-8和160组成的组的氨基酸序列中引入t3a氨基酸取代而产生的氨基酸序列。在一些实施方案中,il-2肽或其功能片段包含选自由seqidno:243-251和260组成的组的氨基酸序列。在一些实施方案中,il-2肽或其功能片段包含选自由seqidno:775-792和813-822组成的组的氨基酸序列。
在一些实施方案中,il-2肽或其功能片段包含与野生型il-2的氨基酸序列相比具有一个或多个降低il-2肽或其功能片段对il-2rα(cd25)的亲和力的氨基酸取代的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基38、42、45和62中的一者或多者是丙氨酸(a)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基38、42、45和62是丙氨酸(a)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基38、42、45和62是丙氨酸(a),且氨基酸残基125是丝氨酸(s)、甘氨酸(g)或丙氨酸(a)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基38和42是丙氨酸(a),且氨基酸残基125是丝氨酸(s)、甘氨酸(g)或丙氨酸(a)。在一些实施方案中,il-2多肽或其功能片段包含通过在seqidno:160或251的氨基酸序列中用氨基酸残基r38、f42、y45和e62取代丙氨酸而产生的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含通过在seqidno:160或251的氨基酸序列中用氨基酸残基r38、f42、y45和e62取代丙氨酸(a)和用氨基酸残基c125取代丝氨酸(s)、甘氨酸(g)或丙氨酸(a)产生的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基42是赖氨酸(k)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基42是赖氨酸(k),且氨基酸残基125是丝氨酸(s)、甘氨酸(g)或丙氨酸(a)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基42和45是丙氨酸(a),且氨基酸残基72是甘氨酸(g)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基42和45是丙氨酸(a),氨基酸残基72是甘氨酸(g),且氨基酸残基125是丝氨酸(s)、甘氨酸(g)或丙氨酸(a)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基62是精氨酸(r)或丝氨酸(s)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基42是谷氨酸(e)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基43是丙氨酸(a)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基45是天冬酰胺(n)、精氨酸(r)或丙氨酸(a)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基45是丙氨酸(a),且氨基酸残基62是丝氨酸(s)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基42是丝氨酸(s),氨基酸残基62是丝氨酸(s)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基38是甘氨酸(g),氨基酸残基45是丙氨酸(a),且氨基酸残基62是丝氨酸(s)。
在一些实施方案中,il-2肽或其功能片段包含通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代中的一者或多者而产生的氨基酸序列:r38a、f42a、f42e、f42k、k43a、y45a、y45n、y45r、e62a、e62r、e62s、l72g、c125s、c125g和c125a。
在一些实施方案中,il-2多肽或其功能片段包含与野生型il-2的氨基酸序列相比具有一个或多个增强il-2多肽或其功能片段对il-2rβ(cd122)的亲和力的氨基酸取代的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基80是苯丙氨酸(f),氨基酸残基81是天冬氨酸(d),氨基酸残基85是缬氨酸(v),氨基酸残基86是缬氨酸(v),或者氨基酸残基92是苯丙氨酸(f),或其组合。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基80是苯丙氨酸(f),氨基酸残基81是天冬氨酸(d),氨基酸残基85是缬氨酸(v),氨基酸残基86是缬氨酸(v),或者氨基酸残基92是苯丙氨酸(f),或其组合,且氨基酸残基125是丝氨酸(s)、甘氨酸(g)或丙氨酸(a)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基80是苯丙氨酸(f),氨基酸残基81是天冬氨酸(d),氨基酸残基85是缬氨酸(v),氨基酸残基86是缬氨酸(v),且氨基酸残基92是苯丙氨酸(f)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基80是苯丙氨酸(f),氨基酸残基81是天冬氨酸(d),氨基酸残基85是缬氨酸(v),氨基酸残基86是缬氨酸(v),氨基酸残基92是苯丙氨酸(f),且氨基酸残基125是丝氨酸(s)、甘氨酸(g)或丙氨酸(a)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基18是半胱氨酸(c)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基20是丙氨酸(a)、亮氨酸(l)或苯丙氨酸(f)。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基16是异亮氨酸。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基29是亮氨酸(l)。
在一些实施方案中,il-2肽或其功能片段包含通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代中的一者或多者而产生的氨基酸序列:l18c、d20a、d20l、d20f、h16i、n29l、l80f、r81d、l85v、i86v、i92f、c125s、c125g和c125a。
在一些实施方案中,il-2多肽或其功能片段包含与野生型il-2的氨基酸序列相比具有一个或多个降低il-2肽或其功能片段对il-2rα(cd25)的亲和力的氨基酸取代和与野生型il-2的氨基酸序列相比具有一个或多个增强il-2多肽或其功能片段对il-2rβ(cd122)的亲和力的氨基酸取代的氨基酸序列。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基38、42、45和62中的一者或多者是丙氨酸(a),氨基酸残基42是赖氨酸(k),氨基酸残基72是甘氨酸(g),氨基酸残基80是苯丙氨酸(f),氨基酸残基81是天冬氨酸(d),氨基酸残基85是缬氨酸(v),氨基酸残基86是缬氨酸(v),或者氨基酸残基92是苯丙氨酸(f),或其组合。如此,在一些实施方案中,il-2多肽或其功能片段包含与成熟形式的野生型il-2相比包含以下氨基酸取代中的一者或多者的氨基酸序列:d20a、d20l、d20f、h16i、l18c、n29l、r38a、f42a、f42e、f42k、k43a、y45a、y45n、y45r、e62a、e62r、e62s、l72g、l80f、r81d、l85v、i86v、i92f、c125s、c125g和c125a。
在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基38是甘氨酸(g)、丙氨酸(a)、赖氨酸(k)或色氨酸(w),氨基酸残基42是丙氨酸(a)、赖氨酸(k)或异亮氨酸(i),氨基酸残基45是丙氨酸(a)或天冬酰胺(n),氨基酸残基62是丙氨酸(a)或亮氨酸(l),或者氨基酸残基68是缬氨酸(v),或其组合。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基38是赖氨酸(k),氨基酸残基42是谷氨酰胺(q),氨基酸残基45是谷氨酸(e),或者氨基酸残基68是缬氨酸(v),或其组合。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基38是丙氨酸(a),氨基酸残基42是异亮氨酸(i),氨基酸残基45是天冬酰胺(n),氨基酸残基62是亮氨酸(l),或者氨基酸残基68是缬氨酸(v),或其组合。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基38是赖氨酸(k),氨基酸残基42是赖氨酸(k),氨基酸残基45是精氨酸(r),氨基酸残基62是亮氨酸(l),或者氨基酸残基68是缬氨酸(v),或其组合。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基38是丙氨酸(a)或赖氨酸(k),氨基酸残基42是丙氨酸(a),氨基酸残基45是丙氨酸(a),或者氨基酸残基62是丙氨酸(a),或其组合。在一些实施方案中,il-2多肽或其功能片段包含由seqidno:1-8、160、243-251、260、775-792和813-822中的任一者的氨基酸序列中的一个或多个氨基酸取代产生的氨基酸序列,使得氨基酸残基42是异亮氨酸(i),氨基酸残基45是谷氨酸(e),或者氨基酸残基68是缬氨酸(v),或其组合。
在一些实施方案中,il-2多肽或其功能片段包含通过向针对本文所述的il-2多肽或其功能片段的氨基酸序列中的任一者中引入或进一步引入c125s、c125g或c125a取代而产生的氨基酸序列。
在一些实施方案中,出于移除o-糖基化位点的目的,从il-2多肽或其功能片段的氨基酸序列中移除一个或多个氨基酸残基。在一些实施方案中,il-2多肽或其功能片段包含通过缺失本文公开的任何il-2多肽或其功能片段的氨基酸序列的前三个氨基酸残基(残基1-3)而产生的氨基酸序列。在一些实施方案中,出于移除o-糖基化位点的目的,将一个或多个氨基酸残基取代到il-2多肽或其功能片段的氨基酸序列中。在一些实施方案中,il-2多肽或其功能片段包含通过向本文公开的任何il-2多肽或其功能片段的氨基酸序列的前三个氨基酸残基(残基1-3)中的一者或多者中引入氨基酸取代而产生的氨基酸序列。
il-2多肽或其功能片段包含氨基末端和羧基末端。在一些实施方案中,半衰期延长结构域与il-2多肽或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,掩蔽部分与il-2多肽或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,接头与il-2多肽或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,接头的可切割肽与il-2多肽或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,接头的n末端间隔区结构域或c末端间隔区结构域与il-2多肽或其功能片段的氨基末端或羧基末端连接。
2.il-15多肽
在一些实施方案中,细胞因子或其功能片段是il-15多肽或其功能片段。在真核细胞中,il-15作为162个氨基酸的前体多肽被合成,其然后通过移除氨基酸残基1-48被加工成成熟il-15。这产生由114个氨基酸(氨基酸残基49-162)组成的成熟形式的il-15,其以成熟的活性形式被分泌(参见seqidno:167)。
在一些实施方案中,il-15多肽或其功能片段是能够与白介素-15受体(il-15r)或其组分(例如,il-15rα、il-2rβ和/或il-2rγ链)结合或以其它方式表现出对白介素-15受体(il-15r)或其组分(例如,il-15rα、il-2rβ和/或il-2rγ链)的亲和力的任何天然存在的白介素-15(il-15)蛋白或其修饰变体。在一些实施方案中,il-15多肽或其功能片段是由seqidno:166的氨基酸残基49-162组成的成熟形式的il-15。在一些实施方案中,il-15多肽或其功能片段包含seqidno:167的氨基酸序列。在一些实施方案中,il-15多肽或其功能片段包含与seqidno:166或167的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,il-15多肽或其功能片段包含通过对seqidno:167的氨基酸序列进行至少一个氨基酸修饰而产生的氨基酸序列。至少一个氨基酸修饰中的每一者可以是任何氨基酸修饰,如取代、插入或缺失。在一些实施方案中,il-15多肽或其功能片段包含由seqidno:167的氨基酸序列中的至少1个、至少2个、至少3个、至少4个、至少5个、至少6个、至少7个、至少8个、至少9个或至少10个氨基酸取代产生的氨基酸序列。
il-15多肽或其功能片段包含氨基末端和羧基末端。在一些实施方案中,半衰期延长结构域与il-15多肽或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,掩蔽部分与il-15多肽或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,接头与il-15多肽或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,接头的可切割肽与il-15多肽或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,接头的n末端间隔区结构域或c末端间隔区结构域与il-15多肽或其功能片段的氨基末端或羧基末端连接。
b.掩蔽部分
如本文提供的掩蔽部分是指能够与细胞因子或其功能片段结合或以其它方式表现出对细胞因子或其功能片段的亲和力的部分,使得在一些实施方案中,所述结合降低细胞因子或其功能片段对其同源受体或蛋白质的亲和力。例如,针对il-2多肽或其功能片段的掩蔽部分能够与il-2多肽或其功能片段结合或以其它方式表现出对il-2多肽或其功能片段的亲和力,使得在一些实施方案中,所述结合降低il-2多肽或其功能片段对其同源受体或蛋白质(例如,il-2r或其组分,如il-2rα和/或il-2rβ链)的亲和力。当与细胞因子或其功能片段结合时,掩蔽部分阻断、封闭、抑制(例如降低)或以其它方式阻止(例如,掩蔽)细胞因子或其功能片段的活性或与其同源受体或蛋白质的结合。在包括第一掩蔽部分和第二掩蔽部分的一些实施方案中,掩蔽部分之一(例如,第一掩蔽部分)的存在阻断、封闭、抑制(例如降低)或以其它方式阻止(例如,掩蔽)细胞因子或其功能片段的活性或与其同源受体或蛋白质的结合,而在一些实施方案中,另一掩蔽部分(例如,第二掩蔽部分)可在第一掩蔽部分切割之后保持与细胞因子或其功能片段缔合,并且仍然允许或者有可能甚至促进细胞因子或其功能片段与其同源受体或蛋白质在结合第一掩蔽部分的位点的结合。参见例如图7b。测定蛋白质(例如,细胞因子)与同源蛋白质(例如,细胞因子受体)结合程度的方法是本领域中熟知的。
本文提供的掩蔽型细胞因子包含掩蔽部分。掩蔽部分包含氨基末端和羧基末端。在一些实施方案中,掩蔽型细胞因子包含单个掩蔽部分。在一些实施方案中,掩蔽型细胞因子包含一个以上掩蔽部分,其每一者可以是本文所述的任何掩蔽部分。在一些实施方案中,掩蔽型细胞因子包含第一掩蔽部分和第二掩蔽部分。要理解的是,例如提到“掩蔽部分”或“所述掩蔽部分”可指包含单个掩蔽部分的掩蔽型细胞因子中的掩蔽部分,或者其可指包含第一掩蔽部分和第二掩蔽部分的掩蔽型细胞因子中的第一掩蔽部分,或者其可指包含第一掩蔽部分和第二掩蔽部分的掩蔽型细胞因子中的第二掩蔽部分,或者其可指包含第一掩蔽部分和第二掩蔽部分的掩蔽型细胞因子中的第一掩蔽部分和第二掩蔽部分。
在一些实施方案中,掩蔽部分与细胞因子或其功能片段连接。在一些实施方案中,掩蔽部分经由第一接头与细胞因子或其功能片段连接。在一些实施方案中,掩蔽型细胞因子包含与掩蔽部分连接的半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子包含经由第二接头与掩蔽部分连接的半衰期延长结构域。在一些实施方案中,掩蔽部分与细胞因子或其功能片段连接,并与半衰期延长结构域连接。在一些实施方案中,细胞因子或其功能片段与掩蔽肽的氨基末端连接,且半衰期延长结构域与掩蔽肽的羧基末端连接。在一些实施方案中,细胞因子或其功能片段与掩蔽肽的羧基末端连接,且半衰期延长结构域与掩蔽肽的氨基末端连接。在一些实施方案中,半衰期延长结构域与掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,第二接头与掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,掩蔽部分与第一接头连接,并且与第二接头连接。在一些实施方案中,第一接头与掩蔽肽的氨基末端连接,且第二接头与掩蔽肽的羧基末端连接。在一些实施方案中,第一接头与掩蔽肽的羧基末端连接,且第二接头与掩蔽肽的氨基末端连接。
在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分与细胞因子或其功能片段连接,且第二掩蔽部分与细胞因子或其功能片段连接。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分经由第一接头与细胞因子或其功能片段连接,且第二掩蔽部分经由第二接头与细胞因子或其功能片段连接。在一些实施方案中,掩蔽型细胞因子包含与第一掩蔽部分或第二掩蔽部分连接的半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子包含经由第三接头与第一掩蔽部分或第二掩蔽部分连接的半衰期延长结构域。在一些实施方案中,第一接头与第一掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,第二接头与第二掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,半衰期延长结构域与第一掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,半衰期延长结构域与第二掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,第三接头与第一掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,第三接头与第二掩蔽部分的氨基末端或羧基末端连接。
在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分与第一半衰期延长结构域连接,第二掩蔽部分与第一掩蔽部分连接,且细胞因子或其功能片段与第二半衰期延长结构域连接。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分经由第一接头与第一半衰期延长结构域连接,第二掩蔽部分经由第二接头与第一掩蔽部分连接,且细胞因子或其功能片段经由第三接头与第二半衰期延长结构域连接。在一些实施方案中,第一接头与第一半衰期延长结构域的氨基末端或羧基末端连接。在一些实施方案中,第二接头与第二掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,第二半衰期延长结构域与细胞因子或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,第一半衰期延长结构域与第一掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,第三接头与第二半衰期延长结构域的氨基末端或羧基末端连接。在一些实施方案中,第三接头与细胞因子或其功能片段的氨基末端或羧基末端连接。
在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第二掩蔽部分与第一半衰期延长结构域连接,第一掩蔽部分与第二掩蔽部分连接,且细胞因子或其功能片段与第二半衰期延长结构域连接。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第二掩蔽部分经由第一接头与第一半衰期延长结构域连接,第一掩蔽部分经由第二接头与第二掩蔽部分连接,且细胞因子或其功能片段经由第三接头与第二半衰期延长结构域连接。在一些实施方案中,第一接头与第一半衰期延长结构域的氨基末端或羧基末端连接。在一些实施方案中,第二接头与第一掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,第二半衰期延长结构域与细胞因子或其功能片段的氨基末端或羧基末端连接。在一些实施方案中,第一半衰期延长结构域与第二掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,第三接头与第二半衰期延长结构域的氨基末端或羧基末端连接。在一些实施方案中,第三接头与细胞因子或其功能片段的氨基末端或羧基末端连接。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,掩蔽部分与第一半衰期延长结构域连接。在一些实施方案中,第一半衰期延长结构域与掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,掩蔽部分经由第一接头与第一半衰期延长结构域连接。在一些实施方案中,第一接头与掩蔽部分的氨基末端或羧基末端连接。
在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分与第一半衰期延长结构域连接,且第二掩蔽部分与细胞因子或其功能片段连接。在一些实施方案中,第二掩蔽部分进一步与第二半衰期延长结构域连接。在一些实施方案中,第一掩蔽部分经由第一接头与第一半衰期延长结构域连接,和/或第二掩蔽部分或细胞因子或其功能片段经由第二接头与第二半衰期延长结构域连接。在一些实施方案中,第二掩蔽部分经由第三接头与细胞因子或其功能片段连接。
在一些实施方案中,第一半衰期延长结构域与第一掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,细胞因子或其功能片段与第二掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,第一接头与第一掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,第二接头与第二掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,第三接头与第二掩蔽部分的氨基末端或羧基末端连接。在一些实施方案中,第二接头与第二掩蔽部分的氨基末端连接,且第三接头与第二掩蔽部分的羧基末端连接。在一些实施方案中,第二接头与第二掩蔽部分的羧基末端连接,且第三接头与第二掩蔽部分的氨基末端连接。
在一些实施方案中,掩蔽部分包含选自由seqidno:9、10、161-165、187-218、221-229、231和261组成的组的氨基酸序列。在一些实施方案中,掩蔽部分包含与选自由seqidno:9、10、161-165、187-218、221-229、231和261组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,掩蔽部分包含seqidno:261的氨基酸序列。在一些实施方案中,掩蔽部分包含与seqidno:261的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含第一掩蔽部分和第二掩蔽部分。在一些实施方案中,第一掩蔽部分包含seqidno:9或231的氨基酸序列,且第二掩蔽部分包含选自由seqidno:10、161-165、187-218、221-229和261组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与seqidno:9或231的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与选自由seqidno:10、161-165、187-218、221-229和261组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第一掩蔽部分包含选自由seqidno:10、161-165、187-218、221-229和261组成的组的氨基酸序列,且第二掩蔽部分包含seqidno:9或231的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与选自由seqidn0:10、161-165、187-218、221-229和261组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与seqidno:9或231的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第一掩蔽部分包含seqidno:9或231的氨基酸序列,且第二掩蔽部分包含seqidno:261的氨基酸序列。在一些实施方案中,第二掩蔽部分包含seqidno:9或231的氨基酸序列,且第一掩蔽部分包含seqidno:261的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与seqidno:261的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与seqidno:9或231的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第二掩蔽部分包含与seqidno:261的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第一掩蔽部分包含与seqidno:9或231的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,第一掩蔽部分包含seqidno:9或231的氨基酸序列,且第二掩蔽部分包含选自由seqidno:10、161-165、221-226和261组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与seqidno:9或231的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与选自由seqidno:10、161-165、221-226和261组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第一掩蔽部分包含选自由seqidno:10、161-165、221-226和261组成的组的氨基酸序列,且第二掩蔽部分包含seqidno:9或231的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与自由seqidno:10、161-165、221-226和261组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与seqidno:9或231的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第一掩蔽部分包含seqidno:9或231的氨基酸序列,且第二掩蔽部分包含选自由seqidno:10、161-165、221-226、261、826和827组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与seqidno:9或231的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与选自由seqidno:10、161-165、221-226、261、826和827组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第二掩蔽部分包含seqidno:9或231的氨基酸序列,且第一掩蔽部分包含选自由seqidno:10、161-165、221-226、261、826和827组成的组的氨基酸序列。在一些实施方案中,第二掩蔽部分包含与seqidno:9或231的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第一掩蔽部分包含与选自由seqidno:10、161-165、221-226、261、826和827组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,第一掩蔽部分包含seqidno:9或231的氨基酸序列,且第二掩蔽部分包含选自由seqidno:187-218组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与seqidno:9或231的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与选自由seqidno:187-218组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第一掩蔽部分包含选自由seqidno:187-218组成的组的氨基酸序列,且第二掩蔽部分包含seqidno:9或231的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与选自由seqidno:187-218组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与seqidno:9或231的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,第一掩蔽部分包含seqidno:9或231的氨基酸序列,且第二掩蔽部分包含选自由seqidno:227-229组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与seqidno:9或231的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与选自由seqidno:227-229组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第一掩蔽部分包含选自由seqidno:227-229组成的组的氨基酸序列,且第二掩蔽部分包含seqidno:9或231的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与选自由seqidno:227-229组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与seqidno:9或231的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,第一掩蔽部分包含seqidno:9的氨基酸序列,且第二掩蔽部分包含seqidno:10的氨基酸序列。在一些实施方案中,第一掩蔽部分包含seqidno:10的氨基酸序列,且第二掩蔽部分包含seqidno:9的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与seqidno:9的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与seqidno:10的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与seqidno:10的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与seqidno:9的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,掩蔽部分包含通过对seqidno:10或261进行以下氨基酸取代中的一者或多者产生的氨基酸序列:c122s、c168s、r42a、k71a、t73a、t74a、v75a、h133a、y134a、r137d、q162w、e170a和q188a。在一些实施方案中,包含通过一个或多个氨基酸取代产生的氨基酸序列的掩蔽部分包含seqidno:826的氨基酸序列。
在一些实施方案中,掩蔽部分包含选自由seqidno:10、161-165、219-229、232-234、261和823-825组成的组的氨基酸序列。在一些实施方案中,掩蔽部分包含与选自由seqidno:10、161-165、219-229、232-234、261和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,掩蔽部分包含seqidno:261的氨基酸序列。在一些实施方案中,掩蔽部分包含与seqidno:261的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,掩蔽部分包含seqidno:826或827的氨基酸序列,或者包含与seqidno:826或827的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽型细胞因子包含第一掩蔽部分和第二掩蔽部分。在一些实施方案中,第一掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:10、161-165、219-229和261组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含选自由seqidno:10、161-165、219-229和261组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与选自由seqidno:10、161-165、219-229和261组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与选自由seqidno:232-234和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第二掩蔽部分包含与选自由seqidno:10、161-165、219-229和261组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第一掩蔽部分包含与选自由seqidno:232-234和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,第一掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:10、161-165、219-229、261、826和827组成的组的氨基酸序列。在一些实施方案中,第二掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列,且第一掩蔽部分包含选自由seqidno:10、161-165、219-229、261、826和827组成的组的氨基酸序列。在一些实施方案中,所述第一掩蔽部分包含与选自由seqidno:10、161-165、219-229、261、826和827组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与选自由seqidno:232-234和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第二掩蔽部分包含与选自由seqidno:10、161-165、219-229、261、826和827组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第一掩蔽部分包含与选自由seqidno:232-234和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第一掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列,且第二掩蔽部分包含seqidno:826或827的氨基酸序列。在一些实施方案中,第二掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列,且第一掩蔽部分包含seqidno:826或827的氨基酸序列。
在一些实施方案中,第一掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:10、161-165、221-226和261组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含选自由seqidno:10、161-165、221-226和261组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与选自由seqidno:10、161-165、221-226和261组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与选自由seqidno:232-234和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第二掩蔽部分包含与选自由seqidno:10、161-165、221-226和261组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第一掩蔽部分包含与选自由seqidno:232-234和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,第一掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:227-229组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含选自由seqidno:227-229组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与选自由seqidno:227-229组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与选自由seqidno:232-234和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第二掩蔽部分包含与选自由seqidno:227-229组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第一掩蔽部分包含与选自由seqidno:232-234和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,第一掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:219和220组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含选自由seqidno:219和220组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列。在一些实施方案中,第一掩蔽部分包含与选自由seqidno:219和220组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二掩蔽部分包含与选自由seqidno:232-234和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,第二掩蔽部分包含与选自由seqidno:219和220组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第一掩蔽部分包含与选自由seqidno:232-234和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,掩蔽部分包含通过向seqidno:232-234和823-825中的任一者的氨基酸序列中引入以下氨基酸取代中的一者或多者而产生的氨基酸序列:r24a、r26a、k34a、s40a、l42a和p67a。在一些实施方案中,掩蔽部分包含与选自由seqidno:232-234和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,并且通过向与选自由seqidno:232-234和823-825组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列中引入以下氨基酸取代中的一者或多者被进一步修饰:r24a、r26a、k34a、s40a、l42a和p67a。
在一些实施方案中,掩蔽部分包含保持或以其它方式显示出对il-2的亲和力的il-2rα(也称为cd25)或其片段、部分或变体。在一些实施方案中,掩蔽部分包含il-2rα(也称为cd25)或其片段、部分或变体,并且包含seqidno:9或231的氨基酸序列。在一些实施方案中,掩蔽部分包含保持或以其它方式显示出对il-2和/或il-15的亲和力的il-2rβ(也称为cd122)或其片段、部分或变体。在一些实施方案中,掩蔽部分包含il-2rβ(也称为cd122)或其片段、部分或变体,并且包含选自由seqidno:10、161-165、221-226、261、826和827组成的组的氨基酸序列。在一些实施方案中,掩蔽部分包含保持或以其它方式显示出对il-2和/或il-15的亲和力的il-2rγ(也称为cd132)或其片段、部分或变体。在一些实施方案中,掩蔽部分包含保持或以其它方式显示出对il-15的亲和力的il-15rα(也称为cd215)或其片段、部分或变体。在一些实施方案中,掩蔽部分包含il-15rα(也称为cd215)或其片段、部分或变体,并且包含选自由seqidno:232-234和823-825组成的组的氨基酸序列。在一些实施方案中,掩蔽部分包含抗体或其片段的抗原结合结构域。在一些实施方案中,掩蔽部分包含抗il-2抗体或其片段的抗原结合结构域。在一些实施方案中,掩蔽部分包含抗il-15抗体或其片段的抗原结合结构域。
在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分包含保持或以其它方式显示出对il-2的亲和力的il-2rα或其片段、部分或变体,且第二掩蔽部分包含保持或以其它方式显示出对il-2的亲和力的il-2rβ或其片段、部分或变体。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分包含保持或以其它方式显示出对il-2的亲和力的il-2rβ或其片段、部分或变体,且第二掩蔽部分包含保持或以其它方式显示出对il-2的亲和力的il-2rα或其片段、部分或变体。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分包含保持或以其它方式显示出对il-2的亲和力的il-2rα或其片段、部分或变体,且第二掩蔽部分包含保持或以其它方式显示出对il-2的亲和力的il-2rγ或其片段、部分或变体。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分包含保持或以其它方式显示出对il-2的亲和力的il-2rγ或其片段、部分或变体,且第二掩蔽部分包含保持或以其它方式显示出对il-2的亲和力的il-2rα或其片段、部分或变体。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分包含保持或以其它方式显示出对il-2的亲和力的il-2rα或其片段、部分或变体,且第二掩蔽部分包含抗il-2抗体或其片段的抗原结合结构域。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分包含抗il-2抗体或其片段的抗原结合结构域,且第二掩蔽部分包含保持或以其它方式显示出对il-2的亲和力的il-2rα或其片段、部分或变体。
在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分包含保持或以其它方式显示出对il-15的亲和力的il-15rα或其片段、部分或变体,且第二掩蔽部分包含保持或以其它方式显示出对il-15的亲和力的il-2rβ或其片段、部分或变体。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分包含保持或以其它方式显示出对il-15的亲和力的il-2rβ或其片段、部分或变体,且第二掩蔽部分包含保持或以其它方式显示出对il-15的亲和力的il-15rα或其片段、部分或变体。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分包含保持或以其它方式显示出对il-15的亲和力的il-15rα或其片段、部分或变体,且第二掩蔽部分包含保持或以其它方式显示出对il-15的亲和力的il-2rγ或其片段、部分或变体。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分包含保持或以其它方式显示出对il-15的亲和力的il-2rγ或其片段、部分或变体,且第二掩蔽部分包含保持或以其它方式显示出对il-15的亲和力的il-15rα或其片段、部分或变体。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分包含保持或以其它方式显示出对il-15的亲和力的il-15rα或其片段、部分或变体,并且第二掩蔽部分包含抗il-15抗体或其片段的抗原结合结构域。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分包含抗il-15抗体或其片段的抗原结合结构域,且第二掩蔽部分包含保持或以其它方式显示出对il-15的亲和力的il-15rα或其片段、部分或变体。
c.接头
如本文提供的接头是指用于将两种组分如本文所述的任何掩蔽型细胞因子的两种组分连接在一起的两个以上氨基酸的肽。在一些实施方案中,接头包含可切割肽。在一些实施方案中,接头包含氨基末端间隔区结构域(n末端间隔区结构域)和/或羧基末端间隔区结构域(c末端间隔区结构域)。在一些实施方案中,接头包含n末端间隔区结构域、可切割肽和/或c末端间隔区结构域。在一些实施方案中,接头由n末端间隔区结构域组成。在一些实施方案中,接头由c末端间隔区结构域组成。在一些实施方案中,接头由n末端间隔区结构域和c末端间隔区结构域组成。在一些实施方案中,接头由可切割肽组成。在一些实施方案中,接头由n末端间隔区结构域、可切割肽和c末端间隔区结构域组成。在一些实施方案中,接头由n末端间隔区结构域和可切割肽组成。在一些实施方案中,接头由可切割肽和c末端间隔区结构域组成。在一些实施方案中,接头由可切割肽组成。
在一些实施方案中,掩蔽型细胞因子包含接头。在一些实施方案中,掩蔽型细胞因子包含单个接头。在一些实施方案中,掩蔽型细胞因子包含一个以上接头,其每一者可以是本文所述的任何接头。在一些实施方案中,掩蔽型细胞因子包含第一接头和第二接头。在一些实施方案中,掩蔽型细胞因子包含第一接头、第二接头和第三接头。在一些实施方案中,掩蔽型细胞因子包含第一接头、第二接头、第三接头和第四接头。例如,提到“接头”或“所述接头”可指包含单个接头的掩蔽型细胞因子中的接头,或者其可指包含第一接头和第二接头的掩蔽型细胞因子中的第一接头,或者其可指包含第一接头和第二接头的掩蔽型细胞因子中的第二接头,或者其可指包含第一接头和第二接头的掩蔽型细胞因子中的第一接头和第二接头,或者其可指包含第一接头、第二接头和第三接头的掩蔽型细胞因子中的第一接头、第二接头和/或第三接头,或者其可指包含第一接头、第二接头、第三接头和第四接头的掩蔽型细胞因子中的第一接头、第二接头、第三接头和/或第四接头。
要理解的是,以下术语中的每一者被认为是如本文所述的“接头”:接头、第一接头、第二接头、第三接头和第四接头,以及任何其它编号的接头(例如,第五接头、第六接头等)。如此,在一些实施方案中,掩蔽型细胞因子可包含接头、第一接头、第二接头、第三接头和/或第四接头,其每一者被认为是如本文所述的“接头”,并且本文所述的任何接头可以是如本文所述的接头、第一接头、第二接头、第三接头和/或第四接头。
还要理解的是,“连接”在一起的两种组分包括其中两种组分直接连接在一起的实施方案以及其中两种组分经由如本文所述的接头连接在一起的实施方案。例如,“与掩蔽部分连接的半衰期延长结构域”被解释为意指半衰期延长结构域的氨基酸序列直接与掩蔽部分的氨基酸序列连接,或者半衰期延长结构域的氨基酸序列经由接头如本文所述的任何接头与掩蔽部分的氨基酸序列连接。
接头包含氨基末端和羧基末端。在一些实施方案中,掩蔽部分与接头的氨基末端或羧基末端连接。在一些实施方案中,细胞因子或其功能片段与接头的氨基末端或羧基末端连接。在一些实施方案中,细胞因子或其功能片段与接头的氨基末端连接,且掩蔽部分与接头的羧基末端连接。在一些实施方案中,细胞因子或其功能片段与接头的羧基末端连接,且掩蔽部分与接头的氨基末端连接。在一些实施方案中,半衰期延长结构域与接头的氨基末端或羧基末端连接。在一些实施方案中,半衰期延长结构域与接头的氨基末端连接,掩蔽部分与接头的羧基末端连接。在一些实施方案中,半衰期延长结构域与接头的羧基末端连接,且掩蔽部分与接头的氨基末端连接。在一些实施方案中,半衰期延长结构域与接头的氨基末端连接,且细胞因子或其功能片段与接头的羧基末端连接。在一些实施方案中,半衰期延长结构域与接头的羧基末端连接,且细胞因子或其功能片段与接头的氨基末端连接。
在包含各自与细胞因子或其功能片段连接的第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分或第二掩蔽部分与接头的氨基末端连接,且细胞因子或其功能片段与接头的羧基末端连接。在包含各自与细胞因子或其功能片段连接的第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分或第二掩蔽部分与接头的羧基末端连接,且细胞因子或其功能片段与接头的氨基末端连接。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,掩蔽部分与接头的氨基末端连接,且第一半衰期延长结构域或第二半衰期延长结构域与接头的羧基末端连接。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,掩蔽部分与接头的羧基末端连接,且第一半衰期延长结构域或第二半衰期延长结构域与接头的氨基末端连接。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,细胞因子或其功能片段与接头的氨基末端连接,且第一半衰期延长结构域或第二半衰期延长结构域与接头的羧基末端连接。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,细胞因子或其功能片段与接头的羧基末端连接,且第一半衰期延长结构域或第二半衰期延长结构域与接头的氨基末端连接。
在包含与第一半衰期延长结构域连接的第一掩蔽部分、与细胞因子或其功能片段连接的第二掩蔽部分且其中第二掩蔽部分或细胞因子或其功能片段与第二半衰期延长结构域连接的一些实施方案中,第一掩蔽部分与接头的氨基末端连接,且第一半衰期延长结构域与接头的羧基末端连接。在包含与第一半衰期延长结构域连接的第一掩蔽部分、与细胞因子或其功能片段连接的第二掩蔽部分且其中第二掩蔽部分或细胞因子或其功能片段与第二半衰期延长结构域连接的一些实施方案中,第一掩蔽部分与接头的羧基末端连接,且第一半衰期延长结构域与接头的氨基末端连接。在包含与第一半衰期延长结构域连接的第一掩蔽部分、与细胞因子或其功能片段连接的第二掩蔽部分且其中第二掩蔽部分或细胞因子或其功能片段与第二半衰期延长结构域连接的一些实施方案中,第二掩蔽部分与接头的氨基末端连接,且细胞因子或其功能片段与接头的羧基末端连接。在包含与第一半衰期延长结构域连接的第一掩蔽部分、与细胞因子或其功能片段连接的第二掩蔽部分且其中第二掩蔽部分或细胞因子或其功能片段与第二半衰期延长结构域连接的一些实施方案中,第二掩蔽部分与接头的羧基末端连接,且细胞因子或其功能片段与接头的氨基末端连接。在包含与第一半衰期延长结构域连接的第一掩蔽部分、与细胞因子或其功能片段连接的第二掩蔽部分且其中第二掩蔽部分或细胞因子或其功能片段与第二半衰期延长结构域连接的一些实施方案中,第二掩蔽部分与接头的氨基末端连接,且第二半衰期延长结构域与接头的羧基末端连接。在包含与第一半衰期延长结构域连接的第一掩蔽部分、与细胞因子或其功能片段连接的第二掩蔽部分且其中第二掩蔽部分或细胞因子或其功能片段与第二半衰期延长结构域连接的一些实施方案中,第二掩蔽部分与接头的羧基末端连接,且第二半衰期延长结构域与接头的氨基末端连接。在包含与第一半衰期延长结构域连接的第一掩蔽部分、与细胞因子或其功能片段连接的第二掩蔽部分且其中第二掩蔽部分或细胞因子或其功能片段与第二半衰期延长结构域连接的一些实施方案中,细胞因子或其功能片段与接头的氨基末端连接,且第二半衰期延长结构域与接头的羧基末端连接。在包含与第一半衰期延长结构域连接的第一掩蔽部分、与细胞因子或其功能片段连接的第二掩蔽部分且其中第二掩蔽部分或细胞因子或其功能片段与第二半衰期延长结构域连接的一些实施方案中,细胞因子或其功能片段与接头的羧基末端连接,且第二半衰期延长结构域与接头的氨基末端连接。
在包含经由第一接头与第一半衰期延长结构域连接的第一掩蔽部分、经由第二接头与第一掩蔽部分连接的第二掩蔽部分和经由第三接头与第二半衰期延长结构域连接的细胞因子或其功能片段的一些实施方案中,第一掩蔽部分与第一接头的羧基末端连接,且第一半衰期延长结构域与第一接头的氨基末端连接,第二掩蔽部分与第二接头的羧基末端连接,第一掩蔽部分与第二接头的氨基末端连接,细胞因子或其功能片段与第三接头的羧基末端连接,且第二半衰期延长结构域与第三接头的氨基末端连接。
在包含经由第一接头与第一半衰期延长结构域连接的第一掩蔽部分、经由第二接头与第一掩蔽部分连接的第二掩蔽部分和经由第三接头与第二半衰期延长结构域连接的细胞因子或其功能片段的一些实施方案中,第一掩蔽部分与第一接头的氨基末端连接,且第一半衰期延长结构域与第一接头的羧基末端连接,第二掩蔽部分与第二接头的氨基末端连接,第一掩蔽部分与第二接头的羧基末端连接,细胞因子或其功能片段与第三接头的氨基末端连接,且第二半衰期延长结构域与第三接头的羧基末端连接。
在包含经由第一接头与第一半衰期延长结构域连接的第二掩蔽部分、经由第二接头与第二掩蔽部分连接的第一掩蔽部分和经由第三接头与第二半衰期延长结构域连接的细胞因子或其功能片段的一些实施方案中,第二掩蔽部分与第一接头的羧基末端连接,且第一半衰期延长结构域与第一接头的氨基末端连接,第一掩蔽部分与第二接头的羧基末端连接,第二掩蔽部分与第二接头的氨基末端连接,细胞因子或其功能片段与第三接头的羧基末端连接,且第二半衰期延长结构域与第三接头的氨基末端连接。
在包含经由第一接头与第一半衰期延长结构域连接的第二掩蔽部分、经由第二接头与第二掩蔽部分连接的第一掩蔽部分和经由第三接头与第二半衰期延长结构域连接的细胞因子或其功能片段的一些实施方案中,第二掩蔽部分与第一接头的氨基末端连接,且第一半衰期延长结构域与第一接头的羧基末端连接,第一掩蔽部分与第二接头的氨基末端连接,第二掩蔽部分与第二接头的羧基末端连接,细胞因子或其功能片段与第三接头的氨基末端连接,且第二半衰期延长结构域与第三接头的羧基末端连接。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域与第二半衰期延长结构域连接。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域经由接头与第二半衰期延长结构域连接。
在一些实施方案中,接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列。在一些实施方案中,接头包含选自由seqidno:20-153、235-242、264、268-317、323-338、340-347、356-415、420-491、494-501、504-535、538-555、727、794和799组成的组的氨基酸序列。在一些实施方案中,接头包含选自由seqidno:11-19、262、263、318-320、348-354、416-419、492、493、502、503、536、537、668、691、724、725、762-771、797、798和800-812组成的组的氨基酸序列。在一些实施方案中,接头包含seqidno:262的氨基酸序列。在一些实施方案中,接头包含seqidno:28的氨基酸序列。在一些实施方案中,接头包含选自由seqidno:20-95、235、268和269组成的组的氨基酸序列。在一些实施方案中,接头包含选自由seqidno:20-33组成的组的氨基酸序列。在一些实施方案中,接头包含选自由seqidno:34-44组成的组的氨基酸序列。在一些实施方案中,接头包含选自由seqidno:45-95组成的组的氨基酸序列。在一些实施方案中,接头包含seqidno:235的氨基酸序列。在一些实施方案中,接头包含seqidno:28的氨基酸序列。在一些实施方案中,接头包含seqidno:268的氨基酸序列。在一些实施方案中,接头包含seqidno:269的氨基酸序列。在一些实施方案中,接头包含选自由seqidno:263、318-322、339、348-355、416-419、492、493、502、503、536、537、668、691、724、725、727、762-771、794、795和797-812组成的组的氨基酸序列。
在一些实施方案中,接头包含选自由seqidno:794、795和797-812组成的组的氨基酸序列。在一些实施方案中,接头包含选自由seqidno:270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。
在一些实施方案中,接头包含与选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:11-19、262、263、318-320、348-354、416-419、492、493、502、503、536、537、668、691、724、725、762-771、797、798和800-812组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:20-33组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:34-44组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:45-95组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与seqidno:235的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与seqidno:262的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:263、318-320、348-354、416-419、492、493、502、503、536、537、668、691、724、725、762-771、797、798和800-812组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:318-320组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:348-354组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:416-419组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:492、493、502、503、536、537组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:668、691、724、725、762-771、797、798和800-812组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:762-771、797、798和800-812组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:762-771组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:797、798和800-812组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,接头包含与选自由seqidno:800-812组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
下面更详细地描述接头的一些实施方案的可切割肽和间隔区结构域。
1.可切割肽
在一些实施方案中,接头包含可切割肽。在具有一个以上包含可切割肽的接头的一些实施方案中,可切割肽可以被称为第一可切割肽、第二可切割肽或第三可切割肽,其每一者被认为是“可切割肽”,并且可以是本文所述的任何可切割肽。例如,提到“可切割肽”或“所述可切割肽”可指包含单个可切割肽的掩蔽型细胞因子中的可切割肽,或者其可指包含第一可切割肽和第二可切割肽的掩蔽型细胞因子中的第一可切割肽,或者其可指包含第一可切割肽和第二可切割肽的掩蔽型细胞因子中的第二可切割肽,或者其可指包含第一可切割肽和第二可切割肽的掩蔽型细胞因子中的第一可切割肽和第二可切割肽,或者其可指包含第一可切割肽、第二可切割肽和第三可切割肽的掩蔽型细胞因子中的第一可切割肽、第二可切割肽和/或第三可切割肽。可以想象的是,在一些实施方案中,根据本文的教导可以存在三个以上可切割肽。
可切割肽是包括切割位点如蛋白酶切割位点的多肽。在一些实施方案中,可切割肽包含一个以上切割位点。如本文所用的“切割位点”是指用于切割包含本文所述的可切割肽的任何接头中所见的可切割肽的一部分的可识别位点。因此,切割位点可见于如本文所述的可切割肽的序列中。在一些实施方案中,切割位点是被切割剂识别并切割的氨基酸序列。示例性切割剂包括蛋白质、酶、dna酶、rna酶、金属、酸和碱。
在一些实施方案中,可切割肽包含蛋白酶切割位点。在一些实施方案中,蛋白酶切割位点是肿瘤相关蛋白酶切割位点。如本文提供的“肿瘤相关蛋白酶切割位点”是由蛋白酶识别的氨基酸序列,所述蛋白酶的表达对于肿瘤细胞或其肿瘤细胞环境是特异性的或上调的。在一些实施方案中,蛋白酶切割位点是由选自由以下组成的组的一种或多种酶识别的切割位点:abhd12、adam12、abhd12b、abhd13、abhd17a、adam19、adam20、adam21、adam28、adam30、adam33、adam8、abhd17a、adamdec1、adamts1、adamts10、adamts12、adamts13、adamts14、adamts15、adamts16、adamts17、adamts18、adamts19、adamts2、adamts20、adamts3、adamts4、abhd17b、adamts5、adamts6、adamts7、adamts8、adamts9、adamtsl1、adamtsl2、adamtsl3、abhd17c、adamtsl5、astl、bmp1、cela1、cela2a、cela2b、cela3a、cela3b、adam10、adam15、adam17、adam9、adamts4、ctse、ctsf、adamtsl4、cma1、ctrb1、ctrc、ctso、ctr1、ctsa、ctsw、ctsb、ctsc、ctsd、esp1、ctsg、ctsh、gzma、gzmb、gzmh、ctsk、gzmm、ctsl、ctss、ctsv、ctsz、htra4、klk10、klk11、klk13、klk14、klk2、klk4、dpp4、klk6、klk7、klkb1、ece1、ece2、ecel1、masp2、mep1a、mep1b、elane、fap、gzma、mmp11、gzmk、hgfac、hpn、htra1、mmp11、mmp16、mmp17、mmp19、htra2、mmp20、mmp21、htra3、htra4、kel、mmp23b、mmp24、mmp25、mmp26、mmp27、mmp28、klk5、mmp3、mmp7、mmp8、mmp9、lgmn、lnpep、masp1、pappa、pappa2、pcsk1、napsa、pcsk5、pcsk6、mme、mmp1、mmp10、plat、plau、plg、prss1、prss12、prss2、prss21、prss3、prss33、prss4、prss55、prss57、mmp12、prss8、prss9、prtn3、mmp13、mmp14、st14、tmprss10、tmprss11a、tmprss11d、tmprss11e、tmprss11f、tmprss12、tmprss13、mmp15、tmprss15、mmp2、tmprss2、tmprss3、tmprss4、tmprss5、tmprss6、tmprss7、tmprss9、nrdc、ovch1、pamr1、pcsk3、phex、tinag、tpsab1、tpsd1和tpsg1。在一些实施方案中,蛋白酶切割位点是由选自由以下组成的组的一种或多种酶识别的切割位点:adam17、htra1、prss1、fap、gzmk、napsa、mmp1、mmp2、mmp9、mmp10、mmp7、mmp12、mmp28、adamts9、hgfac和htra3。
在若干实施方案中,蛋白酶切割位点是基质金属蛋白酶(mmp)切割位点、含解整联蛋白和金属蛋白酶结构域(adam)金属蛋白酶切割位点、前列腺特异性抗原(psa)蛋白酶切割位点、尿激酶型纤溶酶原激活物(upa)蛋白酶切割位点、膜型丝氨酸蛋白酶1(mt-sp1)蛋白酶切割位点、蛋白裂解酶蛋白酶切割位点(st14)或豆荚蛋白蛋白酶切割位点。在若干实施方案中,基质金属蛋白酶(mmp)切割位点是mmp9切割位点、mmp13切割位点或mmp2切割位点。在若干实施方案中,含解整联蛋白和金属蛋白酶结构域(adam)金属蛋白酶切割位点是adam9金属蛋白酶切割位点、adam10金属蛋白酶切割位点或adam17金属蛋白酶切割位点。蛋白酶切割位点可由特定氨基酸序列指定。
在一些实施方案中,可切割肽被选自由以下组成的组的一种或多种酶切割:abhd12、adam12、abhd12b、abhd13、abhd17a、adam19、adam20、adam21、adam28、adam30、adam33、adam8、abhd17a、adamdec1、adamts1、adamts10、adamts12、adamts13、adamts14、adamts15、adamts16、adamts17、adamts18、adamts19、adamts2、adamts20、adamts3、adamts4、abhd17b、adamts5、adamts6、adamts7、adamts8、adamts9、adamtsl1、adamtsl2、adamtsl3、abhd17c、adamtsl5、astl、bmp1、cela1、cela2a、cela2b、cela3a、cela3b、adam10、adam15、adam17、adam9、adamts4、ctse、ctsf、adamtsl4、cma1、ctrb1、ctrc、ctso、ctr1、ctsa、ctsw、ctsb、ctsc、ctsd、esp1、ctsg、ctsh、gzma、gzmb、gzmh、ctsk、gzmm、ctsl、ctss、ctsv、ctsz、htra4、klk10、klk11、klk13、klk14、klk2、klk4、dpp4、klk6、klk7、klkb1、ece1、ece2、ecel1、masp2、mep1a、mep1b、elane、fap、gzma、mmp11、gzmk、hgfac、hpn、htra1、mmp11、mmp16、mmp17、mmp19、htra2、mmp20、mmp21、htra3、htra4、kel、mmp23b、mmp24、mmp25、mmp26、mmp27、mmp28、klk5、mmp3、mmp7、mmp8、mmp9、lgmn、lnpep、masp1、pappa、pappa2、pcsk1、napsa、pcsk5、pcsk6、mme、mmp1、mmp10、plat、plau、plg、prss1、prss12、prss2、prss21、prss3、prss33、prss4、prss55、prss57、mmp12、prss8、prss9、prtn3、mmp13、mmp14、st14、tmprss10、tmprss11a、tmprss11d、tmprss11e、tmprss11f、tmprss12、tmprss13、mmp15、tmprss15、mmp2、tmprss2、tmprss3、tmprss4、tmprss5、tmprss6、tmprss7、tmprss9、nrdc、ovch1、pamr1、pcsk3、phex、tinag、tpsab1、tpsd1和tpsg1。在一些实施方案中,可切割肽被选自由以下组成的组的一种或多种酶切割:adam17、htra1、prss1、fap、gzmk、napsa、mmp1、mmp2、mmp9、mmp10、mmp7、mmp12、mmp28、adamts9、hgfac和htra3。在一些实施方案中,可切割肽被选自由upa和mmp14组成的组的一种或多种酶切割。在一些实施方案中,可切割肽被选自由蛋白裂解酶和mmp14组成的组的一种或多种酶切割。在一些实施方案中,可切割肽被选自由豆荚蛋白和mmp14组成的组的一种或多种酶切割。在一些实施方案中,可切割肽被选自由蛋白裂解酶和upa组成的组的一种或多种酶切割。在一些实施方案中,可切割肽被选自由upa和豆荚蛋白组成的组的一种或多种酶切割。在一些实施方案中,可切割肽被选自由蛋白裂解酶和豆荚蛋白组成的组的一种或多种酶切割。在一些实施方案中,可切割肽被选自由upa、蛋白裂解酶和mmp14组成的组的一种或多种酶切割。在一些实施方案中,可切割肽被选自由upa、豆荚蛋白和mmp14组成的组的一种或多种酶切割。在一些实施方案中,可切割肽被选自由蛋白裂解酶、豆荚蛋白和mmp14组成的组的一种或多种酶切割。在一些实施方案中,可切割肽被选自由蛋白裂解酶、豆荚蛋白和upa组成的组的一种或多种酶切割。
在一些实施方案中,可切割肽是共定位在表达细胞因子受体的区域或组织中的蛋白酶的底物。所述细胞因子受体可以是任何细胞因子受体。在一些实施方案中,细胞因子受体选自由以下组成的组:cxcr1、cxcr2、cxcr3、cxcr4、cxcr5、cxcr6、cxcr7、ccr1、ccr2、ccr3、ccr4、ccr5、ccr6、ccr7、ccr8、ccr9、ccr10、ccr11、xcr1、cx3cr1、il-1rap、il-1rapl1、il-1rapl2、il-1rl1、il-1rl2、il-1r1、il-1r2、il-2r、il-2rα、il-2rβ、il-2rγ、il-3rα、il-4r、il-5rα、il-6r、il-6st、il-7r、il-9r、il-10rα、il-10rβ、il-11rα、il-12rβ1、il-12rβ2、il-13rα1、il-13rα2、il-15rα、il-17ra、il-17rb、il-17rc、il-17rd、il-17re、il-18rap、il-18r1、il-20rα、il-20rβ、il-21r、il-22rα1、il-22rα2、il-23r、il-27rα、il-28rα、il-31ra、ifnar1、ifnar2、ifngr1、ifngr2、ifnlr1、gmrα(cd116)、cd131、ghr、prlr、epor、lifr(cd118)、osmrβ、tpo-r(cd110)、csf-1r、edar、tnfrsf1a、tnfrsf1b、ltbr、tnfrsf4、cd40、fas、tnfrsf6b、cd27、tnfrsf8、tnfrsf9、tnfrsf10a、tnfrsf10b、tnfrsf10c、tnfrsf10d、tnfrsf11a、tnfrsf11b、tnfrsf12a、tnfrsf13b、tnfrsf13c、tnfrsf14、ngfr、tnfrsf17、tnfrsf18、tnfrsf19、relt、tnfrsf21、tnfrsf25和eda2r。
在一些实施方案中,可切割肽是5聚体(即长度为5个氨基酸的肽)、6聚体(即长度为6个氨基酸的肽)、7聚体(即长度为7个氨基酸的肽)、8聚体(即长度为8个氨基酸的肽)、9聚体(即长度为9个氨基酸的肽)、10聚体(即长度为10个氨基酸的肽)、11聚体(即长度为11个氨基酸的肽)、12聚体(即长度为12个氨基酸的肽)、13聚体(即长度为13个氨基酸的肽)、14聚体(即长度为14个氨基酸的肽)、15聚体(即长度为15个氨基酸的肽)、16聚体(即长度为16个氨基酸的肽)、17聚体(即长度为17个氨基酸的肽)或18聚体(即长度为18个氨基酸的肽)。示例性可切割肽序列示于表1中。
表1.示例性可切割肽序列
在一些实施方案中,可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。在一些实施方案中,可切割肽包含选自由seqidno:270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。在一些实施方案中,可切割肽包含选自由seqidno:281、293、297、399-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。在一些实施方案中,可切割肽包含seqidno:96的氨基酸序列。在一些实施方案中,可切割肽包含seqidno:264的氨基酸序列。在一些实施方案中,可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。在一些实施方案中,可切割肽包含选自由seqidno:96-131和264组成的组的氨基酸序列以及选自由seqidno:236-242组成的组的氨基酸序列。在一些实施方案中,可切割肽包含选自由seqidno:96-131组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。在可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列以及选自由seqidno:236-242组成的组的氨基酸序列的实施方案中,两个氨基酸序列可以按任何顺序连接。例如,在可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列以及选自由seqidno:236-242组成的组的氨基酸序列的实施方案中,选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。在可切割肽包含选自由seqidno:96-131和264组成的组的氨基酸序列以及选自由seqidno:236-242组成的组的氨基酸序列的一些实施方案中,选自由seqidno:96-131和264组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-131和264组成的组的氨基酸序列的n末端或c末端连接。
在一些实施方案中,一个或多个另外的氨基酸通过添加并入到可切割肽的氨基酸序列中。在一些实施方案中,通过添加并入到可切割肽的氨基酸序列中的一个或多个氨基酸选自由以下组成的组:亲水性氨基酸(例如,赖氨酸、精氨酸、组氨酸、天冬氨酸、谷氨酸、丝氨酸、苏氨酸、天冬酰胺或谷氨酰胺)、疏水性氨基酸(例如,丙氨酸、缬氨酸、异亮氨酸、亮氨酸、甲硫氨酸、苯丙氨酸、酪氨酸、色氨酸、半胱氨酸、甘氨酸或脯氨酸)、极性氨基酸(例如,丝氨酸、苏氨酸、半胱氨酸、天冬酰胺、谷氨酰胺或酪氨酸)、非极性氨基酸(例如,甘氨酸、丙氨酸、缬氨酸、脯氨酸、亮氨酸、异亮氨酸、甲硫氨酸、色氨酸或苯丙氨酸)、具有脂族侧链的氨基酸(例如,甘氨酸、丙氨酸、缬氨酸、亮氨酸或异亮氨酸)、具有含羟基侧链的氨基酸(例如,丝氨酸或苏氨酸)、具有含硫侧链的氨基酸(例如,半胱氨酸或甲硫氨酸)、带电荷的氨基酸(例如,精氨酸、赖氨酸、天冬氨酸或谷氨酸)、不带电荷的氨基酸(例如,丝氨酸、苏氨酸、天冬酰胺或谷氨酰胺)、芳族氨基酸(例如,酪氨酸、色氨酸或苯丙氨酸)、环状氨基酸(例如,脯氨酸)、酸性氨基酸(例如,天冬氨酸、天冬酰胺、谷氨酸或谷氨酰胺)、碱性氨基酸(例如,组氨酸、赖氨酸或精氨酸)和大体积氨基酸(例如,苯丙氨酸、酪氨酸或色氨酸)。在一些实施方案中,甘氨酸(g)通过添加到可切割肽的氨基酸序列的n末端和/或c末端而并入。在一些实施方案中,甘氨酸(g)和脯氨酸(p)通过添加到可切割肽的氨基酸序列的n末端和/或c末端而并入,如通过将氨基酸序列gp或pg并入到可切割肽的氨基酸序列的n末端和/或c末端。
可切割肽包含氨基末端和羧基末端。在一些实施方案中,可切割肽与n末端间隔区结构域和/或c末端间隔区结构域连接。在一些实施方案中,n末端间隔区结构域与可切割肽的氨基末端连接。在一些实施方案中,c末端间隔区结构域与可切割肽的羧基末端连接。在一些实施方案中,n末端间隔区结构域与可切割肽的氨基末端连接,且c末端间隔区结构域与可切割肽的羧基末端连接。在一些实施方案中,n末端间隔区结构域与可切割肽的氨基末端连接,且c末端间隔区结构域与可切割肽的羧基末端连接。
在一些实施方案中,可切割肽的氨基末端与除n末端间隔区结构域以外的组分连接。在一些实施方案中,可切割肽的羧基末端与除c末端间隔区结构域以外的组分连接。在一些实施方案中,掩蔽部分与可切割肽的氨基末端或羧基末端连接。在一些实施方案中,细胞因子或其功能片段与可切割肽的氨基末端或羧基末端连接。在一些实施方案中,半衰期延长结构域与可切割肽的氨基末端或羧基末端连接。在一些实施方案中,第一半衰期延长结构域与可切割肽的氨基末端或羧基末端连接。在一些实施方案中,第二半衰期延长结构域与可切割肽的氨基末端或羧基末端连接。
2.间隔区结构域
在一些实施方案中,接头包含间隔区结构域。如本文所用,在一些实施方案中,“间隔区结构域”可指n末端间隔区结构域和/或c末端间隔区结构域。在一些实施方案中,接头包含n末端间隔区结构域和/或c末端间隔区结构域。在一些实施方案中,接头包含n末端间隔区结构域。在一些实施方案中,接头包含c末端间隔区结构域。在一些实施方案中,接头包含n末端间隔区结构域和c末端间隔区结构域。在一些实施方案中,接头包含n末端间隔区结构域和可切割肽。在一些实施方案中,接头包含可切割肽和c末端间隔区结构域。在一些实施方案中,接头包含n末端间隔区结构域、可切割肽和c末端间隔区结构域。
在一些实施方案如具有一个以上n末端间隔区结构域的一些实施方案中,n末端间隔区结构域可以被称为第一n末端间隔区结构域、第二n末端间隔区结构域或第三n末端间隔区结构域,其每一者被认为是“n末端间隔区结构域”,并且可以是本文所述的任何n末端间隔区结构域。同样地,在一些实施方案如具有一个以上c末端间隔区结构域的一些实施方案中,c末端间隔区结构域可以被称为第一c末端间隔区结构域、第二c末端间隔区结构域或第三c末端间隔区结构域,其每一者被认为是“c末端间隔区结构域”,并且可以是本文所述的任何c末端间隔区结构域。例如,提到“n末端间隔区结构域”或“所述n末端间隔区结构域”可指包含单个n末端间隔区结构域的掩蔽型细胞因子中的n末端间隔区结构域,或者其可指包含第一n末端间隔区结构域和第二n末端间隔区结构域的掩蔽型细胞因子中的第一n末端间隔区结构域,或者其可指包含第一n末端间隔区结构域和第二n末端间隔区结构域的掩蔽型细胞因子中的第二n末端间隔区结构域,或者其可指包含第一n末端间隔区结构域和第二n末端间隔区结构域的掩蔽型细胞因子中的第一n末端间隔区结构域和第二n末端间隔区结构域,或者其可指包含第一n末端间隔区结构域、第二n末端间隔区结构域和第三n末端间隔区结构域的掩蔽型细胞因子中的第一n末端间隔区结构域、第二n末端间隔区结构域和/或第三n末端间隔区结构域。
n末端间隔区结构域和c末端间隔区结构域各自包含氨基末端和羧基末端。在一些实施方案中,掩蔽部分与n末端间隔区结构域的氨基末端或羧基末端连接。在一些实施方案中,细胞因子或其功能片段与n末端间隔区结构域的氨基末端或羧基末端连接。在一些实施方案中,半衰期延长结构域与n末端间隔区结构域的氨基末端或羧基末端连接。在一些实施方案中,第一半衰期延长结构域与n末端间隔区结构域的氨基末端或羧基末端连接。在一些实施方案中,第二半衰期延长结构域与n末端间隔区结构域的氨基末端或羧基末端连接。
在一些实施方案中,掩蔽部分与c末端间隔区结构域的氨基末端或羧基末端连接。在一些实施方案中,细胞因子或其功能片段与c末端间隔区结构域的氨基末端或羧基末端连接。在一些实施方案中,半衰期延长结构域与c末端间隔区结构域的氨基末端或羧基末端连接。在一些实施方案中,第一半衰期延长结构域与c末端间隔区结构域的氨基末端或羧基末端连接。在一些实施方案中,第二半衰期延长结构域与c末端间隔区结构域的氨基末端或羧基末端连接。
在一些实施方案中,掩蔽部分与n末端间隔区结构域的氨基末端连接,且半衰期延长结构域与n末端间隔区结构域的羧基末端连接。在一些实施方案中,细胞因子或其功能片段与n末端间隔区结构域的氨基末端连接,且半衰期延长结构域与n末端间隔区结构域的羧基末端连接。在一些实施方案中,掩蔽部分与n末端间隔区结构域的羧基末端连接,半衰期延长结构域与n末端间隔区结构域的氨基末端连接。在一些实施方案中,细胞因子或其功能片段与n末端间隔区结构域的羧基末端连接,且半衰期延长结构域与n末端间隔区结构域的氨基末端连接。
在一些实施方案中,掩蔽部分与c末端间隔区结构域的氨基末端连接,且半衰期延长结构域与c末端间隔区结构域的羧基末端连接。在一些实施方案中,细胞因子或其功能片段与c末端间隔区结构域的氨基末端连接,且半衰期延长结构域与c末端间隔区结构域的羧基末端连接。在一些实施方案中,掩蔽部分与c末端间隔区结构域的羧基末端连接,半衰期延长结构域与c末端间隔区结构域的氨基末端连接。在一些实施方案中,细胞因子或其功能片段与c末端间隔区结构域的羧基末端连接,且半衰期延长结构域与c末端间隔区结构域的氨基末端连接。
在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分或第二掩蔽部分与n末端间隔区结构域的氨基末端连接,且细胞因子或其功能片段与n末端间隔区结构域的羧基末端连接。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分或第二掩蔽部分与n末端间隔区结构域的羧基末端连接,且细胞因子或其功能片段与n末端间隔区结构域的氨基末端连接。
在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分或第二掩蔽部分与c末端间隔区结构域的氨基末端连接,且细胞因子或其功能片段与c末端间隔区结构域的羧基末端连接。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分或第二掩蔽部分与c末端间隔区结构域的羧基末端连接,且细胞因子或其功能片段与c末端间隔区结构域的氨基末端连接。
在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分与c末端间隔区结构域的氨基末端连接,且第二掩蔽部分与c末端间隔区结构域的羧基末端连接。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分与c末端间隔区结构域的羧基末端连接,且第二掩蔽部分与c末端间隔区结构域的氨基末端连接。
在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,半衰期延长结构域与n末端间隔区结构域的氨基末端连接,且第一掩蔽部分或第二掩蔽部分与n末端间隔区结构域的羧基末端连接。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,半衰期延长结构域与n末端间隔区结构域的羧基末端连接,且第一掩蔽部分或第二掩蔽部分与n末端间隔区结构域的氨基末端连接。
在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分与n末端间隔区结构域的氨基末端连接,且第二掩蔽部分与n末端间隔区结构域的羧基末端连接。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分与n末端间隔区结构域的羧基末端连接,且第二掩蔽部分与n末端间隔区结构域的氨基末端连接。
在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,半衰期延长结构域与c末端间隔区结构域的氨基末端连接,且第一掩蔽部分或第二掩蔽部分与c末端间隔区结构域的羧基末端连接。在包含第一掩蔽部分和第二掩蔽部分的一些实施方案中,半衰期延长结构域与c末端间隔区结构域的羧基末端连接,且第一掩蔽部分或第二掩蔽部分与c末端间隔区结构域的氨基末端连接。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,掩蔽部分与n末端间隔区结构域的氨基末端连接,且第一半衰期延长结构域或第二半衰期延长结构域与n末端间隔区结构域的羧基末端连接。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,掩蔽部分与n末端间隔区结构域的羧基末端连接,且第一半衰期延长结构域或第二半衰期延长结构域与n末端间隔区结构域的氨基末端连接。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,细胞因子或其功能片段与n末端间隔区结构域的氨基末端连接,且第一半衰期延长结构域或第二半衰期延长结构域与n末端间隔区结构域的羧基末端连接。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,细胞因子或其功能片段与n末端间隔区结构域的羧基末端连接,且第一半衰期延长结构域或第二半衰期延长结构域与n末端间隔区结构域的氨基末端连接。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,掩蔽部分与c末端间隔区结构域的氨基末端连接,且第一半衰期延长结构域或第二半衰期延长结构域与c末端间隔区结构域的羧基末端连接。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,掩蔽部分与c末端间隔区结构域的羧基末端连接,且第一半衰期延长结构域或第二半衰期延长结构域与c末端间隔区结构域的氨基末端连接。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,细胞因子或其功能片段与c末端间隔区结构域的氨基末端连接,且第一半衰期延长结构域或第二半衰期延长结构域与c末端间隔区结构域的羧基末端连接。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,细胞因子或其功能片段与c末端间隔区结构域的羧基末端连接,且第一半衰期延长结构域或第二半衰期延长结构域与c末端间隔区结构域的氨基末端连接。
在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分与n末端间隔区结构域的氨基末端连接,且第一半衰期延长结构域与n末端间隔区结构域的羧基末端连接。在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分与n末端间隔区结构域的羧基末端连接,且第一半衰期延长结构域与n末端间隔区结构域的氨基末端连接。在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分与c末端间隔区结构域的氨基末端连接,且第一半衰期延长结构域与c末端间隔区结构域的羧基末端连接。在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第一掩蔽部分与c末端间隔区结构域的羧基末端连接,且第一半衰期延长结构域与c末端间隔区结构域的氨基末端连接。
在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第二掩蔽部分与n末端间隔区结构域的氨基末端连接,且细胞因子或其功能片段与n末端间隔区结构域的羧基末端连接。在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第二掩蔽部分与n末端间隔区结构域的羧基末端连接,且细胞因子或其功能片段与n末端间隔区结构域的氨基末端连接。在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第二掩蔽部分与c末端间隔区结构域的氨基末端连接,且细胞因子或其功能片段与c末端间隔区结构域的羧基末端连接。在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第二掩蔽部分与c末端间隔区结构域的羧基末端连接,且细胞因子或其功能片段与c末端间隔区结构域的氨基末端连接。
在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第二半衰期延长结构域与n末端间隔区结构域的氨基末端连接,且细胞因子或其功能片段或第二掩蔽部分与n末端间隔区结构域的羧基末端连接。在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第二半衰期延长结构域与n末端间隔区结构域的羧基末端连接,且细胞因子或其功能片段或第二掩蔽部分与n末端间隔区结构域的氨基末端连接。在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第二半衰期延长结构域与c末端间隔区结构域的氨基末端连接,且细胞因子或其功能片段或第二掩蔽部分与c末端间隔区结构域的羧基末端连接。在包含第一半衰期延长结构域、第二半衰期延长结构域、第一掩蔽部分和第二掩蔽部分的一些实施方案中,第二半衰期延长结构域与c末端间隔区结构域的羧基末端连接,且细胞因子或其功能片段或第二掩蔽部分与c末端间隔区结构域的氨基末端连接。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域经由接头与第二半衰期延长结构域连接。在一些实施方案中,连接第一半衰期延长结构域和第二半衰期延长结构域的接头包含n末端间隔区结构域和/或c末端间隔区结构域。在一些实施方案中,连接第一半衰期延长结构域和第二半衰期延长结构域的接头包含可切割肽和n末端间隔区结构域和/或c末端间隔区结构域。在包含经由接头连接在一起的第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,接头包含氨基末端和羧基末端,第一半衰期延长结构域与接头的氨基末端连接,且第二半衰期延长结构域与接头的羧基末端连接。在包含经由接头连接在一起的第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,接头包含氨基末端和羧基末端,第一半衰期延长结构域与接头的羧基末端连接,且第二半衰期延长结构域与接头的氨基末端连接。
在一些实施方案中,n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。在一些实施方案中,c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。在一些实施方案中,n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列,且c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
在一些实施方案中,n末端间隔区结构域包含选自由seqidno:20-95、235、268和269组成的组的氨基酸序列。在一些实施方案中,c末端间隔区结构域包含选自由seqidno:20-95、235、268和269组成的组的氨基酸序列。在一些实施方案中,n末端间隔区结构域包含选自由seqidno:20-95、235、268和269组成的组的氨基酸序列,且c末端间隔区结构域包含选自由seqidno:20-95、235、268和269组成的组的氨基酸序列。在一些实施方案中,接头包含有包含选自由seqidno:20-95、235、268和269组成的组的氨基酸序列的n末端间隔区结构域和包含选自由seqidno:20-95、235、268和269组成的组的氨基酸序列的c末端间隔区结构域。在一些实施方案中,接头包含有包含seqidno:268的氨基酸序列的n末端间隔区结构域和包含seqidno:269的氨基酸序列的c末端间隔区结构域。在一些实施方案中,接头包含有包含seqidno:268的氨基酸序列的n末端间隔区结构域、包含seqidno:264的氨基酸序列的可切割肽和包含seqidno:269的氨基酸序列的c末端间隔区结构域。在一些实施方案中,接头包含有包含seqidno:269的氨基酸序列的n末端间隔区结构域和包含seqidno:268的氨基酸序列的c末端间隔区结构域。在一些实施方案中,接头包含有包含seqidno:269的氨基酸序列的n末端间隔区结构域、包含seqidno:264的氨基酸序列的可切割肽和包含seqidno:268的氨基酸序列的c末端间隔区结构域。
在一些实施方案中,n末端间隔区结构域包含选自由seqidno:20-95、235、268和269组成的组的氨基酸序列。在一些实施方案中,n末端间隔区结构域包含与seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799中的任一者的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,n末端间隔区结构域包含与seqidno:20-95、235、268和269中的任一者的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,c末端间隔区结构域包含与seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799中的任一者的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,c末端间隔区结构域包含选自由seqidno:20-95、235、268和269组成的组的氨基酸序列。在一些实施方案中,c末端间隔区结构域包含与seqidno:20-95、235、268和269中的任一者的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,n末端间隔区结构域包含选自由seqidno:20-95、235、268和269组成的组的氨基酸序列,且c末端间隔区结构域包含选自由seqidno:20-95、235、268和269组成的组的氨基酸序列。在一些实施方案中,n末端间隔区结构域包含与seqidno:20-95、235、268和269中的任一者的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且c末端间隔区结构域包含与seqidno:20-95、235、268和269中的任一者的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,n末端间隔区结构域包含与seqidno:268的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且c末端间隔区结构域包含与seqidno:269的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,n末端间隔区结构域包含与seqidno:268的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,可切割肽包含seqidno:264的氨基酸序列,且c末端间隔区结构域包含与seqidno:269的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。示例性间隔区结构域(例如,n末端间隔区结构域和/或c末端间隔区结构域)示于表2中。
表2.示例性间隔区结构域
在一些实施方案中,n末端间隔区结构域包含通过修饰本文所述的任何n末端间隔区结构域的氨基酸序列产生的氨基酸序列。在一些实施方案中,n末端间隔区结构域包含通过修饰seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799中的任一者的氨基酸序列产生的氨基酸序列。在一些实施方案中,c末端间隔区结构域包含通过修饰本文所述的任何c末端间隔区结构域的氨基酸序列产生的氨基酸序列。在一些实施方案中,c末端间隔区结构域包含通过修饰seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799中的任一者的氨基酸序列产生的氨基酸序列。在一些实施方案中,n末端间隔区结构域包含通过修饰seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799中的任一者的氨基酸序列产生的氨基酸序列,且c末端间隔区结构域包含通过修饰seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799中的任一者的氨基酸序列产生的氨基酸序列。在一些实施方案中,n末端间隔区结构域和/或c末端间隔区结构域包含seqidno:28的氨基酸序列。
在一些实施方案中,n末端间隔区结构域和/或c末端间隔区结构域由一个或多个氨基酸组成。在一些实施方案中,n末端间隔区结构域和/或c末端间隔区结构域的一个或多个氨基酸选自由以下组成的组:亲水性氨基酸(例如,赖氨酸、精氨酸、组氨酸、天冬氨酸、谷氨酸、丝氨酸、苏氨酸、天冬酰胺或谷氨酰胺)、疏水性氨基酸(例如,丙氨酸、缬氨酸、异亮氨酸、亮氨酸、甲硫氨酸、苯丙氨酸、酪氨酸、色氨酸、半胱氨酸、甘氨酸或脯氨酸)、极性氨基酸(例如,丝氨酸、苏氨酸、半胱氨酸、天冬酰胺、谷氨酰胺或酪氨酸)、非极性氨基酸(例如,甘氨酸、丙氨酸、缬氨酸、脯氨酸、亮氨酸、异亮氨酸、甲硫氨酸、色氨酸或苯丙氨酸)、具有脂族侧链的氨基酸(例如,甘氨酸、丙氨酸、缬氨酸、亮氨酸或异亮氨酸)、具有含羟基侧链的氨基酸(例如,丝氨酸或苏氨酸)、具有含硫侧链的氨基酸(例如,半胱氨酸或甲硫氨酸)、带电荷的氨基酸(例如,精氨酸、赖氨酸、天冬氨酸或谷氨酸)、不带电荷的氨基酸(例如,丝氨酸、苏氨酸、天冬酰胺或谷氨酰胺)、芳族氨基酸(例如,酪氨酸、色氨酸或苯丙氨酸)、环状氨基酸(例如,脯氨酸)、酸性氨基酸(例如,天冬氨酸、天冬酰胺、谷氨酸或谷氨酰胺)、碱性氨基酸(例如,组氨酸、赖氨酸或精氨酸)和大体积氨基酸(例如,苯丙氨酸、酪氨酸或色氨酸)。在一些实施方案中,n末端间隔区结构域和/或c末端间隔区结构域由甘氨酸(g)组成。在一些实施方案中,n末端间隔区结构域和/或c末端间隔区结构域由甘氨酸(g)和脯氨酸(p)组成,并具有gp或pg的氨基酸序列。
要理解的是,如一些实施方案中所述的对“间隔区结构域”的修饰可指对本文所述的任何一个或多个间隔区结构域(例如,本文所述的任何n末端间隔区结构域和/或任何c末端间隔区结构域)的修饰。例如,对间隔区结构域的修饰可指(a)对本文所述的任何n末端间隔区结构域的修饰,(b)对本文所述的任何c末端间隔区结构域的修饰,或(c)对本文所述的任何n末端间隔区结构域和任何c末端间隔区结构域的修饰。如此,本文所述的包括n末端间隔区结构域的任何接头包括其中根据本文所述的修饰对n末端间隔区结构域进行修饰的实施方案,本文所述的包括c末端间隔区结构域的任何接头包括其中根据本文所述的修饰对c末端间隔区结构域进行修饰的实施方案,且本文所述的包括n末端间隔区结构域和c末端间隔区结构域的任何接头包括其中根据本文所述的修饰对n末端间隔区结构域和/或c末端间隔区结构域进行修饰的实施方案。
对n末端间隔区结构域和/或c末端间隔区结构域的序列的修饰可以是对间隔区结构域的氨基酸序列的任何修饰,包括向序列中并入任何另外的氨基酸、用任何氨基酸取代不同的氨基酸和/或从序列中移除任何氨基酸。
在一些实施方案中,一个或多个另外的氨基酸通过添加并入到n末端间隔区结构域和/或c末端间隔区结构域的氨基酸序列中。在一些实施方案中,通过添加并入到n末端间隔区结构域和/或c末端间隔区结构域的氨基酸序列中的一个或多个氨基酸选自由以下组成的组:亲水性氨基酸(例如,赖氨酸、精氨酸、组氨酸、天冬氨酸、谷氨酸、丝氨酸、苏氨酸、天冬酰胺或谷氨酰胺)、疏水性氨基酸(例如,丙氨酸、缬氨酸、异亮氨酸、亮氨酸、甲硫氨酸、苯丙氨酸、酪氨酸、色氨酸、半胱氨酸、甘氨酸或脯氨酸)、极性氨基酸(例如,丝氨酸、苏氨酸、半胱氨酸、天冬酰胺、谷氨酰胺或酪氨酸)、非极性氨基酸(例如,甘氨酸、丙氨酸、缬氨酸、脯氨酸、亮氨酸、异亮氨酸、甲硫氨酸、色氨酸或苯丙氨酸)、具有脂族侧链的氨基酸(例如,甘氨酸、丙氨酸、缬氨酸、亮氨酸或异亮氨酸)、具有含羟基侧链的氨基酸(例如,丝氨酸或苏氨酸)、具有含硫侧链的氨基酸(例如,半胱氨酸或甲硫氨酸)、带电荷的氨基酸(例如,精氨酸、赖氨酸、天冬氨酸或谷氨酸)、不带电荷的氨基酸(例如,丝氨酸、苏氨酸、天冬酰胺或谷氨酰胺)、芳族氨基酸(例如,酪氨酸、色氨酸或苯丙氨酸)、环状氨基酸(例如,脯氨酸)、酸性氨基酸(例如,天冬氨酸、天冬酰胺、谷氨酸或谷氨酰胺)、碱性氨基酸(例如,组氨酸、赖氨酸或精氨酸)和大体积氨基酸(例如,苯丙氨酸、酪氨酸或色氨酸)。
在一些实施方案中,一个或多个氨基酸被取代到n末端间隔区结构域和/或c末端间隔区结构域的氨基酸序列中。在一些实施方案中,被取代到间隔区结构域的氨基酸序列中的一个或多个氨基酸选自由以下组成的组:亲水性氨基酸(例如,赖氨酸、精氨酸、组氨酸、天冬氨酸、谷氨酸、丝氨酸、苏氨酸、天冬酰胺或谷氨酰胺)、疏水性氨基酸(例如,丙氨酸、缬氨酸、异亮氨酸、亮氨酸、甲硫氨酸、苯丙氨酸、酪氨酸、色氨酸、半胱氨酸、甘氨酸或脯氨酸)、极性氨基酸(例如,丝氨酸、苏氨酸、半胱氨酸、天冬酰胺、谷氨酰胺或酪氨酸)、非极性氨基酸(例如,甘氨酸、丙氨酸、缬氨酸、脯氨酸、亮氨酸、异亮氨酸、甲硫氨酸、色氨酸或苯丙氨酸)、具有脂族侧链的氨基酸(例如,甘氨酸、丙氨酸、缬氨酸、亮氨酸或异亮氨酸)、具有含羟基侧链的氨基酸(例如,丝氨酸或苏氨酸)、具有含硫侧链的氨基酸(例如,半胱氨酸或甲硫氨酸)、带电荷的氨基酸(例如,精氨酸、赖氨酸、天冬氨酸或谷氨酸)、不带电荷的氨基酸(例如,丝氨酸、苏氨酸、天冬酰胺或谷氨酰胺)、芳族氨基酸(例如,酪氨酸、色氨酸或苯丙氨酸)、环状氨基酸(例如,脯氨酸)、酸性氨基酸(例如,天冬氨酸、天冬酰胺、谷氨酸或谷氨酰胺)、碱性氨基酸(例如,组氨酸、赖氨酸或精氨酸)和大体积氨基酸(例如,苯丙氨酸、酪氨酸或色氨酸)。
在一些实施方案中,对n末端间隔区结构域和/或c末端间隔区结构域的氨基酸序列的修饰包括用至少一个亲水性氨基酸取代疏水性氨基酸、用至少一个疏水性氨基酸取代亲水性氨基酸、用至少一个极性氨基酸取代非极性氨基酸、用至少一个非极性氨基酸取代极性氨基酸、至少一个带电荷的氨基酸取代不带电荷的氨基酸、用至少一个不带电荷的氨基酸取代带电荷的氨基酸、用至少一个酸性氨基酸取代碱性氨基酸、用至少一个碱性氨基酸取代酸性氨基酸、用至少一个非大体积氨基酸取代大体积氨基酸、用至少一个大体积氨基酸取代非大体积氨基酸、用至少一个具有含羟基侧链或含硫侧链的氨基酸取代脂族氨基酸、用至少一个具有含羟基侧链或含硫侧链的氨基酸取代芳族氨基酸或用至少一个芳族氨基酸取代具有含羟基侧链或含硫侧链的氨基酸。
在一些实施方案中,从n末端间隔区结构域和/或c末端间隔区结构域的氨基酸序列中移除的一个或多个氨基酸选自由以下组成的组:亲水性氨基酸(例如,赖氨酸、精氨酸、组氨酸、天冬氨酸、谷氨酸、丝氨酸、苏氨酸、天冬酰胺或谷氨酰胺)、疏水性氨基酸(例如,丙氨酸、缬氨酸、异亮氨酸、亮氨酸、甲硫氨酸、苯丙氨酸、酪氨酸、色氨酸、半胱氨酸、甘氨酸或脯氨酸)、极性氨基酸(例如,丝氨酸、苏氨酸、半胱氨酸、天冬酰胺、谷氨酰胺或酪氨酸)、非极性氨基酸(例如,甘氨酸、丙氨酸、缬氨酸、脯氨酸、亮氨酸、异亮氨酸、甲硫氨酸、色氨酸或苯丙氨酸)、具有脂族侧链的氨基酸(例如,甘氨酸、丙氨酸、缬氨酸、亮氨酸或异亮氨酸)、具有含羟基侧链的氨基酸(例如,丝氨酸或苏氨酸)、具有含硫侧链的氨基酸(例如,半胱氨酸或甲硫氨酸)、带电荷的氨基酸(例如,精氨酸、赖氨酸、天冬氨酸或谷氨酸)、不带电荷的氨基酸(例如,丝氨酸、苏氨酸、天冬酰胺或谷氨酰胺)、芳族氨基酸(例如,酪氨酸、色氨酸或苯丙氨酸)、环状氨基酸(例如,脯氨酸)、酸性氨基酸(例如,天冬氨酸、天冬酰胺、谷氨酸或谷氨酰胺)、碱性氨基酸(例如,组氨酸、赖氨酸或精氨酸)和大体积氨基酸(例如,苯丙氨酸、酪氨酸或色氨酸)。
对本文所述的间隔区结构域(例如,任何n末端间隔区结构域和/或任何c末端间隔区结构域)的任何修饰可以是对本文所述的任何n末端间隔区结构域和/或c末端间隔区结构域的氨基酸序列进行的修饰,包括seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799中的任一者。对本文所述的间隔区结构域的任何修饰可以是出于任何目的进行的修饰。例如,可以对包括可切割肽的接头的n末端间隔区结构域和/或c末端间隔区结构域进行修饰,目的是改变接头的构象,使得可切割肽的切割效率得以改变。还可以对包括可切割肽的接头的n末端间隔区结构域和/或c末端间隔区结构域进行修饰,目的是改变包括可切割肽的接头的结构,使得可切割肽的切割效率在某些ph条件下得以改变。
d.半衰期延长结构域
体内长半衰期对于治疗性蛋白质很重要。遗憾的是,施用给受试者的细胞因子通常具有短半衰期,因为它们通常通过包括由肾清除和内吞降解的机制从受试者体内快速清除。因此,在本文提供的掩蔽型细胞因子的一些实施方案中,为了延长细胞因子在体内的半衰期,将半衰期延长结构域与掩蔽型细胞因子连接。
在一些实施方案中,本文提供的掩蔽型细胞因子包含选自由抗体及其片段、白蛋白、白蛋白结合蛋白、igg结合蛋白和聚氨基酸序列组成的组的半衰期延长结构域。预期也可采用本领域中可用的延长掩蔽型细胞因子的半衰期的其它机制。半衰期延长结构域包含氨基末端和羧基末端。
在一些实施方案中,掩蔽型细胞因子包含半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子包含单个半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子包含一个以上半衰期延长结构域,其每一者可以是本文所述的任何半衰期延长结构域。在一些实施方案中,掩蔽型细胞因子包含第一半衰期延长结构域和第二半衰期延长结构域。要理解的是,提到“半衰期延长结构域”或“所述半衰期延长结构域”可指包含单个半衰期延长结构域的掩蔽型细胞因子中的半衰期延长结构域,或者其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第一半衰期延长结构域,或者其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第二半衰期延长结构域,或者其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第一半衰期延长结构域和第二半衰期延长结构域。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域与第二半衰期延长结构域连接。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域经由接头与第二半衰期延长结构域连接。在一些实施方案中,连接的第一半衰期延长结构域和第二半衰期延长结构域可以各自是本文所述的任何半衰期延长结构域。例如,在一些实施方案中,连接的第一和第二半衰期延长结构域的第一半衰期延长结构域和/或第二半衰期延长结构域是fc结构域或其片段。在一些实施方案中,连接的第一和第二半衰期延长结构域的第一半衰期延长结构域和/或第二半衰期延长结构域是抗体或其片段、变体或衍生物。
1.抗体及其片段
通过将掩蔽型细胞因子与能够进行fcrn介导的再循环的抗体或其片段连接,可以减少或以其它方式延迟掩蔽型细胞因子从受试者体内清除,从而延长施用的掩蔽型细胞因子的半衰期。
在掩蔽型细胞因子的一些实施方案中,半衰期延长结构域包含抗体或其片段。在一些实施方案中,掩蔽型细胞因子包含一种以上抗体或其片段,其每一者可以是本文所述的任何抗体或其片段。在一些实施方案中,掩蔽型细胞因子包含第一半衰期延长结构域和第二半衰期延长结构域,其每一者包含抗体或其片段。要理解的是,提到“抗体或其片段”或“所述抗体或其片段”可指包含单个半衰期延长结构域的掩蔽型细胞因子中的半衰期延长结构域的抗体或其片段,或者其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第一半衰期延长结构域的抗体或其片段,或者其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第二半衰期延长结构域的抗体或其片段,或者其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第一半衰期延长结构域的抗体或其片段和第二半衰期延长结构域的抗体或其片段。
抗体或其片段可以是任何抗体或其片段。在一些实施方案中,抗体或其片段是能够进行fcrn介导的再循环的任何抗体或其片段,如能够进行fcrn介导的再循环的任何重链多肽或其部分(例如,fc结构域或其片段)。然而,在包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子的一些实施方案中,第一半衰期延长结构域或第二半衰期延长结构域可包含不与fcrn受体结合的抗体或其片段,如轻链多肽。例如,在掩蔽型细胞因子的一些实施方案中,第一半衰期延长结构域包含抗体或其片段,所述抗体或其片段包含不与fcrn受体直接相互作用的轻链多肽或其部分,但掩蔽型细胞因子由于包含能够与fcrn受体相互作用的第二半衰期延长结构域(如通过包含重链多肽)而具有延长的半衰期。本领域中公认fcrn介导的再循环需要fcrn受体与抗体或其片段的fc区结合。例如,研究已显示残基i253、s254、h435和y436(根据kabateu索引编号系统编号)对于人fc区与人fcrn复合物之间的相互作用是重要的。参见例如firan,m.等人,int.immunol.13(2001)993-1002;shields,r.l.等人,j.biol.chem.276(2001)6591-6604)。还检查并报道了残基248-259、301-317、376-382和424-437(根据kabateu索引编号系统编号)的各种突变体。yeung,y.a.等人(j.immunol.182(2009)7667-7671。
在一些实施方案中,抗体或其片段包含重链多肽或轻链多肽。在一些实施方案中,抗体或其片段包含重链多肽或轻链多肽的一部分。在一些实施方案中,抗体或其片段包含fc结构域或其片段。在一些实施方案中,抗体或其片段包含ch2和ch3结构域或其片段。在一些实施方案中,抗体或其片段包含重链多肽的恒定结构域。在一些实施方案中,抗体或其片段包含轻链多肽的恒定结构域。在一些实施方案中,抗体或其片段包含重链多肽或其片段(例如,fc结构域或其片段)。在一些实施方案中,抗体或其片段包含轻链多肽。
在一些实施方案中,重链多肽包含seqidno:158的氨基酸序列。在一些实施方案中,轻链多肽包含seqidno:157的氨基酸序列。在一些实施方案中,重链多肽包含与seqidno:158的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,重链多肽包含seqidno:168的氨基酸序列。在一些实施方案中,重链多肽包含与seqidno:168的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,重链多肽包含seqidno:169的氨基酸序列。在一些实施方案中,重链多肽包含与seqidno:169的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,轻链多肽包含与seqidno:157的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,轻链多肽包含seqidno:170的氨基酸序列。在一些实施方案中,轻链多肽包含与seqidno:170的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,抗体或其片段包含fc结构域或其片段。在一些实施方案中,抗体或其片段是fc结构域或其片段。
在一些实施方案中,fc结构域或其片段包含选自由seqidno:616、619、622、625、721、772-774、793和796组成的组的氨基酸序列。在一些实施方案中,fc结构域或其片段包含与选自由seqidno:616、619、622、625、721、772-774、793和796组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,fc结构域或其片段包含seqidno:154的氨基酸序列。在一些实施方案中,fc结构域或其片段包含与seqidno:154的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,fc结构域或其片段包含seqidno:155的氨基酸序列。在一些实施方案中,fc结构域或其片段包含与seqidno:155的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,fc结构域或其片段包含seqidno:156的氨基酸序列。在一些实施方案中,fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,fc结构域或其片段包含seqidno:265的氨基酸序列。在一些实施方案中,fc结构域或其片段包含与seqidno:265的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,fc结构域或其片段包含seqidno:155的氨基酸序列。在一些实施方案中,fc结构域或其片段包含与seqidno:155的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,fc结构域或其片段包含seqidno:772的氨基酸序列,或者包含与seqidno:772的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,fc结构域或其片段包含seqidno:773的氨基酸序列,或者包含与seqidno:773的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,fc结构域或其片段包含seqidno:774的氨基酸序列,或者包含与seqidno:774的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含选自由seqidno:154-156、265、616、619、622、625、721、772-774、793和796组成的组的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含选自由seqidno:154-156、265、616、619、622、625、721、772-774、793和796组成的组的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与选自由seqidno:154-156、265、616、619、622、625、721、772-774、793和796组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与选自由seqidno:154-156、265、616、619、622、625、721、772-774、793和796组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含表4-11中列出的任何第一半衰期延长结构域的氨基酸序列,且第二半衰期延长结构域包含表4-11中列出的任何第一半衰期延长结构域的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:155的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:155的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:155的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:155的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:155的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:616的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:616的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:155的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:155的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:616的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:616的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:155的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:265的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:265的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:265的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:265的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:155的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:155的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:155的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:155的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:721的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:619的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:619的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:721的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:619的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:721的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:721的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:619的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:721的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:772的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:772的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:721的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:772的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:721的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:721的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:772的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:793的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:622的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:622的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:793的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:622的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:793的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:793的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:622的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:793的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:773的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:773的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:793的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:773的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:793的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:793的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:773的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:796的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:625的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:625的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:796的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:625的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:796的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:796的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:625的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:796的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:774的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:774的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:796的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:774的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:796的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:796的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:774的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:793的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:773的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:774的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:793的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:773的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:793的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:793的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:773的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:796的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:774的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:774的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:796的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:774的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:796的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:796的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:774的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:155的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:155的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:155的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:155的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:772的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:721的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:721的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:772的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:721的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:772的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:772的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidn0:721的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:156的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:157的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:158的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:158的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:157的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:157的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:158的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:158的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列,且第二半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含与seqidno:157的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,fc结构域或其片段包含seqidno:168的氨基酸序列。在一些实施方案中,fc结构域或其片段包含与seqidno:168的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,fc结构域或其片段包含seqidno:169的氨基酸序列。在一些实施方案中,fc结构域或其片段包含与seqidno:169的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,半衰期延长结构域包含通过向半衰期延长结构域的氨基酸序列引入一个或多个修饰而产生的氨基酸序列,如通过向seqidno:154-158、168-170、265、616、619、622、625、721、772-774、793和796中的任一者的氨基酸序列或者向本文所述的半衰期延长结构域的任一氨基酸序列引入一个或多个氨基酸取代、添加或缺失。一个或多个修饰可以是本文所述的任何修饰或改变,在一些实施方案中包括本文公开的促进多肽链的异源二聚化和/或抑制多肽链的同源二聚化、改变效应子功能或增强效应子功能的任何修饰或改变。
在一些实施方案中,半衰期延长结构域包含重链多肽,所述重链多肽包含改变效应子功能的一个或多个氨基酸取代。在一些实施方案中,半衰期延长结构域是igg1重链多肽,并且包含(多个)氨基取代:根据kabateu编号系统编号的n297a、n297g或n297q;l234a和l235a;c220s、c226s、c229s和p238s;c226s、c229s、e233p、l234v和l235a;l234f、l235e和p331s;s267e和l328f;d265a;和/或l234a、l235a和p329g。在一些实施方案中,半衰期延长结构域是igg1重链多肽,并且包含根据kabateu编号系统编号的选自由以下组成的组的一个或多个氨基酸取代:n297a、n297g、n297q、l234a、l235a、c220s、c226s、c229s、p238s、e233p、l234v、l234f、l235e、p331s、s267e、l328f、d265a和p329g。在一些实施方案中,半衰期延长结构域是igg2重链多肽,并且包含(多个)氨基取代:根据kabateu编号系统编号的v234a和g237a;h268q、v309l、a330s和a331s;或v234a、g237a、p238s、h268a、v309l和a330s。在一些实施方案中,半衰期延长结构域是igg2重链多肽,并且包含根据kabateu编号系统编号的选自由以下组成的组的一个或多个氨基酸取代:v234a、g237a、h268q、v309l、a330s、a331s、p238s、h268a和v309l。在一些实施方案中,半衰期延长结构域是igg4重链多肽,并且包含(多个)氨基取代:根据kabateu编号系统编号的l235a、g237a和e318a;s228p、l234a和l235a;h268q、v309l、a330s和p331s;和/或s228p和l235a。在一些实施方案中,半衰期延长结构域是igg2重链多肽,并且包含根据kabateu编号系统编号的选自由以下组成的组的一个或多个氨基酸取代:l235a、g237a、e318a、s228p、l234a、h268q、v309l、a330s和p331s。
在一些实施方案中,半衰期延长结构域包含重链多肽,所述重链多肽包含增强效应子功能的一个或多个氨基酸取代。在一些实施方案中,半衰期延长结构域是igg1重链多肽,并且包含(多个)氨基酸取代:根据kabateu编号系统编号的s298a、e333a和k334a;s239d和i332e;s239d、a330l和i332e;p247i和a339d或a339q;d280h和k290s;d280h、k290s和s298d或s298v;f243l、r292p和y300l;f243l、r292p、y300l和p396l;f243l、r292p、y300l、v305i和p396l;g236a、s239d和i332e;k326a和e333a;k326w和e333s;k290e、s298g和t299a;k290e、s298g、t299a和k326e;k290n、s298g和t299a;k290n、s298g、t299a和k326e;k334v;l235s、s239d和k334v;k334v和q331m、s239d、f243v、e294l或s298t;e233l、q311m和k334v;l234i、q311m和k334v;k334v和s298t、a330m或a330f;k334v、q311m和a330m或a330f;k334v、s298t和a330m或a330f;k334v、s239d和a330m或s298t;l234y、y296w和k290y、f243v或e294l;y296w和l234y或k290y;s239d、a330s和i332e、v264i;f243l和v264i;l328m;i332e;l328m和i332e;v264i和i332e;s239e和i332e;s239q和i332e;s239e;a330y;i332d;l328i和i332e;l328q和i332e;v264t;v240i;v266i;s239d;s239d和i332d;s239d和i332n;s239d和i332q;s239e和i332d;s239e和i332n;s239e和i332q;s239n和i332d;s239n和i332e;s239q和i332d;a330y和i332e;v264i、a330y和i332e;a330l和i332e;v264i、a330l和i332e;l234e、l234y或l234i;l235d、l235s、l235y或l235i;s239t;v240m;v264y;a330i;n325t;i332e和l328d、l328v、l328t或l328i;v264i、i332e和s239e或s239q;s239e、v264i、a330y和i332e;a330y、i332e和s239d或s239n;a330l、i332e和s239d或s239n;v264i、s298a和i332e;s298a、i332e和s239d或s239n;s239d、v264i和i332e;s239d、v264i、s298a和i332e;s239d、v264i、a330l和i332e;s239d、i332e和a330i;p230a;p230a、e233d和i332e;e272y;k274t、k274e、k274r、k274l或k274y;f275w;n276l;y278t;v302i;e318r;s324d、s324i或s324v;k326i或k326t;t335d、t335r或t335y;v240i和v266i;s239d、a330y、i332e和l234i;s239d、a330y、i332e和l235d;s239d、a330y、i332e和v240i;s239d、a330y、i332e和v264t;和/或s239d、a330y、i332e和k326e或k326t。在一些实施方案中,半衰期延长结构域是igg1重链多肽,并且包含选自由以下组成的组的一个或多个氨基酸取代:p230a、e233d、l234e、l234y、l234i、l235d、l235s、l235y、l235i、s239d、s239e、s239n、s239q、s239t、v240i、v240m、f243l、v264i、v264t、v264y、v266i、e272y、k274t、k274e、k274r、k274l、k274y、f275w、n276l、y278t、v302i、e318r、s324d、s324i、s324v、n325t、k326i、k326t、l328m、l328i、l328q、l328d、l328v、l328t、a330y、a330l、a330i、i332d、i332e、i332n、i332q、t335d、t335r和t335y。
在一些实施方案中,半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含改变效应子功能的一个或多个氨基酸取代。在一些实施方案中,半衰期延长结构域是igg1fc结构域或其片段,并且包含(多个)氨基取代:根据kabateu编号系统编号的n297a、n297g或n297q;l234a和l235a;c220s、c226s、c229s和p238s;c226s、c229s、e233p、l234v和l235a;l234f、l235e和p331s;s267e和l328f;d265a;和/或l234a、l235a和p329g。在一些实施方案中,半衰期延长结构域是igg1fc结构域或其片段,并且包含根据kabateu编号系统编号的选自由以下组成的组的一个或多个氨基酸取代:n297a、n297g、n297q、l234a、l235a、c220s、c226s、c229s、p238s、e233p、l234v、l234f、l235e、p331s、s267e、l328f、d265a和p329g。在一些实施方案中,半衰期延长结构域是igg2fc结构域或其片段,并且包含(多个)氨基取代:根据kabateu编号系统编号的v234a和g237a;h268q、v309l、a330s和a331s;和/或v234a、g237a、p238s、h268a、v309l和a330s。在一些实施方案中,半衰期延长结构域是igg2fc结构域或其片段,并且包含根据kabateu编号系统编号的选自由v234a、g237a、h268q、v309l、a330s、a331s、p238s、h268a和v309l组成的组的一个或多个氨基酸取代。在一些实施方案中,半衰期延长结构域是igg4fc结构域或其片段,并且包含(多个)氨基取代:根据kabateu编号系统编号的l235a、g237a和e318a;s228p、l234a和l235a;h268q、v309l、a330s和p331s;和/或s228p和l235a。在一些实施方案中,半衰期延长结构域是igg2fc结构域或其片段,并且包含根据kabateu编号系统编号的选自由l235a、g237a、e318a、s228p、l234a、h268q、v309l、a330s和p331s组成的组的一个或多个氨基酸取代。
在一些实施方案中,半衰期延长结构域包含fc结构域或其片段,所述fc结构域或其片段包含增强效应子功能的一个或多个氨基酸取代。在一些实施方案中,半衰期延长结构域是igg1fc结构域或其片段,并且包含(多个)氨基酸取代:根据kabateu编号系统编号的s298a、e333a和k334a;s239d和i332e;s239d、a330l和i332e;p247i和a339d或a339q;d280h和k290s;d280h、k290s和s298d或s298v;f243l、r292p和y300l;f243l、r292p、y300l和p396l;f243l、r292p、y300l、v305i和p396l;g236a、s239d和i332e;k326a和e333a;k326w和e333s;k290e、s298g和t299a;k290e、s298g、t299a和k326e;k290n、s298g和t299a;k290n、s298g、t299a和k326e;k334v;l235s、s239d和k334v;k334v和q331m、s239d、f243v、e294l或s298t;e233l、q311m和k334v;l234i、q311m和k334v;k334v和s298t、a330m或a330f;k334v、q311m和a330m或a330f;k334v、s298t和a330m或a330f;k334v、s239d和a330m或s298t;l234y、y296w和k290y、f243v或e294l;y296w和l234y或k290y;s239d、a330s和i332e、v264i;f243l和v264i;l328m;i332e;l328m和i332e;v264i和i332e;s239e和i332e;s239q和i332e;s239e;a330y;i332d;l328i和i332e;l328q和i332e;v264t;v240i;v266i;s239d;s239d和i332d;s239d和i332n;s239d和i332q;s239e和i332d;s239e和i332n;s239e和i332q;s239n和i332d;s239n和i332e;s239q和i332d;a330y和i332e;v264i、a330y和i332e;a330l和i332e;v264i、a330l和i332e;l234e、l234y或l234i;l235d、l235s、l235y或l235i;s239t;v240m;v264y;a330i;n325t;i332e和l328d、l328v、l328t或l328i;v264i、i332e和s239e或s239q;s239e、v264i、a330y和i332e;a330y、i332e和s239d或s239n;a330l、i332e和s239d或s239n;v264i、s298a和i332e;s298a、i332e和s239d或s239n;s239d、v264i和i332e;s239d、v264i、s298a和i332e;s239d、v264i、a330l和i332e;s239d、i332e和a330i;p230a;p230a、e233d和i332e;e272y;k274t、k274e、k274r、k274l或k274y;f275w;n276l;y278t;v302i;e318r;s324d、s324i或s324v;k326i或k326t;t335d、t335r或t335y;v240i和v266i;s239d、a330y、i332e和l234i;s239d、a330y、i332e和l235d;s239d、a330y、i332e和v240i;s239d、a330y、i332e和v264t;和/或s239d、a330y、i332e和k326e或k326t。在一些实施方案中,半衰期延长结构域是igg1fc结构域或其片段,并且包含选自由以下组成的组的一个或多个氨基酸取代:p230a、e233d、l234e、l234y、l234i、l235d、l235s、l235y、l235i、s239d、s239e、s239n、s239q、s239t、v240i、v240m、f243l、v264i、v264t、v264y、v266i、e272y、k274t、k274e、k274r、k274l、k274y、f275w、n276l、y278t、v302i、e318r、s324d、s324i、s324v、n325t、k326i、k326t、l328m、l328i、l328q、l328d、l328v、l328t、a330y、a330l、a330i、i332d、i332e、i332n、i332q、t335d、t335r和t335y。
在一些实施方案中,半衰期延长结构域包含增强半衰期延长结构域与fcrn的结合的一个或多个氨基酸取代。在一些实施方案中,一个或多个氨基酸取代增加含fc的多肽(例如,重链多肽或fc结构域或其片段)在酸性ph下对fcrn的结合亲和力。在一些实施方案中,半衰期延长结构域包含选自由以下组成的组的一个或多个氨基酸取代:m428l;t250q和m428l;m252y、s254t和t256e;p257i和n434h;d376v和n434h;p257i和q3111;n434a;n434w;m428l和n434s;v259i和v308f;m252y、s254t和t256e;v259i、v308f和m428l;t307q和n434a;t307q和n434s;t307q、e380a和n434a;v308p和n434a;n434h;和v308p。
在一些实施方案中,掩蔽型细胞因子是二聚体,其通过一个拷贝的掩蔽型细胞因子的半衰期延长结构域与第二个拷贝的掩蔽型细胞因子的相应半衰期延长结构域形成二硫键而形成。
2.白蛋白
白蛋白(本文也称为人血清白蛋白(hsa))是一种天然载体蛋白,由于其大小和对fcrn介导的再循环的敏感性,其具有大约三周的延长的血清半衰期,这阻止了细胞内降解。因此,将掩蔽型细胞因子与白蛋白连接可大为延长掩蔽型细胞因子的半衰期。已经采用了这种方法来延长治疗有益性蛋白质的血浆半衰期。参见例如wo2001/079271a1和wo2003/59934a2,其内容以引用的方式并入本文。成熟形式的hsa是如seqidno:171中所示的585个氨基酸的多肽。
在一些实施方案中,掩蔽型细胞因子包含半衰期延长结构域,所述半衰期延长结构域包含白蛋白多肽或其片段或变体(下文称为“白蛋白”或“白蛋白多肽”)。如本文所用,术语“白蛋白”和“白蛋白多肽”包括白蛋白的片段以及白蛋白的变体。白蛋白多肽包含氨基末端和羧基末端。所述白蛋白多肽可以是任何白蛋白多肽,包括其任何片段或变体,如wo200i/079271a1;wo2003/59934a2;us20160152686a1;wo2012/059486;wo2011/124718;us20070048282中描述的任何白蛋白多肽,其内容以引用的方式并入本文。在一些实施方案中,白蛋白多肽是hsa。
在掩蔽型细胞因子的一些实施方案中,半衰期延长结构域包含白蛋白多肽。在一些实施方案中,掩蔽型细胞因子包含一种以上白蛋白多肽,其每一者可以是本文所述的任何白蛋白多肽。在一些实施方案中,掩蔽型细胞因子包含第一半衰期延长结构域和第二半衰期延长结构域,其每一者包含白蛋白多肽。要理解的是,提到“白蛋白多肽”或“所述白蛋白多肽”可指包含单个半衰期延长结构域的掩蔽型细胞因子中的半衰期延长结构域的白蛋白多肽,或者其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第一半衰期延长结构域的白蛋白多肽,或者其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第二半衰期延长结构域的白蛋白多肽,或者其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第一半衰期延长结构域的白蛋白多肽和第二半衰期延长结构域的白蛋白多肽。
在一些实施方案中,白蛋白多肽与掩蔽部分连接。在一些实施方案中,掩蔽部分与白蛋白多肽的氨基末端或羧基末端连接。在一些实施方案中,白蛋白多肽经由接头与掩蔽部分连接。在一些实施方案中,接头与白蛋白多肽的氨基末端或羧基末端连接。在一些实施方案中,接头的n末端间隔区结构域或c末端间隔区结构域与白蛋白多肽的氨基末端或羧基末端连接。在一些实施方案中,接头的可切割肽与白蛋白多肽的氨基末端或羧基末端连接。在一些实施方案中,白蛋白多肽与细胞因子或其功能片段连接。在一些实施方案中,细胞因子或其功能片段与白蛋白多肽的氨基末端或羧基末端连接。在一些实施方案中,白蛋白多肽经由接头与细胞因子或其功能片段连接。在一些实施方案中,接头与白蛋白多肽的氨基末端或羧基末端连接。
在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸序列。在一些实施方案中,白蛋白多肽包含与seqidno:171的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,白蛋白多肽是由hsa的片段(任选具有一个或多个氨基酸修饰)组成的白蛋白的变体。在一些实施方案中,hsa的片段是野生型hsa的片段。在一些实施方案中,白蛋白多肽包含hsa结构域1(seqidno:171的氨基酸残基1-194)、hsa结构域2(seqidno:171的氨基酸残基195-387)、hsa结构域3(氨基酸残基388-585)、hsa结构域1和2、hsa结构域2和3、hsa结构域1和3或hsa结构域3的两个拷贝。在一些实施方案中,白蛋白多肽由hsa结构域1(seqidno:171的氨基酸残基1-194)、hsa结构域2(seqidno:171的氨基酸残基195-387)、hsa结构域3(氨基酸残基388-585)、hsa结构域1和2、hsa结构域2和3、hsa结构域1和3或hsa结构域3的两个拷贝组成。
在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基1-194。在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基195-387。在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基388-585。在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基1-387。在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基195-585。在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基1-105。在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基120-194。在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基195-291。在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基316-387。在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基388-491。在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基512-585。在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基1-194和388-585。在一些实施方案中,白蛋白多肽包含seqidno:171的氨基酸残基388-585的两个拷贝。
在一些实施方案中,白蛋白多肽包含通过对本文所述的白蛋白多肽的任何实施方案的氨基酸序列进行一个或多个氨基酸修饰而产生的氨基酸序列。在一些实施方案中,白蛋白多肽包含有包含一个或多个增加白蛋白多肽在血清中的半衰期的氨基酸修饰的氨基酸序列。增加白蛋白多肽在血清中的半衰期的示例性氨基酸修饰包括对hsa的e492、n503、d550和/或k573进行的氨基酸取代。在一些实施方案中,白蛋白多肽包含增加白蛋白多肽对fcrn受体的亲和力的一个或多个氨基酸修饰。增加白蛋白多肽对fcrn受体的亲和力的示例性氨基酸修饰包括v418m、t420a、e505g和v547a。在一些实施方案中,白蛋白多肽包含通过对seqidno:171的氨基酸序列的一个或多个氨基酸修饰产生的氨基酸序列。在一些实施方案中,白蛋白多肽包含通过对seqidno:171的氨基酸序列的一个或多个氨基酸修饰产生的氨基酸序列。在一些实施方案中,对本文所述的任何白蛋白多肽的氨基酸序列的一个或多个氨基酸修饰选自由以下组成的组:q417a、h440q、h464q、a490d、e492g/t/p/h、v493p/l、d494n/q/a/e/p、e495q/a、t496a、p499a、k500e/g/d/a/s/c/p/h/f/n/w/t/m/y/v/q/l/i/r、e501a/p/q、n503k/d/h、a504e、e505k/d、t506f/s、h510q、h535q、k536a、p537a、k538a/h、t540s、k541a/d/g/n/e、e542p/d、d550n、k573y/w/p/h/f/v/i/t/n/s/g/m/c/a/e/q/r/l/d、k574n、q580k、l575f、a577t/e、a578r/s、s579c/t、q580k、a581d、a582t和g584a。在一些实施方案中,对本文所述的任何白蛋白多肽的氨基酸序列的一个或多个氨基酸修饰选自由v418m、t420a、e505g和v547a组成的组。
3.结合蛋白
延长掩蔽型细胞因子在血清中的半衰期的另外的策略包括将掩蔽型细胞因子与某些结合蛋白如白蛋白结合蛋白或igg结合蛋白连接。结合蛋白可以是与具有延长的半衰期的血清蛋白如白蛋白或igg结合的任何蛋白。白蛋白和igg是已知在血清中具有长半衰期的多肽。由于白蛋白结合蛋白与血清中的白蛋白结合或以其它方式与血清中的白蛋白缔合,因此与白蛋白结合蛋白连接的掩蔽型细胞因子可在血清中表现出延长的半衰期。同样,由于igg结合蛋白结合血清中的igg或以其它方式与血清中的igg缔合,因此与igg结合蛋白连接的掩蔽型细胞因子可在血清中表现出延长的半衰期。
在例如wo199i/01743、wo2001/45746、wo2002/076489、wo2004/041865或us20070269422a1中描述了白蛋白结合蛋白及使它们与所关注的蛋白连接的方法,其内容以引用的方式并入本文。
在一些实施方案中,半衰期延长结构域包含白蛋白结合蛋白。白蛋白结合蛋白可以是例如wo199i/01743、wo2001/45746、wo2002/076489、wo2004/041865、us20070269422a1;us20160152686a1;dennis等人(2002),jbc277(38):35035-35043中描述的任何白蛋白结合蛋白。
在掩蔽型细胞因子的一些实施方案中,半衰期延长结构域包含白蛋白结合蛋白。在一些实施方案中,掩蔽型细胞因子包含一种以上白蛋白结合蛋白,其每一者可以是本文所述的任何白蛋白结合蛋白。在一些实施方案中,掩蔽型细胞因子包含第一半衰期延长结构域和第二半衰期延长结构域,其每一者包含白蛋白结合蛋白。要理解的是,提到“白蛋白结合蛋白”或“所述白蛋白结合蛋白”可指包含单个半衰期延长结构域的掩蔽型细胞因子中的半衰期延长结构域的白蛋白结合蛋白,或其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第一半衰期延长结构域的白蛋白结合蛋白,或其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第二半衰期延长结构域的白蛋白结合蛋白,或其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第一半衰期延长结构域的白蛋白结合蛋白和第二半衰期延长结构域的白蛋白结合蛋白。
在一些实施方案中,白蛋白结合蛋白包含链球菌蛋白g(spg)的白蛋白结合结构域(abd)。参见例如nygren等人,j.mol.recogn.(1988)1(2):69-74。在一些实施方案中,白蛋白结合蛋白包含spg菌株g148的abd。在一些实施方案中,白蛋白结合蛋白包含spg菌株g148的c末端白蛋白结合结构域3(abd3)。参见例如nilvebrant和hober(2013),comput.struct.biotechol.j.,6:e201303009。在一些实施方案中,白蛋白结合蛋白包含seqidno:172的氨基酸序列。在一些实施方案中,白蛋白结合蛋白包含与seqidno:172的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,白蛋白结合蛋白包含天然或合成肽。在一些实施方案中,白蛋白结合蛋白包含seqidno:173或174的氨基酸序列。在一些实施方案中,白蛋白结合蛋白包含与seqidno:173或174的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,白蛋白结合结构域包含通过向白蛋白结合结构域的氨基酸序列引入一个或多个修饰而产生的氨基酸序列,例如通过向seqidno:172-174中的任一者的氨基酸序列引入一个或多个氨基酸取代、添加或缺失。
在一些实施方案中,白蛋白结合蛋白是与白蛋白结合或以其它方式与白蛋白缔合的单结构域抗体或其片段,如纳米抗体。参见例如wo2004041865a2和us20070269422a1,其内容以引用的方式并入本文。在一些实施方案中,单结构域抗体或其片段包含选自由seqidno:252-259组成的组的氨基酸序列。在一些实施方案中,单结构域抗体或其片段包含与选自由seqidno:252-259组成的组的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,白蛋白结合蛋白与掩蔽部分连接。在一些实施方案中,掩蔽部分与白蛋白结合蛋白的氨基末端或羧基末端连接。在一些实施方案中,白蛋白结合蛋白经由接头与掩蔽部分连接。在一些实施方案中,接头与白蛋白结合蛋白的氨基末端或羧基末端连接。在一些实施方案中,接头的n末端间隔区结构域或c末端间隔区结构域与白蛋白结合结构域的氨基末端或羧基末端连接。在一些实施方案中,接头的可切割肽与白蛋白结合结构域的氨基末端或羧基末端连接。在一些实施方案中,白蛋白结合蛋白与细胞因子或其功能片段连接。在一些实施方案中,细胞因子或其功能片段与白蛋白结合蛋白的氨基末端或羧基末端连接。在一些实施方案中,白蛋白结合蛋白经由接头与细胞因子或其功能片段连接。在一些实施方案中,接头与白蛋白结合蛋白的氨基末端或羧基末端连接。
结合蛋白的另一实例是igg结合蛋白。已经报道了igg结合蛋白。关于igg结合蛋白(包括特异性igg结合蛋白及其应用)的综述,参见例如choe等人,(2016)materials9(12):994,其内容以引用的方式并入本文。
在掩蔽型细胞因子的一些实施方案中,半衰期延长结构域包含igg结合蛋白。在一些实施方案中,掩蔽型细胞因子包含一种以上igg结合蛋白,其每一者可以是本文所述的任何igg结合蛋白。在一些实施方案中,掩蔽型细胞因子包含第一半衰期延长结构域和第二半衰期延长结构域,其每一者包含igg结合蛋白。要理解的是,提到“igg结合蛋白”或“所述igg结合蛋白”可指包含单个半衰期延长结构域的掩蔽型细胞因子中的半衰期延长结构域的igg结合蛋白,或其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第一半衰期延长结构域的igg结合蛋白,或其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第二半衰期延长结构域的igg结合蛋白,或其可指包含第一半衰期延长结构域和第二半衰期延长结构域的掩蔽型细胞因子中的第一半衰期延长结构域的igg结合蛋白和第二半衰期延长结构域的igg结合蛋白。
在一些实施方案中,半衰期延长结构域包含igg结合蛋白。所述igg结合蛋白可以是任何igg结合蛋白。igg结合蛋白可以是例如choe等人(2016)materials9(12):994;us20140046037a1中描述的任何igg结合蛋白。例如,已经显示多种细菌蛋白与哺乳动物igg结合,包括蛋白a、g、l和z以及蛋白lg和la的融合蛋白。参见例如choe等人(2016)materials9(12):994。在一些实施方案中,igg结合蛋白是来自细菌金黄色葡萄球菌的葡萄球菌蛋白a(spa)蛋白或其片段或变体。在一些实施方案中,igg结合结构域是spa的igg结合结构域或其片段或变体。在一些实施方案中,igg结合结构域是spaigg结合结构域e、d、a、b、c和z中的一者或多者或其片段或变体。
在一些实施方案中,igg结合结构域包含选自由seqidno:175-186组成的组的氨基酸序列。在一些实施方案中,igg结合蛋白包含与seqidno:175-186中的任一者的氨基酸序列具有约或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
在一些实施方案中,igg结合结构域包含通过向igg结合结构域的氨基酸序列引入一个或多个修饰而产生的氨基酸序列,如通过向seqidno:175-186中的任一者的氨基酸序列引入一个或多个氨基酸取代、添加或缺失。
在一些实施方案中,igg结合蛋白与掩蔽部分连接。在一些实施方案中,掩蔽部分与igg结合蛋白的氨基末端或羧基末端连接。在一些实施方案中,igg结合蛋白经由接头与掩蔽部分连接。在一些实施方案中,接头与igg结合蛋白的氨基末端或羧基末端连接。在一些实施方案中,接头的n末端间隔区结构域或c末端间隔区结构域与igg结合结构域的氨基末端或羧基末端连接。在一些实施方案中,接头的可切割肽与igg结合结构域的氨基末端或羧基末端连接。在一些实施方案中,igg结合蛋白与细胞因子或其功能片段连接。在一些实施方案中,细胞因子或其功能片段与igg结合蛋白的氨基末端或羧基末端连接。在一些实施方案中,igg结合蛋白经由接头与细胞因子或其功能片段连接。在一些实施方案中,接头与igg结合蛋白的氨基末端或羧基末端连接。
4.抗体衍生物
本文所述的掩蔽型细胞因子或者可与各种抗体衍生物连接,包括但不限于scfv、scfc、双可变结构域(dvd)和基于crossmab方法的抗体衍生物。参见例如klein等人(2012),mabs,4(6):653-663;us20070071675a1。抗体衍生物包括工程化为双特异性抗体或其片段的抗体衍生物。如此,在一些实施方案中,半衰期延长结构域可包含任何抗体衍生物、其变体或融合产物,包括但不限于scfv、scfc、双可变结构域(dvd)、基于crossmab方法的抗体衍生物和双特异性抗体或其片段。
5.聚氨基酸序列
延长掩蔽型细胞因子在血清中的半衰期的另外的策略是通过将掩蔽型细胞因子与聚氨基酸序列连接。如此,在一些实施方案中,半衰期延长结构域包含聚氨基酸序列。聚氨基酸序列可以是当与掩蔽型细胞因子连接时能够延长掩蔽型细胞因子在血清中的半衰期的任何聚氨基酸序列。聚氨基酸序列的实例包括pas多肽和xten多肽。
在一些实施方案中,聚氨基酸序列是包含小氨基酸残基脯氨酸、丙氨酸和任选丝氨酸的多肽链(pas多肽)。pas序列是亲水且不带电荷的聚合物,其具有类似于聚乙二醇(peg)的生物物理特性,其通常与治疗性蛋白质连接,作为延长治疗性蛋白质的体内半衰期的策略。参见例如schlapschy等人(2013)proteineng.des.sel.,26(8):489-501;wo2008155134a1;wo2011144756a1;wo2016130451a1,其内容以引用的方式并入本文。已经观察到,与没有连接pas多肽的天然状态的治疗性蛋白质相比,pas多肽与治疗性蛋白质的连接增加了体内和/或体外稳定性。在一些实施方案中,pas多肽呈现无规卷曲构象。在一些实施方案中,pas多肽形成无规卷曲构象结构域。
在一些实施方案中,半衰期延长结构域包含有包含氨基酸残基脯氨酸和丙氨酸的pas多肽。在一些实施方案中,半衰期延长结构域包含有包含氨基酸残基脯氨酸、丙氨酸和丝氨酸的pas多肽。在一些实施方案中,pas多肽包含至少25个氨基酸残基、至少50个氨基酸残基、至少100个氨基酸残基、至少150个氨基酸残基、至少200个氨基酸残基、至少250个氨基酸残基、至少300个氨基酸残基、至少400个氨基酸残基、至少500个氨基酸残基、至少600个氨基酸残基、至少700个氨基酸残基、至少800个氨基酸残基、至少900个氨基酸残基、至少1000个氨基酸残基、至少1100个氨基酸残基、至少1200个氨基酸残基、至少1300个氨基酸残基、至少1500个氨基酸残基、至少2000个氨基酸残基、至少2500个氨基酸残基或至少3000个氨基酸残基。在一些实施方案中,pas多肽包含至少25个氨基酸残基、至少50个氨基酸残基、至少100个氨基酸残基、至少150个氨基酸残基、至少200个氨基酸残基、至少250个氨基酸残基、至少300个氨基酸残基、至少400个氨基酸残基、至少500个氨基酸残基、至少600个氨基酸残基、至少700个氨基酸残基、至少800个氨基酸残基、至少900个氨基酸残基、至少1000个氨基酸残基、至少1100个氨基酸残基、至少1200个氨基酸残基、至少1300个氨基酸残基、至少1500个氨基酸残基、至少2000个氨基酸残基、至少2500个氨基酸残基或至少3000个氨基酸残基,其中每个氨基酸残基是脯氨酸或丙氨酸。在一些实施方案中,pas多肽包含至少25个氨基酸残基、至少50个氨基酸残基、至少100个氨基酸残基、至少150个氨基酸残基、至少200个氨基酸残基、至少250个氨基酸残基、至少300个氨基酸残基、至少400个氨基酸残基、至少500个氨基酸残基、至少600个氨基酸残基、至少700个氨基酸残基、至少800个氨基酸残基、至少900个氨基酸残基、至少1000个氨基酸残基、至少1100个氨基酸残基、至少1200个氨基酸残基、至少1300个氨基酸残基、至少1500个氨基酸残基、至少2000个氨基酸残基、至少2500个氨基酸残基或至少3000个氨基酸残基,其中每个氨基酸残基是选自由脯氨酸、丙氨酸和丝氨酸组成的组的氨基酸。
在一些实施方案中,聚氨基酸序列是延伸的重组多肽(xten多肽)。xten多肽是具有在生理条件下具有低程度二级或三级结构或没有二级或三级结构的非天然存在的基本上非重复序列的多肽。xten多肽通常具有约36至约3000个氨基酸残基,其中大部分或全部是小的亲水性氨基酸(例如,精氨酸、赖氨酸、苏氨酸、丙氨酸、天冬酰胺、谷氨酰胺、天冬氨酸、谷氨酸、丝氨酸和甘氨酸)。xten多肽的生理化学特性以及非结构化特性部分是由于不成比例地限于4-6种类型的亲水性氨基酸的总氨基酸组成、氨基酸以非重复设计方式的连接以及xten多肽的长度所致。已经观察到xten多肽与治疗性蛋白质的连接改善治疗性蛋白质的溶解性和稳定性,并且增加其半衰期。参见例如podust等人(2016)j.controlledrelease,240:52-66;wo2013130683a2,其内容以引用的方式并入本文。
在一些实施方案中,半衰期延长结构域包含xten多肽,所述xten多肽包含由选自由甘氨酸(g)、丙氨酸(a)、丝氨酸(s)、苏氨酸(t)、谷氨酸(e)和脯氨酸(p)组成的组的四种、五种或六种类型的氨基酸残基组成的氨基酸序列。
在一些实施方案中,xten多肽包含约25至约500个氨基酸残基、约200至约1000个氨基酸残基、约500至约1500个氨基酸残基、约1000至约2000个氨基酸残基或约1500至约3000个氨基酸残基的氨基酸序列。在一些实施方案中,至少约70%、75%、80%或85%的氨基酸序列由非重叠序列基序组成。在一些实施方案中,基序中的每一者具有5至100个氨基酸残基、5至50个氨基酸残基或9至36个氨基酸残基,且其中至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%或100%的基序中的每一者由选自由甘氨酸(g)、丙氨酸(a)、丝氨酸(s)、苏氨酸(t)、谷氨酸(e)和脯氨酸(p)组成的组的四种、五种或六种类型的氨基酸残基组成,在一些实施方案中,全长xten多肽中的任何一种氨基酸类型的含量不超过约40%、约35%、约30%、约25%、约15%、约10%或约8%。
在一些实施方案中,xten多肽包含约25至约500个氨基酸残基、约200至约1000个氨基酸残基、约500至约1500个氨基酸残基、约1000至约2000个氨基酸残基或约1500至约3000个氨基酸残基的氨基酸序列,其中至少约80%的氨基酸序列由非重叠序列基序组成,其中基序中的每一者具有9至36个氨基酸残基,且其中至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%或100%的基序中的每一者由选自由甘氨酸(g)、丙氨酸(a)、丝氨酸(s)、苏氨酸(t)、谷氨酸(e)和脯氨酸(p)组成的组的四种、五种或六种类型的氨基酸残基组成,且其中全长xten多肽中的任何一种氨基酸类型的含量不超过约40%、约35%、约30%、约25%、约15%、约10%或约8%。
6.peg化和糖基化
延长本文提供的掩蔽型细胞因子的半衰期的另外的策略包括peg化和另外的糖基化位点的工程化。下面进一步详细讨论这些策略中的每一者。
“peg化”是指聚乙二醇(peg)聚合物链与诸如药物、治疗性蛋白质、多肽、抗体、抗体片段、抗体衍生物的分子和宏观结构或与本文提供的任何掩蔽型细胞因子或其组分(例如,掩蔽型细胞因子的半衰期延长结构域和/或掩蔽型细胞因子的细胞因子或其功能片段)共价或非共价连接或融合的过程。peg化的益处包括例如(1)显著提高的体内循环半衰期,这归因于由于聚合物将分子的表观尺寸增加到高于肾小球过滤极限而逃避肾清除,和/或通过逃避细胞清除机制,(2)peg连接的分子的降低的抗原性和免疫原性,(3)改善的药代动力学,(4)改善的溶解性,(5)改善的配制和给药选择,(6)经由减少皮下注射部位的损失而提高的生物利用度,(7)peg化分子改善的热稳定性和机械稳定性。
各种分子和宏观结构的peg化方法是本领域中熟知的。参见例如us20140256636a1;fee和damodaran(2010)europeanpharmaceuticalreview,15(1):18-26;chapman等人(1999)naturebiotechnol.,17:780-783;yang等人(2003),proteineng.,16(10):761-770;chapman,adv.drug.deliv.rev.(2002),54(4):531-545,其内容以引用的方式并入本文。
在一些实施方案中,本文任何实施方案的掩蔽型细胞因子是peg化的。例如,在一些实施方案中,这是通过用基团特异性试剂官能化peg来实现的,使得peg与蛋白质(例如,半衰期延长结构域或细胞因子或其功能片段)的缀合可靶向蛋白质的特定侧链基团,如氨基、羧基、巯基或胍基。在一些实施方案中,通过氨基酸取代将半胱氨酸(c)残基以位点特异性方式引入到蛋白质(例如,半衰期延长结构域或细胞因子或其功能片段)中。然后可以使用基于马来酰亚胺化学法的peg试剂将新引入的半胱氨酸残基的硫醇基团靶向peg化。用半胱氨酸替代丝氨酸(s)或苏氨酸(t)的优点在于修饰蛋白的净电荷不因peg化而改变。如此,在一些实施方案中,可以通过引入用于peg化的半胱氨酸残基来修饰或进一步修饰掩蔽型细胞因子的组分,如任何细胞因子或其功能片段和/或任何半衰期延长结构域。
“糖基化”是指将糖或糖基添加到多肽上。多肽的糖基化通常是n连接的或o连接的。n连接是指碳水化合物部分与天冬酰胺残基的侧链的连接。三肽序列天冬酰胺-x-丝氨酸(n-x-s)和天冬酰胺-x-苏氨酸(n-x-t)是碳水化合物部分与天冬酰胺侧链的酶促连接的识别序列,其中x是除脯氨酸(p)以外的任何氨基酸。因此,在多肽中存在这些三肽序列中的任一者产生了潜在的糖基化位点。o连接的糖基化是指一种糖(例如,n-乙酰半乳糖胺、半乳糖或木糖)与羟基氨基酸(最常见的是丝氨酸或苏氨酸,尽管也可以使用5-羟基脯氨酸或5-羟基赖氨酸)的连接。
已经显示天然存在的糖基化提高蛋白质的分子稳定性。参见例如sola等人(2007),cell.mol.lifesci.,64(16):2133-2152。还已经显示,另外的糖基化位点的工程化可以稳定多种蛋白质治疗剂以对抗最主要的生理化学不稳定性。参见例如sola和griebenow(2009),j.pharm.sci.,98(4):1223-1245。已显示通过糖基化得以改善的药学上相关的蛋白质不稳定性当中有例如氧化;交联;ph、化学、热和冷冻诱导的变性/解折叠;沉淀;动力学激活;和聚集。同上。
通过改变氨基酸序列,使得在掩蔽型细胞因子的氨基酸序列中(例如,在半衰期延长结构域和/或细胞因子或其功能片段的氨基酸序列中)产生上述三肽序列中的一者或多者(对于n连接的糖基化位点),由此方便地实现向掩蔽型细胞因子中添加糖基化位点。也可以通过在掩蔽型细胞因子的氨基酸序列中(例如,在半衰期延长结构域和/或细胞因子或其功能片段的氨基酸序列中)添加或取代一个或多个丝氨酸或苏氨酸残基来进行改变(对于o连接的糖基化位点)。
在一些实施方案中,本文任何实施方案的掩蔽型细胞因子通过如下方式被修饰或进一步修饰:改变掩蔽型细胞因子的氨基酸序列(例如,半衰期延长结构域和/或细胞因子或其功能片段的氨基酸序列),使得一个或多个另外的n-x-s和/或n-x-t三肽序列被引入到掩蔽型细胞因子或其组分的氨基酸序列中(用于添加一个或多个n连接的糖基化位点)。在一些实施方案中,本文任何实施方案的掩蔽型细胞因子通过如下方式被修饰或进一步修饰:改变掩蔽型细胞因子或其组分的氨基酸序列(例如,半衰期延长结构域和/或细胞因子或其功能片段的氨基酸序列),使得一个或多个另外的丝氨酸或苏氨酸残基被引入到掩蔽型细胞因子或其组分的氨基酸序列中(用于添加一个或多个o连接的糖基化位点)。在一些实施方案中,通过向掩蔽型细胞因子或其组分的氨基酸序列中添加一个或多个氨基酸来实现用于添加一个或多个n连接的糖基化位点和/或用于添加一个或多个o连接的糖基化位点的氨基酸序列改变。在一些实施方案中,通过取代掩蔽型细胞因子或其组分的氨基酸序列中的一个或多个氨基酸来实现用于添加一个或多个n连接的糖基化位点和/或用于添加一个或多个o连接的糖基化位点的氨基酸序列改变。在一些实施方案中,通过向掩蔽型细胞因子或其组分的氨基酸序列中添加一个或多个氨基酸和通过取代掩蔽型细胞因子或其组分的氨基酸序列中的一个或多个氨基酸来实现用于添加一个或多个n连接的糖基化位点和/或用于添加一个或多个o连接的糖基化位点的氨基酸序列改变。
7.异源二聚化修饰
本文所述的半衰期延长结构域可包括促进两个不同半衰期延长结构域的异源二聚化的一个或多个修饰。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,期望促进第一和第二半衰期延长结构域的异源二聚化,使得有效地产生正确异源二聚形式的掩蔽型细胞因子。如此,可采用本领域中可用的任何策略,包括如klein等人(2012),mabs,4(6):653-663中所述的任何策略,对第一半衰期延长结构域进行一个或多个氨基酸修饰,和对第二半衰期延长结构域进行一个或多个氨基酸修饰。下面详细描述示例性策略和修饰。
a.旋钮入孔方法
促进两个不同半衰期延长结构域的异源二聚化的一种策略是被称为“旋钮入孔”的方法。
在一些实施方案中,掩蔽型细胞因子包含第一半衰期延长结构域和第二半衰期延长结构域,其每一者包含ch3结构域。在一些实施方案中,包含ch3结构域的半衰期延长结构域是重链多肽或其片段(例如,fc结构域或其片段)。可通过“旋钮入孔”技术来改变两个半衰期延长结构域的ch3结构域,该技术在例如wo1996/027011;ridgway,j.b.等人,proteineng.(1996)9(7):617-621;merchant,a.m.等人,nat.biotechnol.(1998)16(7):677-681中用若干实施例进行了详细描述。另参见klein等人(2012),mabs,4(6):653-663。采用旋钮入孔方法,改变两个ch3结构域的相互作用表面,以增加含有两个改变的ch3结构域的两个半衰期延长结构域的异源二聚化。这是通过以下方式来进行的:向半衰期延长结构域中的一个的ch3结构域中引入大体积残基,该ch3结构域充当“旋钮”。然后,为了容纳大体积残基,在另一个半衰期延长结构域中形成可容纳旋钮的“孔”。改变的ch3结构域中的任一者可以是“旋钮”,而另一者可以是“孔”。二硫桥的引入进一步稳定了异源二聚体(merchant,a.m.等人,nat.biotechnol.(1998)16(7);atwell,s.等人,j.mol.biol.(1997)270(1):26-35)以及增加产率。
据报道,通过在重链中引入s354c和t366w突变以产生“旋钮”,并通过在重链中引入y349c、t366s、l368a和y407v突变以产生“孔”(根据kabateu编号系统对残基进行编号),可以实现高于97%的异源二聚化产率。carter等人(2001),j.immunol.methods,248:7-15;klein等人(2012),mabs,4(6):653-663。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含重链多肽或其部分(例如,fc结构域或其片段),所述重链多肽或其部分包含一个或多个产生“旋钮”的氨基酸突变,且第二半衰期延长结构域包含重链多肽或其部分(例如,fc结构域或其片段),所述重链多肽或其部分包含一个或多个产生“孔”的氨基酸突变。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含重链多肽或其部分(例如,fc结构域或其片段),所述重链多肽或其部分包含一个或多个产生“孔”的氨基酸突变,且第二半衰期延长结构域包含重链多肽或其部分(例如,fc结构域或其片段),所述重链多肽或其部分包含一个或多个产生“旋钮”的氨基酸突变。在重链多肽或其部分(例如,fc结构域或其片段)中引入孔或旋钮的方法是本领域中已知的,例如见于wo1996/027011;ridgway,j.b.等人,proteineng.(1996)9(7):617-621;merchant,a.m.等人,nat.biotechnol.(1998)16(7):677-681;klein等人,(2012),mabs,4(6):653-663。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含重链多肽或其部分(例如,fc结构域或其片段),所述重链多肽或其部分包含氨基酸突变s354c和t366w(根据kabateu编号系统编号),且第二半衰期延长结构域包含重链多肽或其部分(例如,fc结构域或其片段),所述重链多肽或其部分包含氨基酸突变y349c、t366s、l368a和y407v(根据kabateu编号系统编号)。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含重链多肽或其部分(例如,fc结构域或其片段),所述重链多肽或其部分包含氨基酸突变y349c、t366s、l368a和y407v(根据kabateu编号系统编号),且第二半衰期延长结构域包含重链多肽或其部分(例如,fc结构域或其片段),所述重链多肽或其部分包含氨基酸突变s354c和t366w(根据kabateu编号系统编号)。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:155的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:155的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:265的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:265的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:155的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段。在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含有包含seqidno:156的氨基酸序列的fc结构域或其片段,且第二半衰期延长结构域包含有包含seqidno:155的氨基酸序列的fc结构域或其片段。
为形成旋钮和孔可进行的取代的另外的实例包括在us20140302037a1中描述的那些,其内容以引用的方式并入本文。例如,在一些实施方案中,可以对各自含有fc结构域的第一半衰期延长结构域(“第一结构域”)和配对的第二半衰期延长结构域(“第二结构域”)进行任何以下氨基酸取代:(a)第一结构域中的y407t和第二结构域中的t366y;(b)第一结构域中的y407a和第二结构域中的t366w;(c)第一结构域中的f405a和第二结构域中的t394w;(d)第一结构域中的f405w和第二结构域中的t394s;(e)第一结构域中的y407t和第二结构域中的t366y;(f)第一结构域中的t366y和f405a以及第二结构域中的t394w和y407t;(g)第一结构域中的t366w和f405w以及第二结构域中的t394s和y407a;(h)第一结构域中的f405w和y407a以及第二结构域中的t366w和t394s;或(i)第一结构域中的t366w和第二结构域中的t366s、l368a和y407v,均根据kabateu编号系统编号。
在一些实施方案中,可以对各自含有fc结构域的第一半衰期延长结构域(“第一结构域”)和配对的第二半衰期延长结构域(“第二结构域”)进行任何以下氨基酸取代:(a)第二结构域中的y407t和第一结构域中的t366y;(b)第二结构域中的y407a和第一结构域中的t366w;(c)第二结构域中的f405a和第一结构域中的t394w;(d)第二结构域中的f405w和第一结构域中的t394s;(e)第二结构域中的y407t和第一结构域中的t366y;(f)第二结构域中的t366y和f405a以及第一结构域中的t394w和y407t;(g)第二结构域中的t366w和f405w以及第一结构域中的t394s和y407a;(h)第二结构域中的f405w和y407a以及第一结构域中的t366w和t394s;或(i)第二结构域中的t366w和第一结构域中的t366s、l368a和y407v,均根据kabateu编号系统编号。
在包含各自包含fc结构域的第一半衰期延长结构域和第二半衰期延长结构域的实施方案中,本文所述的任何异源二聚化改变可用于fc结构域中以促进本文所述的任何掩蔽型细胞因子的异源二聚化。例如,本文所述的任何异源二聚化改变,包括其组合,可用于改变选自由seqidno:154-156、158、168、169、265、616、619、622、625、721、772-774、793和796组成的组的氨基酸序列。
b.离子/静电相互作用
促进两个不同半衰期延长结构域的异源二聚化的另一种策略是通过改变带电残基来稳定有利于异源二聚化的离子相互作用。
在一些实施方案中,掩蔽型细胞因子包含第一半衰期延长结构域和第二半衰期延长结构域,其每一者包含ch3结构域。在一些实施方案中,包含ch3结构域的半衰期延长结构域是重链多肽或其片段(例如,fc结构域或其片段)。已经观察到,改变两个不同fc结构域之间的电荷极性可导致离子相互作用,使得有利于异源二聚化而抑制同源二聚化。参见例如wo2006/106905a1;gunasekaran等人(2010)285(25):19637-19646。例如,观察到fc结构域的带负电荷的e356对与另一fc结构域的带正电荷的k439配对,第一fc结构域的带负电荷的e357、e357和d399分别与第二fc结构域的带正电荷的k439、k370和k409配对。参见wo2006/106905a1;gunasekaran等人(2010)285(25):19637-19646。如此,通过在第一fc结构域中引入e356k、e357k和d399k的突变中的至少两者,并将突变k370e、k409d和k439e引入到第二fc结构域中,可以实现有效的异源二聚化,同时抑制同源二聚体形成。同上。已通过在第一fc链中引入k392d和k409d突变以及通过在第二fc链中引入d399k和e356k突变实现了有效的异源二聚化。gunasekaran等人(2010)285(25):19637-19646。
可以对带电荷的氨基酸对进行的取代的另外的实例包括在us20140302037a1中描述的那些,其内容以引用的方式并入本文。例如,在一些实施方案中,可对各自含有fc结构域的第一半衰期延长结构域(“第一结构域”)和配对的第二半衰期延长结构域(“第二结构域”)进行任何以下氨基酸取代:(a)第一结构域中的k409e和第二结构域中的d399k;(b)第一结构域中的k409e和第二结构域中的d399r;(c)第一结构域中的k409d和第二结构域中的d399k;(d)第一结构域中的k409d和第二结构域中的d399r;(e)第一结构域中的k392e和第二结构域中的d399r;(f)第一结构域中的k392e和第二结构域中的d399k;(g)第一结构域中的k392d和第二结构域中的d399r;(h)第一结构域中的k392d和第二结构域中的d399k;(i)第一结构域中的k409d和k360d以及第二结构域中的d399k和e356k;(j)第一结构域中的k409d和k370d以及第二结构域中的d399k和e357k;(k)第一结构域中的k409d和k392d以及第二结构域中的d399k、e356k和e357k;(1)第一结构域中的k409d和k392d以及第二结构域中的d399k;(m)第一结构域中的k409d和k392d以及第二结构域中的d399k和e356k;(n)第一结构域中的k409d和k392d以及第二结构域中的d399k和e357k;(o)第一结构域中的k409d和k370d以及第二结构域中的d399k和d357k;(p)第一结构域中的d399k以及第二结构域中的k409d和k360d;和/或(q)第一结构域中的k409d和k439d以及第二结构域中的d399k和e356k,均根据kabateu编号系统编号。
在一些实施方案中,可对各自含有fc结构域的第一半衰期延长结构域(“第一结构域”)和配对的第二半衰期延长结构域(“第二结构域”)进行任何以下氨基酸取代:(a)第二结构域中的k409e和第一结构域中的d399k;(b)第二结构域中的k409e和第一结构域中的d399r;(c)第二结构域中的k409d和第一结构域中的d399k;(d)第二结构域中的k409d和第一结构域中的d399r;(e)第二结构域中的k392e和第一结构域中的d399r;(f)第二结构域中的k392e和第一结构域中的d399k;(g)第二结构域中的k392d和第一结构域中的d399r;(h)第二结构域中的k392d和第一结构域中的d399k;(i)第二结构域中的k409d和k360d以及第一结构域中的d399k和e356k;(j)第二结构域中的k409d和k370d以及第一结构域中的d399k和e357k;(k)第二结构域中的k409d和k392d以及第一结构域中的d399k、e356k和e357k;(1)第二结构域中的k409d和k392d以及第一结构域中的d399k;(m)第二结构域中的k409d和k392d以及第一结构域中的d399k和e356k;(n)第二结构域中的k409d和k392d以及第一结构域中的d399k和e357k;(o)第二结构域中的k409d和k370d以及第一结构域中的d399k和d357k;(p)第二结构域中的d399k以及第一结构域中的k409d和k360d;和/或(q)第二结构域中的k409d和k439d以及第一结构域中的d399k和e356k,均根据kabateu编号系统编号。
在一些实施方案中,可对各自含有fc结构域的第一半衰期延长结构域(“第一结构域”)和配对的第二半衰期延长结构域(“第二结构域”)进行任何以下氨基酸取代:(a)第一结构域中的k409d或k409e和第二结构域中的d399k或d399r;(b)第一结构域中的k392d或k392e和第二结构域中的d399k或d399r;(c)第一结构域中的k439d或k439e和第二结构域中的e356k或e356r;和/或(d)第一结构域中的k370d或k370e和第二结构域中的e357k或e357r,均根据kabateu编号系统编号。
在一些实施方案中,可对各自含有fc结构域的第一半衰期延长结构域(“第一结构域”)和配对的第二半衰期延长结构域(“第二结构域”)进行任何以下氨基酸取代:(a)第二结构域中的k409d或k409e和第一结构域中的d399k或d399r;(b)第二结构域中的k392d或k392e和第一结构域中的d399k或d399r;(c)第二结构域中的k439d或k439e和第一结构域中的e356k或e356r;和/或(d)第二结构域中的k370d或k370e和第一结构域中的e357k或e357r,均根据kabateu编号系统编号。
在包含各自包含fc结构域的第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,可在第一半衰期延长结构域和第二半衰期延长结构域两者中进一步包括以下取代中的一者或多者以稳定异源二聚体:r355d、r355e、k360d和k360r。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含重链多肽或其部分(例如,fc结构域或其片段),所述重链多肽或其部分包含一个或多个在抑制同源二聚化的同时促进稳定与第二半衰期延长结构域的离子相互作用的突变,且第二半衰期延长结构域包含一个或多个在抑制同源二聚化的同时促进稳定与第一半衰期延长结构域的离子相互作用的突变。
在包含第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,第一半衰期延长结构域包含重链多肽或其部分(例如,fc结构域或其片段),所述重链多肽或其部分包含氨基酸突变k392d和k409d(根据kabateu编号系统编号),且第二半衰期延长结构域包含重链多肽或其部分(例如,fc结构域或其片段),所述重链多肽或其部分包含氨基酸突变d399k和e356k(根据kabateu编号系统编号)。
在包含各自包含fc结构域的第一半衰期延长结构域和第二半衰期延长结构域的实施方案中,本文所述的任何异源二聚化改变可用于fc结构域中以促进本文所述的任何掩蔽型细胞因子的异源二聚化。例如,本文所述的任何异源二聚化改变,包括其组合,可用于改变选自由seqidno:154-156、158、168、169、265、616、619、622、625、721、772-774、793和796组成的组的氨基酸序列。
c.基于结构和测序的方法
促进两个不同半衰期延长结构域的异源二聚化的另一种策略是通过采用基于结构和序列的方法来确认可促进异源二聚化和/或抑制同源二聚化的改变。
确认促进异源二聚化的改变的方式当中有通过进行结构计算以确定跨越ch3-ch3二聚体界面相互作用的残基的配对变体组合的能量,如moore等人(2011)3(6):546-557所采取的方法,其内容以引用的方式并入本文。moore等人确认了经预测异源二聚体形式相对于同源二聚体形式能量较低的对作为进一步分析的起点。观察到通过在第一fc结构域中引入s364h和f405a突变以及通过在第二fc结构域中引入y349t和t394f突变可以实现89%的异源二聚化产率。同上。
在包含各自包含fc结构域的第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,根据kabateu编号系统编号,第一半衰期延长结构域包含s364h和f405a的氨基酸突变,且第二半衰期延长结构域包含y349t和t394f的氨基酸突变。在包含各自包含fc结构域的第一半衰期延长结构域和第二半衰期延长结构域的一些实施方案中,根据kabateu编号系统编号,第二半衰期延长结构域包含s364h和f405a的氨基酸突变,且第一半衰期延长结构域包含y349t和t394f的氨基酸突变。
在包含各自包含fc结构域的第一半衰期延长结构域和第二半衰期延长结构域的实施方案中,本文所述的任何异源二聚化改变可用于fc结构域中以促进本文所述的任何掩蔽型细胞因子的异源二聚化。例如,本文所述的任何异源二聚化改变,包括其组合,可用于改变选自由seqidno:154-156、158、168、169、265、616、619、622、625、721、772-774、793和796组成的组的氨基酸序列。
e.结合测定
如细胞因子或其功能片段与细胞因子或其功能片段对其具有特异性的结合伴侣(例如,靶蛋白,如细胞因子受体)之间的免疫结合相互作用的强度或亲和力可用相互作用的解离常数(kd)表示,其中较小的kd表示较大的亲和力。例如,il-2细胞因子与il-2r细胞因子受体(例如,il-2r或其组分,如il-2rα、il-2rβ、il-2rγ或其组合)的结合可用kd表示。在一些实施方案中,免疫结合相互作用是在掩蔽型细胞因子(存在或不存在蛋白酶)与靶蛋白如细胞因子受体之间。在il-2细胞因子结合的情况下,靶蛋白可以是il-2r(包含il-2rα、il-2rβ和il-2rγ链)、il-2rα链、il-2rβ链或il-2rα/β二聚复合物。可采用本领域中熟知的方法对蛋白质的免疫结合特性进行定量。例如,一种方法包括测量细胞因子受体(例如,il-2r)/细胞因子(例如,il-2)复合物形成和解离的速率,其中那些速率取决于复合物伴侣的浓度、相互作用的亲和力和在两个方向上同等影响速率的几何参数。“缔合速率常数”(kon)和“解离速率常数”(koff)可通过计算浓度以及缔合和解离的实际速率来确定。koff/kon的比率使得能够取消所有与亲和力无关的参数,并且等于解离常数kd。参见davies等人,annualrevbiochem.59:439-473,(1990)。
在一些方面,与包含掩蔽部分但不包含可切割肽的亲本细胞因子相比,本文所述的掩蔽型细胞因子在用蛋白酶切割时以大约相同或更高的亲和力与靶蛋白结合。靶蛋白可以是任何细胞因子受体。在一些实施方案中,靶蛋白是il-2r(包含il-2rα、il-2rβ和il-2rγ链)。在一些实施方案中,靶蛋白是il-2rα。在一些实施方案中,靶蛋白是il-2rβ。在一些实施方案中,靶蛋白是il-2rα/β二聚复合物。在一些实施方案中,靶蛋白是il-15r(包含il-15rα、il-2rβ和il-2rγ链),或者是其组分,如il-15rα、il-2rβ或il-2rγ或其组合。
在一些实施方案中,本文提供的在接头中不包含可切割肽的掩蔽型细胞因子与靶蛋白的解离常数(kd)≤1μm、≤150nm、≤100nm、≤50nm、≤10nm、≤1nm、≤0.1nm、≤0.01nm或≤0.001nm(例如10-8m或更小,例如10-8m至10-13m,例如10-9m至10-13m)。在一些实施方案中,本文提供的在接头中包含可切割肽的掩蔽型细胞因子在用蛋白酶切割之前与靶蛋白的解离常数(kd)≤1μm、≤150nm、≤100nm、≤50nm、≤10nm、≤1nm、≤0.1nm、≤0.01nm或≤0.001nm(例如10-8m或更小,例如10-8m至10-13m,例如10-9m至10-13m)。在一些实施方案中,本文提供的在接头中包含可切割肽的掩蔽型细胞因子在用蛋白酶切割时与靶蛋白的解离常数(kd)≤1μm、≤150nm、≤100nm、≤50nm、≤10nm、≤1nm、≤0.1nm、≤0.01nm或≤0.001nm(例如10-8m或更小,例如10-8m至10-13m,例如10-9m至10-13m)。在一些实施方案中,本文提供的掩蔽型细胞因子的细胞因子或其功能片段与掩蔽型细胞因子的掩蔽部分的解离常数(kd)≥500μm、≥250μm、≥200μm、≥150μm、≥100μm、≥50μm、≥10μm、≥1μm、≥500nm、≥250nm、≥150nm、≥100nm、≥50nm、≥10nm、≥1nm、≥0.1nm、≥0.01nm或≥0.001nm。在一些实施方案中,本文提供的掩蔽型细胞因子的细胞因子或其功能片段的解离常数(kd)在约200μm与约50nm之间,如约或至少约175μm、约或至少约150μm、约或至少约125μm、约或至少约100μm、约或至少约75μm、约或至少约50μm、约或至少约25μm、约或至少约5μm、约或至少约1μm、约或至少约750nm、约或至少约500nm、约或至少约250nm、约或至少约150nm、约或至少约100nm、约或至少约75nm或约或至少约50nm。评估结合亲和力的测定法是本领域中熟知的。
在一些方面,提供了表现出所需封闭比的掩蔽型细胞因子。如本文所用的术语“封闭比”是指(a)在第一组条件下参数的最大检出水平与(b)在第二组条件下参数的最小检出值的比率。例如,在掩蔽型il-2多肽的情况下,封闭比是指(a)在至少一种能够切割掩蔽型il-2多肽的可切割肽的蛋白酶的存在下与掩蔽型il-2多肽结合的靶蛋白(例如,il-2r蛋白)的最大检出水平与(b)在不存在所述蛋白酶的情况下与掩蔽型il-2多肽结合的靶蛋白(例如,il-2r蛋白)的最小检出水平的比率。因此,可以通过用掩蔽型细胞因子切割前的ec50除以掩蔽型细胞因子切割后的ec50来计算掩蔽型细胞因子的封闭比。掩蔽型细胞因子的封闭比也可计算为掩蔽型细胞因子在用蛋白酶切割前的解离常数与掩蔽型细胞因子在用蛋白酶切割后的解离常数的比率。在一些实施方案中,对于掩蔽型细胞因子更大的封闭比表明在能够切割掩蔽型细胞因子的可切割肽的蛋白酶的存在下比不存在蛋白酶的情况下发生掩蔽型细胞因子结合靶蛋白的程度更大(例如,主要发生)。
在一些实施方案中,本文提供具有最佳封闭比的掩蔽型细胞因子。在一些实施方案中,掩蔽型细胞因子的最佳封闭比表明掩蔽型细胞因子具有可用于本文考虑的方法或组合物的期望特性。在一些实施方案中,本文提供的掩蔽型细胞因子表现出约2至约10,000(例如,约80至约100)的最佳封闭比。在本文提供的任何掩蔽型细胞因子的进一步实施方案中,封闭比为约2至约7,500、约2至约5,000、约2至约2,500、约2至约2,000、约2至约1,000、约2至约900、约2至约800、约2至约700、约2至约600、约2至约500、约2至约400、约2至约300、约2至约200、约2至约100、约2至约50、约2至约25、约2至约15、约2至约10、约5至约10、约5至约15、约5至约20、约10至约100、约20至约100、约30至约100、约40至约100、约50至约100、约60至约100、约70至约100、约80至约100或约100至约1,000。在一些实施方案中,本文提供的掩蔽型细胞因子表现出约2至约1,000的最佳封闭比。可采用本领域中熟知的技术如通过elisa测定在用蛋白酶切割前和/或切割后掩蔽型il-2多肽与靶蛋白的结合。
在一些实施方案中,本文所述的掩蔽部分与如本文所述的细胞因子或其功能片段结合的亲和力低于细胞因子或其功能片段与靶蛋白(例如,细胞因子受体)之间的亲和力。在某些实施方案中,本文提供的掩蔽部分以≥500μm、≥250μm、≥200μm、≥150μm、≥100μm、≥50μm、≥10μm、≥1μm、≥500nm、≥250nm、≥150nm、≥100nm、≥50nm、≥10nm、≥1nm、≥0.1nm、≥0.01nm或≥0.001nm的解离常数(kd)与细胞因子或其功能片段结合。
ii.掩蔽型细胞因子产生
采用本领域中可用的技术制备本文所述的掩蔽型细胞因子,其示例性方法已有描述。
a.抗体产生
掩蔽型细胞因子的一些实施方案包含抗体或其片段。以下部分提供可用于本文提供的掩蔽型细胞因子的一些实施方案的抗体及其抗体片段、变体和衍生物的产生的进一步细节。在一些实施方案中,掩蔽型细胞因子呈由通过二硫键缔合的两个拷贝的掩蔽型细胞因子产生的二聚体的形式。
1.抗体片段
在一些实施方案中,本发明包括抗体片段。所述抗体片段可以是任何抗体片段,如fc结构域、重链的一部分、轻链的一部分、fab、fv或scfv等等。可通过传统方法如酶消化或通过重组技术产生抗体片段。在某些情况下,将抗体片段而不是整个抗体与本文所述的掩蔽型细胞因子连接是有利的。关于某些抗体片段的综述,参见hudson等人(2003)nat.med.9:129-134。
已经开发了多种用于产生抗体片段的技术。传统上,这些片段是经由完整抗体的蛋白水解消化获得的(参见例如morimoto等人,journalofbiochemicalandbiophysicalmethods24:107-117(1992);和brennan等人,science,229:81(1985))。然而,这些片段现在可直接通过重组宿主细胞产生。fab、fv和scfv抗体片段均可在大肠杆菌及其它细胞类型如hek293和cho细胞中表达和由其分泌,因此允许很容易地产生大量的这些片段。或者,可以直接从培养基中回收fab′-sh片段并化学偶联以形成f(ab′)2片段(carter等人,bio/technology10:163-167(1992))。根据另一种方法,可直接从重组宿主细胞培养物中分离f(ab′)2片段。5,869,046号美国专利中描述了包含fcrn/补救受体结合表位残基的具有增加的体内半衰期的fab和f(ab′)2片段。产生用于掩蔽型细胞因子的抗体片段的其它技术对本领域技术人员而言将是显而易见的。在某些实施方案中,掩蔽型细胞因子包含单链fv片段(scfv)。参见wo93/16185;5,571,894和5,587,458号美国专利。可以构建scfv融合蛋白,以在scfv的氨基或羧基末端产生效应蛋白的融合。参见antibodyengineering,borrebaeck编,同上。而且,在一些实施方案中,包含经由多肽接头连接的两个scfv的双scfv可与掩蔽型细胞因子一起使用。
在一些实施方案中,本发明包括线性抗体(例如,如5,641,870号美国专利中所述)或包含经由适当接头连接的抗体的重链和轻链序列的单链免疫球蛋白。这类线性抗体或免疫球蛋白可以是单特异性的或双特异性的。可将这种单链免疫球蛋白二聚化,从而保持与最初是四聚体的抗体类似的结构和活性。而且,在一些实施方案中,抗体或其片段可以是具有单一重链可变区并且没有轻链序列的抗体。这种抗体称为单结构域抗体(sdab)或纳米抗体。这些抗体也包括在根据本发明的抗体的功能片段的含义中。抗体片段可根据本文提供的指导与本文所述的掩蔽型细胞因子连接。
2.人源化抗体
在一些实施方案中,本发明包括人源化抗体或其抗体片段。在一些实施方案中,人源化抗体可以是任何抗体,包括任何抗体片段。将非人抗体人源化的各种方法是本领域中已知的。例如,人源化抗体可具有从非人来源引入其中的一个或多个氨基酸残基。这些非人氨基酸残基通常被称为“输入”残基,其通常取自“输入”可变结构域。可基本上按照winter(jones等人(1986)nature321:522-525;riechmann等人(1988)nature332:323-327;verhoeyen等人(1988)science239:1534-1536)的方法,通过用高变区序列取代人抗体的相应序列来进行人源化。因此,这种“人源化”抗体是嵌合抗体(4,816,567号美国专利),其中基本上少于完整的人可变结构域被来自非人物种的相应序列取代。实际上,人源化抗体通常是人抗体,其中一些高变区残基和可能一些fr残基被来自啮齿动物抗体中的类似位点的残基取代。人源化抗体可根据本文提供的指导与本文所述的掩蔽型细胞因子连接。
3.人抗体
可通过将选自人来源的噬菌体展示文库的fv克隆可变结构域序列与已知的人恒定结构域序列组合来构建本发明的一些实施方案的人抗体。或者,可通过杂交瘤方法制备本发明的一些实施方案的人单克隆抗体,例如通过使用例如小鼠、大鼠、牛(例如,母牛)或兔细胞产生人单克隆抗体。在一些实施方案中,人抗体和人单克隆抗体可以是与任何抗原结合的抗体。在一些实施方案中,可通过如下方式制备本发明的人单克隆抗体,用靶抗原使包含人免疫球蛋白基因座的非人动物免疫,并从免疫动物或从来源于免疫动物的细胞中分离抗体。合适的非人动物的实例包括转基因或转染色体动物,如humab
用于产生人单克隆抗体的人骨髓瘤和鼠-人异源骨髓瘤细胞系已例如由kozborj.immunol.,133:3001(1984);brodeur等人,monoclonalantibodyproductiontechniquesandapplications,第51-63页(marceldekker,inc.,newyork,1987);和boerner等人,j.immunol.,147:86(1991)描述。人抗体可根据本文提供的指导与本文所述的掩蔽型细胞因子连接。
4.双特异性抗体
双特异性抗体是对至少两种不同抗原具有结合特异性的单克隆抗体。在某些实施方案中,双特异性抗体是人或人源化抗体。在一些实施方案中,结合特异性中的一者是针对第一抗原,且另一结合特异性是针对第二抗原,其可以是相同靶蛋白上的两种不同表位,或两种不同靶蛋白上的两种不同表位。双特异性抗体也可用于将细胞毒性剂定位至表达第一抗原和/或第二抗原的细胞。双特异性抗体也可用于募集细胞,如t细胞或天然杀伤细胞,以杀伤某些细胞,例如癌细胞。双特异性抗体可以被制备为全长抗体或抗体片段(例如f(ab′)2双特异性抗体)。双特异性抗体可根据本文提供的指导与本文所述的掩蔽型细胞因子连接。
制备双特异性抗体的方法是本领域中已知的。参见milstein和cuello,nature,305:537(1983);1993年5月13日公布的wo93/08829;traunecker等人,emboj.,10:3655(1991);kontermann和brinkmann,drugdiscoverytoday,20(7):838-847。关于产生双特异性抗体的进一步细节,参见例如suresh等人,methodsinenzymology,121:210(1986)。双特异性抗体包括交联或“异源缀合”抗体。例如,异源缀合物中的抗体之一可与抗生物素蛋白偶联,另一者与生物素偶联。可采用任何方便的交联方法制备异源缀合物抗体。合适的交联剂是本领域中熟知的,并且连同许多交联技术一起公开于4,676,980号美国专利中。
5.单结构域抗体
在一些实施方案中,单结构域抗体根据本文提供的指导与掩蔽型细胞因子连接。所述单结构域抗体可以是任何抗体。单结构域抗体是包含抗体的全部或一部分重链可变结构域或全部或一部分轻链可变结构域的单一多肽链。在某些实施方案中,单结构域抗体是人单结构域抗体(domantis,inc.,waltham,mass.;参见例如6,248,516b1号美国专利)。在一些实施方案中,单结构域抗体由抗体的全部或一部分重链可变结构域组成。在一些实施方案中,单结构域抗体是通过用靶抗原使骆驼免疫获得的骆驼来源的抗体。在一些实施方案中,单结构域抗体是通过用靶抗原使鲨鱼免疫获得的鲨鱼来源的抗体。在一些实施方案中,单结构域抗体是纳米抗体(参见例如,wo2004041865a2和us20070269422a1)。
6.抗体变体
在一些实施方案中,考虑了本文所述的抗体或其片段的氨基酸序列修饰。例如,可能期望提高抗体的fcrn结合亲和力和/或ph依赖性fcrn结合亲和力。也可能期望通过引入某些氨基酸修饰来促进抗体重链的异源二聚化。klein等人(2012),mabs,4(6):653-663描述了促进抗体链的异源二聚化的方法,包括可进行某些修饰以促进异源二聚化。
可通过向编码抗体的核苷酸序列中引入适当的改变或通过肽合成来制备抗体的氨基酸序列变体。这类修饰包括例如从抗体的氨基酸序列内缺失残基和/或向抗体的氨基酸序列内插入残基和/或取代抗体的氨基酸序列内的残基。可以进行缺失、插入和取代的任意组合以获得最终构建体,条件是最终构建体具有所需的特征。可在制备序列之时在本发明的抗体氨基酸序列中引入氨基酸改变。
如cunningham和wells(1989)science,244:1081-1085所述,确认作为诱变优选位置的抗体的某些残基或区域的有用方法称为“丙氨酸扫描诱变”。在此,确认了残基或靶残基组(例如,带电荷的残基如arg、asp、his、lys和glu),并被中性或带负电荷的氨基酸(例如,丙氨酸或聚丙氨酸)置换,以影响氨基酸与抗原的相互作用。然后通过在取代位点处或针对取代位点引入进一步或其它的变体来精修对取代表现出功能敏感性的那些氨基酸位置。因此,尽管引入氨基酸序列变异的位点是预先确定的,但突变本身的性质不需要预先确定。例如,为分析在给定位点的突变的表现,在靶密码子或区域进行ala扫描或随机诱变,并针对所需活性来筛选表达的免疫球蛋白。
氨基酸序列插入包括长度范围从一个残基到含有一百个或更多个残基的多肽的氨基和/或羧基末端融合,以及单个或多个氨基酸残基的序列内插入。末端插入的实例包括具有n末端甲硫氨酰基残基的抗体。抗体分子的其它插入变体包括抗体的n或c末端与增加抗体的血清半衰期的酶或多肽的融合体。
在一些实施方案中,修饰掩蔽型细胞因子以消除、减少或以其它方式阻碍铰链区附近的蛋白酶切割。根据如kabat中的eu索引,igg的“铰链区”通常被定义为包括e216并终止于人igg1的p230,但在功能上,链的柔性部分可以被认为包括被称为上铰链区和下铰链区的另外的残基,如从e216至g237(roux等人,1998jimmunol161:4083),且下铰链被称为fcγr结合通常归因的fc区的残基233至239。可例如根据us20150139984a1(以引用的方式并入本文)中所述的方法以及通过并入其中描述的任何修饰来进行对本文所述的任何掩蔽型细胞因子的修饰。
在一些实施方案中,改善药代动力学的fcrn突变包括但不限于m428l、t250q/m428l、m252y/s254t/t256e、p257i/n434h、d376v/n434h、p257i/q3111、n434a、n434w、m428l/n434s、v259i/v308f、m252y/s254t/t256e、v259i/v308f/m428l、t307q/n434a、t307q/n434s、t307q/e380a/n434a、v308p/n434a、n434h、v308p。在一些实施方案中,这类突变在低ph下增强抗体与fcrn的结合,但在中性ph下不改变抗体亲和力。
在某些实施方案中,改变抗体或其片段以提高或降低抗体糖基化的程度。多肽的糖基化通常是n连接的或o连接的。n连接是指碳水化合物部分与天冬酰胺残基的侧链的连接。三肽序列天冬酰胺-x-丝氨酸和天冬酰胺-x-苏氨酸是碳水化合物部分与天冬酰胺侧链的酶促连接的识别序列,其中x是除脯氨酸以外的任何氨基酸。因此,在多肽中存在这些三肽序列中的任一者产生了潜在的糖基化位点。o连接的糖基化是指糖n-乙酰半乳糖胺、半乳糖或木糖中的一者与羟基氨基酸(最常见的是丝氨酸或苏氨酸,尽管也可以使用5-羟基脯氨酸或5-羟基赖氨酸)的连接。
通过改变氨基酸序列,以便产生或移除上述三肽序列中的一者或多者(对于n连接的糖基化位点),由此方便地实现对掩蔽型细胞因子进行糖基化位点的添加或缺失。也可以通过对原始抗体的序列进行一个或多个丝氨酸或苏氨酸残基的添加、缺失或取代来进行改变(对于o连接的糖基化位点)。
在抗体或其片段包含fc区的情况下,可改变与其连接的碳水化合物。例如,us2003/0157108号美国专利申请(presta,l.)中描述了具有缺乏与抗体的fc区连接的岩藻糖的成熟碳水化合物结构的抗体。另参见us2004/0093621(kyowahakkokogyoco.,ltd)。在jean-mairet等人的wo2003/011878和umana等人的6,602,684号美国专利中提到了在与抗体的fc区连接的碳水化合物中具有二等分n-乙酰葡糖胺(glcnac)的抗体。patel等人的wo1997/30087中报道了在与抗体的fc区连接的寡糖中具有至少一个半乳糖残基的抗体。关于具有与fc区连接的改变的碳水化合物的抗体,另参见wo1998/58964(raju,s.)和wo1999/22764(raju,s.)。关于具有修饰的糖基化的抗原结合分子,另参见us2005/0123546(umana等人)。
在某些实施方案中,糖基化变体包含fc区,其中与fc区连接的碳水化合物结构缺乏岩藻糖或具有减少的岩藻糖。这类变体具有改善的adcc功能。任选地,fc区进一步在其中包含一个或多个进一步改善adcc的氨基酸取代,例如在fc区的位置298、333和/或334处(残基的eu编号)的取代。涉及“脱岩藻糖基化”或“岩藻糖缺乏的”抗体的公布的实例包括:us2003/0157108;wo2000/61739;wo2001/29246;us2003/0115614;us2002/0164328;us2004/0093621;us2004/0132140;us2004/0110704;us2004/0110282;us2004/0109865;wo2003/085119;wo2003/084570;wo2005/035586;wo2005/035778;wo2005/053742;okazaki等人,j.mol.biol.336:1239-1249(2004);yamane-ohnuki等人,biotech.bioeng.87:614(2004)。产生脱岩藻糖基化抗体的细胞系的实例包括缺乏蛋白质岩藻糖基化的lec13cho细胞(ripka等人,arch.biochem.biophys.249:533-545(1986);us2003/0157108a1号美国专利申请,presta,l;和wo2004/056312a1,adams等人,特别是实施例11)和敲除细胞系如α-1,6-岩藻糖基转移酶基因fut8敲除cho细胞(yamane-ohnuki等人,biotech.bioeng.87:614(2004))以及过表达β1,4-n-乙酰葡糖胺基转移酶iii(gnt-iii)和高尔基体μ-甘露糖苷酶ii(manii)的细胞。
在本文的任何实施方案中,掩蔽型细胞因子可以被工程化以提高抗体依赖性细胞介导的细胞毒性(adcc)活性。在一些实施方案中,可在具有α1,6-岩藻糖基转移酶(fut8)敲除的细胞系中产生掩蔽型细胞因子。在一些实施方案中,宿主细胞已被修饰成具有降低的内在α1,6-岩藻糖基化活性。修饰哺乳动物宿主细胞中的岩藻糖基化途径的方法的实例可见于例如yamane-ohnuki和satoh,mabs,1(3):230-236(2009),其内容以引用的方式并入本文。用于部分或完全灭活fut8基因的表达的方法和组合物的实例可见于例如20160194665a1号美国公开;wo2006133148a2,其内容以引用的方式并入本文。在一些实施方案中,在cho细胞的lec13变体(参见例如shields等人,j.biol.chem.,277(30):26733-40(2002))或具有降低的fut8活性的yb2/0细胞系(参见例如shinkawa等人,j.biol.chem.,278(5):3466-73(2003))中产生掩蔽型细胞因子。在一些实施方案中,可以引入针对与α1,6-岩藻糖基化相关的基因的小干扰rna(sirna)(参见例如mori等人,biotechnol.bioeng.88(7):901-908(2004);imai-nishiya等人,bmcbiotechnol.7:84(2007);omasa等人,j.biosci.bioeng.、106(2):168-173(2008))。在一些进一步的实施方案中,可以在过表达β1,4-n-乙酰葡糖胺基转移酶iii(gnt-iii)的细胞系中产生掩蔽型细胞因子。在进一步的实施方案中,所述细胞系另外过表达高尔基体μ-甘露糖苷酶ii(manii)。在本文的一些实施方案中,掩蔽型细胞因子可在fc区中包含至少一个提高adcc活性的氨基酸取代。
在一些实施方案中,改变掩蔽型细胞因子以改善其血清半衰期。为增加细胞因子的血清半衰期,例如可以将fcrn/补救受体结合表位结合到连接抗体(特别是抗体片段)中,如5,739,277号美国专利中所述。如本文所用,术语“补救受体结合表位”是指igg分子(例如,igg1、igg2、igg3或igg4)的fc区的负责增加igg分子的体内血清半衰期的表位(us2003/0190311,6,821,505号美国专利;6,165,745号美国专利;5,624,821号美国专利;5,648,260号美国专利;6,165,745号美国专利;5,834,597号美国专利)。
另一种类型的变体是氨基酸取代变体。这些变体在抗体分子中有至少一个氨基酸残基被不同的残基置换。取代诱变所关注的位点包括高变区,但也考虑fr改变。保守取代在表3中“优选取代”的标题下示出。如果这类取代导致生物活性的所需改变,则可引入更多的实质性改变,在表3中称作“示例性取代”,或如下面关于氨基酸类别进一步描述,并筛选产物。
表3
通过选择对维持(a)取代区域中的多肽主链的结构,例如片或螺旋构象,(b)靶位点处的分子电荷或疏水性,或(c)侧链的体积的影响显著不同的取代来实现抗体生物学特性的实质性修饰。氨基酸可以根据其侧链特性的相似性进行分组(a.l.lehninger,biochemistry,第二版,第73-75页,worthpublishers,newyork(1975)):
(1)非极性的:ala(a)、val(v)、leu(l)、ile(i)、pro(p)、phe(f)、trp(w)、met(m)
(2)不带电荷的极性的:gly(g)、ser(s)、thr(t)、cys(c)、tyr(y)、asn(n)、gln(q)
(3)酸性的:asp(d)、glu(e)
(4)碱性的:lys(k)、arg(r)、his(h)
或者,天然存在的残基可基于共同的侧链特性分成组:
(1)疏水性的:正亮氨酸、met、ala、val、leu、ile;
(2)中性亲水性的:cys、ser、thr、asn、gln;
(3)酸性的:asp、glu;
(4)碱性的:his、lys、arg;
(5)影响链取向的残基:gly、pro;
(6)芳族的:trp、tyr、phe。
非保守取代将需要用这些类别之一的成员交换另一个类别。也可以将这类取代的残基引入到保守取代位点或引入到剩下的(非保守)位点中。
另一种类型的取代变体涉及用天然存在的氨基酸残基取代非天然存在的氨基酸残基。可例如通过trna再编码或通过例如在以引用的方式并入本文的wo2016154675a1中所述的任何方法结合非天然存在的氨基酸残基。
一种类型的取代变体涉及取代亲本抗体(例如,人源化抗体或人抗体)的一个或多个高变区残基。一般地,选择用于进一步开发的所得变体相对于产生它们的亲本抗体将具有改进的(例如,改善的)生物学特性。产生这类取代变体的方便方法涉及使用噬菌体展示、酵母展示或哺乳动物展示的亲和力成熟。简言之,使若干高变区位点(例如,6-7个位点)突变以在每个位点产生所有可能的氨基酸取代。如此产生的抗体从丝状噬菌体颗粒展示为与包装在每个颗粒内的噬菌体外壳蛋白(例如,m13的基因iii产物)的至少一部分的融合体。然后针对生物活性(例如,结合亲和力)筛选噬菌体展示的变体。为了确认用于修饰的候选高变区位点,可以进行扫描诱变(例如,丙氨酸扫描)以确认对抗原结合贡献显著的高变区残基。或者或另外,分析抗原-抗体复合物的晶体结构以确认抗体与抗原之间的接触点可能是有益的。这类接触残基和相邻残基是根据本领域中已知的技术(包括本文详述的那些)进行取代的候选残基。一旦产生了这类变体,就采用本领域中已知的技术(包括本文所述的那些)对变体组进行筛选,并且可选择在一种或多种相关测定中特性优异的抗体用于进一步开发。
通过本领域中已知的多种方法制备编码掩蔽型细胞因子的氨基酸序列变体的核酸分子。这些方法包括但不限于例如从天然来源分离(在天然存在的氨基酸序列变体的情况下)或通过寡核苷酸介导的(或定点)诱变、pcr诱变和盒式诱变较早制备的抗体的变体或非变体形式来制备。
可能期望在本发明的抗体的fc区中引入一个或多个氨基酸修饰,从而产生fc区变体。fc区变体可包含人fc区序列(例如,人igg1、igg2、igg3或igg4fc区),其在一个或多个氨基酸位置(包括铰链半胱氨酸的位置)包含氨基酸修饰(例如取代)。
在一些实施方案中,本文提供的掩蔽型细胞因子包括具有效应子功能增强的igg1、igg2、igg3或igg4同种型的抗体或其片段。在一些实施方案中,本文提供的掩蔽型细胞因子包括具有效应子功能增强的igg1同种型的抗体或其片段。在一些实施方案中,本文提供的掩蔽型细胞因子(例如,掩蔽型il-2多肽或其功能片段或掩蔽型il-15多肽或其功能片段)具有效应子功能增强的igg1同种型。在一些实施方案中,掩蔽型细胞因子是无岩藻糖基化的。在一些实施方案中,掩蔽型细胞因子具有增加的甘露糖部分水平。在一些实施方案中,掩蔽型细胞因子具有增加的二等分聚糖部分水平。在一些实施方案中,igg1包含氨基酸突变。
在一些实施方案中,本文提供的掩蔽型细胞因子包括具有igg1同种型(例如,人igg1同种型)的抗体。在一些实施方案中,igg1包含一个或多个增强效应子功能的氨基酸取代。在一个实施方案中,igg1包含氨基酸取代s298a、e333a和k334a,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代s239d和i332e,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代s239d、a330l和i332e,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代p247i和a339d或a339q,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代d280h、k290s,有或没有s298d或s298v,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代f243l、r292p和y300l,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代f243l、r292p、y300l和p396l,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代f243l、r292p、y300l、v305i和p396l,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代g236a、s239d和i332e,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代k326a和e333a,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代k326w和e333s,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代k290e、s298g、t299a,有或没有k326e,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代k290n、s298g、t299a,有或没有k326e,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代k334v,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代l235s、s239d和k334v,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代k334v和q331m、s239d、f243v、e294l或s298t,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代e233l、q311m和k334v,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代l234i、q311m和k334v,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代k334v和s298t、a330m或a330f,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代k334v、q311m和a330m或a330f,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代k334v、s298t和a330m或a330f,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代k334v、s239d和a330m或s298t,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代l234y、y296w和k290y、f243v或e294l,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代y296w和l234y或k290y,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代s239d、a330s和i332e,其中氨基酸残基根据如kabat中的eu索引编号。
在一些实施方案中,igg1包含一个或多个降低或抑制效应子功能的氨基酸取代。在一个实施方案中,igg1包含氨基酸取代n297a、n297g或n297q,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代l234a或l235a,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代c220s、c226s、c229s和p238s,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代c226s、c229s、e233p、l234v和l235a,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代l234f、l235e和p331s,其中氨基酸残基根据如kabat中的eu索引编号。在一个实施方案中,igg1包含氨基酸取代s267e和l328f,其中氨基酸残基根据如kabat中的eu索引编号。
根据本说明书和本领域的教导,预期在一些实施方案中,掩蔽型细胞因子的抗体或其片段与野生型对应抗体相比例如在fc区中可包含一个或多个改变。例如,认为可以在fc区中进行某些改变,其将导致c1q结合和/或补体依赖性细胞毒性(cdc)改变(即,改善或减弱),例如wo99/51642中所述。关于fc区变体的其它实例,另参见duncan和winternature322:738-40(1988);5,648,260号美国专利;5,624,821号美国专利;和wo94/29351。wo00/42072(presta)和wo2004/056312(lowman)描述了与fcr的结合改善或减弱的抗体变体。这些专利公布的内容特别以引用的方式并入本文。另参见shields等人,j.biol.chem.9(2):6591-6604(2001)。us2005/0014934a1(hinton等人)中描述了具有增加的半衰期和改善的与新生儿fc受体(fcrn)结合的抗体,新生儿fc受体负责将母体igg转移至胎儿(guyer等人,j.immunol.117:587(1976)和kim等人,j.immunol.24:249(1994))。这些抗体包含其中具有一个或多个改善fc区与fcrn的结合的取代的fc区。在6,194,551b1号美国专利、wo99/51642中描述了具有改变的fc区氨基酸序列和增加或降低的c1q结合能力的多肽变体。这些专利公布的内容特别以引用的方式并入本文。另参见idusogie等人,j.immunol.164:4178-4184(2000)。
b.掩蔽型细胞因子-药物缀合物
本发明还提供掩蔽型细胞因子-药物缀合物(mcdc),其包含与一种或多种药剂缀合的本文提供的掩蔽型细胞因子(其可以是本文公开的任何掩蔽型细胞因子)。在一些实施方案中,一种或多种药剂是细胞毒性剂如化疗剂或药物、生长抑制剂、毒素(例如,蛋白质毒素、细菌、真菌、植物或动物来源的酶促活性毒素或其片段)或放射性同位素。在一些实施方案中,一种或多种药剂是免疫刺激剂。
在一些实施方案中,与掩蔽型细胞因子缀合的一种或多种药物包括但不限于类美登素(参见5,208,020、5,416,064号美国专利和欧洲专利ep0425235b1);奥瑞他汀,如单甲基奥瑞他汀药物部分de和df(mmae和mmaf)(参见5,635,483、5,780,588和7,498,298号美国专利);尾海兔素;卡奇霉素或其衍生物(参见5,712,374、5,714,586、5,739,116、5,767,285、5,770,701、5,770,710、5,773,001和5,877,296号美国专利;hinman等人,cancerres.53:3336-3342(1993);和lode等人,cancerres.58:2925-2928(1998));蒽环类药物,如道诺霉素或多柔比星(参见kratz等人,currentmed.chem.13:477-523(2006);jeffrey等人,bioorganic&med.chem.letters16:358-362(2006);torgov等人,bioconj.chem.16:717-721(2005);nagy等人,proc.natl.acad.sci.usa97:829-834(2000);dubowchik等人,bioorg.&med.chem.letters12:1529-1532(2002);king等人,j.med.chem.45:4336-4343(2002);和6,630,579号美国专利);甲氨蝶呤;长春地辛;紫杉烷,如多西他赛、紫杉醇、拉洛他赛、替塞他赛(tesetaxel)和奥他赛;单端孢霉烯;和cc1065。
在另一实施方案中,与掩蔽型细胞因子缀合的一种或多种药物包括但不限于微管蛋白聚合的抑制剂(例如,类美登素和奥瑞他汀)、dna损伤剂(例如,吡咯并苯并二氮杂卓(pbd)二聚体、卡奇霉素、倍癌霉素和吲哚啉并苯并二氮杂卓二聚体)和dna合成抑制剂(例如,依喜替康衍生物dxd)。
在另一实施方案中,掩蔽型细胞因子-药物缀合物包含与酶促活性毒素或其片段缀合的如本文所述的掩蔽型细胞因子,所述酶促活性毒素或其片段包括但不限于白喉a链、白喉毒素的非结合活性片段、外毒素a链(来自铜绿假单胞菌)、蓖麻毒素a链、相思豆毒素a链、莫迪素a链、α-八叠球菌素、油桐蛋白、石竹素蛋白、美洲商陆蛋白(papi、papii和pap-s)、苦瓜抑制剂、泻果素、巴豆素、肥阜草(sapaonariaofficinalis)抑制剂、白树毒素、米托毒素(mitogellin)、局限曲菌素、酚霉素、伊诺霉素和单端孢霉烯。
在另一实施方案中,掩蔽型细胞因子-药物缀合物包含与放射性原子缀合以形成放射性缀合物的如本文所述的掩蔽型细胞因子。多种放射性同位素可用于制备放射性缀合物。实例包括at211、i131、i125、y90、re186、re188、sm153、bi212、p32、pb212和lu的放射性同位素。当放射性缀合物用于检测时,其可包含用于闪烁照相研究的放射性原子,例如tc99m或i123,或用于核磁共振(nmr)成像(也称为磁共振成像,mri)的自旋标记,如碘-123再有、碘-131、铟-111、氟-19、碳-13、氮-15、氧-17、钆、锰或铁。
在一些实施方案中,掩蔽型细胞因子-药物缀合物包含与一种或多种免疫刺激剂缀合的如本文所述的掩蔽型细胞因子。在一些实施方案中,免疫刺激剂是干扰素基因刺激物(sting)激动剂或toll样受体(tlr)激动剂。
sting激动剂可以是sting的任何激动剂。在一些实施方案中,sting激动剂是环状二核苷酸(cdn)。cdn可以是任何cdn或其衍生物或变体。在一些实施方案中,sting激动剂是选自由cgamp、c-二-amp、c-二-gmp、caimp和c-二-imp组成的组的cdn。在一些实施方案中,sting激动剂是选自由cgamp、c-二-amp、c-二-gmp、caimp和c-二-imp组成的组的cdn的衍生物或变体。在一些实施方案中,sting激动剂是4-(2-氯-6-氟苄基)-n-(呋喃-2-基甲基)-3-氧代-3,4-二氢-2h-苯并[b][1,4]噻嗪-6-甲酰胺或其衍生物或变体。参见例如sali等人(2015)plospathog.,11(12):e1005324。
tlr激动剂可以是任何tlr的激动剂,如tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9或tlr10。在一些实施方案中,tlr激动剂是在细胞表面上表达的tlr的激动剂,如tlr1、tlr2、tlr4或tlr5。在一些实施方案中,tlr激动剂是细胞内表达的tlr的激动剂,如tlr3、tlr7、tlr8、tlr9或tlr10。
可使用多种双官能蛋白质偶联剂来制备掩蔽型细胞因子和细胞毒性剂的缀合物,所述双官能蛋白质偶联剂如n-琥珀酰亚胺基-3-(2-吡啶基二硫代)丙酸酯(spdp)、琥珀酰亚胺基-4-(n-马来酰亚胺基甲基)环己烷-1-甲酸酯(smcc)、亚氨基硫杂环戊烷(it)、亚氨酸酯的双官能衍生物(如己二亚氨酸二甲酯hcl)、活性酯(如辛二酸二琥珀酰亚胺酯)、醛(如戊二醛)、双叠氮化合物(如双(对叠氮苯甲酰基)己二胺)、双重氮衍生物(如双-(对重氮苯甲酰基)-乙二胺)、二异氰酸酯(如甲苯2,6-二异氰酸酯)和双活性氟化合物(如1,5-二氟-2,4-二硝基苯)。例如,可如vitetta等人,science238:1098(1987)所述制备蓖麻毒素免疫毒素。碳-14标记的1-异硫氰酸根合苄基-3-甲基二亚乙基三胺五乙酸(mx-dtpa)是用于使放射性核苷酸与抗体缀合的示例性螯合剂。参见wo94/11026。接头可以是促进细胞毒性药物在细胞中释放的“可切割接头”。例如,可以使用酸不稳定接头、肽酶敏感接头、光不稳定接头、二甲基接头或含二硫化物的接头(chari等人,cancerres.52:127-131(1992);5,208,020号美国专利)。
本文的mcdc明确地涵盖但不限于用交联剂试剂制备的这类缀合物,所述交联剂试剂包括但不限于可商购获得的(例如,购自piercebiotechnology,inc.,rockford,il.,u.s.a)的bmps、emcs、gmbs、hbvs、lc-smcc、mbs、mpbh、sbap、sia、siab、smcc、smpb、smph、磺基-emcs、磺基-gmbs、磺基-kmus、磺基-mbs、磺基-siab、磺基-smcc和磺基-smpb以及svsb(琥珀酰亚胺基-(4-乙烯基砜)苯甲酸酯)。
c.载体、宿主细胞和重组方法
为了重组产生本发明的掩蔽型细胞因子,分离一种或多种编码它的核酸,并将其插入到可复制的载体中用于进一步克隆(dna的扩增)或用于表达。采用常规程序很容易分离编码掩蔽型细胞因子(包括其组分)的dna并进行测序。许多载体是可用的。载体的选择部分地取决于要使用的宿主细胞。一般地,宿主细胞是原核或真核(通常是哺乳动物)来源的。将要理解的是,当适用时,抗体或其片段的任何同种型的恒定区均可用于此目的,包括igg、igm、iga、igd和ige恒定区,并且这类恒定区可得自任何人或动物物种。在一些实施方案中,使用一种载体编码掩蔽型细胞因子。在一些实施方案中,使用一种以上载体编码掩蔽型细胞因子。
1.使用原核宿主细胞产生掩蔽型细胞因子
a.载体构建
可采用标准重组技术获得编码本发明的掩蔽型细胞因子的多肽组分的多核苷酸序列。可以从产生抗体的细胞如杂交瘤细胞中分离抗体或其抗体片段的所需多核苷酸序列并进行测序。或者,多核苷酸可采用核苷酸合成仪或pcr技术合成,或者从其它来源获得。一旦获得,则将编码掩蔽型细胞因子的组分的序列插入到能够在原核宿主中复制和表达异源多核苷酸的重组载体中。本领域中可用和已知的许多载体可用于本发明的目的。适当载体的选择将主要取决于要插入载体中的核酸的大小和要用载体转化的特定宿主细胞。每种载体含有多种组分,这取决于其功能(异源多核苷酸的扩增或表达,或这两者)及其与其所驻留的特定宿主细胞的相容性。载体组分通常包括但不限于:复制起点、选择标志物基因、启动子、核糖体结合位点(rbs)、信号序列、异源核酸插入物和转录终止序列。
一般来说,含有复制子和来源于与宿主细胞相容的物种的控制序列的质粒载体与这些宿主结合使用。载体通常携带复制位点,以及能够在转化细胞中提供表型选择的标志序列。例如,通常使用来源于大肠杆菌物种的质粒pbr322转化大肠杆菌。pbr322含有编码氨苄青霉素(amp)和四环素(tet)抗性的基因,因此提供了确认转化细胞的简便方法。pbr322、其衍生物或其它微生物质粒或细菌噬菌体也可含有或被修饰成含有可被微生物有机体用于表达内原性蛋白质的启动子。carter等人,5,648,237号美国专利中详细描述了用于表达特定抗体的pbr322衍生物的实例。
此外,含有复制子和与宿主微生物相容的控制序列的噬菌体载体可用作与这些宿主有关的转化载体。例如,细菌噬菌体如λgem.tm.-11可用于制备可用于转化易感宿主细胞如大肠杆菌le392的重组载体。
本发明的表达载体可包含两个或更多个启动子-顺反子对,其编码多肽组分中的每一者。启动子是位于调节其表达的顺反子上游(5′)的非翻译调控序列。原核启动子通常分为诱导型和组成型两类。诱导型启动子是这样的启动子,其响应于培养条件的变化(例如营养物的存在与否或温度的变化)在其控制下启动增加水平的顺反子转录。
大量由各种潜在的宿主细胞识别的启动子是熟知的。通过经由限制酶消化从源dna中移除启动子并将分离的启动子序列插入到本发明的载体中,可以将选择的启动子与编码掩蔽型细胞因子的任一链的顺反子dna可操作地连接。天然启动子序列和许多异源启动子可用于指导靶基因的扩增和/或表达。在一些实施方案中,使用异源启动子,因为与天然靶多肽启动子相比,它们通常允许表达的靶基因更多的转录和更高的产率。
适用于原核宿主的启动子包括phoa启动子、β-半乳糖苷酶和乳糖启动子系统、色氨酸(trp)启动子系统和杂合启动子如tac或trc启动子。然而,在细菌中起作用的其它启动子(如其它已知的细菌或噬菌体启动子)也是合适的。它们的核苷酸序列已经被公开,从而使技术人员能够使用接头或衔接子将它们与编码例如包含轻链和重链的掩蔽型细胞因子的靶轻链和重链的顺反子可操作地连接(siebenlist等人(1980)cell20:269),以提供任何所需的限制位点。
在本发明的一方面,重组载体中的每个顺反子包含指导表达的多肽跨膜易位的分泌信号序列组分。一般来说,信号序列可以是载体的组分,或者其可以是插入到载体中的靶多肽dna的一部分。为本发明目的选择的信号序列应当是被宿主细胞识别和加工的信号序列(即被信号肽酶切割)。对于不识别和加工对于异源多肽是天然的信号序列的原核宿主细胞,信号序列被选自例如由碱性磷酸酶、青霉素酶、ipp或热稳定肠毒素ii(stii)前导序列、lamb、phoe、pelb、ompa和mbp组成的组的原核信号序列取代。在本发明的一个实施方案中,在表达系统的两个顺反子中使用的信号序列是stii信号序列或其变体。
另一方面,根据本发明的多肽组分的产生可发生在宿主细胞的细胞质中,因此不需要在每个顺反子内存在分泌信号序列。在这方面,例如对于包含免疫球蛋白轻链和重链的实施方案,轻链和重链在有或没有掩蔽部分的序列、接头序列等的情况下被表达,折叠并组装,以在细胞质内形成功能性免疫球蛋白。某些宿主菌株(例如,大肠杆菌trxb-菌株)提供有利于二硫键形成的细胞质条件,从而允许表达的蛋白质亚基的恰当折叠和组装。proba和pluckthungene,159:203(1995)。
也可通过使用表达系统产生本发明的掩蔽型细胞因子,其中可调节表达的多肽组分的定量比率,以便使本发明分泌并恰当组装的抗体的产率最大化。这种调节是至少部分地通过同时调节多肽组分的翻译强度来实现的。
适于表达本发明的掩蔽型细胞因子的原核宿主细胞包括古细菌和真细菌,如革兰氏阴性或革兰氏阳性生物体。有用的细菌的实例包括埃希氏菌(例如,大肠杆菌)、杆菌(例如,枯草芽孢杆菌)、肠杆菌、假单胞菌属(例如,铜绿假单胞菌)、鼠伤寒沙门氏菌、粘质沙雷氏菌、克雷伯氏菌、变形杆菌、志贺氏菌、根瘤菌、透明颤菌或副球菌。在一个实施方案中,使用革兰氏阴性细胞。在一个实施方案中,大肠杆菌细胞用作本发明的宿主。大肠杆菌菌株的实例包括菌株w3110(bachmann,cellularandmolecularbiology,第2卷(washington,d.c.:americansocietyformicrobiology,1987),第1190-1219页;atcc保藏号27,325)及其衍生物,包括具有基因型w3110δfhua(δtona)ptr3laciqlacl8δomptδ(nmpc-fepe)degp41kanr的菌株33d3(5,639,635号美国专利)。其它菌株及其衍生物如大肠杆菌294(atcc31,446)、大肠杆菌b、大肠杆菌λ1776(atcc31,537)和大肠杆菌rv308(atcc31,608)也是合适的。这些实例是说明性而非限制性的。用于构建任何上述具有限定基因型的细菌的衍生物的方法是本领域中已知的,并且描述于例如bass等人,proteins,8:309-314(1990)中。考虑到复制子在细菌细胞中的可复制性,通常有必要选择适当的细菌。例如,当使用熟知的质粒如pbr322、pbr325、pacyc177或pkn410来提供复制子时,大肠杆菌、沙雷氏菌或沙门氏菌种可合适地用作宿主。通常,宿主细胞应分泌最少量的蛋白水解酶,且理想地可以在细胞培养物中掺入另外的蛋白酶抑制剂。
b.掩蔽型细胞因子产生
用上述表达载体转化宿主细胞,并在适当改进的常规营养培养基中培养,用于诱导启动子、选择转化体或扩增编码所需序列的基因。
转化意指将dna引入到原核宿主中,使得dna可作为染色体外元件或通过染色体整合体复制。根据所使用的宿主细胞,采用适于这类细胞的标准技术进行转化。使用氯化钙的钙处理通常用于含有大量细胞壁屏障的细菌细胞。另一种转化方法使用聚乙二醇/dmso。采用的又一种技术是电穿孔。
在本领域中已知且适于培养选择的宿主细胞的培养基中生长用于产生本发明的掩蔽型细胞因子的原核细胞。合适培养基的实例包括luria肉汤(lb)加上必要的营养补充剂。在一些实施方案中,培养基还含有基于表达载体的构建选择的选择剂,以选择性地允许含有表达载体的原核细胞生长。例如,将氨苄青霉素添加到用于使表达氨苄青霉素抗性基因的细胞生长的培养基中。
除了碳、氮和无机磷酸盐来源之外的任何必要的补充剂也可以按适当的浓度包括,单独引入或作为与另一种补充剂或培养基的混合物如复合氮源引入。任选地,培养基可含有选自由谷胱甘肽、半胱氨酸、胱胺、硫乙醇酸盐、二硫赤藓糖醇和二硫苏糖醇组成的组的一种或多种还原剂。
在合适的温度下培养原核宿主细胞。在某些实施方案中,对于大肠杆菌生长,生长温度在约20℃至约39℃;约25℃至约37℃范围内;或约30℃。培养基的ph可以是约5至约9范围内的任何ph,主要取决于宿主生物体。在某些实施方案中,对于大肠杆菌,ph为约6.8至约7.4,或约7.0。
如果在本发明的表达载体中使用诱导型启动子,则在适于启动子激活的条件下诱导蛋白质表达。在本发明的一方面,phoa启动子用于控制多肽的转录。因此,在用于诱导的磷酸盐限制培养基中培养转化的宿主细胞。在某些实施方案中,磷酸盐限制培养基是c.r.a.p.培养基(参见例如,simmons等人,j.immunol.methods(2002),263:133-147)。根据所用的载体构建体,可使用如本领域中已知的多种其它诱导剂。
在一个实施方案中,本发明的表达掩蔽型细胞因子被分泌到宿主细胞的周质中,并从其中回收。蛋白质回收通常涉及破坏微生物,通常是通过诸如渗透压休克、声处理或裂解的方式。一旦细胞被破坏,可通过离心或过滤移除细胞碎片或全细胞。可例如通过亲和树脂色谱法进一步纯化蛋白质。或者,可以将蛋白质转运到培养基中,并在其中分离。可从培养物中移除细胞,过滤并浓缩培养物上清液,用于进一步纯化产生的蛋白质。可采用通常已知的方法如聚丙烯酰胺凝胶电泳(page)和western印迹测定法进一步分离和确认表达的多肽。
在本发明的一方面,通过发酵过程大量进行掩蔽型细胞因子产生。各种大规模补料分批(fed-batch)发酵程序可用于产生重组蛋白。大规模发酵具有至少1000升的容量,并且在某些实施方案中具有约1,000至100,000升的容量。这些发酵罐使用搅拌器叶轮来分配氧气和营养物,特别是葡萄糖。小规模发酵通常是指在体积容量不超过大约100升的发酵罐中的发酵,并且体积容量可以在约1升至约100升范围内。
在发酵过程中,蛋白质表达的诱导通常在细胞已经在合适的条件下生长至所需密度(例如od550为约180-220)后开始,细胞在该阶段处于早期稳定期。根据所用的载体构建体,可以使用如本领域中已知和上文所述的多种诱导剂。可以在诱导之前使细胞生长较短的时段。细胞通常被诱导约12-50小时,尽管可采用更长或更短的诱导时间。
为提高本发明的多肽的产率和品质,可以改变各种发酵条件。例如,为改善例如分泌的抗体多肽的恰当组装和折叠,可使用过表达伴侣蛋白如dsb蛋白(dsba、dsbb、dsbc、dsbd和或dsbg)或fkpa(具有伴侣活性的肽基脯氨酰基顺式、反式异构酶)的另外的载体来共转化宿主原核细胞。已显示伴侣蛋白促进细菌宿主细胞中产生的异源蛋白的恰当折叠和溶解。chen等人(1999)j.biol.chem.274:19601-19605;georgiou等人,6,083,715号美国专利;georgiou等人,6,027,888号美国专利;bothmann和pluckthun(2000)j.biol.chem.275:17100-17105;ramm和pluckthun(2000)j.biol.chem.275:17106-17113;arie等人(2001)mol.microbiol.39:199-210。
为使表达的异源蛋白(特别是对蛋白水解敏感的那些)的蛋白水解最小化,本发明可使用缺乏蛋白水解酶的某些宿主菌株。例如,可以修饰宿主细胞株,以在编码已知的细菌蛋白酶如蛋白酶iii、ompt、degp、tsp、蛋白酶i、蛋白酶mi、蛋白酶v、蛋白酶vi及其组合的基因中实现基因突变。一些大肠杆菌蛋白酶缺乏的菌株是可用的,并且描述于例如joly等人(1998),同上;georgiou等人,5,264,365号美国专利;georgiou等人,5,508,192号美国专利;hara等人,microbialdrugresistance,2:63-72(1996)中。
在一些实施方案中,缺乏蛋白水解酶并用过表达一种或多种伴侣蛋白的质粒转化的大肠杆菌菌株用作本发明的表达系统中的宿主细胞。
c.掩蔽型细胞因子纯化
在一些实施方案中,进一步纯化本文产生的掩蔽型细胞因子,以获得基本上均质的制剂用于进一步测定和使用。可采用本领域中已知的标准蛋白质纯化方法。以下程序是合适的纯化程序的示例:在免疫亲和或离子交换柱上分级、乙醇沉淀、反相hplc、二氧化硅或阳离子交换树脂如deae上的色谱法、色谱聚焦、sds-page、硫酸铵沉淀和使用例如sephadexg-75的凝胶过滤。
在一些实施方案中,固定在固相上的蛋白a用于本发明的掩蔽型细胞因子的免疫亲和纯化。蛋白a是来自金黄色葡萄球菌的41kd细胞壁蛋白,其以高亲和力与抗体的fc区结合。lindmark等人(1983)j.immunol.meth.62:1-13。蛋白a固定的固相可以是包含玻璃或二氧化硅表面的柱或受控孔玻璃柱或硅酸柱。在一些应用中,柱涂有试剂,如甘油,以可能地防止污染物的非特异性粘附。
作为纯化的第一步,可将来源于如上所述的细胞培养物的制剂施加到蛋白a固定的固相上,以允许所关注的掩蔽型细胞因子与蛋白a特异性结合。然后将洗涤固相以移除与固相非特异性结合的污染物。最后,通过洗脱从固相中回收所关注的掩蔽型细胞因子。
根据本领域中已知的标准蛋白质纯化方法,可采用提供与掩蔽型细胞因子的组分的高亲和力结合的其它纯化方法。
2.使用真核宿主细胞产生掩蔽型细胞因子
用于真核宿主细胞的载体通常包括以下非限制性组分中的一者或多者:信号序列、复制起点、一种或多种标志物基因、增强子元件、启动子和转录终止序列。
a.信号序列组分
用于真核宿主细胞的载体还可以含有在所关注的成熟蛋白质或多肽的n末端具有特异性切割位点的信号序列或其它多肽。选择的异源信号序列可以是被宿主细胞识别和加工的信号序列(即被信号肽酶切割)。在哺乳动物细胞表达中,哺乳动物信号序列以及病毒分泌前导序列(例如单纯疱疹gd信号)是可获得的。这种前体区域的dna在阅读框中与编码掩蔽型细胞因子的dna连接。
b.复制起点
一般地,哺乳动物表达载体不需要复制起点组分。例如,通常可使用sv40起点,仅因为其含有早期启动子。
c.选择基因组分
表达和克隆载体可含有选择基因,也称为可选择标志物。典型的选择基因编码这样的蛋白质,其(a)赋予对抗生素或其它毒素例如氨苄青霉素、新霉素、甲氨蝶呤或四环素的抗性,(b)在相关的情况下补充营养缺陷型缺陷,或(c)提供不能从复合培养基获得的关键营养物。
选择方案的一个实例利用药物来阻止宿主细胞的生长。用异源基因成功转化的那些细胞产生赋予抗药性的蛋白质,并因此在选择方案中存活。这种显性选择的实例使用药物新霉素、霉酚酸和潮霉素。
用于哺乳动物细胞的合适的可选择标志物的另一实例是能够确认有能力摄取编码掩蔽型细胞因子的核酸的细胞的那些,如dhfr、胸苷激酶、金属硫蛋白-i和-ii、灵长类动物金属硫蛋白基因、腺苷脱氨酶、鸟氨酸脱羧酶等。
例如,在一些实施方案中,首先通过在含有dhfr的竞争性拮抗剂氨甲蝶呤(mtx)的培养基中培养所有转化体来确认用dhfr选择基因转化的细胞。在一些实施方案中,当使用野生型dhfr时适当的宿主细胞是dhfr活性缺陷的中国仓鼠卵巢(cho)细胞系(例如,atcccrl-9096)。
或者,用编码掩蔽型细胞因子、野生型dhfr蛋白和另一种可选择的标志物如氨基糖苷3′-磷酸转移酶(aph)的dna序列转化或共转化的宿主细胞(特别是含有内源性dhfr的野生型宿主)可通过在含有用于可选择的标志物的选择剂如氨基糖苷抗生素(例如,卡那霉素、新霉素或g418)的培养基中的细胞生长来选择。参见4,965,199号美国专利。宿主细胞可包括ns0,包括谷氨酰胺合成酶(gs)缺乏的细胞系。5,122,464号美国专利和5,891,693号美国专利中描述了使用gs作为用于哺乳动物细胞的可选择的标志物的方法。
d.启动子组分
表达和克隆载体通常含有由宿主生物体识别并与编码所关注的掩蔽型细胞因子(其可以是本文所述的任何掩蔽型细胞因子)的核酸可操作地连接的启动子。用于真核细胞的启动子序列是已知的。例如,几乎所有的真核基因都具有位于转录起始位点上游大约25至30个碱基处的富at区域。在许多基因的转录起点上游70至80个碱基处所见的另一序列是cncaat区域,其中n可以是任何核苷酸。在大多数真核基因的3′端是aataaa序列,其可以是用于将聚a尾添加到编码序列的3′端的信号。在某些实施方案中,任何或所有这些序列都可以被合适地插入到真核表达载体中。
从哺乳动物宿主细胞中的载体转录例如由启动子控制,所述启动子获自病毒如多瘤病毒、禽痘病毒、腺病毒(如腺病毒2)、牛乳头瘤病毒、禽肉瘤病毒、巨细胞病毒、逆转录病毒、乙型肝炎病毒和猿猴病毒40(sv40)的基因组、获自异源哺乳动物启动子例如肌动蛋白启动子或免疫球蛋白启动子、获自热休克启动子,条件是这些启动子与宿主细胞系统相容。
sv40病毒的早期和晚期启动子方便地以sv40限制片段获得,该片段也含有sv40病毒复制起点。人巨细胞病毒的立即早期启动子方便地以hindiiie限制片段获得。4,419,446号美国专利中公开了使用牛乳头瘤病毒作为载体在哺乳动物宿主中表达dna的系统。4,601,978号美国专利中描述了这种系统的改进。另参见reyes等人,nature297:598-601(1982),描述了人β-干扰素cdna在来自单纯疱疹病毒的胸苷激酶启动子控制下在鼠细胞中的表达。或者,劳斯肉瘤病毒长末端重复序列可用作启动子。
e.增强子元件组分
通常通过将增强子序列插入到载体中来增加高等真核细胞对编码本发明的掩蔽型细胞因子的dna的转录。现在已知许多增强子序列来自哺乳动物基因(珠蛋白、弹性蛋白酶、白蛋白、甲胎蛋白和胰岛素)。然而,通常使用来自真核细胞病毒的增强子。实例包括位于复制起点晚期侧(bp100-270)的sv40增强子、人巨细胞病毒早期启动子增强子、鼠巨细胞病毒早期启动子增强子、位于复制起点晚期侧的多瘤增强子和腺病毒增强子。另参见yaniv,nature297:17-18(1982)(描述用于激活真核启动子的增强子元件)。增强子可以在掩蔽型细胞因子编码序列的5′或3′位置剪接到载体中,但通常位于启动子的位点5′。
f.转录终止组分
真核宿主细胞中使用的表达载体还可含有终止转录和稳定mrna所必需的序列。这类序列通常可得自真核或病毒dna或cdna的5′和有时是3′非翻译区。这些区域含有在编码掩蔽型细胞因子的mrna的非翻译部分中转录为聚腺苷酸化片段的核苷酸区段。一种有用的转录终止组分是牛生长激素聚腺苷酸化区。参见wo94/11026和其中公开的表达载体。
g.宿主细胞的选择和转化
用于在本文的载体中克隆或表达dna的合适宿主细胞包括本文所述的高等真核细胞,包括脊椎动物宿主细胞。脊椎动物细胞在培养物(组织培养物)中的繁殖已成为常规程序。有用的哺乳动物宿主细胞系的实例有通过sv40转化的猴肾cv1系(cos-7、atcccrl1651);人胚肾系(用于在悬浮培养物中生长亚克隆的293或293细胞,graham等人,j.genvirol.36:59(1977));幼仓鼠肾细胞(bhk、atccccl10);中国仓鼠卵巢细胞/-dhfr(cho,urlaub等人,proc.natl.acad.sci.usa77:4216(1980));鼠支持细胞(tm4,mather,biol.reprod.23:243-251(1980));猴肾细胞(cv1atccccl70);非洲绿猴肾细胞(vero-76、atcccrl-1587);人宫颈癌细胞(hela、atccccl2);犬肾细胞(mdck、atccccl34);水牛大鼠肝细胞(brl3a、atcccrl1442);人肺细胞(w138、atccccl75);人肝细胞(hepg2、hb8065);鼠乳腺肿瘤(mmt060562、atccccl51);tri细胞(mather等人,annalsn.y.acad.sci.383:44-68(1982));mrc5细胞;fs4细胞;和人肝癌系(hepg2)。
用上述用于掩蔽型细胞因子产生的表达或克隆载体转化宿主细胞,并在适当改进的常规营养培养基中培养,用于诱导启动子、选择转化体或扩增编码所需序列的基因。
h.培养宿主细胞
可以在多种培养基中培养用于产生本发明的掩蔽型细胞因子的宿主细胞。可商购获得的培养基如ham′sf10(sigma)、最小必需培养基((mem),sigma)、rpmi-1640(sigma)和杜氏改良eagle培养基((dmem),sigma)适于培养宿主细胞。此外,ham等人,meth.enz.58:44(1979);barnes等人,anal.biochem.102:255(1980);4,767,704;4,657,866;4,927,762;4,560,655;或5,122,469号美国专利;wo90/03430;wo87/00195;或美国专利re.30,985中描述的任何培养基可用作宿主细胞的培养基。这些培养基中的任一者可根据需要补充激素和/或其它生长因子(如胰岛素、转铁蛋白或表皮生长因子)、盐(如氯化钠、钙、镁和磷酸盐)、缓冲液(如hepes)、核苷酸(如腺苷和胸苷)、抗生素(如gentamycintm药物)、微量元素(定义为通常以微摩尔范围内的最终浓度存在的无机化合物)和葡萄糖或等效能源。也可以包括本领域技术人员已知的适当浓度的任何其它补充剂。培养条件如温度、ph等是先前选择用于表达的宿主细胞采用的那些,并且对于普通技术人员是显而易见的。
i.掩蔽型细胞因子的纯化
当采用重组技术时,掩蔽型细胞因子可在细胞内产生,或者直接分泌到培养基中。如果在细胞内产生掩蔽型细胞因子,则作为第一步,可以例如通过离心或超滤移除无论是宿主细胞还是裂解片段的颗粒碎片。在掩蔽型细胞因子被分泌到培养基中的情况下,可首先使用可商购获得的蛋白质浓缩过滤器(例如amicon或milliporepellicon超滤单元)浓缩来自这类表达系统的上清液。在任何前述步骤中可以包括蛋白酶抑制剂如pmsf,以抑制蛋白水解,并且可以包括抗生素,以阻止偶然带来的污染物的生长。
可采用例如羟基磷灰石色谱法、凝胶电泳、透析和亲和色谱法纯化由细胞制备的掩蔽型细胞因子组合物,其中亲和色谱法是方便的技术。蛋白a作为亲和配体的适合性取决于掩蔽型细胞因子中存在的任何免疫球蛋白fc结构域(如果有的话)的种类和同种型。蛋白a可用于纯化基于人igg1、igg2或igg4重链的抗体(lindmark等人,j.immunol.methods62:1-13(1983))。推荐蛋白g用于所有鼠同种型和人γ3(guss等人,emboj.5:15671575(1986))。亲和配体连接的基质可以是琼脂糖,但其它基质也是可用的。机械稳定的基质如受控孔玻璃或聚(苯乙烯二乙烯基)苯允许比用琼脂糖获得更快的流速和更短的处理时间。在掩蔽型细胞因子包含ch3结构域的情况下,bakerbondabxtm树脂(j.t.baker,phillipsburg,n.j.)可用于纯化。根据要回收的掩蔽型细胞因子,其它蛋白质纯化技术也是可用的,如在离子交换柱上分级、乙醇沉淀、反相hplc、二氧化硅上的色谱法、肝素sepharosetm上的色谱法阴离子或阳离子交换树脂(如聚天冬氨酸柱)上的色谱法、色谱聚焦、sds-page和硫酸铵沉淀。
在任何初步纯化步骤之后,可以对包含所关注的掩蔽型细胞因子和污染物的混合物进行进一步纯化,例如通过低ph疏水相互作用色谱法,使用ph在约2.5-4.5之间的洗脱缓冲液,在低盐浓度(例如,约0-0.25m盐)下进行。
一般来说,制备用于研究、测试和临床使用的掩蔽型细胞因子的各种方法是本领域中得到确认的,与上述方法一致和/或被本领域技术人员认为适于所关注的特定掩蔽型细胞因子。
iii.组合物
在一些方面,本文还提供包含本文所述的任何掩蔽型细胞因子的组合物。在一些实施方案中,所述组合物包含本文所述的任何示例性实施方案的掩蔽型细胞因子。在一些实施方案中,所述组合物包含本文所述的任何掩蔽型细胞因子的二聚体。在一些实施方案中,所述组合物是药物组合物。在一些实施方案中,所述组合物包含掩蔽型细胞因子,并且进一步包含一种或多种如下详述的组分。例如,在一些实施方案中,所述组合物包含一种或多种药学上可接受的载体、赋形剂、稳定剂、缓冲剂、防腐剂、张力剂、非离子表面活性剂或清洁剂或其它治疗剂或活性化合物或其组合。组合物的各种实施方案在本文中有时被称为制剂。
通过将具有所需纯度的活性成分与任选药学上可接受的载体、赋形剂或稳定剂混合来制备用于储存的治疗性制剂(remington:thescienceandpracticeofpharmacy,第20版,lippincottwilliams&wiklins,pub.,gennaroed.,philadelphia,pa.2000)。在所用剂量和浓度下,可接受的载体、赋形剂或稳定剂对接受者是无毒的,并且包括缓冲剂、抗氧化剂,包括抗坏血酸、甲硫氨酸、维生素e、偏亚硫酸氢钠;防腐剂、等渗剂、稳定剂、金属络合物(例如zn-蛋白质络合物);螯合剂如edta和/或非离子表面活性剂。
缓冲剂可用于将ph控制在优化治疗效果的范围内,特别是如果稳定性依赖于ph。缓冲剂可以按约50mm至约250mm范围内的浓度存在。适用于本发明的缓冲剂包括有机酸和无机酸及其盐。例如,柠檬酸盐、磷酸盐、琥珀酸盐、酒石酸盐、富马酸盐、葡糖酸盐、草酸盐、乳酸盐、乙酸盐。另外,缓冲剂可包含组氨酸和三甲胺盐如tris。
可添加防腐剂以防止微生物生长,其通常以约0.2%-1.0%(w/v)的范围存在。通常与治疗剂一起使用的合适防腐剂的实例包括十八烷基二甲基苄基氯化铵;氯化六甲双铵;苯扎卤铵(例如氯化物、溴化物、碘化物)、苄索氯铵;硫柳汞、苯酚、丁醇或苄醇;对羟基苯甲酸烷基酯,如对羟基苯甲酸甲酯或对羟基苯甲酸丙酯;儿茶酚;间苯二酚;环己醇、3-戊醇、间甲酚、邻甲酚、对甲酚、对羟基苯甲酸甲酯、对羟基苯甲酸丙酯、2-苯氧基乙醇、对羟基苯甲酸丁酯、2-苯基乙醇、乙醇、氯丁醇、硫柳汞、溴硝醇、苯甲酸、咪脲、氯己定、脱氢乙酸钠、氯甲酚、对羟基苯甲酸乙酯和氯苯甘醚(3p-氯苯氧基丙烷-1,2-二醇)。
可以存在张力剂,有时称为“稳定剂”,以调节或维持组合物中液体的张力。当与大的带电生物分子如蛋白质和抗体一起使用时,它们通常被称为“稳定剂”,因为它们可以与氨基酸侧链的带电基团相互作用,从而降低分子间和分子内相互作用的可能性。考虑到其它成分的相对量,张力剂可以按约0.1重量%至约25重量%之间或约1重量%至约5重量%之间的任何量存在。在一些实施方案中,张力剂包括多羟基糖醇、三羟基或更多羟基的糖醇,如甘油、赤藓糖醇、阿糖醇、木糖醇、山梨糖醇和甘露糖醇。
另外的赋形剂包括可用作以下中的一者或多者的剂:(1)填充剂,(2)增溶剂,(3)稳定剂,和(4)防止变性或粘附于容器壁的剂。这类赋形剂包括:多羟基糖醇(上文列举);氨基酸,如丙氨酸、甘氨酸、谷氨酰胺、天冬酰胺、组氨酸、精氨酸、赖氨酸、鸟氨酸、亮氨酸、2-苯丙氨酸、谷氨酸、苏氨酸等;有机糖或糖醇,如蔗糖、乳糖、乳糖醇、海藻糖、水苏糖、甘露糖、山梨糖、木糖、核糖、核糖醇、肌醇糖(myoinisitose)、肌醇(myoinisitol)、半乳糖、半乳糖醇、甘油、环醇(例如,肌醇)、聚乙二醇;含硫还原剂,如脲、谷胱甘肽、硫辛酸、硫乙醇酸钠、硫代甘油、α-硫代甘油和硫代硫酸钠;低分子量蛋白质,如人血清白蛋白、牛血清白蛋白、明胶或其它免疫球蛋白;亲水性聚合物,如聚乙烯吡咯烷酮;单糖(例如,木糖、甘露糖、果糖、葡萄糖;二糖(例如,乳糖、麦芽糖、蔗糖);三糖如棉子糖;和多糖,如糊精或葡聚糖。
可以存在非离子表面活性剂或清洁剂(也称为“润湿剂”),以帮助溶解治疗剂以及保护治疗性蛋白质对抗搅动引起的聚集,这也允许制剂暴露于剪切表面应力而不引起活性治疗性蛋白质或抗体的变性。非离子表面活性剂以约0.05mg/ml至约1.0mg/ml或约0.07mg/ml至约0.2mg/ml的范围存在。在一些实施方案中,非离子表面活性剂以约0.001%至约0.1%w/v或约0.01%至约0.1%w/v或约0.01%至约0.025%w/v的范围存在。
合适的非离子表面活性剂包括聚山梨醇酯(20、40、60、65、80等)、泊洛沙姆(184、188等)、
为了用于体内施用,制剂必须是无菌的。可通过无菌过滤膜过滤使制剂无菌。通常将本文的治疗组合物放入具有无菌入口的容器中,例如具有可以被皮下注射针刺穿的塞子的静脉内溶液袋或小瓶。
施用途径是根据已知和公认的方法,如通过经长时间段以合适的方式单次或多次推注或输注,例如通过皮下、静脉内、腹膜内、肌内、动脉内、病灶内或关节内途径注射或输注、局部施用、吸入或通过持续释放或延长释放方式。
本文所述的任何掩蔽型细胞因子可单独使用或与其它治疗剂组合使用,如在本文所述的方法中。术语“与......组合”涵盖包括在同一制剂或分开的制剂中的两种或更多种治疗剂(例如,掩蔽型细胞因子和治疗剂)。在一些实施方案中,“与......组合”是指“同时”施用,在这种情况下,施用本发明的掩蔽型细胞因子与施用一种或多种另外的治疗剂同时发生(例如,施用掩蔽型细胞因子与施用一种或多种另外的治疗剂是同时的或之间相隔一小时以内)。在一些实施方案中,“与......组合”是指顺序施用,在这种情况下,施用本发明的掩蔽型细胞因子发生在施用一种或多种另外的治疗剂之前和/或之后(例如,施用掩蔽型细胞因子与施用一种或多种另外的治疗剂之间相隔超过一小时)。本文考虑的药剂包括但不限于细胞毒性剂、细胞因子、靶向免疫检查点分子的药剂、靶向免疫刺激分子的药剂、生长抑制剂、免疫刺激剂、抗炎剂或抗癌剂。
根据所治疗的特定适应症的需要,本文的制剂还可以含有一种以上的活性化合物,优选具有彼此没有不利影响的互补活性的那些。或者或此外,所述组合物可包含细胞毒性剂、细胞因子、靶向免疫检查点分子或刺激分子的药剂、生长抑制剂、免疫刺激剂、抗炎剂或抗癌剂。这类分子合适地以对预期目的有效的量组合存在。
制剂可以任意合适的状态存在,如液体制剂、固态(冻干)制剂或冷冻制剂。制备用于治疗用途的这些类型的制剂中的每一者的方法是本领域中熟知的。
iv.治疗方法
本文提供了治疗或预防受试者的疾病的方法,包括对受试者施用有效量的本文所述的任何掩蔽型细胞因子或其组合物。在一些实施方案中,提供了治疗或预防受试者的疾病的方法,包括对受试者施用有效量的掩蔽型细胞因子。在一些实施方案中,提供了治疗或预防受试者的疾病的方法,包括对受试者施用有效量的本文所述的任何实施方案的掩蔽型细胞因子。在一些实施方案中,提供了治疗或预防受试者的疾病的方法,包括对受试者施用本文所述的任何组合物。在一些实施方案中,受试者(例如,人患者)已被诊断为患有肿瘤性病症(例如,癌症)或有发生这类病症的风险。
为了预防或治疗疾病,活性剂的适当剂量将取决于如本文所定义的要治疗的疾病的类型、疾病的严重程度和病程、施用药剂是为了预防还是治疗、先前的疗法、受试者的临床病史和对药剂的反应以及主治医师的判断。合适地一次性或在一系列治疗中对受试者施用药剂。
在本文所述方法的一些实施方案中,施用本文所述的掩蔽型细胞因子之间的间隔为约一周或更长。在本文所述方法的一些实施方案中,施用本文所述的掩蔽型细胞因子之间的间隔为约两天或更长、约三天或更长、约四天或更长、约五天或更长或约六天或更长。在本文所述方法的一些实施方案中,施用本文所述的掩蔽型细胞因子之间的间隔为约一周或更长、约两周或更长、约三周或更长或约四周或更长。在本文所述方法的一些实施方案中,施用本文所述的掩蔽型细胞因子之间的间隔为约一个月或更长、约两个月或更长或约三个月或更长。如本文所用,施用之间的间隔是指掩蔽型细胞因子的一次施用与掩蔽型细胞因子的下一次施用之间的时间段。如本文所用,约一个月的间隔包括四周。在一些实施方案中,治疗包括多次施用掩蔽型细胞因子,其中施用之间的间隔可以变化。例如,在一些实施方案中,第一次施用与第二次施用之间的间隔为约一周,且随后的施用之间的间隔为约两周。在一些实施方案中,第一次施用与第二次施用之间的间隔为约两天、三天、四天、或五天、或六天,且随后的施用之间的间隔为约一周。
在一些实施方案中,在一段时间内多次施用掩蔽型细胞因子。对受试者多次施用的剂量在一些实施方案中可以是每次施用相同的剂量,或者在一些实施方案中,可以两种或更多种不同的剂量对受试者施用掩蔽型细胞因子。例如,在一些实施方案中,最初以一个剂量一次或多次施用掩蔽型细胞因子,之后在稍后的时间点开始以第二剂量一次或多次施用。
在一些实施方案中,以平稳剂量施用本文所述的掩蔽型细胞因子。在一些实施方案中,以每剂约25mg至约500mg的剂量对受试者施用本文所述的掩蔽型细胞因子。在一些实施方案中,以每剂约25mg至约50mg、约50mg至约75mg、约75mg至约100mg、约100mg至约125mg、约125mg至约150mg、约150mg至约175mg、约175mg至约200mg、约200mg至约225mg、约225mg至约250mg、约250mg至约275mg、约275mg至约300mg、约300mg至约325mg、约325mg至约350mg、约350mg至约375mg、约375mg至约400mg、约400mg至约425mg、约425mg至约450mg、约450mg至约475mg或约475mg至约500mg的剂量对受试者施用掩蔽型细胞因子。
在一些实施方案中,以基于受试者的体重或体表面积(bsa)的剂量对受试者施用本文所述的掩蔽型细胞因子。根据疾病的类型和严重程度,约1μg/kg至15mg/kg(例如0.1mg/kg-10mg/kg)的掩蔽型细胞因子可以是对患者施用的初始候选剂量,无论是例如通过一次或多次分开施用还是通过连续输注。一个典型的日剂量范围可以是约1μg/kg至100mg/kg或更多,这取决于上面提到的因素。对于若干天或更长时间的重复施用,根据病情,治疗通常将持续到出现疾病症状的所需抑制为止。掩蔽型细胞因子的一个示例性剂量范围是约0.05mg/kg至约10mg/kg。因此,可以对患者施用约0.5mg/kg、2.0mg/kg、4.0mg/kg或10mg/kg(或其任意组合)的一个或多个剂量。在一些实施方案中,以约0.1mg/kg至约10mg/kg或约1.0mg/kg至约10mg/kg的剂量对受试者施用本文所述的掩蔽型细胞因子。在一些实施方案中,以约为0.1mg/kg、0.5mg/kg、1.0mg/kg、1.5mg/kg、2.0mg/kg、2.5mg/kg、3.0mg/kg、3.5mg/kg、4.0mg/kg、4.5mg/kg、5.0mg/kg、5.5mg/kg、6.0mg/kg、6.5mg/kg、7.0mg/kg、7.5mg/kg、8.0mg/kg、8.5mg/kg、9.0mg/kg、9.5mg/kg或10.0mg/kg中的任一者的剂量对受试者施用本文所述的掩蔽型细胞因子。在一些实施方案中,以约或至少约0.1mg/kg、约或至少约0.5mg/kg、约或至少约1.0mg/kg、约或至少约1.5mg/kg、约或至少约2.0mg/kg、约或至少约2.5mg/kg、约或至少约3.0mg/kg、约或至少约3.5mg/kg、约或至少约4.0mg/kg、约或至少约4.5mg/kg、约或至少约5.0mg/kg、约或至少约5.5mg/kg、约或至少约6.0mg/kg、约或至少约6.5mg/kg、约或至少约7.0mg/kg、约或至少约7.5mg/kg、约或至少约8.0mg/kg、约或至少约8.5mg/kg、约或至少约9.0mg/kg、约或至少约9.5mg/kg、约或至少约10.0mg/kg、约或至少约15.0mg/kg、约或至少约20mg/kg、约或至少约30mg/kg、约或至少约40mg/kg、约或至少约50mg/kg、约或至少约60mg/kg、约或至少约70mg/kg、约或至少约80mg/kg、约或至少约90mg/kg或者约或至少约100mg/kg的剂量对受试者施用本文所述的掩蔽型细胞因子。可以采用上述任何给药频率。
在一些实施方案中,以平稳剂量施用本文所述的掩蔽型il-2多肽。在一些实施方案中,以每剂约25mg至约500mg的剂量对受试者施用本文所述的掩蔽型il-2多肽。在一些实施方案中,以每剂约25mg至约50mg、约50mg至约75mg、约75mg至约100mg、约100mg至约125mg、约125mg至约150mg、约150mg至约175mg、约175mg至约200mg、约200mg至约225mg、约225mg至约250mg、约250mg至约275mg、约275mg至约300mg、约300mg至约325mg、约325mg至约350mg、约350mg至约375mg、约375mg至约400mg、约400mg至约425mg、约425mt至约450mg、约450mg至约475mg或约475mg至约500mg的剂量对受试者施用掩蔽型il-2多肽。
在一些实施方案中,以基于受试者的体重或体表面积(bsa)的剂量对受试者施用本文所述的掩蔽型il-2多肽。根据疾病的类型和严重程度,约1μg/kg至15mg/kg(例如0.1mg/kg-10mg/kg)的掩蔽型il-2多肽可以是对患者施用的初始候选剂量,无论是例如通过一次或多次分开施用还是通过连续输注。一个典型的日剂量范围可以是约1μg/kg至100mg/kg或更多,这取决于上面提到的因素。对于若干天或更长时间的重复施用,根据病情,治疗通常将持续到出现疾病症状的所需抑制为止。掩蔽型il-2多肽的一个示例性剂量范围是约0.05mg/kg至约10mg/kg。因此,可以对患者施用约0.5mg/kg、2.0mg/kg、4.0mg/kg或10mg/kg(或其任意组合)的一个或多个剂量。在一些实施方案中,以约0.1mg/kg至约10mg/kg或约1.0mg/kg至约10mg/kg的剂量对受试者施用本文所述的掩蔽型il-2多肽。在一些实施方案中,以约为0.1mg/kg、0.5mg/kg、1.0mg/kg、1.5mg/kg、2.0mg/kg、2.5mg/kg、3.0mg/kg、3.5mg/kg、4.0mg/kg、4.5mg/kg、5.0mg/kg、5.5mg/kg、6.0mg/kg、6.5mg/kg、7.0mg/kg、7.5mg/kg、8.0mg/kg、8.5mg/kg、9.0mg/kg、9.5mg/kg或10.0mg/kg中的任一者的剂量对受试者施用本文所述的掩蔽型il-2多肽。在一些实施方案中,以约或至少约0.1mg/kg、约或至少约0.5mg/kg、约或至少约1.0mg/kg、约或至少约1.5mg/kg、约或至少约2.0mg/kg、约或至少约2.5mg/kg、约或至少约3.0mg/kg、约或至少约3.5mg/kg、约或至少约4.0mg/kg、约或至少约4.5mg/kg、约或至少约5.0mg/kg、约或至少约5.5mg/kg、约或至少约6.0mg/kg、约或至少约6.5mg/kg、约或至少约7.0mg/kg、约或至少约7.5mg/kg、约或至少约8.0mg/kg、约或至少约8.5mg/kg、约或至少约9.0mg/kg、约或至少约9.5mg/kg、约或至少约10.0mg/kg、约或至少约15.0mg/kg、约或至少约20mg/kg、约或至少约30mg/kg、约或至少约40mg/kg、约或至少约50mg/kg、约或至少约60mg/kg、约或至少约70mg/kg、约或至少约80mg/kg、约或至少约90mg/kg或者约或至少约100mg/kg的剂量对受试者施用本文所述的掩蔽型il-2多肽。可以采用上述任何给药频率。
在一些实施方案中,以平稳剂量施用本文所述的掩蔽型il-15多肽。在一些实施方案中,以每剂约25mg至约500mg的剂量对受试者施用本文所述的掩蔽型il-15多肽。在一些实施方案中,以每剂约25mg至约50mg、约50mg至约75mg、约75mg至约100mg、约100mg至约125mg、约125mg至约150mg、约150mg至约175mg、约175mg至约200mg、约200mg至约225mg、约225mg至约250mg、约250mg至约275mg、约275mg至约300mg、约300mg至约325mg、约325mg至约350mg、约350mg至约375mg、约375mg至约400mg、约400mg至约425mg、约425mg至约450mg、约450mg至约475mg或约475mg至约500mg的剂量对受试者施用掩蔽型il-15多肽。
在一些实施方案中,以基于受试者的体重或体表面积(bsa)的剂量对受试者施用本文所述的掩蔽型il-15多肽。根据疾病的类型和严重程度,约1μg/kg至15mg/kg(例如0.1mg/kg-10mg/kg)的掩蔽型il-15多肽可以是对患者施用的初始候选剂量,无论是例如通过一次或多次分开施用还是通过连续输注。一个典型的日剂量范围可以是约1μg/kg至100mg/kg或更多,这取决于上面提到的因素。对于若干天或更长时间的重复施用,根据病情,治疗通常将持续到出现疾病症状的所需抑制为止。因此,可以对患者施用约0.5mg/kg、2.0mg/kg、4.0mg/kg或10mg/kg(或其任意组合)的一个或多个剂量。在一些实施方案中,以每剂约25mg至约500mg的剂量对受试者施用本文所述的掩蔽型il-15多肽。在一些实施方案中,以约0.1mg/kg至约10mg/kg或约1.0mg/kg至约10mg/kg的剂量对受试者施用本文所述的掩蔽型il-15多肽。在一些实施方案中,以约为0.1mg/kg、0.5mg/kg、1.0mg/kg、1.5mg/kg、2.0mg/kg、2.5mg/kg、3.0mg/kg、3.5mg/kg、4.0mg/kg、4.5mg/kg、5.0mg/kg、5.5mg/kg、6.0mg/kg、6.5mg/kg、7.0mg/kg、7.5mg/kg、8.0mg/kg、8.5mg/kg、9.0mg/kg、9.5mg/kg或10.0mg/kg中的任一者的剂量对受试者施用本文所述的掩蔽型il-15多肽。在一些实施方案中,以约或至少约0.1mg/kg、约或至少约0.5mg/kg、约或至少约1.0mg/kg、约或至少约1.5mg/kg、约或至少约2.0mg/kg、约或至少约2.5mg/kg、约或至少约3.0mg/kg、约或至少约3.5mg/kg、约或至少约4.0mg/kg、约或至少约4.5mg/kg、约或至少约5.0mg/kg、约或至少约5.5mg/kg、约或至少约6.0mg/kg、约或至少约6.5mg/kg、约或至少约7.0mg/kg、约或至少约7.5mg/kg、约或至少约8.0mg/kg、约或至少约8.5mg/kg、约或至少约9.0mg/kg、约或至少约9.5mg/kg、约或至少约10.0mg/kg、约或至少约15.0mg/kg、约或至少约20mg/kg、约或至少约30mg/kg、约或至少约40mg/kg、约或至少约50mg/kg、约或至少约60mg/kg、约或至少约70mg/kg、约或至少约80mg/kg、约或至少约90mg/kg或者约或至少约100mg/kg的剂量对受试者施用本文所述的掩蔽型il-15多肽。可以采用上述任何给药频率。
本文考虑的治疗方法是用本文所述的任何掩蔽型细胞因子或组合物治疗病症或疾病。在一些实施方案中,治疗方法使用本文所述的任何掩蔽型il-2多肽或本文所述的任何掩蔽型il-15多肽或包含本文所述的掩蔽型细胞因子的任何组合物。可用本发明的制剂治疗的病症或疾病包括白血病、淋巴瘤、头颈癌、结肠直肠癌、前列腺癌、胰腺癌、黑素瘤、乳腺癌、成神经细胞瘤、肺癌、卵巢癌、骨肉瘤、膀胱癌、宫颈癌、肝癌、肾癌、皮肤癌(例如,梅克尔细胞癌)或睾丸癌。
在一些实施方案中,本文提供通过施用本文所述的任何掩蔽型细胞因子或组合物来治疗或预防癌症的方法。在一些实施方案中,本文提供通过施用本文所述的掩蔽型il-2多肽或掩蔽型il-15多肽或包含掩蔽型细胞因子的任何组合物来治疗或预防癌症的方法。如本文所用,术语“癌症”是指见于哺乳动物的所有类型的癌症、赘生物或恶性肿瘤,包括白血病、淋巴瘤、黑素瘤、神经内分泌肿瘤、癌和肉瘤。可用本文提供的掩蔽型细胞因子、药物组合物或方法治疗的示例性癌症包括淋巴瘤、肉瘤、膀胱癌、骨癌、脑肿瘤、宫颈癌、结肠癌、食道癌、胃癌、头颈癌、肾癌、骨髓瘤、甲状腺癌、白血病、前列腺癌、乳腺癌(例如三阴性、er阳性、er阴性、化疗抗性、赫赛汀抗性、her2阳性、多柔比星抗性、他莫昔芬抗性、导管癌、小叶癌、原发性、转移性)、卵巢癌、胰腺癌、肝癌(例如肝细胞癌)、肺癌(例如非小细胞肺癌、鳞状细胞肺癌、腺癌、大细胞肺癌、小细胞肺癌、类癌、肉瘤)、多形性成胶质细胞瘤、神经胶质瘤、黑素瘤、前列腺癌、去势抵抗性前列腺癌、乳腺癌、三阴性乳腺癌、成胶质细胞瘤、卵巢癌、肺癌、鳞状细胞癌(例如,头、颈或食道)、结肠直肠癌、白血病、急性髓性白血病、淋巴瘤、b细胞淋巴瘤或多发性骨髓瘤。另外的实例包括甲状腺癌、内分泌系统癌、脑癌、乳腺癌、宫颈癌、结肠癌、头颈癌、食道癌、肝癌、肾癌、肺癌、非小细胞肺癌、黑素瘤、间皮瘤、卵巢癌、肉瘤、胃癌、子宫癌或成神经管细胞瘤、霍奇金病、非霍奇金淋巴瘤、多发性骨髓瘤、成神经细胞瘤、神经胶质瘤、多形性成胶质细胞瘤、卵巢癌、横纹肌肉瘤、原发性血小板增多症、原发性巨球蛋白血症、原发性脑肿瘤、癌症、恶性胰腺胰岛瘤、恶性类癌、泌尿系统膀胱癌、癌前皮肤病变、睾丸癌、淋巴瘤、甲状腺癌、成神经细胞瘤、食道癌、生殖泌尿道癌、恶性高钙血症、子宫内膜癌、肾上腺皮质癌、内分泌或外分泌胰腺肿瘤、甲状腺髓样癌(medullarythyroidcancer)、甲状腺髓样癌(medullarythyroidcarcinoma)、黑素瘤、结肠直肠癌、乳头状甲状腺癌、肝细胞癌、乳头佩吉特病、叶状肿瘤、小叶癌、导管癌、胰腺星状细胞癌、肝星状细胞癌或前列腺癌。
在一些实施方案中,本文提供通过施用本文所述的任何掩蔽型细胞因子或组合物来治疗或预防白血病的方法。术语“白血病”泛指血液形成器官的进行性恶性疾病,并且通常以白细胞及其前体在血液和骨髓中的畸态增殖和发育为特征。白血病通常基于以下情况进行临床分类:(1)疾病的持续时间和特征-急性或慢性;(2)涉及的细胞的类型;髓样(骨髓性)、淋巴样(成淋巴)或单核细胞的;和(3)血液中异常细胞数增加或不增加-白血病或白细胞缺乏(亚白血病)。可用本文提供的化合物、药物组合物或方法治疗的示例性白血病包括例如急性非淋巴细胞性白血病、慢性淋巴细胞性白血病、急性粒细胞性白血病、慢性粒细胞性白血病、急性前髓细胞性白血病、成人t细胞白血病、白细胞缺乏性白血病、白血病性白血病、嗜碱性白血病、胚细胞白血病、牛白血病、慢性髓细胞性白血病、皮肤白血病、胚胎性白血病、嗜酸性白血病、格罗斯白血病、毛细胞白血病、成血细胞性白血病、血胚细胞性白血病、组织细胞性白血病、干细胞白血病、急性单核细胞性白血病、白细胞减少性白血病、淋巴性白血病、成淋巴细胞性白血病、淋巴细胞性白血病、成淋巴性白血病、淋巴样白血病、淋巴肉瘤细胞白血病、肥大细胞白血病、巨核细胞白血病、微成髓细胞白血病、单核细胞白血病、成髓细胞白血病、髓细胞性白血病、髓性粒细胞性白血病、髓细胞单核细胞白血病、内格利型白血病、浆细胞白血病、多发性骨髓瘤、浆细胞性白血病、前髓细胞性白血病、里德尔细胞白血病(riedercellleukemia)、希林氏白血病(schilling′sleukemia)、干细胞白血病、亚白血病性白血病或未分化细胞白血病。
在一些实施方案中,本文提供通过施用本文所述的任何掩蔽型细胞因子或组合物来治疗或预防肉瘤的方法。术语“肉瘤”通常是指由类似胚胎结缔组织的物质组成的肿瘤,并且通常由包埋在纤维状或均质物质中的紧密堆积的细胞组成。可用本文提供的化合物、药物组合物或方法治疗的肉瘤包括软骨肉瘤、纤维肉瘤、淋巴肉瘤、黑肉瘤、粘液肉瘤、骨肉瘤、abemethy肉瘤、脂肉瘤、脂肪肉瘤、肺泡样软组织肉瘤、成釉细胞肉瘤、葡萄状肉瘤、绿色肉瘤、绒毛膜癌、胚胎性肉瘤、维尔姆斯瘤肉瘤、子宫内膜肉瘤、基质肉瘤、尤因氏肉瘤、筋膜肉瘤、成纤维细胞肉瘤、巨细胞肉瘤、粒细胞肉瘤、霍奇金肉瘤、特发性多发性色素沉着出血性肉瘤、b细胞免疫母细胞肉瘤、淋巴瘤、t细胞免疫母细胞肉瘤、延森氏肉瘤、卡波西肉瘤、枯氏细胞肉瘤、血管肉瘤、白血病肉瘤、恶性间质瘤肉瘤、骨膜外肉瘤、网状细胞肉瘤、劳斯肉瘤、浆液囊性肉瘤、滑膜肉瘤或毛细血管扩张性肉瘤。
在一些实施方案中,本文提供通过施用本文所述的任何掩蔽型细胞因子或组合物来治疗或预防黑素瘤的方法。术语“黑素瘤”意指由皮肤及其它器官的黑素细胞系统产生的肿瘤。可用本文提供的化合物、药物组合物或方法治疗的黑素瘤包括例如肢端雀斑样痣黑素瘤、无黑素性黑素瘤、良性幼年黑素瘤、cloudman黑素瘤、s91黑素瘤、harding-passey黑素瘤、幼年黑素瘤、恶性雀斑样痣黑素瘤、恶性黑素瘤、结节性黑素瘤、甲下黑素瘤或浅表扩散性黑素瘤。
在一些实施方案中,本文提供通过施用本文所述的任何掩蔽型细胞因子或组合物来治疗或预防癌的方法。术语“癌”是指由倾向于浸润周围组织并产生转移的上皮细胞构成的恶性新生物。可用本文提供的化合物、药物组合物或方法治疗的示例性癌包括例如甲状腺髓样癌、家族性甲状腺髓样癌、腺泡癌、腺泡状癌、腺样囊性癌、腺样囊性癌、腺癌(carcinomaadenomatosum)、肾上腺皮质癌、肺泡癌、肺泡细胞癌、基底细胞癌(basalcellcarcinoma)、基底上皮细胞癌(carcinomabasocellulare)、基底样癌、基底鳞状细胞癌、细支气管肺泡癌、细支气管癌、支气管源性癌、脑样癌、胆管细胞癌、绒毛膜癌、胶质癌、粉刺癌、子宫体癌、筛状癌、铠甲状癌、面部皮肤癌、柱状癌、柱状细胞癌、管癌、导管癌、硬癌、胚胎性癌、脑样癌、表皮样癌、腺样上皮癌、外生性癌、溃疡癌、纤维癌、胶样癌(gelatinifornicarcinoma)、胶状癌、巨细胞癌(giantcellcarcinoma)、巨细胞癌(carcinomagigantocellulare)、腺样癌、颗粒细胞癌、毛发基质癌、血样癌、肝细胞癌、许特耳细胞癌(hurthlecellcarcinoma)、透明癌、肾上腺样癌、幼稚型胚胎性癌、原位癌、表皮内癌、上皮内癌、krompecher癌、库尔奇茨基细胞癌(kulchitzky-cellcarcinoma)、大细胞癌、豆状癌(lenticularcarcinoma)、豆状癌(carcinomalenticulare)、脂肪瘤癌、小叶癌、淋巴上皮癌、髓样癌、髓质癌、黑素癌、软癌、粘液性癌(mucinouscarcinoma)、粘液性癌(carcinomamuciparum)、粘液细胞癌、粘液表皮样癌、粘液癌(carcinomamucosum)、粘液癌(mucouscarcinoma)、粘液瘤样癌、鼻咽癌、燕麦细胞癌、骨化性癌、骨样癌、乳头状癌、门静脉周癌、浸润前癌、棘细胞癌、软糊状癌、肾细胞肾癌、储备细胞癌、肉瘤样癌、施奈德癌(schneideriancarcinoma)、硬癌、阴囊癌、印戒细胞癌、单纯癌、小细胞癌、马铃薯状癌、球状细胞癌、纺锤细胞癌、海绵状癌、鳞状癌、鳞状细胞癌、绳捆癌、血管扩张性癌、毛细血管扩张癌、移行细胞癌、结节性皮癌、小管癌、结节性皮癌、疣状癌或绒毛状癌。
在一些实施方案中,本文提供通过施用本文所述的任何掩蔽型细胞因子或组合物来治疗或预防转移性癌症的方法。如本文所用,术语“转移”、“转移性”和“转移性癌症”可互换使用,并且是指肿瘤性疾病或病症例如癌症从一个器官或另一个非相邻器官或身体部分的扩散。癌症发生在起源部位,例如乳腺,该部位被称为原发性肿瘤,例如原发性乳腺癌。原发性肿瘤或起源部位中的一些癌细胞获得穿透和浸润局部区域中的周围正常组织的能力和/或穿透淋巴系统或血管系统的壁循环通过系统到达身体中的其它部位和组织的能力。由原发性肿瘤的癌细胞形成的第二种临床上可检测的肿瘤被称为转移性或继发性肿瘤。当癌细胞转移时,推测转移性肿瘤及其细胞与原始肿瘤的类似。因此,如果肺癌转移到乳腺,则乳腺部位的继发性肿瘤由异常肺细胞而不是异常乳腺细胞组成。乳腺中的继发性肿瘤是指转移性肺癌。因此,短语转移性癌症是指其中受试者患有或曾经患有原发性肿瘤且患有一种或多种继发性肿瘤的疾病。短语非转移性癌症或患有非转移性癌症的受试者是指其中受试者患有原发性肿瘤但没患一种或多种继发性肿瘤的疾病。例如,转移性肺癌是指患有原发性肺肿瘤或有原发性肺肿瘤病史并且在第二个位置或多个位置(例如在乳腺中)有一种或多种继发性肿瘤的受试者的疾病。
在一些实施方案中,本文提供通过与抗癌剂组合施用本文所述的任何掩蔽型细胞因子或组合物来治疗或预防癌症的方法。所述抗癌剂可以是能够减少癌症生长、干扰癌细胞复制、直接或间接杀伤癌细胞、减少转移、减少肿瘤血液供应或降低细胞存活的任何药剂。在一些实施方案中,所述抗癌剂选自由以下组成的组:pd-1抑制剂、egfr抑制剂、her2抑制剂、vegfr抑制剂、ctla-4抑制剂、btla抑制剂、b7h4抑制剂、b7h3抑制剂、csfir抑制剂、hvem抑制剂、cd27抑制剂、kir抑制剂、nkg2a抑制剂、nkg2d激动剂、tweak抑制剂、alk抑制剂、cd52靶向抗体、ccr4靶向抗体、pd-l1抑制剂、kit抑制剂、pdgfr抑制剂、baff抑制剂、hdac抑制剂、vegf配体抑制剂、cd19靶向分子、folr1靶向分子、dll3靶向分子、dkk1靶向分子、muc1靶向分子、muc16靶向分子、psma靶向分子、msln靶向分子、ny-es0-1靶向分子、b7h3靶向分子、b7h4靶向分子、bcma靶向分子、cd29靶向分子、cd151靶向分子、cd123靶向分子、cd33靶向分子、cd37靶向分子、cdh19靶向分子、cea靶向分子、claudin18.2靶向分子、clec12a靶向分子、egfrviii靶向分子、epcam靶向分子、epha2靶向分子、fcrh5靶向分子、flt3靶向分子、gd2靶向分子、磷脂酰肌醇蛋白聚糖3靶向分子、gpa33靶向分子、gprc5d靶向分子、il-23r靶向分子、il-1rap靶向分子、mcsp靶向分子、ron靶向分子、ror1靶向分子、steap2靶向分子、tfr靶向分子、cd166靶向分子、tpbg靶向分子、trop2靶向分子、蛋白酶体抑制剂、abl抑制剂、cd30抑制剂、flt3抑制剂、met抑制剂、ret抑制剂、il-1β抑制剂、mek抑制剂、ros1抑制剂、braf抑制剂、cd38抑制剂、rankl抑制剂、b4galnt1抑制剂、slamf7抑制剂、idh2抑制剂、mtor抑制剂、cd20靶向抗体、btk抑制剂、pi3k抑制剂、fit3抑制剂、parp抑制剂、cdk4抑制剂、cdk6抑制剂、fgfr抑制剂、raf抑制剂、jak1抑制剂、jak2抑制剂、jak3抑制剂、il-6抑制剂、il-17抑制剂、平滑化(smoothened)抑制剂、il-6r抑制剂、bcl2抑制剂、ptch抑制剂、pigf抑制剂、tgfb抑制剂、cd28激动剂、cd3激动剂、cd40激动剂、gitr激动剂、ox40激动剂、vista激动剂、cd137激动剂、lag3抑制剂、tim3抑制剂、tigit抑制剂和il-2r抑制剂。
在一些实施方案中,本文提供通过与抗炎剂组合施用本文所述的任何掩蔽型细胞因子来治疗或预防癌症的方法。所述抗炎剂可以是能够预防、抵抗、抑制或以其它方式减轻炎症的任何药剂。
在一些实施方案中,所述抗炎剂是环氧合酶(cox)抑制剂。cox抑制剂可以是抑制cox-1和/或cox-2的活性的任何药剂。在一些实施方案中,cox抑制剂选择性地抑制cox-1(即,cox抑制剂抑制cox-1的活性超过其抑制cox-2的活性)。在一些实施方案中,cox抑制剂选择性地抑制cox-2(即,cox抑制剂抑制cox-2的活性超过其抑制cox-1的活性)。在一些实施方案中,cox抑制剂抑制cox-1和cox-2两者。
在一些实施方案中,cox抑制剂是选择性cox-1抑制剂,并且选自由sc-560、fr122047、p6、莫苯唑酸、tfap、氟比洛芬和酮洛芬组成的组。在一些实施方案中,cox抑制剂是选择性cox-2抑制剂,并且选自由以下组成的组:塞来昔布、罗非昔布、美洛昔康、吡罗昔康、德拉昔布、帕瑞昔布、伐地昔布、依托昔布、色烯衍生物、色满衍生物、n-(2-环己氧基硝基苯基)甲磺酰胺、帕瑞考昔、罗美昔布、rs57067、t-614、bms-347070、jte-522、s-2474、svt-2016、ct-3、abt-963、sc-58125、尼美舒利、氟舒胺、ns-398、l-745337、rwj-63556、l-784512、达布飞龙、cs-502、las-34475、las-34555、s-33516、双氯芬酸、甲芬那酸和sd-8381。在一些实施方案中,cox抑制剂选自由布洛芬、萘普生、酮咯酸、吲哚美辛、阿司匹林、萘普生、托美汀、吡罗昔康和甲氯芬那酸酯组成的组。在一些实施方案中,cox抑制剂选自由以下组成的组:sc-560、fr122047、p6、莫苯唑酸、tfap、氟比洛芬、酮洛芬、塞来昔布、罗非昔布、美洛昔康、吡罗昔康、德拉昔布、帕瑞昔布、伐地昔布、依托昔布、色烯衍生物、色满衍生物、n-(2-环己氧基硝基苯基)甲磺酰胺、帕瑞考昔、罗美昔布、rs57067、t-614、bms-347070、jte-522、s-2474、svt-2016、ct-3、abt-963、sc-58125、尼美舒利、氟舒胺、ns-398、l-745337、rwj-63556、l-784512、达布飞龙、cs-502、las-34475、las-34555、s-33516、双氯芬酸、甲芬那酸、sd-8381、布洛芬、萘普生、酮咯酸、吲哚美辛、阿司匹林、萘普生、托美汀、吡罗昔康和甲氯芬那酸酯。
在一些实施方案中,所述抗炎剂是nf-κb抑制剂。nf-κb抑制剂可以是抑制nf-κb途径的活性的任何药剂。在一些实施方案中,nf-κb抑制剂选自由ikk复合物抑制剂、iκb降解抑制剂、nf-κb核易位抑制剂、p65乙酰化抑制剂、nf-κbdna结合抑制剂、nf-κb反式激活抑制剂和p53诱导抑制剂组成的组。
在一些实施方案中,ikk复合物抑制剂选自由tpca-1、nf-κb激活抑制剂vi(bot-64)、bms-345541、氨来占诺、sc-514(gk-01140)、imd-0354和ikk-16组成的组。在一些实施方案中,iκb降解抑制剂选自由bay-11-7082、mg-115、mg-132、乳胞素、环氧酶素、小白菊内酯、卡非佐米和mln-4924(pevonedistat)组成的组。在一些实施方案中,nf-κb核易位抑制剂选自由jsh-23和咯利普兰组成的组。在一些实施方案中,p65乙酰化抑制剂选自由没食子酸和漆树酸组成的组。在一些实施方案中,nf-κbdna结合抑制剂选自由gyy-4137、p-xsc、cv-3988和前列腺素e2(pge2)组成的组。在一些实施方案中,nf-κb反式激活抑制剂选自由ly-294002、渥曼青霉素和美沙拉明组成的组。在一些实施方案中,p53诱导抑制剂选自由奎纳克林和夫拉平度组成的组。在一些实施方案中,nf-κb抑制剂选自由以下组成的组:tpca-1、nf-κb激活抑制剂vi(bot-64)、bms-345541、氨来占诺、sc-514(gk-01140)、imd-0354、ikk-16、bay-11-7082、mg-115、mg-132、乳胞素、环氧酶素、小白菊内酯、卡非佐米、mln-4924(pevonedistat)、jsh-23咯利普兰、没食子酸、漆树酸、gyy-4137、p-xsc、cv-3988、前列腺素e2(pge2)、ly-294002、渥曼青霉素、美沙拉嗪、奎纳克林和夫拉平度。
在一些实施方案中,本文提供通过与抗癌治疗性蛋白质组合施用本文所述的任何掩蔽型细胞因子或组合物来治疗或预防癌症的方法。抗癌治疗性蛋白质可以是能够减少癌症生长、干扰癌细胞复制、直接或间接杀伤癌细胞、减少转移、减少肿瘤血液供应或降低细胞存活的任何治疗性蛋白质。示例性抗癌治疗性蛋白质可呈抗体或其片段、抗体衍生物、双特异性抗体、嵌合抗原受体(car)t细胞、融合蛋白或双特异性t细胞衔接子(bite)的形式。
在一些实施方案中,本文提供通过施用本文所述的任何掩蔽型细胞因子或组合物来治疗或预防炎性或自身免疫性疾病的方法。术语“炎性疾病”是指由炎症引起、导致的疾病或导致炎症的疾病。术语“自身免疫性疾病”是指其中受试者自身的免疫系统攻击其自身的细胞或组织的疾病。
在一些实施方案中,所述炎性或自身免疫性疾病选自由以下组成的组:动脉粥样硬化、肥胖症、炎性肠病(ibd)、类风湿性关节炎、过敏性脑炎、银屑病、特应性皮肤病、骨质疏松症、腹膜炎、肝炎、狼疮、乳糜泻、舍格伦综合征、风湿性多肌痛、多发性硬化(ms)、强直性脊柱炎、1型糖尿病、斑秃、血管炎和颞动脉炎、移植物抗宿主病(gvhd)、哮喘、copd、副肿瘤性自身免疫性疾病、软骨炎症、幼年型关节炎、幼年型类风湿性关节炎、少关节幼年型类风湿性关节炎、多关节幼年型类风湿性关节炎、全身发作性幼年型类风湿性关节炎、幼年型强直性脊柱炎、幼年型肠病性关节炎、幼年型反应性关节炎、幼年型赖特尔综合征、sea综合征(血清阴性、接骨点病变、关节病综合征)、幼年型皮肌炎、幼年型银屑病关节炎、幼年型硬皮病、幼年型全身性红斑狼疮、幼年型血管炎、少关节类风湿性关节炎、全身发作性类风湿性关节炎、肠病性关节炎、反应性关节炎、赖特尔综合征、皮肌炎、银屑病关节炎、硬皮病、血管炎、肌炎、多肌炎、皮肌炎、结节性多动脉炎、韦格纳肉芽肿病、动脉炎、风湿性多肌痛、结节病、硬化症、原发性胆汁性硬化、硬化性胆管炎、银屑病、斑块状银屑病、滴状银屑病、反型银屑病、脓疱性银屑病、红皮病性银屑病、皮炎、特应性皮炎、动脉粥样硬化、斯蒂尔病、全身性红斑狼疮(sle)、重症肌无力、克罗恩病、溃疡性结肠炎、乳糜泻、鼻窦炎、具有息肉的鼻窦炎、嗜酸性食管炎、嗜酸性支气管炎、格林-巴利病、甲状腺炎(例如,格雷夫斯病)、阿狄森病、雷诺现象、自身免疫性肝炎、移植排斥、肾损伤、丙型肝炎诱导的血管炎和自发性妊娠丢失。
v.制品或试剂盒
在另一方面,提供了包含本文所述的任何掩蔽型细胞因子的制品或试剂盒。所述制品或试剂盒可进一步包括在本发明的方法中使用细胞因子的说明书。因此,在某些实施方案中,所述制品或试剂盒包括在治疗或预防个体的病症(例如,癌症)的方法中使用掩蔽型细胞因子的说明书,所述方法包括对个体施用有效量的掩蔽型细胞因子。例如,在某些实施方案中,所述制品或试剂盒包括在治疗或预防个体的病症(例如,癌症)的方法中使用掩蔽型il-2多肽的说明书,所述方法包括对个体施用有效量的掩蔽型il-2多肽。在某些实施方案中,所述个体是人。在一些实施方案中,所述个体患有选自由白血病、淋巴瘤、头颈癌、结肠直肠癌、前列腺癌、胰腺癌、黑素瘤、乳腺癌、成神经细胞瘤、肺癌、卵巢癌、骨肉瘤、膀胱癌、宫颈癌、肝癌、肾癌、皮肤癌或睾丸癌组成的组的疾病。
所述制品或试剂盒可进一步包括容器。合适的容器包括例如瓶、小瓶(例如,双室小瓶)、注射器(如单室或双室注射器)、试管和静脉内(iv)袋。容器可由诸如玻璃或塑料的多种材料形成。容器容纳制剂。在一些实施方案中,所述制剂是冻干制剂。在一些实施方案中,所述制剂是冷冻制剂。在一些实施方案中,所述制剂是液体制剂。
所述制品或试剂盒可进一步包括标签或包装插页,其位于容器上或与容器关联,可指示制剂的重构和/或使用说明。标签或包装插页可进一步指示制剂可用于或旨在用于皮下、静脉内或其它施用模式以治疗或预防个体的病症(例如,癌症)。容纳制剂的容器可以是单次使用的小瓶或多次使用的小瓶,其允许重复施用重构制剂。所述制品或试剂盒可进一步包括包含合适稀释剂的第二容器。所述制品或试剂盒可进一步包括从商业、治疗和使用者角度出发所需的其它材料,包括其它缓冲剂、稀释剂、过滤器、针、注射器和带有使用说明书的包装插页。
在具体的实施方案中,本发明提供用于单剂量施用单位的试剂盒。这类试剂盒包括治疗性细胞因子的水性制剂的容器,包括单室或多室预填充注射器。示例性预填充注射器可得自德国vettergmbh,ravensburg。
本文的制品或试剂盒任选进一步包括包含第二药物的容器,其中掩蔽型细胞因子是第一药物,且所述制品或试剂盒进一步包括标签或包装插页上的关于用有效量的第二药物治疗受试者的说明书。
在另一实施方案中,本文提供包含本文所述的用于在自动注射器装置中施用的制剂的制品或试剂盒。自动注射器可以被描述为一种注射装置,其在启动时将递送其内含物,而无需患者或施用者采取另外的必要动作。当递送速率必须恒定且递送时间超过片刻时,它们特别适合于治疗制剂的自给药。
vi.定义
除另有定义外,本文使用的所有技术术语、符号以及其它技术和科学术语或专有名词旨在具有与要求保护的主题所属领域的普通技术人员通常所理解的含义相同的含义。在一些情况下,为了清楚和/或为了便于参考,本文定义了具有通常所理解的含义的术语,并且本文包括这类定义不一定应当被解释为表示与本领域中通常理解的内容有显著差异。
要理解的是,本发明不限于特定的组合物或生物系统,这些当然是可以变化的。还要理解的是,本文使用的术语仅用于描述特定的实施方案,并不旨在进行限制。如在本说明书和所附权利要求中所用,单数形式“一种(个)”和“该(所述)”包括复数指代项,除非内容中另有明确规定。因此,例如提到“il-2多肽”任选包括两种或更多种这类多肽的组合等。
如本文所用的术语“约”是指这一技术领域的技术人员易知的各个值通常的误差范围。本文提到“约”某一值或参数包括(并描述)涉及该值或参数本身的实施方案。
要理解的是,本文描述的本发明的各方面和实施方案包括“包含”各方面和实施方案、“由各方面和实施方案组成”和“基本上由各方面和实施方案组成”。
如本文所用,术语“和/或”是指与该术语相关联的任一项目、项目的任意组合或所有项目。例如,短语“a、b和/或c”旨在涵盖以下实施方案中的每一者:a、b和c;a、b或c;a或b;a或c;b或c;a和b;a和c;b和c;a和b或c;b和a或c;c和a或b;a(单独);b(单独);和c(单独)。
术语“抗体”包括多克隆抗体、单克隆抗体(包括具有免疫球蛋白fc区的全长抗体)、具有多表位特异性的抗体组合物、多特异性抗体(例如,双特异性抗体、双抗体和单链分子以及抗体片段(例如,fab、f(ab’)2和fv)。术语“免疫球蛋白”(ig)在本文中可与“抗体”互换使用。
术语“双抗体”是指具有两个抗原结合位点的小抗体片段,其包含与同一多肽链(vh-vl)中的轻链可变(vl)结构域连接的重链可变(vh)结构域。
基本4链抗体单元是由两条相同的轻(l)链和两条相同的重(h)链组成的异四聚体糖蛋白。igm抗体由5个基本异四聚体单元以及称为j链的附加多肽组成,并且含有10个抗原结合位点,而iga抗体包含2-5个基本4链单元,它们可聚合形成与j链组合的多价组装体。在igg的情况下,4链单元通常为约150,000道尔顿。每条l链通过一个共价二硫键与h链连接,而两条h链根据h链同种型而通过一个或多个二硫键彼此连接。每条h和l链还具有规则间隔的链内二硫桥。每条h链在n末端具有可变结构域(vh),之后是对于α和γ链中的每一者的三个恒定结构域(ch),和对于μ和ε同种型的四个ch结构域。每条l链在n末端具有可变结构域(vl),之后是在其另一端的恒定结构域。vl与vh对齐,且cl与重链的第一恒定结构域(ch1)对齐。据信特定的氨基酸残基在轻链与重链可变结构域之间形成界面。vh和vl在一起配对形成单个抗原结合位点。关于不同类别的抗体的结构和特性,参见例如basicandclinicalimmunology,第8版,danielp.sties、abbai.terr和tristramg.parsolw(编),appleton&lange,norwalk,ct,1994,第71页和第6章。
来自任何脊椎动物物种的l链可基于其恒定结构域的氨基酸序列而归属于被称为κ和λ的两种明显不同的类型之一。根据重链的恒定结构域(ch)的氨基酸序列,免疫球蛋白可归属于不同的类别或同种型。有五类免疫球蛋白:iga、igd、ige、igg和igm,分别具有命名为α、δ、ε、γ和μ的重链。γ和α类根据ch序列和功能的相对较小的差异被进一步分成子类,例如,人表达以下子类:igg1、igg2、igg3、igg4、iga1和iga2。igg1抗体可以多种被称为同种异型的多态性变体存在(在jefferis和lefranc2009.mabs第1卷第4期1-7中有综述),其中的任一者都适用于本发明。人群中常见的同种异型变体是由字母a、f、n、z命名的那些。
“分离的”抗体是已经从其产生环境的组分中(例如,天然或重组地)确认、分离和/或回收的抗体。在一些实施方案中,分离的多肽不与来自其产生环境的所有其它组分缔合。其产生环境的污染组分如来源于重组转染细胞的污染组分是通常会干扰抗体的研究、诊断或治疗用途的物质,并且可包括酶、激素及其它蛋白质或非蛋白质溶质。在一些实施方案中,多肽被纯化:(1)至大于95重量%的抗体,如通过例如lowry方法测定,并且在一些实施方案中纯化至大于99重量%;(1)至足以通过使用旋杯测序仪获得至少15个残基的n末端或内部氨基酸序列的程度,或(3)使用考马斯蓝或银染色在非还原或还原条件下通过sds-page达到同质性。分离的抗体包括重组细胞内原位的抗体,因为抗体的天然环境的至少一种组分将不存在。然而,通常通过至少一个纯化步骤制备分离的多肽或抗体。
如本文所用的术语“单克隆抗体”是指获自基本上同质的抗体群体的抗体,即构成该群体的个别抗体是相同的,除了可能以少量存在的可能是天然存在的突变和/或翻译后修饰(例如,异构化、酰胺化)外。在一些实施方案中,单克隆抗体在重链和/或轻链处具有c末端切割。例如,1、2、3、4或5个氨基酸残基在重链和/或轻链的c末端被切割。在一些实施方案中,c末端切割从重链中移除了c末端赖氨酸。在一些实施方案中,单克隆抗体在重链和/或轻链处具有n末端切割。例如,1、2、3、4或5个氨基酸残基在重链和/或轻链的n末端被切割。在一些实施方案中,可通过重组技术制备截短形式的单克隆抗体。在一些实施方案中,单克隆抗体是高度特异性的,针对单个抗原位点。在一些实施方案中,单克隆抗体是高度特异性的,针对多个抗原位点(如双特异性抗体或多特异性抗体)。修饰语“单克隆”表示抗体的特征为获自基本上同质的抗体群体,并且不应被解释为需要通过任何特定的方法产生抗体。例如,可通过多种技术制备根据本发明使用的单克隆抗体,包括例如杂交瘤方法、重组dna方法、噬菌体展示技术和在具有部分或全部人免疫球蛋白基因座或编码人免疫球蛋白序列的基因的动物中产生人或人样抗体的技术。
术语“全长抗体”、“完整抗体”或“全抗体”可互换使用,指基本上完整形式的抗体,而不是抗体片段。具体地,全抗体包括具有包括fc区的重链和轻链的那些。恒定结构域可以是天然序列恒定结构域(例如,人天然序列恒定结构域)或其氨基酸序列变体。在一些情况下,完整抗体可具有一种或多种效应子功能。
“抗体片段”包含完整抗体的一部分,如完整抗体的抗原结合区和/或可变区,和/或完整抗体的恒定区。抗体片段的实例包括抗体的fc区、fc区的一部分或抗体的包含fc区的一部分。抗原结合抗体片段的实例包括域抗体(dab)、fab、fab′、f(ab′)2和fv片段;双抗体;线性抗体(参见5,641,870号美国专利,实施例2;zapata等人,proteineng.8(10):1057-1062[1995]);单链抗体分子,和由抗体片段形成的多特异性抗体。单重链抗体或单轻链抗体可以被工程化,或者在重链的情况下,可分离自被工程化以产生单重链分子的骆驼科动物、鲨鱼、文库或小鼠。
抗体的木瓜蛋白酶消化产生两个相同的抗原结合片段,称为“fab”片段,和残余“fc”片段,这一名称反映了易于结晶的能力。fab片段由整个l链以及h链的可变区结构域(vh)和一条重链的第一恒定结构域(ch1)组成。每个fab片段就抗原结合而言是单价的,即其具有单个抗原结合位点。抗体的胃蛋白酶处理产生单个大f(ab′)2片段,其大致对应于具有不同抗原结合活性且仍然能够交联抗原的两个二硫键连接的fab片段。fab′片段与fab片段的不同之处在于在ch1结构域的羧基末端具有几个另外的残基,包括来自抗体铰链区的一个或多个半胱氨酸。fab′-sh在本文中是其中恒定结构域的半胱氨酸残基带有游离硫醇基团的fab′的名称。f(ab′)2抗体片段最初作为fab′片段对产生,在它们之间具有铰链半胱氨酸。抗体片段的其它化学偶联也是已知的。fc片段包含通过二硫键保持在一起的两条h链的羧基末端部分。抗体的效应子功能由fc区中的序列和聚糖决定,该区域也被见于某些类型的细胞的fc受体(fcr)识别。
术语“fc区”在本文中用于定义免疫球蛋白重链的c末端区域,包括天然序列fc区和变体fc区。尽管免疫球蛋白重链的fc区的边界可以变化,但人igg重链fc区通常被限定为从位置cys226或pro230的氨基酸残基延伸到其羧基末端。用于本发明抗体的合适的天然序列fc区包括人igg1、igg2、igg3和igg4。
术语“细胞因子”是指分泌的多肽或其活性片段或突变体,其调节细胞、特别是免疫系统的细胞的活性。细胞因子的实例包括例如趋化因子、干扰素、白介素、淋巴因子和肿瘤坏死因子。该术语涵盖任何细胞因子蛋白或其功能片段或变体。除另指出外,该术语涵盖来自任何脊椎动物来源、包括哺乳动物如灵长类动物(例如,人)和啮齿动物(例如,大鼠和小鼠)的任何天然细胞因子。该术语涵盖细胞因子的未加工形式以及由在细胞中加工产生的细胞因子的任何形式。该术语还涵盖细胞因子的天然存在的变体。该术语还涵盖细胞因子的非天然存在的变体,如截短、缺失、细胞因子与另一分子连接的形式以及由氨基酸序列的至少一个氨基酸改变(例如,通过取代、添加或缺失)引起的变体。在一些方面,与天然存在的细胞因子多肽相比,变体或同源物在整个序列或序列的一部分(例如,50、100、125或150或更多个连续氨基酸部分)上具有至少90%、95%、96%、97%、98%、99%或100%氨基酸序列同一性。
如本文所用的术语“il-2”或“il-2多肽”是指任何白介素-2(il-2)蛋白或其功能片段或变体。除另指出外,该术语涵盖来自任何脊椎动物来源、包括哺乳动物如灵长类动物(例如,人)和啮齿动物(例如,大鼠和小鼠)的任何天然il-2。该术语涵盖未加工的il-2(例如,由氨基酸残基1-153组成的全长前体形式的il-2)以及由在细胞中加工产生的任何形式的il-2(例如,由氨基酸残基21-153组成的成熟形式的il-2)。如此,该术语涵盖由seqidno:160的氨基酸序列及其序列变体编码的蛋白质。该术语还涵盖il-2的天然存在的变体。该术语还涵盖il-2的非天然存在的变体,如截短、缺失、il-2与另一分子连接的形式以及由氨基酸序列的至少一个氨基酸改变(例如,通过取代、添加或缺失)引起的变体。在一些方面,与天然存在的il-2多肽如由seqidno:159或160的氨基酸序列编码的il-2多肽相比,变体或同源物在整个序列或序列的一部分(例如,50、100或133个连续氨基酸部分)上具有至少90%、95%、96%、97%、98%、99%或100%氨基酸序列同一性。如此,术语“il-2”或“il-2多肽”包括包含seqidno:1-8、159、160、230、243-251、260、775-792和813-822中的任一者的氨基酸序列的il-2蛋白,包括其变体,如通过对seqidno:1-8、159、160、230、243-251、260、775-792和813-822中的任一者的氨基酸序列进行一个或多个氨基酸取代而产生的变体。
如本文所用的术语“il-15”或“il-15多肽”是指任何白介素-15(il-15)蛋白或其功能片段或变体。除另指出外,该术语涵盖来自任何脊椎动物来源、包括哺乳动物如灵长类动物(例如,人)和啮齿动物(例如,大鼠和小鼠)的任何天然il-15。该术语涵盖未加工的il-15(例如,由氨基酸残基1-162组成的全长前体形式的il-15)以及由在细胞中加工产生的任何形式的il-15(例如,由氨基酸残基49-162组成的成熟形式的il-15)。如此,该术语涵盖由seqidno:167的氨基酸序列及其序列变体编码的蛋白质。该术语还涵盖il-15的天然存在的变体。该术语还涵盖il-15的非天然存在的变体,如截短、缺失、il-15与另一分子连接的形式以及由氨基酸序列的至少一个氨基酸改变(例如,通过取代、添加或缺失)引起的变体。在一些方面,与天然存在的il-15多肽如由seqidno:166或167的氨基酸序列编码的il-15多肽相比,变体或同源物在整个序列或序列的一部分(例如,50、100或114个连续氨基酸部分)上具有至少90%、95%、96%、97%、98%、99%或100%氨基酸序列同一性。如此,术语“il-15”或“il-15多肽”包括包含seqidno:166或167的氨基酸序列的il-15蛋白,包括其变体,如通过对seqidno:166或167的氨基酸序列进行一个或多个氨基酸取代而产生的变体。
细胞因子的“功能片段”包含全长细胞因子蛋白的一部分,其保持或具有改善的细胞因子受体结合能力(例如,与全长细胞因子蛋白相比在至少50%、80%、90%、95%、96%、97%、98%、99%或100%活性内)。全长细胞因子蛋白可以是野生型细胞因子蛋白的全长细胞因子蛋白,或者其可以是细胞因子蛋白的修饰变体的全长细胞因子蛋白,如通过一个或多个氨基酸取代修饰的全长细胞因子。细胞因子受体结合能力可例如通过细胞因子与细胞因子的同源受体或其组分(例如,异源三聚体受体复合物的一条或多条链)结合的能力来显示。如本文所用,“全长”可指呈其未加工(即,前体)形式或其加工(即,成熟)形式的细胞因子的全长。该术语还涵盖全长蛋白的一部分,其保持或具有改善的细胞因子受体结合能力(例如,与全长细胞因子蛋白相比在至少50%、80%、90%、95%、96%、97%、98%、99%或100%活性内),并且已被进一步修饰成包括对氨基酸序列的一个或多个修饰,如一个或多个氨基酸缺失、添加或取代。因此,细胞因子的功能片段不仅涵盖全长细胞因子蛋白的一部分,而且还涵盖全长细胞因子蛋白的一部分的变体。例如,il-2多肽的功能片段包含全长il-2蛋白的一部分,其保持或具有改善的il-2r结合能力(例如,与全长野生型il-2相比在至少50%、80%、90%、95%、96%、97%、98%、99%或100%活性内)。il-2r结合能力可例如通过单独或彼此组合地与il-2r的il-2rα链、il-2rβ链和/或il-2rγ链结合的能力来显示。il-2的功能片段包括例如包含seqidno:159的全长il-2序列的氨基酸残基21-153的il-2蛋白以及其变体,如包括对氨基酸序列的一个或多个取代的变体。如此,il-2的功能片段包括例如包含seqidno:1-8、160、230、243-251、260、775-792和813-822中的任一者的氨基酸序列的il-2蛋白。il-15的功能片段包括例如包含seqidno:167的氨基酸序列的il-15蛋白。
如本文用于描述任何细胞因子或其功能片段的术语“可激活的”意指细胞因子或其功能片段已经被修饰成包含掩蔽部分,并且在一些实施方案中包含允许在优选环境中激活细胞因子或其功能片段的其它组分。例如,已经被修饰成包含用于在优选环境中激活的掩蔽部分的细胞因子或其功能片段在本文中可以被称为“可激活的细胞因子”或“掩蔽型细胞因子”或“可激活的掩蔽型细胞因子”。如此,术语“掩蔽型(masked)细胞因子”包括已经被修饰成包含掩蔽部分,并且在一些实施方案中包含允许在优选环境中激活细胞因子或其功能片段的其它组分如可切割肽的任何细胞因子或其功能片段。
如本文所用的术语“掩蔽部分”是指这样的肽,其能够与细胞因子或其功能片段结合或以其它方式表现出对细胞因子或其功能片段的亲和力,使得掩蔽部分阻断、封闭、抑制(例如,降低)或以其它方式阻止(例如,掩蔽)细胞因子或其功能片段的活性或与其同源受体或蛋白质的结合。在一些实施方案中,掩蔽部分是细胞因子受体或其亚基或功能片段。
如本文所用的术语“细胞因子受体”是指本领域范围内与一种或多种细胞因子结合的任何受体,包括但不限于il-1、il-2、il-3、il-4、il-5、il-6、il-7、il-8、il-9、il-10、il-11、il-12、il-13、il-14、il-15、il-16、il-17、il-18、il-19、il-20、il-21、il-22、il-23、il-24、il-25、il-26、il-27、il-28a、il-28b、il-29、il-30、il-31、il-32、il-33、il-34、il-35、il-36、il-37、粒细胞-巨噬细胞集落刺激因子(gm-csf)、巨噬细胞集落刺激因子(m-csf)、肿瘤坏死因子α(tnf-α)、转化生长因子β(tgf-β)、ifn-γ(伽玛)、cd252、cd154、cd178、cd70、cd153、4-1bb-l、trail、rankl、apo3l、cd256、cd257、cd258、tl1、aitrl、eda1、干扰素(ifn)-α(阿尔法)、ifn-β(贝塔)、ifn-γ(伽玛)、生长激素(gh)、促红细胞生成素(epo)、促乳素(prl)、白血病抑制因子(lif)、制瘤素(osm)和促血小板生成素(tpo)的受体。一些细胞因子受体整体或部分地作为一个以上亚基的异源聚合复合物或作为同源聚合复合物起作用。该术语还涵盖单独或者当与一种或多种其它细胞因子受体亚基复合时(例如,作为异源聚合或同源聚合复合物)能够与一种或多种细胞因子结合的细胞因子受体的亚基。如此,提到作为例如三个亚基的异源聚合复合物的“细胞因子受体”包括提到包含所有三个亚基的异源聚合复合物以及提到单独或彼此各种组合的每个亚基。细胞因子受体的非限制性实例包括cxcr1、cxcr2、cxcr3、cxcr4、cxcr5、cxcr6、cxcr7、ccr1、ccr2、ccr3、ccr4、ccr5、ccr6、ccr7、ccr8、ccr9、ccr10、ccr11、xcr1、cx3cr1、il-1rap、il-1rapl1、il-1rapl2、il-1rl1、il-1rl2、il-1r1、il-1r2、il-2r、il-2rα、il-2rβ、il-2rγ、il-3rα、il-4r、il-5rα、il-6r、il-6st、il-7r、il-9r、il-10rα、il-10rβ、il-11rα、il-12rβ1、il-12rβ2、il-13rα1、il-13rα2、il-15rα、il-17ra、il-17rb、il-17rc、il-17rd、il-17re、il-18rap、il-18r1、il-20rα、il-20rβ、il-21r、il-22rα1、il-22rα2、il-23r、il-27rα、il-28rα、il-31ra、ifnar1、ifnar2、ifngr1、ifngr2、ifnlr1、gmrα(cd116)、cd131、ghr、prlr、epor、lifr(cd118)、osmrβ、tpo-r(cd110)、csf-1r、edar、tnfrsf1a、tnfrsf1b、ltbr、tnfrsf4、cd40、fas、tnfrsf6b、cd27、tnfrsf8、tnfrsf9、tnfrsf10a、tnfrsf10b、tnfrsf10c、tnfrsf10d、tnfrsf11a、tnfrsf11b、tnfrsf12a、tnfrsf13b、tnfrsf13c、tnfrsf14、ngfr、tnfrsf17、tnfrsf18、tnfrsf19、relt、tnfrsf21、tnfrsf25和eda2r。
如本文所用的术语“il-2r”或“il-2受体”或“il-2细胞因子受体”是指包含三条分开且非共价连接的链的高亲和力il-2受体复合物:il-2rα链(也称为cd25)、il-2rβ链(也称为cd122)和il-2rγ链(也称为cd132)。il-2能够与il-2rα链结合。il-2还能够与同il-2rβ链组合的il-2rα链结合。il-2还能够以最高的亲和力与同il-2rβ和il-2rγ链组合的il-2rα链结合。在一些情况下,该术语还涵盖il-2rα链、il-2rβ链或il-2rγ链或其组合。
如本文所用的术语“il-15r”或“il-15受体”或“il-15细胞因子受体”是指包含三条分开且非共价连接的链的高亲和力il-15受体复合物:il-15rα链、il-2rβ链和il-2rγ链。il-15能够与il-15rα链、il-2rβ链和il-2rγ链的异源二聚体以及同il-2rβ链和il-2rγ链组合的il-15ra链结合。在一些情况下,该术语还涵盖il-15rα链、il-2rβ链或il-2rγ链或其组合。
术语“半衰期延长结构域”是指为了延长靶组分在血清中的半衰期而与靶组分(例如,细胞因子或其功能片段或掩蔽部分)连接的结构域。术语“半衰期延长结构域”涵盖例如抗体、抗体片段、双特异性抗体、白蛋白、结合蛋白(例如,白蛋白结合蛋白和igg结合蛋白)、聚氨基酸序列和抗体衍生物(例如,scfv、scfc、双可变结构域和基于crossmab方法的抗体衍生物)。
相对于参考多肽序列的“氨基酸序列同一性百分比(%)”定义为在比对序列,并且必要时引入缺口以实现最大序列同一性百分比后,而且不考虑任何保守取代作为序列同一性的一部分,在候选序列中与参考多肽序列中的氨基酸残基相同的氨基酸残基的百分比。可以本领域技术人员已知的各种方式实现用于确定氨基酸序列同一性百分比的比对,例如使用公众可获得的计算机软件,如blast、blast-2、align或megalign(dnastar)软件。本领域技术人员可确定用于比对序列的适当参数,包括在被比较的序列的全长上实现最大比对所需的任何算法。例如,给定氨基酸序列a与、同或针对给定氨基酸序列b的氨基酸序列同一性%(其可替代地表述为给定氨基酸序列a具有或包含与、同或针对给定氨基酸序列b的特定氨基酸序列同一性%)计算如下:
100乘以分数x/y
其中x是在该程序的a和b的比对中评分为序列相同匹配的氨基酸残基数,且其中y是b中氨基酸残基的总数。将要理解的是,在氨基酸序列a的长度不等于氨基酸序列b的长度的情况下,a与b的氨基酸序列同一性%将不等于b与a的氨基酸序列同一性%。
抗体“效应子功能”是指可归因于抗体的fc区(天然序列fc区或氨基酸序列变体fc区)并且随抗体同种型而变化的那些生物活性。抗体效应子功能的实例包括:c1q结合和补体依赖性细胞毒性;fc受体结合;抗体依赖性细胞介导的细胞毒性(adcc);吞噬作用;细胞表面受体(例如,b细胞受体)的下调;和b细胞激活。
如本文所用的“结合亲和力”是指分子(例如,细胞因子)的单个结合位点与其结合伴侣(例如,细胞因子受体)之间的非共价相互作用的强度。在一些实施方案中,结合蛋白(例如,细胞因子)的亲和力通常可由解离常数(kd)表示。可通过本领域中已知的常用方法测量亲和力,包括本文所述的方法。
编码本文所述的细胞因子多肽的“分离的”核酸分子是从至少一种污染核酸分子中确认和分离的核酸分子,其通常在其所产生的环境中与所述污染核酸分子缔合。在一些实施方案中,分离的核酸不与同产生环境相关的所有组分缔合。编码本文的多肽和细胞因子多肽的分离的核酸分子的形式不同于其所见的天然形式或环境。因此分离的核酸分子与编码本文天然存在于细胞中的多肽和细胞因子多肽的核酸有区别。
术语“药物制剂”是指这样的制剂,其形式允许活性成分的生物活性是有效的,并且不含对将施用制剂的受试者具有不可接受的毒性的另外的组分。这类制剂是无菌的。
如本文所用的“载体”包括药学上可接受的载体、赋形剂或稳定剂,它们在所用的剂量和浓度下对暴露于其的细胞或哺乳动物无毒。通常生理上可接受的载体是ph缓冲水溶液。生理上可接受的载体的实例包括缓冲剂,如磷酸盐、柠檬酸盐及其它有机酸;抗氧化剂,包括抗坏血酸;低分子量(小于约10个残基)多肽;蛋白质,如血清白蛋白、明胶或免疫球蛋白;亲水性聚合物,如聚乙烯吡咯烷酮;氨基酸,如甘氨酸、谷氨酰胺、天冬酰胺、精氨酸或赖氨酸;单糖、二糖及其它碳水化合物,包括葡萄糖、甘露糖或糊精;螯合剂,如edta;糖醇,如甘露糖醇或山梨糖醇;成盐抗衡离子,如钠;和/或非离子表面活性剂,如tweentm、聚乙二醇(peg)和pluronicstm。
如本文所用,术语“治疗”是指设计成在临床病理学过程中改变所治疗的个体或细胞的自然过程的临床干预。理想的治疗效果包括降低疾病进展的速率、减轻或缓和疾病状态以及缓解或改善预后。如果例如与病症(例如,肿瘤性疾病)相关的一种或多种症状减轻或消除,则个体被成功地“治疗”。例如,如果治疗导致患有疾病的患者的生活质量提高、治疗疾病所需的其它用药的剂量减少、疾病复发的频率降低、疾病的严重程度减轻,疾病的发生或进展延迟和/或个体的生存期延长,则个体被成功地“治疗”。
如本文所用,“与......结合”或“与......组合”是指施用一种治疗形式加之另一种治疗形式。如此,“与......结合”或“与......组合”是指对个体施用一种治疗形式是在施用其它治疗形式之前、期间或之后。
如本文所用,术语“预防”包括针对个体中疾病的发生或复发提供预防。个体可能倾向于患、易患病症或者有发生病症的风险,但尚未被诊断患有所述病症。在一些实施方案中,本文所述的掩蔽型细胞因子用于延迟病症的发展。
如本文所用,有发生病症的“风险”的个体可能具有或可能不具有可检测的疾病或疾病症状,并且在本文所述的治疗方法之前可能显示或可能未显示可检测的疾病或疾病症状。“有风险”表示个体具有一种或多种风险因素,其是如本领域中已知的与疾病的发展关联的可测量参数。具有这些风险因素中的一者或多者的个体比没有这些风险因素中的一者或多者的个体发生病症的可能性更高。
“有效量”是指至少在剂量和持续时间段上有效实现所需或指示的效果(包括治疗或预防结果)所必需的量。可在一次或多次施用中提供有效量。“治疗有效量”是至少实现特定病症的可测量的改善所需的最小浓度。本文的治疗有效量可根据诸如患者的疾病状态、年龄、性别和体重以及抗体在个体中引发所需反应的能力等因素而变化。治疗有效量也可以是治疗有益效果超过掩蔽型细胞因子的任何毒性或有害效果的量。“预防有效量”是指在剂量和持续时间段上有效实现所需预防结果所必需的量。典型但不是必须地,因为受试者在疾病之前或疾病的早期阶段使用预防剂量,所以预防有效量可小于治疗有效量。
“慢性”施用是指以连续而非急性模式施用药物,以便持续延长的时间段维持初始治疗效果(活性)。“间歇”施用不是没有中断而连续进行的治疗,实际上是周期性进行的治疗。
如本文所用,“个体”或“受试者”是哺乳动物。用于治疗目的的“哺乳动物”包括人、家养和农场动物,以及动物园动物、竞技动物或宠物动物,如狗、马、兔、牛、猪、仓鼠、沙鼠、小鼠、雪貂、大鼠、猫等。在一些实施方案中,个体或受试者是人。
vii.示例性实施方案
在所提供的实施方案中有:
1.一种掩蔽型细胞因子,其包含:
a)掩蔽部分;和
b)细胞因子或其功能片段,
其中掩蔽部分经由第一接头与细胞因子或其功能片段连接。
2.实施方案1的掩蔽型细胞因子,其进一步包含与掩蔽部分或细胞因子或其功能片段连接的半衰期延长结构域。
3.实施方案2的掩蔽型细胞因子,其中半衰期延长结构域经由第二接头与掩蔽部分或细胞因子或其功能片段连接。
4.实施方案2或实施方案3的掩蔽型细胞因子,其中:
i)掩蔽型细胞因子在n至c末端或在c至n末端方向上包含:a)掩蔽部分;b)第一接头;c)细胞因子或其功能片段;和d)半衰期延长结构域;
ii)掩蔽型细胞因子在n至c末端或在c至n末端方向上包含:a)掩蔽部分;b)第一接头;c)细胞因子或其功能片段;d)第二接头;和e)半衰期延长结构域;
iii)掩蔽型细胞因子在n至c末端或在c至n末端方向上包含:a)细胞因子或其功能片段;b)第一接头;c)掩蔽部分;和d)半衰期延长结构域;或
iv)掩蔽型细胞因子在n至c末端或在c至n末端方向上包含:a)细胞因子或其功能片段;b)第一接头;c)掩蔽部分;d)第二接头;和e)半衰期延长结构域。
5.实施方案1-4中任一项的掩蔽型细胞因子,其中细胞因子或其功能片段是il-2多肽或其功能片段。
6.实施方案5的掩蔽型细胞因子,其中il-2多肽或其功能片段包含选自由seqidno:1-8、160、230、243-251、260、775-792和813-822组成的组的氨基酸序列。
7.实施方案5的掩蔽型细胞因子,其中il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入降低il-2多肽或其功能片段对cd25(il-2rα)的亲和力的一个或多个氨基酸取代而产生的氨基酸序列。
8.实施方案7的掩蔽型细胞因子,其中氨基酸序列是通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代中的一者或多者产生的:r38a、f42a、f42k、f42e、k43a、y45a、y45n、y45r、e62a、e62r、e62s和l72g。
9.实施方案5的掩蔽型细胞因子,其中il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代而产生的氨基酸序列。
10.实施方案9的掩蔽型细胞因子,其中氨基酸序列是通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代中的一者或多者产生的:h16i、l18c、d20a、d20l、d20f、n29l、l80f、r81d、l85v、i86v和i92f。
11.实施方案7或实施方案8的掩蔽型细胞因子,其中氨基酸序列是通过进一步引入增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代产生的。
12.实施方案11的掩蔽型细胞因子,其中增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代选自由h16i、l18c、d20a、d20l、d20f、n29l、l80f、r81d、l85v、i86v和i92f组成的组。
13.实施方案5的掩蔽型细胞因子,其中il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入稳定il-2多肽或其功能片段的一个或多个氨基酸取代而产生的氨基酸序列。
14.实施方案13的掩蔽型细胞因子,其中氨基酸序列是通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代之一产生的:c125s、c125a和c125g。
15.实施方案7-12中任一项的掩蔽型细胞因子,其中氨基酸序列是通过进一步引入稳定il-2多肽或其功能片段的一个或多个氨基酸取代产生的。
16.实施方案15的掩蔽型细胞因子,其中稳定il-2多肽或其功能片段的一个或多个氨基酸取代是氨基酸取代c125s、c125a或c125g。
17.实施方案5-16中任一项的掩蔽型细胞因子,其中掩蔽部分包含选自由seqidno:9、10、161-165、187-218、221-229、231、261、826和827组成的组的氨基酸序列。
18.实施方案1-4中任一项的掩蔽型细胞因子,其中细胞因子或其功能片段是il-15多肽或其功能片段。
19.实施方案18的掩蔽型细胞因子,其中il-15多肽或其功能片段包含seqidno:167的氨基酸序列。
20.实施方案18或实施方案19的掩蔽型细胞因子,其中掩蔽部分包含选自由seqidno:10、161-165、219-229、232-234、261和823-827组成的组的氨基酸序列。
21.实施方案18或实施方案19的掩蔽型细胞因子,其中掩蔽部分包含通过向seqidno:232-234和823-825中的任一者的氨基酸序列中引入以下氨基酸取代中的一者或多者而产生的氨基酸序列:r24a、r26a、k34a、s40a、l42a和p67a。
22.实施方案2-21中任一项的掩蔽型细胞因子,其中半衰期延长结构域是抗体或其片段。
23.实施方案22的掩蔽型细胞因子,其中抗体或其片段包含重链多肽或轻链多肽。
24.实施方案23的掩蔽型细胞因子,其中重链多肽包含选自由seqidno:158、168和169组成的组的氨基酸序列。
25.实施方案23的掩蔽型细胞因子,其中重链多肽包含改变效应子功能的一个或多个氨基酸取代。
26.实施方案25的掩蔽型细胞因子,其中重链多肽:
a)是igg1重链多肽,并且包含(多个)氨基酸取代:
i)n297a、n297g或n297q;
ii)l234a和l235a;
iii)c220s、c226s、c229s和p238s;
iv)c226s、c229s、e233p、l234v和l235a;
v)l234f、l235e和p331s;
vi)s267e和l328f;
vii)d265a;
viii)l234a、l235a和p329g;
b)是igg2重链多肽,并且包含(多个)氨基酸取代:
i)v234a和g237a;
ii)h268q、v309l、a330s和a331s;或
iii)v234a、g237a、p238s、h268a、v309l、a330s和p331s;或
e)是igg4重链多肽,并且包含(多个)氨基酸取代:
i)l235a、g237a和e318a;
ii)s228p、l234a和l235a;
iii)h268q、v309l、a330s和p331s;或
iv)s228p和l235a,根据kabateu编号系统编号。
27.实施方案25的掩蔽型细胞因子,其中重链多肽包含增强效应子功能的一个或多个氨基酸取代。
28.实施方案27的掩蔽型细胞因子,其中重链多肽是igg1重链多肽,并且包含(多个)氨基酸取代:
a)s298a、e333a和k334a;
b)s239d和i332e;
c)s239d、a330l和i332e;
d)p247i和a339d或a339q;
e)d280h和k290s;
f)d280h、k290s和s298d或s298v;
g)f243l、r292p和y300l;
h)f243l、r292p、y300l和p396l;
i)f243l、r292p、y300l、v305i和p396l;
j)g236a、s239d和i332e;
k)k326a和e333a;
l)k326w和e333s;
m)k290e、s298g和t299a;
n)k290e、s298g、t299a和k326e;
o)k290n、s298g和t299a;
p)k290n、s298g、t299a和k326e;
q)k334v;
r)l235s、s239d和k334v;
s)k334v和q331m、s239d、f243v、e294l或s298t;
t)e233l、q311m和k334v;
u)l234i、q311m和k334v;
v)k334v和s298t、a330m或a330f;
w)k334v、q311m和a330m或a330f;
x)k334v、s298t和a330m或a330f;
y)k334v、s239d和a330m或s298t;
z)l234y、y296w和k290y、f243v或e294l;
aa)y296w和l234y或k290y;
ab)s239d、a330s和i332e,
ac)v264i;
ad)f243l和v264i;
ae)l328m;
af)i332e;
ag)l328m和i332e;
ah)v264i和i332e;
ai)s239e和i332e;
aj)s239q和i332e;
ak)s239e;
al)a330y;
am)i332d;
an)l328i和i332e;
ao)l328q和i332e;
ap)v264t;
aq)v240i;
ar)v266i;
as)s239d;
at)s239d和i332d;
au)s239d和i332n;
av)s239d和i332q;
aw)s239e和i332d;
ax)s239e和i332n;
ay)s239e和i332q;
az)s239n和i332d;
ba)s239n和i332e;
bb)s239q和i332d;
bc)a330y和i332e;
bd)v264i、a330y和i332e;
be)a330l和i332e;
bf)v264i、a330l和i332e;
bg)l234e、l234y或l234i;
bh)l235d、l235s、l235y或l235i;
bi)s239t;
bj)v240m;
bk)v264y;
bl)a330i;
bm)n325t;
bn)i332e和l328d、l328v、l328t或l328i;
bo)v264i、i332e和s239e或s239q;
bp)s239e、v264i、a330y和i332e;
bq)a330y、i332e和s239d或s239n;
br)a330l、i332e和s239d或s239n;
bs)v264i、s298a和i332e;
bt)s298a、i332e和s239d或s239n;
bu)s239d、v264i和i332e;
bv)s239d、v264i、s298a和i332e;
bw)s239d、v264i、a330l和i332e;
bx)s239d、i332e和a330i;
by)p230a;
bz)p230a、e233d和i332e;
ca)e272y;
cb)k274t、k274e、k274r、k274l或k274y;
cd)f275w;
ce)n276l;
cf)y278t;
cg)v302i;
ch)e318r;
ci)s324d、s324i或s324v;
cj)k326i或k326t;
ck)t335d、t335r或t335y;
cl)v240i和v266i;
cm)s239d、a330y、i332e和l234i;
cn)s239d、a330y、i332e和l235d;
co)s239d、a330y、i332e和v240i;
cp)s239d、a330y、i332e和v264t;或
cq)s239d、a330y、i332e和k326e或k326t,根据kabateu编号系统编号。
29.实施方案23的掩蔽型细胞因子,其中轻链多肽包含seqidno:157或170的氨基酸序列。
30.实施方案22的掩蔽型细胞因子,其中抗体或其片段是片段可结晶结构域(fc结构域)或其片段。
31.实施方案30的掩蔽型细胞因子,其中fc结构域或其片段包含改变效应子功能的一个或多个氨基酸取代。
32.实施方案31的掩蔽型细胞因子,其中fc结构域或其功能片段:
a)是igg1fc结构域或其功能片段,并且包含(多个)氨基酸取代:
i)n297a、n297g或n297q;
ii)l234a和l235a;
iii)c220s、c226s、c229s和p238s;
iv)c226s、c229s、e233p、l234v和l235a;
v)l234f、l235e和p331s;
vi)s267e和l328f;
vii)d265a;
viii)l234a、l235a和p329g;
b)是igg2fc结构域或其功能片段,并且包含(多个)氨基酸取代:
i)v234a和g237a;
ii)h268q、v309l、a330s和a331s;或
iii)v234a、g237a、p238s、h268a、v309l、a330s和p331s;或
e)是igg4fc结构域或其功能片段,并且包含(多个)氨基酸取代:
i)l235a、g237a和e318a;
ii)s228p、l234a和l235a;
iii)h268q、v309l、a330s和p331s;或
iv)s228p和l235a,根据kabateu编号系统编号。
33.实施方案31的掩蔽型细胞因子,其中fc结构域或其功能片段包含增强效应子功能的一个或多个氨基酸取代。
34.实施方案33的掩蔽型细胞因子,其中fc结构域或其功能片段是igg1fc结构域或其功能片段,并且包含(多个)氨基酸取代:
a)s298a、e333a和k334a;
b)s239d和i332e;
c)s239d、a330l和i332e;
d)p247i和a339d或a339q;
e)d280h和k290s;
f)d280h、k290s和s298d或s298v;
g)f243l、r292p和y300l;
h)f243l、r292p、y300l和p396l;
i)f243l、r292p、y300l、v305i和p396l;
j)g236a、s239d和1332e;
k)k326a和e333a;
l)k326w和e333s;
m)k290e、s298g和t299a;
n)k290e、s298g、t299a和k326e;
o)k290n、s298g和t299a;
p)k290n、s298g、t299a和k326e;
q)k334v;
r)l235s、s239d和k334v;
s)k334v和q331m、s239d、f243v、e294l或s298t;
t)e233l、q311m和k334v;
u)l234i、q311m和k334v;
v)k334v和s298t、a330m或a330f;
w)k334v、q311m和a330m或a330f;
x)k334v、s298t和a330m或a330f;
y)k334v、s239d和a330m或s298t;
z)l234y、y296w和k290y、f243v或e294l;
aa)y296w和l234y或k290y;
ab)s239d、a330s和i332e,
ac)v264i;
ad)f243l和v264i;
ae)l328m;
af)i332e;
ag)l328m和i332e;
ah)v264i和i332e;
ai)s239e和i332e;
aj)s239q和i332e;
ak)s239e;
al)a330y;
am)i332d;
an)l328i和i332e;
ao)l328q和i332e;
ap)v264t;
aq)v240i;
ar)v266i;
as)s239d;
at)s239d和i332d;
au)s239d和i332n;
av)s239d和i332q;
aw)s239e和i332d;
ax)s239e和i332n;
ay)s239e和i332q;
az)s239n和i332d;
ba)s239n和i332e;
bb)s239q和i332d;
bc)a330y和i332e;
bd)v264i、a330y和i332e;
be)a330l和i332e;
bf)v264i、a330l和i332e;
bg)l234e、l234y或l234i;
bh)l235d、l235s、l235y或l235i;
bi)s239t;
bj)v240m;
bk)v264y;
bl)a330i;
bm)n325t;
bn)i332e和l328d、l328v、l328t或l328i;
bo)v264i、i332e和s239e或s239q;
bp)s239e、v264i、a330y和i332e;
bq)a330y、i332e和s239d或s239n;
br)a330l、i332e和s239d或s239n;
bs)v264i、s298a和i332e;
bt)s298a、i332e和s239d或s239n;
bu)s239d、v264i和i332e;
bv)s239d、v264i、s298a和i332e;
bw)s239d、v264i、a330l和1332e;
bx)s239d、i332e和a330i;
by)p230a;
bz)p230a、e233d和i332e;
ca)e272y;
cb)k274t、k274e、k274r、k274l或k274y;
cd)f275w;
ce)n276l;
cf)y278t;
cg)v302i;
ch)e318r;
ci)s324d、s324i或s324v;
cj)k326i或k326t;
ck)t335d、t335r或t335y;
cl)v240i和v266i;
cm)s239d、a330y、1332e和l234i;
cn)s239d、a330y、i332e和l235d;
co)s239d、a330y、i332e和v240i;
cp)s239d、a330y、i332e和v264t;或
cq)s239d、a330y、i332e和k326e或k326t,根据kabateu编号系统编号。
35.实施方案30-32中任一项的掩蔽型细胞因子,其中fc结构域或其片段包含seqidno:154的氨基酸序列。
36.实施方案2-21中任一项的掩蔽型细胞因子,其中半衰期延长结构域是白蛋白多肽或其片段。
37.实施方案36的掩蔽型细胞因子,其中自蛋白多肽或其片段包含seqidno:171的氨基酸序列。
38.实施方案2-21中任一项的掩蔽型细胞因子,其中半衰期延长结构域是白蛋白结合蛋白或其片段。
39.实施方案38的掩蔽型细胞因子,其中自蛋白结合蛋白或其片段包含选自由seqidno:172-174和252-259组成的组的氨基酸序列。
40.实施方案2-21中任一项的掩蔽型细胞因子,其中半衰期延长结构域是igg结合蛋白或其片段。
41.实施方案40的掩蔽型细胞因子,其中igg结合蛋白或其功能片段包含选自由seqidno:175-186组成的组的氨基酸序列。
42.实施方案2-21中任一项的掩蔽型细胞因子,其中半衰期延长结构域是聚氨基酸序列。
43.实施方案42的掩蔽型细胞因子,其中聚氨基酸序列是pas多肽或xten多肽。
44.实施方案43的掩蔽型细胞因子,其中pas多肽包含至少25、至少50、至少100、至少150、至少200、至少250、至少300、至少400、至少500、至少600、至少700、至少800、至少900、至少1000、至少1100、至少1200、至少1300、至少1500、至少2000、至少2500或至少3000个氨基酸残基,其中每个氨基酸残基是脯氨酸或丙氨酸残基。
45.实施方案43的掩蔽型细胞因子,其中pas多肽包含至少25、至少50、至少100、至少150、至少200、至少250、至少300、至少400、至少500、至少600、至少700、至少800、至少900、至少1000、至少1100、至少1200、至少1300、至少1500、至少2000、至少2500或至少3000个氨基酸残基,其中每个氨基酸残基选自由脯氨酸、丙氨酸和丝氨酸残基组成的组。
46.实施方案43的掩蔽型细胞因子,其中xten多肽包含约25至约500、约200至约1000、约500至约1500、约1000至约2000或约1500至约3000个氨基酸残基的氨基酸序列,其中至少约70%、75%、80%或85%的氨基酸序列由非重叠序列基序组成,其中基序中的每一者具有5至100个氨基酸残基、5至50个氨基酸残基或9至36个氨基酸残基,且其中至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%或100%的基序中的每一者由选自由甘氨酸(g)、丙氨酸(a)、丝氨酸(s)、苏氨酸(t)、谷氨酸(e)和脯氨酸(p)组成的组的四种、五种或六种类型的氨基酸残基组成,且其中全长xten多肽中的任何一种氨基酸类型的含量不超过约40%、约35%、约30%、约25%、约15%、约10%或约8%。
47.实施方案1-46中任一项的掩蔽型细胞因子,其中掩蔽型细胞因子进一步包含与掩蔽型细胞因子连接的一条或多条peg聚合物链。
48.实施方案47的掩蔽型细胞因子,其中一条或多条peg聚合物链与细胞因子或其功能片段和/或半衰期延长结构域连接。
49.实施方案1-48中任一项的掩蔽型细胞因子,其中通过改变掩蔽型细胞因子的氨基酸序列,使得产生一个或多个另外的n连接的和/或o连接的糖基化位点,由此来修饰或进一步修饰掩蔽型细胞因子。
50.实施方案49的掩蔽型细胞因子,其中通过改变掩蔽型细胞因子的氨基酸序列,使得一个或多个另外的天冬酰胺-x-丝氨酸(n-x-s)和/或天冬酰胺-x-苏氨酸(n-x-t)三肽序列被引入到掩蔽型细胞因子的氨基酸序列中,由此修饰或进一步修饰掩蔽型细胞因子,其中x是除脯氨酸以外的任何氨基酸。
51.实施方案49或实施方案50的掩蔽型细胞因子,其中通过改变掩蔽型细胞因子的氨基酸序列,使得一个或多个另外的丝氨酸或苏氨酸残基被引入到掩蔽型细胞因子的氨基酸序列中,由此修饰或进一步修饰掩蔽型细胞因子。
52.实施方案1-51中任一项的掩蔽型细胞因子,其中第一接头包含第一可切割肽。
53.实施方案1-52中任一项的掩蔽型细胞因子,其中第一接头包含第一n末端间隔区结构域和/或第一c末端间隔区结构域。
54.实施方案53的掩蔽型细胞因子,其中第一接头包含:
a)第一n末端间隔区结构域、第一可切割肽和第一c末端间隔区结构域;
b)第一n末端间隔区结构域和第一可切割肽;
c)第一n末端间隔区结构域和第一c末端间隔区结构域;
d)第一可切割肽和第一c末端间隔区结构域;
e)第一n末端间隔区结构域;或
f)第一c末端间隔区结构域。
55.实施方案53或实施方案54的掩蔽型细胞因子,其中第一可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。
56.实施方案53-55中任一项的掩蔽型细胞因子,其中第一n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
57.实施方案53-55中任一项的掩蔽型细胞因子,其中第一c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
58.实施方案53或实施方案54的掩蔽型细胞因子,其中第一可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
59.实施方案58的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
60.实施方案1-59中任一项的掩蔽型细胞因子,其中第一接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列。
61.实施方案3-60中任一项的掩蔽型细胞因子,其中第二接头包含第二可切割肽。
62.实施方案3-61中任一项的掩蔽型细胞因子,其中第二接头包含第二n末端间隔区结构域和/或第二c末端间隔区结构域。
63.实施方案62的掩蔽型细胞因子,其中第二接头包含:
a)第二n末端间隔区结构域、第二可切割肽和第二个第一c末端间隔区结构域;
b)第二n末端间隔区结构域和第二可切割肽;
c)第二n末端间隔区结构域和第二c末端间隔区结构域;
d)第二可切割肽和第二c末端间隔区结构域;
e)第二n末端间隔区结构域;或
f)第二c末端间隔区结构域。
64.实施方案61-63中任一项的掩蔽型细胞因子,其中第二可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。
65.实施方案62-64中任一项的掩蔽型细胞因子,其中第二n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
66.实施方案62-65中任一项的掩蔽型细胞因子,其中第二c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
67.实施方案62或实施方案63的掩蔽型细胞因子,其中第二可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
68.实施方案67的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
69.实施方案3-68中任一项的掩蔽型细胞因子,其中第二接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列。
70.一种掩蔽型细胞因子,其包含:
a)第一掩蔽部分;
b)细胞因子或其功能片段,
其中第一掩蔽部分经由第一接头与细胞因子或其功能片段连接;和
c)第二掩蔽部分,
其中第二掩蔽部分经由第二接头与细胞因子或其功能片段连接。
71.实施方案70的掩蔽型细胞因子,其进一步包含与第一掩蔽部分或第二掩蔽部分连接的半衰期延长结构域。
72.实施方案71的掩蔽型细胞因子,其中半衰期延长结构域经由第三接头与第一掩蔽部分或第二掩蔽部分连接。
73.实施方案71或实施方案72的掩蔽型细胞因子,其中:
i)掩蔽型细胞因子在n至c末端或c至n末端方向上包含:a)第一掩蔽部分;b)第一接头;c)细胞因子或其功能片段;d)第二接头;e)第二掩蔽部分;和f)半衰期延长结构域;
ii)掩蔽型细胞因子在n至c末端或c至n末端方向上包含:a)第一掩蔽部分;b)第一接头;c)细胞因子或其功能片段;d)第二接头;e)第二掩蔽部分;f)第三接头;和g)半衰期延长结构域;
iii)掩蔽型细胞因子在n至c末端或c至n末端方向上包含:a)第二掩蔽部分;b)第二接头;c)细胞因子或其功能片段;d)第一接头;e)第一掩蔽部分;和f)半衰期延长结构域;或
iv)掩蔽型细胞因子在n至c末端或c至n末端方向上包含:a)第二掩蔽部分;b)第二接头;c)细胞因子或其功能片段;d)第一接头;e)第一掩蔽部分;f)第三接头;和g)半衰期延长结构域。
74.实施方案70-73中任一项的掩蔽型细胞因子,其中细胞因子或其功能片段是il-2多肽或其功能片段。
75.实施方案74的掩蔽型细胞因子,其中il-2多肽或其功能片段包含:
a)选自由seqidno:1-8、160、230、243-251、260、775-792和813-822组成的组的氨基酸序列;或
b)通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代中的一者或多者产生的氨基酸序列:h16i、l18c、d20a、d20l、d20f、n29l、r38a、f42a、f42k、f42e、f43a、y45a、y45n、y45r、e62a、e62r、e62s、l72g、l80f、r81d、l85v、i86v、i92f和c125s。
76.实施方案74或实施方案75的掩蔽型细胞因子,其中第一掩蔽部分包含选自由seqidno:9、10、161-165、187-218、221-229、231和261组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:9、10、161-165、187-218、221-229、231和261组成的组的氨基酸序列,且其中第一掩蔽部分和第二掩蔽部分的氨基酸序列不同。
77.实施方案74-76中任一项的掩蔽型细胞因子,其中:
a)第一掩蔽部分包含seqidno:9或231的氨基酸序列,且第二掩蔽部分包含选自由seqidno:10、161-165、187-218、221-226和261组成的组的氨基酸序列;或
b)第一掩蔽部分包含选自由seqidno:10、161-165、187-218、221-226和261组成的组的氨基酸序列,且第二掩蔽部分包含seqidno:9或231的氨基酸序列。
78.实施方案70-73中任一项的掩蔽型细胞因子,其中细胞因子或其功能片段是il-15多肽或其功能片段。
79.实施方案78的掩蔽型细胞因子,其中il-15多肽或其功能片段包含seqidno:167的氨基酸序列。
80.实施方案78或实施方案79的掩蔽型细胞因子,其中:
a)第一掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:10、161-165、219-229和261组成的组的氨基酸序列;
b)第一掩蔽部分包含选自由seqidno:10、161-165、219-229和261组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列;
c)第一掩蔽部分包含通过向seqidno:232-234和823-825中的任一者的氨基酸序列中引入以下氨基酸取代中的一者或多者而产生的氨基酸序列:r24a、r26a、k34a、s40a、l42a和p67a,且第二掩蔽部分包含选自由seqidno:10、161-165、219-229和261组成的组的氨基酸序列;或
d)第一掩蔽部分包含选自由seqidno:10、161-165、219-229和261组成的组的氨基酸序列,且第二掩蔽部分包含通过向seqidno:232-234和823-825中的任一者的氨基酸序列中引入以下氨基酸取代中的一者或多者而产生的氨基酸序列:r24a、r26a、k34a、s40a、l42a和p67a。
81.实施方案71-80中任一项的掩蔽型细胞因子,其中半衰期延长结构域是抗体或其片段。
82.实施方案81的掩蔽型细胞因子,其中抗体或其片段包含重链多肽或轻链多肽。
83.实施方案82的掩蔽型细胞因子,其中重链多肽包含选自由seqidno:158、168和169组成的组的氨基酸序列。
84.实施方案82的掩蔽型细胞因子,其中重链多肽包含改变效应子功能的一个或多个氨基酸取代。
85.实施方案84的掩蔽型细胞因子,其中重链多肽:
a)是igg1重链多肽,并且包含(多个)氨基酸取代:
i)n297a、n297g或n297q;
ii)l234a和l235a;
iii)c220s、c226s、c229s和p238s;
iv)c226s、c229s、e233p、l234v和l235a;
v)l234f、l235e和p331s;
vi)s267e和l328f;
vii)d265a;
viii)l234a、l235a和p329g;
b)是igg2重链多肽,并且包含(多个)氨基酸取代:
i)v234a和g237a;
ii)h268q、v309l、a330s和a331s;或
iii)v234a、g237a、p238s、h268a、v309l、a330s和p331s;或
e)是igg4重链多肽,并且包含(多个)氨基酸取代:
i)l235a、g237a和e318a;
ii)s228p、l234a和l235a;
iii)h268q、v309l、a330s和p331s;或
iv)s228p和l235a,根据kabateu编号系统编号。
86.实施方案84的掩蔽型细胞因子,其中重链多肽包含增强效应子功能的一个或多个氨基酸取代。
87.实施方案86的掩蔽型细胞因子,其中重链多肽是igg1重链多肽,并且包含(多个)氨基酸取代:
a)s298a、e333a和k334a;
b)s239d和i332e;
c)s239d、a330l和i332e;
d)p247i和a339d或a339q;
e)d280h和k290s;
f)d280h、k290s和s298d或s298v;
g)f243l、r292p和y300l;
h)f243l、r292p、y300l和p396l;
i)f243l、r292p、y300l、v305i和p396l;
j)g236a、s239d和i332e;
k)k326a和e333a;
l)k326w和e333s;
m)k290e、s298g和t299a;
n)k290e、s298g、t299a和k326e;
o)k290n、s298g和t299a;
p)k290n、s298g、t299a和k326e;
q)k334v;
r)l235s、s239d和k334v;
s)k334v和q331m、s239d、f243v、e294l或s298t;
t)e233l、q311m和k334v;
u)l234i、q311m和k334v;
v)k334v和s298t、a330m或a330f;
w)k334v、q311m和a330m或a330f;
x)k334v、s298t和a330m或a330f;
y)k334v、s239d和a330m或s298t;
z)l234y、y296w和k290y、f243v或e294l;
aa)y296w和l234y或k290y;
ab)s239d、a330s和i332e,
ac)v264i;
ad)f243l和v264i;
ae)l328m;
af)i332e;
ag)l328m和i332e;
ah)v264i和i332e;
ai)s239e和i332e;
aj)s239q和i332e;
ak)s239e;
al)a330y;
am)i332d;
an)l328i和i332e;
ao)l328q和i332e;
ap)v264t;
aq)v240i;
ar)v266i;
as)s239d;
at)s239d和i332d;
au)s239d和i332n;
av)s239d和i332q;
aw)s239e和i332d;
ax)s239e和i332n;
ay)s239e和i332q;
az)s239n和i332d;
ba)s239n和i332e;
bb)s239q和i332d;
bc)a330y和i332e;
bd)v264i、a330y和i332e;
be)a330l和i332e;
bf)v264i、a330l和i332e;
bg)l234e、l234y或l234i;
bh)l235d、l235s、l235y或l235i;
bi)s239t;
bj)v240m;
bk)v264y;
bl)a330i;
bm)n325t;
bn)i332e和l328d、l328v、l328t或l328i;
bo)v264i、i332e和s239e或s239q;
bp)s239e、v264i、a330y和i332e;
bq)a330y、i332e和s239d或s239n;
br)a330l、i332e和s239d或s239n;
bs)v264i、s298a和i332e;
bt)s298a、i332e和s239d或s239n;
bu)s239d、v264i和1332e;
bv)s239d、v264i、s298a和i332e;
bw)s239d、v264i、a330l和i332e;
bx)s239d、i332e和a330i;
by)p230a;
bz)p230a、e233d和i332e;
ca)e272y;
cb)k274t、k274e、k274r、k274l或k274y;
cd)f275w;
ce)n276l;
cf)y278t;
cg)v302i;
ch)e318r;
ci)s324d、s324i或s324v;
cj)k326i或k326t;
ck)t335d、t335r或t335y;
cl)v240i和v266i;
cm)s239d、a330y、i332e和l234i;
cn)s239d、a330y、i332e和l235d;
co)s239d、a330y、i332e和v240i;
cp)s239d、a330y、i332e和v264t;或
cq)s239d、a330y、i332e和k326e或k326t,根据kabateu编号系统编号。
88.实施方案82的掩蔽型细胞因子,其中轻链多肽包含seqidno:157或170的氨基酸序列。
89.实施方案81的掩蔽型细胞因子,其中抗体或其片段是片段可结晶结构域(fc结构域)或其片段。
90.实施方案89的掩蔽型细胞因子,其中fc结构域或其片段包含改变效应子功能的一个或多个氨基酸取代。
91.实施方案90的掩蔽型细胞因子,其中fc结构域或其片段:
a)是igg1fc结构域或其片段,并且包含(多个)氨基取代:
i)n297a、n297g或n297q;
ii)l234a和l235a;
iii)c220s、c226s、c229s和p238s;
iv)c226s、c229s、e233p、l234v和l235a;
v)l234f、l235e和p331s;
vi)s267e和l328f;
vii)d265a;
viii)l234a、l235a和p329g;
b)是igg2fc结构域或其片段,并且包含(多个)氨基酸取代:
i)v234a和g237a;
ii)h268q、v309l、a330s和a331s;或
iii)v234a、g237a、p238s、h268a、v309l、a330s和p331s;或
e)是igg4fc结构域或其片段,并且包含(多个)氨基酸取代:
i)l235a、g237a和e318a;
ii)s228p、l234a和l235a;
iii)h268q、v309l、a330s和p331s;或
iv)s228p和l235a,根据kabateu编号系统编号。
92.实施方案90的掩蔽型细胞因子,其中fc结构域或其片段包含增强效应子功能的一个或多个氨基酸取代。
93.实施方案92的掩蔽型细胞因子,其中fc结构域或其片段是igg1fc结构域或其片段,并且包含(多个)氨基酸取代:
a)s298a、e333a和k334a;
b)s239d和1332e;
c)s239d、a330l和1332e;
d)p247i和a339d或a339q;
e)d280h和k290s;
f)d280h、k290s和s298d或s298v;
g)f243l、r292p和y300l;
h)f243l、r292p、y300l和p396l;
i)f243l、r292p、y300l、v305i和p396l;
j)g236a、s239d和i332e;
k)k326a和e333a;
l)k326w和e333s;
m)k290e、s298g和t299a;
n)k290e、s298g、t299a和k326e;
o)k290n、s298g和t299a;
p)k290n、s298g、t299a和k326e;
q)k334v;
r)l235s、s239d和k334v;
s)k334v和q331m、s239d、f243v、e294l或s298t;
t)e233l、q311m和k334v;
u)l234i、q311m和k334v;
v)k334v和s298t、a330m或a330f;
w)k334v、q311m和a330m或a330f;
x)k334v、s298t和a330m或a330f;
y)k334v、s239d和a330m或s298t;
z)l234y、y296w和k290y、f243v或e294l;
aa)y296w和l234y或k290y;
ab)s239d、a330s和i332e,
ac)v264i;
ad)f243l和v264i;
ae)l328m;
af)i332e;
ag)l328m和i332e;
ah)v264i和i332e;
ai)s239e和i332e;
aj)s239q和i332e;
ak)s239e;
al)a330y;
am)i332d;
an)l328i和i332e;
ao)l328q和i332e;
ap)v264t;
aq)v240i;
ar)v266i;
as)s239d;
at)s239d和i332d;
au)s239d和i332n;
av)s239d和i332q;
aw)s239e和i332d;
ax)s239e和i332n;
ay)s239e和i332q;
az)s239n和i332d;
ba)s239n和i332e;
bb)s239q和i332d;
bc)a330y和i332e;
bd)v264i、a330y和i332e;
be)a330l和i332e;
bf)v264i、a330l和i332e;
bg)l234e、l234y或l234i;
bh)l235d、l235s、l235y或l235i;
bi)s239t;
bj)v240m;
bk)v264y;
bl)a330i;
bm)n325t;
bn)i332e和l328d、l328v、l328t或l328i;
bo)v264i、i332e和s239e或s239q;
bp)s239e、v264i、a330y和i332e;
bq)a330y、i332e和s239d或s239n;
br)a330l、i332e和s239d或s239n;
bs)v264i、s298a和i332e;
bt)s298a、i332e和s239d或s239n;
bu)s239d、v264i和i332e;
bv)s239d、v264i、s298a和i332e;
bw)s239d、v264i、a330l和i332e;
bx)s239d、i332e和a330i;
by)p230a;
bz)p230a、e233d和i332e;
ca)e272y;
cb)k274t、k274e、k274r、k274l或k274y;
cd)f275w;
ce)n276l;
cf)y278t;
cg)v302i;
ch)e318r;
ci)s324d、s324i或s324v;
cj)k326i或k326t;
ck)t335d、t335r或t335y;
cl)v240i和v266i;
cm)s239d、a330y、i332e和l234i;
cn)s239d、a330y、i332e和l235d;
co)s239d、a330y、i332e和v240i;
cp)s239d、a330y、i332e和v264t;或
cq)s239d、a330y、i332e和k326e或k326t,根据kabateu编号系统编号。
94.实施方案89的掩蔽型细胞因子,其中fc结构域或其片段包含seqidno:154的氨基酸序列。
95.实施方案71-77中任一项的掩蔽型细胞因子,其中半衰期延长结构域是白蛋白多肽或其功能片段。
96.实施方案95的掩蔽型细胞因子,其中自蛋白多肽或其功能片段包含seqidno:171的氨基酸序列。
97.实施方案71-77中任一项的掩蔽型细胞因子,其中半衰期延长结构域是白蛋白结合蛋白或其功能片段。
98.实施方案97的掩蔽型细胞因子,其中自蛋白结合蛋白或其功能片段包含选自由seqidno:172-174和252-259组成的组的氨基酸序列。
99.实施方案71-77中任一项的掩蔽型细胞因子,其中半衰期延长结构域是igg结合蛋白或其功能片段。
100.实施方案99的掩蔽型细胞因子,其中igg结合蛋白或其功能片段包含选自由seqidno:175-186组成的组的氨基酸序列。
101.实施方案71-77中任一项的掩蔽型细胞因子,其中半衰期延长结构域是聚氨基酸序列。
102.实施方案101的掩蔽型细胞因子,其中聚氨基酸序列是pas多肽或xten多肽。
103.实施方案102的掩蔽型细胞因子,其中pas多肽包含至少25、至少50、至少100、至少150、至少200、至少250、至少300、至少400、至少500、至少600、至少700、至少800、至少900、至少1000、至少1100、至少1200、至少1300、至少1500、至少2000、至少2500或至少3000个氨基酸残基,其中每个氨基酸残基是脯氨酸或丙氨酸残基。
104.实施方案102的掩蔽型细胞因子,其中pas多肽包含至少25、至少50、至少100、至少150、至少200、至少250、至少300、至少400、至少500、至少600、至少700、至少800、至少900、至少1000、至少1100、至少1200、至少1300、至少1500、至少2000、至少2500或至少3000个氨基酸残基,其中每个氨基酸残基选自由脯氨酸、丙氨酸和丝氨酸残基组成的组。
105.实施方案102的掩蔽型细胞因子,其中xten多肽包含约25至约500、约200至约1000、约500至约1500、约1000至约2000或约1500至约3000个氨基酸残基的氨基酸序列,其中至少约70%、75%、80%或85%的氨基酸序列由非重叠序列基序组成,其中基序中的每一者具有5至100个氨基酸残基、5至50个氨基酸残基或9至36个氨基酸残基,且其中至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%或100%的基序中的每一者由选自由甘氨酸(g)、丙氨酸(a)、丝氨酸(s)、苏氨酸(t)、谷氨酸(e)和脯氨酸(p)组成的组的四种、五种或六种类型的氨基酸残基组成,且其中全长xten多肽中的任何一种氨基酸类型的含量不超过约40%、约35%、约30%、约25%、约15%、约10%或约8%。
106.实施方案70-105中任一项的掩蔽型细胞因子,其中掩蔽型细胞因子进一步包含与掩蔽型细胞因子连接的一条或多条peg聚合物链。
107.实施方案106的掩蔽型细胞因子,其中一条或多条peg聚合物链与细胞因子或其功能片段和/或半衰期延长结构域连接。
108.实施方案70-107中任一项的掩蔽型细胞因子,其中通过改变掩蔽型细胞因子的氨基酸序列,使得产生一个或多个另外的n连接的和/或o连接的糖基化位点,由此来修饰或进一步修饰掩蔽型细胞因子。
109.实施方案108的掩蔽型细胞因子,其中通过改变掩蔽型细胞因子的氨基酸序列,使得一个或多个另外的天冬酰胺-x-丝氨酸(n-x-s)和/或天冬酰胺-x-苏氨酸(n-x-t)三肽序列被引入到掩蔽型细胞因子的氨基酸序列中,由此修饰或进一步修饰掩蔽型细胞因子,其中x是除脯氨酸以外的任何氨基酸。
110.实施方案108或实施方案109的掩蔽型细胞因子,其中通过改变掩蔽型细胞因子的氨基酸序列,使得一个或多个另外的丝氨酸或苏氨酸残基被引入到掩蔽型细胞因子的氨基酸序列中,由此修饰或进一步修饰掩蔽型细胞因子。
111.实施方案70-110中任一项的掩蔽型细胞因子,其中第一接头包含第一可切割肽。
112.实施方案70-111中任一项的掩蔽型细胞因子,其中第一接头包含第一n末端间隔区结构域和/或第一c末端间隔区结构域。
113.实施方案112的掩蔽型细胞因子,其中第一接头包含:
a)第一n末端间隔区结构域、第一可切割肽和第一c末端间隔区结构域;
b)第一n末端间隔区结构域和第一可切割肽;
c)第一n末端间隔区结构域和第一c末端间隔区结构域;
d)第一可切割肽和第一c末端间隔区结构域;
e)第一n末端间隔区结构域;或
f)第一c末端间隔区结构域。
114.实施方案111-113中任一项的掩蔽型细胞因子,其中第一可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。
115.实施方案112-114中任一项的掩蔽型细胞因子,其中第一n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
116.实施方案112-115中任一项的掩蔽型细胞因子,其中第一c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
117.实施方案111-113中任一项的掩蔽型细胞因子,其中第一可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
118.实施方案117的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
119.实施方案70-118中任一项的掩蔽型细胞因子,其中第一接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列。
120.实施方案70-119中任一项的掩蔽型细胞因子,其中第二接头包含第二可切割肽。
121.实施方案70-120中任一项的掩蔽型细胞因子,其中第二接头包含第二n末端间隔区结构域和/或第二c末端间隔区结构域。
122.实施方案121的掩蔽型细胞因子,其中第二接头包含:
a)第二n末端间隔区结构域、第二可切割肽和第二个第一c末端间隔区结构域;
b)第二n末端间隔区结构域和第二可切割肽;
c)第二n末端间隔区结构域和第二c末端间隔区结构域;
d)第二可切割肽和第二c末端间隔区结构域;
e)第二n末端间隔区结构域;或
f)第二c末端间隔区结构域。
123.实施方案120-122中任一项的掩蔽型细胞因子,其中第二可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。
124.实施方案121-123中任一项的掩蔽型细胞因子,其中第二n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
125.实施方案121-124中任一项的掩蔽型细胞因子,其中第二c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
126.实施方案120-122中任一项的掩蔽型细胞因子,其中第二可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
127.实施方案126的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
128.实施方案70-127中任一项的掩蔽型细胞因子,其中第二接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列。
129.实施方案72-128中任一项的掩蔽型细胞因子,其中第三接头包含第三可切割肽。
130.实施方案72-129中任一项的掩蔽型细胞因子,其中第三接头包含第三n末端间隔区结构域和/或第三c末端间隔区结构域。
131.实施方案130的掩蔽型细胞因子,其中第三接头包含:
a)第三n末端间隔区结构域、第三可切割肽和第三个第一c末端间隔区结构域;
b)第三n末端间隔区结构域和第三可切割肽;
c)第三n末端间隔区结构域和第三c末端间隔区结构域;
d)第三可切割肽和第三c末端间隔区结构域;
e)第三n末端间隔区结构域;或
f)第三c末端间隔区结构域。
132.实施方案129-131中任一项的掩蔽型细胞因子,其中第三可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。
133.实施方案130-132中任一项的掩蔽型细胞因子,其中第三n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
134.实施方案130-133中任一项的掩蔽型细胞因子,其中第三c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
135.实施方案129-131中任一项的掩蔽型细胞因子,其中第三可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
136.实施方案135的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
137.实施方案72-136中任一项的掩蔽型细胞因子,其中第三接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列。
138.实施方案52-137中任一项的掩蔽型细胞因子,其中第一可切割肽、第二可切割肽和/或第三可切割肽是共定位在表达细胞因子受体的区域或组织中的蛋白酶的底物。
139.实施方案138的掩蔽型细胞因子,其中细胞因子受体是il-2细胞因子受体或il-15细胞因子受体。
140.实施方案1-139中任一项的掩蔽型细胞因子,其中第一可切割肽、第二可切割肽和第三可切割肽中的一者或多者被选自由以下组成的组的一种或多种酶切割:abhd12、adam12、abhd12b、abhd13、abhd17a、adam19、adam20、adam21、adam28、adam30、adam33、adam8、abhd17a、adamdec1、adamts1、adamts10、adamts12、adamts13、adamts14、adamts15、adamts16、adamts17、adamts18、adamts19、adamts2、adamts20、adamts3、adamts4、abhd17b、adamts5、adamts6、adamts7、adamts8、adamts9、adamtsl1、adamtsl2、adamtsl3、abhd17c、adamtsl5、astl、bmp1、cela1、cela2a、cela2b、cela3a、cela3b、adam10、adam15、adam17、adam9、adamts4、ctse、ctsf、adamtsl4、cma1、ctrb1、ctrc、ctso、ctr1、ctsa、ctsw、ctsb、ctsc、ctsd、esp1、ctsg、ctsh、gzma、gzmb、gzmh、ctsk、gzmm、ctsl、ctss、ctsv、ctsz、htra4、klk10、klk11、klk13、klk14、klk2、klk4、dpp4、klk6、klk7、klkb1、ece1、ece2、ecel1、masp2、mep1a、mep1b、elane、fap、gzma、mmp11、gzmk、hgfac、hpn、htra1、mmp11、mmp16、mmp17、mmp19、htra2、mmp20、mmp21、htra3、htra4、kel、mmp23b、mmp24、mmp25、mmp26、mmp27、mmp28、klk5、mmp3、mmp7、mmp8、mmp9、lgmn、lnpep、masp1、pappa、pappa2、pcsk1、napsa、pcsk5、pcsk6、mme、mmp1、mmp10、plat、plau、plg、prss1、prss12、prss2、prss21、prss3、prss33、prss4、prss55、prss57、mmp12、prss8、prss9、prtn3、mmp13、mmp14、st14、tmprss10、tmprss11a、tmprss11d、tmprss11e、tmprss11f、tmprss12、tmprss13、mmp15、tmprss15、mmp2、tmprss2、tmprss3、tmprss4、tmprss5、tmprss6、tmprss7、tmprss9、nrdc、ovch1、pamr1、pcsk3、phex、tinag、tpsab1、tpsd1和tpsg1。
141.实施方案2-69和71-140中任一项的掩蔽型细胞因子,其中半衰期延长结构域与药剂缀合。
142.实施方案141的掩蔽型细胞因子,其中所述药剂是微管蛋白聚合的抑制剂、dna损伤剂或dna合成抑制剂。
143.实施方案142的掩蔽型细胞因子,其中所述药剂是类美登素、奥瑞他汀、吡咯并苯并二氮杂卓(pbd)二聚体、卡奇霉素、倍癌霉素、吲哚啉并苯并二氮杂卓二聚体或依喜替康衍生物dxd。
144.实施方案141的掩蔽型细胞因子,其中所述药剂是免疫刺激剂。
145.实施方案144的掩蔽型细胞因子,其中所述免疫刺激剂是干扰素基因刺激物(sting)激动剂或toll样受体(tlr)激动剂。
146.实施方案145的掩蔽型细胞因子,其中所述sting激动剂是环二核苷酸(cdn)。
147.实施方案146的掩蔽型细胞因子,其中所述cdn选自由cgamp、c-二-amp、c-二-gmp、caimp、c-二-imp、4-(2-氯-6-氟苄基)-n-(呋喃-2-基甲基)-3-氧代-3,4-二氢-2h-苯并[b][1,4]噻嗪-6-甲酰胺组成的组。
148.实施方案145的掩蔽型细胞因子,其中tlr激动剂是选自由tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9和tlr10组成的组的tlr的激动剂。
149.一种掩蔽型细胞因子,其包含:
a)第一半衰期延长结构域和第二半衰期延长结构域;
b)掩蔽部分;和
c)细胞因子或其功能片段,
其中掩蔽部分与第一半衰期延长结构域连接,
其中细胞因子或其功能片段与第二半衰期延长结构域连接,且
其中第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰。
150.实施方案149的掩蔽型细胞因子,其中掩蔽部分经由第一接头与第一半衰期延长结构域连接;和/或其中细胞因子或其功能片段经由第二接头与第二半衰期延长结构域连接。
151.实施方案149或实施方案150的掩蔽型细胞因子,其中细胞因子或其功能片段是il-2多肽或其功能片段。
152.实施方案151的掩蔽型细胞因子,其中il-2多肽或其功能片段包含选自由seqidno:1-8、160、230、243-251、260、775-792和813-822组成的组的氨基酸序列。
153.实施方案151的掩蔽型细胞因子,其中il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入降低il-2多肽或其功能片段对cd25(il-2rα)的亲和力的一个或多个氨基酸取代而产生的氨基酸序列。
154.实施方案153的掩蔽型细胞因子,其中氨基酸序列是通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代中的一者或多者产生的:r38a、f42a、f42k、f42e、k43a、y45a、y45n、y45r、e62a、e62r、e62s和l72g。
155.实施方案151的掩蔽型细胞因子,其中il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代而产生的氨基酸序列。
156.实施方案155的掩蔽型细胞因子,其中氨基酸序列是通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代中的一者或多者产生的:h16i、l18c、d20a、d20l、d20f、n29l、l80f、r81d、l85v、i86v和i92f。
157.实施方案153或实施方案154的掩蔽型细胞因子,其中氨基酸序列是通过进一步引入增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代产生的。
158.实施方案157的掩蔽型细胞因子,其中增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代选自由h16i、l18c、d20a、d20l、d20f、n29l、l80f、r81d、l85v、i86v和i92f组成的组。
159.实施方案151的掩蔽型细胞因子,其中il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入稳定il-2多肽或其功能片段的一个或多个氨基酸取代而产生的氨基酸序列。
160.实施方案159的掩蔽型细胞因子,其中氨基酸序列是通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代之一产生的:c125s、c125a和c125g。
161.实施方案153-158中任一项的掩蔽型细胞因子,其中氨基酸序列是通过进一步引入稳定il-2多肽或其功能片段的一个或多个氨基酸取代产生的。
162.实施方案161的掩蔽型细胞因子,其中稳定il-2多肽或其功能片段的一个或多个氨基酸取代是氨基酸取代c125s、c125a或c125g。
163.实施方案151-162中任一项的掩蔽型细胞因子,其中掩蔽部分包含选自由seqidno:9、10、161-165、187-218、221-229、231、261、826和827组成的组的氨基酸序列。
164.实施方案149或实施方案150的掩蔽型细胞因子,其中细胞因子或其功能片段是il-15多肽或其功能片段。
165.实施方案164的掩蔽型细胞因子,其中il-15多肽或其功能片段包含seqidno:167的氨基酸序列。
166.实施方案164或实施方案165的掩蔽型细胞因子,其中掩蔽部分包含选自由seqidno:10、161-165、219-229、232-234、261和823-827组成的组的氨基酸序列。
167.实施方案164或实施方案165的掩蔽型细胞因子,其中掩蔽部分包含通过向seqidno:232-234和823-825中的任一者的氨基酸序列中引入以下氨基酸取代中的一者或多者而产生的氨基酸序列:r24a、r26a、k34a、s40a、l42a和p67a。
168.实施方案149-167中任一项的掩蔽型细胞因子,其中第一半衰期延长结构域是第一抗体或其片段,且第二半衰期延长结构域是第二抗体或其片段。
169.实施方案168的掩蔽型细胞因子,其中:
a)第一抗体或其片段包含第一重链多肽,且第二抗体或其片段包含第二轻链多肽;或
b)第一抗体或其片段包含第一轻链多肽,且第二抗体或其片段包含第二重链多肽。
170.实施方案169的掩蔽型细胞因子,其中第一重链多肽或第二重链多肽包含改变效应子功能的一个或多个氨基酸取代。
171.实施方案170的掩蔽型细胞因子,其中第一重链多肽或第二重链多肽:
a)是igg1同种型,并且包含(多个)氨基取代:
i)n297a、n297g或n297q;
ii)l234a和l235a;
iii)c220s、c226s、c229s和p238s;
iv)c226s、c229s、e233p、l234v和l235a;
v)l234f、l235e和p331s;
vi)s267e和l328f;
vii)d265a;
viii)l234a、l235a和p329g;
b)是igg2同种型,并且包含(多个)氨基酸取代:
i)v234a和g237a;
ii)h268q、v309l、a330s和a331s;或
iii)v234a、g237a、p238s、h268a、v309l、a330s和p331s;或
e)是igg4同种型,并且包含(多个)氨基酸取代:
i)l235a、g237a和e318a;
ii)s228p、l234a和l235a;
iii)h268q、v309l、a330s和p331s;或
iv)s228p和l235a,根据kabateu编号系统编号。
172.实施方案170的掩蔽型细胞因子,其中第一重链多肽或第二重链多肽包含增强效应子功能的一个或多个氨基酸取代。
173.实施方案172的掩蔽型细胞因子,其中第一重链多肽或第二重链多肽是igg1重链多肽,并且包含(多个)氨基酸取代:
a)s298a、e333a和k334a;
b)s239d和i332e;
c)s239d、a330l和i332e;
d)p247i和a339d或a339q;
e)d280h和k290s;
f)d280h、k290s和s298d或s298v;
g)f243l、r292p和y300l;
h)f243l、r292p、y300l和p396l;
i)f243l、r292p、y300l、v305i和p396l;
j)g236a、s239d和i332e;
k)k326a和e333a;
l)k326w和e333s;
m)k290e、s298g和t299a;
n)k290e、s298g、t299a和k326e;
o)k290n、s298g和t299a;
p)k290n、s298g、t299a和k326e;
q)k334v;
r)l235s、s239d和k334v;
s)k334v和q331m、s239d、f243v、e294l或s298t;
t)e233l、q311m和k334v;
u)l234i、q311m和k334v;
v)k334v和s298t、a330m或a330f;
w)k334v、q311m和a330m或a330f;
x)k334v、s298t和a330m或a330f;
y)k334v、s239d和a330m或s298t;
z)l234y、y296w和k290y、f243v或e294l;
aa)y296w和l234y或k290y;
ab)s239d、a330s和i332e,
ac)v264i;
ad)f243l和v264i;
ae)l328m;
af)i332e;
ag)l328m和i332e;
ah)v264i和i332e;
ai)s239e和i332e;
aj)s239q和i332e;
ak)s239e;
al)a330y;
am)i332d;
an)l328i和i332e;
ao)l328q和i332e;
ap)v264t;
aq)v240i;
ar)v266i;
as)s239d;
at)s239d和i332d;
au)s239d和i332n;
av)s239d和i332q;
aw)s239e和i332d;
ax)s239e和i332n;
ay)s239e和i332q;
az)s239n和i332d;
ba)s239n和i332e;
bb)s239q和i332d;
bc)a330y和i332e;
bd)v264i、a330y和i332e;
be)a330l和i332e;
bf)v264i、a330l和i332e;
bg)l234e、l234y或l234i;
bh)l235d、l235s、l235y或l235i;
bi)s239t;
bj)v240m;
bk)v264y;
bl)a330i;
bm)n325t;
bn)i332e和l328d、l328v、l328t或l328i;
bo)v264i、i332e和s239e或s239q;
bp)s239e、v264i、a330y和i332e;
bq)a330y、i332e和s239d或s239n;
br)a330l、i332e和s239d或s239n;
bs)v264i、s298a和i332e;
bt)s298a、i332e和s239d或s239n;
bu)s239d、v264i和i332e;
bv)s239d、v264i、s298a和1332e;
bw)s239d、v264i、a330l和i332e;
bx)s239d、i332e和a330i;
by)p230a;
bz)p230a、e233d和i332e;
ca)e272y;
cb)k274t、k274e、k274r、k274l或k274y;
cd)f275w;
ce)n276l;
cf)y278t;
cg)v302i;
ch)e318r;
ci)s324d、s324i或s324v;
cj)k326i或k326t;
ck)t335d、t335r或t335y;
cl)v240i和v266i;
cm)s239d、a330y、i332e和l234i;
cn)s239d、a330y、i332e和l235d;
co)s239d、a330y、i332e和v240i;
cp)s239d、a330y、i332e和v264t;或
cq)s239d、a330y、i332e和k326e或k326t,根据kabateu编号系统编号。
174.实施方案169的掩蔽型细胞因子,其中第一重链多肽包含选自由seqidno:158、168和169组成的组的氨基酸序列,且第二重链多肽包含选自由seqidno:158、168和169组成的组的氨基酸序列。
175.实施方案169的掩蔽型细胞因子,其中第一轻链多肽包含seqidno:157或170的氨基酸序列,且第二轻链多肽包含seqidno:157或170的氨基酸序列。
176.实施方案168的掩蔽型细胞因子,其中第一抗体或其片段是第一片段可结晶结构域(fc结构域)或其片段,且第二抗体或其片段是第二fc结构域或其片段。
177.实施方案176的掩蔽型细胞因子,其中第一fc结构域或其片段和/或第二fc结构域或其片段包含改变效应子功能的一个或多个氨基酸取代。
178.实施方案177的掩蔽型细胞因子,其中第一fc结构域或其片段和/或第二fc结构域或其片段:
a)是igg1fc结构域或其片段,并且包含(多个)氨基取代:
i)n297a、n297g或n297q;
ii)l234a和l235a;
iii)c220s、c226s、c229s和p238s;
iv)c226s、c229s、e233p、l234v和l235a;
v)l234f、l235e和p331s;
vi)s267e和l328f;
vii)d265a;
viii)l234a、l235a和p329g;
b)是igg2fc结构域或其片段,并且包含(多个)氨基酸取代:
i)v234a和g237a;
ii)h268q、v309l、a330s和a331s;或
iii)v234a、g237a、p238s、h268a、v309l、a330s和p331s;或
e)是igg4fc结构域或其片段,并且包含(多个)氨基酸取代:
i)l235a、g237a和e318a;
ii)s228p、l234a和l235a;
iii)h268q、v309l、a330s和p331s;或
iv)s228p和l235a,根据kabateu编号系统编号。
179.实施方案177的掩蔽型细胞因子,其中第一fc结构域或其片段和/或第二fc结构域或其片段包含增强效应子功能的一个或多个氨基酸取代。
180.实施方案179的掩蔽型细胞因子,其中第一fc结构域或其片段和/或第二fc结构域或其片段是igg1fc结构域或其片段,并且包含(多个)氨基酸取代:
a)s298a、e333a和k334a;
b)s239d和i332e;
c)s239d、a330l和i332e;
d)p247i和a339d或a339q;
e)d280h和k290s;
f)d280h、k290s和s298d或s298v;
g)f243l、r292p和y300l;
h)f243l、r292p、y300l和p396l;
i)f243l、r292p、y300l、v305i和p396l;
j)g236a、s239d和i332e;
k)k326a和e333a;
l)k326w和e333s;
m)k290e、s298g和t299a;
n)k290e、s298g、t299a和k326e;
o)k290n、s298g和t299a;
p)k290n、s298g、t299a和k326e;
q)k334v;
r)l235s、s239d和k334v;
s)k334v和q331m、s239d、f243v、e294l或s298t;
t)e233l、q311m和k334v;
u)l234i、q311m和k334v;
v)k334v和s298t、a330m或a330f;
w)k334v、q311m和a330m或a330f;
x)k334v、s298t和a330m或a330f;
y)k334v、s239d和a330m或s298t;
z)l234y、y296w和k290y、f243v或e294l;
aa)y296w和l234y或k290y;
ab)s239d、a330s和i332e,
ac)v264i;
ad)f243l和v264i;
ae)l328m;
af)i332e;
ag)l328m和i332e;
ah)v264i和i332e;
ai)s239e和i332e;
aj)s239q和i332e;
ak)s239e;
al)a330y;
am)i332d;
an)l328i和i332e;
ao)l328q和i332e;
ap)v264t;
aq)v240i;
ar)v266i;
as)s239d;
at)s239d和i332d;
au)s239d和i332n;
av)s239d和i332q;
aw)s239e和i332d;
ax)s239e和i332n;
ay)s239e和i332q;
az)s239n和i332d;
ba)s239n和i332e;
bb)s239q和i332d;
bc)a330y和i332e;
bd)v264i、a330y和i332e;
be)a330l和i332e;
bf)v264i、a330l和i332e;
bg)l234e、l234y或l234i;
bh)l235d、l235s、l235y或l235i;
bi)s239t;
bj)v240m;
bk)v264y;
bl)a330i;
bm)n325t;
bn)i332e和l328d、l328v、l328t或l328i;
bo)v264i、i332e和s239e或s239q;
bp)s239e、v264i、a330y和i332e;
bq)a330y、i332e和s239d或s239n;
br)a330l、i332e和s239d或s239n;
bs)v264i、s298a和i332e;
bt)s298a、i332e和s239d或s239n;
bu)s239d、v264i和i332e;
bv)s239d、v264i、s298a和i332e;
bw)s239d、v264i、a330l和i332e;
bx)s239d、i332e和a330i;
by)p230a;
bz)p230a、e233d和i332e;
ca)e272y;
cb)k274t、k274e、k274r、k274l或k274y;
cd)f275w;
ce)n276l;
cf)y278t;
cg)v302i;
ch)e318r;
ci)s324d、s324i或s324v;
cj)k326i或k326t;
ck)t335d、t335r或t335y;
cl)v240i和v266i;
cm)s239d、a330y、i332e和l234i;
cn)s239d、a330y、i332e和l235d;
co)s239d、a330y、i332e和v240i;
cp)s239d、a330y、i332e和v264t;或
cq)s239d、a330y、i332e和k326e或k326t,根据kabateu编号系统编号。
181.实施方案176的掩蔽型细胞因子,其中:
a)第一fc结构域或其片段包含seqidno:155的氨基酸序列,且第二fc结构域或其片段包含seqidno:156的氨基酸序列;
b)第一fc结构域或其片段包含seqidno:156的氨基酸序列,且第二fc结构域或其片段包含seqidno:155的氨基酸序列;
c)第一fc结构域或其片段包含seqidno:154的氨基酸序列,且第二fc结构域或其片段包含seqidno:154的氨基酸序列;
d)第一fc结构域或其片段包含seqidno:265的氨基酸序列,且第二fc结构域或其片段包含seqidno:156的氨基酸序列;
e)第一fc结构域或其片段包含seqidno:156的氨基酸序列,且第二fc结构域或其片段包含seqidno:265的氨基酸序列;
f)第一fc结构域或其片段包含seqidno:155的氨基酸序列,且第二fc结构域或其片段包含seqidno:616的氨基酸序列;
g)第一fc结构域或其片段包含seqidno:616的氨基酸序列,且第二fc结构域或其片段包含seqidno:155的氨基酸序列;
h)第一fc结构域或其片段包含seqidno:157的氨基酸序列,且第二fc结构域或其片段包含seqidno:158的氨基酸序列;
i)第一fc结构域或其片段包含seqidno:158的氨基酸序列,且第二fc结构域或其片段包含seqidno:157的氨基酸序列;
j)第一fc结构域或其片段包含seqidno:796的氨基酸序列,且第二fc结构域或其片段包含seqidno:774的氨基酸序列;
k)第一fc结构域或其片段包含seqidno:774的氨基酸序列,且第二fc结构域或其片段包含seqidno:796的氨基酸序列;
l)第一fc结构域或其片段包含seqidno:721的氨基酸序列,且第二fc结构域或其片段包含seqidno:619的氨基酸序列;
m)第一fc结构域或其片段包含seqidno:619的氨基酸序列,且第二fc结构域或其片段包含seqidno:721的氨基酸序列;
n)第一fc结构域或其片段包含seqidno:721的氨基酸序列,且第二fc结构域或其片段包含seqidno:772的氨基酸序列;
o)第一fc结构域或其片段包含seqidno:772的氨基酸序列,且第二fc结构域或其片段包含seqidno:721的氨基酸序列;
p)第一fc结构域或其片段包含seqidno:793的氨基酸序列,且第二fc结构域或其片段包含seqidno:622的氨基酸序列;
q)第一fc结构域或其片段包含seqidno:622的氨基酸序列,且第二fc结构域或其片段包含seqidno:793的氨基酸序列;
r)第一fc结构域或其片段包含seqidno:793的氨基酸序列,且第二fc结构域或其片段包含seqidno:773的氨基酸序列;
s)第一fc结构域或其片段包含seqidno:773的氨基酸序列,且第二fc结构域或其片段包含seqidno:793的氨基酸序列;
t)第一fc结构域或其片段包含seqidno:796的氨基酸序列,且第二fc结构域或其片段包含seqidno:625的氨基酸序列;
u)第一fc结构域或其片段包含seqidno:625的氨基酸序列,且第二fc结构域或其片段包含seqidno:796的氨基酸序列;
v)第一fc结构域或其片段包含seqidno:156的氨基酸序列,且第二fc结构域或其片段包含seqidno:156的氨基酸序列;
w)第一fc结构域或其片段包含seqidno:796的氨基酸序列,且第二fc结构域或其片段包含seqidno:625的氨基酸序列;或
x)第一fc结构域或其片段包含seqidno:625的氨基酸序列,且第二fc结构域或其片段包含seqidno:796的氨基酸序列。
182.实施方案149-167中任一项的掩蔽型细胞因子,其中第一半衰期延长结构域是第一scfv或其片段,且第二半衰期延长结构域是第二scfv或其片段。
183.实施方案149-167中任一项的掩蔽型细胞因子,其中第一半衰期延长结构域是第一fc结构域或其片段,且第二半衰期延长结构域是第二fc结构域或其片段,并且其中第一fc结构域或其片段与第二fc结构域或其片段连接。
184.实施方案183的掩蔽型细胞因子,其中第一fc结构域或其片段经由第三接头与第二fc结构域或其片段连接。
185.实施方案149-167中任一项的掩蔽型细胞因子,其中:
a)第一半衰期延长结构域是scfv或其片段,且第二半衰期延长结构域是抗体或其片段;或
b)第一半衰期延长结构域是抗体或其片段,且第二半衰期延长结构域是scfv或其片段。
186.实施方案168-181中任一项的掩蔽型细胞因子,其中促进第一和第二半衰期延长结构域的缔合的修饰包括:
a)根据kabateu编号系统编号,在第一抗体或其片段中引入s354c和t366w突变,并在第二抗体或其片段中引入y349c、t366s、l368a和y407v突变;
b)根据kabateu编号系统编号,在第二抗体或其片段中引入s354c和t366w突变,并在第一抗体或其片段中引入y349c、t366s、l368a和y407v突变;
c)根据kabateu编号系统编号,在第一抗体或其片段中引入k392d和k409d突变,并在第二抗体或其片段中引入d399k和e356k突变;
d)根据kabateu编号系统编号,在第二抗体或其片段中引入k392d和k409d突变,并在第一抗体或其片段中引入d399k和e356k突变;
e)根据kabateu编号系统编号,在第一抗体或其片段中引入s364h和f405a突变,并在第二抗体或其片段中引入y349t和t394f突变;或
f)根据kabateu编号系统编号,在第二抗体或其片段中引入s364h和f405a突变,并在第一抗体或其片段中引入y349t和t394f突变。
187.实施方案168-181中任一项的掩蔽型细胞因子,其中通过如下方式产生第一抗体或其片段的氨基酸序列和第二抗体或其片段的氨基酸序列:
a)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入s354c和t366w突变,并在seqidno:154或169的氨基酸序列中引入y349c、t366s、l368a和y407v突变;
b)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入s354c和t366w突变,并在seqidno:154或169的氨基酸序列中引入y349c、t366s、l368a和y407v突变;
c)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d和k409d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
d)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d和k409d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
e)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入s364h和f405a突变,并在seqidno:154或169的氨基酸序列中引入y349t和t394f突变;或
f)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入s364h和f405a突变,并在seqidno:154或169的氨基酸序列中引入y349t和t394f突变。
188.实施方案168-181中任一项的掩蔽型细胞因子,其中促进第一和第二半衰期延长结构域的缔合的修饰包括:
a)根据kabateu编号系统编号,在第一抗体或其片段中引入y407t突变,并在第二抗体或其片段中引入t366y突变;
b)根据kabateu编号系统编号,在第一抗体或其片段中引入y407a突变,并在第二抗体或其片段中引入t366w突变;
c)根据kabateu编号系统编号,在第一抗体或其片段中引入f405a突变,并在第二抗体或其片段中引入t394w突变;
d)根据kabateu编号系统编号,在第一抗体或其片段中引入f405w突变,并在第二抗体或其片段中引入t394s突变;
e)根据kabateu编号系统编号,在第一抗体或其片段中引入y407t突变,并在第二抗体或其片段中引入t366y突变;
f)根据kabateu编号系统编号,在第一抗体或其片段中引入t366y和f405a突变,并在第二抗体或其片段中引入t394w和y407t突变;
g)根据kabateu编号系统编号,在第一抗体或其片段中引入t366w和f405w突变,并在第二抗体或其片段中引入t394s和y407a突变;
h)根据kabateu编号系统编号,在第一抗体或其片段中引入f405w和y407a突变,并在第二抗体或其片段中引入t366w和t394s突变;
i)根据kabateu编号系统编号,在第一抗体或其片段中引入t366w突变,并在第二抗体或其片段中引入t366s、l368a和y407v突变;
j)根据kabateu编号系统编号,在第二抗体或其片段中引入y407t突变,并在第一抗体或其片段中引入t366y突变;
k)根据kabateu编号系统编号,在第二抗体或其片段中引入y407a突变,并在第一抗体或其片段中引入t366w突变;
l)根据kabateu编号系统编号,在第二抗体或其片段中引入f405a突变,并在第一抗体或其片段中引入t394w突变;
m)根据kabateu编号系统编号,在第二抗体或其片段中引入f405w突变,并在第一抗体或其片段中引入t394s突变;
n)根据kabateu编号系统编号,在第二抗体或其片段中引入y407t突变,并在第一抗体或其片段中引入t366y突变;
o)根据kabateu编号系统编号,在第二抗体或其片段中引入t366y和f405a突变,并在第一抗体或其片段中引入t394w和y407t突变;
p)根据kabateu编号系统编号,在第二抗体或其片段中引入t366w和f405w突变,并在第一抗体或其片段中引入t394s和y407a突变;
q)根据kabateu编号系统编号,在第二抗体或其片段中引入f405w和y407a突变,并在第一抗体或其片段中引入t366w和t394s突变;或
r)根据kabateu编号系统编号,在第二抗体或其片段中引入t366w突变,并在第一抗体或其片段中引入t366s、l368a和y407v突变。
189.实施方案168-181中任一项的掩蔽型细胞因子,其中通过如下方式产生第一抗体或其片段的氨基酸序列和第二抗体或其片段的氨基酸序列:
a)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407t突变,并在seqidno:154或169的氨基酸序列中引入t366y突变;
b)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407a突变,并在seqidno:154或169的氨基酸序列中引入t366w突变;
c)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405a突变,并在seqidno:154或169的氨基酸序列中引入t394w突变;
d)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405w突变,并在seqidno:154或169的氨基酸序列中引入t394s突变;
e)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407t突变,并在seqidno:154或169的氨基酸序列中引入t366y突变;
f)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366y和f405a突变,并在seqidno:154或169的氨基酸序列中引入t394w和y407t突变;
g)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366w和f405w突变,并在seqidno:154或169的氨基酸序列中引入t394s和y407a突变;
h)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405w和y407a突变,并在seqidno:154或169的氨基酸序列中引入t366w和t394s突变;
i)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366w突变,并在seqidno:154或169的氨基酸序列中引入t366s、l368a和y407v突变;
j)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407t突变,并在seqidno:154或169的氨基酸序列中引入t366y突变;
k)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407a突变,并在seqidno:154或169的氨基酸序列中引入t366w突变;
l)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405a突变,并在seqidno:154或169的氨基酸序列中引入t394w突变;
m)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405w突变,并在seqidno:154或169的氨基酸序列中引入t394s突变;
n)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407t突变,并在seqidno:154或169的氨基酸序列中引入t366y突变;
o)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366y和f405a突变,并在seqidno:154或169的氨基酸序列中引入t394w和y407t突变;
p)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366w和f405w突变,并在seqidno:154或169的氨基酸序列中引入t394s和y407a突变;
q)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405w和y407a突变,并在seqidno:154或169的氨基酸序列中引入t366w和t394s突变;或
r)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366w突变,并在seqidno:154或169的氨基酸序列中引入t366s、l368a和y407v突变。
190.实施方案168-181中任一项的掩蔽型细胞因子,其中促进第一和第二半衰期延长结构域的缔合的修饰包括:
a)根据kabateu编号系统编号,在第一抗体或其片段中引入k409e突变,并在第二抗体或其片段中引入d399k突变;
b)根据kabateu编号系统编号,在第一抗体或其片段中引入k409e突变,并在第二抗体或其片段中引入d399r突变;
c)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d突变,并在第二抗体或其片段中引入d399k突变;
d)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d突变,并在第二抗体或其片段中引入d399r突变;
e)根据kabateu编号系统编号,在第一抗体或其片段中引入k392e突变,并在第二抗体或其片段中引入d399r突变;
f)根据kabateu编号系统编号,在第一抗体或其片段中引入k392e突变,并在第二抗体或其片段中引入d399k突变;
g)根据kabateu编号系统编号,在第一抗体或其片段中引入k392d突变,并在第二抗体或其片段中引入d399r突变;
h)根据kabateu编号系统编号,在第一抗体或其片段中引入k392d突变,并在第二抗体或其片段中引入d399k突变;
i)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k360d突变,并在第二抗体或其片段中引入d399k和e356k突变;
j)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k370d突变,并在第二抗体或其片段中引入d399k和e357k突变;
k)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k392d突变,并在第二抗体或其片段中引入d399k、e356k和e357k突变;
l)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k392d突变,并在第二抗体或其片段中引入d399k突变;
m)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k392d突变,并在第二抗体或其片段中引入d399k和e356k突变;
n)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k392d突变,并在第二抗体或其片段中引入d399k和e357k突变;
o)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k370d突变,并在第二抗体或其片段中引入d399k和e357k突变;
p)根据kabateu编号系统编号,在第一抗体或其片段中引入d399k突变,并在第二抗体或其片段中引入k409d和k360d突变;
q)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k439d突变,并在第二抗体或其片段中引入d399k和e356k突变;
r)根据kabateu编号系统编号,在第二抗体或其片段中引入k409e突变,并在第一抗体或其片段中引入d399k突变;
s)根据kabateu编号系统编号,在第二抗体或其片段中引入k409e突变,并在第一抗体或其片段中引入d399r突变;
t)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d突变,并在第一抗体或其片段中引入d399k突变;
u)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d突变,并在第一抗体或其片段中引入d399r突变;
v)根据kabateu编号系统编号,在第二抗体或其片段中引入k392e突变,并在第一抗体或其片段中引入d399r突变;
w)根据kabateu编号系统编号,在第二抗体或其片段中引入k392e突变,并在第一抗体或其片段中引入d399k突变;
x)根据kabateu编号系统编号,在第二抗体或其片段中引入k392d突变,并在第一抗体或其片段中引入d399r突变;
y)根据kabateu编号系统编号,在第二抗体或其片段中引入k392d突变,并在第一抗体或其片段中引入d399k突变;
z)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k360d突变,并在第一抗体或其片段中引入d399k和e356k突变;
aa)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k370d突变,并在第一抗体或其片段中引入d399k和e357k突变;
ab)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k392d突变,并在第一抗体或其片段中引入d399k、e356k和e357k突变;
ac)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k392d突变,并在第一抗体或其片段中引入d399k突变;
ad)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k392d突变,并在第一抗体或其片段中引入d399k和e356k突变;
ae)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k392d突变,并在第一抗体或其片段中引入d399k和e357k突变;
af)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k370d突变,并在第一抗体或其片段中引入d399k和e357k突变;
ag)根据kabateu编号系统编号,在第二抗体或其片段中引入d399k突变,并在第一抗体或其片段中引入k409d和k360d突变;或
ah)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k439d突变,并在第一抗体或其片段中引入d399k和e356k突变。
191.实施方案168-181中任一项的掩蔽型细胞因子,其中通过如下方式产生第一抗体或其片段的氨基酸序列和第二抗体或其片段的氨基酸序列:
a)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409e突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
b)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409e突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
c)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
d)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
e)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392e突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
f)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392e突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
g)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
h)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
i)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k360d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
j)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k370d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
k)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k、e356k和e357k突变;
l)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
m)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
n)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
o)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k370d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
p)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入d399k突变,并在seqidno:154或169的氨基酸序列中引入k409d和k360d突变;
q)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k439d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
r)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409e突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
s)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409e突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
t)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
u)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
v)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392e突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
w)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392e突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
x)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
y)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
z)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k360d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
aa)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k370d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
ab)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k、e356k和e357k突变;
ac)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
ad)根据kabateu编号系统编号,在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
ae)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
af)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k370d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
ag)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入d399k突变,并在seqidno:154或169的氨基酸序列中引入k409d和k360d突变;或
ah)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k439d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变。
192.实施方案150-191中任一项的掩蔽型细胞因子,其中第一接头包含第一可切割肽;和/或其中第二接头包含第二可切割肽。
193.实施方案150-192中任一项的掩蔽型细胞因子,其中第一接头包含第一n末端间隔区结构域和/或第一c末端间隔区结构域。
194.实施方案193的掩蔽型细胞因子,其中第一接头包含:
a)第一n末端间隔区结构域、第一可切割肽和第一c末端间隔区结构域;
b)第一n末端间隔区结构域和第一可切割肽;
c)第一n末端间隔区结构域和第一c末端间隔区结构域;
d)第一可切割肽和第一c末端间隔区结构域;
e)第一n末端间隔区结构域;或
f)第一c末端间隔区结构域。
195.实施方案150-194中任一项的掩蔽型细胞因子,其中第二接头包含第二n末端间隔区结构域和/或第二c末端间隔区结构域。
196.实施方案195的掩蔽型细胞因子,其中第二接头包含:
a)第二n末端间隔区结构域、第二可切割肽和第二c末端间隔区结构域;
b)第二n末端间隔区结构域和第二可切割肽;
c)第二n末端间隔区结构域和第二c末端间隔区结构域;
d)第二可切割肽和第二c末端间隔区结构域;
e)第二n末端间隔区结构域;或
f)第二c末端间隔区结构域。
197.实施方案192-196中任一项的掩蔽型细胞因子,其中第一可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列;和/或其中第二可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。
198.实施方案193-197中任一项的掩蔽型细胞因子,其中第一n末端间隔区结构域包含选自由seqidno:20-95235、263、268、269、727、794、799和857-878组成的组的氨基酸序列,和/或第一c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
199.实施方案192-196中任一项的掩蔽型细胞因子,其中第一可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
200.实施方案199的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
201.实施方案195-200中任一项的掩蔽型细胞因子,其中第二n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列,和/或第二c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
202.实施方案192-201中任一项的掩蔽型细胞因子,其中第二可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
203.实施方案202的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
204.实施方案150-203中任一项的掩蔽型细胞因子,其中第一接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列,和/或第二接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列。
205.实施方案184-204中任一项的掩蔽型细胞因子,其中第三接头包含第三n末端间隔区结构域和/或第三c末端间隔区结构域。
206.实施方案205的掩蔽型细胞因子,其中第三n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列,和/或第三c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
207.实施方案192-206中任一项的掩蔽型细胞因子,其中第一可切割肽和/或第二可切割肽是共定位在表达细胞因子受体的区域或组织中的蛋白酶的底物。
208.实施方案207的掩蔽型细胞因子,其中细胞因子受体是il-2细胞因子受体或il-15细胞因子受体。
209.实施方案184-208中任一项的掩蔽型细胞因子,其中第一可切割肽和/或第二可切割肽被选自由以下组成的组的一种或多种酶切割:abhd12、adam12、abhd12b、abhd13、abhd17a、adam19、adam20、adam21、adam28、adam30、adam33、adam8、abhd17a、adamdec1、adamts1、adamts10、adamts12、adamts13、adamts14、adamts15、adamts16、adamts17、adamts18、adamts19、adamts2、adamts20、adamts3、adamts4、abhd17b、adamts5、adamts6、adamts7、adamts8、adamts9、adamtsl1、adamtsl2、adamtsl3、abhd17c、adamtsl5、astl、bmp1、cela1、cela2a、cela2b、cela3a、cela3b、adam10、adam15、adam17、adam9、adamts4、ctse、ctsf、adamtsl4、cma1、ctrb1、ctrc、ctso、ctr1、ctsa、ctsw、ctsb、ctsc、ctsd、esp1、ctsg、ctsh、gzma、gzmb、gzmh、ctsk、gzmm、ctsl、ctss、ctsv、ctsz、htra4、klk10、klk11、klk13、klk14、klk2、klk4、dpp4、klk6、klk7、klkb1、ece1、ece2、ecel1、masp2、mep1a、mep1b、elane、fap、gzma、mmp11、gzmk、hgfac、hpn、htra1、mmp11、mmp16、mmp17、mmp19、htra2、mmp20、mmp21、htra3、htra4、kel、mmp23b、mmp24、mmp25、mmp26、mmp27、mmp28、klk5、mmp3、mmp7、mmp8、mmp9、lgmn、lnpep、masp1、pappa、pappa2、pcsk1、napsa、pcsk5、pcsk6、mme、mmp1、mmp10、plat、plau、plg、prss1、prss12、prss2、prss21、prss3、prss33、prss4、prss55、prss57、mmp12、prss8、prss9、prtn3、mmp13、mmp14、st14、tmprss10、tmprss11a、tmprss11d、tmprss11e、tmprss11f、tmprss12、tmprss13、mmp15、tmprss15、mmp2、tmprss2、tmprss3、tmprss4、tmprss5、tmprss6、tmprss7、tmprss9、nrdc、ovch1、pamr1、pcsk3、phex、tinag、tpsab1、tpsd1和tpsg1。
210.实施方案149-209中任一项的掩蔽型细胞因子,其中第一半衰期延长结构域和/或第二半衰期延长结构域与药剂缀合。
211.实施方案210的掩蔽型细胞因子,其中所述药剂是微管蛋白聚合的抑制剂、dna损伤剂或dna合成抑制剂。
212.实施方案211的掩蔽型细胞因子,其中所述药剂是类美登素、奥瑞他汀、吡咯并苯并二氮杂卓(pbd)二聚体、卡奇霉素、倍癌霉素、吲哚啉并苯并二氮杂卓二聚体或依喜替康衍生物dxd。
213.实施方案210的掩蔽型细胞因子,其中所述药剂是免疫刺激剂。
214.实施方案213的掩蔽型细胞因子,其中所述免疫刺激剂是干扰素基因刺激物(sting)激动剂或toll样受体(tlr)激动剂。
215.实施方案214的掩蔽型细胞因子,其中所述sting激动剂是环二核苷酸(cdn)。
216.实施方案215的掩蔽型细胞因子,其中所述cdn选自由cgamp、c-二-amp、c-二-gmp、caimp、c-二-imp、4-(2-氯-6-氟苄基)-n-(呋喃-2-基甲基)-3-氧代-3,4-二氢-2h-苯并[b][1,4]噻嗪-6-甲酰胺组成的组。
217.实施方案214的掩蔽型细胞因子,其中tlr激动剂是选自由tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9和tlr10组成的组的tlr的激动剂。
218.一种掩蔽型细胞因子,其包含:
a)第一半衰期延长结构域和第二半衰期延长结构域;
b)第一掩蔽部分和第二掩蔽部分;和
c)细胞因子或其功能片段,
其中第一掩蔽部分与第一半衰期延长结构域连接,
其中第二掩蔽部分与细胞因子或其功能片段连接。
其中第二掩蔽部分或细胞因子或其功能片段与第二半衰期延长结构域连接,且
其中第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰。
219.实施方案218的掩蔽型细胞因子,其中:
a)第一掩蔽部分经由第一接头与第一半衰期延长结构域连接;和/或
b)第二掩蔽部分或细胞因子或其功能片段经由第二接头与第二半衰期延长结构域连接。
220.实施方案218或实施方案219的掩蔽型细胞因子,其中第二掩蔽部分经由第三接头与细胞因子或其功能片段连接。
221.实施方案218-220中任一项的掩蔽型细胞因子,其中细胞因子或其功能片段是il-2多肽或其功能片段。
222.实施方案221的掩蔽型细胞因子,其中il-2多肽或其功能片段包含选自由seqidno:1-8、160、243-251、230、243-251、260、775-792和813-822组成的组的氨基酸序列。
223.实施方案221的掩蔽型细胞因子,其中il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入降低il-2多肽或其功能片段对cd25(il-2rα)的亲和力的一个或多个氨基酸取代而产生的氨基酸序列。
224.实施方案223的掩蔽型细胞因子,其中氨基酸序列是通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代中的一者或多者产生的:r38a、f42a、f42k、f42e、k43a、y45a、y45n、y45r、e62a、e62r、e62s和l72g。
225.实施方案221的掩蔽型细胞因子,其中il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代而产生的氨基酸序列。
226.实施方案225的掩蔽型细胞因子,其中氨基酸序列是通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代中的一者或多者产生的:h16i、l18c、d20a、d20l、d20f、n29l、l80f、r81d、l85v、186v和i92f。
227.实施方案223或实施方案224的掩蔽型细胞因子,其中氨基酸序列是通过进一步引入增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代产生的。
228.实施方案227的掩蔽型细胞因子,其中增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代选自由h16i、l18c、d20a、d20l、d20f、n29l、l80f、r81d、l85v、i86v和i92f组成的组。
229.实施方案221的掩蔽型细胞因子,其中il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入稳定il-2多肽或其功能片段的一个或多个氨基酸取代而产生的氨基酸序列。
230.实施方案229的掩蔽型细胞因子,其中氨基酸序列是通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代之一产生的:c125s、c125a和c125g。
231.实施方案223-228中任一项的掩蔽型细胞因子,其中氨基酸序列是通过进一步引入稳定il-2多肽或其功能片段的一个或多个氨基酸取代产生的。
232.实施方案231的掩蔽型细胞因子,其中稳定il-2多肽或其功能片段的一个或多个氨基酸取代是氨基酸取代c125s、c125a或c125g。
233.实施方案221-232中任一项的掩蔽型细胞因子,其中第一掩蔽部分包含选自由seqidno:9、10、161-165、187-218、221-229、231、261、826和827组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:9、10、161-165、187-218、221-229、231、261、826和827组成的组的氨基酸序列,并且其中第一掩蔽部分和第二掩蔽部分的氨基酸序列不同。
234.实施方案221-233中任一项的掩蔽型细胞因子,其中:
a)第一掩蔽部分包含seqidno:9或231的氨基酸序列,且第二掩蔽部分包含选自由seqidno:10、161-165、187-218、221-226、261、826和827组成的组的氨基酸序列;或
b)第一掩蔽部分包含选自由seqidno:10、161-165、187-218、221-226、261、826和827组成的组的氨基酸序列,且第二掩蔽部分包含seqidno:9或231的氨基酸序列。
235.实施方案218-220中任一项的掩蔽型细胞因子,其中细胞因子或其功能片段是il-15多肽或其功能片段。
236.实施方案235的掩蔽型细胞因子,其中il-15多肽或其功能片段包含seqidno:167的氨基酸序列。
237.实施方案235或实施方案236的掩蔽型细胞因子,其中
a)第一掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:10、161-165、219-229、261、826和827组成的组的氨基酸序列;
b)第一掩蔽部分包含选自由seqidno:10、161-165、219-229、261、826和827组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列;
c)第一掩蔽部分包含通过向seqidno:232-234和823-825中的任一者的氨基酸序列中引入以下氨基酸取代中的一者或多者而产生的氨基酸序列:r24a、r26a、k34a、s40a、l42a和p67a,且第二掩蔽部分包含选自由seqidno:10、161-165、219-229、261、826和827组成的组的氨基酸序列;或
d)第一掩蔽部分包含选自由seqidno:10、161-165、219-229、261、826和827组成的组的氨基酸序列,且第二掩蔽部分包含通过向seqidno:232-234和823-825中的任一者的氨基酸序列中引入以下氨基酸取代中的一者或多者而产生的氨基酸序列:r24a、r26a、k34a、s40a、l42a和p67a。
238.实施方案218-237中任一项的掩蔽型细胞因子,其中第一半衰期延长结构域是第一抗体或其片段,且第二半衰期延长结构域是第二抗体或其片段。
239.实施方案238的掩蔽型细胞因子,其中:
a)第一抗体或其片段包含第一重链多肽,且第二抗体或其片段包含第二轻链多肽;或
b)第一抗体或其片段包含第一轻链多肽,且第二抗体或其片段包含第二重链多肽。
240.实施方案239的掩蔽型细胞因子,其中第一重链多肽或第二重链多肽包含改变效应子功能的一个或多个氨基酸取代。
241.实施方案240的掩蔽型细胞因子,其中第一重链多肽或第二重链多肽:
a)是igg1同种型,并且包含(多个)氨基取代:
i)n297a、n297g或n297q;
ii)l234a和l235a;
iii)c220s、c226s、c229s和p238s;
iv)c226s、c229s、e233p、l234v和l235a;
v)l234f、l235e和p331s;
vi)s267e和l328f;
vii)d265a;
viii)l234a、l235a和p329g;
b)是igg2同种型,并且包含(多个)氨基酸取代:
i)v234a和g237a;
ii)h268q、v309l、a330s和a331s;或
iii)v234a、g237a、p238s、h268a、v309l、a330s和p331s;或
e)是igg4同种型,并且包含(多个)氨基酸取代:
i)l235a、g237a和e318a;
ii)s228p、l234a和l235a;
iii)h268q、v309l、a330s和p331s;或
iv)s228p和l235a,根据kabateu编号系统编号。
242.实施方案240的掩蔽型细胞因子,其中第一重链多肽或第二重链多肽包含增强效应子功能的一个或多个氨基酸取代。
243.实施方案242的掩蔽型细胞因子,其中第一重链多肽或第二重链多肽是igg1重链多肽,并且包含(多个)氨基酸取代:
a)s298a、e333a和k334a;
b)s239d和i332e;
c)s239d、a330l和i332e;
d)p247i和a339d或a339q;
e)d280h和k290s;
f)d280h、k290s和s298d或s298v;
g)f243l、r292p和y300l;
h)f243l、r292p、y300l和p396l;
i)f243l、r292p、y300l、v305i和p396l;
j)g236a、s239d和i332e;
k)k326a和e333a;
l)k326w和e333s;
m)k290e、s298g和t299a;
n)k290e、s298g、t299a和k326e;
o)k290n、s298g和t299a;
p)k290n、s298g、t299a和k326e;
q)k334v;
r)l235s、s239d和k334v;
s)k334v和q331m、s239d、f243v、e294l或s298t;
t)e233l、q311m和k334v;
u)l234i、q311m和k334v;
v)k334v和s298t、a330m或a330f;
w)k334v、q311m和a330m或a330f;
x)k334v、s298t和a330m或a330f;
y)k334v、s239d和a330m或s298t;
z)l234y、y296w和k290y、f243v或e294l;
aa)y296w和l234y或k290y;
ab)s239d、a330s和i332e,
ac)v264i;
ad)f243l和v264i;
ae)l328m;
af)i332e;
ag)l328m和i332e;
ah)v264i和i332e;
ai)s239e和i332e;
aj)s239q和i332e;
ak)s239e;
al)a330y;
am)i332d;
an)l328i和i332e;
ao)l328q和i332e;
ap)v264t;
aq)v240i;
ar)v266i;
as)s239d;
at)s239d和i332d;
au)s239d和i332n;
av)s239d和i332q;
aw)s239e和i332d;
ax)s239e和i332n;
ay)s239e和i332q;
az)s239n和i332d;
ba)s239n和i332e;
bb)s239q和i332d;
bc)a330y和i332e;
bd)v264i、a330y和i332e;
be)a330l和i332e;
bf)v264i、a330l和i332e;
bg)l234e、l234y或l234i;
bh)l235d、l235s、l235y或l235i;
bi)s239t;
bj)v240m;
bk)v264y;
bl)a330i;
bm)n325t;
bn)i332e和l328d、l328v、l328t或l328i;
bo)v264i、i332e和s239e或s239q;
bp)s239e、v264i、a330y和i332e;
bq)a330y、i332e和s239d或s239n;
br)a330l、i332e和s239d或s239n;
bs)v264i、s298a和i332e;
bt)s298a、i332e和s239d或s239n;
bu)s239d、v264i和i332e;
bv)s239d、v264i、s298a和i332e;
bw)s239d、v264i、a330l和i332e;
bx)s239d、i332e和a330i;
by)p230a;
bz)p230a、e233d和i332e;
ca)e272y;
cb)k274t、k274e、k274r、k274l或k274y;
cd)f275w;
ce)n276l;
cf)y278t;
cg)v302i;
ch)e318r;
ci)s324d、s324i或s324v;
cj)k326i或k326t;
ck)t335d、t335r或t335y;
cl)v240i和v266i;
cm)s239d、a330y、i332e和l234i;
cn)s239d、a330y、i332e和l235d;
co)s239d、a330y、i332e和v240i;
cp)s239d、a330y、i332e和v264t;或
cq)s239d、a330y、i332e和k326e或k326t,根据kabateu编号系统编号。
244.实施方案239的掩蔽型细胞因子,其中第一重链多肽包含选自由seqidno:158、168和169组成的组的氨基酸序列,且第二重链多肽包含选自由seqidno:158、168和169组成的组的氨基酸序列。
245.实施方案239的掩蔽型细胞因子,其中第一轻链多肽包含seqidno:157或170的氨基酸序列,且第二轻链多肽包含seqidno:157或170的氨基酸序列。
246.实施方案238的掩蔽型细胞因子,其中第一抗体或其片段是第一片段可结晶结构域(fc结构域)或其片段,且第二抗体或其片段是第二fc结构域或其片段。
247.实施方案246的掩蔽型细胞因子,其中第一fc结构域或其片段和/或第二fc结构域或其片段包含改变效应子功能的一个或多个氨基酸取代。
248.实施方案247的掩蔽型细胞因子,其中第一fc结构域或其片段和/或第二fc结构域或其片段:
a)是igg1fc结构域或其片段,并且包含(多个)氨基取代:
i)n297a、n297g或n297q;
ii)l234a和l235a;
iii)c220s、c226s、c229s和p238s;
iv)c226s、c229s、e233p、l234v和l235a;
v)l234f、l235e和p331s;
vi)s267e和l328f;
vii)d265a;
viii)l234a、l235a和p329g;
b)是igg2fc结构域或其片段,并且包含(多个)氨基酸取代:
i)v234a和g237a;
ii)h268q、v309l、a330s和a331s;或
iii)v234a、g237a、p238s、h268a、v309l、a330s和p331s;或
e)是igg4fc结构域或其片段,并且包含(多个)氨基酸取代:
i)l235a、g237a和e318a;
ii)s228p、l234a和l235a;
iii)h268q、v309l、a330s和p331s;或
iv)s228p和l235a,根据kabateu编号系统编号。
249.实施方案247的掩蔽型细胞因子,其中第一fc结构域或其片段和/或第二fc结构域或其片段包含增强效应子功能的一个或多个氨基酸取代。
250.实施方案249的掩蔽型细胞因子,其中第一fc结构域或其片段和/或第二fc结构域或其片段是igg1fc结构域或其片段,并且包含(多个)氨基酸取代:
a)s298a、e333a和k334a;
b)s239d和i332e;
c)s239d、a330l和i332e;
d)p247i和a339d或a339q;
e)d280h和k290s;
f)d280h、k290s和s298d或s298v;
g)f243l、r292p和y300l;
h)f243l、r292p、y300l和p396l;
i)f243l、r292p、y300l、v305i和p396l;
j)g236a、s239d和i332e;
k)k326a和e333a;
l)k326w和e333s;
m)k290e、s298g和t299a;
n)k290e、s298g、t299a和k326e;
o)k290n、s298g和t299a;
p)k290n、s298g、t299a和k326e;
q)k334v;
r)l235s、s239d和k334v;
s)k334v和q331m、s239d、f243v、e294l或s298t;
t)e233l、q311m和k334v;
u)l234i、q311m和k334v;
v)k334v和s298t、a330m或a330f;
w)k334v、q311m和a330m或a330f;
x)k334v、s298t和a330m或a330f;
y)k334v、s239d和a330m或s298t;
z)l234y、y296w和k290y、f243v或e294l;
aa)y296w和l234y或k290y;
ab)s239d、a330s和i332e,
ac)v264i;
ad)f243l和v264i;
ae)l328m;
af)i332e;
ag)l328m和i332e;
ah)v264i和i332e;
ai)s239e和i332e;
aj)s239q和i332e;
ak)s239e;
al)a330y;
am)i332d;
an)l328i和i332e;
ao)l328q和i332e;
ap)v264t;
aq)v240i;
ar)v266i;
as)s239d;
at)s239d和i332d;
au)s239d和i332n;
av)s239d和i332q;
aw)s239e和i332d;
ax)s239e和i332n;
ay)s239e和i332q;
az)s239n和i332d;
ba)s239n和i332e;
bb)s239q和i332d;
bc)a330y和i332e;
bd)v264i、a330y和i332e;
be)a330l和i332e;
bf)v264i、a330l和i332e;
bg)l234e、l234y或l234i;
bh)l235d、l235s、l235y或l235i;
bi)s239t;
bj)v240m;
bk)v264y;
bl)a330i;
bm)n325t;
bn)i332e和l328d、l328v、l328t或l328i;
bo)v264i、i332e和s239e或s239q;
bp)s239e、v264i、a330y和i332e;
bq)a330y、i332e和s239d或s239n;
br)a330l、i332e和s239d或s239n;
bs)v264i、s298a和i332e;
bt)s298a、i332e和s239d或s239n;
bu)s239d、v264i和i332e;
bv)s239d、v264i、s298a和i332e;
bw)s239d、v264i、a330l和i332e;
bx)s239d、i332e和a330i;
by)p230a;
bz)p230a、e233d和i332e;
ca)e272y;
cb)k274t、k274e、k274r、k274l或k274y;
cd)f275w;
ce)n276l;
cf)y278t;
cg)v302i;
ch)e318r;
ci)s324d、s324i或s324v;
cj)k326i或k326t;
ck)t335d、t335r或t335y;
cl)v240i和v266i;
cm)s239d、a330y、i332e和l234i;
cn)s239d、a330y、i332e和l235d;
co)s239d、a330y、i332e和v240i;
cp)s239d、a330y、i332e和v264t;或
cq)s239d、a330y、i332e和k326e或k326t,根据kabateu编号系统编号。
251.实施方案246的掩蔽型细胞因子,其中:
a)第一fc结构域或其片段包含seqidno:155的氨基酸序列,且第二fc结构域或其片段包含seqidno:156的氨基酸序列;
b)第一fc结构域或其片段包含seqidno:156的氨基酸序列,且第二fc结构域或其片段包含seqidno:155的氨基酸序列;
c)第一fc结构域或其片段包含seqidno:154的氨基酸序列,且第二fc结构域或其片段包含seqidno:154的氨基酸序列;
d)第一fc结构域或其片段包含seqidno:265的氨基酸序列,且第二fc结构域或其片段包含seqidno:156的氨基酸序列;
e)第一fc结构域或其片段包含seqidno:156的氨基酸序列,且第二fc结构域或其片段包含seqidno:265的氨基酸序列;
f)第一fc结构域或其片段包含seqidno:155的氨基酸序列,且第二fc结构域或其片段包含seqidno:616的氨基酸序列;
g)第一fc结构域或其片段包含seqidno:616的氨基酸序列,且第二fc结构域或其片段包含seqidno:155的氨基酸序列;
h)第一fc结构域或其片段包含seqidno:157的氨基酸序列,且第二fc结构域或其片段包含seqidno:158的氨基酸序列;
i)第一fc结构域或其片段包含seqidno:158的氨基酸序列,且第二fc结构域或其片段包含seqidno:157的氨基酸序列;
j)第一fc结构域或其片段包含seqidno:796的氨基酸序列,且第二fc结构域或其片段包含seqidno:774的氨基酸序列;
k)第一fc结构域或其片段包含seqidno:774的氨基酸序列,且第二fc结构域或其片段包含seqidno:796的氨基酸序列;
l)第一fc结构域或其片段包含seqidno:721的氨基酸序列,且第二fc结构域或其片段包含seqidno:619的氨基酸序列;
m)第一fc结构域或其片段包含seqidno:619的氨基酸序列,且第二fc结构域或其片段包含seqidno:721的氨基酸序列;
n)第一fc结构域或其片段包含seqidno:721的氨基酸序列,且第二fc结构域或其片段包含seqidno:772的氨基酸序列;
o)第一fc结构域或其片段包含seqidno:772的氨基酸序列,且第二fc结构域或其片段包含seqidno:721的氨基酸序列;
p)第一fc结构域或其片段包含seqidno:793的氨基酸序列,且第二fc结构域或其片段包含seqidno:622的氨基酸序列;
q)第一fc结构域或其片段包含seqidno:622的氨基酸序列,且第二fc结构域或其片段包含seqidno:793的氨基酸序列;
r)第一fc结构域或其片段包含seqidno:793的氨基酸序列,且第二fc结构域或其片段包含seqidno:773的氨基酸序列;
s)第一fc结构域或其片段包含seqidno:773的氨基酸序列,且第二fc结构域或其片段包含seqidno:793的氨基酸序列;
t)第一fc结构域或其片段包含seqidno:796的氨基酸序列,且第二fc结构域或其片段包含seqidno:625的氨基酸序列;
u)第一fc结构域或其片段包含seqidno:625的氨基酸序列,且第二fc结构域或其片段包含seqidno:796的氨基酸序列;
v)第一fc结构域或其片段包含seqidno:156的氨基酸序列,且第二fc结构域或其片段包含seqidno:156的氨基酸序列;
w)第一fc结构域或其片段包含seqidno:796的氨基酸序列,且第二fc结构域或其片段包含seqidno:625的氨基酸序列;或
x)第一fc结构域或其片段包含seqidno:625的氨基酸序列,且第二fc结构域或其片段包含seqidno:796的氨基酸序列。
252.实施方案218-237中任一项的掩蔽型细胞因子,其中第一半衰期延长结构域是第一scfv或其片段,且第二半衰期延长结构域是第二scfv或其片段。
253.实施方案218-237中任一项的掩蔽型细胞因子,其中第一半衰期延长结构域是第一fc结构域或其片段,且第二半衰期延长结构域是第二fc结构域或其片段,并且其中第一fc结构域或其片段与第二fc结构域或其片段连接。
254.实施方案253的掩蔽型细胞因子,其中第一fc结构域或其片段经由第四接头与第二fc结构域或其片段连接。
255.实施方案218-237中任一项的掩蔽型细胞因子,其中:
a)第一半衰期延长结构域是scfv或其片段,且第二半衰期延长结构域是抗体或其片段;或
a)第一半衰期延长结构域是抗体或其片段,且第二半衰期延长结构域是scfv或其片段。
256.实施方案238-251中任一项的掩蔽型细胞因子,其中促进第一和第二半衰期延长结构域的缔合的修饰包括:
a)根据kabateu编号系统编号,在第一抗体或其片段中引入s354c和t366w突变,并在第二抗体或其片段中引入y349c、t366s、l368a和y407v突变;
b)根据kabateu编号系统编号,在第二抗体或其片段中引入s354c和t366w突变,并在第一抗体或其片段中引入y349c、t366s、l368a和y407v突变;
c)根据kabateu编号系统编号,在第一抗体或其片段中引入k392d和k409d突变,并在第二抗体或其片段中引入d399k和e356k突变;
d)根据kabateu编号系统编号,在第二抗体或其片段中引入k392d和k409d突变,并在第一抗体或其片段中引入d399k和e356k突变;
e)根据kabateu编号系统编号,在第一抗体或其片段中引入s364h和f405a突变,并在第二抗体或其片段中引入y349t和t394f突变;或
f)根据kabateu编号系统编号,在第二抗体或其片段中引入s364h和f405a突变,并在第一抗体或其片段中引入y349t和t394f突变。
257.实施方案238-251中任一项的掩蔽型细胞因子,其中通过如下方式产生第一抗体或其片段的氨基酸序列和第二抗体或其片段的氨基酸序列:
a)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入s354c和t366w突变,并在seqidno:154或169的氨基酸序列中引入y349c、t366s、l368a和y407v突变;
b)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入s354c和t366w突变,并在seqidno:154或169的氨基酸序列中引入y349c、t366s、l368a和y407v突变;
c)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d和k409d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
d)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d和k409d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
e)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入s364h和f405a突变,并在seqidno:154或169的氨基酸序列中引入y349t和t394f突变;或
f)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入s364h和f405a突变,并在seqidno:154或169的氨基酸序列中引入y349t和t394f突变。
258.实施方案238-251中任一项的掩蔽型细胞因子,其中促进第一和第二半衰期延长结构域的缔合的修饰包括:
a)根据kabateu编号系统编号,在第一抗体或其片段中引入y407t突变,并在第二抗体或其片段中引入t366y突变;
b)根据kabateu编号系统编号,在第一抗体或其片段中引入y407a突变,并在第二抗体或其片段中引入t366w突变;
c)根据kabateu编号系统编号,在第一抗体或其片段中引入f405a突变,并在第二抗体或其片段中引入t394w突变;
d)根据kabateu编号系统编号,在第一抗体或其片段中引入f405w突变,并在第二抗体或其片段中引入t394s突变;
e)根据kabateu编号系统编号,在第一抗体或其片段中引入y407t突变,并在第二抗体或其片段中引入t366y突变;
f)根据kabateu编号系统编号,在第一抗体或其片段中引入t366y和f405a突变,并在第二抗体或其片段中引入t394w和y407t突变;
g)根据kabateu编号系统编号,在第一抗体或其片段中引入t366w和f405w突变,并在第二抗体或其片段中引入t394s和y407a突变;
h)根据kabateu编号系统编号,在第一抗体或其片段中引入f405w和y407a突变,并在第二抗体或其片段中引入t366w和t394s突变;
i)根据kabateu编号系统编号,在第一抗体或其片段中引入t366w突变,并在第二抗体或其片段中引入t366s、l368a和y407v突变;
j)根据kabateu编号系统编号,在第二抗体或其片段中引入y407t突变,并在第一抗体或其片段中引入t366y突变;
k)根据kabateu编号系统编号,在第二抗体或其片段中引入y407a突变,并在第一抗体或其片段中引入t366w突变;
l)根据kabateu编号系统编号,在第二抗体或其片段中引入f405a突变,并在第一抗体或其片段中引入t394w突变;
m)根据kabateu编号系统编号,在第二抗体或其片段中引入f405w突变,并在第一抗体或其片段中引入t394s突变;
n)根据kabateu编号系统编号,在第二抗体或其片段中引入y407t突变,并在第一抗体或其片段中引入t366y突变;
o)根据kabateu编号系统编号,在第二抗体或其片段中引入t366y和f405a突变,并在第一抗体或其片段中引入t394w和y407t突变;
p)根据kabateu编号系统编号,在第二抗体或其片段中引入t366w和f405w突变,并在第一抗体或其片段中引入t394s和y407a突变;
q)根据kabateu编号系统编号,在第二抗体或其片段中引入f405w和y407a突变,并在第一抗体或其片段中引入t366w和t394s突变;或
r)根据kabateu编号系统编号,在第二抗体或其片段中引入t366w突变,并在第一抗体或其片段中引入t366s、l368a和y407v突变。
259.实施方案238-251中任一项的掩蔽型细胞因子,其中通过如下方式产生第一抗体或其片段的氨基酸序列和第二抗体或其片段的氨基酸序列:
a)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407t突变,并在seqidno:154或169的氨基酸序列中引入t366y突变;
b)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407a突变,并在seqidno:154或169的氨基酸序列中引入t366w突变;
c)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405a突变,并在seqidno:154或169的氨基酸序列中引入t394w突变;
d)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405w突变,并在seqidno:154或169的氨基酸序列中引入t394s突变;
e)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407t突变,并在seqidno:154或169的氨基酸序列中引入t366y突变;
f)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366y和f405a突变,并在seqidno:154或169的氨基酸序列中引入t394w和y407t突变;
g)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366w和f405w突变,并在seqidno:154或169的氨基酸序列中引入t394s和y407a突变;
h)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405w和y407a突变,并在seqidno:154或169的氨基酸序列中引入t366w和t394s突变;
i)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366w突变,并在seqidno:154或169的氨基酸序列中引入t366s、l368a和y407v突变;
j)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407t突变,并在seqidno:154或169的氨基酸序列中引入t366y突变;
k)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407a突变,并在seqidno:154或169的氨基酸序列中引入t366w突变;
l)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405a突变,并在seqidno:154或169的氨基酸序列中引入t394w突变;
m)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405w突变,并在seqidno:154或169的氨基酸序列中引入t394s突变;
n)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407t突变,并在seqidno:154或169的氨基酸序列中引入t366y突变;
o)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366y和f405a突变,并在seqidno:154或169的氨基酸序列中引入t394w和y407t突变;
p)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366w和f405w突变,并在seqidno:154或169的氨基酸序列中引入t394s和y407a突变;
q)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405w和y407a突变,并在seqidno:154或169的氨基酸序列中引入t366w和t394s突变;或
r)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366w突变,并在seqidno:154或169的氨基酸序列中引入t366s、l368a和y407v突变。
260.实施方案238-251中任一项的掩蔽型细胞因子,其中促进第一和第二半衰期延长结构域的缔合的修饰包括:
a)根据kabateu编号系统编号,在第一抗体或其片段中引入k409e突变,并在第二抗体或其片段中引入d399k突变;
b)根据kabateu编号系统编号,在第一抗体或其片段中引入k409e突变,并在第二抗体或其片段中引入d399r突变;
c)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d突变,并在第二抗体或其片段中引入d399k突变;
d)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d突变,并在第二抗体或其片段中引入d399r突变;
e)根据kabateu编号系统编号,在第一抗体或其片段中引入k392e突变,并在第二抗体或其片段中引入d399r突变;
f)根据kabateu编号系统编号,在第一抗体或其片段中引入k392e突变,并在第二抗体或其片段中引入d399k突变;
g)根据kabateu编号系统编号,在第一抗体或其片段中引入k392d突变,并在第二抗体或其片段中引入d399r突变;
h)根据kabateu编号系统编号,在第一抗体或其片段中引入k392d突变,并在第二抗体或其片段中引入d399k突变;
i)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k360d突变,并在第二抗体或其片段中引入d399k和e356k突变;
j)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k370d突变,并在第二抗体或其片段中引入d399k和e357k突变;
k)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k392d突变,并在第二抗体或其片段中引入d399k、e356k和e357k突变;
l)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k392d突变,并在第二抗体或其片段中引入d399k突变;
m)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k392d突变,并在第二抗体或其片段中引入d399k和e356k突变;
n)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k392d突变,并在第二抗体或其片段中引入d399k和e357k突变;
o)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k370d突变,并在第二抗体或其片段中引入d399k和e357k突变;
p)根据kabateu编号系统编号,在第一抗体或其片段中引入d399k突变,并在第二抗体或其片段中引入k409d和k360d突变;
q)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k439d突变,并在第二抗体或其片段中引入d399k和e356k突变;
r)根据kabateu编号系统编号,在第二抗体或其片段中引入k409e突变,并在第一抗体或其片段中引入d399k突变;
s)根据kabateu编号系统编号,在第二抗体或其片段中引入k409e突变,并在第一抗体或其片段中引入d399r突变;
t)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d突变,并在第一抗体或其片段中引入d399k突变;
u)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d突变,并在第一抗体或其片段中引入d399r突变;
v)根据kabateu编号系统编号,在第二抗体或其片段中引入k392e突变,并在第一抗体或其片段中引入d399r突变;
w)根据kabateu编号系统编号,在第二抗体或其片段中引入k392e突变,并在第一抗体或其片段中引入d399k突变;
x)根据kabateu编号系统编号,在第二抗体或其片段中引入k392d突变,并在第一抗体或其片段中引入d399r突变;
y)根据kabateu编号系统编号,在第二抗体或其片段中引入k392d突变,并在第一抗体或其片段中引入d399k突变;
z)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k360d突变,并在第一抗体或其片段中引入d399k和e356k突变;
aa)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k370d突变,并在第一抗体或其片段中引入d399k和e357k突变;
ab)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k392d突变,并在第一抗体或其片段中引入d399k、e356k和e357k突变;
ac)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k392d突变,并在第一抗体或其片段中引入d399k突变;
ad)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k392d突变,并在第一抗体或其片段中引入d399k和e356k突变;
ae)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k392d突变,并在第一抗体或其片段中引入d399k和e357k突变;
af)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k370d突变,并在第一抗体或其片段中引入d399k和e357k突变;
ag)根据kabateu编号系统编号,在第二抗体或其片段中引入d399k突变,并在第一抗体或其片段中引入k409d和k360d突变;或
ah)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k439d突变,并在第一抗体或其片段中引入d399k和e356k突变。
261.实施方案238-251中任一项的掩蔽型细胞因子,其中通过如下方式产生第一抗体或其片段的氨基酸序列和第二抗体或其片段的氨基酸序列:
a)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409e突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
b)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409e突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
c)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
d)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
e)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392e突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
f)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392e突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
g)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
h)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
i)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k360d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
j)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k370d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
k)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k、e356k和e357k突变;
l)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
m)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
n)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
o)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k370d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
p)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入d399k突变,并在seqidno:154或169的氨基酸序列中引入k409d和k360d突变;
q)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k439d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
r)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409e突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
s)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409e突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
t)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
u)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
v)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392e突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
w)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392e突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
x)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
y)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
z)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k360d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
aa)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k370d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
ab)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k、e356k和e357k突变;
ac)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
ad)根据kabateu编号系统编号,在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
ae)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
af)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k370d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
ag)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入d399k突变,并在seqidno:154或169的氨基酸序列中引入k409d和k360d突变;或
ah)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k439d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变。
262.实施方案219-261中任一项的掩蔽型细胞因子,其中第一接头包含第一可切割肽;和/或其中第二接头包含第二可切割肽。
263.实施方案219-262中任一项的掩蔽型细胞因子,其中第一接头包含第一n末端间隔区结构域和/或第一c末端间隔区结构域。
264.实施方案263的掩蔽型细胞因子,其中第一接头包含:
a)第一n末端间隔区结构域、第一可切割肽和第一c末端间隔区结构域;
b)第一n末端间隔区结构域和第一可切割肽;
c)第一n末端间隔区结构域和第一c末端间隔区结构域;
d)第一可切割肽和第一c末端间隔区结构域;
e)第一n末端间隔区结构域;或
f)第一c末端间隔区结构域。
265.实施方案219-264中任一项的掩蔽型细胞因子,其中第二接头包含第二n末端间隔区结构域和/或第二c末端间隔区结构域。
266.实施方案265的掩蔽型细胞因子,其中第二接头包含:
a)第二n末端间隔区结构域、第二可切割肽和第二c末端间隔区结构域;
b)第二n末端间隔区结构域和第二可切割肽;
c)第二n末端间隔区结构域和第二c末端间隔区结构域;
d)第二可切割肽和第二c末端间隔区结构域;
e)第二n末端间隔区结构域;或
f)第二c末端间隔区结构域。
267.实施方案262-266中任一项的掩蔽型细胞因子,其中第一可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列;和/或其中第二可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。
268.实施方案263-267中任一项的掩蔽型细胞因子,其中第一n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列,和/或第一c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
269.实施方案262-266中任一项的掩蔽型细胞因子,其中第一可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
270.实施方案269的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
271.实施方案265-270中任一项的掩蔽型细胞因子,其中第二n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列,和/或第二c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
272.实施方案262-271中任一项的掩蔽型细胞因子,其中第二可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
273.实施方案272的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
274.实施方案218-273中任一项的掩蔽型细胞因子,其中第一接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列,和/或第二接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列。
275.实施方案219-274中任一项的掩蔽型细胞因子,其中第三接头包含可切割肽。
276.实施方案219-275中任一项的掩蔽型细胞因子,其中第三接头包含第三n末端间隔区结构域和/或第三c末端间隔区结构域。
277.实施方案276的掩蔽型细胞因子,其中第三接头包含:
a)第三n末端间隔区结构域、第三可切割肽和第三c末端间隔区结构域;
b)第三n末端间隔区结构域和第三可切割肽;
c)第三n末端间隔区结构域和第三c末端间隔区结构域;
d)第三可切割肽和第三c末端间隔区结构域;
e)第三n末端间隔区结构域;或
f)第三c末端间隔区结构域。
278.实施方案275-277中任一项的掩蔽型细胞因子,其中第三可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列;和/或其中第三可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。
279.实施方案276-278中任一项的掩蔽型细胞因子,其中第三n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列,和/或第三c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
280.实施方案275-279中任一项的掩蔽型细胞因子,其中第三可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
281.实施方案280的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
282.实施方案219-281中任一项的掩蔽型细胞因子,其中第三接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列,和/或第三接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列。
283.实施方案254-282中任一项的掩蔽型细胞因子,其中第四接头包含第四n末端间隔区结构域和/或第四c末端间隔区结构域。
284.实施方案283的掩蔽型细胞因子,其中第四n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列,和/或第四c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
285.实施方案262-284中任一项的掩蔽型细胞因子,其中第一可切割肽、第二可切割肽和/或第三可切割肽是共定位在表达细胞因子受体的区域或组织中的蛋白酶的底物。
286.实施方案285的掩蔽型细胞因子,其中细胞因子受体是il-2细胞因子受体或il-15细胞因子受体。
287.实施方案262-286中任一项的掩蔽型细胞因子,其中第一可切割肽、第二可切割肽和/或第三可切割肽被选自由以下组成的组的一种或多种酶切割:abhd12、adam12、abhd12b、abhd13、abhd17a、adam19、adam20、adam21、adam2r、adam30、adam33、adam8、abhd17a、adamdec1、adamts1、adamts10、adamts12、adamts13、adamts14、adamts15、adamts16、adamts17、adamts18、adamts19、adamts2、adamts20、adamts3、adamts4、abhd17b、adamts5、adamts6、adamts7、adamts8、adamts9、adamtsl1、adamtsl2、adamtsl3、abhd17c、adamtsl5、astl、bmp1、cela1、cela2a、cela2b、cela3a、cela3b、adam10、adaml5、adaml7、adam9、adamts4、ctse、ctsf、adamtsl4、cma1、ctrb1、ctrc、ctso、ctr1、ctsa、ctsw、ctsb、ctsc、ctsd、esp1、ctsg、ctsh、gzma、gzmb、gzmh、ctsk、gzmm、ctsl、ctss、ctsv、ctsz、htra4、klk10、klk11、klk13、klk14、klk2、klk4、dpp4、klk6、klk7、klkb1、ece1、ece2、ecel1、masp2、mep1a、mep1b、elane、fap、gzm[a、mmp11、gzmk、hgfac、hpn、htra1、mmp11、mmp16、mmp17、mmp19、htra2、mmp20、mmp21、htra3、htra4、kel、mmp23b、mmp24、mmp25、mmp26、mmp27、mmp28、klk5、mmp3、mmp7、mmp8、mmp9、lgmn、lnpep、masp1、pappa、pappa2、pcsk1、napsa、pcsk5、pcsk6、mme、mmp1、mmp10、plat、plau、plg、prss1、prss12、prss2、prss21、prss3、prss33、prss4、prss55、prss57、mmp12、prss8、prss9、prtn3、mmp13、mmp14、st14、tmprss10、tmprss11a、tmprss11d、tmprss11e、tmprss11f、tmprss12、tmprss13、mmp15、tmprss15、mmp2、tmprss2、tmprss3、tmprss4、tmprss5、tmprss6、tmprss7、tmprss9、nrdc、ovch1、pamr1、pcsk3、phex、tinag、tpsab1、tpsd1和tpsg1。
288.实施方案218-287中任一项的掩蔽型细胞因子,其中第一半衰期延长结构域和/或第二半衰期延长结构域与药剂缀合。
289.实施方案288的掩蔽型细胞因子,其中所述药剂是微管蛋白聚合的抑制剂、dna损伤剂或dna合成抑制剂。
290.实施方案289的掩蔽型细胞因子,其中所述药剂是类美登素、奥瑞他汀、吡咯并苯并二氮杂卓(pbd)二聚体、卡奇霉素、倍癌霉素、吲哚啉并苯并二氮杂卓二聚体或依喜替康衍生物dxd。
291.实施方案288的掩蔽型细胞因子,其中所述药剂是免疫刺激剂。
292.实施方案291的掩蔽型细胞因子,其中所述免疫刺激剂是干扰素基因刺激物(sting)激动剂或toll样受体(tlr)激动剂。
293.实施方案292的掩蔽型细胞因子,其中所述sting激动剂是环二核苷酸(cdn)。
294.实施方案293的掩蔽型细胞因子,其中所述cdn选自由cgamp、c-二-amp、c-二-gmp、caimp、c-二-imp、4-(2-氯-6-氟苄基)-n-(呋喃-2-基甲基)-3-氧代-3,4-二氢-2h-苯并[b][1,4]噻嗪-6-甲酰胺组成的组。
295.实施方案292的掩蔽型细胞因子,其中tlr激动剂是选自由tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9和tlr10组成的组的tlr的激动剂。
296.一种编码实施方案1-295和320-409中任一项的掩蔽型细胞因子的核酸。
297.一种包含实施方案296的核酸的载体。
298.实施方案297的载体,其是表达载体。
299.一种包含实施方案296的核酸的宿主细胞。
300.一种产生掩蔽型细胞因子的方法,包括在产生所述掩蔽型细胞因子的条件下培养实施方案299的宿主细胞。
301.实施方案300的方法,进一步包括回收由宿主细胞产生的掩蔽型细胞因子。
302.一种通过实施方案300或实施方案301的方法产生的掩蔽型细胞因子。
303.一种包含实施方案1-295和320-409中任一项的掩蔽型细胞因子的组合物。
304.一种包含实施方案302的掩蔽型细胞因子的组合物。
305.实施方案303或实施方案304的组合物,其进一步包含抗炎剂或抗癌剂。
306.实施方案305的组合物,其中所述抗癌剂选自由以下组成的组:pd-1抑制剂、egfr抑制剂、her2抑制剂、vegfr抑制剂、ctla-4抑制剂、btla抑制剂、b7h4抑制剂、b7h3抑制剂、csfir抑制剂、hvem抑制剂、cd27抑制剂、kir抑制剂、nkg2a抑制剂、nkg2d激动剂、tweak抑制剂、alk抑制剂、cd52靶向抗体、ccr4靶向抗体、pd-l1抑制剂、kit抑制剂、pdgfr抑制剂、baff抑制剂、hdac抑制剂、vegf配体抑制剂、cd19靶向分子、folr1靶向分子、dll3靶向分子、dkk1靶向分子、muc1靶向分子、muc16靶向分子、psma靶向分子、msln靶向分子、ny-es0-1靶向分子、b7h3靶向分子、b7h4靶向分子、bcma靶向分子、cd29靶向分子、cd151靶向分子、cd123靶向分子、cd33靶向分子、cd37靶向分子、cdh19靶向分子、cea靶向分子、claudin18.2靶向分子、clec12a靶向分子、egfrviii靶向分子、epcam靶向分子、epha2靶向分子、fcrh5靶向分子、flt3靶向分子、gd2靶向分子、磷脂酰肌醇蛋白聚糖3靶向分子、gpa33靶向分子、gprc5d靶向分子、il-23r靶向分子、il-1rap靶向分子、mcsp靶向分子、ron靶向分子、ror1靶向分子、steap2靶向分子、tfr靶向分子、cd166靶向分子、tpbg靶向分子、trop2靶向分子、蛋白酶体抑制剂、abl抑制剂、cd30抑制剂、flt3抑制剂、met抑制剂、ret抑制剂、il-1β抑制剂、mek抑制剂、ros1抑制剂、braf抑制剂、cd38抑制剂、rankl抑制剂、b4galnt1抑制剂、slamf7抑制剂、idh2抑制剂、mtor抑制剂、cd20靶向抗体、btk抑制剂、pi3k抑制剂、flt3抑制剂、parp抑制剂、cdk4抑制剂、cdk6抑制剂、fgfr抑制剂、raf抑制剂、jak1抑制剂、jak2抑制剂、jak3抑制剂、il-6抑制剂、il-17抑制剂、平滑化(smoothened)抑制剂、il-6r抑制剂、bcl2抑制剂、ptch抑制剂、pigf抑制剂、tgfb抑制剂、cd28激动剂、cd3激动剂、cd40激动剂、gitr激动剂、ox40激动剂、vista激动剂、cd137激动剂、lag3抑制剂、tim3抑制剂、tigit抑制剂和il-2r抑制剂。
307.实施方案305的组合物,其中所述抗炎剂是环氧合酶(cox)抑制剂或nf-κb抑制剂。
308.实施方案307的组合物,其中所述cox抑制剂是cox-1和/或cox-2抑制剂。
309.实施方案307或实施方案308的组合物,其中所述cox抑制剂选自由以下组成的组:sc-560、fr122047、p6、莫苯唑酸、tfap、氟比洛芬、酮洛芬、塞来昔布、罗非昔布、美洛昔康、吡罗昔康、德拉昔布、帕瑞昔布、伐地昔布、依托昔布、色烯衍生物、色满衍生物、n-(2-环己氧基硝基苯基)甲磺酰胺、帕瑞考昔、罗美昔布、rs57067、t-614、bms-347070、jte-522、s-2474、svt-2016、ct-3、abt-963、sc-58125、尼美舒利、氟舒胺、ns-398、l-745337、rwj-63556、l-784512、达布飞龙、cs-502、las-34475、las-34555、s-33516、双氯芬酸、甲芬那酸、sd-8381、布洛芬、萘普生、酮咯酸、吲哚美辛、阿司匹林、萘普生、托美汀、吡罗昔康和甲氯芬那酸酯。
310.实施方案307的组合物,其中所述nf-κb抑制剂选自由ikk复合物抑制剂、iκb降解抑制剂、nf-κb核易位抑制剂、p65乙酰化抑制剂、nf-κbdna结合抑制剂、nf-κb反式激活抑制剂和p53诱导抑制剂组成的组。
311.实施方案307或实施方案308的组合物,其中所述nf-κb抑制剂选自由以下组成的组:tpca-1、nf-κb激活抑制剂vi(bot-64)、bms-345541、氨来占诺、sc-514(gk-01140)、imd-0354、ikk-16、bay-11-7082、mg-115、mg-132、乳胞素、环氧酶素、小白菊内酯、卡非佐米、mln-4924(pevonedistat)、jsh-23咯利普兰、没食子酸、漆树酸、gyy-4137、p-xsc、cv-3988、前列腺素e2(pge2)、ly-294002、渥曼青霉素、美沙拉嗪、奎纳克林和夫拉平度。
312.一种药物组合物,其包含实施方案1-295和320-409中任一项的掩蔽型细胞因子和药学上可接受的载体。
313.一种药物组合物,其包含实施方案302的掩蔽型细胞因子和药学上可接受的载体。
314.一种试剂盒,其包含实施方案1-295和320-409中任一项的掩蔽型细胞因子,或实施方案303-311中任一项的组合物,或实施方案312或313的药物组合物。
315.一种治疗或预防受试者的肿瘤性疾病的方法,所述方法包括对受试者施用有效量的实施方案1-295和320-409中任一项的掩蔽型细胞因子或实施方案303-311中任一项的组合物。
316.实施方案315的方法,其中所述肿瘤性疾病是癌症。
317.实施方案316的方法,其中所述癌症是白血病、淋巴瘤、头颈癌、结肠直肠癌、前列腺癌、胰腺癌、黑素瘤、乳腺癌、成神经细胞瘤、肺癌、卵巢癌、骨肉瘤、膀胱癌、宫颈癌、肝癌、肾癌、皮肤癌或睾丸癌。
318.一种治疗或预防受试者的炎性或自身免疫性疾病的方法,所述方法包括对受试者施用有效量的实施方案1-295和320-409中任一项的掩蔽型细胞因子或实施方案303-311中任一项的组合物。
319.实施方案318的方法,其中所述炎性或自身免疫性疾病选自由以下组成的组:动脉粥样硬化、肥胖症、炎性肠病(ibd)、类风湿性关节炎、过敏性脑炎、银屑病、特应性皮肤病、骨质疏松症、腹膜炎、肝炎、狼疮、乳糜泻、舍格伦综合征、风湿性多肌痛、多发性硬化(ms)、强直性脊柱炎、1型糖尿病、斑秃、血管炎和颞动脉炎、移植物抗宿主病(gvhd)、哮喘、copd、副肿瘤性自身免疫性疾病、软骨炎症、幼年型关节炎、幼年型类风湿性关节炎、少关节幼年型类风湿性关节炎、多关节幼年型类风湿性关节炎、全身发作性幼年型类风湿性关节炎、幼年型强直性脊柱炎、幼年型肠病性关节炎、幼年型反应性关节炎、幼年型赖特尔综合征、sea综合征(血清阴性、接骨点病变、关节病综合征)、幼年型皮肌炎、幼年型银屑病关节炎、幼年型硬皮病、幼年型全身性红斑狼疮、幼年型血管炎、少关节类风湿性关节炎、全身发作性类风湿性关节炎、肠病性关节炎、反应性关节炎、赖特尔综合征、皮肌炎、银屑病关节炎、硬皮病、血管炎、肌炎、多肌炎、皮肌炎、结节性多动脉炎、韦格纳肉芽肿病、动脉炎、风湿性多肌痛、结节病、硬化症、原发性胆汁性硬化、硬化性胆管炎、银屑病、斑块状银屑病、滴状银屑病、反型银屑病、脓疱性银屑病、红皮病性银屑病、皮炎、特应性皮炎、动脉粥样硬化、斯蒂尔病、全身性红斑狼疮(sle)、重症肌无力、克罗恩病、溃疡性结肠炎、乳糜泻、鼻窦炎、具有息肉的鼻窦炎、嗜酸性食管炎、嗜酸性支气管炎、格林-巴利病、甲状腺炎(例如,格雷夫斯病)、阿狄森病、雷诺现象、自身免疫性肝炎、移植排斥、肾损伤、丙型肝炎诱导的血管炎和自发性妊娠丢失。
320.一种掩蔽型细胞因子,其包含:
a)包含seqidno:155的氨基酸序列的第一半衰期延长结构域和包含seqidno:156的氨基酸序列的第二半衰期延长结构域;
b)包含seqidno:261的氨基酸序列的掩蔽部分;以及
c)包含seqidno:3的氨基酸序列的细胞因子或其功能片段,
其中掩蔽部分与第一半衰期延长结构域连接,
其中细胞因子或其功能片段与第二半衰期延长结构域连接,且
其中第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰。
321.实施方案320的掩蔽型细胞因子,其中掩蔽部分经由第一接头与第一半衰期延长结构域连接,且其中细胞因子或其功能片段经由第二接头与第二半衰期延长结构域连接。
322.实施方案321的掩蔽型细胞因子,其中第一接头包含seqidno:28的氨基酸序列。
323.实施方案321或实施方案322的掩蔽型细胞因子,其中第二接头包含有包含seqidno:264的氨基酸序列的可切割肽。
324.实施方案321-323中任一项的掩蔽型细胞因子,其中第二接头包含seqidno:811的氨基酸序列。
325.实施方案320-324中任一项的掩蔽型细胞因子,其中所述掩蔽型细胞因子包含seqidno:266的氨基酸序列。
326.实施方案320-325中任一项的掩蔽型细胞因子,其中所述掩蔽型细胞因子包含seqidno:267的氨基酸序列。
327.实施方案320-326中任一项的掩蔽型细胞因子,其中所述掩蔽型细胞因子包含seqidno:266和267的氨基酸序列。
328.实施方案1的掩蔽型细胞因子,其中所述掩蔽型细胞因子包含选自由seqidno:585-597、602、610-614、627-636、642和643组成的组的氨基酸序列。
329.实施方案70的掩蔽型细胞因子,其中所述掩蔽型细胞因子包含选自由seqidno:567和598-601组成的组的氨基酸序列。
330.实施方案149的掩蔽型细胞因子,其中所述掩蔽型细胞因子包含以下氨基酸序列:seqidno:562和563;或seqidno:608和603;或seqidno:604和603;或seqidno:605和603;或seqidno:606和603;或seqidno:615和617;或seqidno:266和267;或seqidno:618和620;或seqidno:621和623;或seqidno:624和626;或seqidno:608和267;或seqidno:663和664;或seqidno:665和666;或seqidno:667和267;或seqidno:669和267;或seqidno:670和671;或seqidno:670和671;或seqidno:672和267;或seqidno:673和267;或seqidno:674和267;或seqidno:675和267;或seqidno:676和267;或seqidno:677和267;或seqidno:678和267;或seqidno:679和267;或seqidno:680和267;或seqidno:681和267;或seqidno:682和267;或seqidno:683和267;或seqidno:684和267;或seqidno:685和267;或seqidno:686和267;seqidno:687和267;或seqidno:688和267;或seqidno:689和267;或seqidno:690和267;或seqidno:692和267;或seqidno:693和267;或seqidno:694和267;或seqidno:695和267;或seqidno:696和267;或seqidno:697和267;或seqidno:698和267;或seqidno:699和267;或seqidno:700和267;或seqidno:701和267;或seqidno:702和267;或seqidno:703和267;或seqidno:704和267;或seqidno:705和267;或seqidno:706和267;或seqidno:707和267;或seqidno:708和267;或seqidno:709和267;或seqidno:710和267;或seqidno:711和267;或seqidno:712和667;或seqidno:713和267;或seqidno:714和267;或seqidno:716和699;或seqidno:717和267;或seqidno:718和267;或seqidno:719和267;或seqidno:720和267;或seqidno:722和267;或seqidno:723和267;或seqidno:720和267;或seqidno:728和267;或seqidno:729和267;或seqidno:730和267;或seqidno:731和267;或seqidno:732和267;或seqidno:733和267;或seqidno:734和267;或seqidno:735和267;或seqidno:736和267;或seqidno:737和267;或seqidno:738和267;或seqidno:739和267;或seqidno:740和267;或seqidno:741和267;或seqidno:742和267;或seqidno:743和267;或seqidno:744和267;或seqidno:745和267;或seqidno:746和267;或seqidno:674和828;或seqidno:674和829;或seqidno:726和830;或seqidno:726和829;或seqidno:747和671;或seqidno:715和267;或seqidno:715和671;或seqidno:748和671;或seqidno:749和671;或seqidno:750和671;或seqidno:751和671;或seqidno:752和671;或seqidno:753和671;或seqidno:754和671;或seqidno:758和671;或seqidno:759和671;或seqidno:760和671;或seqidno:761和671。
331.实施方案218的掩蔽型细胞因子,其中所述掩蔽型细胞因子包含以下氨基酸序列:seqidno:755和616;或seqidno:756和616;或seqidno:757和616。
332.一种掩蔽型细胞因子,其包含:
a)第一半衰期延长结构域和第二半衰期延长结构域;
b)第一掩蔽部分和第二掩蔽部分;以及
c)细胞因子或其功能片段,
其中第一掩蔽部分与第一半衰期延长结构域连接,
其中第二掩蔽部分与第一掩蔽部分连接,
其中细胞因子或其功能片段与第二半衰期延长结构域连接,且
其中第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰。
333.实施方案332的掩蔽型细胞因子,其中:
a)第一掩蔽部分经由第一接头与第一半衰期延长结构域连接;和/或
b)第二掩蔽部分经由第二接头与第一掩蔽部分连接。
334.实施方案332或333的掩蔽型细胞因子,其中所述细胞因子或其功能片段经由第三接头与第二半衰期延长结构域连接。
335.实施方案332-334中任一项的掩蔽型细胞因子,其中所述细胞因子或其功能片段是il-2多肽或其功能片段。
336.实施方案335的掩蔽型细胞因子,其中il-2多肽或其功能片段包含选自由seqidno:1-8、160、243-251、230、243-251、260、775-792和813-822组成的组的氨基酸序列。
337.实施方案335的掩蔽型细胞因子,其中il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入降低il-2多肽或其功能片段对cd25(il-2rα)的亲和力的一个或多个氨基酸取代而产生的氨基酸序列。
338.实施方案337的掩蔽型细胞因子,其中氨基酸序列是通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代中的一者或多者产生的:r38a、f42a、f42k、f42e、k43a、y45a、y45n、y45r、e62a、e62r、e62s和l72g。
339.实施方案335的掩蔽型细胞因子,其中il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代而产生的氨基酸序列。
340.实施方案339的掩蔽型细胞因子,其中氨基酸序列是通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代中的一者或多者产生的:h16i、l18c、d20a、d20l、d20f、n29l、l80f、r81d、l85v、i86v和i92f。
341.实施方案337或实施方案338的掩蔽型细胞因子,其中氨基酸序列是通过进一步引入增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代产生的。
342.实施方案341的掩蔽型细胞因子,其中增加il-2多肽或其功能片段对il-2rβ或il-2rγ的亲和力的一个或多个氨基酸取代选自由h16i、l18c、d20a、d20l、d20f、n29l、l80f、r81d、l85v、i86v和i92f组成的组。
343.实施方案335的掩蔽型细胞因子,其中il-2多肽或其功能片段包含通过向il-2多肽或其功能片段的氨基酸序列中引入稳定il-2多肽或其功能片段的一个或多个氨基酸取代而产生的氨基酸序列。
344.实施方案343的掩蔽型细胞因子,其中氨基酸序列是通过向seqidno:1-8、160、243-251、260、775-792和813-822中的任一者中引入以下氨基酸取代之一产生的:c125s、c125a和c125g。
345.实施方案337-342中任一项的掩蔽型细胞因子,其中氨基酸序列是通过进一步引入稳定il-2多肽或其功能片段的一个或多个氨基酸取代产生的。
346.实施方案345的掩蔽型细胞因子,其中稳定il-2多肽或其功能片段的一个或多个氨基酸取代是氨基酸取代c125s、c125a或c125g。
347.实施方案335-346中任一项的掩蔽型细胞因子,其中第一掩蔽部分包含选自由seqidno:9、10、161-165、187-218、221-229、231、261、826和827组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:9、10、161-165、187-218、221-229、231、261、826和827组成的组的氨基酸序列,并且其中第一掩蔽部分和第二掩蔽部分的氨基酸序列不同。
348.实施方案335-347中任一项的掩蔽型细胞因子,其中:
a)第一掩蔽部分包含seqidno:9或231的氨基酸序列,且第二掩蔽部分包含选自由seqidno:10、161-165、187-218、221-226、261、826和827组成的组的氨基酸序列;或
b)第一掩蔽部分包含选自由seqidno:10、161-165、187-218、221-226、261、826和827组成的组的氨基酸序列,且第二掩蔽部分包含seqidno:9或231的氨基酸序列。
349.实施方案332-334中任一项的掩蔽型细胞因子,其中所述细胞因子或其功能片段是il-15多肽或其功能片段。
350.实施方案349的掩蔽型细胞因子,其中il-15多肽或其功能片段包含seqidno:167的氨基酸序列。
351.实施方案349或实施方案350的掩蔽型细胞因子,其中
a)第一掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:10、161-165、219-229、261、826和827组成的组的氨基酸序列;
b)第一掩蔽部分包含选自由seqidno:10、161-165、219-229、261、826和827组成的组的氨基酸序列,且第二掩蔽部分包含选自由seqidno:232-234和823-825组成的组的氨基酸序列;
c)第一掩蔽部分包含通过向seqidno:232-234和823-825中的任一者的氨基酸序列中引入以下氨基酸取代中的一者或多者而产生的氨基酸序列:r24a、r26a、k34a、s40a、l42a和p67a,且第二掩蔽部分包含选自由seqidno:10、161-165、219-229、261、826和827组成的组的氨基酸序列;或
d)第一掩蔽部分包含选自由seqidno:10、161-165、219-229、261、826和827组成的组的氨基酸序列,且第二掩蔽部分包含通过向seqidno:232-234和823-825中的任一者的氨基酸序列中引入以下氨基酸取代中的一者或多者而产生的氨基酸序列:r24a、r26a、k34a、s40a、l42a和p67a。
352.实施方案332-351中任一项的掩蔽型细胞因子,其中第一半衰期延长结构域是第一抗体或其片段,且第二半衰期延长结构域是第二抗体或其片段。
353.实施方案352的掩蔽型细胞因子,其中:
a)第一抗体或其片段包含第一重链多肽,且第二抗体或其片段包含第二轻链多肽;或
b)第一抗体或其片段包含第一轻链多肽,且第二抗体或其片段包含第二重链多肽。
354.实施方案353的掩蔽型细胞因子,其中第一重链多肽或第二重链多肽包含改变效应子功能的一个或多个氨基酸取代。
355.实施方案354的掩蔽型细胞因子,其中第一重链多肽或第二重链多肽:
a)是igg1同种型,并且包含(多个)氨基取代:
i)n297a、n297g或n297q;
ii)l234a和l235a;
iii)c220s、c226s、c229s和p238s;
iv)c226s、c229s、e233p、l234v和l235a;
v)l234f、l235e和p331s;
vi)s267e和l328f;
vii)d265a;
viii)l234a、l235a和p329g;
b)是igg2同种型,并且包含(多个)氨基酸取代:
i)v234a和g237a;
ii)h268q、v309l、a330s和a331s;或
iii)v234a、g237a、p238s、h268a、v309l、a330s和p331s;或
e)是igg4同种型,并且包含(多个)氨基酸取代:
i)l235a、g237a和e318a;
ii)s228p、l234a和l235a;
iii)h268q、v309l、a330s和p331s;或
iv)s228p和l235a,根据kabateu编号系统编号。
356.实施方案353的掩蔽型细胞因子,其中第一重链多肽或第二重链多肽包含增强效应子功能的一个或多个氨基酸取代。
357.实施方案356的掩蔽型细胞因子,其中第一重链多肽或第二重链多肽是igg1重链多肽,并且包含(多个)氨基酸取代:
a)s298a、e333a和k334a;
b)s239d和i332e;
c)s239d、a330l和i332e;
d)p247i和a339d或a339q;
e)d280h和k290s;
f)d280h、k290s和s298d或s298v;
g)f243l、r292p和y300l;
h)f243l、r292p、y300l和p396l;
i)f243l、r292p、y300l、v305i和p396l;
j)g236a、s239d和i332e;
k)k326a和e333a;
l)k326w和e333s;
m)k290e、s298g和t299a;
n)k290e、s298g、t299a和k326e;
o)k290n、s298g和t299a;
p)k290n、s298g、t299a和k326e;
q)k334v;
r)l235s、s239d和k334v;
s)k334v和q331m、s239d、f243v、e294l或s298t;
t)e233l、q311m和k334v;
u)l234i、q311m和k334v;
v)k334v和s298t、a330m或a330f;
w)k334v、q311m和a330m或a330f;
x)k334v、s298t和a330m或a330f;
y)k334v、s239d和a330m或s298t;
z)l234y、y296w和k290y、f243v或e294l;
aa)y296w和l234y或k290y;
ab)s239d、a330s和i332e,
ac)v264i;
ad)f243l和v264i;
ae)l328m;
af)i332e;
ag)l328m和i332e;
ah)v264i和i332e;
ai)s239e和i332e;
aj)s239q和i332e;
ak)s239e;
al)a330y;
am)i332d;
an)l328i和i332e;
ao)l328q和i332e;
ap)v264t;
aq)v240i;
ar)v266i;
as)s239d;
at)s239d和i332d;
au)s239d和i332n;
av)s239d和i332q;
aw)s239e和i332d;
ax)s239e和i332n;
ay)s239e和i332q;
az)s239n和i332d;
ba)s239n和i332e;
bb)s239q和i332d;
bc)a330y和i332e;
bd)v264i、a330y和i332e;
be)a330l和i332e;
bf)v264i、a330l和i332e;
bg)l234e、l234y或l234i;
bh)l235d、l235s、l235y或l235i;
bi)s239t;
bj)v240m;
bk)v264y;
bl)a330i;
bm)n325t;
bn)i332e和l328d、l328v、l328t或l328i;
bo)v264i、i332e和s239e或s239q;
bp)s239e、v264i、a330y和i332e;
bq)a330y、i332e和s239d或s239n;
br)a330l、i332e和s239d或s239n;
bs)v264i、s298a和i332e;
bt)s298a、i332e和s239d或s239n;
bu)s239d、v264i和i332e;
bv)s239d、v264i、s298a和i332e;
bw)s239d、v264i、a330l和i332e;
bx)s239d、i332e和a330i;
by)p230a;
bz)p230a、e233d和i332e;
ca)e272y;
cb)k274t、k274e、k274r、k274l或k274y;
cd)f275w;
ce)n276l;
cf)y278t;
cg)v302i;
ch)e318r;
ci)s324d、s324i或s324v;
cj)k326i或k326t;
ck)t335d、t335r或t335y;
cl)v240i和v266i;
cm)s239d、a330y、i332e和l234i;
cn)s239d、a330y、i332e和l235d;
co)s239d、a330y、i332e和v240i;
cp)s239d、a330y、i332e和v264t;或
cq)s239d、a330y、i332e和k326e或k326t,根据kabateu编号系统编号。
358.实施方案353的掩蔽型细胞因子,其中第一重链多肽包含选自由seqidno:158、168和169组成的组的氨基酸序列,且第二重链多肽包含选自由seqidno:158、168和169组成的组的氨基酸序列。
359.实施方案353的掩蔽型细胞因子,其中第一轻链多肽包含seqidno:157或170的氨基酸序列,且第二轻链多肽包含seqidno:157或170的氨基酸序列。
360.实施方案352的掩蔽型细胞因子,其中第一抗体或其片段是第一片段可结晶结构域(fc结构域)或其片段,且第二抗体或其片段是第二fc结构域或其片段。
361.实施方案360的掩蔽型细胞因子,其中第一fc结构域或其片段和/或第二fc结构域或其片段包含改变效应子功能的一个或多个氨基酸取代。
362.实施方案361的掩蔽型细胞因子,其中第一fc结构域或其片段和/或第二fc结构域或其片段:
a)是igg1fc结构域或其片段,并且包含(多个)氨基取代:
i)n297a、n297g或n297q;
ii)l234a和l235a;
iii)c220s、c226s、c229s和p238s;
iv)c226s、c229s、e233p、l234v和l235a;
v)l234f、l235e和p331s;
vi)s267e和l328f;
vii)d265a;
viii)l234a、l235a和p329g;
b)是igg2fc结构域或其片段,并且包含(多个)氨基酸取代:
i)v234a和g237a;
ii)h268q、v309l、a330s和a331s;或
iii)v234a、g237a、p238s、h268a、v309l、a330s和p331s;或
e)是igg4fc结构域或其片段,并且包含(多个)氨基酸取代:
i)l235a、g237a和e318a;
ii)s228p、l234a和l235a;
iii)h268q、v309l、a330s和p331s;或
iv)s228p和l235a,根据kabateu编号系统编号。
363.实施方案361的掩蔽型细胞因子,其中第一fc结构域或其片段和/或第二fc结构域或其片段包含增强效应子功能的一个或多个氨基酸取代。
364.实施方案363的掩蔽型细胞因子,其中第一fc结构域或其片段和/或第二fc结构域或其片段是igg1fc结构域或其片段,并且包含(多个)氨基酸取代:
a)s298a、e333a和k334a;
b)s239d和i332e;
c)s239d、a330l和i332e;
d)p247i和a339d或a339q;
e)d280h和k290s;
f)d280h、k290s和s298d或s298v;
g)f243l、r292p和y300l;
h)f243l、r292p、y300l和p396l;
i)f243l、r292p、y300l、v305i和p396l;
j)g236a、s239d和i332e;
k)k326a和e333a;
l)k326w和e333s;
m)k290e、s298g和t299a;
n)k290e、s298g、t299a和k326e;
o)k290n、s298g和t299a;
p)k290n、s298g、t299a和k326e;
q)k334v;
r)l235s、s239d和k334v;
s)k334v和q331m、s239d、f243v、e294l或s298t;
t)e233l、q311m和k334v;
u)l234i、q311m和k334v;
v)k334v和s298t、a330m或a330f;
w)k334v、q311m和a330m或a330f;
x)k334v、s298t和a330m或a330f;
y)k334v、s239d和a330m或s298t;
z)l234y、y296w和k290y、f243v或e294l;
aa)y296w和l234y或k290y;
ab)s239d、a330s和i332e,
ac)v264i;
ad)f243l和v264i;
ae)l328m;
af)i332e;
ag)l328m和i332e;
ah)v264i和i332e;
ai)s239e和i332e;
aj)s239q和i332e;
ak)s239e;
al)a330y;
am)i332d;
an)l328i和i332e;
ao)l328q和i332e;
ap)v264t;
aq)v240i;
ar)v266i;
as)s239d;
at)s239d和i332d;
au)s239d和i332n;
av)s239d和i332q;
aw)s239e和i332d;
ax)s239e和i332n;
ay)s239e和i332q;
az)s239n和i332d;
ba)s239n和i332e;
bb)s239q和i332d;
bc)a330y和i332e;
bd)v264i、a330y和i332e;
be)a330l和i332e;
bf)v264i、a330l和i332e;
bg)l234e、l234y或l234i;
bh)l235d、l235s、l235y或l235i;
bi)s239t;
bj)v240m;
bk)v264y;
bl)a330i;
bm)n325t;
bn)i332e和l328d、l328v、l328t或l328i;
bo)v264i、i332e和s239e或s239q;
bp)s239e、v264i、a330y和i332e;
bq)a330y、i332e和s239d或s239n;
br)a330l、i332e和s239d或s239n;
bs)v264i、s298a和i332e;
bt)s298a、i332e和s239d或s239n;
bu)s239d、v264i和i332e;
bv)s239d、v264i、s298a和i332e;
bw)s239d、v264i、a330l和i332e;
bx)s239d、i332e和a330i;
by)p230a;
bz)p230a、e233d和i332e;
ca)e272y;
cb)k274t、k274e、k274r、k274l或k274y;
cd)f275w;
ce)n276l;
cf)y278t;
cg)v302i;
ch)e318r;
ci)s324d、s324i或s324v;
cj)k326i或k326t;
ck)t335d、t335r或t335y;
cl)v240i和v266i;
cm)s239d、a330y、i332e和l234i;
cn)s239d、a330y、i332e和l235d;
co)s239d、a330y、i332e和v240i;
cp)s239d、a330y、i332e和v264t;或
cq)s239d、a330y、i332e和k326e或k326t,根据kabateu编号系统编号。
365.实施方案360的掩蔽型细胞因子,其中:
a)第一fc结构域或其片段包含seqidno:155的氨基酸序列,且第二fc结构域或其片段包含seqidno:156的氨基酸序列;
b)第一fc结构域或其片段包含seqidno:156的氨基酸序列,且第二fc结构域或其片段包含seqidno:155的氨基酸序列;
c)第一fc结构域或其片段包含seqidno:154的氨基酸序列,且第二fc结构域或其片段包含seqidno:154的氨基酸序列;
d)第一fc结构域或其片段包含seqidno:265的氨基酸序列,且第二fc结构域或其片段包含seqidno:156的氨基酸序列;
e)第一fc结构域或其片段包含seqidno:156的氨基酸序列,且第二fc结构域或其片段包含seqidno:265的氨基酸序列;
f)第一fc结构域或其片段包含seqidno:155的氨基酸序列,且第二fc结构域或其片段包含seqidno:616的氨基酸序列;
g)第一fc结构域或其片段包含seqidno:616的氨基酸序列,且第二fc结构域或其片段包含seqidno:155的氨基酸序列;
h)第一fc结构域或其片段包含seqidno:157的氨基酸序列,且第二fc结构域或其片段包含seqidno:158的氨基酸序列;
i)第一fc结构域或其片段包含seqidno:158的氨基酸序列,且第二fc结构域或其片段包含seqidno:157的氨基酸序列;
j)第一fc结构域或其片段包含seqidno:796的氨基酸序列,且第二fc结构域或其片段包含seqidno:774的氨基酸序列;
k)第一fc结构域或其片段包含seqidno:774的氨基酸序列,且第二fc结构域或其片段包含seqidno:796的氨基酸序列;
l)第一fc结构域或其片段包含seqidno:721的氨基酸序列,且第二fc结构域或其片段包含seqidno:619的氨基酸序列;
m)第一fc结构域或其片段包含seqidno:619的氨基酸序列,且第二fc结构域或其片段包含seqidno:721的氨基酸序列;
n)第一fc结构域或其片段包含seqidno:721的氨基酸序列,且第二fc结构域或其片段包含seqidno:772的氨基酸序列;
o)第一fc结构域或其片段包含seqidno:772的氨基酸序列,且第二fc结构域或其片段包含seqidno:721的氨基酸序列;
p)第一fc结构域或其片段包含seqidno:793的氨基酸序列,且第二fc结构域或其片段包含seqidno:622的氨基酸序列;
q)第一fc结构域或其片段包含seqidno:622的氨基酸序列,且第二fc结构域或其片段包含seqidno:793的氨基酸序列;
r)第一fc结构域或其片段包含seqidno:793的氨基酸序列,且第二fc结构域或其片段包含seqidno:773的氨基酸序列;
s)第一fc结构域或其片段包含seqidno:773的氨基酸序列,且第二fc结构域或其片段包含seqidno:793的氨基酸序列;
t)第一fc结构域或其片段包含seqidno:796的氨基酸序列,且第二fc结构域或其片段包含seqidno:625的氨基酸序列;
u)第一fc结构域或其片段包含seqidno:625的氨基酸序列,且第二fc结构域或其片段包含seqidno:796的氨基酸序列;
v)第一fc结构域或其片段包含seqidno:156的氨基酸序列,且第二fc结构域或其片段包含seqidno:156的氨基酸序列;
w)第一fc结构域或其片段包含seqidno:796的氨基酸序列,且第二fc结构域或其片段包含seqidno:625的氨基酸序列;或
x)第一fc结构域或其片段包含seqidno:625的氨基酸序列,且第二fc结构域或其片段包含seqidno:796的氨基酸序列。
366.实施方案332-351中任一项的掩蔽型细胞因子,其中第一半衰期延长结构域是第一scfv或其片段,且第二半衰期延长结构域是第二scfv或其片段。
367.实施方案332-351中任一项的掩蔽型细胞因子,其中第一半衰期延长结构域是第一fc结构域或其片段,且第二半衰期延长结构域是第二fc结构域或其片段,并且其中第一fc结构域或其片段与第二fc结构域或其片段连接。
368.实施方案367的掩蔽型细胞因子,其中第一fc结构域或其片段经由第四接头与第二fc结构域或其片段连接。
369.实施方案232-351中任一项的掩蔽型细胞因子,其中:
a)第一半衰期延长结构域是scfv或其片段,且第二半衰期延长结构域是抗体或其片段;或
a)第一半衰期延长结构域是抗体或其片段,且第二半衰期延长结构域是scfv或其片段。
370.实施方案352-365中任一项的掩蔽型细胞因子,其中促进第一和第二半衰期延长结构域的缔合的修饰包括:
a)根据kabateu编号系统编号,在第一抗体或其片段中引入s354c和t366w突变,并在第二抗体或其片段中引入y349c、t366s、l368a和y407v突变;
b)根据kabateu编号系统编号,在第二抗体或其片段中引入s354c和t366w突变,并在第一抗体或其片段中引入y349c、t366s、l368a和y407v突变;
c)根据kabateu编号系统编号,在第一抗体或其片段中引入k392d和k409d突变,并在第二抗体或其片段中引入d399k和e356k突变;
d)根据kabateu编号系统编号,在第二抗体或其片段中引入k392d和k409d突变,并在第一抗体或其片段中引入d399k和e356k突变;
e)根据kabateu编号系统编号,在第一抗体或其片段中引入s364h和f405a突变,并在第二抗体或其片段中引入y349t和t394f突变;或
f)根据kabateu编号系统编号,在第二抗体或其片段中引入s364h和f405a突变,并在第一抗体或其片段中引入y349t和t394f突变。
371.实施方案352-365中任一项的掩蔽型细胞因子,其中通过如下方式产生第一抗体或其片段的氨基酸序列和第二抗体或其片段的氨基酸序列:
a)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入s354c和t366w突变,并在seqidno:154或169的氨基酸序列中引入y349c、t366s、l368a和y407v突变;
b)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入s354c和t366w突变,并在seqidno:154或169的氨基酸序列中引入y349c、t366s、l368a和y407v突变;
c)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d和k409d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
d)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d和k409d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
e)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入s364h和f405a突变,并在seqidno:154或169的氨基酸序列中引入y349t和t394f突变;或
f)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入s364h和f405a突变,并在seqidno:154或169的氨基酸序列中引入y349t和t394f突变。
372.实施方案352-365中任一项的掩蔽型细胞因子,其中促进第一和第二半衰期延长结构域的缔合的修饰包括:
a)根据kabateu编号系统编号,在第一抗体或其片段中引入y407t突变,并在第二抗体或其片段中引入t366y突变;
b)根据kabateu编号系统编号,在第一抗体或其片段中引入y407a突变,并在第二抗体或其片段中引入t366w突变;
c)根据kabateu编号系统编号,在第一抗体或其片段中引入f405a突变,并在第二抗体或其片段中引入t394w突变;
d)根据kabateu编号系统编号,在第一抗体或其片段中引入f405w突变,并在第二抗体或其片段中引入t394s突变;
e)根据kabateu编号系统编号,在第一抗体或其片段中引入y407t突变,并在第二抗体或其片段中引入t366y突变;
f)根据kabateu编号系统编号,在第一抗体或其片段中引入t366y和f405a突变,并在第二抗体或其片段中引入t394w和y407t突变;
g)根据kabateu编号系统编号,在第一抗体或其片段中引入t366w和f405w突变,并在第二抗体或其片段中引入t394s和y407a突变;
h)根据kabateu编号系统编号,在第一抗体或其片段中引入f405w和y407a突变,并在第二抗体或其片段中引入t366w和t394s突变;
i)根据kabateu编号系统编号,在第一抗体或其片段中引入t366w突变,并在第二抗体或其片段中引入t366s、l368a和y407v突变;
j)根据kabateu编号系统编号,在第二抗体或其片段中引入y407t突变,并在第一抗体或其片段中引入t366y突变;
k)根据kabateu编号系统编号,在第二抗体或其片段中引入y407a突变,并在第一抗体或其片段中引入t366w突变;
l)根据kabateu编号系统编号,在第二抗体或其片段中引入f405a突变,并在第一抗体或其片段中引入t394w突变;
m)根据kabateu编号系统编号,在第二抗体或其片段中引入f405w突变,并在第一抗体或其片段中引入t394s突变;
n)根据kabateu编号系统编号,在第二抗体或其片段中引入y407t突变,并在第一抗体或其片段中引入t366y突变;
o)根据kabateu编号系统编号,在第二抗体或其片段中引入t366y和f405a突变,并在第一抗体或其片段中引入t394w和y407t突变;
p)根据kabateu编号系统编号,在第二抗体或其片段中引入t366w和f405w突变,并在第一抗体或其片段中引入t394s和y407a突变;
q)根据kabateu编号系统编号,在第二抗体或其片段中引入f405w和y407a突变,并在第一抗体或其片段中引入t366w和t394s突变;或
r)根据kabateu编号系统编号,在第二抗体或其片段中引入t366w突变,并在第一抗体或其片段中引入t366s、l368a和y407v突变。
373.实施方案352-365中任一项的掩蔽型细胞因子,其中通过如下方式产生第一抗体或其片段的氨基酸序列和第二抗体或其片段的氨基酸序列:
a)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407t突变,并在seqidno:154或169的氨基酸序列中引入t366y突变;
b)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407a突变,并在seqidno:154或169的氨基酸序列中引入t366w突变;
c)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405a突变,并在seqidno:154或169的氨基酸序列中引入t394w突变;
d)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405w突变,并在seqidno:154或169的氨基酸序列中引入t394s突变;
e)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407t突变,并在seqidno:154或169的氨基酸序列中引入t366y突变;
f)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366y和f405a突变,并在seqidno:154或169的氨基酸序列中引入t394w和y407t突变;
g)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366w和f405w突变,并在seqidno:154或169的氨基酸序列中引入t394s和y407a突变;
h)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405w和y407a突变,并在seqidno:154或169的氨基酸序列中引入t366w和t394s突变;
i)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366w突变,并在seqidno:154或169的氨基酸序列中引入t366s、l368a和y407v突变;
j)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407t突变,并在seqidno:154或169的氨基酸序列中引入t366y突变;
k)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407a突变,并在seqidno:154或169的氨基酸序列中引入t366w突变;
l)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405a突变,并在seqidno:154或169的氨基酸序列中引入t394w突变;
m)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405w突变,并在seqidno:154或169的氨基酸序列中引入t394s突变;
n)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入y407t突变,并在seqidno:154或169的氨基酸序列中引入t366y突变;
o)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366y和f405a突变,并在seqidno:154或169的氨基酸序列中引入t394w和y407t突变;
p)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366w和f405w突变,并在seqidno:154或169的氨基酸序列中引入t394s和y407a突变;
q)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入f405w和y407a突变,并在seqidno:154或169的氨基酸序列中引入t366w和t394s突变;或
r)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入t366w突变,并在seqidno:154或169的氨基酸序列中引入t366s、l368a和y407v突变。
374.实施方案352-365中任一项的掩蔽型细胞因子,其中促进第一和第二半衰期延长结构域的缔合的修饰包括:
a)根据kabateu编号系统编号,在第一抗体或其片段中引入k409e突变,并在第二抗体或其片段中引入d399k突变;
b)根据kabateu编号系统编号,在第一抗体或其片段中引入k409e突变,并在第二抗体或其片段中引入d399r突变;
c)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d突变,并在第二抗体或其片段中引入d399k突变;
d)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d突变,并在第二抗体或其片段中引入d399r突变;
e)根据kabateu编号系统编号,在第一抗体或其片段中引入k392e突变,并在第二抗体或其片段中引入d399r突变;
f)根据kabateu编号系统编号,在第一抗体或其片段中引入k392e突变,并在第二抗体或其片段中引入d399k突变;
g)根据kabateu编号系统编号,在第一抗体或其片段中引入k392d突变,并在第二抗体或其片段中引入d399r突变;
h)根据kabateu编号系统编号,在第一抗体或其片段中引入k392d突变,并在第二抗体或其片段中引入d399k突变;
i)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k360d突变,并在第二抗体或其片段中引入d399k和e356k突变;
j)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k370d突变,并在第二抗体或其片段中引入d399k和e357k突变;
k)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k392d突变,并在第二抗体或其片段中引入d399k、e356k和e357k突变;
l)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k392d突变,并在第二抗体或其片段中引入d399k突变;
m)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k392d突变,并在第二抗体或其片段中引入d399k和e356k突变;
n)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k392d突变,并在第二抗体或其片段中引入d399k和e357k突变;
o)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k370d突变,并在第二抗体或其片段中引入d399k和e357k突变;
p)根据kabateu编号系统编号,在第一抗体或其片段中引入d399k突变,并在第二抗体或其片段中引入k409d和k360d突变;
q)根据kabateu编号系统编号,在第一抗体或其片段中引入k409d和k439d突变,并在第二抗体或其片段中引入d399k和e356k突变;
r)根据kabateu编号系统编号,在第二抗体或其片段中引入k409e突变,并在第一抗体或其片段中引入d399k突变;
s)根据kabateu编号系统编号,在第二抗体或其片段中引入k409e突变,并在第一抗体或其片段中引入d399r突变;
t)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d突变,并在第一抗体或其片段中引入d399k突变;
u)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d突变,并在第一抗体或其片段中引入d399r突变;
v)根据kabateu编号系统编号,在第二抗体或其片段中引入k392e突变,并在第一抗体或其片段中引入d399r突变;
w)根据kabateu编号系统编号,在第二抗体或其片段中引入k392e突变,并在第一抗体或其片段中引入d399k突变;
x)根据kabateu编号系统编号,在第二抗体或其片段中引入k392d突变,并在第一抗体或其片段中引入d399r突变;
y)根据kabateu编号系统编号,在第二抗体或其片段中引入k392d突变,并在第一抗体或其片段中引入d399k突变;
z)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k360d突变,并在第一抗体或其片段中引入d399k和e356k突变;
aa)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k370d突变,并在第一抗体或其片段中引入d399k和e357k突变;
ab)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k392d突变,并在第一抗体或其片段中引入d399k、e356k和e357k突变;
ac)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k392d突变,并在第一抗体或其片段中引入d399k突变;
ad)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k392d突变,并在第一抗体或其片段中引入d399k和e356k突变;
ae)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k392d突变,并在第一抗体或其片段中引入d399k和e357k突变;
af)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k370d突变,并在第一抗体或其片段中引入d399k和e357k突变;
ag)根据kabateu编号系统编号,在第二抗体或其片段中引入d399k突变,并在第一抗体或其片段中引入k409d和k360d突变;或
ah)根据kabateu编号系统编号,在第二抗体或其片段中引入k409d和k439d突变,并在第一抗体或其片段中引入d399k和e356k突变。
375.实施方案352-365中任一项的掩蔽型细胞因子,其中通过如下方式产生第一抗体或其片段的氨基酸序列和第二抗体或其片段的氨基酸序列:
a)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409e突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
b)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409e突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
c)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
d)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
e)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392e突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
f)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392e突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
g)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
h)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
i)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k360d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
j)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k370d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
k)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k、e356k和e357k突变;
l)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
m)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
n)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
o)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k370d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
p)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入d399k突变,并在seqidno:154或169的氨基酸序列中引入k409d和k360d突变;
q)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k439d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
r)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409e突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
s)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409e突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
t)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
u)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
v)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392e突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
w)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392e突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
x)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d突变,并在seqidno:154或169的氨基酸序列中引入d399r突变;
y)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
z)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k360d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
aa)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k370d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
ab)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k、e356k和e357k突变;
ac)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k突变;
ad)根据kabateu编号系统编号,在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变;
ae)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k392d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
af)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k370d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e357k突变;
ag)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入d399k突变,并在seqidno:154或169的氨基酸序列中引入k409d和k360d突变;或
ah)根据kabateu编号系统编号,分别在seqidno:154或169的氨基酸序列中引入k409d和k439d突变,并在seqidno:154或169的氨基酸序列中引入d399k和e356k突变。
376.实施方案333-375中任一项的掩蔽型细胞因子,其中第一接头包含第一可切割肽;和/或其中第二接头包含第二可切割肽。
377.实施方案333-376中任一项的掩蔽型细胞因子,其中第一接头包含第一n末端间隔区结构域和/或第一c末端间隔区结构域。
378.实施方案377的掩蔽型细胞因子,其中第一接头包含:
a)第一n末端间隔区结构域、第一可切割肽和第一c末端间隔区结构域;
b)第一n末端间隔区结构域和第一可切割肽;
c)第一n末端间隔区结构域和第一c末端间隔区结构域;
d)第一可切割肽和第一c末端间隔区结构域;
e)第一n末端间隔区结构域;或
f)第一c末端间隔区结构域。
379.实施方案333-378中任一项的掩蔽型细胞因子,其中第二接头包含第二n末端间隔区结构域和/或第二c末端间隔区结构域。
380.实施方案379的掩蔽型细胞因子,其中第二接头包含:
a)第二n末端间隔区结构域、第二可切割肽和第二c末端间隔区结构域;
b)第二n末端间隔区结构域和第二可切割肽;
c)第二n末端间隔区结构域和第二c末端间隔区结构域;
d)第二可切割肽和第二c末端间隔区结构域;
e)第二n末端间隔区结构域;或
f)第二c末端间隔区结构域。
381.实施方案376-380中任一项的掩蔽型细胞因子,其中第一可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列;和/或其中第二可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。
382.实施方案377-381中任一项的掩蔽型细胞因子,其中第一n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列,和/或第一c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
383.实施方案376-380中任一项的掩蔽型细胞因子,其中第一可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
384.实施方案383的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
385.实施方案379-384中任一项的掩蔽型细胞因子,其中第二n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列,和/或第二c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
386.实施方案376-385中任一项的掩蔽型细胞因子,其中第二可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
387.实施方案386的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
388.实施方案333-387中任一项的掩蔽型细胞因子,其中第一接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列,和/或第二接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列。
389.实施方案334-388中任一项的掩蔽型细胞因子,其中第三接头包含第三可切割肽。
390.实施方案334-389中任一项的掩蔽型细胞因子,其中第三接头包含第三n末端间隔区结构域和/或第三c末端间隔区结构域。
391.实施方案390的掩蔽型细胞因子,其中第三接头包含:
a)第三n末端间隔区结构域、第三可切割肽和第三c末端间隔区结构域;
b)第三n末端间隔区结构域和第三可切割肽;
c)第三n末端间隔区结构域和第三c末端间隔区结构域;
d)第三可切割肽和第三c末端间隔区结构域;
e)第三n末端间隔区结构域;或
f)第三c末端间隔区结构域。
392.实施方案389-391中任一项的掩蔽型细胞因子,其中第三可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列;和/或其中第三可切割肽包含选自由seqidno:96-153、236-242、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列。
393.实施方案390-392中任一项的掩蔽型细胞因子,其中第三n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列,和/或第三c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
394.实施方案389-393中任一项的掩蔽型细胞因子,其中第三可切割肽包含选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列和选自由seqidno:236-242组成的组的氨基酸序列。
395.实施方案394的掩蔽型细胞因子,其中选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列包含n末端和c末端,且选自由seqidno:236-242组成的组的氨基酸序列与选自由seqidno:96-153、264、270-302、306-317、342-347、356-415、420-491、494-501、504-535和538-555组成的组的氨基酸序列的n末端或c末端连接。
396.实施方案334-395中任一项的掩蔽型细胞因子,其中第三接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列,和/或第三接头包含选自由seqidno:11-153、235-242、262-264、268-320、323-338、340-354、356-555、668、691、724、725、727、762-771、794和797-812组成的组的氨基酸序列。
397.实施方案368-396中任一项的掩蔽型细胞因子,其中第四接头包含第四n末端间隔区结构域和/或第四c末端间隔区结构域。
398.实施方案397的掩蔽型细胞因子,其中第四n末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列,和/或第四c末端间隔区结构域包含选自由seqidno:20-95、235、268、269、303-305、323-338、340、341、727、794和799组成的组的氨基酸序列。
399.实施方案376-398中任一项的掩蔽型细胞因子,其中第一可切割肽、第二可切割肽和/或第三可切割肽是共定位在表达细胞因子受体的区域或组织中的蛋白酶的底物。
400.实施方案399的掩蔽型细胞因子,其中细胞因子受体是il-2细胞因子受体或il-15细胞因子受体。
401.实施方案376-400中任一项的掩蔽型细胞因子,其中第一可切割肽、第二可切割肽和/或第三可切割肽被选自由以下组成的组的一种或多种酶切割:abhd12、adam12、abhd12b、abhd13、abhd17a、adam19、adam20、adam21、adam28、adam30、adam33、adam8、abhd17a、adamdec1、adamts1、adamts10、adamts12、adamts13、adamts14、adamts15、adamts16、adamts17、adamts18、adamts19、adamts2、adamts20、adamts3、adamts4、abhd17b、adamts5、adamts6、adamts7、adamts8、adamts9、adamtsl1、adamtsl2、adamtsl3、abhd17c、adamtsl5、astl、bmp1、cela1、cela2a、cela2b、cela3a、cela3b、adam10、adam15、adam17、adam9、adamts4、ctse、ctsf、adamtsl4、cma1、ctrb1、ctrc、ctso、ctr1、ctsa、ctsw、ctsb、ctsc、ctsd、esp1、ctsg、ctsh、gzma、gzmb、gzmh、ctsk、gzmm、ctsl、ctss、ctsv、ctsz、htra4、klk10、klk11、klk13、klk14、klk2、klk4、dpp4、klk6、klk7、klkb1、ece1、ece2、ecel1、masp2、mep1a、mep1b、elane、fap、gzma、mmp11、gzmk、hgfac、hpn、htra1、mmp11、mmp16、mmp17、mmp19、htra2、mmp20、mmp21、htra3、htra4、kel、mmp23b、mmp24、mmp25、mmp26、mmp27、mmp28、klk5、mmp3、mmp7、mmp8、mmp9、lgmn、lnpep、masp1、pappa、pappa2、pcsk1、napsa、pcsk5、pcsk6、mme、mmp1、mmp10、plat、plau、plg、prss1、prss12、prss2、prss21、prss3、prss33、prss4、prss55、prss57、mmp12、prss8、prss9、prtn3、mmp13、mmp14、st14、tmprss10、tmprss11a、tmprss11d、tmprss11e、tmprss11f、tmprss12、tmprss13、mmp15、tmprss15、mmp2、tmprss2、tmprss3、tmprss4、tmprss5、tmprss6、tmprss7、tmprss9、nrdc、ovch1、pamr1、pcsk3、phex、tinag、tpsab1、tpsd1和tpsg1。
402.实施方案332-401中任一项的掩蔽型细胞因子,其中第一半衰期延长结构域和/或第二半衰期延长结构域与药剂缀合。
403.实施方案402的掩蔽型细胞因子,其中所述药剂是微管蛋白聚合的抑制剂、dna损伤剂或dna合成抑制剂。
404.实施方案403的掩蔽型细胞因子,其中所述药剂是类美登素、奥瑞他汀、吡咯并苯并二氮杂卓(pbd)二聚体、卡奇霉素、倍癌霉素、吲哚啉并苯并二氮杂卓二聚体或依喜替康衍生物dxd。
405.实施方案402的掩蔽型细胞因子,其中所述药剂是免疫刺激剂。
406.实施方案405的掩蔽型细胞因子,其中所述免疫刺激剂是干扰素基因刺激物(sting)激动剂或toll样受体(tlr)激动剂。
407.实施方案406的掩蔽型细胞因子,其中所述sting激动剂是环二核苷酸(cdn)。
408.实施方案407的掩蔽型细胞因子,其中所述cdn选自由cgamp、c-二-amp、c-二-gmp、caimp、c-二-imp、4-(2-氯-6-氟苄基)-n-(呋喃-2-基甲基)-3-氧代-3,4-二氢-2h-苯并[b][1,4]噻嗪-6-甲酰胺组成的组。
409.实施方案406的掩蔽型细胞因子,其中tlr激动剂是选自由tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9和tlr10组成的组的tlr的激动剂。
viii.实施例
通过参考以下实施例将会更充分地理解本发明。然而,它们不应被解释为限制本发明的范围。要理解的是,本文描述的实施例和实施方案仅用于说明的目的,且据此的各种修改或变动将是本领域技术人员容易想到的,并且属于本申请的实质和范畴以及所附权利要求的范围内。
尽管一些实施例描述了“掩蔽型”形式的il-2多肽构建体或il-15多肽构建体的工程化、产生和/或测试,但一些实施例也使用亲本“非掩蔽型”形式的il-2多肽构建体或il-15多肽构建体,如用于比较,或包括本文所述的一种或多种组分的其它构建体,它们作为用于比较的对照进行测试。因此,描述例如对掩蔽型il-2多肽构建体进行的测试不一定意味着非掩蔽型形式的构建体也没有被测试。
实例1:掩蔽型il-2多肽和掩蔽型il-15多肽的工程化
根据本文的教导产生掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体。在随后的实施例中,一些实验涉及使用单体形式的掩蔽型il-2和il-15多肽构建体,且一些实验涉及使用二聚体形式的掩蔽型il-2和il-15多肽构建体,如通过二硫键连接相同掩蔽型多肽构建体的两个拷贝形成的二聚体(同源二聚体),或由两种不同的多肽形成的异源二聚体(参见例如,表8-11)。
产生掩蔽型il-2多肽构建体,其包括il-2多肽或其功能片段、掩蔽部分和半衰期延长结构域,如白蛋白、抗体或其片段(例如,fc区、重链和/或轻链)、白蛋白结合肽、igg结合肽或聚氨基酸序列。还产生一些il-2多肽构建体,其包括与半衰期延长结构域连接的il-2多肽或其功能片段,而不包括掩蔽部分。一些构建体还包括接头,所述接头包含可切割肽,并将掩蔽部分与il-2多肽或其功能片段连接,从而产生可激活的掩蔽型il-2多肽构建体。一些构建体还包括将il-2多肽或其功能片段与半衰期延长结构域连接的接头。一些构建体还包括将il-2多肽或其功能片段与掩蔽部分连接的接头。在将il-2多肽或其功能片段与掩蔽部分连接的接头中不包括可切割肽的掩蔽型il-2多肽构建体也称为不可激活的掩蔽型il-2多肽构建体或不可激活的il-2多肽构建体,因为它们不包括可切割肽。表4中提供了示例性il-2多肽构建体的结构和组成。
产生掩蔽型il-15多肽构建体,其包括il-15多肽或其功能片段、掩蔽部分和半衰期延长结构域,如白蛋白、抗体或其片段(例如,fc区、重链和/或轻链)、白蛋白结合肽、igg结合肽或聚氨基酸序列。还产生一些il-15多肽构建体,其包括与半衰期延长结构域连接的il-15多肽或其功能片段,而不包括掩蔽部分。一些构建体还包括接头,所述接头包含可切割肽,并将掩蔽部分与il-15多肽或其功能片段连接,从而产生可激活的掩蔽型il-15多肽构建体。一些构建体还包括将il-15多肽或其功能片段与半衰期延长结构域连接的接头。一些构建体还包括将il-15多肽或其功能片段与掩蔽部分连接的接头。在将il-15多肽或其功能片段与掩蔽部分连接的接头中不包括可切割肽的掩蔽型il-15多肽构建体也称为不可激活的掩蔽型il-15多肽构建体或不可激活的il-15多肽构建体,因为它们不包括可切割肽。还产生一些包括掩蔽部分的il-15多肽构建体,所述掩蔽部分包含seqidno:261的氨基酸序列。表5中提供了示例性il-15多肽构建体的结构和组成。
还产生掩蔽型il-2多肽构建体,其包括il-2多肽或其功能片段、第一掩蔽部分、第二掩蔽部分和半衰期延长结构域,如白蛋白、抗体或其片段(例如,fc区、重链和/或轻链)、白蛋白结合肽、igg结合肽或聚氨基酸序列。一些构建体还包括将第一掩蔽部分与il-2多肽或其功能片段连接的接头。一些构建体还包括将第二掩蔽部分与il-2多肽或其功能片段连接的接头。一些构建体在将第一掩蔽部分与il-2多肽或其功能片段连接的接头和/或将第二掩蔽部分与il-2多肽或其功能片段连接的接头中包括可切割肽,从而产生可激活的掩蔽型il-2多肽构建体。一些构建体还包括将第二掩蔽部分与半衰期延长结构域连接的接头。在将il-2多肽或其功能片段与第一掩蔽部分或第二掩蔽部分连接的任一接头中不包括可切割肽的掩蔽型il-2多肽构建体也称为不可激活的掩蔽型il-2多肽构建体或不可激活的il-2多肽构建体,因为它们不包括可切割肽。表6中提供了示例性il-2多肽构建体的结构和组成。
还产生掩蔽型il-15多肽构建体,其包括il-15多肽或其功能片段、第一掩蔽部分、第二掩蔽部分和半衰期延长结构域,如白蛋白、抗体或其片段(例如,fc区、重链和/或轻链)、白蛋白结合肽、igg结合肽或聚氨基酸序列。一些构建体还包括将第一掩蔽部分与il-15多肽或其功能片段连接的接头。一些构建体还包括将第二掩蔽部分与il-15多肽或其功能片段连接的接头。一些构建体在将第一掩蔽部分与il-15多肽或其功能片段连接的接头和/或将第二掩蔽部分与il-15多肽或其功能片段连接的接头中包括可切割肽,从而产生可激活的掩蔽型il-15多肽构建体。一些构建体还包括将第二掩蔽部分与半衰期延长结构域连接的接头。一些构建体还包括与第一半衰期延长结构域缔合的第二半衰期延长结构域。在将il-15多肽或其功能片段与第一掩蔽部分或第二掩蔽部分连接的任一接头中不包括可切割肽的掩蔽型il-15多肽构建体也称为不可激活的掩蔽型il-15多肽构建体或不可激活的il-2多肽构建体,因为它们不包括可切割肽。表7中提供了示例性il-15多肽构建体的结构和组成。
还产生了掩蔽型il-2多肽构建体,其包括il-2多肽或其功能片段、掩蔽部分、第一半衰期延长结构域和第二半衰期延长结构域,如白蛋白、抗体或其片段(例如,fc区、重链和/或轻链)、白蛋白结合肽、igg结合肽或聚氨基酸序列。掩蔽部分与第一半衰期延长结构域连接,il-2多肽或其功能片段与第二半衰期延长结构域连接,且第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰。在一个示例性实施方案中,掩蔽部分与第一半衰期延长结构域连接,并且包括seqidno:267的氨基酸序列,且il-2多肽或其功能片段与第二半衰期延长结构域连接,并且包括seqidno:266的氨基酸序列,且第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰。在非掩蔽型il-2多肽构建体的一个示例性实施方案中,该实施方案包含与第一半衰期延长结构域连接的il-2多肽或其功能片段,并且包含第二半衰期延长结构域,其中il-2多肽或其功能片段与第一半衰期延长结构域连接,并且包括seqidno:266的氨基酸序列,且第二半衰期延长结构域包括seqidno:265的氨基酸序列。一些构建体还包括将掩蔽部分与第一半衰期延长结构域连接的接头,和/或将il-2多肽或其功能片段与第二半衰期延长结构域连接的接头。一些构建体的第一和第二半衰期延长结构域也是连接的。在一些构建体中,一些构建体的第一和第二半衰期延长结构域通过接头连接。一些构建体在将掩蔽部分与第一半衰期延长结构域连接的接头和/或将il-2多肽或其功能片段与第二半衰期延长结构域连接的接头中包括可切割肽,从而产生可激活的掩蔽型il-2多肽构建体。在将il-2多肽或其功能片段与第二半衰期延长结构域连接的接头或将掩蔽部分与第一半衰期延长结构域连接的接头中不包括可切割肽的掩蔽型il-2多肽构建体也称为不可激活的掩蔽型il-2多肽构建体或不可激活的il-2多肽构建体,因为它们不包括可切割肽。表8中提供了示例性il-2多肽构建体的结构和组成。
还产生了掩蔽型il-15多肽构建体,其包括il-15多肽或其功能片段、掩蔽部分、第一半衰期延长结构域和第二半衰期延长结构域,如白蛋白、抗体或其片段(例如,fc区、重链和/或轻链)、白蛋白结合肽、igg结合肽或聚氨基酸序列。掩蔽部分与第一半衰期延长结构域连接,il-15多肽或其功能片段与第二半衰期延长结构域连接,且第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰。一些构建体还包括将掩蔽部分与第一半衰期延长结构域连接的接头,和/或将il-15多肽或其功能片段与第二半衰期延长结构域连接的接头。一些构建体的第一和第二半衰期延长结构域也是连接的。在一些构建体中,一些构建体的第一和第二半衰期延长结构域通过接头连接。一些构建体在将掩蔽部分与第一半衰期延长结构域连接的接头和/或将il-15多肽或其功能片段与第二半衰期延长结构域连接的接头中包括可切割肽,从而产生可激活的掩蔽型il-15多肽构建体。在将il-15多肽或其功能片段与第二半衰期延长结构域连接的接头或将掩蔽部分与第一半衰期延长结构域连接的接头中不包括可切割肽的掩蔽型il-15多肽构建体也称为不可激活的掩蔽型il-15多肽构建体或不可激活的il-15多肽构建体,因为它们不包括可切割肽。表9中提供了示例性il-15多肽构建体的结构和组成。
还产生了掩蔽型il-2多肽构建体,其包括il-2多肽或其功能片段、第一掩蔽部分、第二掩蔽部分、第一半衰期延长结构域和第二半衰期延长结构域,如白蛋白、抗体或其片段(例如,fc区、重链和/或轻链)、白蛋白结合肽、igg结合肽或聚氨基酸序列。第一掩蔽部分与第一半衰期延长结构域连接,第二掩蔽部分与il-2多肽或其功能片段连接,第二掩蔽部分或il-2多肽或其功能片段与第二半衰期延长结构域连接,且第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰。一些构建体还包括将第一掩蔽部分与第一半衰期延长结构域连接的接头,和/或将第二掩蔽部分与il-2多肽或其功能片段连接的接头。一些构建体的第一和第二半衰期延长结构域也是连接的。在一些构建体中,一些构建体的第一和第二半衰期延长结构域通过接头连接。一些构建体在将第一掩蔽部分与第一半衰期延长结构域连接的接头中包括可切割肽,和/或在将第二掩蔽部分与il-2多肽或其功能片段连接的接头中包括可切割肽,从而产生可激活的掩蔽型il-2多肽构建体。在将第一掩蔽部分与第一半衰期延长结构域连接的接头或将第二掩蔽部分与il-2多肽或其功能片段连接的接头中不包括可切割肽的掩蔽型il-2多肽构建体也称为不可激活的掩蔽型il-2多肽构建体或不可激活的il-2多肽构建体,因为它们不包括可切割肽。表10中提供了示例性il-2多肽构建体的结构和组成。
还产生了掩蔽型il-15多肽构建体,其包括il-15多肽或其功能片段、第一掩蔽部分、第二掩蔽部分、第一半衰期延长结构域和第二半衰期延长结构域,如白蛋白、抗体或其片段(例如,fc区、重链和/或轻链)、白蛋白结合肽、igg结合肽或聚氨基酸序列。第一掩蔽部分与第一半衰期延长结构域连接,第二掩蔽部分与il-15多肽或其功能片段连接,第二掩蔽部分或il-15多肽或其功能片段与第二半衰期延长结构域连接,且第一半衰期延长结构域和第二半衰期延长结构域含有促进第一和第二半衰期延长结构域缔合的修饰。一些构建体还包括将第一掩蔽部分与第一半衰期延长结构域连接的接头,和/或将第二掩蔽部分与il-15多肽或其功能片段连接的接头。一些构建体的第一和第二半衰期延长结构域也是连接的。在一些构建体中,一些构建体的第一和第二半衰期延长结构域通过接头连接。一些构建体在将第一掩蔽部分与第一半衰期延长结构域连接的接头中包括可切割肽,和/或在将第二掩蔽部分与il-15多肽或其功能片段连接的接头中包括可切割肽,从而产生可激活的掩蔽型il-15多肽构建体。在将第一掩蔽部分与第一半衰期延长结构域连接的接头或将第二掩蔽部分与il-15多肽或其功能片段连接的接头中不包括可切割肽的掩蔽型il-15多肽构建体也称为不可激活的掩蔽型il-15多肽构建体或不可激活的il-15多肽构建体,因为它们不包括可切割肽。表11中提供了示例性il-2多肽构建体的结构和组成。
实例2:掩蔽型il-2和il-15多肽的体外表征
采用若干体外细胞和功能测定来表征在实施例1中产生的掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体。
产生
将编码构建体(例如,掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体)的质粒转染到expi293细胞(lifetechnologiesa14527)或hek293-6e细胞(nationalresearchcouncil;nrc)中。以peipro(polyplustransfection,115-100)与总dna为1∶1的比率,使用1mg总dna进行转染。将dna和pei各自添加到50ml的optimem(lifetechnologies31985088)培养基中,并进行无菌过滤。将dna和pei合并10分钟,并分别添加到expi293细胞或hek293细胞中,对于expi293细胞,细胞密度为1.8-2.8x106个细胞/ml或0.85-1.20x106个细胞/m,且活力为至少95%。按照与用于expi293转染相同的方案,以细胞密度和至少95%的活力进行hek293-6e转染。5-7天后,通过以3000xg离心沉淀细胞,并通过0.2μm膜过滤上清液。将蛋白a树脂(captiva,repligenca-pri-0005)添加到过滤的上清液中,并在4℃下摇动温育至少2小时。将树脂填充到柱中,用15个柱体积的20mm柠檬酸盐,ph6.5洗涤,然后用15个柱体积的20mm柠檬酸盐、500mm氯化钠,ph6.5洗涤。用20mm柠檬酸盐、100mmnacl,ph2.9从柱中洗脱结合的蛋白质。
下表12中提供产生的示例性构建体,包括亲本(例如,非掩蔽型)和掩蔽型构建体的滴度(mg/l)。
表12
sds-page分析
对于sds-page分析,用4xlaemmli样品缓冲液(biorad目录号1610747)制备蛋白质样品。对于还原的样品,添加0.1mbondbreakertcep溶液(thermoscientific77720),并将样品在65℃下加热5分钟。将蛋白质上样到12孔nupage4-12%bis-tris蛋白质凝胶(invitrogennp0322box)中,每孔上样4μg蛋白质。使用simplybluesafestain(invitrogenlc6065)对凝胶染色。
如图8中所示,在示例性构建体(ak304、ak305、ak307、ak308、ak309、ak310、ak311、ak312、ak313、ak314和ak315)的产生和纯化之后,对流通(ft)样品(即,未与蛋白a柱结合的蛋白)和洗脱(e)样品(即,与蛋白a柱结合并从其中洗脱的蛋白)进行sds-page分析。此示例性数据表明,可以成功地产生并纯化如本文所述的构建体。
报道子生物测定
对掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体以及非掩蔽型亲本构建体或其它对照进行报道子生物测定,以监测下游途径如jak-stat途径的激活。
在一些研究中,hek-blueil-2报道细胞(invivogen)用于根据以下方法测试jak-stat途径的激活。将hek-blueil-2细胞传代6(p6)(97%活)用测定培养基(dmem+10%热灭活fbs)洗涤2x,以5e4个细胞/孔铺板于3个板中的150ul测定培养基中,并在测定培养基中静置约2小时,以允许粘附于板。将每种测试的构建体在测定培养基中稀释至300pm,然后沿板1∶2稀释。添加每种稀释液50ul,达到75pm的最终起始浓度。24小时后收获hek-blueil-2细胞上清液,与quantiblue(180ul+20ul上清液)加上3孔/板的测定培养基一起在37℃下温育1小时。使用biotekneo2在625nm读取吸光度。在一项研究中,连同重组人il-15(rhil-15)作为阳性对照,在之前暴露或不暴露于mmp10蛋白酶的情况下,根据此方案测试示例性掩蔽型il-15多肽构建体ak248。如图22a和22b中所示,当使用掩蔽型il-15多肽构建体ak248(没有蛋白酶切割)时,没有可检测的jak-stat途径的激活,但在被激活蛋白酶切割之后,观察到jak-stat途径的强烈激活水平。这表明示例性il-15多肽可以被有效地掩蔽,并且也可以通过蛋白酶切割而被激活。
在一些研究中,ctll2细胞用于根据以下方法测试jak-stat途径的激活。将ctll2细胞以每孔40,000个细胞铺板于含10%fbs的rpmi中。添加所关注的构建体的稀释液(例如,掩蔽型il-15多肽构建体ak248,之前有或没有暴露于mmp蛋白酶,或阳性对照如rhil-15),并在37℃下温育。6小时后,添加bio-glo试剂,并用bioteksynergyneo2读板器测量发光。
受体结合
评估实施例1中产生的掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体的结合。对于掩蔽型il-2多肽构建体,在一些实验中,用受体亚基如il-2rα(也称为cd25)、il-2rβ(也称为cd122)或il-2rγ(也称为cd132)或其组合包被elisa板。对于掩蔽型il-15多肽构建体,在一些实验中,用受体亚基如il-15rα、il-2rβ(也称为cd122)或il-2rγ(也称为cd132)或其组合包被elisa板。使掩蔽型il-2多肽构建体或掩蔽型il-15多肽构建体的稀释液与受体亚基结合,并使用抗hufc-hrp检测抗体进行检测。在有和没有蛋白酶切割的条件下测定掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体的结合。
细胞上受体结合
评估实施例1中产生的掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体的细胞上受体结合。使掩蔽型il-2多肽构建体或il-15多肽构建体的稀释液与外周血淋巴细胞或组织培养细胞如ctll2细胞结合,并使用抗hufc-fitc或抗白蛋白-fitc检测抗体通过荧光激活细胞分选(facs)进行检测。在有和没有蛋白酶切割的条件下测定掩蔽型il-2多肽构建体和il-15多肽构建体的结合。
受体结合亲和力
评估实施例1中产生的掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体的结合亲和力。例如,在室温和/或37℃下进行表面等离振子共振(spr)。使il-2受体(例如,il-2rα、il-2rβ或il-2rγ或其组合)经由edc/nhs化学法与cm5芯片(gehealthcare)偶联。使il-15受体(例如,il-15rα、il-2rβ或il-2rγ或其组合)经由edc/nhs化学法与cm5芯片(gehealthcare)偶联。使掩蔽型il-2多肽构建体或掩蔽型il-15多肽构建体以一定浓度范围在芯片上流过,以获得缔合及解离速率的解离常数。在有和没有蛋白酶切割的条件下测定掩蔽型il-2多肽构建体和il-15多肽构建体的结合亲和力。
对于测试掩蔽型和非掩蔽型il-2多肽构建体的结合的一些spr研究,将reichert羧甲基葡聚糖水凝胶表面传感器芯片用所关注的构建体(例如,掩蔽型il-2多肽构建体或非掩蔽型il-2多肽构建体)以在10mm乙酸钠,ph5.0(在edc和nhs中1∶1稀释)中30ug/ml包被并固定。制备cd25-fc或fc-cd122在pbs中的稀释液(cd25:16nm、8nm、4nm、2nm、1nm,且cd122:500nm、250nm、125nm、62.5nm、31.25nm)。采用reichert4通道spr,使cd25或cd122的稀释液在具有固定化构建体的芯片上流过,以测定在25℃下的缔合速率。在平衡时(大约3-4分钟),将流动缓冲液换成pbs,以测定1分钟内的解离速率。在各次运行之间,将芯片用10mm甘氨酸,ph2.0再生。根据本文的教导和实施例,采用类似的方法测试掩蔽型和非掩蔽型il-15多肽构建体与适当浓度的适当结合伴侣的结合。
图9a-9d描述测试示例性掩蔽型il-2多肽构建体(ak215和ak216)与cd25-fc结合的spr分析的结果。图9a描述ak215与cd25-fc之间的相互作用,图9b描述ak216与cd25-fc之间的相互作用,且图9c描述重组人il2(rhil2)对照与cd25-fc之间的相互作用。图9d提供汇总针对每种相互作用的缔合常数(ka)、解离常数(kd)、平衡解离常数(kd)以及chi2值和u值获得的数据的表格。这些结果表明,这些示例性掩蔽型il-2多肽构建体没有表现出与cd25-fc的可检测的结合,而rhil2对照表现出可检测的结合。
图10a-10d描述测试示例性掩蔽型il-2多肽构建体(ak216和ak218)与cd122-fc结合的spr分析的结果。图10a描述ak216与cd122-fc之间的相互作用,图10b描述ak218与cd122-fc之间的相互作用,且图10c描述重组人il2(rhil2)对照与cd122-fc之间的相互作用。图10d提供汇总针对每种相互作用的缔合常数(ka)、解离常数(kd)、平衡解离常数(kd)以及chi2值和u值获得的数据的表格。这些结果表明,这些示例性掩蔽型il-2多肽构建体没有表现出与cd122-fc的可检测的结合,而rhil2对照表现出可检测的结合。下面在表13中提供测试的各种构建体的另外的示例性spr数据,包括掩蔽型和非掩蔽型构建体。对于一些结构,当适用时,测定先前有或没有被蛋白酶切割的构建体的kd。
表13
切割
在存在或不存在蛋白酶的情况下温育掩蔽型il-2肽构建体,并且蛋白酶(如果有的话)如通过添加edta在不同的时间点灭活后,如上所述通过进行受体结合测定来评估掩蔽型il-2多肽构建体的切割速率。在存在或不存在蛋白酶的情况下温育掩蔽型il-15肽构建体,并且蛋白酶(如果有的话)如通过添加edta在不同的时间点灭活后,如上所述通过进行受体结合测定来评估掩蔽型il-15多肽构建体的切割速率。还采用还原和非还原聚丙烯酰胺凝胶电泳(page)以及通过质谱全质谱和肽图谱分析来评估切割速率。还采用离体测定法评估切割速率,其中将掩蔽型il-2多肽构建体或掩蔽型il-15多肽构建体暴露于人、小鼠或食蟹猴外周血淋巴细胞或正常人体组织或人体肿瘤组织。
对于一些蛋白酶激活研究,将mmp10在mmp切割缓冲液中稀释至50ng/ul,并用1mmapma在37℃下激活2h。将激活蛋白酶的5μl蛋白酶(总共250ng)与1um的掩蔽型细胞因子构建体(例如,掩蔽型il-2多肽构建体)一起温育,并在37℃下温育2小时。使用anykdtmcriteriontmtgxstain-freetm蛋白凝胶,通过sds-page评估切割。采用类似的方法测试通过其它蛋白酶切割。
图11a描述在通过蛋白酶如与肿瘤环境相关的蛋白酶切割之前(左)和之后(右)的掩蔽型il-2多肽的示例性结构。图11b描述在不存在(左泳道)或存在(右泳道)mmp10蛋白酶的情况下温育的示例性掩蔽型il-2多肽构建体的sds-page分析。
增殖
评估il-2和il-15反应性组织培养细胞系如ctll2、yt、tf1b、lgl、hh和ct6在用实施例1中产生的掩蔽型il-2多肽构建体或掩蔽型il-15多肽构建体处理后的增殖。对于涉及掩蔽型il-2多肽构建体的实验,将细胞在缺乏il-2的培养基中的96孔组织培养板中铺板2-4小时,然后用各种浓度的掩蔽型il-2多肽构建体处理。对于涉及掩蔽型il-15多肽构建体的实验,将细胞在缺乏il-15的培养基中的96孔组织培养板中铺板2-4小时,然后用各种浓度的掩蔽型il-15多肽构建体处理。在37℃下温育24-48小时后,通过添加mts、阿拉玛蓝、萤光素酶或类似的代谢检测试剂来测定细胞数,并通过板分光光度计读数器检测比色、荧光或荧光素酶读数。
还评估了免疫细胞在用实施例1中产生的掩蔽型il-2多肽构建体或掩蔽型il-15多肽构建体处理后的增殖。用各种浓度的构建体处理人、小鼠或食蟹猴外周血单核细胞(pbmc),通过对特定细胞类型染色并经由荧光激活细胞分选(facs)分析来测定细胞类型如自然杀伤(nk)细胞、cd8+t细胞、cd4+t细胞和/或treg细胞的增殖。在一些实验中,用对照处理一些pbmc用于比较。在一些实验中,用阿地白介素处理一些pbmc,作为掩蔽型il-2多肽处理的对照。在一些实验中,在有和没有蛋白酶切割(例如,激活)的条件下测试掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体。在一些实验中,nk细胞被染色为cd45+cd3-cd56+,cd8+t细胞被染色为cd45+cd3+cd8+,cd4+t细胞被染色为cd45+cd3+cd4+cd25-,且treg细胞被染色为cd45+cd3+cd4+cd25+foxp3+。在一些实验中,pbmc被处理五天的时间。在一些实验中,pbmc也用细胞增殖的标志物ki67染色。在一些实验中,pbmc在处理之前用cfse(sigma-aldrich)标记,并通过测定cfse稀释的程度来测量增殖。在一些实验中,以一种或多种浓度施用每种构建体以及阿地白介素和/或其它对照,如0.0001nm至500nm范围内的一种或多种浓度。
stat5激活
还评估了信号转导子和转录的激活子5(stat5)在用实施例1中产生的掩蔽型il-2多肽构建体或掩蔽型il-15多肽构建体处理之后的激活。将pbmc用构建体处理指定的时间段,然后立即固定以保持蛋白质如stat5的磷酸化状态。在一些实验中,用对照处理一些pbmc用于比较。在一些实验中,用阿地白介素处理一些pbmc,作为掩蔽型il-2多肽处理的对照。在一些实验中,在有和没有蛋白酶切割(例如,激活)的条件下测试掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体。在一些实验中,将pbmc处理10分钟、15分钟、20分钟或25分钟。在一些实验中,以一种或多种浓度施用每种构建体以及阿地白介素和/或其它对照,如0.0001nm至500nm范围内的一种或多种浓度。在一些实验中,然后用对磷酸化stat5(磷酸-stat5)特异性的抗体对固定和透化的pbmc进行染色,并通过流式细胞术进行分析。在一些实验中,测量stat5的总水平和磷酸化水平。通过对特定细胞类型染色来确定某些细胞类型如nk细胞、cd8+t细胞、cd4+t细胞和/或treg细胞的磷酸-stat5状态。在一些实验中,nk细胞被染色为cd45+cd3-cd56+,cd8+t细胞被染色为cd45+cd3+cd8+,cd4+t细胞被染色为cd45+cd3+cd4+cd25-,且treg细胞被染色为cd45+cd3+cd4+cd25+foxp3+。
还评估了在用实施例1中产生的掩蔽型il-2多肽构建体或掩蔽型il-15多肽构建体处理之后小鼠细胞系如ctll-2细胞中的stat5的激活。在一些实验中,用对照处理一些ctll-2细胞用于比较。在一些实验中,用阿地白介素处理一些ctll-2细胞,作为掩蔽型il-2多肽处理的对照。在一些实验中,在有和没有蛋白酶切割(例如,激活)的条件下测试掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体。在一些实验中,将ctll-2细胞处理10分钟、15分钟、20分钟或25分钟,然后固定以保持蛋白质如stat5的磷酸化状态。在一些实验中,以一种或多种浓度施用每种构建体以及阿地白介素和/或其它对照。在一些实验中,测量stat5的总水平和磷酸化水平。
在一些研究中,通过以下方法测定由il-2诱导的细胞内stat5激活(pstat5信号)的水平。将冷冻的人pbmc在水浴中解冻,并添加到39ml预温热的培养基(rpmi1640培养基加上10%fbs、1%p/s、1%nea)中,旋转并以10e6个细胞/ml在培养基中重构。将细胞以每孔5e5个细胞在96孔板中铺板。将在培养基中稀释的il-2(例如,rhil-2或示例性的含il-2的多肽构建体)添加到每个孔中,并在37℃下温育20分钟。然后将细胞用200ul/孔固定缓冲液(ebiosciences)在4℃下固定过夜。离心后,将固定的细胞重悬于200ul冷bdphosflow缓冲液中,并在4℃下温育30分钟。洗涤细胞两次后,将它们在冰上用biolegendhumantrustainfcx(在染色缓冲液中,在50ul总共每个样品中2.5ul)处理5分钟。添加染色抗体;5ulpstat5-apc(py694,bd)、10ulcd56-bv421(5.1h11,biolegend)、10ulcd4-percp/cy5.5(a161a1,biolegend)和10ulcd3-fitc(ucht1,biolegend),并在冰上避光温育30分钟。将细胞洗涤2次并重悬,并通过流式细胞术进行分析。
图12a-12d描述如上所述使用示例性构建体ak032、ak035、ak041或作为对照的rhil-2的stat5激活研究的结果。对于nk细胞、cd8+t细胞、效应t细胞(teff)和调控性t细胞(treg),显示了stat5激活的水平(%)。ak032和ak035构建体包括与fc结构域连接的il-2多肽,且ak041构建体包括与cd25结构域和cd122结构域连接的il-2多肽。如图所示,在一些实施方案中,工程化il-2多肽构建体可降低treg细胞的激活,同时保持或增强cd8+t细胞和nk细胞的激活。
图13a-13c描述如上所述使用示例性构建体ak081和ak032的stat5激活研究的结果。测试了有和没有之前暴露于mmp10的ak081构建体。还测试了同种型对照以及无il-2阴性对照。对于nk细胞、cd8+t细胞和cd4+t细胞,显示了stat5激活的水平(%)。ak032和ak081构建体包括与fc结构域连接的il-2多肽,且ak081构建体在将il-2多肽与fc结构域连接的接头中包括可切割肽。如图所示,在有或没有类似于非掩蔽型二聚体ak032il-2多肽构建体的蛋白酶激活的情况下,非掩蔽型单体ak081il-2多肽构建体刺激pbmc的stat5激活。
图14a-14d描述如上所述使用示例性构建体ak081和ak111以及包括rhil-2和抗rsv抗体的对照的stat5激活研究的结果。还测试了无处理的对照。ak111构建体是包括野生型形式的il-2多肽(c125a突变除外)的示例性掩蔽型il-2多肽构建体。如图14a-14c所示,与非掩蔽型il-2多肽构建体ak081相比,掩蔽型il-2多肽构建体ak111表现出降低的stat5激活。图14d提供ak081、ak111构建体以及rhil-2对照的ec50(pm)和倍数变化数据。
图15a-15d描述如上所述使用示例性构建体ak167和ak168以及包括rhil-2和抗rsv抗体的对照的stat5激活研究的结果。还测试了无处理的对照。ak168构建体是示例性掩蔽型il-2多肽构建体,其包括消除或降低cd25结合的突变形式的il-2多肽。ak167构建体是包括相同突变il-2多肽的亲本非掩蔽型形式的ak168构建体。如图15a-15c中所示,与rhil-2对照相比,非掩蔽型ak167构建体表现出降低的stat5激活,且掩蔽型il-2多肽构建体ak168不诱导可检测的stat5激活。图15d提供ak167、ak168构建体以及rhil-2对照的ec50(pm)和倍数变化数据。检测不到ak168构建体的ec50(n.d.)。
图16a-16d描述如上所述使用有(+mmp10)或没有之前暴露于mmp10蛋白酶的示例性构建体ak165和ak166以及同种型对照和il-2-fc对照的stat5激活研究的结果。ak166构建体是包括野生型形式的il-2多肽(c125a突变除外)的示例性掩蔽型il-2多肽构建体。ak165构建体是包括相同il-2多肽的亲本非掩蔽型形式的ak166构建体。如图16a中所示的图例也适用于图16b,且如图16c中所示的图例也适用于图16d。如图16a-16d中所示,对于掩蔽型ak166构建体(没有蛋白酶切割),stat5激活大大减弱,但在暴露于激活蛋白酶mmp10之后恢复到类似于il2-fc对照的水平。
图17a-17c描述如上所述使用有(+mmp10)或没有之前暴露于mmp10蛋白酶的示例性构建体ak109和ak110以及同种型对照和il-2-fc对照的stat5激活研究的结果。ak109和ak110构建体是包括具有不同异源二聚化突变的半衰期延长结构域的示例性掩蔽型il-2多肽构建体。如图17b中所示的图例也适用于图17a。如图17a-17c中所示,对于掩蔽型ak109和ak110构建体(没有蛋白酶切割),stat5激活大大减弱,但在暴露于激活蛋白酶mmp10之后大大增加到接近il2-fc对照的水平。
图18a-18d描述如上所述使用构建体ak211、ak235、ak253、ak306、ak310、ak314和ak316以及rhil-2对照的stat5激活研究的结果。这包括这样的构建体,即亲本非掩蔽型构建体(ak235、ak253、ak306、ak310、ak314),其包括调节cd25结合的各种突变。图18d提供每种测试构建体以及rhil-2对照的ec50数据。
图19a-19d描述如上所述使用已被蛋白酶激活的构建体ak081、ak167、ak216、ak218、ak219、ak220和ak223以及rhil-2对照的stat5激活研究的结果。还测试了无处理的对照。这包括掩蔽型il-2多肽构建体(ak216、ak218、ak219、ak220和ak223),其包括调节cd25结合的各种突变。在测试构建体激活stat5的能力之前,预先将它们暴露于激活蛋白酶。图19d提供每种测试构建体以及rhil-2对照的ec50数据。
图20a-20c描述如上所述使用构建体ak081、ak189、ak190和ak210以及抗rsv对照的stat5激活研究的结果。这包括掩蔽型il-2多肽构建体(ak189、ak190、ak210),其包括具有c125a突变的il-2多肽,并且包括相同的可切割肽序列(raaavksp;seqidno:121),但由于蛋白酶切割序列的n末端上的氨基酸残基不同而具有不同的接头序列。如图20a中所示的图例也适用于图20b和20c。
图21a-21c描述如上所述使用构建体ak167、ak191、ak192和ak193以及抗rsv对照的stat5激活研究的结果。这包括掩蔽型il-2多肽构建体(ak189、ak190、ak210),其包括具有r38a、f42a、y45a、e62a和c125a突变的il-2多肽,并且包括相同的可切割肽序列(raaavksp;seqidno:121),但由于蛋白酶切割序列的n末端上的氨基酸残基不同而具有不同的接头序列。如图21a中所示的图例也适用于图20b和20c。
实例3:掩蔽型il-2和il-15多肽的体内表征
药代动力学
使用小鼠模型在体内评估实施例1中产生的掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体的药代动力学。
用构建体对小鼠进行静脉内或皮下处理,并随着时间的推移测量血浆中的构建体浓度。在一些实验中,用对照处理一些小鼠用于比较。在一些实验中,用阿地白介素处理一些小鼠,作为掩蔽型il-2多肽处理的对照。在一些实验中,被处理的小鼠患有肿瘤。在一些实验中,被处理的小鼠没有肿瘤。在一些实验中,用构建体处理小鼠,并在处理过程中的不同时间抽取血液,这可包括在开始处理之前抽取血液,并对其进行处理以获得血浆。在一些实验中,在两周、三周或四周或更长时间的处理过程中的不同时间点抽取血液。在一些实验中,测量施用的构建体以及阿地白介素和/或其它对照的平均血浆浓度。在稀释到pbstween中后用il-2和人fc特异性elisa,在血浆样品中检测掩蔽型il-2多肽构建体,并使用对每种构建体生成的标准曲线进行定量。在稀释到pbstween中后用il-15和人fc特异性elisa,在血浆样品中检测掩蔽型il-15多肽构建体,并使用对每种构建体生成的标准曲线进行定量。通过用抗hufc-hrp和抗huil-2-hrp的western印迹和通过全质谱和肽质谱测定全长和切割构建体的百分比。
还使用小鼠模型在体内评估肿瘤中的掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体的药代动力学。用构建体对患有肿瘤的小鼠进行静脉内或皮下处理,并评估构建体在小鼠肿瘤中的浓度。在一些实验中,用对照处理一些小鼠用于比较。在一些实验中,用阿地白介素处理一些小鼠,作为掩蔽型il-2多肽处理的对照。分析肿瘤中构建体的存在以及特定蛋白酶的存在。在一些实验中,分析肿瘤的全长和切割构建体的存在和百分比。
根据以下方法进行一些药代动力学研究。c57bl/6雌性小鼠购自charlesriverlaboratories,并且在研究开始时为8-10周龄。向每只小鼠的右侧皮下注射mc38肿瘤细胞(每只小鼠5x105个细胞)。在肿瘤大小达到~100mm3时(第0天),小鼠接受单次2mg/kg静脉内剂量的在pbs中的所关注的构建体(例如,非掩蔽型亲本il-2多肽构建体、掩蔽型il-2多肽构建体或不可切割的掩蔽型il-2多肽构建体)。测试的构建体包括例如ak032、ak081、ak111、ak167、ak168、ak191、ak197、ak203、ak209和ak211。在给药后5分钟、第1天、第2天和第5天收集血浆。利用抗人igg(克隆m1310g05,biolegend)作为捕获抗体和各种检测抗体,采用elisa测定药物水平。利用针对人igg(ab97225,abcam)或cd122(克隆9a2,ancell)和il-2(poly5176,biolegend)的hrp或生物素缀合检测抗体分别检测总药物水平和未切割的药物水平。
图23a-23d描述如上所述使用构建体ak032、ak081、ak111、ak167和ak168以及抗rsv对照在荷瘤小鼠中进行的药代动力学研究的结果。图23a提供对每种测试构建体的结构的简化描述。如图所示,ak111和ak168是示例性掩蔽型il-2多肽构建体。ak167和ak168构建体包括消除或降低与cd25结合的突变(r38a、f42a、y45a和e62a)。图23b通过检测人igg显示血浆中的fc水平(μg/ml),图23c通过检测人cd122显示血浆中的fc-cd122水平(μg/ml),且图23d通过检测人il-2显示血浆中的fc-il2水平(μg/ml)。
图24a-24d描述如上所述使用构建体ak167、ak191、ak197、ak203、ak209和ak211以及抗rsv对照在荷瘤小鼠中进行的药代动力学研究的结果。图24a提供对每种测试构建体的结构的简化描述。如图所示,ak168、ak191、ak197、ak203和ak209是示例性掩蔽型il-2多肽构建体,其各自在将il-2多肽与半衰期延长结构域连接的接头中包括不同的可切割肽序列。图24b通过检测人igg显示血浆中的fc水平(μg/ml),图24c通过检测人il-2显示血浆中的fc-il2水平(μg/ml),且图24d通过检测人cd122显示血浆中的fc-cd122水平(μg/ml)。如图24b、24c和24d中所示,测试的掩蔽型il-2多肽构建体当中,血浆中的fc水平、fc-il2水平和fc-cd122水平相似。
小鼠中的生物活性
使用小鼠模型如c57bl/6小鼠在体内评估实施例1中产生的掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体的体内生物活性。用构建体处理小鼠,并评估体内生物活性。在一些实验中,用对照处理一些小鼠用于比较。在一些实验中,用阿地白介素处理一些小鼠,作为掩蔽型il-2多肽处理的对照。在一些实验中,被处理的小鼠患有肿瘤。在一些实验中,被处理的小鼠没有肿瘤。在一些实验中,在小鼠中评估免疫细胞的剂量依赖性扩增。在一些实验中,用不同剂量的构建体、阿地白介素或其它对照处理小鼠。在一些实验中,在两周的过程中处理小鼠。在不同的时间点从小鼠中收集血液,然后使用针对所关注的免疫细胞标志物的抗体进行染色。在一些实验中,还测定了某些循环细胞类型如cd8+t细胞、nk细胞和treg细胞的增殖和扩增的纵向动力学,以及cd8+t细胞和nk细胞与cd4+cd25+foxp3+treg细胞的比率。在一些实验中,评估小鼠的血管渗漏,如通过器官湿重和组织学测定,在某些器官如肺和肝中评估水肿和淋巴细胞浸润。
在一些研究中,通过进行以下方法来评估血管渗漏,以便评估由基于il-2的疗法介导的潜在毒性相关作用。使用购自charlesriverlaboratories并且在研究开始时重18-22克的8-10周龄c57bl/6雌性小鼠进行重复剂量毒性研究。5只小鼠的组持续4或5天每天接受腹膜内注射pbs中的掩蔽型和非掩蔽型il-2构建体。测试的构建体包括ak081、ak111、ak167和ak168。还施用对照抗体作为对照。最后一次给药后两小时,所有小鼠接受静脉内注射0.1ml在pbs中的1%伊文思蓝(sigma,目录号e2129)。施用伊文思蓝后两小时,麻醉小鼠,并用pbs中的10u/ml肝素灌注。收获脾、肺和肝,并在4℃下在3ml的4%pfa中固定2天,之后以nanodroponec(thermofisherscientific,waltham,ma)作为伊文思蓝的血管渗漏的指示剂,在650nm测量上清液的吸光度。将固定的器官包埋在石蜡中,切片,并用苏木精和曙红染色。由novovitahistopathlaboratory,llc.(allston,ma)根据标准程序进行组织病理学研究和定量。图30a-30d描述如上所述使用示例性掩蔽型il-2多肽构建体ak111和ak168以及非掩蔽型il-2多肽构建体ak081和ak167及抗rsv对照评估血管渗漏的体内研究的结果。图30a显示体重损失的百分比(%),且图30b、30c和30d分别显示肝、肺和脾各自以克表示的重量。
对于ak081、ak111、ak167和ak168构建体以及抗rsv对照,还评估了如通过测量染料向组织中的渗漏程度所指示的血管渗漏,对于肝和肺,结果分别示于图31a和31b中。基于在650nm的吸光度测量染料渗漏的程度。
对于ak081、ak111、ak167和ak168构建体以及抗rsv对照,还评估了如通过测量单核细胞血管周围侵入肝和肺的程度所指示的血管渗漏,对于肝和肺,结果分别示于图32a和32b中。各自描绘了肝中的单核细胞平均数(图32a)和肺中的单核细胞平均数(图32b)。如图32b中所示,例如,与非掩蔽型构建体ak081和ak167不同,掩蔽型il-2多肽构建体ak111和ak168在肺中不产生可检测数量的单核细胞。
浸润性免疫细胞表型
评估了用实施例1中产生的掩蔽型il-2多肽构建体或掩蔽型il-15多肽构建体处理的小鼠模型中在体内浸润肿瘤的免疫细胞的表型。用构建体处理小鼠,并评估肿瘤浸润性免疫细胞的表型。在一些实验中,用对照处理一些小鼠用于比较。在一些实验中,用阿地白介素处理一些小鼠,作为掩蔽型il-2多肽处理的对照。用构建体、阿地白介素或另一种对照处理荷瘤的小鼠,并在初始给药之后如初始给药后五天、七天或十天的不同时间点收集肿瘤、组织如肝、肺和脾以及血液。在一些实验中,免疫细胞分离自肿瘤、组织和血液,并采用流式细胞术进行表型评估。在一些实验中,使用所关注的标志物如对于cd8+t细胞、记忆cd8+t细胞、激活的nk细胞、cd4+t细胞和cd4+treg细胞的那些来评估分离的免疫细胞。
在一些研究中,采用以下方法评估在体内浸润肿瘤的免疫细胞的表型。c57bl/6雌性小鼠购自charlesriverlaboratories,并且在研究开始时为8-10周龄。向每只小鼠的右侧皮下注射mc38肿瘤细胞(每只小鼠5x105个细胞)。在肿瘤大小达到~100mm3时(第0天),小鼠接受单次2mg/kg静脉内剂量的在pbs中的所关注的构建体(例如,非掩蔽型亲本il-2多肽构建体、掩蔽型il-2多肽构建体或不可切割的掩蔽型il-2多肽构建体)。在第5天,通过co2窒息使小鼠无痛致死,并收获肿瘤、肝、脾和血液。通过机械破碎并通过40μm细胞过滤器由脾制备细胞悬浮液。使用miltenyi肿瘤解离试剂盒试剂(miltenyi目录号130-096-730)酶促消化肿瘤组织,并将gentlemacs解离器(miltenyi)用于机械解离步骤。使用ack缓冲液(gibco目录号a10492)裂解脾和肿瘤细胞悬浮液以及血液中的红细胞。用以下抗体对细胞悬浮液进行染色:cd45(克隆30-f11,ebioscience)、cd3(克隆2c11,biolegend)、cd8(克隆53-6.7,bdbiosciences)、cd4(克隆rm-45,bdbiosciences)、foxp3(mf-14,biolegend)、cd25(3c7,biolegend)、cd44(克隆im7,ebioscience)和nkp46(29a1.4,ebioscience)。在macsquant分析器流式细胞仪(milenyi)上进行数据采集,并使用flowjo分析数据。
图25a-25l中显示如上所述使用ak032、ak081、ak111、ak167和ak168构建体以及抗rsvigg对照进行的测试脾、血液和肿瘤中的cd4、cd8、nk和treg百分比的体内反应的研究结果。ak111和ak168是示例性掩蔽型il-2多肽构建体。
图26a-26l中显示如上所述使用ak167、ak168、ak191、ak197、ak203、ak209和ak211构建体以及抗rsvigg对照进行的测试脾、血液和肿瘤中的cd4、cd8、nk和treg百分比的体内反应的研究结果。ak168、ak191、ak197、ak203和ak209是示例性掩蔽型il-2多肽构建体,其各自在将il-2多肽与半衰期延长结构域连接的接头中包括不同的可切割肽序列。与不可切割的ak211构建体相比,采用单向anova进行统计分析。
图27a-27l中显示如上所述使用ak235、ak191、ak192、ak193、ak210、ak189、ak190和ak211构建体进行的测试脾、血液和肿瘤中的cd4、cd8、nk和treg百分比的体内反应的研究结果。ak191、ak192、ak193、ak210、ak189和ak190是示例性掩蔽型il-2多肽构建体,其各自在将il-2多肽与半衰期延长结构域连接的接头中包括可切割肽序列。在这些构建体当中,接头序列也不同,这取决于所用的接头序列。ak189、ak190和ak210包括具有c125a突变的il-2多肽,ak191、ak192和ak193包括具有c125a、r38a、f42a、y45a和e62a突变的il-2多肽。ak235构建体是非掩蔽型构建体,且ak211构建体包括不可切割的接头序列。与不可切割的ak211构建体相比,采用单向anova进行统计分析。
图28a-28i中显示如上所述使用如上所述的ak235、ak191、ak192、ak193、ak210、ak189、ak190和ak211构建体进行的测试脾、血液和肿瘤中的体内t细胞激活的研究结果。t细胞激活被测量为脾、血液和肿瘤中的cd8+t细胞、cd4+t细胞或foxp3+细胞中的cd25的平均荧光强度(mfi)。与不可切割的ak211构建体相比,采用单向anova进行统计分析。
体内切割
评估了掩蔽型细胞因子构建体(例如,掩蔽型il-2多肽构建体或掩蔽型il-15多肽构建体)的体内切割。在一些研究中,施用对照抗体用于比较。在一些研究中,通过在小鼠中施用所关注的构建体,并在一段时间后捕获人igg,然后测量例如人igg、cd122和il-2或il-15的水平,由此来评估体内切割。
在测试掩蔽型il-2多肽构建体的体内切割的一些研究中,采用利用抗人igg(克隆m1310g05,biolegend)作为捕获抗体和各种检测抗体的elisa测定药物水平(即,施用的构建体包括切割副产物的水平)。利用针对人igg(ab97225,abcam)或cd122(克隆9a2,ancell)和il-2(poly5176,biolegend)的hrp或生物素缀合检测抗体分别检测总药物水平和未切割的药物水平。通过从总药物浓度中减去未切割(即,完整的)来计算切割和释放的il-2的浓度。图29a-29d描述测试示例性掩蔽型il-2多肽构建体ak168(可切割肽序列:mpydlyhp;seqidno:96)和ak209(可切割肽序列:vplsly;seqidno:135)的体内切割的研究结果。ak167构建体是可切割的非掩蔽型il-2多肽构建体,其包括与掩蔽型ak168构建体相同的il-2多肽。如图29b-29d中所示,掩蔽型(ak168和ak209)和非掩蔽型(ak167)构建体均被有效切割,并且两个可切割肽序列均被切割。图29e描述对于ak167、ak168和ak209构建体的总水平和对于非切割形式的每种构建体的水平的总血浆igg浓度(μg/ml)的药代动力学研究结果。
肿瘤根除和转移的抑制
使用小鼠模型如同基因mc38、ct26和b16f10肿瘤模型在体内评估实施例1中产生的掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体促进肿瘤根除和抑制转移的能力。
给小鼠皮下植入肿瘤细胞,并使肿瘤生长到可触及的大小。用掩蔽型il-2构建体或掩蔽型il-15多肽构建体处理荷瘤小鼠,并在处理过程中测量肿瘤体积。在一些实验中,用对照处理一些小鼠用于比较。在一些实验中,用阿地白介素处理一些小鼠,作为掩蔽型il-2多肽处理的对照。在处理过程中定期测量肿瘤体积。在一些实验中,在处理过程中还定期测量体重。在一些实验中,在处理过程中产生血浆样品,并分析药代动力学、药效动力学、切割和血液标志物,如对于cd8+t细胞、记忆cd8+t细胞、激活的nk细胞、cd4+t细胞和cd4+treg细胞的那些。
还使用适合转移研究的小鼠模型如用于评估肺转移的同基因ct26肿瘤模型来评估掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体抑制转移的能力。给小鼠皮下植入肿瘤细胞。在一些实验中,在处理之前使肿瘤生长到可触及的大小。在一些实验中,在肿瘤生长到可触及的大小之前开始处理。用掩蔽型il-2构建体或掩蔽型il-15多肽构建体处理荷瘤小鼠,并评估肿瘤细胞向组织如肺、肝和淋巴结中的转移。
在一些研究中,同基因肿瘤模型用于根据以下方法评估掩蔽型il-2多肽构建体减小肿瘤体积的能力。c57bl/6雌性小鼠购自charlesriverlaboratories,并且在研究开始时为8-10周龄。向每只小鼠的右侧皮下注射mc38肿瘤细胞(每只小鼠5x105个细胞)。在肿瘤大小达到~125mm3时(第0天),使小鼠随机接受2mg/kg剂量的在pbs中的ak081、ak111、ak167或ak168或作为对照的抗rsv抗体。小鼠腹膜内给药,一周三次,6个剂量。使用带表卡尺计算肿瘤体积(长度*(宽度^2)/2),并且每周两次记录体重。图33a和33b显示在处理过程中评估肿瘤体积和体重的同基因肿瘤模型研究的结果。如图33a中所示,与抗rsv对照相比,使用示例性il-2多肽构建体(包括掩蔽型构建体ak111和ak168)的处理随着时间的推移导致肿瘤生长抑制。如图33b中所示,当用掩蔽型构建体ak111和ak168处理小鼠时,观察到一般没有体重减轻。
食蟹猴中的生物活性
在食蟹猴中体内评估实施例1中产生的掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体的体内生物活性。用构建体处理食蟹猴,并评估体内生物活性、药代动力学和切割。在一些实验中,用对照处理一些猴子用于比较。在一些实验中,用阿地白介素处理一些猴子,作为掩蔽型il-2多肽处理的对照。在一些实验中,用不同剂量的构建体、阿地白介素或其它对照处理猴子。在不同的时间点从猴子中收集血液,然后评估某些细胞类型,如cd8+t细胞、记忆cd8+t细胞、激活nk细胞、cd4+t细胞和cd4+treg细胞,和/或如用于总淋巴细胞、ki67+和可溶性cd25的剂量反应的所关注的标志物。在一些实验中,评估某些循环t和nk细胞类型的增殖和扩增的纵向动力学。在一些实验中,通过elisa、page和质谱法测定掩蔽型il-2多肽构建体和掩蔽型il-15多肽构建体的药代动力学和切割。
为测试示例性掩蔽型il-2多肽构建体在非人灵长类动物中的安全特性,根据以下方法进行剂量范围研究。随机分配3只健康雄性食蟹猴(食蟹猕猴)的组接受2ml/kg单次静脉内推注剂量的可激活的(即,可切割的)掩蔽型il-2多肽蛋白或不可切割的掩蔽型il-2多肽蛋白,在100mm柠檬酸钠缓冲液(ph5.5)中为10、30和100nmol/kg。第三组接受3、10和30nmol/kg的亲本非掩蔽型可切割蛋白作为阳性对照。考虑亲本非掩蔽型分子的较高效力,此第三组给药的范围较低。考虑分子量的差异,按摩尔计算剂量。在给药前和给药后1、24、48、72、96、168、264和336小时收集血液样品。自动化血液分析仪用于监测淋巴细胞亚群和血清化学的变化。如上所述采用定制elisa由血浆测量总药物水平和完整(即,未切割的)药物水平。用elisa(r&dsystems,目录号dr2a00)测量可溶性cd25水平以监测免疫刺激。采用定制多路电化学发光测定法(mesoscalediscovery)对炎性细胞因子的血浆水平进行定量。监测血压,作为血管渗漏综合征的指标。采用捕获il-2并检测人fc的elisa和通过捕获人fc并检测人fc的elisa分析pk。
本发明的范围并不旨在限于所公开的特定实施方案,这些实施方案例如是为了说明本发明的各个方面而提供的。根据本文的描述和教导将会显而易见对所述组合物和方法的各种修改。可在不偏离本公开的真实范围和实质的情况下实施这类变化,并且这类变化旨在属于本公开的范围内。
ix.序列
- 还没有人留言评论。精彩留言会获得点赞!