一种细胞捕获与筛选的方法与流程
本发明属于细胞生物学实验装置技术领域,尤其是涉及一种细胞捕获与筛选的方法及其所采用的细胞捕获与筛选芯片。
背景技术:
近年来,抗体新药在恶性肿瘤、自身免疫病等重大疾病的治疗中显示了良好的疗效,国际国内对抗体类药物的开发成为新热点,竞争也异常激烈。在抗体新药的开发过程中,需要建立和应用多项关键技术,包括抗体筛选和功能确认、细胞株构建和工艺开发、中试工艺放大和临床前研究等多项关键技术。目前,国内在抗体筛选和工艺开发方面,存在很多技术难点,如目前大多数采用的通过杂交瘤细胞技术的抗体筛选方法有很多弊端,无法实现大通量筛选,无法同时获取上万抗体的序列和亲和力数据等,导致获取最优化的抗体序列的概率较低。因此,建立一种可实现大通量筛选,更有效得实现精细化的细胞捕获与筛选方法是必然需求。
细胞作为生命体结构和生命活动的基本单元,是生命科学和生物医学研究的基础。细胞筛选为基于细胞分析的药物筛选、细胞内基因表达等的研究提供基础信息。快速、高通量、无标记的细胞筛选方法不仅可以为生物学研究提供极大的便利,同时可以为生物医学研究提供直接的帮助,有利于生命过程研究和重大疾病的早期诊断。
目前的细胞筛选方法主要有激光法、荧光标记法和基于光阱力的无标记的方法。
其中,激光法的激光聚焦束阵列过程比较缓慢,它的方法是将一种类型的细胞偏转一定角度进入到一个单独的收集存储池中,其他类型细胞则直接进入另外一种存储池中,从而实现细胞筛选,但是这种方法的缺点就是细胞类型差异小时会在空间连续偏转,使得细胞的分离不显著;因此,这个方法不适用于高通量、高灵敏度细胞筛选;而荧光标记法存在明显的局限性,可能会影响细胞活性;而基于光阱力的无标记的方法中,存在通量低、灵敏度低等问题。
中国专利文献(申请号为:201410131357.3)公开了一种用于细胞筛选的微流控芯片。该芯片包括t型槽、主通道部分和分支通道,t型槽包括进液通道和2个鞘流通道,其特征在于所述主通道的末端分离出两个子通道:一个子通道的末端形成四个射线状连接的导向通道,另一个子通道连接废液池;四个导向通道中的每个导向通道间隔为30°;每个子通道连接的分支通道包括两个90°的弯角,逆时针分布,在与子通道相连接的分支通道起始部分与主通道垂直,然后依次进行两次逆时针90°转角,形成分支通道,在分支通道末端连接着2个细胞收集器,2号细胞收集器与分支通道末端平行连接,1号细胞收集器与分支通道末端成30°角连接。该发明的缺点在于利用激光法,仍然不能实现高通量和高灵敏度的细胞筛选。
中国专利文献(申请号为:201610398852.x)公开了一种基于尺寸检测循环肿瘤细胞的微流控装置及方法,该装置包括:依次连接的溶液存储室,微流控芯片,废液收集针筒以及动力系统;微流控芯片由玻璃基底层和pdms芯片层贴合而成,pdms芯片层包括依次连通的进样口;由柱子阵列形成的团块过滤区域;目标细胞筛选区域,包括彼此平行间隔延伸的通过过滤通道连通的若干主管道和侧管道,主管道的前端敞开,后端设置过滤通道,侧管道的前端封闭,后端敞开,主管道和侧管道具有大于循环肿瘤细胞的尺寸的第一高度,过滤通道具有小于循环肿瘤细胞的尺寸的第二高度;以及出样口。该发明的缺点在于芯片结构复杂,流道分布多且紧密,制造工艺复杂,成本高,不利于批量生产,且不能实现多块芯片的自由组合,细胞筛选类型受限。
因此,有必要研发出一种灵敏度高,通量大,芯片结构简单,操作便捷,成本低,可灵活组合使用芯片的细胞捕获与筛选的方法。
技术实现要素:
本发明要解决的技术问题是提供一种灵敏度高,通量大,芯片结构简单,操作便捷,成本低,可灵活组合使用芯片的细胞捕获与筛选的方法。
为解决上述技术问题,本发明采用的技术方案是,该细胞捕获与筛选的方法,具体包括以下步骤:
(1)采用至少一个细胞捕获与筛选芯片,从所述细胞捕获与筛选芯片的进样口加入待筛选细胞悬液,所述细胞悬液进入所述细胞捕获与筛选芯片的流道;
(2)所述细胞悬液在所述流道中向所述细胞捕获与筛选芯片的出样口流动,直至反应后的细胞悬液流至所述细胞捕获与筛选芯片的出样口;
(3)从所述出样口流出筛选细胞或细胞复合物。
采用上述技术方案,从进样口加入待筛选细胞悬液,细胞悬液进入流道后,在内部自行向前流动或在泵的控制下向前流动可与固定在流道壁上或腔体中的物质进行反应,反应后的细胞悬液通过流道继续向前流动,可继续与后续流道壁上或腔体中的物质依次反应,最终从出样口流出筛选细胞或细胞复合物,实现对细胞的筛选,从而解决通量低、灵敏度低等问题,其中细胞捕获与筛选芯片可以为不同的结构、面积、体积、流动速度,也可以由多个不同结构的细胞捕获与筛选芯片串行组合在一起使用,在流道壁或腔体中预固定物质,预固定物质可以与杂质细胞反应结合,吸附杂质细胞等,待筛选细胞流出,收集检测;或预固定物质与待筛选细胞反应结合,杂质细胞等流出后,再洗脱收集待筛选细胞来检测;保证待筛选细胞通过流道从出样口流出,从而增加细胞筛选的灵敏度。
作为本发明的优选技术方案,所述步骤(2)中在流动过程所述流道壁或/和腔体中的至少一个预固定物质进行反应,直至反应后的细胞悬液流至所述细胞捕获与筛选芯片的出样口。可以在细胞捕获与筛选芯片中设置腔体与流道相连接,在流道壁预包吸附物质,吸附杂质细胞,在腔体中设置吸附物质或固定荧光标记反应物质,荧光标记物与杂质细胞或待筛选细胞反应,待筛选细胞或杂质细胞反应后流出,检测细胞的筛选效率;检测待筛选细胞的量或与杂质细胞反应间接反映待筛选细胞量,即反应后的细胞悬液通过流道继续向前流动,在后续的流道和腔体中依次反应,最终从出样口流出待筛选细胞或细胞复合物,或者通过荧光物质,直接或间接检测待筛选细胞的量或筛选率。细胞捕获与筛选芯片的流道的长度需要根据筛选率需要来确定。
作为本发明的优选技术方案,该细胞捕获与筛选的方法采用至少两个所述细胞捕获与筛选芯片,相邻两个所述细胞捕获与筛选芯片以串联的方式相连接。细胞捕获与筛选芯片可以串联组合使用,细胞捕获与筛选芯片的流道的长度与细胞捕获与筛选芯片串联的个数需要根据筛选率的需要来确定。
作为本发明的优选技术方案,所述步骤(1)中由配套检测仪器控制或采用移液器向所述进样口加入待筛选细胞悬液。
本发明进一步改进在于,所述细胞捕获与筛选芯片包括进样口、出样口和流道,所述进样口与所述出样口通过所述流道相连通;所述流道从所述进样口至所述出样口之间具有若干个拐角。由玻璃基片和聚二甲基硅氧烷pdms芯片层贴合而成的细胞捕获与筛选芯片,其中流道的高度与宽度需要根据筛选率的需要来确定。
作为本发明的优选技术方案,两个相邻所述拐角之间的流道为直线型。将流道设置成直线型可以最大程度地实现细胞流动与流道长度的优化,可以利用细胞粒径来筛选,即依次连接流道宽度和高度渐小到允许待筛细胞通过的芯片。
作为本发明的优选技术方案,所述流道与腔体交替串联,两个非拐角的相邻所述腔体之间的所述流道的距离相同。在直线型流道之间均匀设置腔体,增大了细胞载量,同时可以在腔体中设置吸附物质,也可固定抗体进行免疫反应,或者固定其他反应物质,使待筛细胞或杂质细胞反应生成新的细胞复合物,再对待筛细胞或其新的细胞复合物进行后期收集或检测;串行腔体流道的细胞捕获与筛选芯片亦可根据筛选需求与其他形状流道的细胞捕获与筛选芯片组合使用。
作为本发明的优选技术方案,所述流道包括主流道一、主流道二和面腔体流道,所述主流道一的一端与所述进样口相连接,所述主流道一的另一端沿与所述主流道一垂直方向向所述出样口方向延伸且连接所述面腔体流道,所述面腔体流道还与所述主流道二沿其垂直方向向所述进样口方向的延伸端相连接,所述主流道二的另一端与所述出样口相连接。将流道设置为主流道一和主流道二之间夹一个面腔体流道,这样的结构能够实现液体完全充满腔体,不会出现气泡;同时面腔体流道的设置增加了细胞载量,适用于筛选高通量的样本细胞悬液;面腔体流道的细胞捕获与筛选芯片亦可根据筛选需求与其他形状流道的细胞捕获与筛选芯片组合使用。
作为本发明的优选技术方案,所述流道的宽度范围为20~500μm,所述流道高度范围为20~500μm,所述流道的宽高比为1:1~2:1;所述流道的细胞液载量为1~2500μl。
作为本发明的优选技术方案,所述腔体的直径为1000-6500μm,所述腔体的深度与腔体直径的比例为1:1~1:2。
作为本发明的优选技术方案,所述面腔体流道为六边形流道,所述六边形流道的内部设有向上凸起的柱子,所述六边形流道的面积为100~1000mm2;所述六边形流道的高度为0.1~2mm,所述六边形流道的细胞液载量为10~2000μl。设置向上凸起的柱子的作用是保证面腔体流道的深度一致,柱子的数量为4个。
与现有技术相比,本发明具有的有益效果为:
(1)设计了3种结构流道的细胞捕获与筛选芯片,可以单独选择一种结构使用,也可以多种结构串联组合使用;
(2)细胞捕获与筛选芯片可以与检测仪器控制使用或者移液器加液直接使用;
(3)该细胞捕获与筛选的方法细胞筛选灵敏度高,通量大,结构简单,操作便捷,成本低,可灵活组合使用;
(4)该方法能应用范围广,可利用吸附杂质细胞和吸附待筛选细胞两种方式来最终获得待筛选细胞。
附图说明
下面结合附图和本发明的实施方式进一步详细说明:
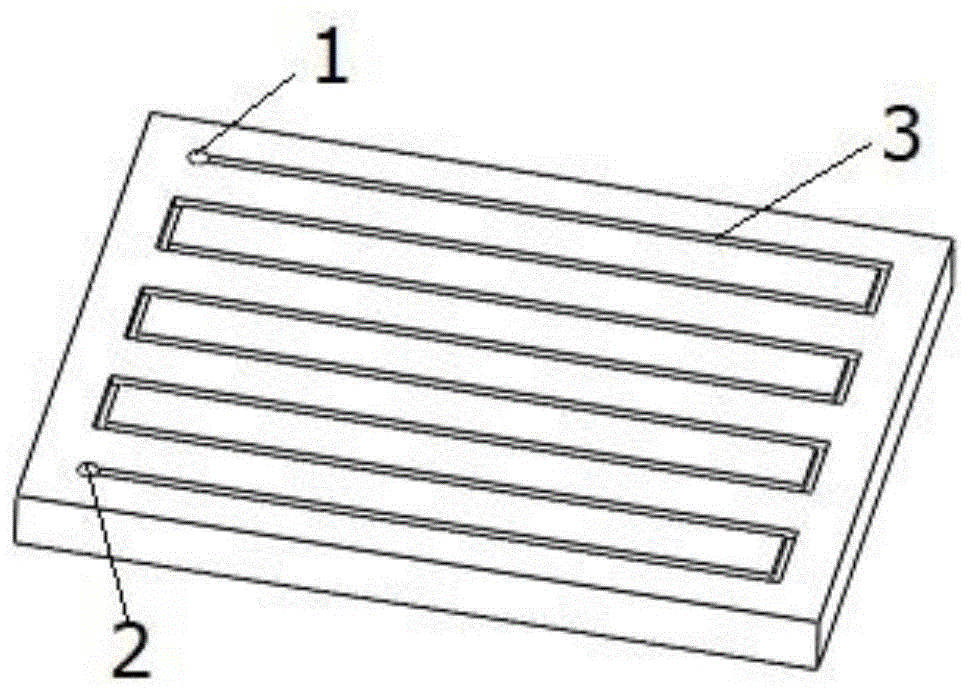
图1是本发明实施例4的结构图;
图2是本发明实施例5的结构图;
图3是本发明实施例6的结构图;
图4是本发明实施例7的结构图;
图5是本发明实施例8的结构图;
图6是本发明实施例9的结构图;
其中1-进样口;2-出样口;3-流道;301-主流道一;302-主流道二;303-面腔体流道;304-延伸端;4-腔体;5-柱子。
具体实施方式
实施例1:该细胞捕获与筛选的方法,具体包括以下步骤:
(1)采用一个流道3为直线型的细胞捕获与筛选芯片,由配套检测仪器控制或采用移液器向所述进样口1加入待筛选细胞悬液,所述细胞悬液进入所述细胞捕获与筛选芯片的流道3;
(2)所述细胞悬液在所述流道中向所述细胞捕获与筛选芯片的出样口2流动,直至反应后的细胞悬液流至所述细胞捕获与筛选芯片的出样口2;
(3)从所述出样口2流出筛选细胞或细胞复合物。
从进样口1加入待筛选细胞悬液,细胞悬液进入流道3后,在内部自行向前流动或在泵的控制下向前流动可与固定在流道壁上的物质进行反应,反应后的细胞悬液通过流道3继续向前流动,可继续与后续流道壁上的物质依次反应,最终从出样口流出筛选细胞或细胞复合物,实现对细胞的筛选,从而解决通量低、灵敏度低等问题,其中细胞捕获与筛选芯片的流道还可以为腔体与直线串联的,也可以为面腔体流道。
实施例2:该细胞捕获与筛选的方法,具体包括以下步骤:
(1)采用一个流道3为直线与腔体交替串联的细胞捕获与筛选芯片,由配套检测仪器控制或采用移液器向所述进样口1加入待筛选细胞悬液,所述细胞悬液进入所述细胞捕获与筛选芯片的流道3;
(2)所述细胞悬液在所述流道中向所述细胞捕获与筛选芯片的出样口2流动,且在流动过程依次与所述流道壁上的多个预固定物质和多个腔体4中的预固定物质进行反应,反应后的细胞悬液通过流道3继续向前流动,在后续的流道和腔体中依次反应,最终从出样口流出待筛选细胞或细胞复合物,其中流道壁预包吸附物质,吸附杂质细胞,在腔体中固定荧光标记反应物质,荧光标记物与杂质细胞或待筛选细胞反应,待筛选细胞或杂质细胞反应后流出,检测待筛选细胞的筛选效率;直至反应后的细胞悬液流至所述细胞捕获与筛选芯片的出样口;
(3)从所述出样口流出筛选细胞或细胞复合物。
实施例3:该细胞捕获与筛选的方法,具体包括以下步骤:
(1)采用两个细胞捕获与筛选芯片串联,其中一个细胞捕获与筛选芯片的流道3为直线型,另一个细胞捕获与筛选芯片的流道3为直线与腔体交替串联的,由配套检测仪器控制或采用移液器向所述进样口加入待筛选细胞悬液,所述细胞悬液进入所述细胞捕获与筛选芯片的流道;
(2)所述细胞悬液在所述流道3中向所述细胞捕获与筛选芯片的出样口2流动,且在流动过程依次与所述流道壁上的多个预固定物质和多个腔体4中的预固定物质进行反应,反应后的细胞悬液通过流道继续向前流动,在后续的流道和腔体中依次反应,最终从出样口流出待筛选细胞或细胞复合物,其中流道壁预包吸附物质,吸附杂质细胞,在腔体4中固定荧光标记反应物质,荧光标记物与待筛选细胞反应,待筛选细胞或杂质细胞反应后流出,检测待筛选细胞的筛选效率;直至反应后的细胞悬液流至所述细胞捕获与筛选芯片的出样口2;
(3)从所述出样口流出筛选细胞或细胞复合物。
实施例4:如图1所示,细胞捕获与筛选芯片包括进样口1、出样口2和流道3,所述进样口1与所述出样口2通过所述流道3相连通;所述流道3从所述进样口1至所述出样口2之间具有14个拐角;由玻璃基片和聚二甲基硅氧烷pdms芯片层贴合而成的细胞捕获与筛选芯片,两个相邻所述拐角之间的流道3为直线型;其中所述流道3的宽度范围为200μm,所述流道3高度范围为200μm,所述流道3的宽高比为1:1;所述流道3的细胞液载量为25μl。
实施例5:如图2所示,细胞捕获与筛选芯片包括进样口1、出样口2和流道3,所述进样口1与所述出样口2通过所述流道3相连通;所述流道3从所述进样口1至所述出样口2之间具有8个拐角;由玻璃基片和聚二甲基硅氧烷pdms芯片层贴合而成的细胞捕获与筛选芯片,两个相邻所述拐角之间的流道3为直线型;所述流道3与腔体4交替串联,两个非拐角的相邻所述腔体4之间的所述流道的距离相同;其中所述流道3的宽度范围为200μm,所述流道3高度范围为200μm,所述流道3的宽高比为1:1;所述流道3的细胞液载量为300μl;所述腔体4的直径为1000μm,所述腔体4的深度与腔体4直径的比例为1:1;其中细胞载流量与流道3的宽度、高度和腔体的大小以及腔体个数有关系。
实施例6:如图3所示,细胞捕获与筛选芯片包括进样口1、出样口2和流道3,所述进样口1与所述出样口2通过所述流道3相连通;所述流道3从所述进样口1至所述出样口2之间具有4个拐角;由玻璃基片和聚二甲基硅氧烷pdms芯片层贴合而成的细胞捕获与筛选芯片,所述流道3包括主流道一301、主流道二302和面腔体流道303,所述主流道一301的一端与所述进样口1相连接,所述主流道一301的另一端沿与所述主流道一301垂直方向向所述出样口2方向延伸且连接所述面腔体流道303,所述面腔体流道303还与所述主流道二302沿其垂直方向向所述进样口1方向的延伸端304相连接,所述主流道二302的另一端与所述出样口2相连接;所述面腔体流道303为六边形流道,所述六边形流道的内部设有向上凸起的柱子5,所述六边形流道的面积为500mm2;所述六边形流道的高度为0.5mm,所述六边形流道的细胞液载量为250μl;设置向上凸起的柱子5的作用是保证面腔体流道的深度一致,柱子5的数量为4个。
实施例7:如图4所示,与实施例4不同之处在于,流道3的宽高比为2:1;所述流道3的细胞液载量为75μl;具体的,细胞捕获与筛选芯片包括进样口1、出样口2和流道3,所述进样口1与所述出样口2通过所述流道3相连通;所述流道3从所述进样口1至所述出样口2之间具有14个拐角;由玻璃基片和聚二甲基硅氧烷pdms芯片层贴合而成的细胞捕获与筛选芯片,两个相邻所述拐角之间的流道3为直线型;其中所述流道3的宽度范围为400μm,所述流道3高度范围为200μm,所述流道3的宽高比为2:1;所述流道3的细胞液载量为75μl。
实施例8:如图5所示,与实施例5不同之处在于,腔体4的数量和大小不同,所述腔体4的数量为13个;所述腔体4的直径为3000μm;具体地,细胞捕获与筛选芯片包括进样口1、出样口2和流道3,所述进样口1与所述出样口2通过所述流道3相连通;所述流道3从所述进样口1至所述出样口2之间具有4个拐角;由玻璃基片和聚二甲基硅氧烷pdms芯片层贴合而成的细胞捕获与筛选芯片,两个相邻所述拐角之间的流道3为直线型;所述流道3与33个腔体4交替串联,两个非拐角的相邻所述腔体4之间的所述流道的距离相同;其中所述流道3的宽度范围为200μm,所述流道3高度范围为200μm,所述流道3的宽高比为1:1;所述流道3的细胞液载量为1000μl;所述腔体4的直径为3000μm,所述腔体4的深度与腔体4直径的比例为1:1。
实施例9:如图6所示,与实施例8不同之处在于,腔体4的数量和大小不同,所述腔体的数量为10个;所述腔体4的直径为6000μm;具体地,细胞捕获与筛选芯片包括进样口1、出样口2和流道3,所述进样口1与所述出样口2通过所述流道3相连通;所述流道3从所述进样口1至所述出样口2之间具有4个拐角;由玻璃基片和聚二甲基硅氧烷pdms芯片层贴合而成的细胞捕获与筛选芯片,两个相邻所述拐角之间的流道3为直线型;所述流道3与33个腔体交替串联,两个非拐角的相邻所述腔体4之间的所述流道的距离相同;其中所述流道3的宽度范围为200μm,所述流道3高度范围为200μm,所述流道3的宽高比为1:1;所述流道3的细胞液载量为1000μl;所述腔体4的直径为6000μm,所述腔体4的深度与腔体4直径的比例为1:1。
以上显示和描述了本发明的基本原理、主要特征及优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,例如改变细胞捕获与筛选芯片的数量和细胞捕获与筛选芯片流道的形状与大小等,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!