制造对苯二甲酸的方法与流程
1.本发明是关于制造对苯二甲酸的方法。
背景技术:
2.聚酯具有优异的机械强度及化学安定性,因此已广泛地应用于各种用途。然而,由于不同产品的成份组成皆不同,添加物也不同,因此增加了不同产品中的聚酯回收的难度。
3.在聚对苯二甲酸乙二酯制品的回收中,其中一个阶段是形成对苯二甲酸晶体。然而,目前的技术中,形成的对苯二甲酸晶体的粒径过小(例如约10微米),过小的粒径增加后续加工的难度。一般来说,工业上使用的对苯二甲酸晶体的粒径需要大于30微米,才能有较好的加工品质。因此,亟需一种新颖的对苯二甲酸的制造方法,以解决上述问题。
技术实现要素:
4.本发明的目的在于提供一种对苯二甲酸的制造方法,可以基本上克服现有技术中形成的对苯二甲酸晶体的粒径过小,从而增加后续加工的难度的问题。
5.根据本揭露的一态样,制造对苯二甲酸的方法,包含:提供一被滴定液,此被滴定液为水;将对苯二甲酸二钠水溶液以及一酸性滴定液加入被滴定液中,以形成对苯二甲酸晶体及一滴定终点溶液;以及分离对苯二甲酸晶体与滴定终点溶液。
6.根据本发明一或多个实施方式,在将对苯二甲酸二钠水溶液以及酸性滴定液加入被滴定液中的过程中,被滴定液的ph值为1.0-3.5。
7.根据本发明一或多个实施方式,将对苯二甲酸二钠水溶液以及酸性滴定液加入被滴定液中,被滴定液的温度介于50℃-90℃。
8.根据本发明一或多个实施方式,滴定终点溶液的ph值为1.0-3.5。
9.根据本发明一或多个实施方式,在将对苯二甲酸二钠水溶液以及酸性滴定液加入被滴定液中之前,更包含将一晶种加入被滴定液中。
10.根据本发明一或多个实施方式,晶种为对苯二甲酸。
11.根据本发明一或多个实施方式,以对苯二甲酸二钠水溶液的对苯二甲酸二钠的重量为100重量份计,晶种为0.05至0.2重量份。
12.根据本发明一或多个实施方式,酸性滴定液为稀硫酸水溶液。
13.根据本发明一或多个实施方式,稀硫酸水溶液的重量百分浓度为10%-50%。
14.根据本发明一或多个实施方式,对苯二甲酸晶体的中位粒径dv
50
为70-150微米。
15.与现有技术相比,本发明的对苯二甲酸的制造方法的优点在于:本发明形成的对苯二甲酸晶体的粒径大于30微米,因此可以直接用于后续的加工应用,而不需要额外的再结晶等步骤。
附图说明
16.为让本发明的上述和其他目的、特征、优点与实施方式能更明显易懂,所附图式的
详细说明如下:
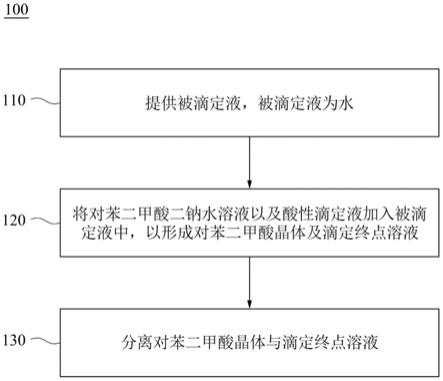
17.图1绘示根据本发明的某些实施例的制造对苯二甲酸的方法100的流程图;
18.图2绘示根据本发明实施例1的对苯二甲酸晶体的粒径分布图;
19.符号说明:
20.100:方法
21.110、120、130:步骤。
具体实施方式
22.以下揭露提供许多不同实施例或示例,以建置所提供的标的物的不同特征。以下叙述的成份和排列方式的特定示例是为了简化本公开。这些当然仅是作为示例,其目的不在构成限制。举例而言,元件的尺寸不被揭露的范围或数值所限制,但可以取决于元件的制程条件与/或所需的特性。
23.除非内容中有其他清楚的指称,本文所使用的单数词包含复数的指称对象。通过参考「一实施例」这样特定的指称,在至少其中之一的本揭露的实施例中,表示一种特定的特征、结构或特色,因此在各处的「在一实施例」,这样的片语通过特别的指称出现时,并不需要参考相同的实施方式,更进一步,在一或多实施方式中,这些特别的特征、结构、或特色可以依合适的情况相互组合。
24.本发明提供一种制造对苯二甲酸的方法。请参考图1,其绘示根据本发明的某些实施例的制造对苯二甲酸的方法100的流程图。
25.请参考步骤110,提供被滴定液,其中被滴定液为水。此处的「被滴定液为水」指的是被滴定液包含水或是被滴定液实质上由水所组成。换句话说,在某些实施例中,被滴定液可以包含水以外的成份。
26.在一些实施例中,可以将晶种加入被滴定液中。藉由加入结构规则的晶体,溶液里的分子不需要太依赖随机流动,即可容易地进行交互作用。在溶液中,溶质结晶产生出晶格的相变化被称为成核。换句话说,加入晶种的效果就是缩短了结晶过程中的成核时间。因此,加入晶种可以使后续步骤更容易形成对苯二甲酸晶体,且形成的对苯二甲酸晶体的粒径也会较大。在一些实施例中,此晶种可以为对苯二甲酸。换句话说,可以藉由加入少许商用对苯二甲酸,使得整体制程速度加快,生成的对苯二甲酸晶体品质更佳。
27.接着请参考步骤120,将对苯二甲酸二钠水溶液以及酸性滴定液加入被滴定液中,以形成对苯二甲酸晶体及滴定终点溶液。值得注意的是,在此步骤中,对苯二甲酸二钠水溶液及酸性滴定液是同时分别加入被滴定液中。在一些实施例中,是使用两台蠕动泵将对苯二甲酸二钠水溶液及酸性滴定液分别注入被滴定液中。详细而言,本发明是采用双柱滴定法。
28.在一些实施例中,对苯二甲酸二钠水溶液包含纯水以及对苯二甲酸二钠。在某些实施例中,对苯二甲酸二钠水溶液的重量百分率为2wt%-10wt%,例如3wt%、5wt%、7wt%或9wt%。
29.在一些实施例中,在对苯二甲酸二钠水溶液以及酸性滴定液加入被滴定液的过程中,被滴定液的ph值维持在1.0-3.5,例如1.5、2.0、2.5或3.0。在一些实施例中,可以先将酸性滴定液加入被滴定液中,待被滴定液的ph值为1.0-3.5时,再将对苯二甲酸二钠水溶液以
及酸性滴定液加入被滴定液中,同时调控被滴定液的ph值为1.0-3.5。本发明藉由控制被滴定液的ph值在上述范围,以形成品质较佳的对苯二甲酸晶体,例如粒径较大的对苯二甲酸晶体。由于本发明使用双柱滴定法,因此可以更精确的控制被滴定液的ph值。在某些实施例中,滴定终点溶液的ph值为1.0-3.5,例如1.5、2.0、2.5或3.0。需了解的是,此处的滴定终点指的是将反应物(对苯二甲酸二钠)反应完的状况。若在滴定过程中,被滴定液的ph值低于1.0或高于3.5,或滴定终点溶液的ph值低于1.0或高于3.5,则生成的对苯二甲酸晶体的纯度较低。
30.本发明的对苯二甲酸二钠水溶液(碱性)以及酸性滴定液(酸性)的流速及浓度需要互相搭配,以使被滴定液的ph值维持在特定范围。举例来说,对苯二甲酸二钠水溶液的流速为每分钟5-10毫升,例如每分钟6毫升、7毫升、8毫升或9毫升。酸性滴定液的流速为每分钟1-5毫升,例如每分钟2毫升、3毫升或4毫升。上述的流速仅为例示性的,根据对苯二甲酸二钠水溶液及酸性滴定液的使用量以及酸性滴定液的种类而有不同。在大规模量产时,对苯二甲酸二钠水溶液及酸性滴定液的流速可达每分钟数升。在一些实施例中,上述的滴定完成时间为约1-8小时,例如2小时、3小时、4小时、5小时、6小时或7小时。若滴定完成时间小于1小时,则形成的对苯二甲酸晶体的粒径较小。若滴定完成时间大于8小时,则使得整体制程的时间过长,影响生产效率。
31.值得注意的是,若滴定过程中,被滴定液的ph值超出上述的范围,例如大于3.5或低于1.0,则形成的对苯二甲酸晶体的粒径较小。
32.此外,在一些实施例中,可以在50℃-90℃下将对苯二甲酸二钠水溶液以及酸性滴定液加入被滴定液,例如60℃、70℃或80℃。在一些实施例中,将对苯二甲酸二钠水溶液以及酸性滴定液加入被滴定液时,被滴定液的温度为50℃-90℃,例如60℃、70℃或80℃。藉由控制滴定的温度在上述范围,亦可以使形成的对苯二甲酸晶体品质更佳,例如粒径较大的对苯二甲酸晶体。
33.在一些实施例中,酸性滴定液可以为稀硫酸水溶液。在某些实施例中,此稀硫酸水溶液的重量百分浓度可以为10%-50%,例如20%、30%或40%。
34.请参考步骤130,分离对苯二甲酸晶体与滴定终点溶液。由于对苯二甲酸晶体难溶于滴定终点溶液,因此可以使用任何固液分离的方法。在一些实施例中,可以使用重力过滤或减压过滤(即利用重力或减压方式辅助进行过滤)。
35.在一些实施例中,对苯二甲酸晶体的中位粒径dv
50
为70-200微米。在一些实施例中,对苯二甲酸晶体的中位粒径dv
50
大于70微米,例如75微米、80微米、85微米或90微米。如前述,一般来说,工业上使用的对苯二甲酸晶体的粒径需要大于30微米,才能有较好的加工品质。因此,本发明形成的对苯二甲酸晶体可以直接用于后续的加工应用,不需要额外的再结晶等步骤。在一些实施例中,对苯二甲酸晶体的中位粒径dv
50
小于150微米,例如140微米、130微米、120微米、110微米或100微米。
36.以下例示性描述本发明的一些实施例及比较例。需了解的是,以下的实施例是例示性的,因此并不意欲限制本发明的实施方式。
37.实施例1
38.将50克对苯二甲酸二钠(alfa aesar
tm
,99+%)加入1000克纯水中,以形成对苯二甲酸二钠水溶液。另外,配制60克的40%稀硫酸溶液,并准备800克的纯水作为被滴定液。之
后,在上述纯水(被滴定液)中加入0.05克对苯二甲酸,并在50℃-90℃下使用搅拌机缓慢搅拌。将对苯二甲酸二钠水溶液以及稀硫酸溶液滴入被滴定液中,并以蠕动泵控制对苯二甲酸二钠水溶液以及稀硫酸溶液的滴定流速。对苯二甲酸二钠水溶液的流速为每分钟8毫升,稀硫酸的流速为每分钟1.5-3.5毫升,使得被滴定液的ph值维持在1.0-3.5。在滴定期间,对苯二甲酸缓慢析出。滴定终点是为对苯二甲酸二钠水溶液用完的时候。之后,以抽气过滤的方式分离对苯二甲酸与被滴定液,并使用激光粒径分析仪量测粒径。
39.比较例1
40.将50克对苯二甲酸二钠(alfa aesar
tm
,99+%)以及0.05克对苯二甲酸加入1000克纯水中,以形成对苯二甲酸二钠水溶液。另外,配制60克的40%稀硫酸溶液。之后,在60℃下使用搅拌机缓慢搅拌对苯二甲酸二钠水溶液(被滴定液)。将稀硫酸溶液滴入被滴定液中,并以蠕动泵控制稀硫酸溶液的滴定流速。稀硫酸的流速为每分钟0.3毫升。在滴定期间,对苯二甲酸缓慢析出。当被滴定液的ph值为1.0-3.5时,即达到滴定终点。之后,以抽气过滤的方式分离对苯二甲酸与被滴定液,并使用激光粒径分析仪量测粒径。
41.以下表1为上述实施例1及比较例1生成的对苯二甲酸晶体的dv
10
、dv
50
、dv
90
以及过滤完成时间,其中dv
10
代表10%的对苯二甲酸晶体的直径小于或等于此值,dv
50
代表50%的对苯二甲酸晶体的直径小于或等于此值,dv
90
代表90%的对苯二甲酸晶体的直径小于或等于此值。
42.表1
[0043] 实施例1比较例1dv
10
34.75.27dv
50
(中位粒径)75.538.8dv
90
173.3262.8过滤完成时间(sec)2242
[0044]
从表1可以发现,实施例1的中位粒径dv
50
为75.5微米,远大于比较例1的中位粒径dv
50
,显示本发明的方法确实可以获得粒径较大的对苯二甲酸晶体。再者,由dv
10
、dv
50
及dv
90
可以了解实施例1的粒径分布较为集中,而比较例1的粒径分布较为分散。在后续的应用上,粒径分布过广会导致加工上的困难。因此,本发明的方法形成的对苯二甲酸晶体有利于后续的加工。
[0045]
此外,实施例1的过滤完成时间仅须比较例1的过滤完成时间的一半。由于比较例1形成的对苯二甲酸晶体的粒径较小,导致过滤时生成的滤饼密度较高,因而影响了过滤完成时间。相较于比较例1,使用本发明的方法可以使粒径提升将近两倍,在同样过滤量下,过滤时间缩短约52%。
[0046]
值得注意的是,实施例1在滴定过程中ph值维持在1.0-3.5。然而,比较例1的被滴定液为对苯二甲酸二钠水溶液,因此初始为偏碱性(例如ph值为约8),随着酸性滴定液滴入,ph值下降至1.0-3.5,达到滴定终点。从实施例1与比较例1之间可以了解,滴定过程中的ph值对于对苯二甲酸晶体的粒径有一定程度的影响。
[0047]
请参考图2,其绘示根据本发明实施例1的对苯二甲酸晶体的粒径分布图。在图2中,曲线为累积百分比,对应左侧的纵轴。长条图为各粒径的百分比,对应右侧的纵轴。从图2可以发现,本发明的对苯二甲酸晶体的粒径分布类似于高斯分布,有利于后续加工。此外,
实施例1的对苯二甲酸晶体有将近40%的粒径大于100微米,大幅增加对苯二甲酸晶体的可用性。
[0048]
本发明提供的制造对苯二甲酸的方法,可以大幅提升形成的对苯二甲酸晶体的粒径,使得制作出来的对苯二甲酸晶体可以直接用于后续加工。值得注意的是,本发明采用双柱滴定法,将对苯二甲酸二钠溶液及酸性滴定液分别加入被滴定液中,因此可以精确的控制滴定过程的被滴定液的ph值。由于滴定过程的ph值维持在特定范围,因此形成的对苯二甲酸晶体的中位粒径可以大于75微米。
[0049]
虽然本揭露已以实施方式揭露如上,然其并非用以限定本揭露,任何熟习此技术者,在不脱离本揭露的精神与范围内,当可作各种更动与润饰,因此本揭露的保护范围当视后附的申请专利范围所界定者为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1