一种Ⅱ型犬腺病毒的可视化等温扩增检测试剂及其应用的制作方法
本发明涉及病毒检测技术领域,特别是涉及一种ⅱ型犬腺病毒的可视化等温扩增检测试剂及其应用。
背景技术:
犬腺病毒(canineadenovirus,cav)属于腺病毒科哺乳动物腺病毒属的成员之一,是一种无囊膜的直径为80-110nm的颗粒,其衣壳蛋白呈20面体结构。cav-2感染广泛流行于犬科动物中,主要引起犬的传染性喉气管炎和肠炎,以三月龄至一岁的犬科动物的感染率最高。由于此年龄阶段,幼犬体内来自母体抗体水平下降,加上环境污染和预防不及时,一旦感染对机体产生极大损伤。感染后多表现为高热、咳嗽、浆液性至粘液性鼻漏,扁桃体炎、喉气管炎和肺炎。其病理变化表现为肺膨胀不全、充血,且有出血点,并伴有不同程度的肝脏病变,表现为肝脏肿大,有纤维素性渗出物,支气管淋巴结充血、淤血。cav-2与犬瘟热病毒(cdv)或其他病毒性疾病混合感染时,容易引起继发病症,增加宿主死亡风险。cav-2病毒感染动物模型用于研究病毒重要基因在病毒感染过程的作用以及筛选毒株,以期为研究ⅱ型犬腺病毒病的发病机理、评价和预测抗病毒药物的疗效提供重要依据。
核酸扩增是基因诊断技术中最常用的方法之一,目前核酸扩增的方法有聚合酶链式反应(pcr)、依赖核酸序列扩增(nasba)、自主序列复制(sr)以及链置换技术(sda)等,都能将微量标本进行快速扩增,但在特异性、简便程度、温度和试剂仪器要求等方面各有缺点。现有技术在ⅱ型犬腺病毒研究的普通检测中,具有效率低、难操作、成本高、在生产实际中难以推广的缺陷。
技术实现要素:
本发明的一个目的是要提供ⅱ型犬腺病毒的可视化等温扩增检测试剂及其应用,缩短了检测时间,提高了特异性和敏感性,以及提高了操作的方便性、降低了成本。
特别地,本发明提供了用于检测ⅱ型犬腺病毒的可视化等温扩增引物组,所述引物组由以下引物组成:
上游内引物fip:
cgagggcattgtaggcggtg-gaattc-gggtaccctagacagaggc;
下游内引物bip:
ccaaggccggggctaacaac-ggcacctgggctaaagtg;
上游外引物f3:gctggacatggccagtac;
下游外引物b3:tcacagttatggcacctgc;
加速上游环状引物lf1:ccgctgtaaggcttgaaggag
加速下游环状引物lb1:ctttttaatggacagggtgccaata。
一种ⅱ型犬腺病毒的可视化等温扩增检测试剂,所述试剂为ⅱ型犬腺病毒的可视化等温检测试剂,所述试剂包括上述的引物组。
优选的,所述试剂还包括如下组分:10×反应缓冲液、dntps、mg2+、bstdna聚合酶、去离子水、模板dna和显色试剂。
优选的,所述试剂中mg2+的浓度为6mmol·l-1。
优选的,所述试剂中dntps的浓度为1.5mmol·l-1;作为优选,所述试剂中显色试剂为酚红与甲酚红混合指示剂。
优选的,所述试剂还包括阳性对照。
一种ⅱ型犬腺病毒的可视化等温扩增检测试剂盒,所述试剂盒为ⅱ型犬腺病毒的可视化等温检测试剂盒,其特征在于:所述试剂盒包括上述任一项优选的可视化等温扩增检测试剂。
上述任一项所述的检测试剂或上述的检测试剂盒在如下任一种条件下的应用:
一、不以疾病的诊断和治疗为目的的检测或辅助检测ⅱ型犬腺病毒;
二、制备用于检测或辅助检测ⅱ型犬腺病毒的产品;
三、不以疾病的诊断和治疗为目的的检测或辅助检测待测动物样品是否感染ⅱ型犬腺病毒;
四、制备用于检测或辅助检测待测动物样品是否感染ⅱ型犬腺病毒的产品;
五、不以疾病的诊断和治疗为目的的检测待测病毒是否为ⅱ型犬腺病毒;
六、制备用于检测或辅助检测待测病毒是否为ⅱ型犬腺病毒的产品。
一种检测或辅助检测待测动物样品是否感染ⅱ型犬腺病毒的方法,该方法不以疾病的诊断和治疗为目的,包括以下步骤:
反应步骤:从待测动物肛门、唾液或泪腺分泌物拭子样品提取基因组dna作为模板,采用上述任一项所述的检测试剂或上述的检测试剂盒进行环介导等温扩增,得到扩增产物;作为优选,所述环介导等温扩增的反应条件为:恒温63℃,反应40min;
确认步骤:按照下述任一方法确定待测动物样品是否感染ⅱ型犬腺病毒:
a、扩增产物呈现橙黄色则待测动物样品感染ⅱ型犬腺病毒;扩增产物呈现紫红色则待测动物样品未感染ⅱ型犬腺病毒;
b、将扩增产物进行琼脂糖凝胶电泳,电泳条带呈梯状分布,则待测动物样品感染ⅱ型犬腺病毒;仅有一条引物条带,则待测动物样品未感染ⅱ型犬腺病毒。
一种检测或辅助检测待测病毒为ⅱ型犬腺病毒的方法,该方法不以疾病的诊断和治疗为目的,包括以下步骤:
反应步骤:从待测病毒中提取基因组dna作为模板,采用上述任一项所述的检测试剂或上述的检测试剂盒进行环介导等温扩增,得到扩增产物;作为优选,所述环介导等温扩增的反应条件为:恒温63℃,反应40min;
确认步骤:按照下述任一方法确定待测病毒是否为ⅱ型犬腺病毒:
a、扩增产物呈现橙黄色则待测病毒是ⅱ型犬腺病毒;扩增产物呈现紫红色则待测病毒不是ⅱ型犬腺病毒;
b、将扩增产物进行琼脂糖凝胶电泳,电泳条带呈梯状分布,则待测动物病毒是ⅱ型犬腺病毒;仅有一条引物条带,则待测病毒不是ⅱ型犬腺病毒。
本发明提供了一种ⅱ型犬腺病毒的可视化等温扩增检测试剂及其应用,主要有以下几点有益效果:
1、本发明使用两对特异性引物,四个识别区域,相对现有的检测方法,特异性更高。
2、本发明检测ⅱ型犬腺病毒的的环介导等温试剂盒具有高灵敏性:将抽提出的ⅱ型犬腺病毒dna进行10倍递进稀释后作为lamp反应模板,以同样的模板浓度用pcr方法进行检测,结果表明:lamp方法比常规pcr扩增的方法至少高10倍。由此可见,本发明lamp方法具有更高的灵敏度。
3、本发明检测ⅱ型犬腺病毒的的环介导等温试剂盒具有高特异性:将临床上常见的犬类病毒性疾病:cpv(犬细小病毒)及cacv(犬圆环病毒)、cdv(犬瘟热病毒)、crcov(犬冠状病毒)和cbov(犬博卡病毒)分别作为检测对象,用本发明的方法进行检测,仅cav-2为阳性,具有高特异性。
4、本发明检测ⅱ型犬腺病毒的的环介导等温试剂具有快速性:相对普通pcr反应数小时的反应时间和检测时间,本发明检测方法仅需1个小时即可完成整个反应和结果判定。
5、本发明检测ⅱ型犬腺病毒的的环介导等温试剂具有可操作性:相对于常规pcr,ⅱ型犬腺病毒环介导等温扩检测试剂盒不需要昂贵的pcr仪,只需要一个简单的恒温水浴锅即可完成反应;且结果的检测可以直接肉眼判定,无需凝胶电泳等特殊仪器,因此本发明试剂盒具有较强的可操作性。
6、本发明检测方法容易操作,成本低廉,可广泛应用。
根据下文结合附图对本发明具体实施例的详细描述,本领域技术人员将会更加明了本发明的上述以及其他目的、优点和特征。
附图说明
后文将参照附图以示例性而非限制性的方式详细描述本发明的一些具体实施例。附图中相同的附图标记标示了相同或类似的部件或部分。本领域技术人员应该理解,这些附图未必是按比例绘制的。附图中:
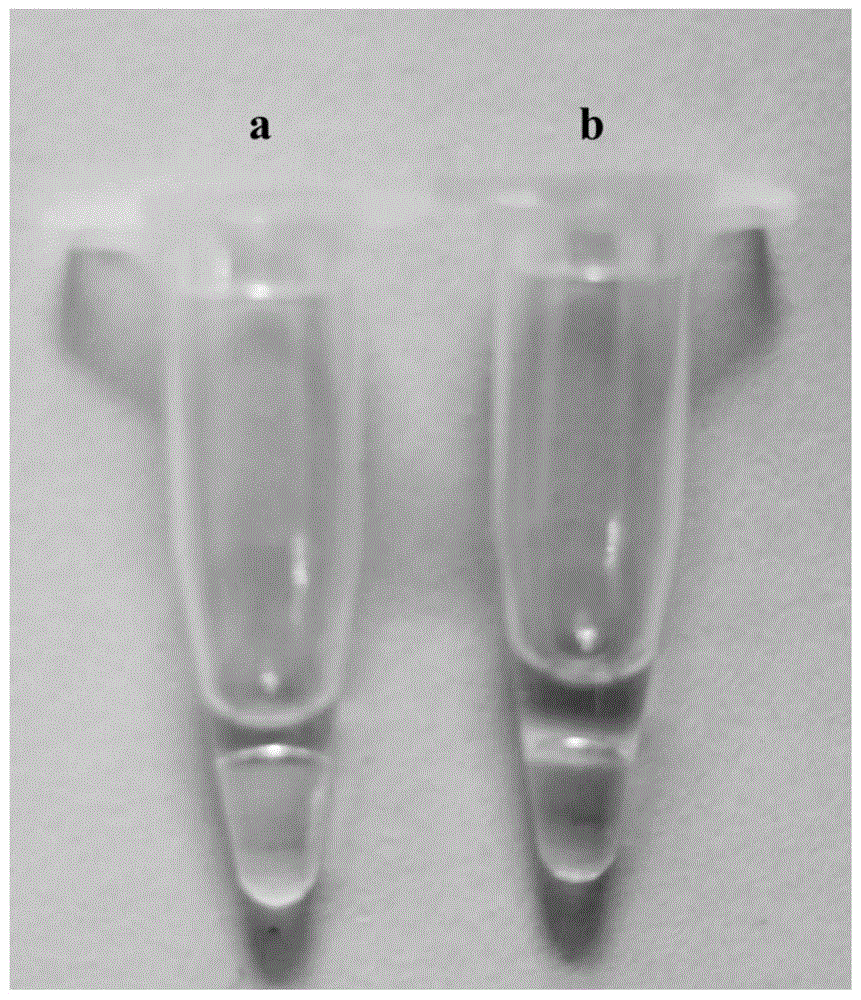
图1为cav-2基因保守区lamp扩增添加核酸染料的变色结果(此染料为反应前加入),a和b分别显示了lamp扩增结果的肉眼可观察,a在自然光下阳性管为橙黄色,而b的阴性管保持紫红色。
图2为cav-2lamp反应特异性试验图。
图3为cav-2lamp反应产物的酶切鉴定结果图。
图4为cav-2lamp反应灵敏度试验图。
图5为cav-2常规pcr反应灵敏度试验图。
具体实施方式
以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为市售。
本研究所涉及的环介导等温扩增技术,能够在1h内,水浴锅环境等温条件下,把拷贝数很低的dna片段扩增到109个拷贝。反应过程中,由于反应溶液中的mg2+与dntp析出的焦磷酸根离子结合产生副产物焦磷酸镁白色沉淀,因此,仅用肉眼观察或使用浊度仪检测浊度就可以判读结果,浊度仪还可以对起始模板定量。环介导等温扩增技术的特点是分别使用对应于靶序列中6个基因区段的2对特殊引物(外引物f3,b3;内引物fip,bip),利用bstdnapolymerase在延伸dna同时的链置换活性,对目的片段进行链置换扩增,不需要双链dna模板的预变性、退火及繁琐的循环变温过程,整个反应在恒温条件(61~63℃左右)下几十分钟即可完成核酸扩增,扩增效率一般高达到109-1010个数量级,大量的核酸产物可使反应结果通过在终产物中加入核酸染料的方法直接用肉眼观察。
1、试剂相关材料
ⅱ型犬腺病毒为实验室分离保存毒株。病毒基因组dna/rna提取试剂盒(北京全式金生物技术有限公司),betaine(sigma公司),bstdna聚合酶及10×反应缓冲液(biolabsinc公司),dntp(clontech公司),mg2+及dl2000(takara公司)。显色试剂为0.025mmol·l-1酚红和0.08mmol·l-1甲酚红混合染色液,均购自solarbio公司。
2、lamp引物的设计与合成
参考目前已发表的cav-2序列,针对cav-2病毒属的保守区域,利用在线设计软件primerexplorerv4分别设计4条引物(f1c和b1c分别与扩增下游的f1区和b1区反向互补,以利于成环和链置换反应的进行),引物包括上游内引物fip(fip由f1c、f2和gaattc(ecorⅰ酶切位点序列)作为连接子组成)、下游内引物bip(bip由b1c、b2组成),此为利于后续扩增产物的酶切鉴定、上游外引物f3和下游外引物b3,序列分别如下:
上游内引物fip:
cgagggcattgtaggcggtg-gaattc-gggtaccctagacagaggc;
下游内引物bip:
ccaaggccggggctaacaac-ggcacctgggctaaagtg;
上游外引物f3:gctggacatggccagtac;
下游外引物b3:tcacagttatggcacctgc;
加速上游环状引物lf1:ccgctgtaaggcttgaaggag
加速下游环状引物lb1:ctttttaatggacagggtgccaata
其中:
fip由f1c和f2和gaattc(ecorⅰ酶切位点序列)组成;
bip由b1c、b2组成。
f1c:cgagggcattgtaggcggtg;
f2:gggtaccctagacagaggc
b1c:ccaaggccggggctaacaac;
b2:ggcacctgggctaaagtg。
表1lamp检测cav-2(ⅱ型犬腺病毒)的引物
设计完成的引物由北京奥科生物工程公司合成,合成后的引物用超纯水稀释成10mmol/ml溶液,-20℃保存。
3、病毒基因组提取
利用北京全式金生物技术有限公司的病毒基因组dna/rna提取试剂盒,提取细胞培养ⅱ型犬腺病毒液、疑似有ⅱ型犬腺病毒感染的患病动物组织样品、特异性对照病毒样品的病毒基因组dna。
4、ⅱ型犬腺病毒lamp反应体系的建立
ⅱ型犬腺病毒检测试剂包括如下组分(m=mol·l-1):
其中,阳性对照为ⅱ型犬腺病毒样品的基因组dna。
将上述组分混匀后放置于pcr仪内或者水浴锅中恒温63℃作用40min;反应结束后,可以将扩增产物用2%琼脂糖凝胶(含0.5μg/ml的溴化乙锭)电泳检测,电泳条件为80v、30min;也可直接肉眼观察其颜色变色,两者判定结果一致。肉眼观察时,阳性结果显示为橙黄色,阴性结果显示为紫红色。
lamp检测结果如图1所示,图1的a和b分别显示了lamp扩增结果的肉眼可观察,自然光下阳性管为橙黄色,而阴性管保持紫红色。
图1为lamp添加核酸染料的变色结果(此染料为反应前加入)图。其中a:阳性扩增产物;b:阴性对照。
5、ⅱ型犬腺病毒lamp检测方法条件的优化
5.1反应时间优化
配置反应体系,每个时间条件的样品设置3个重复,分别在恒温水浴锅中反应30min、40min、50min、60min后取出,待反应产物全部取出后,各取5μl产物,用2%琼脂糖凝胶(含0.5μg/ml的溴化乙锭)电泳对反应产物进行检测。
5.2反应温度的优化
配置反应体系,每个温度条件样品设置3个重复,分别在60℃、61℃、62℃、63℃、64℃、63℃五个反应温度中反应40min后,反应结束后各取5μl产物进行2%琼脂糖凝胶(含0.5μg/ml的溴化乙锭)电泳检测。
5.3反应中各重要组分浓度的优化
在25μl反应体系中,引物浓度、反应所需酶单位与所用模板浓度不变,改变组分mgso4的浓度,摸索mgso4浓度对扩增效率的影响,加入量依次为为7mm、6mm、5mm、4mm、3mm、2mm、1mm、0mm,每个浓度梯度设置3个重复。待所有浓度梯度反应结束后,进行2%琼脂糖凝胶电泳检测;设置不同dntps浓度的反应体系优化,其梯度设置为1.8mm、1.5mm、1.2mm、0.9mm、0.6mm,所有分组反应都以去离子水作为模板设阴性对照,每个浓度梯度设置3个重复。待所有浓度梯度反应结束后,进行2%琼脂糖凝胶电泳检测。
6、ⅱ型犬腺病毒lamp检测方法的优化结果
6.1反应时间优化结果:当反应时间不同时,会随着时间延伸电泳条带越来越明显,在恒温水浴锅中反应60min时,结果最佳。
6.2反应温度优化结果:当反应温度不同时,会出现电泳条带亮度差异,在63℃下反应时,效果最佳。
6.3反应中各重要组分浓度的优化结果:
当mgso4浓度不同时,会出现电泳条带亮度差异,当mgso4浓度为6mm时,效果最佳。
当dntps浓度不同时,会出现电泳条带亮度差异,当dntps浓度为1.5mm时,效果最佳。
6.4优化体系和条件
通过上述条件的优化,ⅱ型犬腺病毒可视化等温扩增检测试剂盒的最后优化的体系为:
环介导等温扩增的反应条件为63℃作用1h。
6.225μl检测体系的ⅱ型犬腺病毒可视化等温扩增检测试剂盒包括如下组分:
7、lamp的特异性试验
以临床上常见的犬类病毒性疾病:犬细小病毒(cpv)、犬瘟热病毒(cdv)、犬i型腺病毒(cav-1)、犬圆环病毒(cacv)、犬博卡病毒(cbov)获得的dna或反转录获得的cdna为检测对象,用cav-2引物进行lamp检测,来验证其反应的特异性,并设置阳性对照,结果参见图2。
lamp检测的反应体系包括如下组分:
其中,ⅱ型犬腺病毒模板dna为使用病毒dna/rna提取试剂盒提取的ⅱ型犬腺病毒基因组dna。
扩增结果显示只有阳性对照出现弥散状条带,其他5种病毒均未出现,说明以其它病毒作为模板时没有阳性扩增,本发明设计的cav-2lamp引物具有高度的特异性。
图2为cav-2lamp反应特异性试验图。其中m:dna分子标准量标准dl2000;泳道1~6分别为cav-2lamp特异性引物检测犬细小病毒(cpv)、犬瘟热病毒(cdv)、犬i型腺病毒(cav-1)、犬圆环病毒(cacv)、犬博卡病毒(cbov)和cav-2的结果。
7.1扩增产物的酶切鉴定
为进一步验证扩增反应的特异性,将lamp反应后产物进行酶切鉴定,在20μl反应体系中加入以下组分,用ecorⅰ对阳性lamp产物进行消化。
将上述反应产物混匀后,37℃反应2h,反应后取出5μl产物,用2%琼脂糖凝胶(含0.5μg/ml的溴化乙锭)对酶切产物进行检测。
结果:理论计算中,cav-2扩增产物经内切酶ecorⅰ消化后,应成为三条大小分别为75bp,139bp和162bp的主带。图3中结果与理论值完全相符,说明本发明建立的检测方法具有很好的特异性。
图3为cav-2lamp反应产物的酶切鉴定结果图。其中m:dna分子标准量标准dl2000;1:cav-2lamp终产物;2:内切酶ecorⅰ消化后的结果。
8、lamp的敏感性试验
取抽提出的病毒液dna产物进行10倍递进稀释至10-7,并分成两部分,一部分用优化后的lamp方法检测,测定该方法的敏感性;另一部分用常规pcr方法检测,将两者检测结果进行比较,参见图4和图5,以验证其反应的敏感性。
结果表明:lamp方法比常规pcr扩增的方法至少高10倍。由此可见,本发明lamp方法具有更高的敏感性。
图4为cav-2lamp反应灵敏度试验图,其中m:dna分子标准量标准dl2000;图4和图5中1~6分别为模板稀释至10-1、10-2、10-3、10-4、10-5、10-6,7为阴性对照。
9、lamp实际应用的符合性
临床采集疑似ⅱ型犬腺病毒感染的组织病样,提取样品基因组,利用建立的的lamp检测方法和常规的pcr以及荧光定量pcr方法进行检测,通过对三种方法实际应用中检测结果比较,验证lamp的符合性。
结果表明:利用ⅱ型犬腺病毒环介导等温扩检测试剂盒和常规pcr以及荧光定量pcr对获得的样品进行检测,发现lamp的检出率显著高于传统的pcr方法,与荧光定量pcr方法出率较为相近,且传统的pcr和荧光定量pcr检出的阳性样品都可以被lamp方法所检出。
至此,本领域技术人员应认识到,虽然本文已详尽示出和描述了本发明的多个示例性实施例,但是,在不脱离本发明精神和范围的情况下,仍可根据本发明公开的内容直接确定或推导出符合本发明原理的许多其他变型或修改。因此,本发明的范围应被理解和认定为覆盖了所有这些其他变型或修改。
- 还没有人留言评论。精彩留言会获得点赞!