一种磺酰胺咪唑盐化合物及其制备方法和应用与流程
本发明属于有机合成和药物化学领域,具体涉及一种磺酰胺咪唑盐化合物及其制备方法和应用。
背景技术:
在有机合成和药物化学中,利用光催化产生的自由基具有很好的反应活性和底物适用性,对自由基受体例如烯烃、炔烃、芳香族化合物都有非常多样化的加成反应。光催化作为一种绿色高效的合成手段,被很多工业生产和药物开发合成广泛利用,避免大量的氧化还原剂和金属试剂对环境的污染和反应体系的干扰,尤其适合多官能团的敏感分子的合成。发展新型光催化自由基试剂具有极高的应用价值。
技术实现要素:
本发明的目的在于提供一种磺酰胺咪唑盐化合物的制备方法,主要包括:将咪唑类化合物的二氯甲烷溶液与磺酸酐进行反应,再与三氟甲磺酸烷基酯反应,然后减压除去溶剂得到磺酰胺咪唑盐的粗品,经用乙醚洗涤得到磺酰胺咪唑盐纯品;该发明涵盖的磺酰胺咪唑盐化合物具有化学性质稳定、成本低、易提纯等优点。
本发明还提供了所述磺酰胺咪唑盐化合物在光催化条件下产生自由基催化其他反应的应用。
为了实现上述目的,本发明采用的技术方案为:一种磺酰胺咪唑盐化合物的制备方法,所述制备方法包括以下步骤:
(1)将咪唑类化合物溶于二氯甲烷,然后加入三乙胺和磺酸酐类化合物或磺酰氟类化合物,搅拌反应;
(2)待步骤(1)反应结束后,除去溶剂并萃取,对有机相进行干燥、抽滤,得到含咪唑磺酰胺的溶液,然后加入三氟甲磺酸烷基酯,经反应得到所述的磺酰胺咪唑盐粗产品;经洗涤得到纯的磺酰胺咪唑盐化合物。
具体地,所述制备方法包括以下步骤:
(1)将咪唑类化合物溶于二氯甲烷,然后加入三乙胺和磺酸酐类化合物或磺酰氟类化合物,搅拌反应;
(2)待步骤(1)反应结束后,除去溶剂并萃取,对有机相进行干燥、抽滤,得到含咪唑磺酰胺的溶液,然后加入三氟甲磺酸烷基酯,经反应得到所述的磺酰胺咪唑盐粗产品;经洗涤得到纯的磺酰胺咪唑盐化合物。
所述步骤(1)将咪唑类化合物溶于置有二氯甲烷溶剂的圆底烧瓶中,形成含咪唑类化合物的有机溶液,向其加入三乙胺和磺酸酐类化合物;优选地,在0℃搅拌反应;优选地,咪唑类化合物、三乙胺和磺酸酐类化合物或磺酰氟类化合物的摩尔比为1:(1.5-3.5):(1.3-3.5);
所述步骤(2)中,应用减压蒸馏除去溶剂;用二氯甲烷进行萃取;应用无水硫酸镁对有机相进行干燥;加入三氟甲磺酸烷基酯进行反应的时间为8-12h;应用乙醚洗涤所述的磺酰胺咪唑盐粗产品;其中,咪唑磺酰胺/三氟甲磺酸烷基酯的摩尔比为1:(1.3-3.5)。
所述步骤(1)的反应条件为:空气环境下,0℃条件下搅拌反应0.5h。
所述步骤(1)中,咪唑类化合物与二氯甲烷溶剂的用量比为1mmol:2ml。
所述步骤(2)中,用乙醚进行洗涤,洗涤1-2次后得到磺酰胺咪唑盐;其中,乙醚与磺酰胺咪唑盐化合物的用量比为2ml:1mmol。
步骤(1)中,所述咪唑类化合物的结构式为
步骤(2)中,所述咪唑磺酰胺化合物的结构式为
优选地,所述咪唑类化合物选自
采用上述方法制备的磺酰胺咪唑盐化合物,其结构式为:
r2和r3连同与其连接的碳原子一起形成苯环,或者r2和r3分别独立的选自h、c1-10烷基、苯基、杂芳基或其它芳基;所述烷基、苯基的任意位被卤素、硝基、甲氧基、烷基、脂基、腈基、三氟甲基取代;
r1选自h、c2-10烷基、苯基、杂芳基或其它芳基;r4为-f、-cf3、-cf2h、-cf2br、-c2f5、-c4f9、-c6f13、-c8f17、-cf2cf2o(cf2)7cf2cl、苄基、烷基、芳基或杂芳基中的任意一种;所述烷基、苯基的任意位被卤素、硝基、甲氧基、烷基、脂基、腈基、三氟甲基取代,所述苯基上取代基的数量为0-5;尤其地,所述烷基任意位被氟取;r5为-me、-et等各种烷基。
本发明另一方面提供所述的类磺酰胺咪唑盐化合物作为催化剂的应用,所述催化剂用于在光催化条件下产生自由基并催化其他反应。
本发明的有益效果为:与现有技术相比,该发明涵盖的磺酰胺咪唑盐化合物不仅具有化学性质稳定、成本低、易提纯、产率高等优点以外,且由于有机离子盐结构的引入,能够适应各种自由基反应;通过修饰咪唑结构,能够选择性生成各种碳自由基,且产生的自由基具有很好的反应活性和底物适用性,对自由基受体例如烯烃、炔烃、芳香族化合物都有非常多样化的合成反应。
附图说明
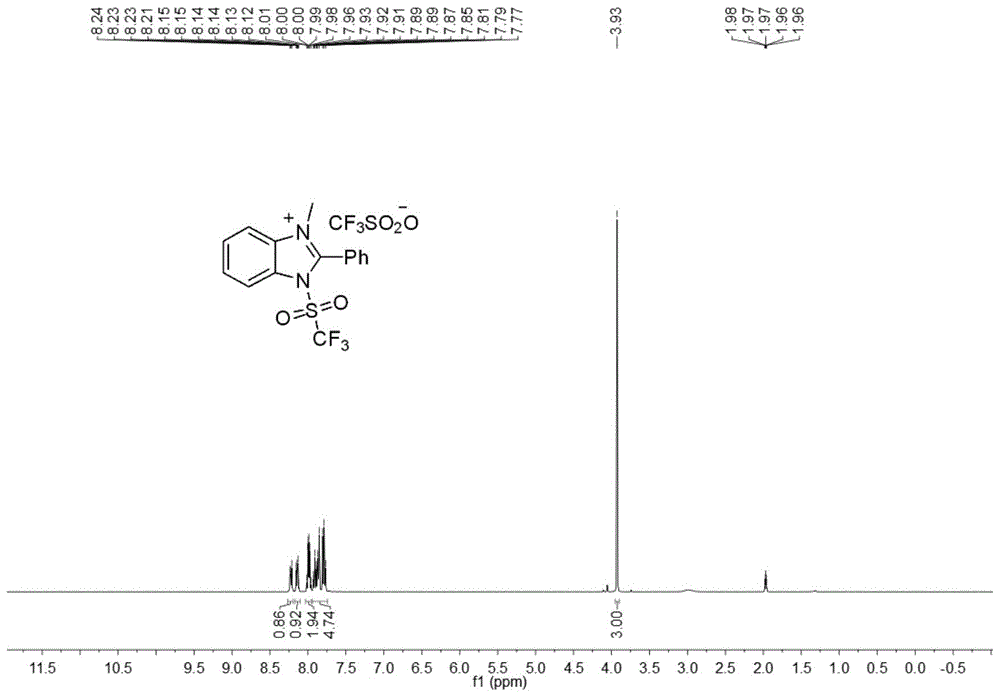
图1为实施例1磺酰胺咪唑盐c1的核磁共振氢谱图;
图2为实施例1磺酰胺咪唑盐c1的核磁共振碳谱图;
图3为实施例1磺酰胺咪唑盐c1的19fnmr谱图;
图4为实施例2磺酰胺咪唑盐c2的核磁共振氢谱图;
图5为实施例2磺酰胺咪唑盐c2的核磁共振碳谱图;
图6为实施例2磺酰胺咪唑盐c2的19fnmr谱图;
图7为实施例3磺酰胺咪唑盐c3的核磁共振氢谱图;
图8为实施例3磺酰胺咪唑盐c3的核磁共振碳谱图;
图9为实施例3磺酰胺咪唑盐c3的19fnmr谱图;
图10为实施例4磺酰胺咪唑盐c4的核磁共振氢谱图;
图11为实施例4磺酰胺咪唑盐c4的核磁共振碳谱图;
图12为实施例4磺酰胺咪唑盐c4的19fnmr谱图;
图13为试验例化合物d-1的核磁共振氢谱图;
图14为试验例化合物d-1的核磁共振碳谱图;
图15为试验例化合物d-1的19fnmr谱图;
图16为试验例化合物e-1的核磁共振氢谱图;
图17为试验例化合物e-1的核磁共振碳谱图;
图18为试验例化合物e-1的19fnmr谱图;
图19为磺酰胺咪唑盐化合物的化学反应通式。
具体实施方式
以下对本发明的具体实施方式进行详细说明。应当理解的是,此处所描述的具体实施方式仅用于说明和解释本发明,并不局限于这些实施例。实施例中,所有反应原料和溶剂等都为安耐吉试剂产品。
实施例1
一种磺酰胺咪唑盐化合物的制备方法,所述制备方法包括以下步骤:
(1)将100mmol咪唑类化合物a1溶于置有200ml二氯甲烷溶剂的圆底烧瓶中,形成含咪唑类化合物a1的有机溶液,向其加入150mmol三乙胺和130mmol三氟甲磺酸酐类化合物,0℃搅拌反应0.5h;
(2)反应结束后,减压蒸馏除去溶剂,然后用二氯甲烷萃取多次,通过无水硫酸镁对有机相进行干燥、抽滤,得到咪唑磺酰胺b1的二氯甲烷溶液,然后加入130mmol三氟甲磺酸甲酯,反应8-12h,得到所述的磺酰胺咪唑盐粗产品,最后用200ml乙醚洗涤得到纯的磺酰胺咪唑盐化合物。其中,产物磺酰胺咪唑盐c1的产率为91%,白色固体。
所得磺酰胺咪唑盐化合物c1的产品结构式为:
产品的核磁共振氢谱数据:
1hnmr(400mhz,cd3cn)δ8.24–8.21(m,1h),8.15–8.12(m,1h),8.01–7.96(m,2h),7.93–7.77(m,5h),3.93(s,5h);
产品的核磁共振碳谱数据:
13cnmr(101mhz,cd3cn)δ154.9,134.7,132.8,131.3,131,130.6,130.2,129.8,121.6(q,j=319.0hz),120.3,119.4(q,j=321.0hz),115.8,115.6,35.1;
产品的19fnmr数据:
19fnmr(377mhz,cd3cn)δ-73.91,-79.32;
产品的红外数据:
ir(neat)ν(cm-1):3069.5,3045.2,1608.3,1569.2,1448.1,1263.6,1218.8,1131.2,1028.7,965.4,799.5,762.2,697.0;
产品的高分辨质谱数据:
hrms(esi):caledforc15h12f3n2o2s+[m]+341.0566;found341.0571.
实施例2
一种磺酰胺咪唑盐化合物的制备方法,所述制备方法包括以下步骤:
(1)将100mmol咪唑类化合物a2溶于置有200ml二氯甲烷溶剂的圆底烧瓶中,形成含咪唑类化合物a2的有机溶液,向其加入150mmol三乙胺和130mmol三氟甲磺酸酐类化合物,0℃搅拌反应0.5h;
(2)反应结束后,减压蒸馏除去溶剂,然后用二氯甲烷萃取多次,通过无水硫酸镁对有机相进行干燥、抽滤,得到咪唑磺酰胺b2的二氯甲烷溶液,然后加入130mmol三氟甲磺酸甲酯,反应8-12h,得到所述的磺酰胺咪唑盐粗产品,最后用200ml乙醚洗涤得到纯的磺酰胺咪唑盐化合物。其中,产物磺酰胺咪唑盐c2的产率为82%,白色固体。
所得磺酰胺咪唑盐化合物c2的产品结构式为:
产品的核磁共振氢谱数据:
1hnmr(400mhz,cd3cn)δ10.01(s,1h),8.21-8.16(m,2h),8.08–8.00(m,2h),4.37(d,j=0.8hz,3h);
产品的核磁共振碳谱数据:
13cnmr(101mhz,cd3cn)δ145.67,133.5,131.4,130.1,129.9,121.6(q,j=319.0hz),119.4(q,j=321.0hz),115.9,114.9,35.95;
产品的19fnmr数据:
19fnmr(377mhz,cdcl3)δ-68.85(d,j=1.3hz),-74.08.
产品的红外数据:
ir(neat)ν(cm-1):3076.9,3011.7,2987.5,2950.2,1619.5,1578.5,1449.9,1285.9,1218.8,1129.4,1025.0,971.0,771.6,751.1;
产品的高分辨质谱数据:
hrms(esi):caledforc9h8f3n2o2s+[m]+265.0253;found265.0261.
实施例3
一种磺酰胺咪唑盐化合物的制备方法,所述制备方法包括以下步骤:
(1)将100mmol咪唑类化合物a3溶于置有200ml二氯甲烷溶剂的圆底烧瓶中,形成含咪唑类化合物a3的有机溶液,向其加入150mmol三乙胺和130mmol三氟甲磺酸酐类化合物,0℃搅拌反应0.5h;
(2)反应结束后,减压蒸馏除去溶剂,然后用二氯甲烷萃取多次,通过无水硫酸镁对有机相进行干燥、抽滤,得到咪唑磺酰胺b3的二氯甲烷溶液,然后加入130mmol三氟甲磺酸甲酯,反应8-12h,得到所述的磺酰胺咪唑盐粗产品,最后用200ml乙醚洗涤得到纯的磺酰胺咪唑盐化合物。其中,产物磺酰胺咪唑盐c3的产率为89%,白色固体。
所得磺酰胺咪唑盐化合物c3的产品结构式为:
产品的核磁共振氢谱数据:
1hnmr(400mhz,cd3cn)δ8.15–8.09(m,1h),8.06–8.00(m,1h),7.90–7.84(m,2h),4.14(s,3h),3.15(s,3h);
产品的核磁共振碳谱数据:
13cnmr(101mhz,cd3cn)δ157.6,132.4,130.4,130.1,129.5,121.9(q,j=319.0hz),120.0(q,j=321.0hz),115.3,115.0,34.2,13.9;
产品的19fnmr数据:
19fnmr(377mhz,cd3cn)δ-69.29,-74.04.
产品的红外数据:
ir(neat)ν(cm-1):3136.6,3093.7,1627.0,1448.1,1399.6,1217.0,1127.5,1030.6,971.0,896.4,760.4,687.7;
产品的高分辨质谱数据:
hrms(esi):caledforc10h10f3n2o2s+[m]+279.0410;found279.0417.
实施例4
一种磺酰胺咪唑盐化合物的制备方法,所述制备方法包括以下步骤:
(1)将100mmol咪唑类化合物a4溶于置有200ml二氯甲烷溶剂的圆底烧瓶中,形成含咪唑类化合物a4的有机溶液,向其加入150mmol三乙胺和130mmol三氟甲磺酸酐类化合物,0℃搅拌反应0.5h;
(2)反应结束后,减压蒸馏除去溶剂,然后用二氯甲烷萃取多次,通过无水硫酸镁对有机相进行干燥、抽滤,得到咪唑磺酰胺b4的二氯甲烷溶液,然后加入130mmol三氟甲磺酸甲酯,反应8-12h,得到所述的磺酰胺咪唑盐粗产品,最后用200ml乙醚洗涤得到纯的磺酰胺咪唑盐化合物。其中,产物磺酰胺咪唑盐c4的产率为92%,白色固体。
所得磺酰胺咪唑盐化合物c4的产品结构式为:
产品的核磁共振氢谱数据:
1hnmr(400mhz,cd3cn)δ8.12(s,1h),7.95–7.93(m,1h),7.86–7.81(m,1h),7.78–7.69(m,4h),3.73(s,3h);
产品的核磁共振碳谱数据:
13cnmr(101mhz,cdcl3)δ150.22(s),134.41(s),131.4,129.8,126.7,123.3,121.6(q,j=319.0hz),119.4(q,j=321.0hz),119.6,37.8;
产品的19fnmr数据:
19fnmr(376mhz,cd3cn)δ-73.72,-79.23;
产品的红外数据:
ir(neat)ν(cm-1):3160.8,3125.4,1610.2,1487.2,1451.8,1263.6,1220.7,1120.1,1151.7,1075.3,1030.6,937.4,769.7,685.8;
产品的高分辨质谱数据:
hrms(esi):caledforc11h10f3n2o2s+[m]+291.0410;found291.0407.
试验例1
实施例1所得磺酰胺咪唑盐化合物c1在光催化条件下产生自由基并催化其他反应的应用为:
其中,化合物d转化为化合物d-1的产率为:82%
试验例2
实施例2所得磺酰胺咪唑盐化合物c2在光催化条件下产生自由基并催化其他反应的应用为:
其中,化合物d转化为化合物d-1的产率为:31%
试验例3
实施例3所得磺酰胺咪唑盐化合物c3在光催化条件下产生自由基并催化其他反应的应用为:
其中,化合物d转化为化合物d-1的产率为:37%
试验例4
实施例4所得磺酰胺咪唑盐化合物c4在光催化条件下产生自由基并催化其他反应的应用为:
其中,化合物d转化为化合物d-1的产率为:52%
化合物d-1的核磁共振氢谱数据:
1hnmr(400mhz,cdcl3)δ7.99–7.95(m,2h),7.43–7.39(m,2h),4.31(t,j=6.4hz,2h),2.38–2.25(m,1h),2.19–2.04(m,1h),1.84–1.73(m,2h),1.70–1.55(m,2h),1.40–1.31(m,1h),1.24(s,12h).
化合物d-1的核磁共振碳谱数据:
13cnmr(101mhz,cdcl3)δ165.7,139.3,131.0,128.8,128.7,127.3(q,j=277.0hz),83.7,65.1,35.0(q,j=28.0hz),27.8,27.2,24.8,24.7.thesignaloftheα-b-carbonwasnotobserved.
化合物d-1的19fnmr数据:
19fnmr(377mhz,cdcl3)δ-64.90(t,j=11.2hz).
化合物d-1的11bnmr数据:
11bnmr(128mhz,cdcl3)δ33.92.
化合物d-1的红外数据:
ir(neat)ν(cm-1):2980.0,2935.3,1720.2,1595.3,1373.5,1269.2,1136.8,1090.2,1015.7,851.7,758.5,685.8;
化合物d-1的高分辨质谱数据:
hrms(esi):caledforc19h25bclf3o4na+[m+na]+443.1379;found443.1378.
试验例5
试验例4所得三氟甲基硼酸酯化合物d-1在金属催化条件下将硼酸酯转化为其他反应的应用为:
其中,化合物d-1转化为化合物e-1的产率为:76%
化合物e-1的核磁共振氢谱数据:
1hnmr(400mhz,cdcl3)δ7.98–7.95(m,2h),7.44–7.40(m,2h),4.98–4.79(m,1h),4.41–4.32(m,2h),2.64–2.26(m,2h),2.05–1.73(m,4h).
化合物e-1的核磁共振碳谱数据:
13cnmr(101mhz,cdcl3)δ165.7,139.5,130.9,128.8,128.5,125.3(qd,j=276.8,3.9hz),87.2(dq,j=172.9,3.2hz),64.4,39.4(qd,j=28.6,23.0hz),31.7(d,j=21.1hz),24.2(d,j=3.9hz).
化合物e-1的19fnmr数据:
19fnmr(377mhz,cdcl3)δ-64.06–-64.14(m),-182.59–-182.97(m).
化合物e-1的红外数据:
ir(neat)ν(cm-1):2957.6,1718.3,1595.3,1489.1,1403.3,1269.2,1090.2,1015.7,849.8,758.5,685.8,592.6,523.7.
化合物e-1的高分辨质谱数据:
hrms(esi):caledforc13h13clf4o2na+[m+na]+335.0432;found335.0429。
与现有技术相比,本发明涵盖的磺酰胺咪唑盐化合物不仅具有化学性质稳定、成本低、易提纯、产率高等优点以外,且由于有机离子盐结构的引入,能够适应各种自由基反应;通过修饰咪唑结构,能够选择性生成各种碳自由基,且产生的自由基具有很好的反应活性和底物适用性,对自由基受体例如烯烃、炔烃、芳香族化合物都有非常多样化的合成反应。另外,本发明的磺酰胺咪唑盐化合物可以更好的催化硼化反应,如通过催化生成单频哪醇硼(bpin)中间体,可用于多种目标化合物的合成。
需要说明的是,在本文中,诸如第一和第二等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括一个……”限定的要素,并不排除在包括所述要素的过程、方法、物品或者设备中还存在另外的相同要素。
以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
- 还没有人留言评论。精彩留言会获得点赞!