一种酶法选择性催化制备4-衣康酸单辛酯的方法与流程
本发明属于生物化工和酶催化领域。具体涉及一种酶法选择性催化制备4-衣康酸单辛酯的方法。
技术背景
衣康酸是含有一个c=c不饱和双键的二元羧酸,在化工、高分子材料、医药领域有重要应用。近年来,衣康酸作为小分子抗炎药物,在治疗慢性炎症,降低寨卡病毒感染,调控体内代谢通路方面备受瞩目(hooftman&o’neill.trendsinimmunology.2019,40(8),687-698)。衣康酸可以通过迈克尔加成反应与代谢通路关键酶的半胱氨酸残基实现烷基化结合,进而发挥调控作用,例如与keap1蛋白151位半胱氨酸残基的烷基化反应激活nrf2通路,发挥抗炎作用(mills,e.l.,ryan,d.g.,prag,h.a.,dikovskaya,d.,menon,d.,zaslona,z.,...&szpyt,j.(2018).itaconateisananti-inflammatorymetabolitethatactivatesnrf2viaalkylationofkeap1.nature,556(7699),113.)。如何实现衣康酸的高效细胞内运输是发挥衣康酸及其衍生物免疫调控功能的关键。衣康酸作为一种小分子二元羧酸,其亲水性较强,难以跨过细胞的磷脂双分子层。2018年,mills等人在nature上发表了关于4-衣康酸单辛酯(酯化位点远离c=c双键)通过激活keap1-nrf2通路调控免疫功能,发挥抗炎功效的报道(mills,&szpyt,(2018).nature,556(7699),113.)。4-衣康酸单辛酯(4-octylitaconate)是衣康酸的正辛醇酯化衍生物,其疏水性远大于衣康酸,可以有效地实现细胞内递送。
目前,关于4-衣康酸单辛酯的合成报道只有通过衣康酸酸酐的正辛醇开环反应以及衣康酸在酸催化条件下与正辛醇的酯化反应。mills等人报道了衣康酸酸酐与正辛醇在室温下的加成反应,然而产率只有33%(mills,&szpyt,(2018).nature,556(7699),113.)。gargallo等人报道衣康酸与正辛醇在酸性条件下直接酯化制备4-衣康酸单辛酯的反应过程,但通过该方法制备的4-单酯产率仅为35%,且产物中二酯副产物含量较高(gargallo,l.,aguirre,c.,leiva,a.,
需要注意的是,mills等人特别强调单酯的位置选择性,4-衣康酸单酯衍生物(酯化位点远离c=c双键)是最有效地激活keap1-nrf2-are通路的衣康酸衍生物(mills,&szpyt,(2018).nature,556(7699),113.)。are(抗氧化反应元件)的激活,可以调节抗氧化蛋白和ii相解毒酶的表达,调控抗氧化酶基因的转录活性,保护肝脏免受中间活性物质的引起的氧化损伤。are的激活,可以启动下游多种保护性基因的表达,包括抗氧化蛋白类基因、ii相解毒酶基因、分子伴侣类基因和抗炎因子类基因邓。可以起到增强组织抗氧化能力、保护组织免受毒物损伤、抗肿瘤、抗炎症等功效。
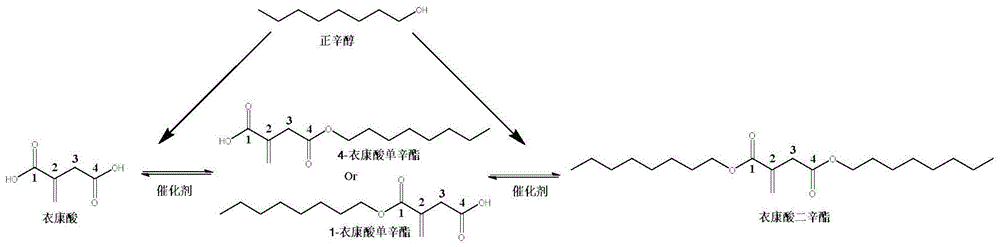
综上,衣康酸单酯的合成或采用高成本的衣康酸酸酐为底物,或副产物较多,单酯转化率不高,后续分离成本较高。以衣康酸和正辛醇为底物的4-衣康酸单辛酯制备工艺的主要难点在于两点:一,在衣康酸生成单酯与二酯的级联反应中(参见图1),需要较高的单酯转化率,并减少副产物二酯的生成,降低后续分离压力;二,在生成的单酯中,需要较高的位置转移性,即生成4-衣康酸单酯(参见图1),而不是副产物1-衣康酸单酯。目前,作为具有重要医疗和材料应用前景的衣康酸单酯化衍生物的高选择性合成途径亟需开发。
技术实现要素:
:
本发明的目的在于提供一种酶法选择性催化制备4-衣康酸单辛酯的方法,首次使用脂肪酶作为催化剂,以衣康酸和正辛醇或其衍生物为底物,在溶剂体系和无溶剂体系下,选择性合成4-衣康酸单辛酯,4-衣康酸单辛酯的产率较高(无溶剂体系93%,溶剂体系98%),生成的单辛酯选择性为100%(4-衣康酸单辛酯),酶催化剂与反应液容易分离,反应过程绿色环保。
本发明的目的是提供一种酶法选择性催化制备4-衣康酸单辛酯的方法,步骤如下:以衣康酸和正辛醇或正辛醇衍生酯为原料,以脂肪酶催化酯化反应;所述衣康酸和正辛醇或正辛醇衍生酯的摩尔比为1:(2-60);待酯化反应结束后,经过萃取、旋蒸、热分离,得到4-衣康酸单辛酯。
优选的,所述衣康酸和正辛醇或正辛醇衍生酯的摩尔比为1:(2-40)。
更优选的,所述衣康酸和正辛醇或正辛醇衍生酯的摩尔比为1:(5-30)。
优选的,所述酯化反应的反应温度为5-95℃,反应时间为4-120小时。
优选的,所述反应温度为20-90℃下,反应时间4-60小时。
更优选的,所述反应温度为30-70℃下,反应时间12-48小时。
优选的,所述脂肪酶来源于动物、植物或微生物中的一种。
更优选的,所述脂肪酶包括但不限于为诺维信435脂肪酶(novozym435),诺维信rmim脂肪酶(lipozymermim),诺维信tlim脂肪酶(lipozymetlim),解酯耶式酵母脂肪酶(candidasp.99-125lipase)或猪胰脂肪酶中的一种。
更优选的,所述脂肪酶为诺维信435脂肪酶。
优选的,所述脂肪酶的用量为所述衣康酸质量的10%-200%。
更优选的,所述脂肪酶的用量为所述衣康酸质量的10%-100%。
更优选的,所述脂肪酶的用量为所述衣康酸质量的30-60%。
更优选的,所述脂肪酶的用量为所述衣康酸质量的50%。
优选的,所述正辛醇衍生酯包括但不限于甲酸辛酯或乙酸辛酯中的一种。
优选的,所述酯化反应过程在溶剂体系或无溶剂体系条件下进行。
本发明的反应体系无论采用溶剂体系还是无溶剂体系,脂肪酶均表现出较高的单酯催化选择性和位置选择性。
优选的,所述酯化反应在溶剂体系下进行。
优选的,所述溶剂的用量为正辛醇或正辛醇衍生酯用量体积的0.2-10倍。
更优选的,所述溶剂的用量为正辛醇或正辛醇衍生酯用量体积的1倍。
优选的,所述溶剂为有机溶剂,所述有机溶剂包括但不限于氯仿、甲苯、正己烷、正庚烷、丙酮、丁酮、苯、环己烷或异辛烷中的一种。
优选的,所述酯化反应过程在常压条件下或减压条件下进行。
所述常压条件为:1.013×105pa;所述减压条件为:800-1200pa。
优选的,所述酯化反应过程中,搅拌转速为50-800rpm。
优选的,所述萃取步骤如下:向所述酯化反应后的产物体系中按照体积比1:(0.2-20)加入水相溶液,混合后,静置6-12h,除去水相,并收集有机相。
更优选的,所述水相溶液为饱和食盐水,即水中通过加入过量食盐,使盐水处于饱和状态。
优选的,所述旋蒸步骤如下:将所述有机相经60-80℃,80-120rpm,8-15分钟旋蒸得到粗产品。
优选的,所述热分离步骤如下:将经过所述萃取、旋蒸步骤制得的粗产品,在真空度0.5pa-100pa,加热温度20℃-100℃条件下进行热分离,得到的白色固体即为4-衣康酸单辛酯。
优选的,所述热分离步骤如下:将经过所述萃取、旋蒸步骤制得的粗产品,在真空度1pa-10pa,加热温度30℃-50℃。
更优选的,所述热分离条件为:真空度1pa,加热温度30℃。该条件下,可以实现4-衣康酸单辛酯与正辛醇或正辛醇衍生酯的较好分离度。
优选的,所述热分离为减压蒸馏、旋转蒸发或短程蒸馏中的一种。分离得到的正辛醇或正辛醇衍生酯,可用于循环使用。
所述酶法选择性催化4-衣康酸单辛酯的制备方法在生物反应器中进行。
优选的,所述反应器包含但不局限于金属浴反应器、摇床反应器、常规搅拌反应器、真空反应体系、填料床反应体系或旋转填料床反应体系中的一种。
优选的,所述脂肪酶用量为30-60%,所述衣康酸与正辛醇或正辛醇衍生酯的摩尔比为1:(5-30)(溶剂体系下,所述溶剂的用量为正辛醇或正辛醇衍生酯体积的1倍体积),所述酯化反应温度为30-70℃,所述搅拌转速为200rpm,所述酯化时间为12-48小时(溶剂体系下,所述酯化时间为24小时)。该工艺具有单酯转化率高、单酯选择性高、专一性强、条件温和、分离简单、催化效率高、反应时间短等优点。
优选的,所述脂肪酶用量为50%,所述衣康酸与正辛醇或正辛醇衍生酯的摩尔比为1:10(溶剂体系下,所述溶剂的用量为正辛醇或正辛醇衍生酯体积的1倍体积),所述酯化反应温度为50℃,所述搅拌转速为200rpm,所述酯化时间为36小时(溶剂体系下,所述酯化时间为24小时)。
优选的,在所述酯化反应中,将反应液布氏漏斗过滤除酶后,倒入分液漏斗中,按1:(0.2-20)的体积加入饱和食盐水,混匀并静止6-12h,分去下层水相以除去衣康酸;收集有机相,旋蒸(70℃,100rpm,10分钟)去除微量水分和溶剂后,用于后续分离过程,分离得到的溶剂可以循环利用。
有益效果:
本发明提供一种酶法选择性催化制备4-衣康酸单辛酯的方法,具有反应条件温和、分离简单、选择性强、催化效率高、反应时间短、循环使用寿命长等优点。
(1)本发明的催化剂利用脂肪酶有限催化活性空间的孔道效应和单羧酸催化特性,有助于提升单酯化过程的选择性;并且衣康酸c1位置的羧基靠近c2位置的c=c双键(参见图2),进入酶口袋的较高位阻。因此,衣康酸4位置的羧基活性要大于1位置的羧基活性,进而实现较高的4-衣康酸单辛酯的制备;
(2)本发明运用反应底物在脂肪酶催化微环境下的微观相分配原理,当衣康酸发生单酯化反应后,形成的衣康酸单酯在疏水作用力的驱使下,会瞬间脱离酶的催化位点到周围疏水环境中,实现了衣康酸单酯的大量累积;
(3)本发明的催化剂为脂肪酶催化剂,具备易分离,反应条件温和,过程绿色环保,批次使用寿命高等优点。
(4)本发明运用热分离手段,通过不同组分饱和蒸汽压的差异,实现过量正辛醇或正辛醇衍生酯与目标产物的分离,工艺操作简单,产品纯度高,易于产业化。
(5)本发明获得了高衣康酸转化率,其转化率高达99%,4-衣康酸单辛酯产率高达98.5%,同时本发明制备的制备方法获得了100%的4-衣康酸单辛酯选择性(见附图4;与核磁结构解析)
附图说明:
图1为在常规催化剂存在下,衣康酸和正辛醇或正辛醇衍生酯的酯化反应过程;
图2为在脂肪酶存在下,衣康酸和正辛醇或正辛醇衍生酯的酯化反应过程;
图3为本发明的实施例1中,溶剂体系条件下反应液中组分含量的气相图谱;
图4为本发明的实施例1中,分离后产物中各组分含量的气相图谱;
图5为本发明的实验例1中,产品与标品的核磁结构鉴定-h谱-600m;
图6为本发明的实验例1中,产品与标品的核磁结构鉴定-c谱-600m;
图7为本发明的实验例1中,产品的二维核磁结构鉴定(hmbc)-600m。
具体实施方式:
一种酶法选择性催化制备4-衣康酸单辛酯的方法,步骤如下:以衣康酸和正辛醇或正辛醇衍生酯类为原料,加入脂肪酶,进行酯化反应;所述衣康酸和正辛醇或正辛醇衍生酯摩尔比为1:(2-60);待酯化反应结束后,经过萃取、旋蒸、热分离,得到4-衣康酸单辛酯,其中,衣康酸和正辛醇或正辛醇衍生酯的酯化反应过程参照附图2。
基于衣康酸与4-衣康酸单辛酯的亲疏水差异(衣康酸更易溶于水,正辛醇或正辛醇衍生酯、4-衣康酸单辛酯、有机溶剂难溶于水),可以通过萃取分离(水-有机相)的方式去除未反应的衣康酸;经萃取分离后,有机相中含有微量水分或溶剂体系反应过程中的有机溶剂(如甲苯等),可以通过旋蒸的方法去除;此时,反应体系中只含有过量正辛醇或正辛醇衍生酯与4-衣康酸单辛酯,可以通过热分离的方法(特定的压力和温度条件下),分离出正辛醇或正辛醇衍生酯。
所述酯化反应温度为5-95℃下,反应时间为4-120小时。
作为本发明的一个实施例,所述衣康酸和正辛醇或正辛醇衍生酯摩尔比为1:2,1:4,1;6,1:8,1:10,1:12,1:14,1:16,1:18,1:20,1:22,1:24,1:26,1:28,1:30,1:32,1:34,1:36,1:38,1:40,1:42,1:44,1:46,1:48,1:50,1:52,1:54,1:56,1:58,1:60。优选条件下,所述衣康酸和正辛醇或正辛醇衍生酯摩尔比为1:(2-40)。更优选条件下,所述衣康酸和正辛醇或正辛醇衍生酯摩尔比为1:(5-30)。
作为本发明的一个实施例,反应温度为5℃、10℃、15℃、20℃、25℃、30℃、35℃、40℃、45℃、50℃、55℃、60℃、65℃、70℃、75℃、80℃、85℃、90℃、95℃,反应时间可以为4h、10h、20h、30h、40h、50h、60h、70h、80h、90h、100h、110h、120h。优选条件下,反应条件为20-90℃下,反应时间4-60小时,更优选条件下,反应条件为30-70℃下,反应时间12-48小时。
在20-90℃下,脂肪酶可以表现出更高的酶活力;该反应是级联反应,反应时间较短会导致衣康酸转化率不高,反应时间过长会导致衣康酸二辛酯的含量增高;底物摩尔比会影响产物的产率,过高的正辛醇或正辛醇衍生酯使用量会增加后续分离的压力。
所述脂肪酶来源于动物、植物或微生物中的一种。
优选条件下,所述脂肪酶包括但不限于为诺维信435(novozym435),诺维信脂肪酶rmim(lipozymermim),诺维信脂肪酶tlim(lipozymetlim)解酯耶式酵母脂肪酶(candidasp.99-125lipase)或猪胰脂肪酶中的一种。
上述四种脂肪酶均为商业化脂肪酶,其中novozym435来源于黑曲霉菌aspergillusniger,固定化载体为疏水性大孔树脂,采购自诺维信公司;lipozymermim来源于米曲霉aspergillusoryzae,固定化载体为酚醛树脂,采购自诺维信公司;lipozymetlim来源于绵毛嗜热丝孢菌thermomyceslanuginosa,固定化载体为二氧化硅,采购自诺维信公司;candidasp.99-125脂肪酶来源于解酯耶式酵母,粉末颗粒,采购自北京凯泰公司;猪胰脂肪酶(casno.9001-62-1),粉末颗粒,采购自tci公司。
更优选条件下,所述脂肪酶为诺维信435脂肪酶。在最优选条件下,衣康酸的转化率大于98%(气相色谱表征),4-衣康酸单辛酯的选择性为100%。
作为本发明的一个实施例,所述脂肪酶的用量为所述衣康酸质量的10%、20%、30%、40%、50%、60%、70%、80%、90%、100%、110%、120%、130%、140%、150%、160%、170%、180%、190%、200%。较高的脂肪酶用量会缩短反应时间,但会增加成本;过低脂肪酶用量不能达到较好的4-衣康酸单辛酯转化率。
优选条件下,所述脂肪酶的用量为所述衣康酸质量的10%-100%。较高的脂肪酶用量会有可能导致副产物衣康酸二辛酯的生成,脂肪酶在优选条件下,具有更为显著的4-衣康酸单辛酯转化率。更优选的,所述脂肪酶的用量为所述衣康酸质量的30-60%。
所述正辛醇衍生酯包括但不限于甲酸辛酯或乙酸辛酯中的一种。
所述酯化反应过程在溶剂体系或无溶剂体系条件下进行。
本发明的反应体系无论采用溶剂体系还是无溶剂体系,脂肪酶均表现出较高的单酯催化选择性和位置选择性。
优选条件下,所述酯化反应在溶剂体系下进行。脂肪酶催化的酯化反应依赖于其位于有限活性中心口袋的催化三联体结构,当衣康酸被催化与正辛醇或正辛醇衍生酯发生酯化反应之后,生成的4-衣康酸单辛酯的疏水性增加。溶剂体系条件下,更有利于生成的4-衣康酸单辛酯脱出催化活性中心,通过酶周围的微观相分配,实现4-衣康酸单辛酯在溶剂内的累积。
作为本发明的一个实施例,所述溶剂的用量为正辛醇或正辛醇衍生酯用量体积的0.2、1、2、3、4、5、6、7、8、9、10倍。
所述溶剂包括但不限于为氯仿、甲苯、正己烷、正庚烷、丙酮、丁酮、苯、环己烷或异辛烷中的一种。
所述酯化反应过程在常压条件下或减压条件下。
所述常压条件为:1.013×105pa;所述减压条件为:1000pa
优选条件下,所述酯化反应过程中,搅拌转速为50-800rpm。
所述萃取、旋蒸、热分离过程中,在所述酯化反应后,少量未反应的衣康酸(小于1%)可以通过双相体系(水相—有机相)萃取分离去除衣康酸;收集有机相,通过旋蒸去除微量水分和甲苯等有机溶剂后,用于后续分离过程,分离得到的溶剂可以循环利用。
优选条件下,所述萃取步骤如下:
向所述酯化反应后的产物体系中按照体积比1:(0.2-20)加入水相溶液,混合后,静置6-12h,除去水相,并收集有机相。
更优选条件下,所述水相溶液为饱和食盐水。
作为本发明的一个实施例,向所述酯化反应后的产物体系中按照体积比1:1加入饱和食盐水,混匀并静止12h,分去下层水相以除去衣康酸;收集有机相。所述萃取少量未反应衣康酸的水相包含但不局限于去离子水,饱和食盐水,以及含有各种离子浓度的水相。所述萃取少量未反应衣康酸的有机相包括4-衣康酸单辛酯、过量辛醇,和/或有机溶剂。
所述旋蒸步骤如下:将所述有机相经60-80℃,80-120rpm,8-15分钟旋蒸得到粗产品。即在无溶剂反应体系脱除水,在溶剂反应体系脱除水和溶剂。有机相中含有微量水分或溶剂体系反应过程中的有机溶剂(如甲苯等),可以通过旋蒸的方法去除。
所述热分离步骤如下:将经过所述萃取、旋蒸步骤制得的粗产品,在真空度0.51pa-100pa,加热温度20℃-100℃条件下进行热分离,得到的白色固体即为4-衣康酸单辛酯。
溶剂经过旋蒸后,反应体系中只含有过量正辛醇或正辛醇衍生酯与4-衣康酸单辛酯,正辛醇或正辛醇衍生酯类的常压沸点大于190℃,常规的旋蒸条件下,难以去除正辛醇或正辛醇衍生酯类,且4-衣康酸单辛酯与正辛醇的极性较近,难以通过硅胶柱层析的方法分离;而这两种物质的沸点差异较明显,在一定压力、温度条件下,可以通过热分离的方法(特定的压力和温度条件下),实现4-衣康酸单辛酯和正辛醇的分离。
优选条件下,所述热分离步骤如下:将经过所述萃取、旋蒸步骤制得的粗产品,在真空度1pa-10pa,加热温度30℃-50℃。
更优选条件下,所述热分离条件为:真空度1pa,加热温度30℃。该条件下,可以实现4-衣康酸单辛酯与正辛醇或正辛醇衍生酯的较好分离度。
所述热分离为减压蒸馏、旋转蒸发或短程蒸馏中的一种。分离得到的正辛醇或正辛醇衍生酯,可用于循环使用。所述方法在生物反应器中进行。
所述反应器包含但不局限于金属浴反应器、摇床反应器、常规搅拌反应器、真空反应体系、填料床反应体系、旋转填料床反应体系等。
优选的,所述脂肪酶用量为30-60%,所述衣康酸与正辛醇或正辛醇衍生酯的摩尔比为1:(5-30)(溶剂体系下,所述溶剂的用量为正辛醇或正辛醇衍生酯体积的1倍体积),所述酯化反应温度为30-70℃,所述搅拌转速为200rpm,所述酯化时间为12-48小时(溶剂体系下,所述酯化时间为24小时)。该工艺具有单酯转化率高、单酯选择性高、专一性强、条件温和、分离简单、催化效率高、反应时间短等优点。
优选的,所述脂肪酶用量为50%,所述衣康酸与正辛醇或正辛醇衍生酯的摩尔比为1:10(溶剂体系下,所述溶剂的用量为正辛醇或正辛醇衍生酯体积的1倍体积),所述酯化反应温度为50℃,所述搅拌转速为200rpm,所述酯化时间为36小时(溶剂体系下,所述酯化时间为24小时)。
本发明将脂肪酶首次应用于衣康酸的辛酯化反应,无溶剂体系下,4-衣康酸单辛酯的产量可达到93%(溶剂体系下可达到98%),单辛酯的选择性达到100%(溶剂体系下同样达到100%)。
在所述酯化反应中,将反应液布氏漏斗过滤除酶后,倒入分液漏斗中,加入饱和食盐水,混匀并静止12h,分去下层水相以除去衣康酸;收集有机相,旋蒸(70℃,100rpm,10分钟)去除微量水分和溶剂后,用于后续分离过程,分离得到的溶剂可以循环利用。
下面将结合具体实施例对本发明做进一步说明。应理解,下述实施例是为了更好的说明本发明,而非限制本说明。
实施例1:溶剂体系下,常压制备4-衣康酸单辛酯。
步骤1.在常压条件下(1.013×105pa),以1g衣康酸(7.69mmol)和10g(76.9mmol)正辛醇为原料,加入0.5g的novozym435脂肪酶(10000u/g),加入溶剂甲苯12ml(甲苯:正辛醇=1:1体积比),于50℃,200rpm摇床反应器中进行酯化反应24h;气相色谱测定衣康酸的转化率99%,4-衣康酸单辛酯的产率为98%(参见附图3);
步骤2.酯化反应结束后,通过溶剂过滤器(0.45μm尼龙过滤膜)过滤除去脂肪酶,将反应液倒入分液漏斗并按照反应液与饱和食盐水体积比1:1加入饱和食盐水(浓度约为35%),充分混合振荡,静置6h,除去下层水相,并收集有机相。将有机相进行旋蒸(70℃,100rpm,10分钟)上清有机相除去少量水分和甲苯,得到粗产品;
步骤3.将步骤2中制得的粗产品,经过短程蒸馏的热分离方法,并设置短程蒸馏的条件为:外加热壁30℃,内冷凝2℃,刮板转速150rpm,进料速度1ml/min,真空度1pa,除去过量正辛醇后得到的白色固体即为4-衣康酸单辛酯(0.89g),总收率89%,产品中4-衣康酸单辛酯的纯度95%(参见图4)。
步骤4.脂肪酶使用10批次,酶活保持在初始酶活的80%以上。
实施例2:溶剂体系下,减压制备4-衣康酸单辛酯。
步骤1.在减压条件下(1000pa),在三口烧瓶中,投入1g衣康酸(7.69mmol)和10g(76.9mmol)正辛醇为原料,加入0.5gnovozym435脂肪酶(10000u/g),加入溶剂甲苯12ml(甲苯:正辛醇=1:1体积比),控制水浴锅40℃,200rpm摇床反应器中进行酯化反应,接入玻璃分水器,进行酯化反应12h;气相色谱测定衣康酸的转化率99%,4-衣康酸单辛酯的产率为97%;
步骤2.酯化反应结束后,通过溶剂过滤器(0.45μm尼龙过滤膜)过滤除去脂肪酶,将反应液倒入分液漏斗并按照反应液与饱和食盐水体积比1:1加入饱和食盐水,充分混合振荡,静置6h,除去下层水相,并收集有机相。将有机相进行旋蒸(70℃,100rpm,10分钟)上清有机相除去少量水分和甲苯,得到粗产品;
步骤3.将步骤2中制得的粗产品,经过短程蒸馏的热分离方法,并设置短程蒸馏的条件为:外加热壁30℃,内冷凝2℃,刮板转速150rpm,进料速度1ml/min,真空度1pa,除去过量正辛醇后得到的白色固体即为4-衣康酸单辛酯(0.90g),总收率90%,产品中4-衣康酸单辛酯的纯度94%。
正辛醇与衣康酸在酯化反应过程中,不断生成水,相较于常压反应条件,在减压条件下(1000pa),水分不断被移除推动反应向正向(即酯化方向)进行,从而显著缩短反应时间,由常压条件的24h缩短为减压条件的12h。
实施例3:溶剂体系下,填充床反应器连续制备4-衣康酸单辛酯。
步骤1.在常压条件下(1.013×105pa),以5g衣康酸(7.69mmol)和50g(76.9mmol)正辛醇为原料,加入溶剂甲苯60ml(甲苯:正辛醇=1:1体积比)混合均匀,作为反应底物;
步骤2.在长20cm,内径1cm,外径2cm的钢制夹套填充床反应器中,填入2.5gnovozym435脂肪酶(10000u/g),两端填入玻璃珠,通过柱塞泵将反应底物由下至上泵入填充床反应器中,流速0.4ml/min,夹套温度由循环水浴控制30℃。停留时间10min时;气相色谱测定衣康酸的转化率51%,4-衣康酸单辛酯的产量50%;循环进料4次时,衣康酸的转化率95%,4-衣康酸单辛酯的产率为94%。所有反应液,四次循环通过填充床反应器的总反应时间为19.17h.
步骤3.酯化反应结束后(不需过滤除酶),将反应液倒入分液漏斗并按照反应液与饱和食盐水体积比1:1加入饱和食盐水,充分混合振荡,静置6h,除去下层水相,并收集有机相。将有机相进行旋蒸(70℃,100rpm,10分钟)上清有机相除去少量水分和甲苯,得到粗产品;由于水不溶于甲苯,因此直接取上清甲苯回收,得到58ml甲苯。
步骤4.将步骤3中制得的粗产品,经过旋蒸蒸发的热分离方法,并设置旋蒸蒸发的条件为:加热温度120℃,冷凝温度-5℃,转速110rpm,真空度1pa,除去过量正辛醇后得到的白色固体即为4-衣康酸单辛酯(4.4g),总收率88%,产品中4-衣康酸单辛酯的纯度91%。
由于使用填充床反应器中,底物物料与酶催化剂的混合效果略低于直接混合的效果,导致转化率略有降低。并且旋蒸作为热分离的手段,分离效率不如短程蒸馏,造成纯度较低。
实施例4:溶剂体系下,金属浴反应器制备4-衣康酸单辛酯。
步骤1.在常压条件下(1.013×105pa),在4ml棕色小瓶中,加入0.1g衣康酸(0.769mmol)和1g(7.69mmol)正辛醇为原料,加入0.05gnovozym435脂肪酶(10000u/g),加入溶剂甲苯1.2ml(甲苯:正辛醇=1:1体积比),于50℃,800rpm金属浴反应器中进行酯化反应20h;气相色谱测定衣康酸的转化率98%,4-衣康酸单辛酯的产率为97%;
步骤2.酯化反应结束后,通过溶剂过滤器(0.45μm尼龙过滤膜)过滤除去脂肪酶,将反应液倒入分液漏斗并按照反应液与饱和食盐水体积比1:1加入饱和食盐水,充分混合振荡,静止6h,除去下层水相,并收集有机相。将有机相进行旋蒸(70℃,100rpm,10分钟)上清有机相除去少量水分和甲苯,得到粗产品;
步骤3.将步骤2中制得的粗产品,经过减压蒸馏的热分离方法,并设置减压蒸馏的条件为:加热150℃,循环水冷凝18℃,沸石2粒,真空度3×10-2mbar,30分钟,除去过量正辛醇后得到的白色固体即为4-衣康酸单辛酯(0.08g),总收率80%,产品中4-衣康酸单辛酯的纯度94%。
在减压过程中,部分产物,随着正辛醇蒸到了冷凝管里;造成了产物的收率略有降低。
实施例5:无溶剂体系下,常压制备4-衣康酸单辛酯。
步骤1.在常压条件下(1.013×105pa),以1g衣康酸(7.69mmol)和20g(153.8mmol)正辛醇为原料,加入0.5gnovozym435脂肪酶(10000u/g),在无溶剂体系条件下,于50℃,200rpm摇床反应器中进行酯化反应36h,气相色谱测定衣康酸的转化率98%,4-衣康酸单辛酯的产率为93%。
在溶剂体系,更有利于单辛酯的瞬间脱除酶分子的催化位点;进而实现单辛酯的累积在无溶剂体系中,而在无溶剂体系,其累积量略低。
步骤2.酯化反应结束后,通过溶剂过滤器(0.45μm尼龙过滤膜)过滤除去脂肪酶,将反应液倒入分液漏斗并按照反应液与饱和食盐水体积比1:1加入饱和食盐水,充分混合振荡,静置6h,除去下层水相,并收集有机相。将有机相进行旋蒸(70℃,100rpm,10分钟)上清有机相除去少量水分,得到粗产品;
步骤3.将步骤2中制得的粗产品,经过短程蒸馏的热分离方法,并设置短程蒸馏的条件为:外加热壁30℃,内冷凝2℃,刮板转速150rpm,进料速度1ml/min,真空度1pa,除去过量正辛醇后得到的白色固体即为4-衣康酸单辛酯(0.8g),总收率84%,产品中4-衣康酸单辛酯的纯度90%。
本发明实施例中,未反应完的衣康酸较多,需要重复步骤2,去除多余的衣康酸;这个过程中,可能会因为有机相与水相的乳化现象,造成收率的降低。
实施例6:无溶剂体系下,减压制备4-衣康酸单辛酯。
步骤1.在减压条件下(1000pa),在三口烧瓶中,投入1g衣康酸(7.69mmol)和20g(153.8mmol)正辛醇为原料,加入0.5gnovozym435脂肪酶(10000u/g),在无溶剂体系条件下,控制水浴锅40℃,采用真空反应体系即油泵抽真空的方式控制反应体系的真空度为1000pa。搅拌电机200rpm,进行酯化反应20h,气相色谱测定衣康酸的转化率99%,4-衣康酸单辛酯的产率为90%;
步骤2.酯化反应结束后,通过溶剂过滤器(0.45μm尼龙过滤膜)过滤除去脂肪酶,将反应液倒入分液漏斗并按照反应液与饱和食盐水体积比1:1加入饱和食盐水,充分混合振荡,静置6h,除去下层水相,并收集有机相。将有机相进行旋蒸(70℃,100rpm,10分钟)上清有机相除去少量水分,得到粗产品;
步骤3.将步骤2中制得的粗产品,经过短程蒸馏的热分离方法,并设置短程蒸馏的条件为:外加热壁30℃,内冷凝2℃,刮板转速150rpm,进料速度1ml/min,真空度1pa,除去过量正辛醇后得到的白色固体即为4-衣康酸单辛酯(0.83g),总收率83%,产品中4-衣康酸单辛酯的纯度88%。
待分离底物纯度的降低造成了产物纯度略有降低以及略难分离。
实施例7:无溶剂体系下,以甲酸辛酯为底物,常压制备4-衣康酸单辛酯。
步骤1.在常压条件下(1.013×105pa),以1g衣康酸(7.69mmol)和24g(151.7mmol)甲酸辛酯为原料,加入0.5gnovozym435脂肪酶(10000u/g),在无溶剂体系条件下,于50℃,200rpm摇床反应器中进行酯化反应30h,气相色谱测定衣康酸的转化率96%,4-衣康酸单辛酯的产率为94%;
步骤2.酯化反应结束后,通过溶剂过滤器(0.45μm尼龙过滤膜)过滤除去脂肪酶,将反应液倒入分液漏斗并按照反应液与饱和食盐水体积比1:1.5加入饱和食盐水,充分混合振荡,静置6h,除去下层水相,并收集有机相。将有机相进行旋蒸(70℃,100rpm,10分钟)上清有机相除去少量水分和甲苯,得到粗产品;
步骤3.将步骤2中制得的粗产品,经过短程蒸馏的热分离方法,并设置短程蒸馏的条件为:外加热壁30℃,内冷凝2℃,刮板转速150rpm,进料速度1ml/min,真空度1pa,除去过量甲酸辛酯后得到的白色固体即为4-衣康酸单辛酯(0.85g),总收率85%,产品中4-衣康酸单辛酯的纯度92%。
与实施例5相比,正辛醇衍生物,即甲酸辛酯与正辛醇同样作为反应底物,对目标产物的转化率、纯度等影响不大;正辛醇衍生物即甲酸辛酯作为反应底物,目标产物——4-衣康酸单辛酯的产率略高,可是是由于其对脂肪酶的酶活抑制效果更小,而正辛醇含有的羟基(-oh)可能会影响脂肪酶的部分酶活力。
实验例1:产物的核磁结构表征
为了表征利用本发明制备方法制备获得产品的结构性质,因此将本发明制备的产品与4-衣康酸单辛酯标准品的核磁结构进行对照验证。
实验步骤如下:
步骤1.取30mg实施例1中制备得到的高纯度产品(纯度≥95%),溶于适量氘代氯仿中,装入核磁管中,混合均匀;根据相同步骤,使用4-衣康酸单辛酯标品(商业化标准品,ark,ak00807135,98%纯度,30mg)制备作为参照的核磁样品;
步骤2.在bruker600m磁共振分析仪中分别测定产品与样品的h谱、c谱,与产物的二维核磁谱图(hmbc);(参见图5、图6、图7)
步骤3.本发明的产品与标品的h谱、c谱完全对应,据文献报道(richard,j.v.,delaite,c.,riess,g.,&schuller,a.s.(2016).acomparativestudyofthethermalpropertiesofhomologousseriesofcrystallisablen-alkylmaleateanditaconatemonoesters.thermochimicaacta,623,136-143),4-衣康酸单辛酯与1-衣康酸单辛酯c=c的末端氢会有明显偏移;并且本专利的产品的h谱数据与richard等人报道的4-衣康酸单辛酯的h谱数据相一致;二维核磁谱图(hmbc)进一步表明,本发明的产物中不含有1-衣康酸单辛酯,所有的衣康酸单辛酯都是4-衣康酸单辛酯。
实验例2:无溶剂体系下,常压条件下,不同脂肪酶对4-衣康酸单辛酯产量的影响。
为了说明不同脂肪酶以及常规催化剂对于4-衣康酸单辛酯的转化率的影响,因此将实验分为六组,其中:
实验组1:为0.5g诺维信435脂肪酶(采购自诺维信公司);
实验组2:0.5g诺维信rmim脂肪酶(采购自诺维信公司);
实验组3:0.5g诺维信tlim脂肪酶(采购自诺维信公司);
实验组4:0.5g解酯耶式酵母脂肪酶(candidasp.99-125lipase);
实验组5:0.5g猪胰脂肪酶(casno.9001-62-1,采购自tci公司);
对照组:50μl的浓硫酸作为催化剂。
实验方法:
步骤1.将实验分为六组,在常压条件下(1.013×105pa),分别制备1g衣康酸(7.69mmol)和20g(153.8mmol)正辛醇为原料,分别加入0.5g诺维信435脂肪酶,0.5g诺维信rmim脂肪酶,0.5g诺维信tlim脂肪酶,0.5g解酯耶式酵母脂肪酶(candidasp.99-125lipase),0.5g猪胰脂肪酶,以及50μl的浓硫酸作为催化剂。在无溶剂体系条件下,于50℃,200rpm摇床反应器中进行酯化反应36h。
步骤2分别从每组中取20μl经过酯化反应的产品,加入1.8ml甲醇,高速离心(8000rpm,3min)去除游离的酶蛋白;分别取上清液1.6ml,装入进样瓶中,通过气相色谱测定4-衣康酸单辛酯的产量。
步骤3.实验结果发现:浓硫酸作为催化剂,绝大部分衣康酸被转化为衣康酸二辛酯(约70%),仅产生少量的4-衣康酸单辛酯(约30%)。脂肪酶作为催化剂,具有催化剂容易分离,反应条件温和等优点;且生成的都是4-衣康酸单辛酯,但是4-衣康酸单辛酯的产率不同。诺维信435脂肪酶,诺维信rmim脂肪酶,诺维信tlim脂肪酶,candidasp.99-125lipase脂肪酶和猪胰脂肪酶作为催化剂,其4-衣康酸单辛酯的产率分别为93%,60%,58%,62%,和50%。可以看出,利用本发明的脂肪酶制备得到的4-衣康酸单辛酯的转化率均较高,其中novozym435脂肪酶的转化率较为显著,是由于其单位酶活力较高,并且其活性中心的口袋较浅,方便衣康酸进入,发生酯化反应;其它脂肪酶的4-衣康酸单辛酯产率相比而言稍有降低,是由于其活性中心的口袋较深,衣康酸进入的难度稍有增加。
- 还没有人留言评论。精彩留言会获得点赞!