检测新型冠状病毒S基因的引物和探针及其试剂盒和方法与流程
本发明涉及生物技术应用领域,具体是涉及一种检测新型冠状病毒s基因的引物和探针及其试剂盒和方法。
背景技术:
新型冠状病毒在临床实践过程中,一些弱症状、病毒载量低的初诊患者样本、样本中抑制物高的患者样本、治疗后待复核出院的患者样本等,不能被明确诊断,造成了极大的传染隐患、安全风险以及资源消耗。
因此,在使用已知的一步法实时荧光rt-pcr技术检测和定量分析样品中某特定靶核酸的实践中,为了减少和避免检测结果的假阴性或假阳性,提高定量分析的准确性,如何基于已知的靶多核苷酸序列设计、筛选及制备适当的引物和寡核苷酸探针成为了一个关键性的基本技术环节。
技术实现要素:
为解决上述技术问题,本发明提供了一种检测新型冠状病毒s基因的引物和探针及其试剂盒和方法。
本发明的技术方案是:一种检测新型冠状病毒s基因的引物和探针,包括2019-ncov新型冠状病毒s基因、内参基因rpp30的特异性引物及探针,其序列分别为:
1)2019-ncov新型冠状病毒s基因:正向引物:seqidno:1,反向引物:seqidno:2,探针:seqidno:3;
2)内参基因rpp30:正向引物:seqidno:4,反向引物:seqidno:5,探针:seqidno:6。
进一步地,如seqidno:3和seqidno:6所示的探针的5’端标记有荧光基团fam,3’端标记有淬灭基团tamra或bhq-1,同时为了降低反应体系的干扰,合成的引物和探针进行hplc纯化。
本发明还公开了一种检测新型冠状病毒s基因的试剂盒,其含有上述的引物和探针。
进一步地,所述试剂盒内的反应体系主要含有:rt-pcr反应液、酶混合液、solution(10×),且反应体系ph控制在6.5~8.5。
更进一步地,所述试剂盒内的反应体系具体成分为:
其中,上述正向引物、反向引物及探针的含量为所对应的2019-ncov新型冠状病毒s基因、内参基因rpp30的引物及探针各半。
更进一步地,所述pt-pcr反应液、酶混合液、solution(10×)分别为:
1)pt-pcr反应液含有tris-hci20-40mm、kci100-200mm、mgso43-6mm;
2)酶混合液含有耐热taqdna聚合酶、mmlv逆转录酶、核糖核酸酶抑制剂和dntp,其中高耐受性taqdna聚合酶的用量为4-6mm、mmlv逆转录酶的用量为2-2.5mm、核糖核酸酶抑制剂的用量为12-20mm,dntp的用量为10mm,混合并通过酶保存液补足至4ul;
3)solution(10×):四甲基氯化铵20-40mm、海藻糖4%体积比、甘油0.05-0.1mm、三氮化钠4.5e-2~9e-2。
本发明还提供了一种使用上述引物和探针或上述试剂盒的用于2019-ncov新型冠状病毒基因检测方法。
进一步地,所述检测方法包括以下步骤:
s1:从检测样本中提取病毒的rna作为模板,使用权利要求1所述引物及探针配置扩增反应体系,进行实时荧光pcr扩增得到扩增曲线;
s2:对所述扩增曲线进行分析,并对检测样本中是否2019-ncov新型冠状病毒做出判断。
进一步地,所述扩增反应体系的反应参数及扩增程序如下:
本发明的试剂盒检测原理为:
采用荧光定量pcr(聚合酶链式反应),因其pcr反应模板仅为dna,因此在进行pcr反应前,将新型冠状病毒核酸(rna)逆转录为dna,通过pcr反应体系中包含的特异性引物以及taqman探针;
探针完整时,报告基团发射的荧光信号被淬灭基团吸收;如pcr反应体系存在靶序列,pcr反应时探针与模板结合,dna聚合酶沿模板利用酶的外切酶活性将探针酶切降解,报告基团与淬灭基团分离发出荧光,每扩增一条dna链就有一个荧光分子产生;
通过赛默飞公司出售的abi7500荧光pcr扩增仪监测出荧光到达预先设定阈值的循环数(ct值)与病毒核酸浓度有关,病毒核酸浓度越高,ct值越小,pcr仪器软件系统自动绘制出实时扩增曲线,实现即时结果判断;从而达到快速、实时、定量检测新型冠状病毒的目的。
本发明的有益效果是:
(1)本发明采用设计s基因的特异性引物及探针进行新型冠状病毒检测,可快速、准确对新冠病毒进行鉴定和检测,从而避免了新冠病毒检测的假阴性和假阳性,且通过采用一步法荧光pcr,并且可有效的防止多重操作污染。
(2)本发明设计的内参基因rpp30其具有表达量大,不受任何内源性或外源性因素的影响,且不存在假基因的优点,避免造成新冠病毒检测的假阴性和假阳性。
(3)本发明的检测方法及试剂盒可用于鼻/咽拭子/全血/血清样本中新冠病毒核酸定性检测,检测灵敏度高,特异性强,且操作简便、检测可靠性高。
附图说明
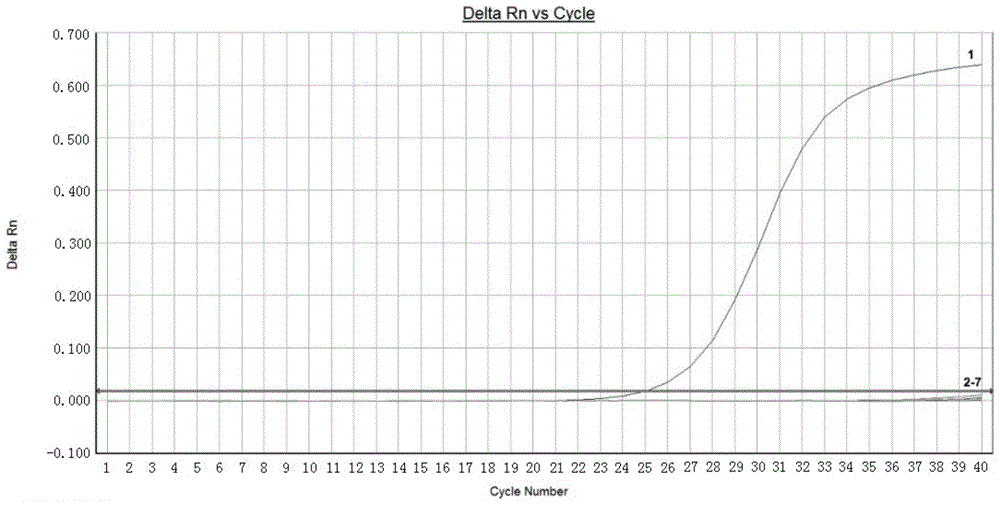
图1是本发明具体实施例的荧光定量pcr特异性实验曲线图,其中,1:2019-ncov新型冠状病毒;2:sars冠状病毒;3:流感病毒a型;4:流感病毒b型;5:流感病毒c型病毒;6:冠状病毒229e;7:偏肺病毒hmp。
图2是本发明具体实施例的荧光定量pcr灵敏度实验曲线图,其中,1:1×100copies/μl;2:1×101copies/μl;3:1×102copies/μl;4:1×103copies/μl;5:1×104copies/μl;6:1×105copies/μl;7:1×106copies/μl;8:1×107copies/μl;9:1×108copies/μl。
图3是本发明具体实施例的荧光定量pcr标准曲线。
具体实施方式
本发明所述一种检测新型冠状病毒s基因的引物和探针及其试剂盒和方法,是基于相应型别s基因段设计的特异性引物和探针。
实施例1(引物及探针的设计)
1)通过使用核酸分析软件对已知的2019-ncov新型冠状病s基因的核苷酸序列进行同源性比较,通过严格的比对分析,在找出同源区段的基础上,以2019-ncov新型冠状病毒s基因为扩增靶位点,使用适当的引物设计软件根据引物及探针设计原则选择高度保守区段设计特异性引物和探针序列,
2)合成所需的探针序列,氨解处理后分别在其5’端标记作为荧光发生基团的fam,并在其3’端标记借助活性连接臂偶联上作为荧光淬灭或抑制基团的tamra或bhq-1;以fplc层析法纯化荧光标记的探针;然后,使用变性条件下的聚丙烯酰胺凝胶(20%)电泳法和分光光度法物理鉴定所合成的引物和探针;
3)将选定的s基因引物和探针序列以及rpp30内参基因的引物和探针,序列由takara宝生物(大连)公司合成,所有引物以及探针序列如表1所示:
表1引物序列和探针序列
实施例2(2019-ncov新型冠状病毒检测试剂盒)
制备2019-ncov新型冠状病毒试剂盒,其反应体系具体成分如下表2所示:
表2试剂盒反应体系具体成分
其中,pt-pcr反应液含有tris-hci35mm、kci170mm、mgso45mm;
酶混合液中高耐受性taqdna聚合酶的用量为5mm、mmlv逆转录酶的用量为2.2mm、核糖核酸酶抑制剂的用量为18mm,dntp的用量为10mm,混合并通过酶保存液补足至4ul;
solution(10×):四甲基氯化铵30mm、海藻糖4%体积比、甘油0.07mm、三氮化钠7.5e-2;
上述s基因正向引物、s基因反向引物、s基因探针、rpp30内参基因正向引物、rpp30内参基因反向引物、rpp30内参基因探针分别如seqidno:1、2、3、4、5、6所示。
实施例3(rt-pcr扩增程序)
构建rt-pcr扩增程序,具体如下表3所示:
表3pcr反应扩增程序
实施例4(2019-ncov新型冠状病毒检测试剂盒的检测方法)
1、对照样品的准备:
1)阳性对照样品:以含有目的扩增区域的假病毒作为2019-ncov新型冠状病毒的阳性对照样品,其具体为人工合成的浓度1×106copies/ml的2019-ncov新型冠状病毒序列重组的假病毒;
2)阴性对照样品:以无菌生理盐水作为阴性对照样品;
3)特异性参考对照样品:以sars冠状病毒、流感病毒a型,流感病毒b型、流感病毒c型病毒、冠状病毒229e、偏肺病毒hmp作为特异性参考对照。
2、样本的采集:临床医师根据实际情况进行对应部位样本采集,可检测的样本包括鼻/咽拭子/全血/血清;采集的样本按照常规要求处理后,密封保存并低温送检。
3、检测方法
1)rna提取及处理:取上述检测样本各100μl,通过常规rna/dna提取方法提取,得到50μl核酸提取产物,使用depc水对核酸提取产物10倍稀释后作为模板;
2)pcr反应:根据实施例2配置2019-ncov新型冠状病毒试剂盒的反应体系,并将阴性对照、特异性参考对照、阳性对照各5μl分别加入,使用赛默飞公司生产的型号为abi7500的pcr仪,按实施例1设计的2019-ncov新型冠状病毒引物和探针,以及根据实施例3构建的扩增程序,进行实时荧光pcr扩增得到扩增曲线;
3)结果分析:分析扩增曲线的实验结果,如扩增曲线有明显指数增长期,则判定为阳性,否则为阴性;结果表明,阳性对照测试结果为阳性,阴性对照和特异性参考对照的检测结果均为阴性;说明由本发明的引物和探针构成的试剂盒具有良好的特异性。
实施例5(特异性实验)
分别以sars冠状病毒、流感病毒a型,流感病毒b型、流感病毒c型病毒、冠状病毒229e、偏肺病毒hmp以及2019-ncov新型冠状病毒的dna作为模板,进行荧光定量pcr反应,检测该方法的特异性。结果所示,仅2019-ncov质粒存在明显的扩增,其他样品均无扩增(图1);通过图1结果可知,该方法特异性较好。
实施例6(灵敏度实验)
制备1×100-1×108copies/μl的2019-ncov新型冠状病毒阳性标准质粒,每个梯度设置3个重复,进行荧光定量pcr反应,进行该产品的敏感性实验。结果显示,该方法可以有效检测出10拷贝的样本,当样本浓度大于10copies/μl时均能出现明显的扩增(图2)。
以ct值为纵坐标,拷贝数为横坐标,建立标准曲线(图3);标准曲线见图3,标准曲线方程为:y=15.683x0.0428;r2=0.9963。
序列表
<110>贵州医科大学
<120>检测新型冠状病毒s基因的引物和探针及其试剂盒和方法
<130>无
<170>patentinversion3.5
<210>1
<211>29
<212>rna
<213>人工序列
<221>misc_feature
<222>(1)-(29)
<223>根据实验要求而设计,作为新型冠状病毒(2019-ncov)s基因的正向引物序列
<400>1
gctagttatcagactcagactaattctcc29
<210>2
<211>25
<212>rna
<213>人工序列
<221>misc_feature
<222>(1)-(25)
<223>根据实验要求而设计,作为新型冠状病毒(2019-ncov)s基因的反向引物序列
<400>2
gacatagtgtaggcaatgatggatt25
<210>3
<211>25
<212>rna
<213>人工序列
<221>misc_feature
<222>(1)-(25)
<223>根据实验要求而设计,作为新型冠状病毒(2019-ncov)s基因的探针序列
<400>3
actagctacactacgtgcccgccga25
<210>4
<211>20
<212>rna
<213>人工序列
<221>misc_feature
<222>(1)-(20)
<223>根据实验要求而设计,作为rpp30内参基因的正向引物序列
<400>4
acgaggtgggacttcagcat20
<210>5
<211>19
<212>rna
<213>人工序列
<221>misc_feature
<222>(1)-(19)
<223>根据实验要求而设计,作为rpp30内参基因的反向引物序列
<400>5
cgcagagccttcaggtcag19
<210>6
<211>24
<212>rna
<213>人工序列
<221>misc_feature
<222>(1)-(24)
<223>根据实验要求而设计,作为rpp30内参基因的探针序列
<400>6
aacccgctcgcaggtccaaatctg24
- 还没有人留言评论。精彩留言会获得点赞!