一种基于噻吩并香豆素的比率型探针及其制备和应用
1.本发明属于荧光分析和生物小分子的检测领域,特别涉及一种基于噻吩并香豆素的比率型探针及其制备和应用。
背景技术:
2.次氯酸盐(hclo/clo-)在许多生理和病理过程中发挥着重要作用。然而,高浓度的次氯酸根离子也会导致癌症、关节炎、神经元变性和帕金森氏病等严重疾病。因此,检测生物系统中次氯酸盐的浓度具有重要意义。
3.相比于“off-on”荧光探针,比率型荧光探针可以有效消除环境因素引起的数据失真,具有准确度更高的优点。因此,设计和合成一种快速、灵敏、高选择性的比率型荧光探针,对于改进现有的荧光检测方法是很有意义的。
技术实现要素:
4.为了克服上述现有技术的缺点与不足,本发明的首要目的在于提供一种基于噻吩并香豆素的比率型荧光探针。
5.本发明另一目的在于提供上述基于噻吩并香豆素的比率型荧光探针的制备方法。
6.本发明再一目的在于提供上述基于噻吩并香豆素的比率型荧光探针的应用。
7.本发明的目的通过下述方案实现:
8.一种基于噻吩并香豆素的比率型荧光探针,其结构如下所示:
[0009][0010]
一种上述的基于噻吩并香豆素的比率型荧光探针的制备方法,其包括以下步骤:
[0011]
(1)将丙二酸二苯酯和3-(n,n-二乙氨基)苯酚在溶剂存在条件下加热回流反应,反应结束后将所得反应液纯化得化合物1;
[0012]
(2)在溶剂存在条件下,将化合物1和pocl3进行反应,反应结束后将所得反应液纯化即得化合物2;
[0013]
(3)在溶剂和碱存在条件下,将化合物2和1,4-二硫-2,5-二醇进行反应,反应结束后将所得反应液纯化即得化合物3;
[0014]
(4)在溶剂中,将二氨基马来腈、对甲苯磺酸以及化合物3进行反应,反应结束后将所得反应液纯化即得基于噻吩并香豆素的比率型探针csn。
[0015]
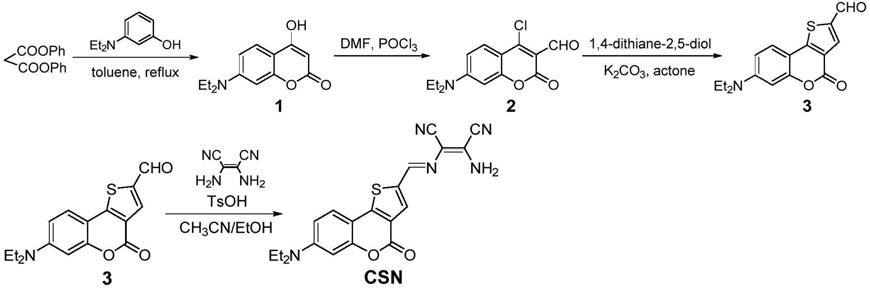
具体反应路线如下所示:
[0016][0017]
步骤(1)中所述的溶剂为甲苯、二甲苯中的至少一种;优选为甲苯;
[0018]
步骤(1)中所述的加热回流反应的时间为6-24h,优选为8h;
[0019]
步骤(1)中所述的丙二酸二苯酯和3-(n,n-二乙氨基)苯酚的摩尔比为1:2-2:1;优选为1:1;
[0020]
步骤(1)中所述的纯化是指将所得反应液过滤,然后用石油醚洗涤,所得灰绿色固体即化合物1;
[0021]
步骤(2)优选为以下步骤:先在氮气气氛下将pocl3加入到溶剂中搅拌形成悬浮液,然后再将化合物1加入到同样的溶剂中形成化合物1的溶液,将化合物1的溶液加入到悬浮液中进行反应,反应结束后将所得反应液纯化即得化合物2;
[0022]
步骤(2)中所述的溶剂为dmf;
[0023]
步骤(2)中所述的反应是指在30-80℃搅拌过夜,优选在60℃搅拌过夜;
[0024]
步骤(2)中所述的化合物1和pocl3的摩尔比为1:1-1:5,优选为1:1.6;
[0025]
步骤(2)中所述的纯化是指将所得反应液冷却至室温后,将反应液倒入冰水中,然后加碱中和并过滤,所得黄色固体即为化合物2;
[0026]
步骤(3)中所述的溶剂为丙酮、二氯甲烷、乙腈中的至少一种;所述的碱为碳酸钾;
[0027]
步骤(3)中所述的化合物2、1,4-二硫-2,5-二醇以及碱的摩尔比为1:0.5-1:1-5,优选为1:0.6:3;
[0028]
步骤(3)中所述的反应是指先在室温下搅拌反应0.5-3h,再升温至35-60℃搅拌反应2-6h;优选为先在室温下搅拌反应1h后再升温至45℃搅拌反应3h,搅拌仅仅为了充分反应,因此可不用限制搅拌速度。
[0029]
步骤(3)中所述的纯化是指将反应结束后的反应液在冰水中冷却静置1h后过滤收集不溶物,然后用乙醇对不溶物进行洗涤,将洗涤后的滤饼溶于二氯甲烷中以除去不溶物,再减压蒸馏除去滤液即得化合物3。
[0030]
步骤(4)中所述的溶剂为乙醇、甲醇、二氯甲烷、四氢呋喃中的至少一种;
[0031]
步骤(4)中所述的二氨基马来腈、对甲苯磺酸以及化合物3得摩尔比为1:0.01:0.02-1:0.1:1,优选为1:0.015:0.1;
[0032]
步骤(4)中所述的反应是指在室温下搅拌反应0.5-2h,优选为在室温下搅拌反应1h;
[0033]
步骤(4)中所述的纯化是指将反应后的溶液旋干,再用无水乙醇重结晶,过滤收集红色固体,然后通过柱层析法纯化,即得到基于噻吩并香豆素的比率型探针csn。
[0034]
本发明所述的基于噻吩并香豆素的比率型探针csn在次氯酸根离子检测时所需的
激发波长范围在350~450nm,而荧光发射光波长范围为420nm-800nm;并且荧光发射光波长在470nm和640nm的荧光光强比值(i470/i640)与次氯酸根离子的浓度呈线性正相关,因此可应用于检测水中次氯酸根离子。
[0035]
本发明基于噻吩并香豆素的比率型探针csn能够在活细胞中通过荧光信号的变化来实现次氯酸根离子含量的检测,因此也可应用于活细胞中次氯酸根离子的检测。
[0036]
本发明相对于现有技术,具有如下的优点及有益技术效果:
[0037]
本发明所述荧光探针csn的制备方法简单,对次氯酸根离子具有很强的荧光响应,并且荧光波长在470nm和640nm处的荧光强度呈现比率型变化;而且本发明所述荧光探针csn可以直接应用于水溶液中和细胞环境中次氯酸根离子的快速检测和生物成像。
附图说明
[0038]
图1为基于噻吩并香豆素的比率型探针csn溶液在加入次氯酸钠前后的颜色外观变化,其中(a)为在uv灯下,(b)为日照光下;
[0039]
图2为基于噻吩并香豆素的比率型探针csn中逐渐滴加次氯酸钠后形成的探针csn测试溶液的荧光发射光谱图;
[0040]
图3为探针csn测试溶液的荧光发射光波长在470nm和640nm的荧光光强比值(i
470
/i
640
)与探针csn测试溶液的次氯酸根离子浓度的线性关系图;
[0041]
图4为基于噻吩并香豆素的比率型探针csn在活细胞中不同次氯酸根离子浓度时的生物成像图。
具体实施方式
[0042]
下面结合实施例和附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。在下面的描述中阐述了很多具体细节以便于充分理解本发明。但是本发明能够以很多不同于在此描述的其它方式来实施,本领域技术人员可以在不违背本发明内涵的情况下做类似改进,因此本发明不受下面公开的具体实施的限制。
[0043]
实施例中所用试剂如无特殊说明均可从市场常规购得。
[0044]
实施例中基于噻吩并香豆素的比率型探针csn的合成路线如下所示:
[0045][0046]
实施例1:化合物1的合成
[0047]
将丙二酸二苯酯(5.1g,20mmol)、3-(n,n-二乙氨基)苯酚(3.3g,20mmol)和甲苯(50ml)在110℃下回流反应8h。待其冷却至室温后,将不溶物进行过滤,并且用石油醚洗涤三次;即可获得绿灰色固体化合物1(2.56g产率55%)。
[0048]1h nmr(400mhz,dmso-d6)δ1.11(t,6h),3.40(q,4h),5.25(s,1h),6.45(d,j=2.4hz,1h),6.65(dd,j=2.4hz,j=9.2hz,1h),7.55(d,j=9hz,1h),11.86(s,1h).
[0049]
实施例2:化合物2的合成
[0050]
在氮气气氛下,将pocl3(2.8ml)逐滴加入dmf(2.8ml)中,并在室温下搅拌30分钟,得到粉红色悬浮液。将化合物1(2.33g,10mmol)的dmf(13ml)溶液逐滴加到上述悬浮液中,接着在60℃下搅拌过夜。次日后待冷却至室温,将反应混合物倒入冰水中,并用氢氧化钠水溶液(5mol/l)对其进行中和,过滤后即可获得黄色固体。将固体用去离子水清洗并干燥,获得化合物2(1.20g,产率88.2%)。
[0051]1h nmr(400mhz,cdcl3)δ10.33(s,1h),7.87(d,j=9.2hz,1h),6.72(dd,j=9.6hz&j=2.0hz,1h),6.47(d,j=2.4hz,1h),3.51(q,j=7.2hz,4h),1.29(t,j=7.2hz,6h).
[0052]
实施例3:化合物3的合成
[0053]
将k2co3(830mg,6.0mmol)和1,4-二硫-2,5-二醇(183mg,1.20mmol)添加到化合物2(560mg,2.0mmol)的丙酮(40ml)溶液中。然后将混合物在室温下搅拌1h,继而升温至45℃再搅拌3h;随后在冰水中冷却静置1h。接着过滤收集黄色沉淀,不溶物用冰乙醇多次洗涤。之后,再将滤饼重新用ch2cl2溶解并去除不溶物。最后将所得滤液进行减压蒸馏,得到黄色固体化合物3(494mg,产率82%)。
[0054]1h nmr(400mhz,dmso-d6)δ9.96(s,1h),8.42(s,1h),7.72(d,j=8.8hz,2h),6.79(dd,j=8.80hz&j=2.0hz,1h),6.64(d,j=2.0hz,1h),3.47(q,j=6.8hz,4h),1.15(t,j=6.8hz,6h).
13
c nmr(150mhz,dmso-d6)δ184.0,156.51,154.96,154.28,151.15,139.16,137.27,125.94,120.60,109.70,103.79,97.00,44.13,12.25.ms-esi(c
16
h
15
no3s):calcd.for[m+h]
+
301.09;found:302.1.
[0055]
实施例4:荧光探针分子csn的制备
[0056]
将二氨基马来腈(359mg,3.3mmol)和对甲苯磺酸(tsoh,8mg,0.05mmol)溶于乙醇(20ml)中,然后滴加化合物3(100mg,0.33mmol)的乙腈溶液(40ml),并在室温下搅拌1h。随后,将反应液旋干,并用无水乙醇重结晶。通过过滤收集红色固体,然后通过柱层析法(ch2cl2:乙酸乙酯=20:1)纯化,得到探针csn作为红色固体(72mg,产率55%).
[0057]1h nmr(400mhz,dmso-d6)δ8.49(s,1h),8.09(s,1h),7.88(bs,2h),7.52(d,j=8.8hz,1h),6.80(d,j=9.2hz,1h),6.63(s,1h),3.46(q,j=6.8hz,4h),1.15(t,j=6.8hz,6h).
13
c nmr(150mhz,dmso-d6)δ156.90,154.29,153.05,150.89,148.52,138.91,132.31,126.80,125.43,121.38,114.82,114.16,110.13,104.76,103.04,97.58,44.61,12.84.hrms-esi(c
20
h
16
o2n5s):calcd.for[m-h]-390.10302;found:390.1038.
[0058]
实施例5荧光探针分子csn对次氯酸根离子的检测
[0059]
(1)含ctab的pbs缓冲溶液的配制
[0060]
准确称取磷酸二氢钾1.70g、十六烷基三甲基溴化铵(ctab,137mg)和氢氧化钠395mg于小烧杯中,接着用二次蒸馏水溶解并转移至250ml容量瓶中;然后定容、摇匀。用ph计测量其ph为7.40后,放入冰箱密封待用。
[0061]
(2)探针的测试溶液的配置
[0062]
用n,n-二甲基甲酰胺(dmf)溶解探针化合物csn,得到1.0
×
10-3
mol/l的探针母液备用。测试时取0.1ml的1.0
×
10-3
mol/l探针母液,加入10ml容量瓶中,并用上述pbs缓冲溶
液定容;接着加入不同体积的次氯酸钠水溶液(10mmol/l),从而获得了不同次氯酸根离子浓度下(0-150μmol/l)的探针csn测试溶液。
[0063]
向基于噻吩并香豆素的比率型探针csn溶液中加入次氯酸钠溶液前后颜色均发生了变化,具体如图1所示,从图1中可以看出,在紫外灯下,颜色由橙红色变成了蓝色;在日照光下颜色由橙黄色变成了淡黄色。
[0064]
图2为向基于噻吩并香豆素的比率型探针csn溶液中逐渐滴加次氯酸钠后的探针csn测试溶液的荧光发射光谱图;图3为向基于噻吩并香豆素的比率型探针csn溶液中逐渐滴加次氯酸钠后的探针csn测试溶液的荧光发射光波长在470nm和640nm的荧光光强比值(i
470
/i
640
)与探针csn测试溶液中次氯酸根离子浓度的线性关系图;从图2和图3中可以看出,随着探针csn测试溶液中次氯酸钠浓度的增加,荧光发射波长在470nm处的强度逐渐増强,而在640nm处的荧光则明显减弱。同时,其荧光光强比值(i
470
/i
640
)与次氯酸根离子浓度呈现出明显的线性关系。
[0065]
(3)荧光探针csn在活细胞中检测次氯酸根离子的应用
[0066]
在荧光成像实验前,将hela细胞种植在14mm玻璃盖玻片上,贴壁24h。然后用10μmol/l的探针csn水溶液在37℃下孵育30分钟,并用pbs缓冲液洗涤(3次);再以413nm半导体激光器为激发光源,在440-480nm处(蓝色信号通道)与600-660nm处(红色信号通道)收集两块的荧光信号。之后,往细胞培养液中加入不同浓度的次氯酸钠并孵育0.5h后,继续以413nm半导体激光器为激发光源,在440-480nm处(蓝色信号通道)与600-660nm处(红色信号通道)收集两块的荧光信号,结果如图4所示,图4中clo前面的浓度指加入次氯酸钠之后次氯酸根离子的终浓度。
[0067]
由图4可以看出,用探针csn在37℃下孵育hela细胞30min,可观察到明显的红色荧光,说明探针csn可以渗透到细胞中。之后,往细胞培养液中加入次氯酸钠并孵育0.5h后,我们可以观测到细胞内的红色荧光随着次氯酸钠浓度提升而逐渐减弱,而细胞内的蓝色荧光却随之增强。上述实验结果充分表明,本发明所述荧光探针csn可以有效检测细胞体内的次氯酸根离子,具有良好的生物应用价值。
[0068]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1