一种定量Pichiapastoris细胞残留的核酸检测试剂盒的制作方法
本发明属于生物工程技术领域,具体涉及一种定量pichiapastoris细胞残留的核酸检测试剂盒。
背景技术:
实时荧光pcr技术是近年来发展迅速的一种核酸检测技术,使用一种带有核电偶联装置(ccd)的pcr扩增仪,通过检测荧光信号的动态变化实时反映pcr的每个循环的扩增水平。ccd能够按照一定的程序周期性地发出特定波长的激发光,收集检测荧光信号,并通过软件分析汇总到工作站得到扩增曲线。taqmanpcr技术是实时荧光pcr的一种。与传统的pcr相对比,其在反应体系中增加了一条两端分别标记荧光报告基团和淬灭基团的探针。探针结构完整时,荧光报告基团发出荧光的能量转移给淬灭基团,呈现淬灭效应。如果扩增过程中有靶序列的存在,扩增的过程中探针分子逐渐被水解切断,荧光报告基团与淬灭基团相互解离,阻断了二者间荧光共振能量转移效应,荧光报告基团发出荧光信号。随着扩增的进行,荧光信号随着目的片段的扩增而呈现线性增强。
与分子杂交方法相比,taqmanpcr技术应用于定量检测中具有如下优点:通过对扩增曲线以及对数增长期的循环阈值(ct)的分析,摒弃分子杂交法受多种因素干扰的终点分析方法,能够对待测样品进行准确定量分析,从而有效监测疫苗纯化的效果;将dna扩增与检测过程融合为一体,可以实时、动态监测dna扩增的全过程,省掉了分子杂交后处理过程,大大缩短了结果分析时间,使得该方法更加快捷、方便;由于采取一种封闭的检测模式,从而减少了气溶胶污染和由此造成的假阳性;由于在普通pcr基础上增加了一条可与模板互补配对的荧光探针,有效结合了pcr和探针杂交的双重特异性,进一步提高了检测目标靶多核苷酸的特异性。因此,该技术在靶多核苷酸样品的检测和定量分析中,已逐渐取代传统的分子杂交方法,在病原体的定量或定性检测中得到十分广泛的应用。
美国食品与药品管理局(fda)已经批准了一些定量检测病原体的pcr诊断试剂盒,如用于hiv、结核分枝杆菌、沙眼衣原体等的实时荧光pcr检测的试剂盒。同样,中国目前也已批准了乙型肝炎、丙型肝炎、hiv和sars等的实时荧光pcr检测试剂盒的生产和临床应用。虽然已经有用染料法实时荧光pcr检测cho细胞dna残留的报道,但在疫苗残留dna的检测中,目前还没有针对pichiapastoris细胞dna残留的精确定量、特异性强的探针法实时荧光定量pcr检测试剂盒。
技术实现要素:
本发明的目的在于克服现有技术的不足,提供一种定量pichiapastoris细胞残留的核酸检测试剂盒,本试剂盒可用于检测疫苗样品中pichiapastoris细胞残留dna,从而对疫苗生产过程中进行质量监测。
本试剂盒的基本原理是利用一对靶多核苷酸的特异性引物和一条靶多聚核苷酸的特异性探针,在含有耐热dna聚合酶、高质量的脱氧核糖核苷三磷酸(dntps)以及mg2+的pcr反应缓冲液中,通过荧光pcr扩增仪实现靶多核苷酸的循环扩增,从而达到快速、定量检测靶多核苷酸的目的。
本发明所提供的检测疫苗样品中pichiapastoris细胞残留dna的试剂盒包括:(1)分别装有pcr扩增反应液、阴性质控品、阳性质控品和定量标准品并加盖密封的多个试剂瓶或管,和(2)分隔并集中包装这些试剂瓶或管的包装盒。其中,所述pcr扩增反应液中用于靶多核苷酸扩增的正向引物pichiapastoris-f和反向引物pichiapastoris-r的序列分别是:
5’-ttattccccgttacccgtagaa-3’(seqidno:1)
5’-tgccctatcaactttcgatggt-3’(seqidno:2)
根据本发明的一个优选实施方案,pcr扩增反应液中用于靶多核苷酸扩增和监测体系的寡核苷酸探针pichiapastoris-p的序列是:
5’-ccatggtaggcctct-3’(seqidno:3)。
根据本发明的另一个优选实施方案,其中pcr扩增反应液由(a)耐热dna聚合酶、(b)脱氧核糖核苷三磷酸(dntps)、(c)含镁离子的缓冲液、(d)能够与双链靶多核苷酸的第一条链结合的正向引物,(e)能够与双链靶多核苷酸的第二条链结合的反向引物,和(f)能够与靶多核苷酸结合并且两末端分别结合有荧光发生基团和荧光淬灭基团的寡核苷酸探针组成。
根据本发明的另一个优选实施方案,其中寡核苷酸探针5’端标记有荧光报告基团,其荧光报告基团为fam,3’端标记有淬灭基团,其淬灭基团为mgb。
根据本发明的另一个优选实施方案,其中用于pcr扩增的最佳反应温度和时间为:50oc2min,95oc预变性10min;然后95oc10s,60oc1min,40个循环。
根据本发明的另一个优选实施方案,其中阴性质控品为hek293基因组dna、cho细胞基因组dna、vero细胞基因组dna。
根据本发明的另一个优选实施方案,其中阳性质控品为pichiapastoris细胞基因组dna。
根据本发明的另一个优选实施方案,其中定量标准品为pichiapastoris细胞基因组dna,原液浓度为30ng/ul,经稀释的使用浓度,分别为300pg/ul,30pg/ul,3pg/ul,0.3pg/ul,0.03pg/ul,0.003pg/ul。
本发明的优点和有益效果为:
1、本发明提供的实时荧光定量pcr检测试剂盒可以检测出pichiapastoris细胞dna的最低浓度为1fg/μl,说明本试剂盒具有非常好的灵敏度。
2、本发明针对pichiapastoris细胞基因组dna的基因保守区设计特异引物和探针,可检测出pichiapastoris细胞基因组dna,但不能检测出非pichiapastoris细胞基因组dna,说明本试剂盒具有很好的特异性。
3、本发明提供的实时荧光定量pcr检测试剂盒可以检测疫苗半成品、成品等样品中pichiapastoris细胞残留dna的试剂盒;可为疫苗半成品、成品等生产环节提供可靠的质控证据,为疫苗安全生产与使用提供重要保障。
附图说明
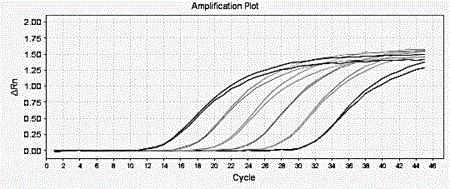
图1为本发明的pichiapastoris细胞dna定量标准品的检测结果图;ct值为10~40,扩增曲线有明显指数增长期,成s型,可明确判定为阳性。
图2为定量标准品扩增结果的标准曲线;针对模板数为300pg/ul、30pg/ul、3pg/ul、0.3pg/ul、0.03pg/ul,0.003pg/ul的反应体系进行taqmanpcr分析。pichiapastoris细胞基因组dna为0.003pg/ul时,检测样品的ct值在32左右,为明显阳性,即检测下限灵敏度可达到0.003pg/ul。绘制得到的标准曲线相关系数(r2)=0.997。
图3定量标准品与其他3种阴性参考品对照的标准曲线,阴性参考品基本呈平直,可明确判定为阴性。3种阴性参考品包括hek293细胞、cho细胞和e.coli细胞。
对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,可以根据以上附图获得其他的相关附图。
具体实施方式
为了使本技术领域的人员更好地理解本发明方案,下面结合具体实施例进一步说明本发明的技术方案。
实施例1:
试剂盒的制备
试剂盒的制备包括以下组成成分:
pichiapastoris细胞基因组dna(30ng/ul)(40ul/管)1管、dna稀释液(7ml/瓶)1瓶、2×qpcr预混液(750ul/管)1管、10×引物探针混合物(150ul/管)1管、超纯水(1.5ml/管)1管。
其中,2×qpcr预混液为商业化试剂(天根),dna稀释液由实验室采用分子生物级试剂自行配置,10×引物探针混合物:将正向引物:反向引物:taqman探针按照1:1:0.2的比例进行混合,得到10×引物探针混合物。引物和探针由上海生工进行合成纯化,序列如下:
正向引物序列:5’-ttattccccgttacccgtagaa-3’(seqidno:1)
反向引物序列:5’-tgccctatcaactttcgatggt-3’(seqidno:2)
taqman探针:5’-ccatggtaggcctct-3’(seqidno:3)
taqman探针5’端的荧光报告基团为fam;3’端的淬灭基团为mgb。
实施例2
pichiapastoris细胞dna的qpcr测试方法
dna的提取标定:按照基因组dna提取试剂盒(天根)说明书提取pichiapastoris细胞的基因组dna,然后利用qubit(invitrogen)将基因组dna的浓度标定至30ng/ul。
将pcr反应所需试剂取出:2×qpcr预混液,引物探针混合物,定量标准品,超纯水。
根据样品的数量确定最终的反应管数从而准备qpcrmix,如下表1.
加样完成后,在abi7500实时荧光定量pcr仪(abi)上进行pcr扩增。反应条件为:50oc2min,95oc预变性10min;95oc10sec,60oc1min,40个循环。
实施例3
pichiapastoris细胞基因组dna标准曲线的绘制
将抽提标定好的pichiapastoris细胞基因组dna(30ng/ul)利用dna稀释液进行梯度稀释,得到st1(300pg/ul),st2(30pg/ul),st3(3pg/ul),st4(0.3pg/ul),st5(0.03pg/ul),st6(0.003pg/ul)。按照表1的加样体系进行加样,然后上机并按照反应程序进行反应。图1为本发明的pichiapastoris细胞dna定量标准品的检测结果图;ct值为10~40,扩增曲线有明显指数增长期,成s型,可明确判定为阳性。用pichiapastoris基因组dna各稀释度浓度的log值对每个稀释度的ct(初始循环数)值作图,二者呈线性递减的关系,该线性曲线即是pichiapastorisgdna定量标准曲线,如图2所示,曲线的r2为0.997,反映扩增反应的扩增效率在90-110%之间。
实施例4
pichiapastoris细胞dna残留检测方法灵敏度测试
将pichiapastoris基因组dna稀释至6fg/μl,4.5fg/μl,3fg/μl,1fg/μl,然后利用反应体系进行测定以确定其检测灵敏度,每个浓度做10个重复。实验结果显示:浓度低至1fg/μl时,其cv至仍<15%(表2),因此,检测反应的灵敏度可低至1fg/μl。
实施例5
pichiapastoris细胞dna残留检测方法的重复性和紧密度测试
对于重复性实验,针对3pg/ul的样本进行检定,做10个重复。如下表所示,实验结果显示:cv值均<15%,表明实验重复性好。
对于中间精密度实验,针对30pg/ul,3pg/ul,0.3pg/ul和0.03pg/ul的四个不同浓度的样本,由三个不同的人员进行定量检测。每个人每组样本独立重复3次。实验结果显示:各组的cv值均<10%,结果如下表4所示。
实施例6
pichiapastoris细胞dna残留检测方法的特异性测试
将单独抽提好的hek293基因组dna、cho细胞基因组dna、pichiapastoris细胞基因组dna和e.coli细胞基因组dna进行梯度稀释,然后按照反应体系进行加样检测并绘制曲线。图3为定量标准品与其他3种阴性参考品对照的标准曲线,实验结果显示:该方法只针对pichiapastoris细胞,具有很高的检测特异性。
以上对本发明做了示例性的描述,应该说明的是,在不脱离本发明的核心的情况下,任何简单的变形、修改或者其他本领域技术人员能够不花费创造性劳动的等同替换均落入本发明的保护范围。
序列表
<110>天津欧德莱生物医药科技有限公司
<120>一种定量pichiapastoris细胞残留的核酸检测试剂盒
<130>1
<160>4
<170>siposequencelisting1.0
<210>1
<211>22
<212>dna
<213>人工合成()
<400>1
ttattccccgttacccgtagaa22
<210>2
<211>22
<212>dna
<213>人工合成()
<400>2
tgccctatcaactttcgatggt22
<210>3
<211>15
<212>dna
<213>人工合成()
<400>3
ccatggtaggcctct15
<210>4
<211>65
<212>dna
<213>人工合成()
<400>4
ttattccccgttacccgtagaaaccatggtaggcctctctcctaccatcgaaagttgata60
gggca65
- 还没有人留言评论。精彩留言会获得点赞!