可应用于肿瘤细胞捕获的小鼠抗细胞表面糖蛋白CD138的单克隆抗体的制作方法
可应用于肿瘤细胞捕获的小鼠抗细胞表面糖蛋白cd138的单克隆抗体
技术领域
[0001]
本发明涉及一种单克隆抗体,尤其是一种可应用于肿瘤细胞捕获的小鼠抗细胞表面糖蛋白cd138的单克隆抗体。
背景技术:
[0002]
cd138是多聚体蛋白聚糖,属于黏附分子整合素跨膜黏结蛋白聚糖家族成员,它主要分布于内皮细胞、上皮细胞、纤维母细胞、角质细胞表面,通过其分子表面的硫酸肝素侧链可结合一系列配基,如细胞黏附分子、基质分子、生长因子、没和酶抑制剂等,以共受体方式调节细胞和微环境之间的相互作用,参与组织器官分化发育、血管形成、组织再生等一系列生理过程的调节,与细胞的增殖、黏附、迁移相关。其可溶性cd138分子在组织损伤修复中可作为碱性纤维母细胞生长因子的拮抗剂或激动剂,参与损伤修复过程,同时也具有抑制肿瘤细胞增殖的作用。随着研究的深入,发现cd138分子的表达在空中恶性肿瘤细胞生长和转移等过程中具有重要作用,而且可作为判断肿瘤预后的指标,对知道临床诊断与免疫治疗具有重要意义,目前市场上鲜有以cd138作为靶标载体的抗体类产品,并且都没有数据表明可以用于活肿瘤细胞富集。同时对于该研究领域缺乏有效的抗体工具。
技术实现要素:
[0003]
本发明的目的为提供一个靶向蛋白研究的工具,对不同癌症患者、癌症不同分期的蛋白表达变化及蛋白网络图谱的更深层次研究得以实现。
[0004]
本发明采用的技术方案如下:一种可应用于肿瘤细胞捕获的小鼠抗细胞表面糖蛋白cd138的单克隆抗体,其工艺包括如下步骤:
[0005]
s1,蛋白qc:采购商业化蛋白;
[0006]
s2,动物免疫:选取6只balb/c小鼠进行抗原免疫,并监测其血清效价以决定最优的免疫小鼠,初次免疫后会经过3到4次的加强,加强后将取小鼠血清检测滴度,筛选出滴度合格的小鼠冲击一次并用于融合,不合格的小鼠将继续一到两次加强至滴度最高后融合;
[0007]
s3,血清检测和筛选:免疫小鼠眼眶取血,并用elisa检测血清滴度,确定其血清效价合格;
[0008]
s4,融合及筛选:取全脾和1/2的淋巴结,与骨髓瘤sp2/0细胞系融合,融合细胞铺到4块384孔板上,进行培养,收集所有孔的上清,用elisa对免疫蛋白进行筛选,镜检有细胞的阳性孔转到96孔板继续培养,生长几天后,收集所有孔的上清,用elisa检测与可溶片段检测原的反应,阳性孔进一步检测不同稀释度的蛋白结合,以进行亲和力排序,每个融合选免疫原亲和力最高的20个亲代克隆进入亚克隆;
[0009]
s5,亚克隆及筛选:通过有限稀释法和elisa筛选进行亚克隆,得到单克隆杂交瘤细胞,细胞铺96孔板,并培养至覆盖约1/6的底部,elisa检测每个孔上清针对免疫抗原的反应,取od值高且细胞状态良好的两个孔进入下轮亚克隆,重复上述步骤直到孔中细胞株阳
性率100%,此时得到单克隆细胞株,经过最后一轮亚克隆后,所有阳性细胞立即扩大培养,一部分冻存供以后使用,另一部分进行上清或腹水制备;
[0010]
s6,抗体上清制备:将最后获得的单克隆细胞株,通过腹部注射到f1小鼠用于抗体生产,产生的腹水用protein a/g纯化,并用于后续检测;
[0011]
s7,抗体验证:对获得的单克隆抗体细胞株进行elisa,western blotting,免疫共沉淀加质谱,抗体芯片等验证,确定最有效抗体。
[0012]
作为本发明的一种优选技术方案:所述s2中balb/c小鼠为8-12周龄的balb/c小鼠。
[0013]
作为本发明的一种优选技术方案:所述s3中血清效价合格线为血清效价大于10k。
[0014]
作为本发明的一种优选技术方案:所述s4中的融合工艺为优化过的peg融合。
[0015]
作为本发明的一种优选技术方案:所述s4中4块384孔板上每孔细胞为102~104。
[0016]
作为本发明的一种优选技术方案:所述s7中的elisa验证具体为:取待检测的抗体包被96孔elisa板,孵育,洗涤后脱脂牛奶过夜封闭,进行pbs洗涤后4℃保存待用;再进行抗原孵育,pbs洗涤,同时设置对照,加入his-hrp,tmb显色反应,酶标仪读数。
[0017]
作为本发明的一种优选技术方案:所述s7中的抗体芯片具体为:使用芯片点样仪将抗-cd138抗体及对照抗体点制于以nc膜为基质的玻璃片,形成直径为100um的抗体点,将a375的全蛋白进行生物素标记,按2ug/ml的浓度孵育在抗体芯片上,室温孵育半小时,pbs轻柔清洗三遍,再用cy3-sa荧光二抗进行孵育,pbs清洗三遍,使用genepix荧光芯片扫描仪523nm扫描芯片。
[0018]
作为本发明的一种优选技术方案:所述的小鼠抗细胞表面糖蛋白cd138的单克隆抗体可变区测序结果为:
[0019]
vhf1
[0020]
evkleesggglvqpggsmelscvas
[0021]
vhcdr1
[0022]
gftfskyw
[0023]
vhf2
[0024]
mnwvrqspekglewvaa
[0025]
vhcdr2
[0026]
irlksnnyat
[0027]
vhf3
[0028]
hyaesvkgrftisrddsknsvylqmnnlrtedtgiyyc
[0029]
vhcdr3
[0030]
tatgnfdv
[0031]
vhf4
[0032]
wgagttvtvss
[0033]
vlf1
[0034]
dikmtqspssmyaslgervtitckas
[0035]
vlcdr1
[0036]
qdinsy
[0037]
vlf2
[0038]
lswfqqkpgkspktlmy
[0039]
vlcdr2
[0040]
ran
[0041]
vlf3
[0042]
rlvdgvpsrfsgsgsgqdysltissleyedmgiyyc
[0043]
vlcdr3
[0044]
lqydefppt
[0045]
vlf4
[0046]
fgggtkveik。
[0047]
本发明的可应用于肿瘤细胞捕获的小鼠抗细胞表面糖蛋白cd138的单克隆抗体具有高亲和力,高特异性,多应用场景等特点,并且可应用于活细胞富集。
附图说明
[0048]
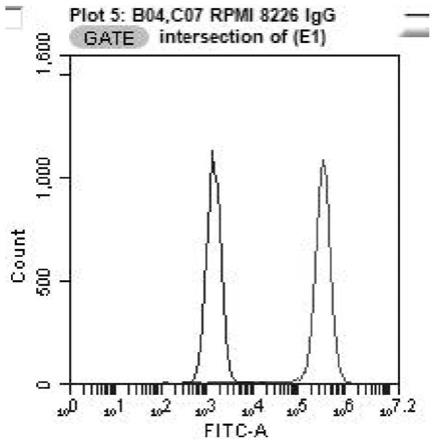
图1为本发明优选实施例中抗体流式细胞术结果图;
[0049]
图2为本发明优选实施例中癌细胞杀伤结果图;
[0050]
图3为本发明优选实施例中抗体芯片检测实验结果图。
具体实施方式
[0051]
需要说明的是,在不冲突的情况下,本申请中的实施例及实施例中的特征可以相互组合,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0052]
参照图1,本发明优选实施例提供了一种可应用于肿瘤细胞捕获的小鼠抗细胞表面糖蛋白cd138的单克隆抗体,其工艺包括如下步骤:
[0053]
s1,蛋白qc:采购商业化蛋白;具体的,在本实施例中采购的为acro公司的货号:sd1-h5228的蛋白。
[0054]
s2,动物免疫:选取6只balb/c小鼠进行抗原免疫,并监测其血清效价以决定最优的免疫小鼠,初次免疫后会经过3到4次的加强,加强后将取小鼠血清检测滴度,筛选出滴度合格的小鼠冲击一次并用于融合,不合格的小鼠将继续一到两次加强至滴度最高后融合;具体的,优化了的佐剂和免疫方法能产生针对大多数抗原的高亲和力的抗体(igg亚型)。
[0055]
s3,血清检测和筛选:免疫小鼠眼眶取血,并用elisa检测血清滴度,确定其血清效价合格;
[0056]
s4,融合及筛选:取全脾和1/2的淋巴结,与骨髓瘤sp2/0细胞系融合,融合细胞铺到4块384孔板上,进行培养,收集所有孔的上清,用elisa对免疫蛋白进行筛选,镜检有细胞的阳性孔转到96孔板继续培养,生长几天后,收集所有孔的上清,用elisa检测与可溶片段检测原的反应,阳性孔进一步检测不同稀释度的蛋白结合,以进行亲和力排序,每个融合选免疫原亲和力最高的20个亲代克隆进入亚克隆;
[0057]
s5,亚克隆及筛选:通过有限稀释法和elisa筛选进行亚克隆,得到单克隆杂交瘤细胞,细胞铺96孔板,并培养至覆盖约1/6的底部,elisa检测每个孔上清针对免疫抗原的反应,取od值高且细胞状态良好的两个孔进入下轮亚克隆,重复上述步骤直到孔中细胞株阳性率100%,此时得到单克隆细胞株,经过最后一轮亚克隆后,所有阳性细胞立即扩大培养,一部分冻存供以后使用,另一部分进行上清或腹水制备;
[0058]
s6,抗体上清制备:将最后获得的单克隆细胞株,在本实施例中最终获得7株单克隆细胞株,通过腹部注射到f1小鼠用于抗体生产,产生的腹水用protein a/g纯化,并用于后续检测;
[0059]
s7,抗体验证:对获得的7株单克隆抗体细胞株进行elisa,western blotting,免疫共沉淀加质谱,抗体芯片等验证,确定最有效抗体。
[0060]
本实施例中:所述s2中balb/c小鼠为8-12周龄的balb/c小鼠。
[0061]
本实施例中:所述s3中血清效价合格线为血清效价大于10k。
[0062]
本实施例中:所述s4中的融合工艺为优化过的peg融合。
[0063]
本实施例中:所述s4中4块384孔板上每孔细胞为102~104。
[0064]
本实施例中:所述s7中的elisa验证具体为:取待检测的抗体包被96孔elisa板,孵育,洗涤后脱脂牛奶过夜封闭,pbs洗涤,4℃保存待用。抗原孵育(梯度稀释),pbs洗涤,同时设置对照。加入his-hrp(抗原带his标签),tmb显色反应,酶标仪读数。
[0065]
在本实施例中,本发明人通过s7的elisa亲和力验证得到8个细胞株的亲和力如下表:
[0066]
nm100502512.56.253.1251.570.780.40.20.1nc亲和力nm2o53.1663.2293.2432.9352.9082.7302.1201.5730.8860.5110.2560.0550.22k193.9003.7793.9003.9003.9553.7792.7461.8821.2980.5110.2630.0580.22b142.7192.5382.4452.1701.5930.9170.5710.2360.1320.0680.0570.0561.573f33.9003.9543.8873.8293.7333.7783.4543.0252.1711.2180.5360.0760.11h16-b3.3903.2863.1312.9552.7162.5872.1811.9481.3330.9520.5090.0560.11f52.7202.2891.9721.4771.0620.7140.5050.2710.1630.1110.0930.0681.571j133.9003.7603.8123.6733.5693.4142.9292.0441.1350.6150.2770.0560.2
[0067]
需要补充的是,在这个实施例中,我们还分别进行了抗体的流式细胞术验证和癌细胞杀伤实验。
[0068]
具体如图1所示,抗体的流式细胞术验证为:rpmi-8226细胞作为检测细胞系,使用pbs清洗,edta消化,转移至离心管中,离心弃上清后用pbs重悬,山羊血清常温封闭1小时,一抗孵育,工作浓度50ug/ml,荧光二抗孵育,工作浓度1:300。结果显示,本抗体可以应用流式细胞实验。
[0069]
如图2所示,癌细胞杀伤实验为:在96孔板中配制100ul细胞rpmi-8226悬液,预培养24小时,向培养板中加入10ul不同稀释梯度的抗-cd138抗体,加入偶联小分子药物的小鼠二抗,培养3天,向每孔加入10ul cck-8溶液,孵育1-4小时,用酶标仪测定再450nm处的吸光度。实验结果显示该抗体对癌细胞rpmi-8226很好的杀伤作用。
[0070]
本实施例中:所述s7中的抗体芯片具体为:使用芯片点样仪将抗-cd138抗体及对照抗体点制于以nc膜为基质的玻璃片,形成直径为100um的抗体点,将a375的全蛋白进行生物素标记,按2ug/ml的浓度孵育在抗体芯片上,室温孵育半小时,pbs轻柔清洗三遍,再用cy3-sa荧光二抗进行孵育,pbs清洗三遍,使用genepix荧光芯片扫描仪523nm扫描芯片。
[0071]
实验结果如图3所示,实验结果显示抗-cd138(克隆1h16-b)对目标蛋白有明显富集结合效果,荧光强度较强而对照抗体没有发生抗原抗体结合反应。
[0072]
本实施例中:所述的小鼠抗细胞表面糖蛋白cd138的单克隆抗体可变区测序结果为:
[0073]
vhf1
[0074]
evkleesggglvqpggsmelscvas
[0075]
vhcdr1
[0076]
gftfskyw
[0077]
vhf2
[0078]
mnwvrqspekglewvaa
[0079]
vhcdr2
[0080]
irlksnnyat
[0081]
vhf3
[0082]
hyaesvkgrftisrddsknsvylqmnnlrtedtgiyyc
[0083]
vhcdr3
[0084]
tatgnfdv
[0085]
vhf4
[0086]
wgagttvtvss
[0087]
vlf1
[0088]
dikmtqspssmyaslgervtitckas
[0089]
vlcdr1
[0090]
qdinsy
[0091]
vlf2
[0092]
lswfqqkpgkspktlmy
[0093]
vlcdr2
[0094]
ran
[0095]
vlf3
[0096]
rlvdgvpsrfsgsgsgqdysltissleyedmgiyyc
[0097]
vlcdr3
[0098]
lqydefppt
[0099]
vlf4
[0100]
fgggtkveik。
[0101]
对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。不应将权利要求中的任何附图标记视为限制所涉及的权利要求。
[0102]
此外,应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当
将说明书作为一个整体,各实施例中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1