一种新型、绿色、高效合成四酚基乙烷的方法与流程
[0001]
本发明属于有机化学领域,具体涉及一种新型、绿色、高效合成四酚基乙烷的方法。
背景技术:
[0002]
四酚基乙烷的分子式为c
26
h
22
o4,结构式为1,是一种高度对称的有机化合物,是重要的化工产品和工业原料。可作为特种环氧和氰酸酯的原材料,通用型环氧树脂的固化剂,酚醛树脂的改性剂和光致抗蚀剂。其中,由四酚基乙烷合成的四酚基乙烷环氧树脂是高度对称的四官能度环氧树脂,具有高环氧值、耐高温性、紫外屏蔽功能和适应aoi自动光学检测功能。因而,可广泛应用于印刷线路板、电子电气材料、成型浇注材料、层压板材料、光学材料、封装材料、黏结剂等领域。
[0003]
此前,国内外文献报道合成四酚基乙烷的方式均为在酸催化剂存在下,苯酚与乙二醛反应。此方式会产生一酚基化合物,二酚基化合物,三酚基化合物等副产物。不仅导致产物收率很低,而且造成产物提纯困难。此外,此方式要使用酸作为催化剂,这样不仅很难控制反应中的放热,而且对设备腐蚀很大。针对这些问题,本发明致力于采用新型、绿色、高效的方式合成四酚基乙烷。
[0004]
技术实现要素:
[0005]
本发明的目的在于提供一种新型、绿色、高效的方法合成四酚基乙烷
[0006]
本发明四酚基乙烷合成方法包括以下步骤:
[0007]
步骤一,光催化剂ccn-k的制备
[0008]
将三聚氰胺置于管式炉中,以2.3℃/min速率升温,550℃恒温4h,自然冷却至室温后,得到产品g-c3n4。然后加入kcl并与g-c3n4混合,研磨成均匀的固体混合物。在氩气保护下,以2.3℃/min速率升温,550℃恒温4h。自然冷却至室温后,将固体混合物用去离子水彻底洗涤以除去金属盐。在真空烘箱中干燥过夜后收集最终产物ccn-k。
[0009]
步骤二,4,4'-(1,2-双(4-(苄氧基)苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)的制备
[0010]
在氩气保护下将4-(4-(苄氧基)亚苄基)-2,6-二叔丁基环己-2,5-二烯-1
-ꢀ
酮、甲酸钠(hcoona)、ccn-k溶于无水乙腈(ch3cn)。随后将h2o加入反应体系。冻抽后置换氩气,重复三次进行除氧。在蓝色led照射下,将反应体系置于40℃反应24h。粗品过滤,并真空浓缩,
得到产品4,4'-(1,2-双(4-(苄氧基)苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)。
[0011]
步骤三,4,4'-(1,2,双(4-羟基苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)的制备
[0012]
在氩气保护下将4,4'-(1,2-双(4-(苄氧基)苯基)乙烷-1,2-二基)双 (2,6-二叔丁基苯酚)、10%钯碳溶于乙酸乙酯(ea)。用氢气置换氩气,在氢气氛围内反应18h。粗品过滤,钯碳回收(能重新使用),滤液真空浓缩后得到产品4,4'-(1,2,双(4-羟基苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)。
[0013]
步骤四,四酚基乙烷的制备
[0014]
在氩气保护下将4,4'-(1,2,双(4-羟基苯基)乙烷-1,2-二基)双(2,6
-ꢀ
二叔丁基苯酚)溶于无水甲苯(toluene),随后在60℃下,将溶于硝基甲烷 (ch3no2)的三氯化铝(alcl3)逐滴滴入反应体系。维持温度反应30min。反应结束后,在60℃下加入冰水淬灭反应,水相用乙酸乙酯(ea)萃取,有机相合并后用饱和食盐水洗,无水硫酸钠(na2so4)干燥。过滤浓缩后粗品经硅胶柱层析纯化得到产品四酚基乙烷。
[0015]
本发明具有如下的技术效果:首先,合成产物四酚基乙烷在印刷线路板、电子电气材料、成型浇注材料、层压板材料、光学材料、封装材料、黏结剂等领域具有重要作用;其次,本发明中插入了可见光催化合成,这是一种高效、安全的环境友好型技术。采用的光催化剂为ccn-k。ccn-k属于半导体光催化剂,相比于ir、ru等金属有机光催化剂具有稳定性好、对人体无毒害、成本低廉、反应条件温和无二次污染等优点。容易大量制备,易于回收,且能循环使用。再而,本发明成本低廉,能大量制备。最后,本发明后处理简单方便,仅步骤四需经硅胶柱层析纯化,其余步骤只需过滤,用乙酸乙酯洗脱,并真空浓缩,即可得到纯产品。
具体实施方式:
[0016]
下面结合实施例对本发明作进一步说明
[0017]
本发明的四酚基乙烷结构式1如下:
[0018][0019]
实施例
[0020]
本发明的四酚基乙烷合成分四步:
[0021]
第一步,光催化剂ccn-k的合成
[0022]
首先称取10g三聚氰胺置于管式炉中,以2.3℃/min速率升温,550℃恒温4h,自然冷却至室温后,得到产品g-c3n4。再加入10g的kcl与1g的g-c3n4混合,研磨得到淡黄色粉末,将其置于管式炉中。在氩气保护下,以2.3℃/min速率升温, 550℃恒温4h。自然冷却至室温后,将固体混合物用去离子水(3
×
10ml)在离心机中以10000r/min的转速离心,去除上层悬液取底部固体。收集的产品在真空烘箱中干燥过夜后得最终产物ccn-k。
[0023]
光催化剂ccn-k的表征图像见说明书附图图7,其中(a)光催化剂ccn-k 的tem图
像;(b)光催化剂ccn-k的hrtem图像;(c-g)光催化剂ccn-k的 tem图像以及相应的元素映射。分别代表c,n,o和k的元素成分。
[0024]
第二步,4,4'-(1,2-双(4-(苄氧基)苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)的合成
[0025]
4,4'-(1,2-双(4-(苄氧基)苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)的结构式2如下:
[0026][0027]
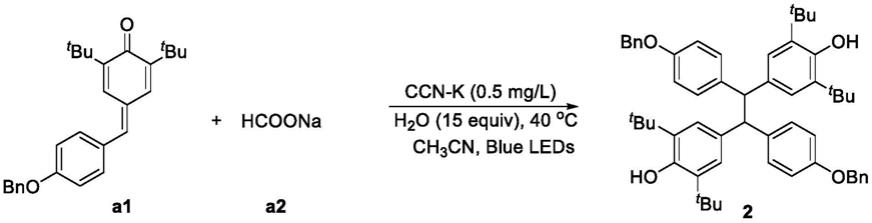
4,4'-(1,2-双(4-(苄氧基)苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)的合成反应过程:
[0028][0029]
在氮气保护下将4-(4-(苄氧基)亚苄基)-2,6-二叔丁基环己-2,5-二烯
-ꢀ
1-酮(1.6g,4mmol,1.0equiv.),甲酸钠(hcoona)(0.544g,8mmol,2.0 equiv.)和ccn-k(40mg)溶于无水乙腈(ch3cn)(80ml)。随后将h2o (1.08ml,60mmol,15.0equiv.)加入反应体系。冻抽后置换氩气,重复三次进行除氧。在两个蓝色led(2
×
24w,465nm)照射下,将反应体系置于40℃反应24h。反应结束后粗品过滤,真空浓缩。得到产品4,4'-(1,2-双(4-(苄氧基)苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)1.6g,产率99%。
[0030]
所得结构式2的物理性质及表征数据:
[0031]
淡黄色固体;1h nmr(500mhz,cdcl3)δ7.40
–
7.25(m,20h),7.07(d,j= 8.4hz,4h),6.96(d,j=8.4hz,4h),6.82(s,8h),6.73(dd,j=15.5,8.4hz,8h),4.94 (s,8h),4.87(s,2h),4.82(s,2h),4.44(s,2h),4.36(s,2h),1.28(d,j=4.9hz,72h). 13
c nmr(126mhz,cdcl3)δ155.61,155.52,150.33,150.15,136.27,136.20,136.10, 135.97,133.83,133.62,133.11,128.50,128.29,127.45,126.78,126.75,126.47,126.36, 124.35,124.18,113.33,113.14,68.88,68.85,55.96,55.74,33.16,33.09,29.30.hrms (esi)m/z calcd.for c
56
h
67
o4[m+h]
+
803.5033,found 803.5045
[0032]
步骤三,4,4'-(1,2,双(4-羟基苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)的合成
[0033]
4,4'-(1,2,双(4-羟基苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚) 的结构式3如下:
[0034][0035]
4,4'-(1,2,双(4-羟基苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚) 的合成反应过程:
[0036][0037]
在氩气保护下将结构式2(1.6g,2mmol,1.0equiv.)和10%pd/c(400mg) 溶于160ml乙酸乙酯(ea)。用氢气置换氩气,在氢气氛围内反应18h。反应完全后,粗品过滤,10%pd/c回收重新利用,滤液经真空浓缩即得到产品4,4'
-ꢀ
(1,2,双(4-羟基苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)1.24g(1:1 d.r.),产率99%。
[0038]
所得结构式3的物理性质及表征数据:
[0039]
白色固体(1:1d.r.);1h nmr(500mhz,cdcl3)δ7.01(d,j=8.3hz,4h), 6.80(s,4h),6.57(d,j=8.3hz,4h),4.83(s,4h),4.40(s,2h),1.28(s,36h).非对映异构体1h nmr(500mhz,dmso)δ8.97(s,2h),7.00(d,j=7.9hz,4h),6.93(s, 4h),6.53
–
6.46(m,6h),4.50(s,2h),1.28(s,36h).
13
c nmr(126mhz,cdcl3)δ 153.23,151.26,136.89,134.98,134.64,129.55,125.21,114.94,56.99,34.18,30.38.非对映异构体
13
c nmr(126mhz,dmso)δ154.59,150.91,138.08,135.56,135.42, 128.99,124.57,114.38,55.22,34.38,30.50.hrms(esi)m/z calcd.for c
42
h
55
o
4 [m+h]
+
623.4094,found 623.4089
[0040]
步骤四,四酚基乙烷的合成
[0041]
四酚基乙烷的结构式1如下:
[0042][0043]
四酚基乙烷的合成反应过程:
[0044][0045]
在氩气保护下将结构式3(1.99g,3.2mmol,1.0equiv.)溶于250ml无水甲苯 (toluene),随后在60℃下,将溶于硝基甲烷(ch3no2)(40ml)的三氯化铝 (alcl3)(5.11g,38.4mmol,12.0equiv.)逐滴滴入反应体系。维持温度反应30 min。反应结束后,在60℃下缓慢加入50ml冰水淬灭,水相再加入乙酸乙酯 (2
×
100ml)萃取。合并有机层,经饱和食盐水洗涤(100ml),无水硫酸钠 (na2so4)干燥后真空浓缩。硅胶柱层析纯化得到产品四酚基乙烷0.65g,产率 51%。
[0046]
所得结构式1的物理性质及表征数据:
[0047]
白色固体;1h nmr(500mhz,cd3od)δ7.01(d,j=7.7hz,8h),6.54(d,j= 7.5hz,8h),4.56(s,2h),3.37(s,4h).
13
c nmr(126mhz,cd3od)δ155.96,137.45, 130.69,115.78,56.54.
[0048]
上述结构式2的4-(4-(苄氧基)亚苄基)-2,6-二叔丁基环己-2,5-二烯-1
-ꢀ
酮为已知化合物,其合成反应参见“引用文献”。
[0049]“copper-catalyzed enantioselective 1,6-boration of para-quinone methides and efficient transformation of gem-diarylmethine boronates to triarylmethanes”(铜催化对醌甲基对苯二酚的1,6-硼酸化反应和硼酸二芳基甲磺酸硼酸酯高效转化为三芳基甲烷),yazhou lou;peng cao;tao jia;yongling zhang;min wang;jian liao, angew.chem.int.ed.2015,54,12134
–
12138.
附图说明
[0050]
图1为四酚基乙烷结构式
[0051]
图2为4,4'-(1,2-双(4-(苄氧基)苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)结构式
[0052]
图3为4,4'-(1,2-双(4-(苄氧基)苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)合成反应路线
[0053]
图4为4,4'-(1,2,双(4-羟基苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)结构式
[0054]
图5为4,4'-(1,2,双(4-羟基苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)合成反应路线
[0055]
图6为4,4'-(1,2,双(4-羟基苯基)乙烷-1,2-二基)双(2,6-二叔丁基苯酚)合成反应路线
[0056]
图7为光催化剂ccn-k的表征图像:(a)光催化剂ccn-k的tem图像;(b) 光催化剂ccn-k的hrtem图像;(c-g)光催化剂ccn-k的tem图像以及相应的元素映射。分别代表c,n,o和k的元素成分。
[0057]
以上各化合反应所用的原料来源列表如下:
[0058][0059]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1