一锅法合成三齿氮配位金属化合物的方法与流程
[0001]
本发明涉及一种三齿氮配位金属化合物的制备方法。
背景技术:
[0002]
高分子材料是现代科学技术和社会发展的支柱,在尖端科技、国防建设和国民经济各个领域已成为不可缺少的重要材料。其中聚烯烃是发展最快、产量最大、用途极广的合成树脂。工业化的聚烯烃催化剂有ziegler-natta型催化剂(de pat889229(1953);it pat 545332(1956)和it pat 536899(1955)),phillips型催化剂(belg.pat.530617(1955))和茂金属型催化剂(w.kaminsky,metalorganiccatalysts for synthesis and polymerization,berlin:springer,1999),以及近年来发展的非茂过渡金属配合物型的高效均聚和共聚催化剂。三齿氮配位的非茂过渡金属催化剂,具有活性高、热稳定性好、立构选择性高的特点,如us 20140316089 报道的高效金属催化剂,可制备高等规聚丙烯和聚烯烃弹性体等。然而,该类催化剂的合成为多步反应,并且所用金属源的价格昂贵,成本较高。例如,合成三齿氮配位的金属铪化合物,需要配体与hf(nme2)2cl2首先反应制备二氯金属铪化合物,然后再与me2mg或者me3al等反应,甲基化后得到相应的金属铪催化剂。不但反应复杂,而且hf(nme2)2cl2等原料成本较高。本发明报道了一种制备该类三齿氮配位金属化合物的新方法,具有反应简单,产率高,原料易得,成本低的特点。
技术实现要素:
[0003]
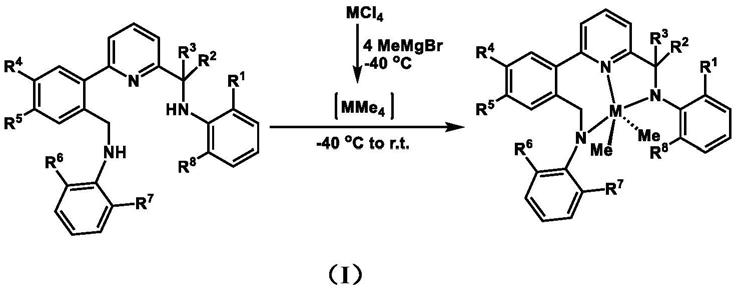
本发明提供了一种一锅法制备三齿氮配位金属化合物的方法,如式(i)所示:
[0004][0005]
其中,m选自钛、锆、铪;r1选自甲基,乙基,氢,异丙基,卤素,苯基,取代苯基;r2选自甲基,乙基,氢,异丙基,卤素,苯基,取代苯基;r3选自甲基,乙基,氢,异丙基,卤素,苯基,取代苯基;r4选自甲基,乙基,氢,异丙基;r5选自甲基,乙基,氢,异丙基,或r5与r4形成环状结构;r6选自甲基,乙基,氢,异丙基,卤素,苯基,取代苯基;r7选自甲基,乙基,氢,异丙基,卤素,苯基,取代苯基;r8选自甲基,乙基,氢,异丙基,卤素,苯基,取代苯基。
[0006]
本发明所提供的制备方法包括以下步骤:
[0007]
氮气氛围下,hfcl4悬浮于无水溶剂中,在-60至-20℃下,加入4摩尔当量的甲基溴化镁,反应2小时;然后在-60至-20℃下加入1摩尔当量的配体,缓慢升至室温反应4-24小
时;减压除去溶剂,加入无水溶剂提取,再次除去溶剂后得到黄色固体产物。
[0008]
上述制备方法中,所述无水溶剂选自苯、甲苯、二甲苯、正己烷。
[0009]
本发明提供了一种一锅法制备三齿氮配位金属化合物的方法。本发明报道了一种制备三齿氮配位金属化合物的新方法,具有反应简单,一锅法合成,无需分离中间产物,产率高,原料易得,成本低的特点。
附图说明
[0010]
图1为化合物[2,6-i
pr-c6h
3-n-ch
2-pyridine-c
10
h
6-ch
2-n-c6h
4-2-me]hfme2的核磁氢谱图;
[0011]
图2为化合物[2,6-i
pr-c6h
3-n-ch
2-pyridine-c6h
4-ch
2-n-c6h
4-2-me]hfme2的核磁氢谱图。
具体实施方式
[0012]
通过实施例进一步说明本发明,但本发明并不限于此。本发明的实施例可以使本专业的技术人员更全面的理解本发明。
[0013]
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
[0014]
以下以具体的实施例描述本发明。
[0015]
实施例1、化合物 [2,6-i
pr-c6h
3-n-ch
2-pyridine-c
10
h
6-ch
2-n-c6h
4-2-me]hfme2的制备方法。
[0016]
氮气氛围下,在100ml schlenk中加入1.92g hfcl4(6.0mmol),加入无水甲苯30ml。在-40℃下,用注射器加入甲基溴化镁的乙醚溶液8ml(24mmol, 3m),然后保持该温度反应2小时。在-40℃下,将3.1g配体 2,6-i
pr-c6h
3-nh-ch
2-pyridine-c
10
h
6-ch
2-nh-c6h
4-2-me(6.0mmol)加入,缓慢升至室温后继续反应12小时。减压除去溶剂,然后加入无水甲苯50ml,过滤后,将滤液抽干得到黄色固体产物3.97g(5.52mmol),产率92%。1h nmr(c6d6): δ7.70(d,1h,j=8.3hz),7.64(d,1h,j=8.1hz),7.44(d,2h,j=8.2hz), 7.28-7.19(m,2h),7.18-6.96(m,8h),6.91(d,1h,j=7.4hz),6.63(d,1h,j=7.8 hz),5.21(d,1h,j=20.5hz),4.89(d,1h,j=20.5hz),4.43(br,1h),4.10(br,1 h),4.00(dt,1h,j=13.7,6.9hz),3.31(br,1h),2.34(br,3h),1.36(d,3h,j=6.8 hz),1.31(d,3h,j=6.8hz),1.15(d,3h,j=6.8hz),0.92(d,3h,j=6.8hz),
ꢀ-
0.06(s,3h),-0.47(br,3h).
[0017]
实施例2、化合物 [2,6-i
pr-c6h
3-n-ch
2-pyridine-c6h
4-ch
2-n-c6h
4-2-me]hfme2的制备方法。
[0018]
氮气氛围下,在100ml schlenk中加入3.20g hfcl4(10.0mmol),加入无水甲苯50ml。在-40℃下,用注射器加入甲基溴化镁的乙醚溶液14ml(42mmol,3m),然后保持该温度反应2小时。在-40℃下,将4.6g配体 2,6-i
pr-c6h
3-nh-ch
2-pyridine-c6h
4-ch
2-nh-c6h
4-2-me(10.0mmol)加入,缓慢升至室温后继续反应12小时。减压除去溶剂,然后加入无水甲苯100ml,过滤后,将滤液抽干得到黄色固体产物6.03g(9.0mmol),产率90%。1h nmr(c6d6): δ7.25(d,1h,j=7.0hz),7.22-7.01(m,10h),6.97(t,1h,j=7.8hz),6.79(d,1h, j=7.4hz),6.54(d,1h,j=7.4hz),5.25(d,1h,j=20.3hz),4.75(d,1h,j=20.3hz),4.47(br,1h),4.09-3.89(m,2h),3.43(br,1h),2.42(br,3h),1.39(d,3h, j=6.9hz),1.35(d,3h,j
=6.8hz),1.23(d,3h,j=6.5hz),1.03(d,3h,j=6.8 hz),-0.09(br,6h).
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1