一种快速、高灵敏性检测和定量酸奶中动物双歧杆菌BB-12的方法与流程
本发明属于农业食品检测技术领域,尤其是一种快速、高灵敏性检测和定量酸奶中动物双歧杆菌bb-12的方法。
背景技术:
动物双歧杆菌乳双歧亚种(动物双歧杆菌bb-12)是世界上临床研究最为充分的双歧杆菌菌株,其保健作用已经在胃肠健康和免疫功能的许多临床研究中得到了验证。目前已有大量的体外实验确定了动物双歧杆菌bb-12的菌株特点和机理。在体内,动物双歧杆菌bb-12表现出了极好的酸胆汁耐受性,它含有胆盐水解酶,并具有很强的粘附性、病原菌抑制性、免疫屏障功能增强性。对于包括足月新生儿在内的健康人群,动物双歧杆菌bb-12作为食品中的膳食成分和膳食补充剂可认为是安全的。有研究表明该菌对婴幼儿有促进肠道菌群平衡、提高抵抗力、降低特应性湿疹的症状及预防湿疹等过敏性疾病、降低呼吸道感染率、促进生长发育、促进婴儿免疫系统成熟、预防腹泻及减少腹泻的发病率、减少便秘发生率、防止轮状病毒感染、降低坏死性小肠结肠炎发生率、降低早期急性中耳炎及复发性呼吸道感染的风险、影响体重、益于牙齿健康等作用。对孕妇具有降低妊娠糖尿病的患病风险、有助胎儿健康、降低小儿特应性皮炎发生率、降低妊娠并发症相关炎因子、预防或控制肥胖、调节葡萄糖水平等作用。对普通人群有助于肠道健康、调节免疫、降低唾液中变形链球菌水平及有助于口腔健康、促进抗生素治疗后有益菌的再次定植等作用。
实时荧光定量pcr技术通过荧光信号分子的不断累积而实现对pcr反应全程进行实时监测,利用已知标准品得到标准曲线再对待测样品进行检测分析。每个模板的起始拷贝数对数与其ct值存在线性关系,起始拷贝数越多则ct值越小。使用荧光定量pcr仪检测已知标准品可得到标准曲线,只要获得待测样品的ct值,即可通过标准曲线公式来计算出该样品的起始拷贝数得出结果。因实时荧光定量pcr与传统定量技术相比较,具有特异灵敏、重复性好、操作简便、定量准确,以及自动化程度较高和对样品的污染小等优点,基于实时荧光定量pcr检测的优越之处。
现有检测细菌数量的方法有:计数器测定法、平板菌落计数法、比浊法、测定细胞重量法和颜色改变单位法等。平板菌落计数法是根据每个活的细菌能长出一个菌落的原理设计的。此法是目前国际上许多国家所采用的方法,限用于形成菌落的微生物,广泛应用于水、牛奶、食物、药品等各种材料的细菌检验,是最常用的活菌计数法。与本发明相比,该方法易受温度、实验环境、人员操作等的影响,平板菌落计数法耗时较长,一般需要3-4天才能得出结果。除此之外,计数器测定法即用血细胞计数器进行计数,该方法操作简便,可立即对纯菌液的细菌个数测定得出结果;电子计数器计数法,该法测定结果较准确,但它只识别颗粒大小,而不能区分是否为细菌;比浊法是根据菌悬液的透光量间接地测定细菌的数量,此法简便快捷,但只能检测含有大量细菌的悬浮液,得出相对的细菌数目,对颜色太深的样品,不能用此法测定;测定细胞重量法,此法适于菌体浓度较高的样品;颜色改变单位法,这种方法通常用于很小的且用一般的比浊法无法计数的微生物,比如支原体等,它是以微生物在培养基中的代谢活力为指标来计数微生物的相对含量的。
与本发明相比,上述方法的检测更多的针对菌液,无法应用到酸奶制品中进行细菌计数的测定,因酸奶中含有大量蛋白质和脂质物质,会极大影响上述方法测定结果的准确性。
通过检索,尚未发现与本发明专利申请相关的专利公开文献。
技术实现要素:
本发明的目的在于鉴于目前动物双歧杆菌bb-12对人体的健康作用以及所拥有的经济效益和前景,克服现有技术的不足之处,提供一种快速、高灵敏性检测和定量酸奶中动物双歧杆菌bb-12的方法。
本发明解决其技术问题所采用的技术方案是:
一种taqman-mgb探针,所述探针为seqno.2、seqno.3、seqno.4。
一种快速、高灵敏性检测和定量酸奶中动物双歧杆菌bb-12的方法,所述方法是通过实时荧光定量pcr技术来实现对动物双歧杆菌bb-12的检测及定量;
具体步骤为:设计动物双歧杆菌bb-12的特异性探针及引物,探针为seqno.2、seqno.3、seqno.4,引物为seqno.5、seqno.6,构建目标序列的过表达载体,再将构建成功的载体导入dh5α感受态细胞,提取质粒进行标准曲线的构建,实现快速、高灵敏性检测和定量酸奶中动物双歧杆菌bb-12;
其中,所述目标序列存在于动物双歧杆菌bb-12的16srrna保守序列上。
而且,所述实时荧光定量pcr技术为探针法。
而且,所述方法还包括对探针及引物有效性判定的手段。
而且,所述对探针及引物有效性判定的手段包括pcr技术、琼脂糖凝胶电泳技术。
而且,具体步骤如下:
第一步、动物双歧杆菌bb-12特异性探针及引物设计:
使用ncbihttps://www.ncbi.nlm.nih.gov/数据库、primerexpress3.0软件比对及设计动物双歧杆菌bb-12特异性mgb探针及引物、标准品质粒特异性引物,动物双歧杆菌bb-12的16srrna碱基序列为seqno.1,动物双歧杆菌bb-12特异性mgb探针为seqno.2、seqno.3、seqno.4,构建载体的引物为seqno.5、seqno.6;
第二步、载体构建、标准曲线的建立
⑴动物双歧杆菌bb-12的培养及dna提取
将进行增菌培养,预先将超净工作台用紫外灯照射,取动物双歧杆菌bb-12菌液加入到莫匹罗星锂盐和半胱氨酸盐酸盐改良mrs液体培养(该培养基是本领域内公知的。购自海博生物产品编号:hb0384-11)中,置于200rpm/min、37℃中震荡过夜培养12~16h;
将增菌后的细菌以分区划线的方法接种于莫匹罗星锂盐和半胱氨酸盐酸盐改良mrs固体平皿中,置于37℃中倒置培养12~16h;挑单个菌落,接种于装有莫匹罗星锂盐和半胱氨酸盐酸盐改良mrs液体培养基中,于200rpm/min、37℃中震荡过夜培养12~16h;
提取试验菌株dna;
⑵普通pcr扩增
在20ul体系中加入动物双歧杆菌bb-12的载体构建特异性引物,pcr扩增反应体系如下:
pcr扩增反应程序如下:
35个循环;
⑶琼脂糖凝胶电泳实验
称取琼脂糖粉末0.4g,量取1×tae溶液20ml,混合并加热至完全融化,澄清且无浑浊;用移液枪吸取核酸染料2μl,摇匀后沿板壁倒入插好梳子的电泳板槽中,待琼脂糖凝胶凝固;拔出梳子,取出琼脂糖凝胶放进含有1×tae电泳液的电泳槽中,在胶孔中用移液枪加样10μl,调节电压100v和电流200ma进行电泳实验;电泳时间20~30min,将琼脂糖凝胶置于凝胶成像仪中进行成像,观察并记录结果;
⑷动物双歧杆菌bb-12标准品载体构建
对琼脂糖凝胶进行目的基因片段的回收提纯;
载体构建具体方法如下:
①在200μl离心管中配置载体连接体系,反应总体系为10μl,体系组分及用量如下
②16℃反应,过夜连接;
③将连接液全部加至50μldh5α感受态细胞中,立即冰浴放置30min;
④立即在42℃水浴锅中热激90s,立即冰浴放置1-2min;
⑤加入500μl4℃融化的soc培养基,37℃、160rpm/min震荡培养1h;
⑥室温下4000rpm/min离心1min,弃掉部分上清,吹打重悬管底沉淀,用涂布棒均匀地涂平板;
⑦将加入载体的dh5α感受态细胞在含有100mg/mlamp+的lb固体琼脂平板上37℃过夜培养,培养不低于17h,待形成单菌落;
⑧挑选菌落,运用pcr方法鉴定插入片段的长度大小,检测目的基因是否构建完全;
⑸质粒提取
对待测样品菌液进行质粒dna的提取;
⑹实时荧光定量标准曲线的建立
将提取的质粒进行10倍梯度稀释,选取100~106梯度的标准品进行荧光pcr扩增,绘制标准曲线;
⑺酸奶样品中动物双歧杆菌bb-12的dna的提取;
⑻实时荧光定量pcr检测动物双歧杆菌bb-12,即得。
本发明取得的优点和积极效果为:
1、本发明所设计的taqman-mgb探针灵敏度高、特异性好、检测所用时间较中华人民共和国国家标准(gb4789.35-2016)更短,因taqman-mgb探针是在基因领域对细菌个数进行检测,因此与中华人民共和国国家标准(gb4789.35-2016)相比不受外在环境及人为认知的影响,检测效果更精确,灵敏度更高。
2、本发明设计动物双歧杆菌bb-12的16srrna保守序列的mgb探针,利用实时荧光定量pcr技术(探针法),可以为酸奶中对动物双歧杆菌bb-12的检测和定量提供快速、灵敏、高效的方法,对探索奶制品中细菌的检测和定量提供启示。
3、本发明方法通过实时荧光定量pcr技术(探针法)来实现对动物双歧杆菌bb-12的检测及定量,该方法快速、灵敏和特异,为酸奶中对动物双歧杆菌bb-12的检测和定量提供技术手段,对探索奶制品中细菌的检测和定量提供启示,为农业食品检测及定量的研究提供启示。
4、本发明可以在酸奶制品中准确定量细菌,实验方法具有重复性好、操作简便、耗时短、定量准确,以及自动化程度较高和对样品的污染小等优点。除此之外,本发明的mgb探针与普通探针相比具有更强的杂交能力、稳定性更强、荧光背景值更低、灵敏度高。且本发明探针的特异性更强,荧光强度更高。
5、本发明所使用taqman探针法原理可以是:探针完整时,报告基团发射的荧光信号被淬灭基团吸收;pcr扩增时,taq酶的5’-3’外切酶活性将探针酶切降解,使报告荧光基团和淬灭荧光基团分离,从而荧光监测系统可接收到荧光信号,即每扩增一条dna链,就有一个荧光分子形成,实现了荧光信号的累积与pcr产物的形成完全同步。将标记有荧光素的taqman探针与模板dna混合后,完成高温变性、低温复性、适温延伸的热循环,并遵守聚合酶链反应规律,与模板dna互补配对的taqman探针被切断,荧光素游离于反应体系中,在特定光激发下发出荧光,随着循环次数的增加,被扩增的目的基因片段呈指数规律增长,通过实时检测与之对应的随扩增而变化荧光信号强度,求得ct值,同时利用数个已知模板浓度的标准品作对照,即可得出待测标本目的基因的拷贝数。
本发明设计的新型taqman-mgb探针使该技术既可进行基因定量分析,又可分析基因突变(snp),taqman-mgb探针与普通探针相比具有在普通探针基础上mgb修饰的探针,它的序列更短,杂交能力更强,更稳定,且taqman-mgb探针分子结合到dna螺旋小沟,通过稳定mgb探针/模板提高杂交稳定性,使短至13个碱基的探针获得高错配区分分辨能力。mgb探针包括一个不发荧光的淬灭集团(nfq),极大消除传统淬灭集团产生的背景荧光,提高信噪比,从而提高检验灵敏性,有望成为基因诊断和个体化用药分析的首选技术平台。
实时荧光定量pcr技术有效地解决了传统定量只能终点检测的局限,实现了每一轮循环均检测一次荧光信号的强度,并记录在电脑软件之中,通过对每个样品ct值的计算,根据标准曲线获得定量结果。本发明设计使用taqman-mgb探针成功对酸奶中动物双歧杆菌bb-12进行检测及定量,实验结果与本实验所测定的样品中的数量与报道的酸奶中的动物双歧杆菌bb-12数量基本一致,证明此测定方法有效可行。
附图说明
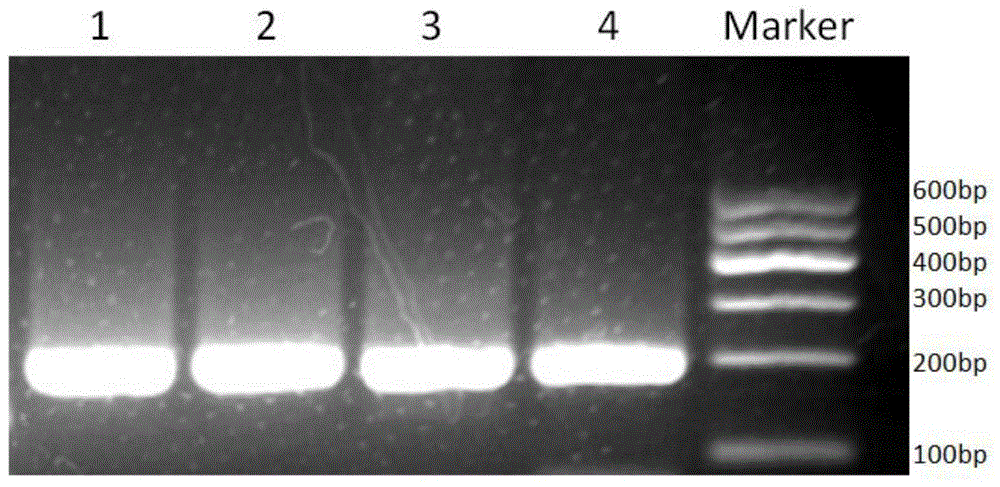
图1为本发明中载体构建引物pcr后的琼脂糖凝胶电泳图;其中,1-4代表4个生物学重复;
图2为本发明中构建载体进行菌液pcr的琼脂糖凝胶电泳图;其中,1-2代表2个生物学重复;
图3为本发明中利用设计探针及配套引物对动物双岐杆菌bb-12以及酸奶中含有的其他细菌进行的荧光定量pcr图,目的是验证所设计的引物特异性和可检出性;图中数字1代表动物双歧杆菌bb-12标准菌株提取dna扩增曲线;数字2和3是含有动物双歧杆菌bb-12的产品中提取的dna扩增曲线;数字4是指提取的大肠杆菌dna、不含动物双歧杆菌bb-12但含有其他酸奶添加菌的提取dna、婴儿双歧杆菌标准菌株提取dna、以及阴性对照(ddh2o)的扩增曲线;
图4为本发明中构建的载体提取质粒10倍梯度稀释作为标准品扩增曲线图;其中,选取100-106七个梯度;
图5为本发明中构建的标准曲线图;
图6为本发明中待测样品dna荧光定量pcr扩增曲线图。
具体实施方式
下面结合实施例,对本发明进一步说明,下属实施例是叙述性的,不是限定性的,不能以下述实施例来限定本发明的保护范围。
本发明中所使用的原料,如无特殊说明,均为常规市售产品,本发明中所使用的方法,如无特殊说明,均为本领域常规方法,本发明所用各物质质量均为常规使用质量。
一种taqman-mgb探针,所述探针为seqno.2、seqno.3、seqno.4。
一种快速、高灵敏性检测和定量酸奶中动物双歧杆菌bb-12的方法,所述方法是通过实时荧光定量pcr技术来实现对动物双歧杆菌bb-12的检测及定量;
具体步骤为:设计动物双歧杆菌bb-12的特异性探针及引物,探针为seqno.2、seqno.3、seqno.4,引物为seqno.5、seqno.6,构建目标序列的过表达载体,再将构建成功的载体导入dh5α感受态细胞,提取质粒进行标准曲线的构建,实现快速、高灵敏性检测和定量酸奶中动物双歧杆菌bb-12;
其中,所述目标序列存在于动物双歧杆菌bb-12的16srrna保守序列上。
较优地,所述实时荧光定量pcr技术为探针法。
较优地,所述方法还包括对探针及引物有效性判定的手段。
较优地,所述对探针及引物有效性判定的手段包括pcr技术、琼脂糖凝胶电泳技术。
较优地,具体步骤如下:
第一步、动物双歧杆菌bb-12特异性探针及引物设计:
使用ncbihttps://www.ncbi.nlm.nih.gov/数据库、primerexpress3.0软件比对及设计动物双歧杆菌bb-12特异性mgb探针及引物、标准品质粒特异性引物,动物双歧杆菌bb-12的16srrna碱基序列为seqno.1,动物双歧杆菌bb-12特异性mgb探针为seqno.2、seqno.3、seqno.4,构建载体的引物为seqno.5、seqno.6;
第二步、载体构建、标准曲线的建立
⑴动物双歧杆菌bb-12的培养及dna提取
将进行增菌培养,预先将超净工作台用紫外灯照射,取动物双歧杆菌bb-12菌液加入到莫匹罗星锂盐和半胱氨酸盐酸盐改良mrs液体培养(该培养基是本领域内公知的。购自海博生物产品编号:hb0384-11)中,置于200rpm/min、37℃中震荡过夜培养12~16h;
将增菌后的细菌以分区划线的方法接种于莫匹罗星锂盐和半胱氨酸盐酸盐改良mrs固体平皿中,置于37℃中倒置培养12~16h;挑单个菌落,接种于装有莫匹罗星锂盐和半胱氨酸盐酸盐改良mrs液体培养基中,于200rpm/min、37℃中震荡过夜培养12~16h;
提取试验菌株dna;
⑵普通pcr扩增
在20ul体系中加入动物双歧杆菌bb-12的载体构建特异性引物,pcr扩增反应体系如下:
pcr扩增反应程序如下:
35个循环;
⑶琼脂糖凝胶电泳实验
称取琼脂糖粉末0.4g,量取1×tae溶液20ml,混合并加热至完全融化,澄清且无浑浊;用移液枪吸取核酸染料2μl,摇匀后沿板壁倒入插好梳子的电泳板槽中,待琼脂糖凝胶凝固;拔出梳子,取出琼脂糖凝胶放进含有1×tae电泳液的电泳槽中,在胶孔中用移液枪加样10μl,调节电压100v和电流200ma进行电泳实验;电泳时间20~30min,将琼脂糖凝胶置于凝胶成像仪中进行成像,观察并记录结果;
⑷动物双歧杆菌bb-12标准品载体构建
对琼脂糖凝胶进行目的基因片段的回收提纯;
载体构建具体方法如下:
①在200μl离心管中配置载体连接体系,反应总体系为10μl,体系组分及用量如下
②16℃反应,过夜连接;
③将连接液全部加至50μldh5α感受态细胞中,立即冰浴放置30min;
④立即在42℃水浴锅中热激90s,立即冰浴放置1-2min;
⑤加入500μl4℃融化的soc培养基,37℃、160rpm/min震荡培养1h;
⑥室温下4000rpm/min离心1min,弃掉部分上清,吹打重悬管底沉淀,用涂布棒均匀地涂平板;
⑦将加入载体的dh5α感受态细胞在含有100mg/mlamp+的lb固体琼脂平板上37℃过夜培养,培养不低于17h,待形成单菌落;
⑧挑选菌落,运用pcr方法鉴定插入片段的长度大小,检测目的基因是否构建完全;
⑸质粒提取
对待测样品菌液进行质粒dna的提取;
⑹实时荧光定量标准曲线的建立
将提取的质粒进行10倍梯度稀释,选取100~106梯度的标准品进行荧光pcr扩增,绘制标准曲线;
⑺酸奶样品中动物双歧杆菌bb-12的dna的提取;
⑻实时荧光定量pcr检测动物双歧杆菌bb-12,即得。
本发明的一种设计思路是:
设计动物双歧杆菌bb-12的特异性探针及引物,构建目标序列的过表达载体,再将构建成功的载体导入dh5α感受态细胞,提取质粒进行标准曲线的构建,将待测样品与标准品质粒一同进行实时荧光定量pcr,得到标准曲线公式,计算得出样本拷贝数。实现快速、高灵敏性检测和定量酸奶中动物双歧杆菌bb-12。
具体的,相关制备及检测如下:
一种快速、高灵敏性检测和定量酸奶中动物双歧杆菌bb-12的方法,包括以下步骤:
第一步、动物双歧杆菌bb-12特异性探针及引物设计:
本发明使用ncbi(https://www.ncbi.nlm.nih.gov/)数据库、primerexpress3.0软件比对及设计动物双歧杆菌bb-12特异性mgb探针及引物、标准品质粒特异性引物。
具体步骤是:
(1)动物双歧杆菌bb-12特异性mgb探针及引物、标准品质粒特异性引物的设计。
动物双歧杆菌bb-12的16srrna碱基序列(1459bp):
actanagaacgctggcggcgtgcttaacacatgcaagtcgaacgggatccctggcagctt
gctgtcggggtgagagtggcgaacgggtgagtaatgcgtgaccaacctgccctgtgcacc
ggaatagctcctggaaacgggtggtaataccggatgctccgctccatcgcatggtggggt
gggaaatgcttttgcggcatgggatggggtcgcgtcctatcagcttgttggcggggtgat
ggcccaccaaggcgttgacgggtagccggcctgagagggtgacccggccacattgggact
gagatacggcccagactcctacgggaggcagcagtggggaatattgcacaatgggcgcaa
gcctgatgcagcgacgccgcgtgcgggatggaggccttcgggttgtaaaccgcttttgtt
caagggcaaggcacggtttcggccgtgttgagtggattgttcgaataagcaccggctaac
tacgtgccagcagccgcggtaatacgtagggtgcgagcgttatccggatttattgggcgt
aaagggctcgtaggcggttcgtcgcgtccggtgtgaaagtccatcgcctaacggtggatc
tgcgccgggtacgggcgggctggagtgcggtaggggagactggaattcccggtgtaacgg
tggaatgtgtagatatcgggaagaacaccaatggcgaaggcaggtctctgggccgtcact
gacgctgaggagcgaaagcgtggggagcgaacaggattagataccctggtagtccacgcc
gtaaacggtggatgctggatgtggggccctttccacgggtcccgtgtcggagccaacgcg
ttaagcatcccgcctggggagtacggccgcaaggctaaaactcaaagaaattgacggggg
cccgcacaagcggcggagcatgcggattaattcgatgcaacgcgaagaaccttacctggg
cttgacatgtgccggatcgccgtggagacacggtttcccttcggggccggttcacaggtg
gtgcatggtcgtcgtcagctcgtgtcgtgagatgttgggttaagtcccgcaacgagcgca
accctcgccgcatgttgccagcgggtgatgccgggaactcatgtgggaccgccggggtca
actcggaggaaggtggggatgacgtcagatcatcatgccccttacgtccagggcttcacg
catgctacaatggccggtacaacgcggtgcgacacggtgacgtggggcggatcgctgaaa
accggtctcagttcggatcgcagtctgcaactcgactgcgtgaaggcggagtcgctagta
atcgcggatcagcaacgccgcggtgaatgcgttcccgggccttgtacacaccgcccgtca
agtcatgaaagtgggtagcacccgaagccggtggcccgacccttgtggggggagccgtct
aaggtgagactcgtgattg
发明设计探针(命名为:bif-16mgb-tm、bif-16mgb-f/r)及构建载体的引物(命名为:bif-16smgbzt-f/r)如表1所示:
表1特异性引物及目的片段大小
第二步、载体构建、标准曲线的建立
(1)动物双歧杆菌bb-12的培养及dna提取。
将进行增菌培养,预先将超净工作台用紫外灯照射(30min左右),从ep管中取10μl菌液加入到10ml莫匹罗星锂盐和半胱氨酸盐酸盐改良mrs液体培养试管中,置于摇床(设置200rpm/min、37℃)中震荡过夜培养12~16h。
将增菌后的细菌以分区划线(四区划线)的方法接种于莫匹罗星锂盐和半胱氨酸盐酸盐改良mrs固体平皿中,置于温箱(设置37℃)中倒置培养12~16h。挑单个菌落,接种于装有莫匹罗星锂盐和半胱氨酸盐酸盐改良mrs液体培养基(约10ml)的试管中,于摇床(设置200rpm/min、37℃)中震荡过夜培养12~16h。
采用omegae.z.n.abacterildnakit(d3350-00)试剂盒提取试验菌株dna,具体步骤见说明书。
(2)普通pcr扩增
按表1在20ul体系中加入动物双歧杆菌bb-12的载体构建特异性引物,按照表2的体系及表3的pcr扩增反应程序(35个循环)。
表2pcr扩增反应体系
表3pcr扩增反应程序(35cycle)
(3)琼脂糖凝胶电泳实验
称取琼脂糖粉末0.4g,量取1×tae溶液20ml,混合并加热至完全融化(澄清且无浑浊)。用移液枪吸取核酸染料2μl,摇匀后沿板壁缓慢倒入插好梳子的电泳板槽中,待琼脂糖凝胶凝固。轻轻拔出梳子,取出琼脂糖凝胶放进含有1×tae电泳液(现配现用)的电泳槽中,在胶孔中用移液枪加样10μl,调节电压(设定100v)和电流(设定200ma)进行电泳实验。电泳时间约20~30min,将琼脂糖凝胶置于凝胶成像仪中进行成像,观察并记录结果。
(4)动物双歧杆菌bb-12标准品载体构建。
应用琼脂糖凝胶dna回收试剂盒(gelextractionkit型号:cw2302s)对琼脂糖凝胶进行目的基因片段的回收提纯。具体操作见琼脂糖凝胶dna回收试剂盒(gelextractionkit型号:cw2302s)试剂盒说明书。载体构建结果如图1所示,从图1可以看出载体插入片段产物是206bp,与设计的载体构建引物序列产物长度相一致,且特异性高。构建载体进行菌液pcr鉴定,对产物进行琼脂糖凝胶电泳,结果如图2所示,从图2可以看出产物片段是106bp,与设计的taqman-mgb探针产物长度相一致。
载体构建具体方法如下:
1、在200μl离心管中配置载体连接体系,反应总体系为10μl,体系组分及用量如表4所示。
表4载体连接体系
2、16℃反应,过夜连接。
3、将连接液全部加至50μldh5α感受态细胞中,立即冰浴放置30min。
注:若dh5α感受态细胞需分装,用预冷过的1.5ml离心管。
4、立即在42℃水浴锅中热激90s,立即冰浴放置1-2min。
5、加入500μlsoc培养基(4℃融化),放于摇床(设置37℃、160rpm/min)震荡培养1h。
6、室温下用离心机(设置4000rpm/min)离心1min,弃掉部分上清(离心管中约留100μl液体),轻轻吹打重悬管底沉淀,用涂布棒轻轻均匀地涂平板。
7、将加入载体的dh5α感受态细胞在含有amp+(100mg/ml)的lb固体琼脂平板上37℃过夜培养(不低于17h),待形成单菌落。
8、挑选适合的菌落,运用pcr方法鉴定插入片段的长度大小,检测目的基因是否构建完全。
(5)质粒提取。
应用质粒dna小量提取试剂盒(cw2105s,康为世纪)对待测样品菌液进行质粒dna的提取,具体操作见说明书。
(6)实时荧光定量标准曲线的建立。
将提取的质粒进行10倍梯度稀释,选取100~106梯度的标准品进行荧光pcr扩增,绘制标准曲线,结果如图4、图5所示。从图4、图5可以看出该标准曲线构建成功,r2可达0.9999,可信度极高。
第三步、酸奶样品dna的提取
(1)酸奶中细菌dna的提取,具体操作如下:
1、取45ml样品,依次使用4000rpm/min、6000rpm/min、8000rpm/min离心5min,取上清液全部加入同一个离心管中。
2、12000rpm/min离心10min,弃上清液。
3、加2mlctab裂解液和40ul溶菌酶(50mg/ml),35℃,孵育30min。
4、加40ul蛋白酶k(20mg/ml),65℃,孵育1h,13000rpm/min离心1min,取初沉淀。
5、加10ulnacl(1.2mol/ml)溶解初沉淀。
6、加入10ul氯仿震荡20s,1000xg离心1min,取上清。
7、加入0.8倍异丙醇沉淀30min,12000rpm/min离心10min。
8、加70%乙醇,使dna沉淀飘起,除乙醇,自然风干。
9、加适量te缓冲液溶解dna。
(2)实时荧光定量pcr检测动物双歧杆菌bb-12。
将标准品和待测酸奶提取dna样品共同进行荧光定量pcr扩增,在20μl体系中按表5加入各种成分后进行荧光定量pcr检测。扩增程序如表6(40个循环)所示。
表5荧光定量pcr反应体系
表6pcr扩增反应程序
结果得到标准曲线公式:y=-3.8511x+47.02r2=0.9999
第四步、数据统计分析
将荧光定量pcr得到的结果进行统计学计算,得到结果如图3、图6和表7所示。本实验所测定的样品中动物双歧杆菌bb-12的数量与报道的酸奶中的数量基本一致。
表7同一产品不同瓶中动物双歧杆菌bb-12的数量(copies/ml)
注:以上酸奶均为目前在售品牌的酸奶,将其简称为1、2、3。
由上表可知,不同瓶中的酸奶中,动物双歧杆菌bb-12的数量存在一定差异,分析原因是由于酸奶样品提取dna的方法及样品中含有大量蛋白质、脂肪等其他物质干扰造成dna提取有损耗。但本实验所测定的样品中动物双歧杆菌bb-12的数量与报道的酸奶中的数量基本一致(益生菌添加量≥106cfu)。
尽管为说明目的公开了本发明的实施例,但是本领域的技术人员可以理解:在不脱离本发明及所附权利要求的精神和范围内,各种替换、变化和修改都是可能的,因此,本发明的范围不局限于实施例所公开的内容。
序列表
<110>天津农学院
<120>一种快速、高灵敏性检测和定量酸奶中动物双歧杆菌bb-12的方法
<160>6
<170>siposequencelisting1.0
<210>1
<211>1459
<212>dna/rna
<213>动物双歧杆菌bb-12的16srrna碱基序列(unknown)
<400>1
actanagaacgctggcggcgtgcttaacacatgcaagtcgaacgggatccctggcagctt60
gctgtcggggtgagagtggcgaacgggtgagtaatgcgtgaccaacctgccctgtgcacc120
ggaatagctcctggaaacgggtggtaataccggatgctccgctccatcgcatggtggggt180
gggaaatgcttttgcggcatgggatggggtcgcgtcctatcagcttgttggcggggtgat240
ggcccaccaaggcgttgacgggtagccggcctgagagggtgacccggccacattgggact300
gagatacggcccagactcctacgggaggcagcagtggggaatattgcacaatgggcgcaa360
gcctgatgcagcgacgccgcgtgcgggatggaggccttcgggttgtaaaccgcttttgtt420
caagggcaaggcacggtttcggccgtgttgagtggattgttcgaataagcaccggctaac480
tacgtgccagcagccgcggtaatacgtagggtgcgagcgttatccggatttattgggcgt540
aaagggctcgtaggcggttcgtcgcgtccggtgtgaaagtccatcgcctaacggtggatc600
tgcgccgggtacgggcgggctggagtgcggtaggggagactggaattcccggtgtaacgg660
tggaatgtgtagatatcgggaagaacaccaatggcgaaggcaggtctctgggccgtcact720
gacgctgaggagcgaaagcgtggggagcgaacaggattagataccctggtagtccacgcc780
gtaaacggtggatgctggatgtggggccctttccacgggtcccgtgtcggagccaacgcg840
ttaagcatcccgcctggggagtacggccgcaaggctaaaactcaaagaaattgacggggg900
cccgcacaagcggcggagcatgcggattaattcgatgcaacgcgaagaaccttacctggg960
cttgacatgtgccggatcgccgtggagacacggtttcccttcggggccggttcacaggtg1020
gtgcatggtcgtcgtcagctcgtgtcgtgagatgttgggttaagtcccgcaacgagcgca1080
accctcgccgcatgttgccagcgggtgatgccgggaactcatgtgggaccgccggggtca1140
actcggaggaaggtggggatgacgtcagatcatcatgccccttacgtccagggcttcacg1200
catgctacaatggccggtacaacgcggtgcgacacggtgacgtggggcggatcgctgaaa1260
accggtctcagttcggatcgcagtctgcaactcgactgcgtgaaggcggagtcgctagta1320
atcgcggatcagcaacgccgcggtgaatgcgttcccgggccttgtacacaccgcccgtca1380
agtcatgaaagtgggtagcacccgaagccggtggcccgacccttgtggggggagccgtct1440
aaggtgagactcgtgattg1459
<210>2
<211>20
<212>dna/rna
<213>bif-16mgb-f(unknown)
<400>2
atagctcctggaaacgggtg20
<210>3
<211>20
<212>dna/rna
<213>bif-16mgb-r(unknown)
<400>3
aacaagctgataggacgcga20
<210>4
<211>20
<212>dna/rna
<213>bif-16mgb-tm(unknown)
<400>4
amtccgctccatcgcatmgb20
<210>5
<211>20
<212>dna/rna
<213>bif-16smgbzt-f(unknown)
<400>5
acatgcaagtcgaacgggat20
<210>6
<211>20
<212>dna/rna
<213>bif-16smgbzt-r(unknown)
<400>6
ccgccaacaagctgatagga20
- 还没有人留言评论。精彩留言会获得点赞!