preS1抗体、乙型肝炎病毒前S1抗体酶免检测试剂盒、制备方法、使用方法与流程
本发明涉及生物工程
技术领域:
,尤其涉及一种pres1抗体、乙型肝炎病毒前s1抗体免检测试剂盒、制备方法、使用方法。
背景技术:
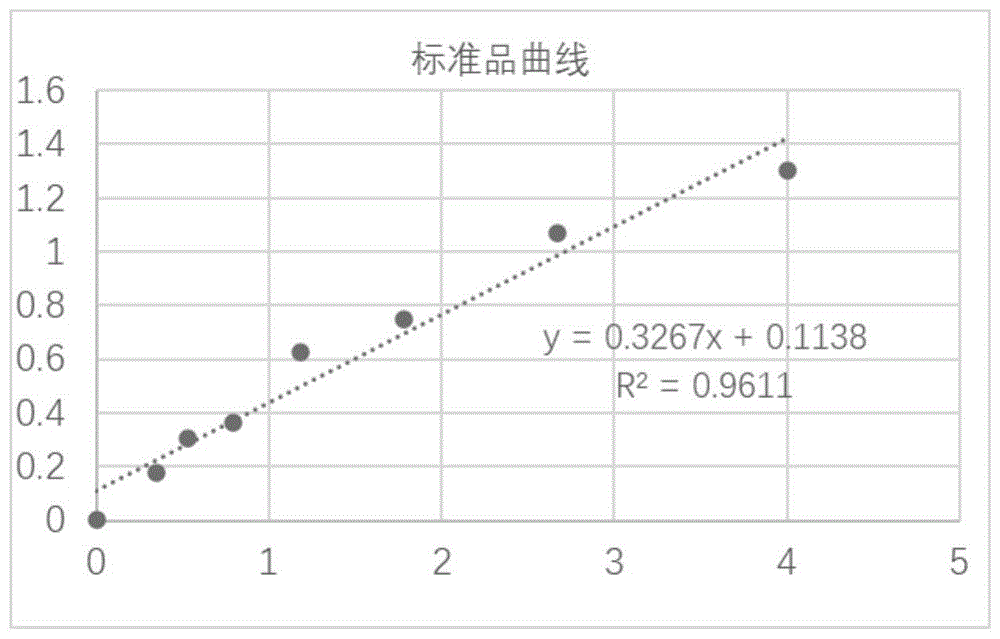
:乙型肝炎病毒前s1存在于乙肝病毒表面抗原的大蛋白中,是乙肝早期诊断和病毒复制的重要指标,前s1抗体可以阻止病毒进入肝细胞,干扰病毒的复制,急性乙肝顺利康复的患者一般都有pres1抗体,而慢性化发展的急性乙肝前s1抗体的检出率较低,乙型肝炎病毒前s1抗体可以作为乙肝早期诊断和判断患者治疗及预后的标记物。但是,现阶段乙肝的诊断主要依靠血清标志物(两对半)检测,pres1抗体检测试剂缺乏,至今国内没有pres1抗体定量检测的试剂盒,乙肝预后判断主要依据患者的dna载量来判定。技术实现要素:为了解决上述技术问题,本发明提供了一种pres1抗体、乙型肝炎病毒前s1抗体酶免检测试剂盒、制备方法、使用方法。根据本发明的第一个方面,提供了一种pres1抗体,pres1抗体包括重链可变区和轻链可变区,pres1抗体的轻链可变区的编码氨基酸的核酸序列如seqidno:1所示,pres1抗体的重链可变区的编码氨基酸的核酸序列如seqidno:2所示。根据本发明的第二个方面,提供了一种制备pres1抗体的方法,方法包括:(a)选择pres1抗体片段,pres1抗体片段的轻链可变区的氨基酸序列如seqidno:3所示,pres1抗体的重链可变区的氨基酸序列如seqidno:4所示;(b)将步骤a中的pres1抗体片段的氨基酸序列转译为密码子优化得到的编码pres1抗体的核酸序列;(c)将优化后的编码pres1抗体的核酸序列进行基因合成,在优化后的编码pres1抗体的核酸序列两端分别连接限制性酶切位点ecori和hindiii,合成得到轻链可变区如seqidno:1所示、重链可变区如seqidno:2所示的核酸序列;(d)将步骤c得到的核酸序列分别连入pcdna3.1真核表达载体上,将pcdna3.1真核表达载体转染到人胚肾细胞细胞中培养,收集细胞上清液,将细胞上清液proteina纯化后得到获得pres1抗体。根据本发明的第三个方面,提供了一种乙型肝炎病毒前s1抗体酶免检测试剂盒,包括:pres1抗原包被酶标反应板、样品稀释液、m×浓缩洗涤液、hrp酶标抗人二抗、tmb底物反应液、终止液以及pres1抗体系列梯度标准品;pres1抗原的核酸序列如seqidno:3所示;pres1抗体包括重链可变区和轻链可变区;pres1抗体的轻链可变区的核酸序列如seqidno:1所示;pres1抗体的重链可变区的核酸序列如seqidno:2所示。可选择地,pres1抗原包被酶标反应板的每个反应孔中封闭包被有第一预定体积的pres1蛋白抗原包被液;pres1蛋白抗原包被液为磷酸换缓冲液稀释pres1蛋白抗原得到的第一预定浓度的pres1蛋白抗原溶液;封闭液为含有羊血清、tween-20、proclin300的磷酸盐缓冲液。可选择地,pres1抗体系列梯度标准品是以pres1抗体缓冲液为溶剂,配制的不同浓度梯度的pres1抗体标准品;其中,pres1抗体缓冲液按体积分数计包括7%~12%羊血清、0.1%~0.4%tween-20、0.05%~0.3%proclin300、余量为磷酸盐缓冲液。可选择地,样品稀释液按体积分数包括7%~12%羊血清、1%-8%nacl、0.1%~0.4%tween-20、0.05%~0.3%proclin300的磷酸盐缓冲液;m×浓缩洗涤液为按体积分数包括m×0.1%~0.5%tween-20的磷酸盐缓冲液;底物反应液为3,3’,5,5’-四甲基联苯胺溶液;终止液为浓度为1~3mol/l的硫酸溶液。根据本发明的第四个方面,提供了一种乙型肝炎病毒前s1抗体酶免检测试剂盒的制备方法,包括以下步骤:s1用磷酸盐缓冲液稀释pres1抗原得到pres1抗原包被液,将pres1抗原包被液注入到酶标反应板的反应孔中包被,包被完毕后用封闭液封闭酶标反应板的反应孔;s2将羊血清、nacl、tween-20、proclin300加入到磷酸盐缓冲液中配制成样品稀释液,装瓶贴标签,按体积分数计样品稀释液包括7%~12%羊血清、1%-8%nacl、0.1%~0.4%tween-20、0.05%~0.3%proclin300;s3将tween-20加入到m×磷酸缓冲液中充分溶解得到tween-20体积分数为m×0.05%的m×浓缩洗涤液,装瓶贴标签;s4用二抗稀释液将hrp标记的抗人二抗稀释成浓度为0.01-2ug/ml的hrp酶标抗人二抗溶液,装瓶贴标签;按体积分数计,二抗稀释液包括7%~12%羊血清、0.1%~0.4%tween-20、0.05%~0.3%proclin300,余量为磷酸缓冲液;s5将3,3’,5,5’-四甲基联苯胺溶液,装瓶贴标签;s6用双蒸水将浓硫酸稀释成浓度1~3mol/l的稀硫酸作为终止液,装瓶贴标签;s7配制pres1抗体标准品缓冲液,向磷酸盐缓冲液中加入羊血清、tween-20、proclin300,配制得到按体积分数计7%~12%羊血清、0.1%~0.4%tween-20、0.05%~0.3%proclin300的pres1抗体缓冲液,用pres1抗体缓冲液稀释将pres1抗体稀释成n个不同浓度梯度的pres1抗体稀释液,n个不同浓度梯度的pres1抗体稀释液分别装瓶贴标签作为pres1抗体系列浓度梯度;将pres1抗原包被酶标反应板、样品稀释液、洗涤液、hrp酶标抗人二抗、底物反应液、终止液以及n瓶pres1抗体标准品组装成试剂盒。可选择地,步骤s1包括:s11用磷酸盐缓冲液稀释pres1抗原,将pres1抗原稀释成第一预定浓度的pres1抗原稀释液,将pres1抗原稀释液注入到酶标反应板的孔中,每个孔注入第一预定体积的抗原稀释液,将酶标反应板转移到第一预定温度环境中孵育第一预定时间;s12用封闭液封闭酶标反应板的反应孔,向每个反应孔中注入第二预定体积的封闭液封闭反应孔中的pres1抗原稀释液,将酶标反应板转移到第二预定温度环境中孵育第二预定时间。可选择地,在步骤s1之前进一步包括pres1抗原的制备步骤,具体如下:在pres序列数据库中选择如seqidno:6所示的氨基酸序列;氨基酸序转译为密码子进行优化,得到编码pres1抗原的核酸序列;在编码pres1抗原的核酸序列两端分别连接限制性酶切位点ndei和hindiii,合成得到如seqidno:5所示的核酸序列;将如seqidno:5所示的核酸序列连接到pet-28a原核表达载体中,再将pet-28a原核表达载体转导入大肠杆菌中完成pres1抗原的表达和纯化,得到pres1抗原。根据本发明的第五个方面,提供了一种乙型肝炎病毒前s1抗体酶免检测试剂盒的使用方法,包括以下步骤:(a)将m×浓缩洗涤液加入到(m-1)倍体积的蒸馏水中,获取1×洗涤液;(b)将样品稀释液加入到酶标板反应孔中,将pres1抗体系列梯度标准品和样品分别加入到含有样品稀释液的酶标反应板的反应孔中,将酶标反应板后转移到第三预定温度环境中,孵育第三预定时间;用1×洗涤液冲洗酶标反应板样品稀释液;(c)将hrp酶标抗人二抗加入到酶标反应板的反应孔中,将酶标反应板置于第四预定度环境中孵育第四预定时间;(d)将底物反应液100ul加入到酶标板的反应孔中,将酶标反应板置于第五预定温度环境中,孵育第五预定时间,pres1抗体标准品或样品稀释液与底物反应液显色孵育;(e)将终止液加入到显色孵育后的酶标反应板的反应孔中,向每个反应孔中加入终止液,终止底物反应;(g)用双波长的光波检测酶标板的每个反应孔的od值。其中,本申请发明人利用试剂盒检测41例儿童血清和经核酸检测hbv阴性的60例健康人群的血清,经检测od值均小于0.05,将试剂盒区分pres1抗体阴阳性的临界值定为0.15。当样本检测的od值小于0.15时,直接将样本判定为pres1抗体阴性;当样本的od值大于0.15时,需要根据标准品检测的od值标准曲线进行计算获得血清、血浆中pres1抗体的含量。本申请的乙型肝炎病毒前s1抗体酶免检测试剂盒,基于定量检测pres1抗体的技术,检测人体血清、血浆中pres1抗体的含量,用于发现早期乙肝感染者,同时还能用于评估患者感染后的预后能力和用药的治疗效果。附图说明构成本发明的一部分的附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:图1是本申请实施例中标准品的pres1抗体标准品系列浓度梯度-od值曲线。具体实施方式为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。需要说明的是,在不冲突的情况下,本申请中的实施例及实施例中的特征向量可以相互任意组合。目前,乙肝的诊断和预后评估主要依赖于乙肝血清标志物(两对半)和乙型肝炎病毒dna的检测。两对半检测难以做到提前发现hbv感染和病情发展及治疗效果进行判断,在判断患者的传染性及治疗效果评估方面有较大局限性。hbvdna的检测需要对病毒核酸提取、pcr体系配制、dna扩增等,步骤比较繁琐;检测价格高、过程较繁琐普及的难度较大。乙型肝炎病毒前s1存在于乙肝病毒表面抗原的大蛋白中,pres1蛋白作为病毒侵入肝细胞必须的识别蛋白,血清中pres1抗体含量,与hbv感染者血清中病毒复制密切相关,能够预判病人治疗的效果和预后状况。pres1血清中抗体含量是乙肝早期诊断和病毒复制的重要指标,前s1抗体可以阻止病毒进入肝细胞,干扰病毒的复制,急性乙肝顺利康复的患者一般都有pres1抗体,而慢性化发展的急性乙肝前s1抗体的检出率较低,可以作为乙肝早期诊断和判断患者治疗及预后的标记物。但是,现阶段国内还没有pres1抗体定量检测的成熟试剂盒。本申请提供了一个乙型肝炎病毒前s1抗体酶免检测试剂盒检测乙肝患者血清中pres1抗体的含量,用于发现早期hbv感染者,并评估病人感染hbv后的预后能力和病人用药的治疗效果。本申请提供了一种pres1抗体,pres1抗体包括重链可变区(vh)和轻链可变区(vl),pres1抗体的和轻链可变区(vl)的核酸序列如seqidno:1所示,重链可变区(vh)的核酸序列如seqidno:2所示。其中,本申请pres1抗体的制备方法,包括步骤如下:a)选择人源化的pres1抗体的氨基酸序列,pres1抗体轻链可变区(vl)的氨基酸序列如seqidno:3所示,重链可变区(vh)的核酸序列如seqidno:4所示。b)将步骤a的氨基酸序列转译为密码子并优化得到的编码pres1抗体的核酸序列;c)将步骤b中优化得到的编码pres1抗体的核酸序列两端分别连接限制性酶切位点ecori和hindiii,合成得到轻链可变区(vl)的核酸序列如seqidno:1所示、重链可变区(vh)的核酸序列如seqidno:2所示的核酸序列。d)将步骤c的的编码pres1抗体的核酸序列分别连入pcdna3.1真核表达载体上,将pcdna3.1真核表达载体转染到人胚肾细胞细胞中培养后收集细胞上清液,将细胞上清液proteina纯化后得到获得pres1抗体。作为一种示例,步骤d)中将pcdna3.1真核表达载体转染到人胚肾细胞细胞中培养6~10天后,收集细胞上清液。本申请的乙型肝炎病毒前s1抗体酶免检测试剂盒,包括:pres1抗原包被酶标反应板、样品稀释液、m×浓缩洗涤液、hrp酶标抗人二抗、底物反应液、终止液以及pres1抗体系列梯度标准品;pres1抗原包被酶标反应板、样品稀释液、洗涤液、hrp酶标抗人二抗、底物反应液、终止液以及pres1抗体系列梯度标准品共同组装在盒体中。pres1抗原的核酸序列如seqidno:5所示;pres1抗体包括重链可变区和轻链可变区,pres1抗体的轻链可变区(vl)的核酸序列如seqidno:1所示,重链可变区(vh)的核酸序列如seqidno:2所示。作为一种示例,pres1抗原包被酶标反应板的每个反应孔中容纳第一预定浓度的pres1抗原包被液第一预定体积,第一预定体积的pres1抗原包被液包被在封闭液中。作为一种示例,pres1抗原包被酶标反应板为48孔或96孔的酶标板,每个反应孔中容纳第一预定浓度的pres1抗原包被液第一预定体积。其中,第一预定体积为100~200ul、第一预定浓度为1~4ug/ml。例如,pres1抗原包被酶标反应板为48孔酶标板,每个反应孔封装有120ul~150ul的pres1抗原稀释液,pres1抗原稀释液的浓度为2~3ug/ml。作为一种示例,pres1抗体系列梯度标准品是以pres1抗体缓冲液为溶剂,配制的不同浓度梯度的pres1抗体系列梯度标准品。其中,pres1抗体缓冲液按体积分数计包括7%~12%羊血清、0.1%~0.4%tween-20、0.05%~0.3%proclin300、余量为磷酸盐缓冲液。其中,磷酸盐缓冲液为含0.05%tweentween-20的ph7.2-7.4的磷酸盐缓冲液,磷酸盐缓冲液的成分为8.0g/l氯化钠、0.2g/l氯化钾、2.9g/l磷酸氢二钠十二水合物和0.2g/l磷酸二氢钾的溶液。作为一种示例,样品稀释液按体积分数包括7%~12%羊血清、0.1%~0.4%tween-20、0.05%~0.3%proclin300,余量为磷酸盐缓冲液。作为一种示例,m×浓缩洗涤液为体积分数包括m×0.1%~0.5%tween-20的m×磷酸盐缓冲液,其中m×浓缩洗涤液为浓度为磷酸盐缓冲液的m倍的浓缩液。作为一种示例,底物反应液为3,3’,5,5’-四甲基联苯胺溶液。作为一种示例,终止液为浓度为1~3mol/l的硫酸溶液。本申请的乙型肝炎病毒前s1抗体酶免检测试剂盒的制备方法,包括以下步骤:s1用磷酸盐缓冲液稀释pres1抗原得到pres1抗原包被液,将pres1抗原包被注入到酶标反应板的反应孔中,进行包被,4℃孵育12-16h,孵育完后用1×洗涤液按300ul/孔洗涤酶标板三次,用200ul封闭液封闭酶标反应板的反应孔,1×洗涤液按300ul/孔洗涤酶标板三次后形成预包被酶标板,其中1×洗涤液为向m×浓缩洗涤液中加入m-1倍的水稀释得到。s2将羊血清、nacl、tween-20、proclin300加入到磷酸盐缓冲液中配制成样品稀释液,装瓶贴标签,按体积分数计样品稀释液包括7%~12%羊血清、0.1%~0.4%tween-20、0.05%~0.3%proclin300。s3将tween-20加入到m×浓缩缓冲液中充分溶解得到tween-20体积分数为0.05%×m的m×浓缩洗涤液,装瓶贴标签。s4将羊血清、tween-20、proclin300加入到磷酸盐缓冲液中配制成二抗稀释液,二抗稀释液按体积分数计包括7%~12%羊血清、0.1%~0.4%tween-20、0.05%~0.3%proclin300,余量为磷酸盐缓冲液;用二抗稀释液稀释hrp酶标抗人二抗得到浓度为0.01-2ug/m的hrp酶标抗人二抗溶液,将hrp酶标抗人二抗溶液装瓶贴标签。s5将3,3’,5,5’-四甲基联苯胺溶液,装瓶贴标签。s6用双蒸水将浓硫酸稀释成浓度1~3mol/l的稀硫酸作为终止液,装瓶贴标签。s7配制pres1抗体缓冲液,向磷酸盐缓冲液中加入羊血清、tween-20、proclin300,配制得到按体积分数计7%~12%羊血清、0.1%~0.4%tween-20、0.05%~0.3%proclin300的pres1抗体缓冲液,用pres1抗体缓冲液稀释pres1抗体将pres1抗体稀释成n个不同浓度梯度作为pres1抗体系列梯度标准品。将pres1抗原包被酶标反应板、样品稀释液、m×浓缩洗涤液、hrp酶标抗人二抗、底物反应液、终止液以及n瓶pres1抗体标准品组装成试剂盒。其中,n为5-7。作为一种示例,步骤s1包括:s11用磷酸盐缓冲液稀释pres1抗原,将pres1抗原稀释成第一预定浓度的pres1抗原包被液,将pres1抗原包被液注入到酶标反应板的孔中,每个孔注入第一预定体积的抗原稀释液,将酶标反应板转移到第一预定温度环境中孵育第一预定时间。s12用封闭液封闭酶标反应板的反应孔,向每个反应孔中注入第二预定体积的封闭液封闭反应孔中的pres1抗原稀释液,将酶标反应板转移到第二预定温度环境中孵育第二预定时间。作为一种示例,pres1抗原包被酶标反应板为48或96孔的酶标反应板;每个反应孔中容纳的第一预定体积为100~200ul的pres1抗原包被液;第一预定浓度为1~4ug/ml;第一预定温度为2~5℃;第一预定时间为6~8小时。例如,步骤s11中pres1抗原包被酶标反应板为48孔酶标板,每个反应孔封装有120ul~150ul的pres1抗原包被液,pres1抗原包被液的浓度为2~3ug/ml。将加入pres1抗原包被酶标反应板转移到2~8℃温度环境中孵育12~16小时。作为一种示例,第二预定体积为150~200ul;第二预定温度为30~40℃;第二预定时间为1~3小时。例如步骤2中向每个反应孔中注入150~200ul的封闭液封闭反应孔中的pres1抗原包被液,将酶标反应板转移到30~40℃温度环境中孵育1~3小时。作为一种示例,在步骤s1之前进一步包括pres1抗原的制备步骤,具体如下:在pres序列数据库中选择如seqidno:6所示的氨基酸序列;氨基酸序列转译为密码子进行优化得到编码pres1的核酸序列。在优化得到的编码pres1的核酸序列两端分别连接限制性酶切位点ndei和hindiii,合成得到如seqidno:5所示的核酸序列。将如seqidno:5所示的氨基酸序列连接到pet-28a原核表达载体中,再将pet-28a原核表达载体转导到大肠杆菌中完成pres1抗原的表达和纯化,得到pres1抗原。本申请的乙型肝炎病毒前s1抗体酶免检测试剂盒的使用方法,包括以下步骤:(a)洗涤液准备:将m×浓缩洗涤液加入m-1倍体积的双蒸水稀释洗涤液,获得1×洗涤液备用。(b)标准品和样品反应:将样品稀释液50-100ul加入到酶标反应孔中,pres1抗体系列梯度标准品和血清、血浆样品分别按照5-10ul加入到酶标反应板的反应孔中;轻轻振荡加入了样品稀释液和pres1抗体标准品的酶标反应板,将酶标反应板转移到第三预定温度环境中,孵育第三预定时间;用1×洗涤液冲洗酶标反应板,300-400ul/孔洗涤3-5次。(c)酶标二抗反应:将hrp酶标抗人二抗加入到酶标反应板的反应孔中,每个反应孔中加入浓度为0.01-2ug/ml的hrp酶标抗人二抗100ul,将酶标反应板置于第四预定度环境中孵育第四预定时间;用1×洗涤液冲洗酶标反应板,300-400ul/孔洗涤3-5次。(d)显色反应:将底物反应液100ul加入到酶标板的反应孔中,将酶标反应板置于第五预定温度环境中,孵育第五预定时间,pres1抗体标准品或样品稀释液与底物反应液显色孵育。(e)终止反应:将终止液加入到显色孵育后的酶标反应板的反应孔中,向每个反应孔中加入终止液,终止底物反应。(f)终止反应:用双波长的光波检测酶标板的每个反应孔的od值。作为一种示例,步骤b中,第三预定温度为25~38℃;第三预定时间为20-60min,将加入了样品稀释液和pres1抗体标准品的酶标反应板转移到37℃温度环境中,孵育60min。作为一种示例,步骤c中,第四预定温度为25~38℃;第四预定时间为20~40min。例如,将hrp酶标抗人二抗加入到pres1抗原包被酶标反应板的反应孔中,将pres1抗原包被酶标反应板置于25~38℃温度环境中孵育20~40min。作为一种示例,步骤d中,第五预定温度为25~38℃;第五预定时间为10~20min。例如,将底物反应液倒入到pres1抗原包被酶标反应板的每个反应孔均浸入在底物反应液中,将pres1抗原包被酶标反应板转移到35~38℃温度环境中孵育10~20min。作为一种示例,od值检测时,可在酶标仪中检测,用450nm参比630nm的双波长光波检测pres1抗原包被酶标反应板的每个反应孔的od值。作为一种示例,当样本检测的od值小于0.15时,直接将样本判定为pres1抗体阴性;当样本的od值大于0.15时,需要根据标准品检测的od值标准曲线进行计算获得血清、血浆中pres1抗体的含量。其中,利用试剂盒检测41例儿童血清和经核酸检测hbv阴性的60例健康人群的血清,经检测od值均小于0.05,将试剂盒区分pres1抗体阴阳性的cutoff值定为0.15。当样本检测的od值小于0.15时,直接将样本判定为pres1抗体阴性;当样本的od值大于0.15时,需要根据标准品检测的od值标准曲线进行计算获得血清、血浆中pres1抗体的含量。下面通过具体实施例进一步说明本申请的乙型肝炎病毒前s1抗体免检测试剂盒的制备方法和使用方法。实施例1乙型肝炎病毒前s1抗体免检测试剂盒的制备方法配制10×pbs缓冲液:氯化钠80g、磷酸氢二钠十二水合物29g、磷酸二氢钾2g、氯化钾2g加入到800ml去离子水中,搅拌至完全溶解,调整溶液的ph值至7.4±0.05,用0.22um滤膜过滤备用。配制1×pbs缓冲液:向10×pbs缓冲液中加入9倍体积的双蒸水稀释成1×pbs稀释液。配制pres1抗原稀释液:用1×pbs稀释液稀释pres1抗原得到抗原浓度为2ug/ml的pres1抗原稀释液。配制封闭液:向1×pbs缓冲液中依次加入羊血清、nacl、tween-20、proclin300配制成封闭液,封闭液中以体积分数计包括8%羊血清、0.25%tween-20、0.1%proclin300。制备pres1抗原包被酶标反应板:准备96孔的酶标反应板,按照120ul/孔向酶标反应板的反应孔中加入pres1抗原稀释液,4℃孵育过夜。洗涤酶标板:用1×pbs缓冲液重复洗涤pres1抗原包被酶标反应板,每个反应孔用350ul洗涤液冲洗3~5次。包被酶标板封:向pres1抗原包被酶标反应板的反应孔中滴入封闭液,每个反应孔滴入180ul封闭液,37℃孵育2h,进行酶标板的封闭。洗涤酶标板:用1×pbs缓冲液配制的0.05%tween-20洗涤液,每孔350ul洗涤液,重复洗涤4次,充分洗涤孵育后的酶标板。酶标板干燥及真空包装:洗涤后的pres1抗原包被酶标反应板放在湿度小于30%的温箱中,温度维持在22-28℃充分干燥12-16小时;干燥完毕后,放入锡箔袋中,真空包装机对锡箔袋抽真空,并进行封口包装,包装好的酶标板在2-8℃条件下可以保存一年。配制样品稀释液:将羊血清、nacl、tween-20、proclin300加入到1×pbs中配制成样品稀释液,样品稀释液按体积分数计包括8%羊血清,8%nacl,0.25%tween-20,0.1%proclin300,将样品稀释液按照12ml/瓶分装并贴上标签。配制洗涤液:向10×pbs缓冲液中加入tween-20配制得到按体积分数计包括0.1%tween-20的洗涤液,将洗涤液按照100ml/瓶分装并贴上标签。配制hrp酶标抗人二抗:向1×pbs缓冲液中加入羊血清、nacl、tween-20、proclin300配制成酶标二抗稀释液,用酶标二抗稀释液按照1:20万稀释hrp酶标抗人二抗至0.05ug/ml;其中,按体积分数计酶标二抗稀释液包括8%羊血清、0.25%tween-20、0.1%proclin300。准备底物反应液:底物反应液购自北京梅科万德生物公司(货号:1001)将3,3’,5,5’-四甲基联苯胺(tmb)溶液按照12ml/瓶分别分装和贴签。配制终止液:用双蒸水将浓硫酸稀释成浓度1~3mol/l的稀硫酸作为终止液,将终止液按照6ml/瓶分装并贴上标签。配制标准品:向1×pbs缓冲液中加入羊血清、nacl、tween-20、proclin300配制成pres1抗体缓冲液,用pres1抗体缓冲液稀释pres1抗体分别稀释获得pres1抗体浓度为4ug/ml、2.67ug/ml、1.78ug/ml、1.19ug/ml、0.79ug/ml、0.53ug/ml、0.35ug/ml的7个梯度的pres1抗体稀释液,将7个浓度的pres1抗体标准品按照200ul/支进行分装作为标准品,分别装瓶贴标签。其中,按体积分数计,pres1抗体缓冲液包括8%羊血清、0.25%tween-20、0.1%proclin300。试剂盒组装:将一板pres1抗原包被酶标反应板、一瓶样品稀释液、一瓶洗涤液、一瓶hrp酶标抗人二抗、一瓶底物反应液、一瓶终止液、7个浓度梯度的7瓶标准品组装成一个试剂盒。其中,在此实施例中,羊血清购买自北京索莱宝生物科技公司;底物反应液3,3’,5,5’-四甲基联苯胺溶液使用的是购买自北京梅科万德生物科技有限公司的tmb溶液;hrp酶标抗人二抗购买自洛阳佰奥通实验材料中心。本实施例的试剂盒用于检测时,如表1所示,pres1抗原包被酶标反应板为8排十二列的96孔反应板,pres1抗原包被酶标反应板的样品与标准品分别加入到不同的反应孔中。表1样品与标准品加入到pres1抗原包被酶标反应板的反应孔1234567891011121标品1样品样品样品样品样品样品样品样品样品样品样品2标品2样品样品样品样品样品样品样品样品样品样品样品3标品3样品样品样品样品样品样品样品样品样品样品样品4标品4样品样品样品样品样品样品样品样品样品样品样品5标品5样品样品样品样品样品样品样品样品样品样品样品6标品6样品样品样品样品样品样品样品样品样品样品样品7标品7样品样品样品样品样品样品样品样品样品样品样品8空白样品样品样品样品样品样品样品样品样品样品样品实施例2乙型肝炎病毒前s1抗体免检测试剂盒的使用方法取12例hbv感1染者血清作为样片并命名为s1-s12,取10例未感染者作为样片并命名为n1-n10。将样品稀释液倒入8通道移液器加样槽中,用移液器将100ul样品稀释液加入到96孔的pres1抗原包被酶标反应板。按照表2分别取对应的标准品和待测血清样品5ul加入到相应的酶标板孔中,震荡混匀,将加样后的pres1抗原包被酶标反应板放置于37℃恒温箱中,孵育30min。表2标准品和待测样品加样1234a标品1s1s9n5b标品2s2s10n6c标品3s3s11n7d标品4s4s12n8e标品5s5n1n9f标品6s6n2n10g标品7s7n3h空白s8n4向洗涤液中加入9倍体积的双蒸水,用稀释后的洗涤液洗涤pres1抗原包被酶标反应板,每孔350ul洗涤液,重复洗涤5次。将按照1:20万稀释的hrp酶标抗人二抗倒入到8通道移液器加样槽中,用移液器将100ulhrp酶标抗人二抗加入到96孔酶标板中,37℃孵育30min。用稀释后的洗涤液洗涤pres1抗原包被酶标反应板,每孔350ul洗涤液,重复洗涤5次。将tmb底物反应液倒入8通道移液器加样槽中,用移液器将100ultmb底物反应液加入到96孔酶标板中,37℃孵育15min酶标二抗孵育结束后,用移液器将50ul的2m稀硫酸加入96孔酶标板中,轻轻震荡混匀,终止底物反应。加入终止液后立即将酶标板放入酶标仪中,用450nm参比630nm的双波长检测终止后酶标板每孔的od值,检测结果如表3。表3标准品和血清样品检测od值1234a1.30440.02180.66070.0008b1.0720.00640.80410.0044c0.7510.40810.00670.077d0.6250.4240.70910.0144e0.36320.20340.00570.0065f0.30580.40810.00360.0194g0.17780.4240.0033h0.00220.00360.001从表3的od检测结果可以看出,未感染hbv健康人群的血清pres1抗体od值均小于0.15,直接判定为pres1抗体阴性;hbv感染者中,s1、s2、s8、s11检测od值也小于0.15,判定为pres1抗体阴性;s3、s4、s5、s6、s7、s9、s10、s12检测的od值大于0.15,为pres1抗体阳性,进一步利用标准品计算血清中pres1抗体的含量。根据表3标准品的od值和各标准品的浓度,进行散点做图,并进行线性拟合获得pres1抗体浓度-od值趋势线及pres1抗体浓度-od值拟合方程,标准曲线如图1所示。拟合的pres1抗体浓度-od值方程为:y=0.3267x+0.1138,其中y为od值,x为pres1抗体浓度。r2=0.9611,r2为根据标准品的pres1抗体浓度-od值的趋势线拟合方程生成的拟合系数。根据拟合后的pres1抗体浓度-od值方程分别计算获得各血清样本中pres1抗体的含量如下表4。表4血清中pres1抗体的含量计算值本申请的乙型肝炎病毒前s1抗体免检测试剂盒,基于定量检测pres1抗体的技术,定检测人体血清、血浆中pres1抗体的含量,用于发现早期乙肝感染者,并评估患者感染后的预后能力和用药的治疗效果。需要说明的是,在本文中,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括……”限定的要素,并不排除在包括所述要素的物品或者设备中还存在另外的相同要素。以上实施例仅用以说明本发明的技术方案而非限制,仅仅参照较佳实施例对本发明进行了详细说明。本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的精神和范围,均应涵盖在本发明的权利要求范围当中。序列表<110>北京安必奇生物科技有限公司<120>pres1抗体、乙型肝炎病毒前s1抗体酶免检测试剂盒、制备方法、使用方法<130>012002386<141>2020-08-21<160>6<170>siposequencelisting1.0<210>1<211>370<212>dna<213>artificialsequence<400>1gaattcatgcaggtgcagctgcaggagagcggcggcggcctggtgcagcccgagggcagc60ctgaagctgagctgcgccgccagcggcttcaccttcaacacctacgccatgcactgggtg120aggcagacccccggcaagggcctggagtgggtggccaggatcaggaacaagagcaacaac180tacgccacctactacgccgacagcgtgaaggacaggttcaccatcagcagggacgacagc240cagaacatgctgtacctgcagatgaacaacctgaagaccgaggacaccgccatgtactac300tgcgtgagggaggccagcggcatggactactggggccagggcaccaccgtgaccgtgagc360caagcttggg370<210>2<211>358<212>dna<213>artificialsequence<400>2gaattcatggacatccagctgacccagagccccagcagcctggccgtgagcgtgggcgag60aaggtgagcatgagctgcaagagcagcctgaacctgctgtacaacaacaaccagctgaac120tacctggcctggtaccagcagaagcccggccagagccccaagctgctgatcagctgggcc180agcaccagggagagcggcgtgcccgacaggttcaccggcagcggcagcggcaccgacttc240accctgaccatcagcagcgtgaaggccgaggacctggccgtgtactactgccagcagtac300tacacctacccctacaccttcggcggcggcaccaagctggagatcaagcaagcttggg358<210>3<211>117<212>prt<213>artificialsequence<400>3glnvalglnleuglngluserglyglyglyleuvalglnproglugly151015serleulysleusercysalaalaserglyphethrpheasnthrtyr202530alamethistrpvalargglnthrproglylysglyleuglutrpval354045alaargileargasnlysserasnasntyralathrtyrtyralaasp505560servallysaspargphethrileserargaspaspserglnasnmet65707580leutyrleuglnmetasnasnleulysthrgluaspthralamettyr859095tyrcysvalargglualaserglymetasptyrtrpglyglnglythr100105110thrvalthrvalser115<210>4<211>113<212>prt<213>artificialsequence<400>4aspileglnleuthrglnserproserserleualavalservalgly151015glulysvalsermetsercyslysserserleuasnleuleutyrasn202530asnasnglnleuasntyrleualatrptyrglnglnlysproglygln354045serprolysleuleuilesertrpalaserthrarggluserglyval505560proaspargphethrglyserglyserglythraspphethrleuthr65707580ileserservallysalagluaspleualavaltyrtyrcysglngln859095tyrtyrthrtyrprotyrthrpheglyglyglythrlysleugluile100105110lys<210>5<211>376<212>dna<213>artificialsequence<400>5ggaattcatatgatgggaggttggtcttccaaacctcgacaaggcatggggacgaatctt60tctgttcccaatcctctgggattctttcccgatcaccagttggaccctgcgttcggagcc120aactcaaacaatccagattgggacttcaaccccaacaaggatcactggccagaggcaaat180caggtaggagcgggagcattcgggccagggttcaccccaccacacggcggtcttttgggg240tggagccctcaggctcagggcatattgacaacagtgccagcagcgcctcctcctgcctcc300accaatcggcagtcaggaagacagcctactcccatctctccacctctaagagacagtcat360cctcagcaagcttggg376<210>6<211>118<212>prt<213>artificialsequence<400>6metglyglytrpserserlysproargglnglymetglythrasnleu151015servalproasnproleuglyphepheproasphisglnleuasppro202530alapheglyalaasnserasnasnproasptrpasppheasnproasn354045lysasphistrpproglualaasnglnvalglyalaglyalaphegly505560proglyphethrproprohisglyglyleuleuglytrpserprogln65707580alaglnglyileleuthrthrvalproalaalaproproproalaser859095thrasnargglnserglyargglnprothrproileserproproleu100105110argaspserhisprogln115当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1