一种用于肿瘤类器官培养条件选择的CTNNB1基因突变的快速鉴定方法与流程
本发明涉及一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法,属于基因检测
技术领域:
。
背景技术:
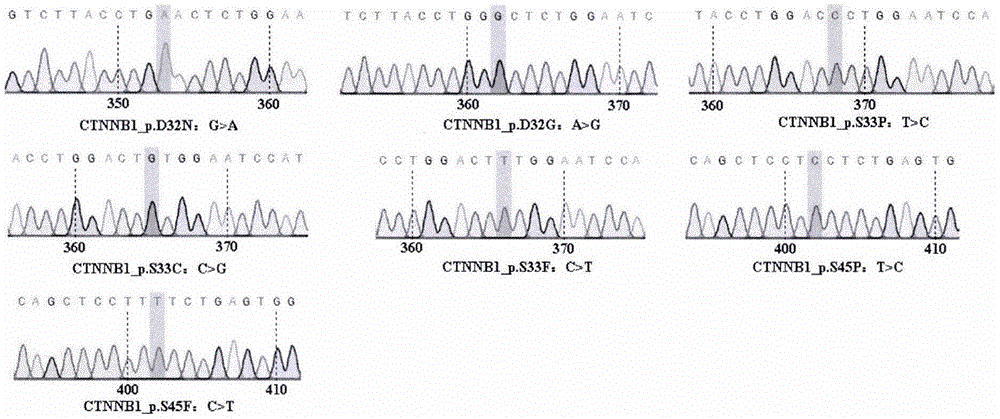
:中国作为一个癌症大国,癌症发病率居高不下,年新发病例约占全球总数的四分之一。国家癌症中心发布的最新一期全国癌症统计数据报告显示:2015年恶性肿瘤发病约392.9万人,发病率为285.83/10万,死亡约233.8万人,这意味着平均每天超过1万人被确诊为癌症,每分钟有7.5人被确诊为癌症。近十多年来,我国癌症发病、死亡数均持续上升,恶性肿瘤发病率每年约有3.9%的增幅,死亡率每年约有2.5%的增幅。目前,随着靶向药物研究的持续深入,多种靶向特定致癌基因的药物不断进入临床,给广大患者带来了福音。然而,由于癌症的本质是受多基因突变影响的疾病,患者肿瘤会随着疾病的进展而不断演化,导致形成患者间的肿瘤异质性和同一肿瘤内的异质性。癌症异质性给靶向精准治疗增加了不确定性,同时也是导致癌症药物治疗耐药性的重要原因之一。为此,拓展针对癌症异质性的精准医疗具有重要的现实意义,而肿瘤类器官技术的兴起则为此提供了全新的更加有效的应用平台。类器官是将具有成体干细胞潜能的细胞或组织在体外进行3d培养而成的三维微观结构。基于患者肿瘤组织的类器官培养被称为肿瘤类器官培养。肿瘤类器官具备自主生长及更新的能力,并且可以保留肿瘤组织特点和一定的遗传稳定性,因此与传统二维培养的肿瘤细胞系相比,肿瘤类器官具有更高的临床相关性和个体多样性,是目前最接近临床状况的体外肿瘤疾病模型。在技术应用上,肿瘤类器官疾病模型不仅在癌症的精准医疗上可用于指导患者用药的选择,同时在抗癌药物研发中,基于保有患者癌症异质性的标本库的建立,肿瘤类器官模型可更有效的评估临床前或临床试验中的先导化合物针对特定类型癌症的药效。肿瘤类器官已成为肿瘤基础研究中既模拟肿瘤生长的“环境”又具有患者特异性(优于实验动物模型)的最佳疾病模型,为临床研究和治疗中“有测序无靶点,有靶点无药物,有药物无疗效”的困境带来了曙光。正因为肿瘤类器官能够保留原始肿瘤的性质,从而通过对肿瘤类器官的药物测试,可为肿瘤来源的病人选取考虑其癌症异质性的治疗方案,由此促进了癌症精准治疗的进一步研究和发展。然而,肿瘤类器官的培养技术面临着一些未知和挑战。挑战之一,肿瘤组织中往往混杂着正常组织,如选择的培养基不正确,随着传代培养,源自正常组织的类器官会逐渐替代肿瘤类器官,导致所培养的肿瘤类器官群体逐渐丧失肿瘤特性,使得针对肿瘤类器官的药敏测试得出非患者实际肿瘤状况的实验数据,对临床用药产生误导,以致延误患者选择精准有效药物的时间。目前,多种方法已经用于应对上述挑战。以肝癌肿瘤类器官为例,基于肿瘤类器官在物理特性、细胞特性、肿瘤特有基因突变方面同正常类器官的区别,研究者采用过四种对肿瘤类器官进行特异性筛选的培养方法,但这些方法均存在着操作繁琐或对实验室要求很高等明显限制因素。第一种方法是在培养过程中人工操作处理,即在显微镜下使用工具剔除无“癌症类器官特征”、表型“正常”的类器官,该方法可行性低、错误率高;第二种方法是利用流式细胞仪将肿瘤组织细胞中的癌症干细胞分选提取,利用筛选出的高纯度的特定肿瘤细胞进行类器官培养,该方法不仅对硬件要求高,同时也存在所选特定癌细胞无法反映患者主要肿瘤性质的风险;第三种方法是根据已知的患者测序结果,调整培养基成分,筛选显示特定的癌症相关突变表型的类器官,该方法的问题是患者测序结果的获得往往滞后于肿瘤类器官的起始培养时间;第四种方法是通过对培养获取的肿瘤类器官进行测序来确定是否有与患者癌症相关的突变,该方法存在成本高和效率低的问题。在众多的癌症组织中,wnt相关突变起着重要作用。wnt信号通路和动物胚胎发育、器官形成及组织再生等生理过程密切相关,它的激活突变可直接导致肿瘤的形成,而ctnnb1基因编码的β-catenin是该信号通路的关键因子。ctnnb1基因的突变在癌症中属于高频突变之一,对肝癌、结直肠癌、乳腺癌等多种癌症存在高致病性,针对ctnnb1基因突变的甄别具有广泛且重要的癌症治疗指导作用。因此,对于目前肿瘤类器官特异性筛选培养方法所面临的明显问题,如何在培养启动之前快速筛选出可使用ctnnb1基因突变相关的类器官培养条件的患者肿瘤组织成为急需解决的技术难题。因此,发明一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法是必要的。技术实现要素:为了解决如何在培养启动之前快速筛选出可使用ctnnb1基因突变相关的类器官培养条件的患者肿瘤组织的技术难题,本发明提供了一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法。该鉴定方法采用实时荧光定量pcr仪的arms-pcr技术,针对一组癌症发生相关的ctnnb1基因的突变位点,设计了专用的mutation引物、arms-pcr扩增引物和探针,建立了一种针对ctnnb1基因突变的快速筛选方法。经对具有不同ctnnb1基因突变的质粒dna的单个检测或多个同时检测的实验验证,该鉴定方法特异性强、灵敏度高,并能一次性快速(4小时内)检测出肿瘤组织中是否含有ctnnb1基因突变,准确高效地确定相应的肿瘤类器官培养条件,以此在提高培养准确率的同时,减少无意义的资源浪费,从而不仅有效的缩短相关检测的周期及成本,并且更加精准地预测药效、选取治疗方案,实现针对ctnnb1基因突变的肿瘤类器官的培养方法的快速选择,由此能更好地为精准医疗服务。本发明解决其技术问题所采用的技术方案是:本发明一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法,该方法检测肿瘤组织的单个ctnnb1基因突变和同时检测肿瘤组织的多个ctnnb1基因突变的有效性验证包括如下实验步骤:(1)筛选出肿瘤ctnnb1基因达到一定频率的功能性突变位点;(2)设计步骤(1)的肿瘤ctnnb1基因中达到一定频率的功能性突变位点的arms-pcr扩增引物和探针;(3)选取能够包含步骤(1)中的功能性突变位点及其arms-pcr扩增引物的dna片段,并设计pcr扩增引物;(4)以正常人基因组dna为模板,对步骤(3)中的pcr扩增引物进行pcr扩增;(5)对步骤(4)中获得的dna片段设计ta克隆引物,进行ta克隆,并转化扩增;(6)设计步骤(1)的肿瘤ctnnb1基因中达到一定频率的功能性突变位点的mutation引物;(7)以步骤(5)中的质粒dna为模板,对步骤(6)中的mutation引物进行pcr扩增,并转化扩增;(8)选取待测样本的适量组织,提取待测样本的基因组dna;(9)将步骤(7)中的质粒dna设为阳性对照,以步骤(8)中的待测样本基因组dna为模板,对步骤(2)中的arms-pcr扩增引物进行pcr扩增;(10)检测结果使用仪器分析并输出结果,通过观察实时荧光定量pcr仪输出的结果中出现曲线和cp值,且阴性对照与空白对照无曲线和cp值,则确定该样本发生突变。所述肿瘤ctnnb1基因达到一定频率的功能性突变位点为:ctnnb1_p.d32n、ctnnb1_p.d32g、ctnnb1_p.s33p、ctnnb1_p.s33c、ctnnb1_p.s33f、ctnnb1_p.s45p、ctnnb1_p.s45f。上述突变位点名称中,ctnnb1是一个基因名称,编码的蛋白β-catenin是wnt信号通路中的关键因子。ctnnb1后面的则是指点突变的位置,比如p.d32n是指点突变位置,对应的氨基酸(第32位)由天冬氨酸(d)突变为天冬酰胺(n);p.d32g是指点突变位置,对应的氨基酸(第32位)由天冬氨酸(d)突变为甘氨酸(g);p.s33p是指点突变位置,对应的氨基酸(第33位)由丝氨酸(s)突变为脯氨酸(p);p.s33c是指点突变位置,对应的氨基酸(第33位)由丝氨酸(s)突变为半胱氨酸(c);p.s33f是指点突变位置,对应的氨基酸(第33位)由丝氨酸(s)突变为苯丙氨酸(f);p.s45p是指点突变位置,对应的氨基酸(第45位)由丝氨酸(s)突变为脯氨酸(p);p.s45f是指点突变位置,对应的氨基酸(第45位)由丝氨酸(s)突变为苯丙氨酸(f)。所述肿瘤ctnnb1基因达到一定频率的功能性突变位点的ta克隆引物的序列为:上游5’-gttaggtggttccctaagggattagg-3’下游5’-tcaacactcactatccacagttcagc-3’ta克隆方法(originaltacloningkit)是把pcr片段与一个具有3’-t突出的载体dna连接起来的方法。这里是指获取用于ta克隆的pcr片段所需的引物。所述肿瘤ctnnb1基因达到一定频率的7个功能性突变位点的mutation引物(mutation引物是将ta克隆获得的无突变质粒dna当做模板,进行点突变pcr实验所需的引物,可得到突变型的质粒dna)、arms-pcr引物和探针的序列为:ctnnb1_p.d32nmutation引物:上游5’-gcaacagtcttacctgaactctggaatcca-3’下游5’-tcaggtaagactgttgctgccagtgac-3’arms-pcr引物:上游5’-ggcagcaacagtcttaccgga-3’下游5’-tgcattctgactttcagtaaggcaa-3’探针:5’-tctggtgccactaccacagctcc-3’ctnnb1_p.d32gmutation引物:上游5’-caacagtcttacctgggctctggaatccat-3’下游5’-cccaggtaagactgttgctgccagtga-3’arms-pcr引物:上游5’-ggcagcaacagtcttaccttgg-3’下游5’-aactgcattctgactttcagtaaggc-3’探针:5’-tctggtgccactaccacagctcc-3’ctnnb1_p.s33pmutation引物:上游5’-cagtcttacctggaccctggaatccattctgg-3’下游5’-ggtccaggtaagactgttgctgccag-3’arms-pcr引物:上游5’-cagcaacagtcttacctggccc-3’下游5’-aaggactgagaaaatccctgttccc-3’探针:5’-tctggtgccactaccacagctcc-3’ctnnb1_p.s33cmutation引物:上游5’-agtcttacctggactgtggaatccattctgg-3’下游5’-cagtccaggtaagactgttgctgcca-3’arms-pcr引物:上游5’-gcagcaacagtcttacctggagtg-3’下游5’-gcattctgactttcagtaaggcaatg-3’探针:5’-tctggtgccactaccacagctcc-3’ctnnb1_p.s33fmutation引物:上游5’-agtcttacctggactttggaatccattctggt-3’下游5’-aagtccaggtaagactgttgctgcca-3’arms-pcr引物:上游5’-tggcagcaacagtcttaccrggaatt-3’下游5’-tgcattctgactttcagtaaggcaatga-3’探针:5’-tctggtgccactaccacagctcc-3’ctnnb1_p.s45pmutation引物:上游5’-actaccacagctcctcctctgagtggtaaaggc-3’下游5’-gaggagctgtggtagtggcaccagaa-3’arms-pcr引物:上游5’-tggtgccactaccacagctcatc-3’下游5’-tgcattctgactttcagtaaggcaatg-3’探针:5’-cctcccaagtcctgtatgagtggga-3’ctnnb1_p.s45fmutation引物:上游5’-actaccacagctccttttctgagtggtaaaggc-3’下游5’-aaaggagctgtggtagtggcaccagaa-3’arms-pcr引物:上游5’-gccactaccacagctccgtt-3’下游5’-actgcattctgactttcagtaaggc-3’探针:5’-cctcccaagtcctgtatgagtggga-3’结论:本发明提供的基于ctnnb1基因突变的快速筛选方法检测wnt信号通路中ctnnb1基因常见的7个突变位点和同时检测多个ctnnb1基因突变,验证结果均显示为阳性,均能够用实时荧光定量pcr仪获得每个突变位点的结果曲线图和cp值。阴性对照及空白对照均没有检测到基因突变,表明本发明检测肿瘤组织的单个ctnnb1基因突变和同时检测肿瘤组织的多个ctnnb1基因突变均具有可行性。本发明的有益效果为:(1)本发明提供的一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法,选择了罹患癌症风险显著相关的癌症热点突变位点,检测的突变位点更前沿,并且相互独立。因此本发明的位点选择具有代表性和独立性。(2)本发明提供的检测技术,成本价格优势明显,并且在肿瘤组织早期检测方面的灵敏度更高,通量更大,可实现单个小样本多检测,并能够精准地指导类器官培养。(3)本发明提供的一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法,能在极短时间内(4小时)鉴定出肿瘤组织中是否含有ctnnb1基因突变,可准确高效地确定相应的肿瘤类器官培养条件。(4)本发明提供的一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法,可操作性强,具有高准确性、高灵敏性的技术优势,检测结果稳定、效果明显,具有显著优势。附图说明下面结合附图对本发明进一步说明。图1是一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法的突变型质粒dna的测序结果图。图2是一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法的以正常人基因组dna为模板,配制pcr反应体系,所得pcr产物的电泳结果图。图中:1.dnaladdermarker,2.pcrproduct。图3是一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法的以步骤(2)的质粒dna为模板,配制mutation反应体系,使用dmt酶处理,所得突变型质粒dna的电泳结果图。图中:1.dnaladdermarker,2.ctnnb1_p.d32n,3.ctnnb1_p.d32g,4.ctnnb1_p.s33p,5.ctnnb1_p.s33c,6.ctnnb1_p.s33f,7.ctnnb1_p.s45p,8.ctnnb1_p.s45f。图4是一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法的arms-pcr实验结果的ctnnb1_p.d32n结果曲线图和cp值。图5是一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法的arms-pcr实验结果的ctnnb1_p.d32g结果曲线图和cp值。图6是一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法的arms-pcr实验结果的ctnnb1_p.s33p结果曲线图和cp值。图7是一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法的arms-pcr实验结果的ctnnb1_p.s33c结果曲线图和cp值。图8是一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法的arms-pcr实验结果的ctnnb1_p.s33f结果曲线图和cp值。图9是一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法的arms-pcr实验结果的ctnnb1_p.s45p结果曲线图和cp值。图10是一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法的arms-pcr实验结果的ctnnb1_p.s45f结果曲线图和cp值图11是一种用于肿瘤类器官培养条件选择的ctnnb1基因突变的快速鉴定方法的arms-pcr实验结果的多个ctnnb1突变结果曲线图和cp值具体实施方式如图所示,本发明基于ctnnb1基因突变的快速筛选方法相关实验过程如下:展示一下实例来具体说明本发明的某些实施例,且不应解释为限制本发明的范围。对本发明公开的内容可以同时从材料、方法和反应条件进行改进,所有这些改进,均应落入本发明的精神和范围之内。非特殊说明,本发明实施例采用的试剂均为市售商品,本发明实施例采用的数据库均为公开的在线数据库。主要试剂:peasy-t1cloningkit、amplitaqdnapolymerase,ld、vader-trap高纯度质粒小提试剂盒、fastmutagenesissystemkit、hipureplasmidminikit、probeqpcrsupermix(2×)。主要仪器:pcr仪、lightcycler480高通量实时荧光定量pcr仪、超净工作台、移液枪、凝胶电泳仪、水浴锅、培养箱、摇床、照胶仪、高速离心机。实施例1:本发明的arms-pcr检测方法检测单个ctnnb1基因突变。1.研究对象选用以7个突变位点:ctnnb1_p.d32n、ctnnb1_p.d32g、ctnnb1_p.s33p、ctnnb1_p.s33c、ctnnb1_p.s33f、ctnnb1_p.s45p、ctnnb1_p.s45f,同时设立正常人基因组dna作为阴性对照,水(h2o)作为空白对照。2.实验步骤(1)设计表1、表2和表3中肿瘤ctnnb1基因达到一定频率的功能性突变位点的ta克隆引物引物、mutation引物、arms-pcr扩增引物和探针。表1:包含7个突变位点及其arms-pcr扩增引物的正常人dna片段的ta克隆引物引物名称引物序列(5’-3’)c-primer-fgttaggtggttccctaagggattaggc-primer-rtcaacactcactatccacagttcagc表2:肿瘤ctnnb1基因中一定频率的功能性突变位点的arms-pcr扩增引物和探针表3:肿瘤ctnnb1基因中达到一定频率的功能性突变位点的mutation引物(2)以正常人基因组dna为模板,按照下表配制pcr反应体系:扩增的热循环参数:steptemperature(℃)time19510:0029500:1535500:1547200:505gotostep2x396727:00pcr产物的电泳结果如图2所示。ta克隆反应体系:componentvolume(μl)freshpcrproduct4peasy-t1cloningvector1totalvolume5克隆成功后转化并测序。(3)以步骤(2)的质粒dna为模板,按照下表分别配制7个突变位点的mutation反应体系:扩增的热循环参数:steptemperature(℃)time1945:0029400:2035500:204722:205gotostep2x2567210:00(4)使用1μldmt酶于37℃处理pcr产物1小时,电泳检测后转化并测序。突变型质粒dna的电泳结果如图3所示。突变型质粒dna的测序结果如图1所示。(5)以步骤(4)的突变型质粒dna为模板,按照下表分别配制7个突变位点的arms-pcr反应体系:同时按照上表分别设立正常人基因组dna的阴性对照和水的空白对照。negativecontrol:blankcontrol:扩增的热循环参数:arms-pcr实验结果的结果曲线图和cp值如图4-图10所示,待测样本出现曲线和cp值,且阴性对照与空白对照无曲线和cp值,则确定该样本发生突变。3.结论建立方法检测ctnnb1基因中常见的7个突变位点,验证结果显示为阳性,均能够用lightcycler480高通量实时荧光定量pcr仪获得结果曲线图和cp值,而阴性对照及空白对照均没有检测到基因突变,表明本发明具有可行性。实施例2:本发明的arms-pcr检测方法同时检测多个ctnnb1基因突变。1.研究对象选用以下7个突变位点:ctnnb1_p.d32n、ctnnb1_p.d32g、ctnnb1_p.s33p、ctnnb1_p.s33c、ctnnb1_p.s33f、ctnnb1_p.s45p、ctnnb1_p.s45f,同时设立正常人基因组dna作为阴性对照,水(h2o)作为空白对照。2.实验步骤(1)使用实施例1中表2的arms-pcr扩增引物和探针。(2)以实施例1中的7个突变型质粒dna为模板,将探针和arms-pcr扩增引物按照下表配制arms-pcr反应体系:同时按照上表设立正常人基因组dna的阴性对照和水的空白对照:negativecontrol:blankcontrol:扩增的热循环参数:arms-pcr实验结果的结果曲线图和cp值如图11所示,待测样本出现曲线和cp值,且阴性对照与空白对照无曲线和cp值,则确定该样本发生突变。3.结论验证结果显示为阳性,能够用lightcycler480高通量实时荧光定量pcr仪获得每个突变位点的结果曲线图和cp值。阴性对照及空白对照均没有检测到基因突变,表明本发明同时检测癌症组织的多个ctnnb1基因突变具有可行性。本发明基于arms-pcr技术,提供一组癌症发生相关的wnt信号通路中ctnnb1基因的突变位点,并设计专用的mutation引物、arms-pcr扩增引物和探针,经实验验证,基于ctnnb1基因突变的快速筛选癌症类器官的培养方法特异性强、灵敏度高,并能一次性检测出可能的突变位点,准确高效。以上显示和描述了本发明的基本原理和主要特征和本发明的优点。以上所述实施例为本发明的优选实施方式,本行业的技术人员应了解,上述实施例和说明书中描述的只是说明本发明的原理,但本发明的实施方式并不受上述实施例的限制,应当指出,对于本领域的普通技术人员来说,在不脱离本发明创造构思的前提下,所做出的若干变形和改进,均应为等效的置换方式,这些都属于本发明的保护范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1