一种有效抑制表皮生长因子受体表达的siRNA序列的制作方法
本发明涉及分子生物学与生物医药技术领域,具体涉及一种有效抑制表皮生长因子受体(epidermalgrowthfactorreceptor,简称为egfr)基因表达的sirna。
背景技术:
脊椎动物细胞的许多生命活动受细胞外信号分子调控。这些信号通常由一些跨膜受体传过细胞膜,其中一类重要受体自身具有蛋白酪氨酸激酶活性,归属于受体蛋白酪氨酸激酶(rptk)家族,表皮生长因子受体(egfr)即是这一家族典型成员,其作用有赖于细胞膜内的信号传导通路,不同的通路其功能不同,相同的通路在不同的细胞甚至同一细胞的不同条件下具有不同的功能。
egfr是一种存在于细胞表面的多功能跨膜蛋白分子,分布很广,其分子量为170kd,由1186个氨基酸残基构成,为原癌基因c-erbb1所编码。人egfr基因位于第7号染色体p13-q22区,其结构分为3个区域:伸向膜外与egf识别并结合的氨基端区域,位于细胞膜中间单链的a-螺旋跨膜区以及具有酪氨酸激酶活性的细胞质内的羧基端区域。细胞内542个氨基酸可分成3个结构域:近膜区(约50个氨基酸)起与pkc(蛋白激酶c)和erkmapk(细胞外信号调节激酶丝裂素活化蛋白激酶)负反馈的结合位点,有证据表明这个区域有一基序(motif)可能联结异源三聚体g蛋白。紧接着是约250个氨基酸酪氨酸激酶区(sh1),一个单一229个氨基酸长的羧基末端尾部包含5个自动磷酸化基序。它与含有sh2(src同源结构域2)或ptb(磷酸酪氨酸结合结构域)连接,至少有3个内在化基元包含一个牢固的转角、转磷酸位点、蛋自分解及降解位点。egfr自动磷酸化基元结构相似、功能余冗,不同于其他的rptk,简单的结构和复杂余冗基序的交替发生表示出一个原始型基因。
egfr的配体与细胞膜上的egfr结合,可使受体形成二聚体,二聚化的受体使其白身酪氨酸激酶被激活;受体上磷酸化的酪氨酸又与位于膜上的生长因子受体结合蛋白2(grb2)的sh2结构域结合,而grb2的sh3结构域则同时与鸟苷酸交换因子sos(sonofsevenless)结合,后者使小分子鸟苷酸结合蛋白ras的gdp解离而结合gtp,从而激活ras;激活的ras进一步与丝/苏氨酸蛋自激酶raf-1的氨基端结合,通过未知机制激活raf-1;raf-1可磷酸化mekl/mek2mapkinase/erkkinade上两个调节性丝氨酸,从而激活mek;mek为特异性激酶,可以使丝/苏氨酸和酪氨酸发生磷酸化,最终高度选择性地激活erk1和erk2。erks为脯氨酸导向的丝/苏氨酸激酶,可以磷酸化与脯氨酸相邻的丝/苏氨酸。在丝裂原刺激后,erk接受上级的级联反应信号,可以转位进人细胞核。因此,erk不仅可以磷酸化胞浆蛋白,而且可以磷酸化一些核内的转录因子如c-fos,c-jun,elk-1,c-myc和atf2等,从而参与细胞增殖与分化的调控。
egfr信号传导的深入研究,对于阐明细胞生长、发育、分裂、细胞间功能同步等多种生理过程及细胞恶性转化等病理过程有重要的意义。egfr在人类许多肿瘤中常发现有过度表达,由于它是早期作为转化γ-erbb癌基因的原癌基因和多数肿瘤发生而被识别,因而egfr介导的下游信号可能代表了攻克肿瘤的新途径。
专利文献cn101671397b公开了一种以表皮生长因子受体为靶点的重组免疫毒素。该重组免疫毒素是由egfr的单链抗体与毒素蛋白gelonin融合表达而成。该技术方案利用单链抗体对egfr高表达肿瘤的靶向性和gelonin的细胞毒作用对肿瘤起到特异的杀伤作用,效果明显。
专利文献cn103333246b公开了一种抗egfr受体并抑制肿瘤生长的抗体药物偶联物的制备方法及在治疗表皮生长因子受体抗原阳性细胞癌症的用途。
专利文献cn106661576a中斯特里克生物公司和贝勒医学院公开了用于制备和使用能够降低两个或更多个基因的表达的rnai的组合物和方法,其包括:降低第一靶基因表达的第一rnai分子;降低所述第一靶基因或第二靶基因的表达的第二rnai分子;和任选地降低所述第一靶基因、第二靶基因或第三靶基因的表达的第三rnai分子,其中所述rnai分子降低例如突变kras、egfr、pik3、ncoa3或erα1的表达水平。
(付建华等.“egfr和e-cadherin与肿瘤的发生发展及其调控机制的研究进展”.实用癌症杂志.2008,23(1):107-109;)中公开:egfr过度表达与肿瘤的形成有一定的正相关,对肿瘤的分裂增殖起重要作用。
专利文献cn102993305a中公开:egfr及其编码基因可用于制备预防和治疗抗肿瘤及其他疾病如炎症及自身免疫性疾病的特异性抗体药物。
rna干扰(rnainterference,rnai)是近年发展起来的一项新的基因沉默技术,sirna是rnai的效应分子,体外合成sirna则是rna干扰技术的最新发展,尤其是在特异性抑制哺乳动物细胞基因表达方面,为基因治疗开创了新的道路。
技术实现要素:
本发明提供一种抑制egfr表达的干扰rna。
具体地,上述干扰rna包含正义链和与其反向互补配对的反义链。
具体地,上述干扰rna选自:sirna、dsrna、shrna、airna、mirna及其组合。
在本发明的一个实施方式中,上述干扰rna为sirna。
在本发明的一个实施方式中,上述干扰rna是化学合成的。
具体地,上述干扰rna包含如seqidno:1所示的核苷酸序列或由如seqidno:1所示的核苷酸序列组成。
具体地,上述干扰rna包含如seqidno:2所示的核苷酸序列或由如seqidno:2所示的核苷酸序列组成。
具体地,上述干扰rna的正义链包含如下核苷酸序列或由以下核苷酸序列组成:5′-gcaacaugucgauggacuu-3′。
具体地,上述干扰rna的反义链包含如下核苷酸序列或由以下核苷酸序列组成:5′-aaguccaucgacauguugc-3′。
具体地,上述干扰rna(如sirna)分子的正义链和/或反义链的末端(如3′末端)还可设有n个悬挂碱基(over-hang),以增加该干扰rna的活性。其中,悬挂碱基可以为相同或不同的脱氧核苷(如脱氧胸苷(dt)、脱氧胞苷(dc)、脱氧尿苷(du)等),n为1-10的整数(如1、2、3、4、5、6、7、8、9、10),特别是2-4的整数;在本发明的一个实施例中,n=2,悬挂碱基可以为dtdt、dtdc或dudu,等等。
具体地,上述干扰rna分子的正义链和反义链的3′末端均设有悬挂碱基dtdt。
具体地,上述干扰rna的正义链包含如下核苷酸序列或由以下核苷酸序列组成:5′-gcaacaugucgauggacuudtdt-3′。
具体地,上述干扰rna的反义链包含如下核苷酸序列或由以下核苷酸序列组成:5′-aaguccaucgacauguugcdtdt-3′。
具体地,上述干扰rna分子中还可包含至少一个修饰的核苷酸,修饰的干扰rna具有比相应未修饰的干扰rna具有更佳的性质,如更高的稳定性,更低的免疫刺激性等。
本发明还提供一种上述干扰rna的递送系统,其包含上述干扰rna和载体。
具体地,上述载体可以采用任何适于将本发明上述干扰rna递送于靶组织或靶细胞等的载体,如现有技术(例如陈中华,朱德生,李军,黄展勤.“非病毒sirna载体研究进展”.中国药理学通报.2015,31(7):910-4;王锐,曲炳楠,杨婧.“载sirna的纳米制剂研究进展”.中国药房.2017,28(31):4452-4455)中公开的那些。
具体地,上述载体为病毒载体,具体如慢病毒、逆转录病毒、腺病毒、单纯疱疹病毒等。
具体地,上述载体为非病毒载体,具体如脂质体、聚合物、多肽、抗体、适配体等或其组合;其中,上述干扰rna与非病毒载体的重量比可以为1:1-50(如1:1、1:5、1:10、1:15、1:20、1:25、1:30、1:35、1:40、1:45、1:50等)。
具体地,上述脂质体可以为阳离子脂质(如invitrogenn公司的lipofectamine系列、1,2-二油酰基-3-三甲基铵丙烷(dotap))、中性离子脂质体(如二油酰磷脂酰胆碱(dopc)、胆固醇等)、阴离子脂质体(如二油酰磷脂酰甘油(dopg)、二油酰磷脂酰乙醇胺(dope)等)或其混合物。
具体地,上述聚合物可以为合成型聚合物(如聚乙烯亚胺、环糊精等)或天然型聚合物(如壳聚糖、端胶原等)或其混合物。
具体地,上述多肽可以为细胞穿透肽(cpp)(如鱼精蛋白、tat肽、transportan肽、penetratin肽、寡聚精氨酸肽等)。
具体地,上述抗体可以为单链抗体(如scfv-tp、scfv-9r等)。
本发明还提供一种药物组合物,其包括上述干扰rna或其递送系统,以及药学上可接受的辅料。
本发明还提供一种上述干扰rna或其递送系统、药物组合物在制备预防和/或治疗egfr相关的疾病的药物中的应用。
本发明还提供一种上述干扰rna或其递送系统在设计用于预防和/或治疗egfr相关的疾病的药物中的应用。
本发明还提供一种上述干扰rna或其递送系统、药物组合物在抑制活细胞中egfr基因表达的应用。
本发明还提供一种在需要其的受试者中抑制egfr表达的方法,其包括向该受试者施用治疗有效量的本发明上述干扰rna或其递送系统、药物组合物的步骤。
本发明还提供一种预防和/或治疗egfr相关的疾病的方法,其包括向受试者施用治疗有效量的本发明上述干扰rna或其递送系统、药物组合物的步骤。
具体地,上述疾病包括,但不限于,癌症、炎症等。
具体地,上述癌症包括,但不限于,肺癌(如非小细胞肺癌)、肝癌、食管癌、白血病、宫颈癌、结直肠癌、胰腺癌、肾癌、膀胱癌、乳腺癌、前列腺癌、胃癌、口腔上皮癌、卵巢癌、头颈癌、脑瘤、胶质细胞瘤等。
本发明还提供一种将本发明上述干扰rna引入细胞的方法,其包括使该细胞与该干扰rna的递送系统接触的步骤。
具体地,上述细胞在受试者体内。
具体地,上述使细胞与干扰rna的递送系统接触的步骤为将干扰rna的递送系统通过全身途径或局部途径施用至受试者体内来接触所述细胞的步骤。
本发明的发明人通过设计、合成,得到一种干扰rna(例如,sirna),其可有效抑制egfr表达,为预防或治疗egfr相关疾病(特别是egfr相关的癌症)提供了新的选择。
附图说明
构成本申请的一部分的说明书附图用来提供对本申请的进一步理解,本申请的示意性实施例及其说明用于解释本申请,并不构成对本申请的不当限定。
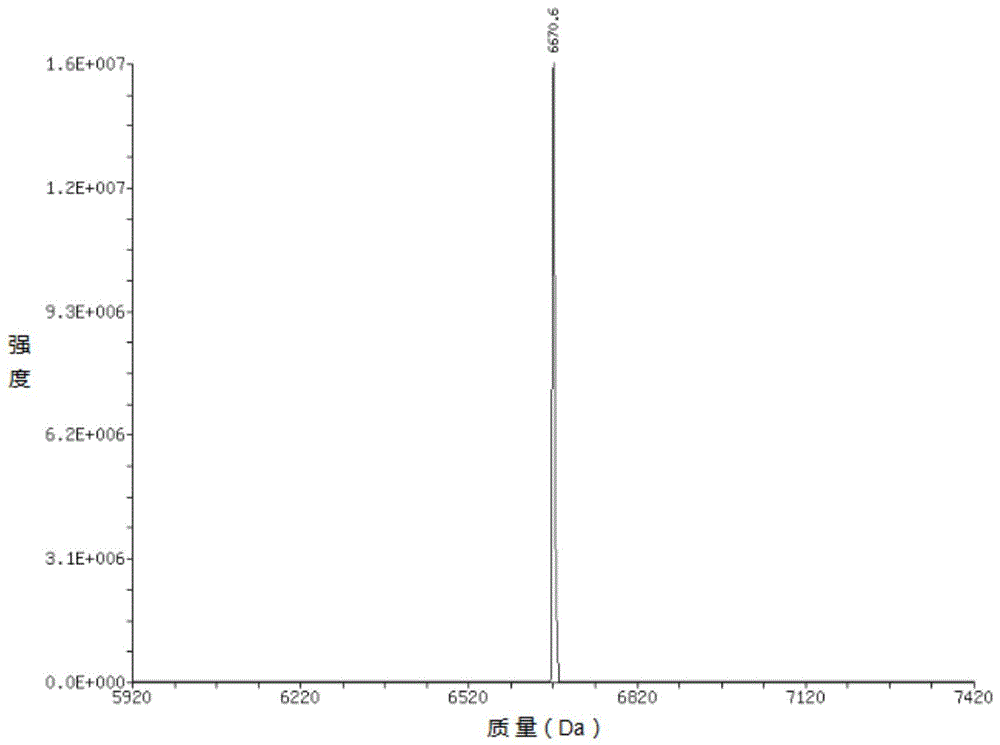
图1所示为egfrsirna正义链质谱图谱。
图2所示为egfrsirna反义链的质谱图谱。
图3所示为egfrmrna在细胞中的表达水平。
具体实施方式
除非另有定义,本发明中所使用的所有科学和技术术语具有与本发明涉及技术领域的技术人员通常理解的相同的含义。
如在本文中所使用的术语“干扰rna”或“rnai”或“干扰rna序列”包括单链rna(例如,成熟mirna、ssrnai寡核苷酸、ssdnai寡核苷酸)或双链rna(即,双链体rna如sirna、dsrna、shrna、airna、或前体mirna),其在当干扰rna与靶基因或序列处于相同细胞中时,能够降低或抑制靶基因或序列的表达(例如,通过介导降解和抑制与干扰rna序列互补的mrna的翻译)。干扰rna因此是指与靶mrna序列互补的单链rna或者由两条互补链或由单条自互补链形成的双链rna。具体地,干扰rna分子是化学合成的。
干扰rna包括“小干扰rna”或“sirna”,sirna分子的每条链包含长度为约15至约60的核苷酸(例如,长度为约15-60、15-50、15-40、15-30、15-25、或19-25的核苷酸,或者长度为15、16、17、18、19、20、21、22、23、24、或25的核苷酸)。在一个具体实施方式中,sirna是化学合成的。本发明的sirna分子能够体外和/或体内沉默靶序列的表达。在其他实施方式中,sirna包含至少一个修饰的核苷酸,例如sirna在双链区中包含一个、两个、三个、四个、五个、六个、七个、八个、九个、十个或更多个修饰的核苷酸。
如在本文中所用,术语“dsrna”或“前体rnai分子”意在包括在体内由核酸内切酶加工以产生活性sirna的任何前体分子。
如在本文中所用,术语“小发夹rna”或“短发夹rna”或“shrna”包括产生紧密发夹转角的短rna序列,所述发夹转角可以用于通过rna干扰来沉默基因表达。shrna发夹结构可由细胞机器裂解为sirna。
通常,微rna(mirna)是长度为约21-23个核苷酸的调节基因表达的单链rna分子。
本发明中,术语“治疗有效量”指的是将引起由研究者、兽医、医学医生或其他临床医生正在寻找的组织、系统或对象的生物学或医学应答的对象化合物的量。术语“治疗有效量”包括以下的活性成分的量:当被施用时,其足以预防治疗的紊乱或疾病的迹象或症状中的一个或多个的发展,或以一定程度减轻治疗的紊乱或疾病的迹象或症状中的一个或多个。治疗有效量将根据活性成分、待治疗的疾病及其严重程度、以及受试者的年龄、体重、性别等而变化。
本发明中,受试者可以为哺乳动物,如,人类、猴、狗、兔、小鼠、大鼠等。
应该指出,以下详细说明都是示例性的,旨在对本申请提供进一步的说明。
实施例1sirna的合成方法
本发明中含有2’-羟基的核糖核苷酸的寡聚核苷酸均按照理论产量1μmol合成规格完成,称取1μmol通用固相支持物3’-胆固醇修饰cpg(chemgenes产品),2’-o-tbdms保护rna亚磷酰胺的单体溶解于无水乙腈溶液中,使其浓度达到0.2m。配制5-乙硫基-1h-四唑(chemgenes产品)乙腈溶液作为活化剂(0.25m),配制0.02m碘的吡啶/水溶液作为氧化剂,以及3%三氯乙酸二氯甲烷溶液作为脱保护试剂,放置于abi394型号dna/rna自动合成仪对应的试剂指定位置。设置合成程序输入指定的寡聚核苷酸碱基序列,开始循环寡聚核苷酸合成,每步偶合时间6分钟,半乳糖配体对应l和s单体偶合时间10-20分钟。经自动循环后,完成寡核苷酸固相合成。以干燥氮气吹干cpg,转移到5mlep管中,加入氨水/乙醇溶液(3/1)2ml,55℃加热16~18小时。在10000rpm的转速下离心10min,取上清液,抽干浓氨水/乙醇后得到白色胶状固体。将固体溶于200μl1mtbafthf溶液,室温震荡20小时。加入0.5ml1mtris-hcl缓冲液(ph7.4),室温震荡15分钟,置于离心抽干机抽至体积为原体积1/2,除去thf。溶液用0.5ml氯仿萃取2次,加入1ml0.1mteaa上样液,将混合溶液倒入固相萃取柱,在htcslc-mssystem(novatia)系统上,完成质谱检测分析。质谱鉴定结果如图1(正义链,sense)、图2(反义链,antisense)所示。一级扫描后以promass软件归一化计算核酸分子量。上述方法分别合成两条单链,质谱鉴定正确后,两条单链以等摩尔比例混合,退火成双链,即为sirna序列。
sirna正义链序列为:5′-gcaacaugucgauggacuudtdt-3′
sirna反义链序列为:5′-aaguccaucgacauguugcdtdt-3′。
实施例2egfrsirna抑制效果
1、细胞培养
细胞名称:293t
a)293t细胞常规培养于37℃,5%的co2的条件下;
b)取50μlopti-mem培养基稀释5μlsirna(或sirnanc,浓度20μm),50μlopti-mem培养基稀释3μllipofectaminernaimax转染试剂,二者混合,轻轻摇匀,静置15min;此外,设置mock及blank对照组;
c)各孔加入上述108μl混合液;
d)取对数生长期的293t细胞,以每孔1.2×105细胞接种于12孔板中,每孔体积892μl,最终每孔总体积1000μl;sirna(或sirnanc)转染浓度均为100nm;
e)转染48h后将12孔板从37℃,5%co2的培养箱中取出,用于提取rna进行后续检测。
2、rna提取
a)trizol裂解:彻底去除细胞培养液,加入1mltrizoltmreagent,移液枪吸打3-5次,让细胞充分裂解,室温放置3~5分钟;
b)加入0.2体积(0.2ml/1mltrizol)的氯仿,votex震荡15s,室温静置5min;
c)4℃,12000rpm离心15min,出现分层,小心吸取上层水相(水相体积约占magzol体积的60%)到新的1.5ml离心管中;
d)加入与上清液等体积的异丙醇(约0.6ml),上下颠倒混匀,-20℃沉淀1h以上;
e)4℃,12000rpm离心30min,管底可见白色沉淀,去掉上清;
f)加75%的乙醇1ml,轻轻吹吸使沉淀飘浮,4℃12000rpm离心5min;
g)重复步骤f;
h)去掉上清液后短暂离心,使用10μl枪吸干,将离心管盖打开干燥,待沉淀干燥至半透明状即加入适量rnase-freeh2o溶解。
i)rna质检,nanodrop检测rna含量,1%琼脂糖凝胶电泳检测rna的完整性。
3、q-pcr检测流程
3.1rna反转录
a)以样品提取的总rna作为模板,建立如下反应体系:
表1反应体系
b)以上体系混匀,离心收集液体至管底,42℃60min,72℃10min;产物即为cdna模板。
3.2定量pcr
a)按下表建立反应体系:
表2反应体系
其中egfr引物和内标基因gapdh引物序列见表3。
表3引物序列
b)按如下程序进行real-timepcr扩增:
95℃预变性10min,然后进入如下循环
*95℃10s
60℃20s
70℃10s
读板
返回*共进行40个循环
制作熔解曲线:70℃至95℃之间,每0.5℃读板一次并停5s。
4、抑制效果
以gapdh为内标基因,通过δδct计算egfrmrna的相对表达量。与转染ncsirna相比,egfrsirna对egfrmrna的抑制率达87%。各组细胞mrna的表达水平见表4,图3。
表4mrna表达水平
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换等,均应包含在本发明的保护范围之内。
本文描述的前述实施例和方法可以基于本领域技术人员的能力、经验和偏好而有所不同。
本发明中,仅按一定顺序列出方法的步骤并不构成对方法步骤顺序的任何限制。
序列表
<110>北京键凯科技股份有限公司
<120>一种有效抑制表皮生长因子受体表达的sirna序列
<130>p0102020070583
<160>2
<170>siposequencelisting1.0
<210>1
<211>19
<212>dna/rna
<213>人工序列(artificialsequence)
<400>1
gcaacaugucgauggacuu19
<210>2
<211>19
<212>dna/rna
<213>人工序列(artificialsequence)
<400>2
aaguccaucgacauguugc19
- 还没有人留言评论。精彩留言会获得点赞!