5′-尿苷单磷酸晶体及其制备方法与流程
本发明涉及属于食品添加剂的精制领域,具体涉及5′-尿苷单磷酸晶体及其制备方法。
背景技术:
5′-尿苷酸,(uridine-5′-monophosphate),参与肝脏解毒物质葡萄糖醛酸的生物合成,肿瘤细胞和被感染的病毒细胞可以有效地释放核苷,有抗病毒效果,可以作为重要的医药中间体,是最重要的抗病毒、抗肿瘤药物之一(expparasitol,1999,adjei)。尿苷酸也是一种重要的功能性食品添加剂,具有助鲜功能和提高生物体免疫功能,其中大多高端婴幼儿奶粉中均有添加,如雀巢、光明、美素佳儿、飞鹤等,是改善促进婴儿肠道发育减轻婴儿腹泻情况的有效成分。也可以用作饲料添加剂,用于猪、牛、鱼、虾等动物的饲养,可改善动物肠绒毛发育,提升动物免疫力和应激能力(动物营养学报,2019,李彪)。同时,也可用作天然植物生长调节剂,以叶面肥的形式喷洒植物,对于提升土豆、甘薯等块茎类植物的亩产很有效果。已报道的5′-尿苷酸的制备方法主要有3种:以糖为基质的微生物直接发酵法、以胞苷为底物的酶催化法和以rna为原料的酶解法。无论哪种方法,要想获得高品质高纯度的产品,其最后一道单元操作都是结晶。5′-尿苷酸与其金属盐系列产品在功能上具有相似性,但在其使用上有各自的特点,现有市场上5′-尿苷酸的产品多以其二钠盐的形式存在,c9h11n2na2o9p,分子量368.14g/mol,casno.3387-36-8,白色粉末,其结晶制备方法在专利zl201310408315.5中已有报道。然而,5′-尿苷酸的结晶一直是业内的难题,主要原因是5′-尿苷酸在水溶液中极易产生分子间缔合,即便体系已达到其临界饱和点,产生过饱和度,分子间无法形成有规律的聚集体(成核),尿苷酸分子之间难以成核,反而以油相的形式进行,产生油水两相,进一步阻碍晶体成核,无法获得高品质的尿苷酸晶体。
技术实现要素:
发明目的:本发明所要解决的技术问题是针对现有技术的不足,提供一种5′-尿苷单磷酸晶体。
本发明还要解决的技术问题是提供上述5′-尿苷单磷酸晶体的制备方法。
为了解决上述第一个技术问题,本发明公开了5′-尿苷单磷酸晶体,其分子式为c18h48n4o29p2,晶体结构为(umph2)2·11h2o,属于正交晶系,空间群为c2221,晶胞参数为
其中,所述的5′-尿苷单磷酸晶体的晶体粉末x-射线衍射分别在2θ为7.70°、8.94°、11.88°、13.98°、15.92°、17.76°、17.92°、20.42°、21.86°、23.24°处有强吸收峰,具体结构信息参见附图2。
其中,所述的5′-尿苷单磷酸晶体的结晶粉末的堆密度不小于0.35g/ml,优选为不小于0.41g/ml,进一步优选为不小于0.46g/ml。
其中,所述的堆积密度为与粉末的流动特性相关的量,堆密度指出在预定条件下每体积单位粉末的重量;堆密度表示为通常以g/ml计的每体积单位的重量。
堆积密度大的粉末,其比重往往较大,可以反映出晶体产品比较厚实,有质感,其稳定性也会相对较好;从另一个角度讲,堆积密度大的产品,颗粒的流动性一般较好,也便于储存和运输,更便于与其他组分高效混合。
具体地,所述颗粒堆积密度按照usp方法ii(第1914页)来测定。
将上述晶体配制成质量分数为5%的水溶液时,体系ph值在1.0~2.5之间,优选1.6~2.3。
为了解决上述第二个技术问题,本发明公开了上述5′-尿苷单磷酸晶体的制备方法,以5′-尿苷酸二钠盐为出发原料,在特定体系下,借助超声辅助成核,以反应结晶耦合溶析结晶的方式促进晶体生长,获得高品质的5′-尿苷酸晶体产品。
具体地,包括如下步骤:
(1)将5′-尿苷酸二钠固体粉末溶于水,配置成5′-尿苷酸二钠水溶液,将其置于设有超声发射装置的结晶器中,开启搅拌,用盐酸调节体系ph为4.0~4.1,在体系温度为5~15℃的条件下稳定30min;
(2)向步骤(1)所得反应体系中缓慢加入异丙醇,搅拌反应30min;
(3)开启超声发射装置,在50w的功率下作用于步骤(2)所得反应体系5~10min,至该体系变浑浊,有明显成核出现;关闭超声发射器,搅拌状态下养晶2h,至该体系中有较多的晶体颗粒出现,且不再增多;
(4)向步骤(3)所得体系中同时加入溶析剂和反应剂至体系的ph降低至0.5~2.0,过程中维持搅拌;
(5)停止滴加溶析剂和反应剂,维持体系温度在5~15℃之间,继续搅拌4~6h;
(6)下罐,晶浆固液分离,洗涤,干燥,即得。
上述过程中对搅拌的速率没有具体的要求,优选为180-300r/min。
上述过程中,步骤(1)~步骤(5)的温度维持为5~15℃。
步骤(1)中,所述的5′-尿苷酸二钠水溶液中5′-尿苷酸二钠的质量分数为5%~20%,优选为8%~15%,进一步优选为10%~12%。
步骤(1)中,盐酸的质量分数为10%~20%。
步骤(1)中,在体系ph为4.0~4.1时,5′-尿苷酸以一价阴离子的形式存在。
步骤(2)中,对于异丙醇的添加速率没有具体的要求,适当慢一点好,如10min内加完所需的异丙醇。
步骤(2)中,控制异丙醇的加入量,使得体系在当前温度下能形成一定的过饱和的度,处于介稳状态,同时,没有分相或相变出现;所述的异丙醇的加入量与步骤(1)中5′-尿苷酸二钠水溶液中5′-尿苷酸二钠的质量分数相关,高浓度体系下,加入异丙醇的量要低于低浓度下加入异丙醇的量。
具体地,当5%≤5′-尿苷酸二钠的质量分数<8%时,异丙醇的体积为5′-尿苷酸二钠水溶液体积的1.0~1.2倍;当8%≤5′-尿苷酸二钠的质量分数<12%时,异丙醇的体积为5′-尿苷酸二钠水溶液体积的0.7~1.0倍;当12%≤5′-尿苷酸二钠的质量分数<16%时,异丙醇的体积为5′-尿苷酸二钠水溶液体积的0.5~0.7倍;当16%≤5′-尿苷酸二钠的质量分数≤20%时,异丙醇的体积为5′-尿苷酸二钠水溶液体积的0.3~0.5倍。
步骤(3)中,开启超声发射装置,利用超声波辅助处于介稳状态下的过饱和溶液成核,诱导5′-尿苷酸以一钠盐的形式首先成核,避免分子间过度缔合而形成油析分相。利用超声波的空化效应,使得处于过饱和状态下体系中的溶质分子获得额外的能量,降低溶质分子间聚集的表面能,促使处于缔合状态下的无规律的溶质分子聚集体克服成核能垒,进而发生有规律的调整,形成晶核并生长至表观可见的晶粒。
步骤(3)中,所述养晶2h是必要的,超声辅助成核后,体系中产生了相变,析出的晶核在搅拌的作用下会增多并长大,消耗掉体系中的过饱和度需要一定的时间,同时这个过程使析出的晶体更加稳定。
步骤(4)中,所述的溶析剂为无水乙醇;所述的反应剂为质量分数为2%~4%的盐酸;其中,所述的溶析剂能够进一步降低溶质在体系中的溶解度,使更多的溶质析出,提高结晶收率;所述的反应剂可以使析出的5′-尿苷酸一钠盐逐步转化为5′-尿苷酸。
步骤(4)中,所述的溶析剂和反应剂需缓慢滴加或泵入,快的速度不利于晶体的长大,过慢的速度会降低结晶过程的效率;优选地,所述的溶析剂的加入速率为2ml/min;所述的反应剂的加入速率为1ml/min;需要指出的是,如果体系放大,则流速可依据实际情况参照比例做出调整。
步骤(4)中,当体系的ph小于2.0时,才能保证体系中的5′-尿苷酸一钠盐较为彻底的转化为5′-尿苷酸。同时,过低的ph会使带来盐酸的过量使用,增加结晶所需反应剂的用量,带来后续结晶母液的废水处理成本增多。因此,结晶终点的ph控制在0.5~2.0,优选1.0~1.5。
步骤(5)中,当体系的ph降低至0.5~2.0后,停止滴加溶析剂和反应剂,维持体系温度不变,继续搅拌4~6h,意在使5′-尿苷酸晶体有一个后熟过程,使晶体的颗粒分布更加均一。
步骤(6)中,所述的晶浆固液分离的方式为抽滤或离心。
步骤(6)中,所述的洗涤是必要的,可以使用乙醇、异丙醇、甲醇、丙醇等溶剂进行洗涤,优选地,用体积分数为90%的乙醇洗涤,有利于洗去晶浆中的杂质。
步骤(6)中,所述的干燥为通过40~50℃鼓风干燥进行烘干。需要指出的是,过高的干燥温度,容易使产品失去部分结晶水,从而引起后续产品的吸潮,过低的温度会使烘干效率降低。烘干时间依据样品的量而定,对于小于1kg的湿滤饼,在铺开呈小于1cm厚度的情况下,4~8h即可完成干燥。需要指出的是,上述结晶粉末会因为干燥方式的不同,或储存环境湿度的不同而展现出不同的表观水含量(包含自由水和结合水),因此,引起结晶粉末可能具有19.5~26.0wt%的水含量,优选23~24wt%。
其中,所述结晶粉末水含量的测定方法为卡尔费休法,可以通过瑞士万通的870titrinoplus实用型容量法卡尔费休水分测定仪进行测定。
本发明所涉及5′-尿苷酸的其他相关检测方法如下:
单晶x-ray衍射测定晶体结构与解析方法:取培养出的5′-尿苷酸单晶,切割成约0.10×0.20×0.30mm3大小的块状,经布鲁克apex-iiccd衍射仪mokα放射源(石墨单色器,
粉末x-ray衍射:研磨后的样品,取约0.1g,通过粉末x射线衍射仪(日本理学smartlab或brukerd8advance)在室温下进行衍射数据收集,光源为cukα射线
5′-尿苷酸液相纯度检测方法:取待测固体样品溶于超纯去离子水,用高效液相色谱仪进行测定,色谱柱为zorbaxsb-aqc18柱,柱规格为250×4.6mm,5μm,检测器为紫外检测器,检测波长254nm。测定过程中柱温为室温,所用流动相为溶剂a(2.3g/l磷酸二氢铵和3.5%(v/v)的甲醇的混合水溶液)和溶剂b(纯甲醇),流速为1ml/min。测定过程采用梯度洗脱方式,总分析时间为15min。首先用溶剂a冲洗色谱柱,然后从第2min到第8min采用线性梯度的方式将流动相变为89%(v/v)的溶剂a和11%(v/v)的溶剂b,并在此梯度维持1min,然后再在1min内变为100%的溶剂a,维持在溶剂a直到分析结束。
钠离子测定方法:取待测固体样品溶于超纯去离子水,使用钠离子浓度计(dws-51,上海仪电科技股份有限公司)进行测定,在测定之前,用二异丙胺将溶液ph调节至10到10.5之间。钠离子浓度计使用前经过氯化钠标准溶液进行标定。
样品稳定性实验:取待测固体粉末样品约20.0g,密封、避光、室温下储存1年和2年,以纯水为对照,分别测试储存1年后样品、储存2年后样品的t430nm(取1g样品,溶于20ml水,分光光度计测试),同时观察其表观流动性。
有益效果:与现有技术相比,本发明具有如下优势:
(1)提供了一种高品质5′-尿苷酸晶体产品的结晶制备方法,解决了5′-尿苷酸在结晶过程中成核困难的问题,获得了稳定性良好的高品质5′-尿苷酸晶体产品,所得产品纯度大于99.5%,收率可达95.4%,堆密度可达0.51g/ml。
(2)本发明提供了5′-尿苷酸的晶体结构,其分子式为c18h48n4o29p2,晶体结构为(umph2)2·11h2o,正交晶系c2221空间群,
附图说明
下面结合附图和具体实施方式对本发明做更进一步的具体说明,本发明的上述和/或其他方面的优点将会变得更加清楚。
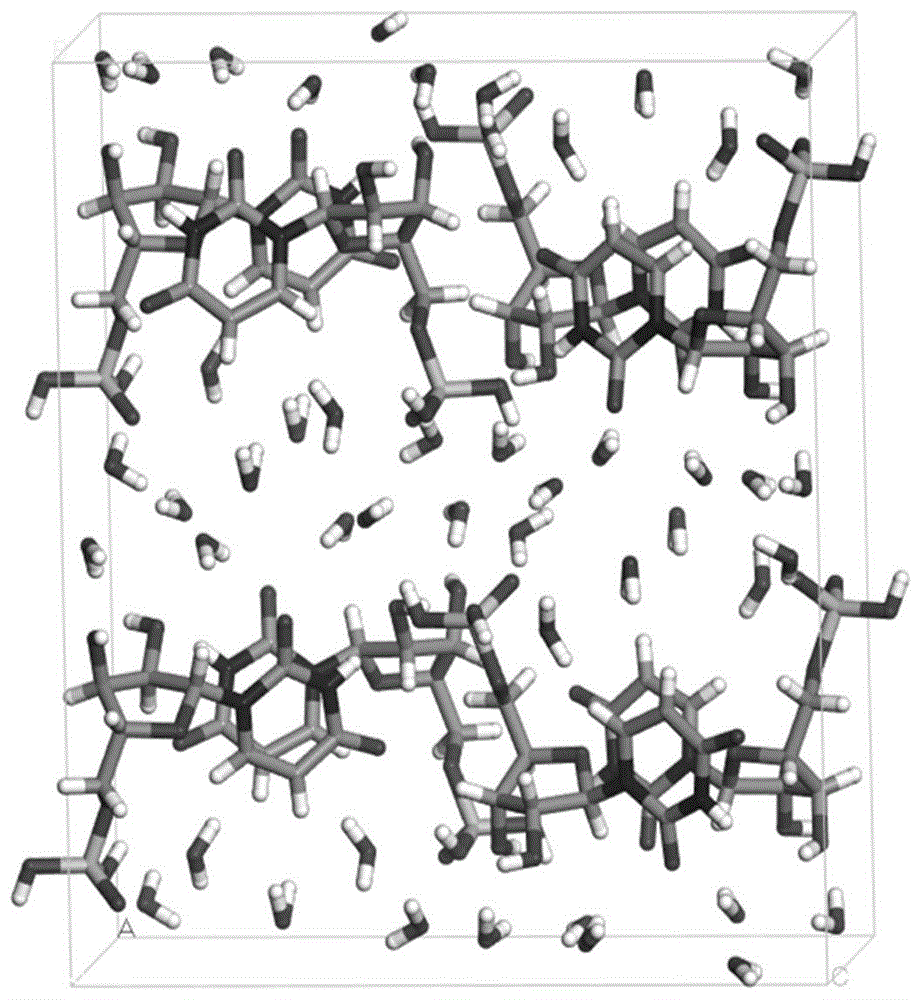
图1为5′-尿苷酸的晶胞堆积图。
图2为5′-尿苷酸晶体粉末的粉末x-射线衍射谱图。
具体实施方式
实施例1:
取50g5′-尿苷酸二钠固体粉末,配置成1000ml水溶液,测试ph为8.0,将其放入带有超声发射装置的结晶器中,开启搅拌,至下罐前保持搅拌速率150r/min,用质量分数为20%的盐酸调节ph至4.05,然后使用循环水浴控制体系温度为10℃(至下罐前,保持温度不变),稳定30min。缓慢加入1.2倍料液体积的异丙醇,继续搅拌30min。开启超声发射装置,在50w作用5min后,发现体系明显变浊,关闭超声发射开关,继续搅拌2h用于养晶,发现过程中晶体数量明显增多至不再增加。2h过后,以2ml/min的流速泵入无水乙醇,同时以1ml/min的流速泵入质量分数为2%的盐酸,检测体系中ph的变化,当ph降至1.0时,停止流加,继续保持搅拌约4h。将晶浆进行抽滤,并用40ml体积分数为90%的乙醇洗涤后,放入40℃烘箱干燥6h,获得5′-尿苷酸晶体产品,430nm下透光为99.8%,结晶收率为82.2%。测得其堆积密度为0.35g/ml,液相色谱纯度99.8%,卡尔费休法测的水分含量为23.2±0.2%,钠离子含量低于50ppm。取此样品约20.0g,密封、避光、室温下储存1年和2年,分别测试储存1年后的样品和储存2年后的样品在430nm下的透光率,分别为99.5%、99.2%,储存后的样品流动性良好,与初始样品相比,无明显差别。
实施例2:
取200g5′-尿苷酸二钠固体粉末,配置成1000ml水溶液,将其放入带有超声发射装置的结晶器中,开启搅拌,至下罐前保持搅拌速率200r/min,用质量分数为10%的盐酸调节ph至4.10,然后使用循环水浴控制体系温度为15℃(至下罐前,保持温度不变),稳定30min。缓慢加入0.3倍料液体积的异丙醇,继续搅拌30min。开启超声发射装置,在50w作用8min后,发现体系明显变浊,关闭超声发射开关,继续搅拌2h用于养晶。2h过后,以2ml/min的流速泵入无水乙醇,同时以1ml/min的流速泵入质量分数为3%的盐酸,检测体系中ph的变化,当ph降至2.0时,停止流加,继续保持搅拌约6h。将晶浆进行抽滤,并用250ml体积分数为90%的乙醇洗涤后,放入45℃烘箱干燥6h,获得5′-尿苷酸晶体产品,430nm下透光为99.8%,结晶收率为95.4%。测得其堆积密度为0.51g/ml,液相色谱纯度99.5%,卡尔费休法测的水分含量为23.8±0.4%,钠离子含量低于50ppm,其晶胞堆积图和粉末x射线衍射图谱分别如图1和图2所示,对应的数据如表1和表2所示。取此样品约20.0g,密封、避光、室温下储存1年和2年,分别测试储存1年后的样品和储存2年后的样品在430nm下的透光率,分别为99.8%、99.6%,储存后的样品流动性良好,与初始样品相比,无明显差别。
表15′-尿苷酸单晶结构数据
表25′-尿苷酸晶体粉末的x-射线衍射数据
实施例3:
取150g5′-尿苷酸二钠固体粉末,配置成1000ml水溶液,将其放入带有超声发射装置的结晶器中,开启搅拌,至下罐前保持搅拌速率200r/min,用质量分数为15%的盐酸调节ph至4.02,然后使用循环水浴控制体系温度为5℃(至下罐前,保持温度不变),稳定30min。缓慢加入0.55倍料液体积的异丙醇,继续搅拌30min。开启超声发射装置,在50w作用10min后,发现体系明显变浊,关闭超声发射开关,继续搅拌2h用于养晶。2h过后,以2ml/min的流速泵入无水乙醇,同时以1ml/min的流速泵入质量分数为4%的盐酸,检测体系中ph的变化,当ph降至0.5时,停止流加,继续保持搅拌约5h。将晶浆进行抽滤,并用150ml体积分数为90%的乙醇洗涤后,放入50℃烘箱干燥4h,获得5′-尿苷酸晶体产品,430nm下透光为99.9%,结晶收率为92.5%。测得其堆积密度为0.48g/ml,液相色谱纯度99.7%,卡尔费休法测的水分含量为23.0±0.5%,钠离子含量低于50ppm。取此样品约20.0g,密封、避光、室温下储存1年和2年,分别测试储存1年后的样品和储存2年后的样品在430nm下的透光率,分别为99.8%、99.4%,储存后的样品流动性良好,与初始样品相比,无明显差别。
实施例4:
取100g5′-尿苷酸二钠固体粉末,配置成1000ml水溶液,将其放入带有超声发射装置的结晶器中,开启搅拌,至下罐前保持搅拌速率200r/min,用质量分数为10%的盐酸调节ph至4.08,然后使用循环水浴控制体系温度为8℃(至下罐前,保持温度不变),稳定30min。缓慢加入0.9倍料液体积的异丙醇,继续搅拌30min。开启超声发射装置,在50w作用5min后,发现体系明显变浊,关闭超声发射开关,继续搅拌2h用于养晶。2h过后,以2ml/min的流速泵入无水乙醇,同时以1ml/min的流速泵入质量分数为2%的盐酸,检测体系中ph的变化,当ph降至1.5时,停止流加,继续保持搅拌约4h。将晶浆进行抽滤,并用100ml体积分数为90%的乙醇洗涤后,放入40℃烘箱干燥8h,获得5′-尿苷酸晶体产品,430nm下透光为99.8%,结晶收率为88.6%。测得其堆积密度为0.40g/ml,液相色谱纯度99.6%,卡尔费休法测的水分含量为23.0±0.3%,钠离子含量低于50ppm。取此样品约20.0g,密封、避光、室温下储存1年和2年,分别测试储存1年后的样品和储存2年后的样品在430nm下的透光率,分别为99.5%、99.3%,储存后的样品流动性良好,与初始样品相比,无明显差别。
对比例1:
同实施例3,不同的是不使用超声波处理。具体地,取150g5′-尿苷酸二钠固体粉末,配置成1000ml水溶液,将其放入结晶器中,用质量分数为15%的盐酸调节ph至4.02,然后使用循环水浴控制体系温度为5℃,稳定30min。缓慢加入0.55倍料液体积的异丙醇,继续搅拌30min。保持超声发射装置处于关闭状态,继续10min后,体系没有明显变化,没有相变发生,继续搅拌2h,体系依然没有任何相变发生。2h过后,以2ml/min的流速泵入无水乙醇,同时以1ml/min的流速泵入质量分数为4%的盐酸,检测体系中ph的变化。流加30min后发现体系开始出现油析现象,流加1h后,停止搅拌,发现体系出现水油两项分层。继续搅拌,继续流加,当ph降至0.5时,停止流加,继续保持搅拌约5h。体系的状态由水油两相转化至膏状固相析出,并粘附在结晶器表面和搅拌桨叶上,无法形成晶态固体。
对比例2:
同实施例3,不同的是调节ph分别至1.0、3.0、3.5、4.5、5.5时(而非4.0-4.1),进行超声处理。具体地,取5份150g5′-尿苷酸二钠固体粉末,配置成5份1000ml水溶液,分别将其放入带有超声发射装置的结晶器中,用质量分数为15%的盐酸分别调节ph至1.0、3.0、3.5、4.5、5.5,然后使用循环水浴控制体系温度为5℃,稳定30min,此时体系没有明显变化。分别缓慢加入0.55倍料液体积的异丙醇于结晶器中,继续搅拌30min,ph为1.0、3.0、3.5的处理此时体系均没有明显变化,ph为4.5和5.5的两个处理,已经发生团状聚结。开启超声发射装置,在50w下作用10min后,ph为1.0、3.0、3.5的处理体系依然没有明显变化,ph为4.5和5.5的两个处理,团状聚集体崩解成小块状,继续作用30min,ph为1.0、3.0、3.5的处理体系仍没有明显变化,ph为4.5和5.5的两个处理,团状聚集体分散成无定形小颗粒状。关闭超声发射开关,继续搅拌2h。2h过后,对于ph为1.0的处理,以2ml/min流速泵入无水乙醇,流加45min后,体系出现明显油析分层,继续流加,体系的状态由水油两相转化至膏状固相析出,并粘附在结晶器表面和搅拌桨叶上,无法形成晶态固体。ph3.0、3.5、4.5和5.5的四个处理,以2ml/min流速泵入无水乙醇,同时以1ml/min的流速泵入质量分数为4%的盐酸,当流加至体系ph低于1.5时,四个结晶器中的均呈现膏状团聚物,无法形成晶态固体。
对比例3:
同实施例3,不同的是调节ph至4.0~4.1后,不使用异丙醇,而直接加入相同当量的乙醇后,进行超声。具体地,取150g5′-尿苷酸二钠固体粉末,配置成1000ml水中,将其放入结晶器中,用质量分数为15%的盐酸调节ph至4.02,然后使用循环水浴控制体系温度为5℃,稳定30min。缓慢加入0.55倍料液体积的乙醇,继续搅拌30min。开启超声发射装置,在50w作用10min后,体系无明显变化,无成核发生,继续超声作用30min后,体系无明显变化,无成核发生。关闭超声发射开关,继续搅拌2h,体系无明显变化,无成核发生。2h过后,以2ml/min的流速泵入无水乙醇,同时以1ml/min的流速泵入质量分数为4%的盐酸,检测体系中ph的变化,流加1h后,发现体系开始出现油析现象,此时停止流加,开启超声波,作用10~15min,体系中出现膏状团聚物,粘附至结晶器和搅拌桨上,无法发生有效成核,进而形成晶态颗粒,导致结晶失败。
对比例4:
同实施例3,不同的是晶浆固液分离后,烘干条件变化,调整为鼓风干燥温度80℃,4h。具体地,取150g5′-尿苷酸二钠固体粉末,配置成1000ml水中,将其放入带有超声发射装置的结晶器中,用质量分数为15%的盐酸调节ph至4.02,然后使用循环水浴控制体系温度为5℃,稳定30min。缓慢加入0.55倍料液体积的异丙醇,继续搅拌30min。开启超声发射装置,在50w作用10min后,发现体系明显变浊,关闭超声发射开关,继续搅拌2h用于养晶。2h过后,以2ml/min的流速泵入无水乙醇,同时以1ml/min的流速泵入质量分数为4%的盐酸,检测体系中ph的变化,当ph降至0.5时,停止流加,继续保持搅拌约5h。将晶浆进行抽滤,并用150ml体积分数为90%的乙醇洗涤后,放入80℃烘箱干燥4h,获得5′-尿苷酸晶体粉末,430nm下透光为99.8%,结晶收率为82.5%。测得其堆积密度为0.46g/ml,液相色谱纯度98.8%,卡尔费休法测的水分含量为8.0±1.4%,钠离子含量低于50ppm。取此样品约20.0g,密封、避光、室温下储存1年和2年,分别测试储存1年后的样品和储存2年后的样品在430nm下的透光率,分别为95.8%、92.2%,储存后的样品颜色略黄,流动性与初始样品相比,无明显差别。
对比例5:
同实施例3,不同的是将0.55倍料液体积的异丙醇分别替换为1.0和0.4倍。结果发现,对于分别加入1.0和0.4倍料液体积的异丙醇的情况,在开启超声发射装置进行超声后,并没有出现晶体成核,体系的过饱和度不能达到有效范围,因而超声并不能达到促进成核的目的。在后续流加无水乙醇和盐酸的过程中,出现油析,进而团聚,无法获得有效晶体产品。
实施例对比例总结梳理见表3。
表3
对比例6:
在现有技术中,并未找到关于5′-尿苷单磷酸结晶的成功报道。在实验中,以采取喷干的方式制备的5′-尿苷单磷酸固体粉末作为对照。
具体地,取500g5′-尿苷酸二钠固体粉末,配置成5000ml水溶液,经过阴离子交换树脂吸附,而后使用1mol/l盐酸进行洗脱,获得5′-尿苷单磷酸水溶液,使用喷雾干燥器直接喷干获得5′-尿苷单磷酸固体粉末,堆密度为0.32g/m,与实施例3所得晶体产品相比,此喷干样品流动性较差。以水为对照,测试得t430nm的透光率为95.6%,同时,放置1年、2年后,测得透光率分别为89.4%、81.6%,储存后的样品颜色较黄。
本发明提供了5′-尿苷单磷酸晶体及其制备方法的思路及方法,具体实现该技术方案的方法和途径很多,以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。本实施例中未明确的各组成部分均可用现有技术加以实现。
- 还没有人留言评论。精彩留言会获得点赞!