羰基吡唑类抗肿瘤化合物及制备方法和应用
1.本发明涉及一种羰基吡唑类抗肿瘤化合物及其制备方法、药物组合物与医药用途,属于医药技术领域。
背景技术:
2.羰基吡唑类化合物具有多种生物学活性,被广泛应用于抗菌、抗病毒、抗疟疾等多种领域,取得了良好的效果。
3.2012年,evripidis等人通过虚拟筛选等手段发现了羰基吡唑类化合物bam7,该化合物能诱导bcl-2家族的促凋亡蛋白bax变构激活,启动线粒体介导的内源性凋亡通路,从而诱导细胞凋亡。考虑到bam7对bax蛋白的亲和力较差(ic
50
=3.3μm),他们以bam7为先导化合物,对其进行结构修饰和改造,得到了活性更高的羰基吡唑类衍生物btsa1。btsa1对bax蛋白的亲和力是bam7的13倍,是目前为止活性最高的bax激动剂。在后续的生物学活性评价中他们发现,btsa1能有效地杀伤血液瘤细胞而不损伤正常细胞,但是btsa1对实体瘤细胞的抑制活性仍有较大的提升空间。本发明以btsa1为先导化合物,以羰基吡唑为母核,经过多轮的结构修饰和改造,发现了一系列结构新颖的羰基吡唑类抗肿瘤化合物。在后续的生物学活性评价中,该类羰基吡唑类化合物表现出很高的实体瘤抑制活性,有望开发成新型高效低毒的抗肿瘤药物。
技术实现要素:
4.本发明提供了一种羰基吡唑类抗肿瘤化合物及制备方法和应用。
5.本发明进一步还提供该化合物的药物组合物及医药用途。
6.本发明的技术方案如下:
7.一、羰基吡唑类抗肿瘤化合物
8.一种羰基吡唑类抗肿瘤化合物,是具有通式i结构的化合物,以及其立体异构体、药学上可接受的盐;
[0009][0010]
通式i中,r1代表被1-3个取代基取代或者未被取代的烷基、烷氧基、环烷基、c
5-c
15
芳基、c
6-c
15
芳基c
1-c6烷基、c
3-c
14
杂芳基、c
3-c
14
杂芳基c
1-c6烷基,所述的取代基选自羟基、氰基、硝基、卤素、c
1-c6烷基、c
1-c6卤烷基、c
1-c6烷氧基、c
3-c8环烷基,所述杂原子独立地选自o、s、n或氧化的s或n;
[0011]
通式i中,r2代表氢或被1-3个取代基取代或者未被取代的的c
1-c
12
烷基、c
1-c
12
烷氧基、c
3-c
14
环烷基、c
6-c
15
芳基、c
6-c
15
芳基c
1-c6烷基、c
3-c
14
杂芳基、c
3-c
14
杂芳基c
1-c6烷基,所述的取代基选自羟基、卤素、烷基、卤烷基、氰基、硝基、胍基、氨基、羧基,所述杂原子
独立地选自o、s、n或氧化的s或n;
[0012]
z代表氢,-cooh,-o-(ch2)
n1-conoh,-co-x-(ch2)
n1-conoh,-o-(ch2)
n2-ar-(ch)
n3-conoh或者-co-x-(ch2)
n2-ar-(ch)
n3-conoh;
[0013]nl
,n2和n3代表0-10的整数;
[0014]
x代表氮原子、氧原子、酰胺;
[0015]
ar代表被1-3个取代基取代或者未被取代的c
5-c7芳基,c
5-c7芳基c
1-c5烷基、c
5-c7芳基c
2-c5烯基、c
3-c6杂芳基、c
3-c6杂芳基c
1-c5烷基、c
3-c6杂芳基c
2-c5烯基,所述的取代基选自c
1-c6卤烷基、c
1-c6烷氧基、卤烷基、卤素、羟基、硝基、氰基、c
3-c8环烷基、芳基、杂芳基。
[0016]
根据本发明优选的,通式i中:
[0017]
r1为被1-3个取代基取代或者未被取代的c
3-c8环烷基、含有5或6个环原子的单环芳基或具有8-15个环原子的双环芳基、含有1-2个杂原子的环原子数为5或6的单杂环芳基或含有1-4个杂原子环原子数为8-15的双杂环芳基,所述的取代基选自羟基、氰基、硝基、卤素、c
1-c6烷基、c
1-c6卤烷基、c
1-c6烷氧基,所述杂原子独立地选自o、s、n或氧化的s或n;
[0018]
r2为氢、被1-3个取代基取代或者未被取代的c
1-c
12
烷基、c
3-c
14
环烷基、c
6-c
10
芳基、c
6-c
10
芳基c
1-c6烷基、c
3-c9杂芳基、c
3-c9杂芳基c
1-c6烷基,所述的取代基选自氰基、卤素、硝基、羧基、甲基、三氟甲基、胍基或者氨基;
[0019]
z代表氢,-cooh,-o-(ch2)
n1-conoh,-co-x-(ch2)
n1-conoh,-o-(ch2)
n2-ar-(ch)
n3-conoh或者-co-x-(ch2)
n2-ar-(ch)
n3-conoh;
[0020]nl
,n2和n3代表0-8的整数;
[0021]
x代表氮原子、氧原子;
[0022]
ar代表被1-3个取代基取代或者未被取代的c
6-c7芳基、c
6-c7芳基c
1-c3烷基、c
6-c7芳基c
2-c3烯基、c
3-c6杂芳基、c
3-c6杂芳基c
1-c3烷基、c
3-c6杂芳基c
2-c3烯基,所述的取代基选自c
1-c6烷基、三氟甲基、卤素、羟基、硝基、氰基。
[0023]
根据本发明进一步优选的,通式i中:
[0024]
r1代表c
5-c6环烷基、噻唑基或取代苯基;
[0025]
r2代表c
1-c6烷基、c
3-c6环烷基、取代或者未被取代的苯基、取代或者未被取代的萘基、所述的取代基选自氰基、卤素、硝基、羧基、甲基、三氟甲基、胍基或者氨基;
[0026]
z代表氢,-cooh,-o-(ch2)
n1-conoh,-co-x-(ch2)
n1-conoh,-o-(ch2)
n2-ar-(ch)
n3-conoh或者-co-x-(ch2)
n2-ar-(ch)
n3-conoh;
[0027]nl
代表3-8的整数,n2代表0-2的整数,n3代表0-3的整数;
[0028]
x代表氮原子、氧原子;
[0029]
ar代表被1-3个取代基取代或者未被取代的苯基、哒嗪基、吡嗪基、吡啶基、吡咯基、吡唑基、噻唑基、咪唑基、噻吩基、噁唑基,所述的取代基选自卤素、甲基、乙基、甲氧基、乙氧基、三氟甲基、羟基、硝基、氰基。
[0030]
根据本发明,更进一步优选的,通式i中:
[0031]
r1代表噻唑;
[0032]
r2苯基;
[0033]
z氢,-cooh,-o-(ch2)
n1-conoh,-co-x-(ch2)
n1-conoh,-o-(ch2)
n2-ar-(ch)
n3-conoh或者-co-x-(ch2)
n2-ar-(ch)
n3-conoh;
[0034]nl
代表3-8的整数;
[0035]
n2为1;
[0036]
n3为0或2;
[0037]
x代表氮原子;
[0038]
ar代表苯环。
[0039]
上述通式i化合物,最优选为如下之一:
[0040]
(z)-n-羟基-4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯甲酰胺(4)
[0041]
(z)-n-(5-(羟氨基)-5-氧戊基)-4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯甲酰胺(20)
[0042]
(z)-n-(6-(羟基氨基)-6-氧己基)-4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯甲酰胺(21)
[0043]
(z)-n-(7-(羟基氨基)-7-氧庚基)-4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯甲酰胺(22)
[0044]
(z)-n-羟基-4-((4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基))-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯甲酰胺基)甲基苯甲酰胺(23)
[0045]
n-(4-((e)-3-(羟基氨基)-3-氧代丙-1-烯-1-基)苄基)-4-(2-((z)-5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基亚基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯甲酰胺(24)
[0046]
(z)-n-羟基-4-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)亚烷基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)丁酰胺(46)
[0047]
(z)-n-羟基-5-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)亚烷基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)戊酰胺(47)
[0048]
(z)-n-羟基-6-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基))-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)己酰胺(48)
[0049]
(z)-n-羟基-7-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)庚酰胺(49)
[0050]
(z)-n-羟基-8-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基))-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)辛酰胺(50)
[0051]
(z)-n-羟基-4-((4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基))-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)甲基)苯甲酰胺(51)
[0052]
(e)-n-羟基-3-(4-((4-(2-((z)-5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)-4],5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)甲基)苯基)丙烯酰胺(52)
[0053]
以上优选化合物,后面的括号内的编号是对应于下面反应路线及表1中的化合物结构的编号。
[0054]
发明详述
[0055]
本文中所用的术语和定义含义如下:
[0056]
本发明所述的“卤素原子”包括氟原子、氯原子、溴原子、碘原子;
[0057]
本发明所述“c
1-10
烷基”指含有1~10个碳原子的烷烃部分去除一个氢原子衍生的直链或支链的烷基,如甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊
基、异戊基、2-甲基丁基、3-甲基丁基、1,1-二甲基丙基、1,2-二甲基丙基、新戊基、1-乙基丙基、正己基、异己基、2-甲基戊基、3-甲基戊基、4-甲基戊基、1,1-二甲基丁基、1,2-二甲基丁基、1,3-二甲基丁基、2,2-二甲基丁基、2,3-二甲基丁基、3,3-二甲基丁基、1-乙基丁基、2-乙基丁基、1,1,2-三甲基丙基、1,2,2-三甲基丙基、1-乙基-1-甲基丙基,1-乙基-2-甲基丙基,庚基,辛基,壬基和癸基。优选c
1-6
烷基,更优选c
1-4
烷基,术语“c
1-6
烷基”、“c1-4烷基”指上述实例中的含有1~6个、1~4个碳原子的具体实例;
[0058]
本发明所述的“c
3-8
环烷基”是指3~8个碳原子的烷烃部分去除一个氢原子衍生的环状烷基,如环丙基、环丁基、1-甲基环丁基、环戊基、环己基、环庚基、环辛基等。优选c
4-7
环烷基、c
4-6
环烷基和c
5-6
环烷基;
[0059]
所述“单杂环基”的实例有:环氧乙烷基、二氧杂环丙烷基、硫杂环丙烷基、氮杂环丙烷基、2h-氮杂环丙烷基、二氮杂环丙烷基、3h-二氮杂环丙烯基、氧氮杂环丙烷基、氧杂环丁烷基、1,2-二氧杂环丁烷基、硫杂环丁烷基、1,2-二硫杂环丁烯基、氮杂环丁烷基、1,2-二氮杂环丁烷基、氮杂环丁二烯基、1,2-二氮杂环丁烯基、呋喃基、四氢呋喃基、噻吩基、2,5-二氢噻吩基、四氢噻吩基、吡咯基、二氢吡咯基、吡咯烷基、1,3-二氧杂环戊烷基、1,3-二氧杂环戊烯-2-酮基、1,2-二硫杂环戊烯基、1,3-二硫杂环戊烷基、咪唑基、4,5-二氢咪唑基、咪唑烷基、吡唑基、4,5-二氢吡唑基、吡唑烷基、噁唑基、4,5-二氢噁唑基、异噁唑基、4,5-二氢异噁唑基、2,3-二氢异噁唑基、1,2,3-噁二唑基、1,2,5-噁二唑基、噻唑基、4,5-二氢噻唑基、异噻唑基、1,2,3-噻二唑基、1,2,4-噻二唑基、1,3,4-噻二唑基、1,2,3-三唑基、1,2,4-三唑基、四唑基、2h-吡喃基、2h-吡喃-2-酮基、3,4-二氢-2h-吡喃基、4h-吡喃基、四氢吡喃基、4h-吡喃-4-酮基、吡啶基、2-吡啶酮基、4-吡啶酮基、哌啶基、1,4-二氧杂环己二烯基、1,4-二硫杂环己二烯基、1,4-氧硫杂环己二烯基、1,4-二氧杂环己烷基、1,3-二氧杂环己烷基、1,3-氧硫杂环己烷基、2h-1,2-噁嗪基、4h-1,2-噁嗪基、6h-1,2-噁嗪基、2h-1,3-噁嗪基、4h-1,3-噁嗪基、6h-1,3-噁嗪基、2h-1,4-噁嗪基、4h-1,4-噁嗪基、5,6-二氢-4h-1,3-噁嗪基、吗啉基、2h-1,3-噻嗪基、4h-1,3-噻嗪基、5,6-二氢-4h-1,3-噻嗪基、6h-1,3-噻嗪基、2h-1,4-噻嗪基、4h-1,4-噻嗪基、哒嗪基、嘧啶基、吡嗪基、哌嗪基、1,2,3-三嗪基、1,2,4-三嗪基、1,3,5-三嗪基、1,2,4,5-四嗪基、氧杂环庚三烯基、硫杂环庚三烯基、1,4-二氧杂环辛三烯基、氮杂环庚三烯基、1,2-二氮杂环庚三烯基、1,3-二氮杂环庚三烯基、1,4-二氮杂环庚三烯基、氮杂环辛四烯基、1,4-二氢-1,4-二氮杂环辛三烯基等;
[0060]“芳基”是指含有芳香环的取代基,如苯基或苄基,其可选地与环烷基稠合,所述环烷基优选地具有4-7个环原子,更优选具有5-6个环原子。优选的芳基含有5-15个碳原子;
[0061]“杂芳基”是芳香杂环,可以是单环或双环基团。他们含有芳杂基含有一个或多个杂原子,优选为1-3个杂原子、甚至更优选1-2个杂原子,所述杂原子独立地选自o、s和n。“芳基烷基”是指c
1-c4亚烷基连接的芳基;
[0062]“芳基烷基”是指c
1-c4亚烷基连接的芳基;
[0063]“芳基烷基”是指c
1-c4亚烷基连接的杂芳基;
[0064]“烯基”,单独或联合地,文中所指为直链烃或支链烃,其含有2-6个,优选为2-4个碳原子;并且含有1-2个碳碳双键,优选为1个碳碳双键;
[0065]“烷氧基”,表示基团―o―烷基;
[0066]
本发明所述“0-8的整数”是指0、1、2、3、4、5、6、7、8;
[0067]
本发明的通式i所示化合物可以通过公知的方法制成药学上可接受的盐,该盐是指式i所示化合物与酸或碱混合制成的盐;
[0068]
适宜的酸加成盐是由形成无毒盐的酸形成。具有代表性的酸加成盐包括但不限于乙酸盐、己二酸盐、藻酸盐、柠檬酸盐、天冬氨酸盐、苯甲酸盐、苯磺酸盐、硫酸氢盐、碳酸氢盐、丁酸盐、樟脑酸盐、樟脑磺酸盐、碳酸盐、柠檬酸盐、二葡糖酸盐(digluconate)、甘油磷酸盐、半硫酸盐(hemisulfate)、庚酸盐、己酸盐、甲酸盐、富马酸盐、葡萄糖酸盐、葡萄糖醛酸盐、谷氨酸盐、盐酸盐、氢溴酸盐、氢碘酸盐、2-羟基乙磺酸盐(isethionate)、乳酸盐、马来酸盐、苹果酸盐、丙二酸盐、甲磺酸盐、烟酸盐、2-萘磺酸盐、烟酸盐(nicotinate)、硝酸盐、乳清酸盐、草酸盐、棕榈酸盐、扑酸盐、果胶酸盐(pectinate)、过硫酸盐、3-苯基丙酸盐、苦味酸盐(picrate)、三甲基乙酸盐(pivalate)、丙酸盐、蔗糖盐、硬脂酸盐、琥珀酸盐、硫酸盐、酒石酸盐、硫氰酸盐、磷酸盐、磷酸氢盐、磷酸二氢盐、对甲苯磺酸盐、三氟乙酸盐及十一酸盐;
[0069]
碱加成盐可在化合物的最后分离和纯化过程中,通过使含有羧酸的部分与适当的碱(如但不限于药用可接受的金属阳离子的氢氧化物、碳酸盐或碳酸氢盐)或者与氨或有机伯胺、仲胺或叔胺反应原位制备。药用可接受的盐包括但不限于基于碱金属或碱土金属的阳离子,如但不限于锂、钠、钾、钙、镁和铝盐等,以及非毒性季氨和胺阳离子,包括铵、四甲基铵、四乙基铵、甲胺、二甲胺、三甲胺、三乙胺、二乙胺、乙胺等。其它可用于形成碱加成盐的代表性有机胺包括乙二胺、乙醇胺、二乙醇胺、哌啶、哌嗪等;
[0070]
本文中的“立体异构体”是指本发明化合物或其生理上的抗肿瘤化合物所有可能的立体异构体的形式。除非特别指出,本发明中涉及的化合物的化学命名包括所有可能的立体化学形式的混合物,所属混合物包含基本结构分子的所有对映体和非对映体,以及基本纯净的化合物单个异构体形式,即其中含有低于10%,优选低于5%,特别是低于2%,最优选低于1%的其它异构体。本发明类肽化合物各种立体异构体形式均明显包含于本发明的范围内;
[0071]
通式i化合物还能以其它被保护的形式或抗肿瘤化合物的形式存在,这些形式对本领域技术人员而言是显而易见的,均应该包含于本发明的范围内;
[0072]
如上所述的取代基自身还可被一个或多个取代基取代。这样的取代基包括在c.hansch和a.leo,substituent constants for correlation analysis in chemistry and biology(1979)中列出的那些取代基;优选的取代基包括烷基、烯基、烷氧基、羟基、硝基、氨基、氨基烷基、氰基、卤素、羧基、硫基、芳基、环烷基、杂芳基、杂环烷基、亚氨基、羟烷基、芳基氧基、芳基烷基及其结合;
[0073]
本发明化合物可以用本领域已知的方法制成任何药物制剂,以口服、肠胃外、直肠或经肺给药等方式施用于需要这种治疗的患者,用于口服给药时,可制成常规的固体制剂,如片剂、胶囊剂、丸剂、颗粒剂等,也可制成口服液体制剂,如口服溶液剂、口服混悬剂、糖浆剂等。制成口服制剂时,可以加入适宜的填充剂、粘合剂、崩解剂、润滑剂等。用于肠胃外给药时,可制成注射剂,包括注射液、注射用无菌粉末与注射用浓溶液。制成注射剂时,可采用现有制药领域中的常规方法生产,配制注射剂时,可以不加入附加剂,也可根据药物的性质加入适宜的附加剂。用于直肠给药时,可制成栓剂等。用于经肺给药时,可制成吸入剂或喷雾剂等;
[0074]
本发明化合物的施用量和施用频率可以根据临床医生或药师的判断考虑例如以下的一些因素而作出调整:患者的年龄、健康状况和大小,以及待治疗病征的严重性。一般而言,本发明化合物的总日服剂量范围为每天约0.1至约2000mg,尽管必要时会有变化,这取决于治疗目的、患者和施用途径。在一个实施方案中,剂量为约1至约200mg/天,以单一剂量或以2-4个分离剂量给药。在另一个实施方案中,剂量为约10至约2000mg/天,以单一剂量或以2-4个分离剂量给药。在另一个实施方案中,剂量为约100至约2000mg/天,以单一剂量或以2-4个分离剂量给药。在又另一个实施方案中,剂量为约500至约2000mg/天,以单一剂量或以2-4个分离剂量给药。本发明的化合物、其药学上可接受的盐、酯或溶剂化物或它们的前药或异构体与其它治疗活性物质联合使用时,它们同时、分开或依次给药,可制成单一给药方式的药物组合物。联合使用的其它治疗活性物质的用药量可基于临床上所用的量,并可根据给药对象、给药途径、疾病、组合等适当选择。对其它治疗活性物质的给药形式没有特殊限制,只要在给药时将本发明的化合物和其它治疗活性物质组合即可。
[0075]“药物组合物(pharmaceutical co熔点osition)”是指含有治疗上显著量的活性药剂的制备物,其以适于给予患者的形式被制备。因此,所述制备物不含有这样量的任何一种组分或多种组分,即,适当谨慎的医疗实施者发现所述制备物不适于给予普通对象。在许多情况下,这种药物组合物是无菌制备物。
[0076]
本发明中所涉及的“室温”具体的温度范围是25-30℃。
[0077]
二、羰基吡唑类抗肿瘤化合物的制备方法
[0078]
一种羰基吡唑类抗肿瘤化合物的制备步骤:
[0079]
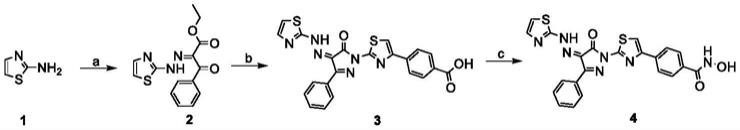
合成路线1:2-氨基噻唑在强酸条件下与亚硝酸钠反应先生成重氮盐,后再与苯甲酰乙酸乙酯反应生成中间体2,在氨基硫脲存在的条件下,中间体2与4-(2-溴乙酰基)苯甲酸反应制得中间体3,而后引入异羟肟酸基团得终化合物4;
[0080]
合成路线2:对乙酰基苯甲酸与各种氨基酸甲酯盐酸盐经酰胺缩合得到中间体5-9,经溴化反应得中间体10-14,经多步环合反应得关键中间体15-19,最后引入异羟肟酸基团得终产物20-24;
[0081]
合成路线3:对羟基苯乙酮与不同结构的溴代甲酸甲酯、反应得到中间体25-31,与溴化铜反应得溴代产物32-38,经多步环化反应得关键中间体39-45,最后引入异羟肟酸基团得终产物46-52;
[0082]
合成路线如下:
[0083]
合成路线1
[0084][0085]
反应试剂和反应条件:(a)(i)亚硝酸钠,浓盐酸,水,0℃,30min;(ii)乙酸钠,本甲酰乙酸乙酯,乙醇,0℃,1h;(b)2-溴苯乙酮或4-(2-溴乙酰基)苯甲酸,氨基硫脲,乙醇,80℃;(c)氯甲酸异丁酯,n-甲基吗啉,四氢呋喃,盐酸羟胺,氢氧化钾,甲醇,rt,6h;
[0086]
合成路线2
[0087][0088]
反应试剂和反应条件:(a)hatu,dipea,二氯甲烷,室温;(b)溴化铜,体积比1:1的乙酸乙酯/氯仿,80℃,3h;(c)氨基硫脲,甲醇,80℃;(d)盐酸羟胺,氢氧化钾,甲醇,室温;
[0089]
合成路线3
[0090][0091]
反应试剂和反应条件:(a)碳酸钾,室温;(b)溴化铜,体积比1:1的乙酸乙酯/氯仿,80℃,3h;(c)氨基硫脲,甲醇,80℃;(d)盐酸羟胺,氢氧化钾,甲醇,室温;
[0092]
所述的氨基酸甲酯盐酸盐是5-氨基戊酸甲酯盐酸盐、6-氨基己酸甲酯盐酸盐、7-氨基庚酸甲酯盐酸盐、8-氨基辛酸甲酯盐酸盐、4-氨甲基苯甲酸甲酯盐酸盐、4-氨甲基肉桂酸甲酯盐酸盐;所述的溴代甲酸甲酯是4-溴代丁酸甲酯、5-溴代戊酸甲酯、6-溴代己酸甲酯、7-溴代庚酸甲酯、8-溴代辛酸甲酯、4-溴甲基苯甲酸甲酯、4-溴甲基肉桂酸甲酯;
[0093]
合成路线中目标化合物的结构如下表1所示:
[0094]
表1目标化合物的结构
[0095][0096][0097]
所述化合物的具体操作步骤将在实施例中详细说明。
[0098]
本领域的技术人员可以对上述步骤进行变动以增加收率,他们可以根据本领域的基本知识设计合成路线,如选择反应物、反应溶剂、反应温度,也可以通过使用各种保护基以避免副反应的发生从而提高收率,这些常规的保护方法可以参见例如t.green protecting groups in organic synthesis。
[0099]
三、羰基吡唑类抗肿瘤化合物的应用
[0100]
本发明还提供了该系列化合物在制备预防或治疗癌症中的应用。
[0101]
此外,本发明还包括一种适于口服给予哺乳动物的药物组合物,包含上述通式i的
任一化合物,药学上可接受的载体,任选包含一种或多种药学上可接受的赋形剂。
[0102]
此外,本发明还包括一种适用于胃肠外给予哺乳动物的药物组合物,包括上述通式i的任一化合物,药学上可接受的载体,任选包含一种或多种药学上可接受的赋形剂。
[0103]
进行体外抗肿瘤细胞增殖活性的测试。
[0104]
化合物的细胞活性测试使用mtt检测法。将肿瘤细胞悬液(人宫颈癌细胞hela)接种于96孔板,每孔加入用培养基稀释的不同浓度的化合物,孵育48小时后用mtt染色,继续孵育4h后用酶标仪在490/570nm处测定每孔的吸光度od值,然后计算出抑制率和ic
50
值,从而确定目标化合物的抗增殖活性。
[0105]
体外bax蛋白亲和力实验结果表明,所有的目标化合物均表现出较好的bax蛋白亲和力,其中化合物23对bax蛋白的亲和力与阳性对照药btsa1相当。
[0106]
体外抗肿瘤细胞增殖实验表明,部分目标化合物,尤其是化合物23对hela细胞展示出较好的抗增殖活性,其对hela细胞的生长抑制活性ic
50
值分别为0.86μm。由此可见本发明中的部分化合物拥有较好抗肿瘤细胞增殖活性,具有很大的开发前景,可用于指导发现新型抗肿瘤活性分子。
具体实施方式
[0107]
下面结合实施例对本发明做进一步的说明,但不限于此。
[0108]
实施例1.(z)-3-氧代-3-苯基-2-(2-(噻唑-2-基)肼基)丙酸乙酯(2)
[0109]
将2-氨基噻唑溶(8g,80mmol)在浓盐酸中冰浴下滴加烟硝酸钠(6.62g,96mmol)的水溶液,滴加完毕后冰浴下反应20min得重氮盐溶液。用乙醇(240ml)溶解苯甲酰乙酸乙酯(12.30g,64mmol),加入乙酸钠(38g,460.8mmol)的水溶液后室温搅拌30min。将重氮盐溶液滴入苯甲酰乙酸乙酯中,冰浴下反应1h,室温反应1h.蒸除乙醇,水相用乙酸乙酯萃取三次,合并有机相,无水硫酸镁干燥后蒸除溶剂得粗品,柱层析得橘红色油状液体,收率54%.1h nmr(400mhz,cdcl3)δ12.80(s,1h),7.96(d,j=7.7hz,2h),7.61(t,j=7.4hz,2h),7.48(t,j=7.7hz,2h),7.39(d,j=3.6hz,1h),6.84(d,j=3.5hz,1h),4.37(q,j=7.2hz,2h),1.32(t,j=7.1hz,3h).
[0110]
(z)-4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯甲酸(3)
[0111]
将4-(2-溴乙酰基)苯甲酸(0.41g,1.66mmol)溶解在乙醇(20ml)中,加入氨基硫脲(0.15g,1.66mmol)室温反应1h,然后加入中间体1(0.5g,1.66mmol),80℃回流3h,有固体析出。冷却至室温,用冰乙醇和乙醚洗涤固体,抽滤得红色固体,收率48%,熔点268-269℃.1h nmr(400mhz,dmso-d6)δ8.16(d,j=7.4hz,2h),8.14
–
8.11(m,2h),8.06
–
8.01(m,3h),7.73(d,j=4.1hz,1h),7.60
–
7.51(m,3h),7.38(d,j=4.0hz,1h).
13
c nmr(101mhz,dmso-d6)δ179.37,167.55,155.33,153.46,149.60,149.30,138.42,132.15,130.88,130.47,130.41,130.36,130.33,128.99,128.50,126.37,114.52,111.81.hrms(ap-esi)m/z,calcd for c
22h14
n6o3s2,([m+h]
+
):475.0642,found:475.0634.
[0112]
(z)-n-羟基-4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯甲酰胺(4)
[0113]
将化合物3(1.59g,4mmol)溶在dmf中,冰浴下滴加氯甲酸异丁酯(0.61ml,
4.8mmol)和n-甲基吗啉(0.58ml,5.2mmol),反应30min得混合酸酐。将新制羟胺溶液(0.53g,16mmol)滴入混合酸酐中,室温反应6h。将反应溶液倒入水中,抽滤得粗品。柱层析得红色固体,收率45%,熔点194-195℃.1h nmr(400mhz,dmso-d6)δ11.29(s,1h),9.05(s,1h),8.23
–
7.93(m,5h),7.86(d,j=8.1hz,2h),7.72(d,j=3.9hz,1h),7.55(q,j=7.2hz,3h),7.35(d,j=3.9hz,1h).
13
c nmr(101mhz,dmso-d6)δ179.76,164.39,155.40,149.41,137.04,133.69,132.33,131.20,130.35,130.26,129.25,128.91,128.51,127.90,126.23,114.76,110.95.hrms(ap-esi)m/z,calcd for c
22h15
n7o3s2,([m+h]
+
):490.0751,found:490.0746.
[0114]
实施例2.5-(4-乙酰基苯甲酰胺基)戊酸甲酯(5)
[0115]
将4-乙酰基苯甲酸(1.64g,10mmol)溶于二氯甲烷中,加入dipea(1.65ml,10mmol)和hatu(4.56g,12mmol)后,室温搅拌30min。加入5-氨基戊酸甲酯盐酸盐(2.01g,11mmol),室温反应8h。用1m hcl,饱和碳酸氢钠溶液、饱和氯化钠溶液洗涤反应液,无水硫酸钠干燥,柱层析得白色固体,收率85%,熔点89-90℃.1h nmr(400mhz,cdcl3)δ8.01(d,j=8.1hz,2h),7.87(d,j=8.0hz,2h),6.48(s,1h),3.69(s,3h),3.49(q,j=6.2hz,2h),2.64(s,3h),2.40(t,j=6.7hz,2h),1.72(qd,j=14.1,7.0hz,4h).
[0116]
6-(4-乙酰基苯甲酰胺基)己酸甲酯(6)
[0117]
具体操作参照化合物5的合成,收率67%,熔点96-98℃.1h nmr(400mhz,cdcl3)δ8.00(d,j=7.9hz,2h),7.86(d,j=7.9hz,2h),6.38(s,1h),3.67(s,3h),3.49(q,j=6.6hz,2h),2.64(s,3h),2.34(t,j=7.3hz,2h),1.76
–
1.60(m,4h),1.50
–
1.34(m,2h).
[0118]
7-(4-乙酰基苯甲酰胺基)庚酸甲酯(7)
[0119]
具体操作参照化合物5的合成,收率96%,熔点101-103℃.1h nmr(400mhz,dmso-d6)δ8.62(t,j=5.1hz,1h),8.02(d,j=7.6hz,2h),7.94(d,j=8.0hz,2h),3.57(s,3h),3.26(dd,j=12.9,6.5hz,2h),2.62(s,3h),2.30(t,j=7.3hz,2h),1.53(s,4h),1.30(s,4h).
[0120]
4-((4-乙酰基苯甲酰胺基)甲基)苯甲酸甲酯(8)
[0121]
具体操作参照化合物5的合成,收率99%,熔点132-134℃.1h nmr(600mhz,cdcl3)δ8.03
–
7.99(m,4h),7.90(d,j=8.4hz,2h),7.42(d,j=8.4hz,2h),6.78(t,j=6.0hz,1h),4.72(d,j=5.9hz,2h),3.91(s,3h),2.63(s,3h).
[0122]
(e)-3-(4-(((4-乙酰基苯甲酰胺基)甲基)苯基)丙烯酸甲酯(9)
[0123]
具体操作参照化合物5的合成,收率71%,熔点175-176℃.1h nmr(400mhz,dmso-d6)δ9.28(t,j=5.7hz,1h),8.04(q,j=8.1hz,4h),7.70(d,j=7.8hz,2h),7.66(d,j=16.0hz,1h),7.38(d,j=7.8hz,2h),6.63(d,j=16.0hz,1h),4.53(d,j=5.8hz,2h),3.73(s,3h),2.63(s,3h).
[0124]
5-(4-(2-溴乙酰基)苯甲酰胺基)戊酸甲酯(10)
[0125]
将中间体5(2.3g,8.3mmol)溶解在乙酸乙酯/氯仿(1:1,80ml)中,加入溴化铜(3.71g,16.6mmol),80℃回流3h.抽滤,滤液柱层析得白色固体,收率72%,熔点82-84℃.1h nmr(400mhz,cdcl3)δ8.05(d,j=8.1hz,2h),7.90(d,j=8.1hz,2h),6.48(s,1h),4.46(s,2h),3.69(s,3h),3.49(q,j=6.2hz,2h),2.40(t,j=6.7hz,2h),1.80
–
1.65(m,4h).
[0126]
6-(4-(2-溴乙酰基)苯甲酰胺基)己酸甲酯(11)
nmr(400mhz,dmso-d6)δ10.35(s,1h),8.51(t,j=5.2hz,1h),8.17(d,j=6.8hz,2h),8.07(d,j=7.8hz,2h),7.98(s,1h),7.93(d,j=7.9hz,2h),7.73(d,j=3.7hz,1h),7.62
–
7.50(m,3h),7.37(d,j=3.7hz,1h),3.27(d,j=6.2hz,2h),1.95(t,j=7.2hz,2h),1.63
–
1.44(m,4h),1.38
–
1.22(m,4h).
13
c nmr(101mhz,dmso-d6)δ179.77,169.61,166.18,155.35,153.40,149.65,149.53,136.83,134.31,132.81,131.07,130.37,129.92,128.96,128.52,128.17,126.09,114.61,110.96,39.70,32.73,29.55,28.85,26.75,25.59.hrms(ap-esi)m/z,calcd for c
29h28
n8o4s2,([m+h]
+
):617.1748,found:617.1735.
[0150]
实施例5.(z)-n-羟基-4-((4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基))-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯甲酰胺基)甲基苯甲酰胺(23)
[0151]
化合物的具体合成方法请参照化合物20的合成,,收率29%,熔点217-219℃.1h nmr(400mhz,dmso-d6)δ12.86(s,1h),11.18(s,1h),9.15(s,1h),8.99(s,1h),8.19(d,j=6.3hz,1h),8.11(d,j=7.9hz,1h),8.05
–
7.84(m,6h),7.72(d,j=7.7hz,2h),7.66(d,j=2.9hz,1h),7.56
–
7.37(m,4h),7.26(d,j=3.1hz,1h),4.54(s,2h).
13
c nmr(101mhz,dmso-d6)δ179.58,166.45,164.64,155.43,153.53,149.67,149.44,143.48,137.21,133.89,133.73,131.79,131.20,130.25,129.15,128.90,128.53,128.31,127.63,127.46,126.21,114.79,111.07,42.99.hrms(ap-esi)m/z,calcd for c
30h22
n8o4s2,([m+h]
+
):623.1278,found:623.1270.
[0152]
实施例6.n-(4-((e)-3-(羟基氨基)-3-氧代丙-1-烯-1-基)苄基)-4-(2-((z)-5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基亚烷基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯甲酰胺(24)
[0153]
化合物的具体合成方法请参照化合物20的合成,收率36%,熔点251-253℃.1h nmr(400mhz,dmso-d6)δ12.34(s,1h),10.09(s,1h),9.15(t,j=5.9hz,1h),8.18(d,j=6.7hz,2h),8.10(d,j=7.8hz,2h),8.00(d,j=7.9hz,2h),7.94(s,1h),7.77
–
7.64(m,3h),7.60(d,j=15.9hz,,1h),7.53(m,3h),7.38(d,j=7.7hz,2h),7.32(d,j=3.3hz,1h),6.50(d,j=15.9hz,1h),4.53(d,j=5.6hz,2h).
13
c nmr(101mhz,dmso-d6)δ181.07,168.08,166.42,155.60,153.45,149.26,144.21,142.59,137.31,133.70,133.29,131.97,129.87,128.90,128.81,128.73,128.58,128.29,128.21,127.94,127.20,126.17,119.20,115.14,110.80,42.99.hrms(ap-esi)m/z,calcd for c
32h24
n8o4s2,([m+h]
+
):649.1435,found:649.1445.
[0154]
实施例7.4-(4-乙酰基苯氧基)丁酸甲酯(25)
[0155]
将对羟基苯乙酮(2.7g,20mmol)溶解在dmf中,加入k2co3(8.3g,60mmol),ki(0.1g)和4-溴丁酸甲酯(3.77ml,30mmol),室温搅拌8h.将反应液倒入水中,乙酸乙酯萃取三次,合并有机相,有机相用饱和氯化钠溶液洗涤两次,无水硫酸钠干燥,抽滤,柱层析得白色固体3.94g,收率83%,熔点64-66℃.1h nmr(400mhz,cdcl3)δ7.92(d,j=8.2hz,2h),6.91(d,j=8.3hz,2h),4.08(t,j=6.0hz,2h),3.70(s,3h),2.55(s,3h),2.53(d,j=7.4hz,2h),2.14(p,j=6.6hz,2h).
[0156]
5-(4-乙酰基苯氧基)戊酸甲酯(26)
[0157]
具体合成方法参照中间体25的合成,收率90%,熔点56-57℃.1h nmr(400mhz,cdcl3)δ7.92(d,j=8.2hz,2h),6.91(d,j=8.2hz,2h),4.03(d,j=5.2hz,2h),3.68(s,
3h),2.55(s,3h),2.41(t,j=6.2hz,2h),1.92
–
1.76(m,4h).
[0158]
6-(4-乙酰基苯氧基)己酸甲酯(27)
[0159]
具体合成方法参照中间体25的合成,收率94%,熔点46-48℃.1h nmr(400mhz,cdcl3)δ7.92(d,j=8.4hz,2h),6.91(d,j=8.4hz,2h),4.02(t,j=6.3hz,2h),3.68(s,3h),2.55(s,3h),2.44
–
2.31(m,2h),1.94
–
1.79(m,2h),1.72(dt,j=15.2,7.4hz,2h),1.52(dt,j=15.1,7.7hz,2h).
[0160]
7-(4-乙酰基苯氧基)庚酸甲酯(28)
[0161]
具体合成方法参照中间体25的合成,收率90%,熔点63-65℃.1h nmr(400mhz,cdcl3)δ7.92(d,j=8.1hz,2h),6.91(d,j=8.2hz,2h),4.02(t,j=6.4hz,2h),3.67(s,3h),2.55(s,3h),2.33(t,j=7.4hz,2h),1.89
–
1.76(m,2h),1.74
–
1.62(m,2h),1.50(dt,j=14.8,7.3hz,2h),1.40(dt,j=14.7,7.4hz,2h).
[0162]
8-(4-乙酰基苯氧基)辛酸甲酯(29)
[0163]
具体合成方法参照中间体25的合成,收率92%,熔点52-54℃.1h nmr(400mhz,cdcl3)δ7.92(d,j=8.4hz,2h),6.91(d,j=8.4hz,2h),4.01(t,j=6.4hz,2h),3.67(s,3h),2.55(s,3h),2.32(t,j=7.4hz,2h),1.79(dq,j=13.4,6.6hz,2h),1.64(dt,j=12.1,6.2hz,2h),1.56
–
1.44(m,2h),1.43
–
1.26(m,4h).
[0164]
4-((4-乙酰基苯氧基)甲基)苯甲酸甲酯(30)
[0165]
具体合成方法参照中间体25的合成,收率88%,熔点119-121℃.1h nmr(400mhz,cdcl3)δ8.07(d,j=7.8hz,2h),7.94(d,j=8.3hz,2h),7.50(d,j=7.9hz,2h),7.00(d,j=8.3hz,2h),5.19(s,2h),3.93(s,3h),2.56(s,3h).
[0166]
(e)-3-(4-(((4-乙酰基苯氧基)甲基)苯基)丙烯酸甲酯(31)
[0167]
具体合成方法参照中间体25的合成,收率84%,熔点150-151℃.1h nmr(400mhz,cdcl3)δ7.94(d,j=8.3hz,2h),7.68(t,j=15.4hz,1h),7.55(d,j=7.9hz,2h),7.45(d,j=7.9hz,2h),7.00(d,j=8.4hz,2h),6.45(d,j=16.0hz,1h),5.15(s,2h),3.81(s,3h),2.55(s,3h).
[0168]
4-(4-(2-溴乙酰基)苯氧基)丁酸甲酯(32)
[0169]
具体合成方法参照中间体10的合成,收率70%,熔点90-92℃.1h nmr(400mhz,cdcl3)δ7.96(d,j=7.9hz,2h),6.94(d,j=8.2hz,2h),4.40(s,2h),4.10(dd,j=12.4,6.3hz,2h),3.70(s,3h),2.54(t,j=7.1hz,2h),2.22
–
2.09(m,2h).
[0170]
5-(4-(2-溴乙酰基)苯氧基)戊酸甲酯(33)
[0171]
具体合成方法参照中间体10的合成,收率83%,熔点61-62℃.1h nmr(400mhz,cdcl3)δ7.95(d,j=8.6hz,2h),6.94(d,j=8.6hz,2h),4.40(s,2h),4.05(d,j=5.4hz,2h),3.68(s,3h),2.41(t,j=6.3hz,2h),1.92
–
1.77(m,4h).
[0172]
6-(4-(2-溴乙酰基)苯氧基)己酸甲酯(34)
[0173]
具体合成方法参照中间体10的合成,收率65%,熔点61-63℃.1h nmr(400mhz,cdcl3)δ7.96(d,j=8.3hz,2h),6.94(d,j=8.3hz,2h),4.40(s,2h),4.04(t,j=6.1hz,2h),3.68(s,3h),2.36(t,j=7.4hz,2h),1.90
–
1.79(m,2h),1.78
–
1.67(m,2h),1.57
–
1.47(m,2h).
[0174]
7-(4-(2-溴乙酰基)苯氧基)庚酸甲酯(35)
[0175]
具体合成方法参照中间体10的合成,收率57%,熔点60-61℃.1h nmr(400mhz,cdcl3)δ7.96(d,j=8.3hz,2h),6.94(d,j=8.3hz,2h),4.40(s,2h),4.08
–
4.00(m,2h),3.67(s,3h),2.33(t,j=7.3hz,2h),1.89
–
1.77(m,2h),1.68(dd,j=14.9,7.4hz,2h),1.50(dt,j=14.2,6.9hz,2h),1.40(dt,j=14.6,7.4hz,2h).
[0176]
8-(4-(2-溴乙酰基)苯氧基)辛酸甲酯(36)
[0177]
具体合成方法参照中间体10的合成,收率53%,熔点62-64℃.1h nmr(400mhz,cdcl3)δ7.96(d,j=8.6hz,2h),6.94(d,j=8.6hz,2h),4.40(s,2h),4.03(t,j=6.3hz,2h),3.67(s,3h),2.32(t,j=7.4hz,2h),1.89
–
1.75(m,2h),1.64(dt,j=14.5,7.4hz,2h),1.55
–
1.44(m,2h),1.44
–
1.31(m,4h).
[0178]
4-((4-(2-溴乙酰基)苯氧基)甲基)苯甲酸甲酯(37)
[0179]
具体合成方法参照中间体10的合成,收率84%,熔点121-123℃.1h nmr(400mhz,cdcl3)δ8.07(d,j=7.7hz,2h),7.98(d,j=8.2hz,2h),7.50(d,j=7.9hz,2h),7.03(d,j=8.2hz,2h),5.21(s,2h),4.39(s,2h),3.93(s,3h).
[0180]
(e)-3-(4-(((4-(2-溴乙酰基)苯氧基)甲基)苯基)丙烯酸甲酯(38)
[0181]
具体合成方法参照中间体10的合成,收率75%,熔点140-141℃.1h nmr(400mhz,cdcl3)δ7.97(d,j=8.4hz,2h),7.70(d,j=16.0hz,1h),7.56(d,j=7.8hz,2h),7.45(d,j=7.8hz,2h),7.03(d,j=8.4hz,2h),6.46(d,j=16.0hz,1h),5.16(s,2h),4.39(s,2h),3.81(s,3h).
[0182]
(z)-4-(4-(2-(5-(氧代-3-苯基)-4-(2-(噻唑-2-基)肼基)亚甲基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)丁酸酯(39)
[0183]
具体合成方法参照中间体15的合成,收率52%,熔点196-198℃.1h nmr(400mhz,dmso-d6)δ8.16(d,j=7.0hz,2h),7.91(d,j=8.0hz,2h),7.72(d,j=3.7hz,1h),7.66(s,1h),7.61
–
7.51(m,3h),7.36(d,j=3.7hz,1h),7.01(d,j=8.1hz,2h),4.04(t,j=6.1hz,2h),3.62(s,3h),2.50
–
2.46(m,2h),2.10
–
1.94(m,2h).
[0184]
(z)-5-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)亚甲基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)戊酸酯(40)
[0185]
具体合成方法参照中间体15的合成,收率54%,熔点173-174℃.1h nmr(400mhz,dmso-d6)δ8.16(d,j=6.9hz,2h),7.91(d,j=8.1hz,2h),7.72(d,j=3.8hz,1h),7.66(s,1h),7.63
–
7.48(m,3h),7.37(d,j=3.8hz,1h),7.01(d,j=8.1hz,2h),4.13
–
3.94(m,2h),3.60(s,3h),2.40(t,j=6.8hz,2h),1.73(dd,j=12.3,6.5hz,4h).
[0186]
(z)-6-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)亚甲基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)己酸酯(41)
[0187]
具体合成方法参照中间体15的合成,收率71%,熔点198-200℃.1h nmr(400mhz,dmso-d6)δ8.16(d,j=6.9hz,2h),7.91(d,j=8.1hz,2h),7.72(d,j=3.7hz,1h),7.66(s,1h),7.63
–
7.50(m,3h),7.36(d,j=3.7hz,1h),7.00(d,j=8.1hz,2h),4.00(t,j=6.2hz,2h),3.59(s,3h),2.34(t,j=7.3hz,2h),1.73(dd,j=13.7,6.6hz,2h),1.61(dt,j=14.7,7.2hz,2h),1.54
–
1.38(m,2h).
[0188]
(z)-7-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)亚甲基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)庚酸酯(42)
[0189]
具体合成方法参照中间体15的合成,收率68%,熔点146-147℃.1h nmr(400mhz,dmso-d6)δ8.16(d,j=7.0hz,2h),7.90(d,j=8.0hz,2h),7.72(d,j=3.7hz,1h),7.66(s,1h),7.54(t,j=9.9hz,3h),7.36(d,j=3.8hz,1h),7.00(d,j=8.2hz,2h),4.00(t,j=6.2hz,2h),3.59(s,3h),2.32(t,j=7.3hz,2h),1.72(dd,j=13.6,6.7hz,2h),1.63
–
1.51(m,2h),1.48
–
1.39(m,2h),1.39
–
1.30(m,2h).
[0190]
(z)-8-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)亚甲基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)辛酸酯(43)
[0191]
具体合成方法参照中间体15的合成,收率76%,熔点166-167℃.1h nmr(400mhz,dmso-d6)δ8.16(d,j=6.8hz,2h),7.90(d,j=8.1hz,2h),7.72(d,j=3.4hz,1h),7.66(s,1h),7.63
–
7.49(m,3h),7.37(d,j=3.7hz,1h),7.00(d,j=8.0hz,2h),4.01(t,j=6.2hz,2h),3.58(s,3h),2.30(t,j=7.6hz,2h),1.72(dd,j=13.4,6.6hz,2h),1.60
–
1.50(m,2h),1.42(d,j=6.7hz,2h),1.32(m,4h).
[0192]
(z)-4-((4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)亚甲基)-4,5-二氢-1h-吡唑-1-)噻唑-4-基)苯氧基)甲基)苯甲酸酯(44)
[0193]
具体合成方法参照中间体15的合成,收率61%,熔点215-216℃.1h nmr(400mhz,dmso-d6)δ8.16(d,j=6.9hz,2h),8.00(d,j=7.5hz,2h),7.94(d,j=8.1hz,2h),7.72(d,j=3.7hz,1h),7.69(s,1h),7.63(d,j=8.1hz,2h),7.60
–
7.50(m,3h),7.37(d,j=3.7hz,1h),7.12(d,j=8.2hz,2h),5.27(s,2h),3.86(s,3h).
[0194]
(e)-3-(4-((4-(2-((z)-5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)亚甲基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)甲基)苯基)丙烯酸酯(45)
[0195]
具体合成方法参照中间体15的合成,收率78%,熔点222-223℃.1h nmr(400mhz,dmso-d6)δ8.16(d,j=6.8hz,2h),7.93(d,j=8.2hz,2h),7.76(d,j=7.8hz,2h),7.72(d,j=4.0hz,1h),7.71
–
7.64(m,2h),7.53(m,5h),7.37(d,j=3.7hz,1h),7.11(d,j=8.3hz,2h),6.66(d,j=16.0hz,1h),5.21(s,2h),3.73(s,3h).
[0196]
(z)-n-羟基-4-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)亚烷基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)丁酰胺(46)
[0197]
具体合成方法参照目标化合物20的合成,收率67%,熔点242-244℃.1h nmr(400mhz,dmso-d6)δ10.44(s,1h),8.72(s,1h),8.21(d,j=6.5hz,2h),7.91(d,j=8.1hz,2h),7.64(s,1h),7.57
–
7.38(m,4h),7.25(d,j=2.7hz,1h),7.00(d,j=8.2hz,2h),4.01(t,j=6.1hz,2h),2.16(t,j=7.2hz,2h),2.02
–
1.90(m,2h).
13
c nmr(101mhz,dmso)δ182.87,169.13,158.71,155.61,153.40,149.95,149.71,141.20,133.19,129.11,128.85,128.58,127.88,127.70,123.08,115.82,115.00,106.49,67.32,29.24,25.34.hrms(ap-esi)m/z,calcd for c
25h21
n7o4s2,([m+h]
+
):548.1169,found:548.1170.
[0198]
实施例8.(z)-n-羟基-5-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)亚烷基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)戊酰胺(47)
[0199]
具体合成方法参照目标化合物20的合成,收率83%,熔点153-155℃.1h nmr(400mhz,dmso-d6)δ10.39(s,1h),8.69(s,1h),8.19(d,j=6.6hz,2h),7.91(d,j=8.3hz,2h),7.67(d,j=3.2hz,1h),7.57(s,1h),7.49(dt,j=21.4,7.3hz,3h),7.29(d,j=3.2hz,1h),7.01(d,j=8.3hz,2h),4.01(d,j=5.8hz,2h),2.04(t,j=6.6hz,2h),1.80
–
1.61(m,
4h).
13
c nmr(101mhz,dmso-d6)δ181.73,169.44,158.86,155.43,153.42,149.97,149.74,138.27,132.38,129.60,128.75,128.51,127.72,127.61,125.59,115.48,115.00,106.82,67.56,32.40,28.68,22.28.hrms(ap-esi)m/z,calcd for c
26h23
n7o4s2,([m+h]
+
):562.1326,found:562.1320.
[0200]
实施例9.(z)-n-羟基-6-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基))-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)己酰胺(48)
[0201]
具体合成方法参照目标化合物20的合成,收率55%,熔点132-134℃.1h nmr(400mhz,dmso-d6)δ10.35(s,1h),8.16(d,j=6.9hz,1h),7.91(d,j=8.2hz,1h),7.72(d,j=3.5hz,1h),7.66(s,1h),7.60
–
7.49(m,1h),7.36(d,j=3.7hz,1h),7.01(d,j=8.2hz,1h),4.00(t,j=6.0hz,1h),1.99(t,j=7.1hz,1h),1.78
–
1.69(m,1h),1.56(dd,j=14.4,7.1hz,1h),1.48
–
1.37(m,1h).
13
c nmr(101mhz,dmso-d6)δ179.00,172.51,169.52,159.01,154.98,153.43,150.29,149.32,132.75,130.92,130.42,130.31,128.99,128.44,127.75,127.29,114.99,114.52,107.31,67.86,32.72,28.94,25.67,21.53.hrms(ap-esi)m/z,calcd for c
27h25
n7o4s2,([m+h]
+
):576.1482,found:576.1481.
[0202]
实施例10.(z)-n-羟基-7-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)亚烷基)-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)庚酰胺(49)
[0203]
具体合成方法参照目标化合物20的合成,收率64%,熔点127-128℃.1h nmr(400mhz,dmso-d6)δ10.33(s,1h),8.16(d,j=6.9hz,2h),7.91(d,j=8.0hz,2h),7.72(d,j=3.5hz,1h),7.65(s,1h),7.61
–
7.49(m,3h),7.36(d,j=3.5hz,1h),7.01(d,j=8.1hz,2h),4.01(t,j=6.2hz,2h),1.96(t,j=7.2hz,2h),1.78
–
1.68(m,2h),1.52(dd,j=14.6,7.2hz,2h),1.47
–
1.39(m,2h),1.36
–
1.28(m,2h).
13
c nmr(101mhz,dmso-d6)δ179.45,169.57,159.03,155.01,153.40,150.28,149.37,132.71,131.00,130.40,130.21,129.00,128.46,127.76,127.30,115.02,114.53,107.30,67.91,32.69,29.09,28.84,25.75,25.56.hrms(ap-esi)m/z,calcd for c
28h27
n7o4s2,([m+h]
+
):590.1639,found:590.1628.
[0204]
实施例11.(z)-n-羟基-8-(4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基))-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)辛酰胺(50)
[0205]
具体合成方法参照目标化合物20的合成,,收率60%,熔点144-145℃.1h nmr(400mhz,dmso-d6)δ10.32(s,1h),8.16(d,j=7.1hz,2h),7.91(d,j=8.2hz,2h),7.72(d,j=3.6hz,1h),7.65(s,1h),7.61
–
7.49(m,3h),7.36(d,j=3.7hz,1h),7.01(d,j=8.1hz,2h),4.01(t,j=6.2hz,2h),1.95(t,j=7.2hz,2h),1.80
–
1.67(m,2h),1.57
–
1.47(m,2h),1.45
–
1.38(m,2h),1.37
–
1.21(m,4h).
13
c nmr(101mhz,dmso-d6)δ179.08,169.62,159.02,154.98,153.42,150.29,149.32,132.76,130.94,130.40,130.27,128.98,128.44,127.75,127.26,114.98,114.53,107.28,67.93,32.73,29.16,29.01,29.00,25.92,25.56.hrms(ap-esi)m/z,calcd for c
29h29
n7o4s2,([m+h]
+
):604.1795,found:604.1787.hplc tr=5.994min(99.01%purity).
[0206]
实施例12.(z)-n-羟基-4-((4-(2-(5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基))-4,5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)甲基)苯甲酰胺(51)
[0207]
具体合成方法参照目标化合物20的合成,收率60%,熔点216-217℃.1h nmr(400mhz,dmso-d6)δ11.22(s,1h),9.03(s,1h),8.18(d,j=7.0hz,2h),7.93(d,j=8.1hz,
2h),7.78(d,j=7.6hz,2h),7.69(d,j=3.3hz,1h),7.62(s,1h),7.59
–
7.46(m,5h),7.31(d,j=3.2hz,1h),7.11(d,j=8.1hz,2h),5.22(s,2h).
13
c nmr(101mhz,dmso-d6)δ180.80,172.51,164.43,158.43,155.27,153.40,149.94,140.67,135.92,132.73,131.87,129.99,129.96,129.90,128.83,128.51,127.93,127.77,127.52,115.44,115.00,107.22,69.18.hrms(ap-esi)m/z,calcd for c
29h21
n7o4s2,([m+h]
+
):596.1169,found:596.1156.
[0208]
实施例13.(e)-n-羟基-3-(4-((4-(2-((z)-5-氧代-3-苯基-4-(2-(噻唑-2-基)肼基)-4],5-二氢-1h-吡唑-1-基)噻唑-4-基)苯氧基)甲基)苯基)丙烯酰胺(52)
[0209]
具体合成方法参照目标化合物20的合成,收率70%,熔点186-188℃.1h nmr(400mhz,dmso-d6)δ10.77(s,1h),9.13(s,1h),8.16(d,j=6.9hz,2h),7.93(d,j=8.2hz,2h),7.71(d,j=3.6hz,1h),7.66(s,1h),7.53(ddd,j=31.3,21.8,11.8hz,8h),7.35(d,j=3.6hz,1h),7.11(d,j=8.2hz,2h),6.48(d,j=15.8hz,1h),5.19(s,2h).
13
c nmr(101mhz,dmso-d6)δ179.19,163.15,158.56,155.07,153.46,150.17,149.38,138.83,138.42,134.86,133.34,131.07,130.32,129.79,128.95,128.64,128.46,128.07,127.79,127.75,119.66,115.42,114.63,107.48,69.35.hrms(ap-esi)m/z,calcd for c
31h23
n7o4s2,([m+h]
+
):622.1326,found:622.1320.
[0210]
目标化合物活性评价
[0211]
实验例1目标化合物抑制人宫颈癌细胞(hela细胞)增殖实验
[0212]
1.[材料]
[0213]
k562,kg1,hl-60,a549,hela,四甲基偶氮唑盐mtt,10%胎牛血清(美国hyclone公司),2.5g
·
l-1胰蛋白酶(美国gibco公司),改良型rpmi1640培养基(美国hyclone公司),96孔板;
[0214]
2.[方法]
[0215]
常规培养细胞,收集对数生长的细胞进行实验;用含胎牛血清10%的rpmi1640培养基将对数生长期的细胞稀释至4
×
104个
·
ml-1
后接种于96孔板中(每孔加100μl),不加细胞的作为空白孔,之后放于恒温孵育箱(37℃,5%二氧化碳)中培养8小时;加入用培养基配制的目标化合物溶液,不加药的作为100%孔,于恒温孵育箱(37℃,5%二氧化碳)中培养48小时后加入30μl mtt,四小时后除去孔中液体(悬浮细胞需离心),加150μl dmso,最后于恒温摇床中振摇10min用酶标仪于570nm波长处测定每孔的吸光度值,计算抑制率和ic
50
值;
[0216][0217]
表2.目标化合物进行体外抑制肿瘤细胞增殖实验结果
[0218][0219]
a表中数据为三次实验的平均值,
“±”
后的数值表示标准误差
[0220]
术语说明:k562,人慢性髓原白血病细胞;hl-60,人早幼粒白血病细胞;
[0221]
结论:所有目标化合物的抗肿瘤增殖活性均优于阳性对照药,其中目标化合物23抑制k562细胞增殖的活性是阳性对照药btsa1的9倍,抑制hl-60细胞增殖的活性是阳性对照药的11倍。
[0222]
上述化合物可深入进行活性研究,开发出更有活性的化合物用于制备预防和治疗癌症的药物。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1