用于2019新型冠状病毒S基因检测的引物组、恒温荧光筛查试剂盒及检测方法
用于2019新型冠状病毒s基因检测的引物组、恒温荧光筛查试剂盒及检测方法
技术领域
1.本发明属于生物技术领域,具体涉及用于2019新型冠状病毒s基因检测的引物组、恒温荧光显色筛查试剂盒及检测方法。
背景技术:
2.严重急性呼吸综合症冠状病毒2(sars-cov-2)是一种单链rna冠状病毒,基因组序列由29903bp构成,该基因组拥有10个基因,可以有效编码10个蛋白。目前,who已将该病毒引发的疾病命名为“2019冠状病毒病”(covid-19)。2019冠状病毒病症状包括发热、咳嗽、全身乏力以及呼吸道症状,并存在有限的人际传播。
3.现行的新型冠状病毒检测方法存在一定的问题,从一些报道来看,经常发生病人做三四次核酸检测,甚至四五次,才知道是阳性还是阴性的现象主要是因现有的新型冠状病毒核酸检测试剂盒有质量问题,试剂盒反转录效率低下;扩增的循环数不够;pcr长度、引物设计、引物的特异等,都是影响试剂盒检测质量的重要影响因素。很多试剂盒在早期研发时,并未完成试剂的优化、质控、灵敏度、特异性测试等等,导致灵敏度不够,检测结果不稳定。病人经常要做三四次核酸检测,甚至是四五次,才知道是阳性还是阴性。即便如此,可能还有很多人检测出来是阴性,但已经出现白肺。或者有些人核酸检测阳转阴,但其实是假阴性。这都是由于设计引物存在较大难度造成的试剂灵敏度及特异性差的问题。亟需开发灵敏度稿,检测结果稳定的检测设计。
4.目前针对新型冠状病毒核酸检测仅有orf1ab及n基因检测指导方法,而尚没有s基因检测方法。最新报道,多家单位成功分离新型冠状病毒2019-ncov毒株的全基因组序列测定和变异分析,与新型冠状病毒2019-ncov参考基因组nc 045512.2相比,很多毒株基因组orf 1a/b基因发生了重要的两个位点突变,提示现有的检测方法、检测靶标需要根据病毒变异情况进行进一步更新和优化。有必要开展新型冠状病毒s基因检测方法研究,研发适用于现场的快速筛查技术方法,适用于现场检测、便捷高效的技术手段。
技术实现要素:
5.为了解决上述现有技术问题,本发明提供一种用于2019新型冠状病毒s基因检测的引物组。本发明的另一个目的是提供一种2019新型冠状病毒检测恒温荧光筛查试剂盒及其检测方法。
6.为实现上述目的,本发明采用以下的技术方案为:
7.一组用于2019新型冠状病毒s基因检测的引物组,其包括外引物f3、外引物b3、内引物fip、内引物bip、环引物lf和环引物lb,其中所述外引物f3的核苷酸序列如seq id no.1所示;所述外引物b3的核苷酸序列如seq id no.2所示;所述内引物fip的核苷酸序列如seq id no.3所示;所述内引物bip的核苷酸序列如seq id no.4所示;所述环引物lf的核苷酸序列如seq id no.5所示;所述环引物的核苷酸序列如seq id no.6所示。
8.如上所述的引物组在制备用于检测2019新型冠状病毒s基因的试剂盒中的应用。
9.一种用于2019新型冠状病毒s基因检测的恒温荧光筛查试剂盒,该试剂盒包括:如上所述的引物组。
10.如上所述的恒温荧光筛查试剂盒,该试剂盒还包括链置换bst dna聚合酶、逆转录酶、syto-9、dntps、tris-hcl、kcl、betaine和mgcl2。
11.如上所述的恒温荧光筛查试剂盒,该试剂盒还包括阳性对照和阴性对照,所述阳性对照为s基因体外转录rna序列的质粒作为阳性对照,所述阴性对照为去核酸的灭菌水。
12.一种对2019新型冠状病毒s基因检测的方法,该方法是非诊断目的的检测方法,具体包括以下步骤:
13.(1)从样品中提取rna;
14.(2)对步骤(1)提取的所述rna进行等温扩增;其中,在反应体系中,采用如上所述用于2019新型冠状病毒s基因检测的引物组;
15.(3)荧光定量pcr仪设定:63℃,15s;63℃,45s,采集信号,共45个循环;
16.(4)结果判定:若有“s”型扩增曲线,则判断为阳性(有核酸扩增),若无“s”型扩增曲线,则判断为阴性(无核酸扩增)。
17.如上所述的恒温显色方法,优选地,在步骤(2)中,所述等温扩增的反应体系,具体如下:反应总体积为25μl,其中,所述反应体系中含有s-1:反应液:8
×
105u/l rnasin,200mm dntps,10mm tris-hcl(ph=8.3),20mm kcl,3.5mm mgcl2,0.8m betaine,内引物fip、内引物bip各1.6μm,外引物f3、外引物b3各0.2μm外引物,环引物lf、环引物lb各0.8μm,syto-90.5μl总共22μl,bst聚合酶0.8μl,amv酶0.2μl,样品rna模板2.0μl。
18.如上所述的恒温显色方法,优选地,同时设置无核酸酶水为阴性对照;采用含s基因体外转录rna的序列的质粒作为阳性对照进行检测。
19.本发明的有益效果在于:
20.本发明开展新型冠状病毒s基因恒温荧光扩增筛查检测方法,创新性设计新型冠状病毒s基因恒温荧光扩增内外环引物组,建立成熟稳定、测试成本低的恒温荧光扩增筛查检测新方法。针对世界公布的新型冠状病毒2019-ncov毒株全基因组序列测定和变异分析结果,针对s基因,自主设计恒温荧光扩增特异性引物,体外转录rna进行验证实验,建立特性、灵敏的新型冠状病毒s基因恒温荧光扩增筛查检测新方法。35-45min即可完成对新型冠状病毒s基因的快速筛查检测,性能指标优于国内外同类方法水平。所研发建立的方法可以在线实现样品的预处理及测试的全过程,使核酸现场快速筛查检验设想成为可能。
21.本发明所设计的新型冠状病毒s基因恒温荧光扩增筛查检测内外环引物组,并建立相应的s基因恒温荧光扩增筛查检测方法及筛查试剂盒,可以解决目前新型冠状病毒核酸检测仅局限于应用恒温扩增芯片法检测s基因,而没有使用廉价、便捷的恒温水浴锅即可完成筛查检测s基因的恒温荧光筛查方法及试剂盒的问题。
附图说明
22.图1为1#引物对筛选结果;图中,nc为阴性对照,pc为阳性对照。
23.图2为2#引物对筛选结果;图中,nc为阴性对照,pc为阳性对照。
24.图3为灵敏度测试扩增结果;图中,nc为阴性对照。
25.图4为本发明检测方法操作流程示意图。
具体实施方式
26.以下实施例用于进一步说明本发明,但不应理解为对本发明的限制。在不背离本发明精神和实质的前提下,对本发明所作的修饰或者替换,均属于本发明的范畴。本发明实施例中所用的amv反转录酶可购自biolabs m0277,bst聚合酶可购自biolabs m0537l恒温荧光扩增反应液购自广州双螺旋公司;lightcycler 480购自罗氏。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段。
27.实施例1 s基因恒温荧光扩增引物组的筛选
28.从新型冠状病毒国家科技资源服务系统(http://nmdc.cn/#/ncov)下载已上传的2019-ncov序列,经比对分析对选择s基因作为检测靶标,位于病毒的spike蛋白区,与其他冠状病毒/细菌/人体基因组无交叉。根据公开的序列人工合成制备s基因质粒体外转录rna阳性对照样本。选取s基因的保守区,采用primer premier 5.0软件自行设计3组恒温荧光扩增引物对,分别标记为1#为第一组、2#为第二组、3#为第三组。每组引物包括外引物f3、外引物b3、内引物fip、内引物bip、环引物lf和环引物lb,并使用primer blast(http://www.ncbi.nlm.nih.gov/tools/primer-blast/)进行评估。
29.采用阳性对照和阴性对照(无核酸酶的灭菌水)通过对3套引物进行筛选,结果显示,其中,1#引物组有非特异性扩增,nc显示为阳性,如图1所示,图中pc表示阳性对于,nc为阴性对照,2#引物组荧光信号时间较早、且较稳定结果如图2所示,图中pc表示阳性对于,nc为阴性对照,第3套引物未检出信号。确定2#引物组作为新型冠状病毒s基因恒温荧光扩增内、外、环引物组。其各引物的核苷酸序列如下(方向为5'to 3'):
30.外引物f3(seq id no.1):5
′-
ttattgccactagtctctagtcagtgt-3
′
31.外引物b3(seq id no.2):5
′-
agtagggactgggtcttcgaat-3
′
32.内引物fip(seq id no.3):5
′-
tgtaaaactgaggatctgaaaactttgttttaaccagaactcaattaccccctg-3
′
33.内引物bip(seq id no.4):5
′-
aatggtactaagaggtttgataaccctttttattatgttagacttctcagtggaa-3
′
34.环引物lf(seq id no.5):5
′-
gggtaataaacaccacgtgtgaaa-3
′
35.环引物lb(seq id no.6):5
′-
ccatttaatgatggtgtttattt-3
′
。
36.实施例2恒温荧光检测方法的建立
37.使用实施例1中确定的2#引物组进行恒温荧光扩增检测,恒温荧光扩增检测体系25μl进行恒温荧光检测,25μl体系含有:其中8
×
105u/l rnasin、200mm dntps、10mm tris-hcl(ph=8.3)、20mm kcl、3.5mm mgcl2、0.8m betaine、1.6μm内引物对(fip、bip,各自为1.6μm)、0.2μm外引物对(f3、b3,各自为0.2μm)、0.8μm环引物对(lf、lb,各自为0.8μm)、syto-9,共22μl,再加入b-1bst聚合酶(105u/l)0.8μl,r-1amv酶(4
×
106u/l)0.2μl,rna模板2.0μl。混匀后置于lightcycler480中进行恒温荧光扩增。
38.反应条件为:荧光定量pcr仪:63℃,15s;63℃,45s,采集信号,共45个循环。
39.使用10pg/μl(106copies/μl)s基因体外转录rna作为阳性检测样本,进行检测,确定具有明显s形扩增曲线,且曲线光滑,说明可进行新型冠状病毒s基因恒温荧光的检测。结
果判定时:有明显s形扩增曲线,且曲线光滑,为阳性,无s形扩增曲线为阴性。
40.实施例3灵敏度检测
41.将s基因体外转录的rna质粒阳性样本,以10倍比梯度进行稀释,浓度分别为1
×
106copies/μl、1
×
105copies/μl、1
×
104copies/μl、1
×
103copies/μl、1
×
102copies/μl、10copies/μl,采用实施例2中的恒温荧光扩增反应体系进行检测,在45分钟以内,1
×
103copies可稳定检出,结果如图3所示,检出限为1
×
103copies。
42.实施例4恒温荧光筛查试剂盒
43.本发明制备的新型冠状病毒s基因恒温荧光筛查检测试剂盒包括链置换bst dna聚合酶、逆转录酶、syto-9、dntps、tris-hcl、kcl、betaine和mgcl2还有实施例1中的引物f3、外引物b3、内引物fip、内引物bip、环引物lf和环引物lb。
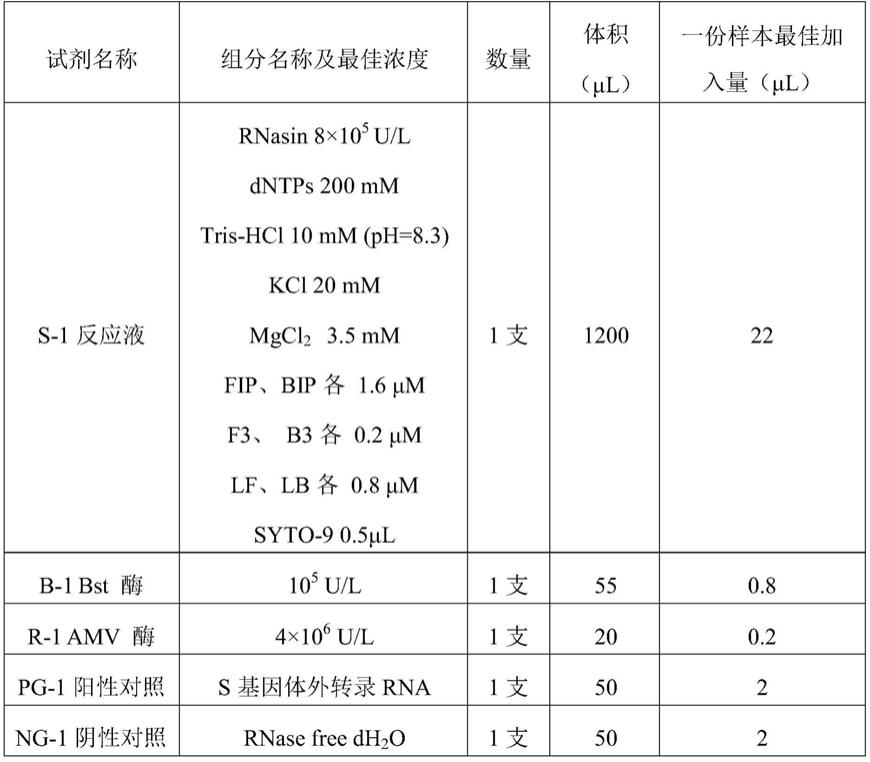
44.根据使用方便,可配置成按反应体系加的试剂,可选择如表1所示。
45.表1试剂盒产品内容
[0046][0047]
实施例5使用试剂盒的检测方法
[0048]
采用实施例4中的试剂盒对样品的检测,可适用样本类型有:咽拭子、鼻咽拭子、肛拭子、血浆等样本;样品应当避免反复冻融。
[0049]
检测的操作流程示意图如图4所示,具体操作步骤如下:
[0050]
1、样本rna提取(也可以按照其他提取试剂盒操作进行)
[0051]
转移20μl蛋白酶k至1.5ml离心管中。转移200μl样本(如咽拭子、鼻咽拭子、肛拭
子、血浆等样本)的保存液至装有蛋白酶k的离心管中,震荡混匀5s。转移200μl buffer vgb、蛋白酶k、carrier rna至样品中,涡旋混匀15s。56℃水浴10min。加入裂解液。向裂解液中加无水乙醇溶液转移至spin column中。弃去滤液。将spin column移至1.5ml rnase free离心管上。用rnase free dh2o清洗,把样本rna用于检测实验或保存于-80℃。
[0052]
2、试剂配制检测
[0053]
(1)取出试剂盒,将试剂完全解冻,各组分离心30s,b-i及r-i为液体,取出后应放置于冰盒上。
[0054]
(2)试剂配制
[0055]
若有n个待检样本,则参照下表,按照n+3个数量计算各组分用量(n个待检样本+1个阴性对照+1个阳性对照+1份备用),将反应液置于0.6ml或者1.5ml离心管中,涡旋混匀,离心30s,分装于0.2ml pcr管中
[0056]
试剂使用量
[0057]
s-1 22
×
(n+3)μl
[0058]
b-1 0.8
×
(n+3)μl
[0059]
r-1 0.2
×
(n+3)μl
[0060]
反应液总体积23
×
(n+3)μl
[0061]
(3)添加待检样本模板
[0062]
向步骤1中已含有反应液的pcr管中分别加入2μl模板,离心30s,应立即进行扩增反应。
[0063]
(4)扩增反应(可根据不同的仪器设置相应的反应条件)
[0064]
荧光定量pcr仪:63℃,15s;63℃,45s,采集信号,共45个循环。
[0065]
(5)检测结果判定
[0066]
空白对照、阴性对照和阳性对照全部满足下述条件,表明检测体系有效:空白对照、阴性对照无“s”型扩增曲线(无核酸扩增),阳性对照有“s”扩增(有核酸扩增)。
[0067]
样本检测结果判定:若有“s”型扩增曲线,则判断为阳性(有核酸扩增),若无“s”型扩增曲线,则判断为阴性(无核酸扩增)。
[0068]
(6)注意事项
[0069]
该试剂的反应体系、扩增管以及阳性对照品在-20℃条件下保存。
[0070]
在试剂使用过程中,每一步用吸管滴加或吸取液体后必须更换新的吸管,不同样品之间滴入或吸出液体也必须更换新的吸管,以防止交叉污染。
[0071]
操作过程中要佩戴一次性或乳胶手套,若检测的样品量大,要提高更换手套的频率,以防止交叉污染。
[0072]
尽量在空气流通的地方向扩增管中加入样品和阳标,防止检测结果出现假阳性。每一次检测都要设置阳性对照和阴性对照以保证被测样品检测结果的可靠性。
[0073]
实施例6特异性检测
[0074]
采用实施例2的恒温荧光检测方法,对冠状病毒229e型质粒、冠状病毒hku1型质粒、冠状病毒oc43型质粒冠状病毒nl63型质粒、甲型流感病毒rna、mers冠状病毒质粒、乙型流感病毒rna、腺病毒质粒、副流感病毒质粒、鼻病毒质粒、呼吸道合胞病毒质粒、肺炎支原体质粒、军团菌核酸、肺炎衣原体质粒、肺炎克雷伯菌核酸、肺炎链球菌质粒、金黄色葡萄球
菌核酸等做特异性扩增试验。检测结果均无扩增曲线,说明本发明建立的方法所用的引物组的特性强,与其它病原不发生交叉反应。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1