烟酰胺单核苷酸的制备方法与流程
1.本发明涉及烟酰胺单核苷酸合成技术领域,具体而言,涉及一种烟酰胺单核苷酸的制备方法。
背景技术:
2.烟酰胺单核苷酸(nmn),别名β-烟酰胺单核苷酸,作为nad
+
补救途径中的中间体,具有抗氧化、减少氧化应激的作用,在一些具体疾病的治疗,如脑卒中、心脏缺血再灌注、阿尔茨海默氏病、帕金森病、急性肾损伤、视网膜退行性疾病、2型糖尿病等中也有良好的表现。特别是在抗衰老方面,nmn可以减缓生物体的生理衰退,增强能量代谢,延长寿命。
[0003][0004]
2018年5月,美国膳食补充剂企业herbalmax将经实验确认可显著延缓衰老并延长寿命的科研成果nmn(nicotinamide mononucleotide烟酰胺单核苷酸)转化为实际产品reinvigorator(中文名“瑞维拓”)并推向市场。这一消息引起了广泛关注。
[0005]
目前,β-烟酰胺单核苷酸生产方法有化学合成方法和酶法合成方法。如journal of biological chemistry,1958(233),493,analytical biochemistry,2011(412)18报道了酶法制备烟酰胺单核苷酸的方法,以烟酰胺核糖为底物,在atp等磷酸供体存在下,在烟酰胺核糖激酶或含有烟酰胺核糖激酶的重组细胞的催化下反应生成β-烟酰胺单核苷酸。
[0006][0007]
有大量文献报道了烟酰胺单核苷酸的化学合成方法,几乎均采用三氯氧磷酰化的方法,例如chem.commun.1999,729
–
730、cn102876759、tetrahedron 65(2009)8378-8383、bioorg.med.chem.lett.12(2002)1135-1137等文献报道以烟酰胺核糖为原料,用三氯氧磷进行磷酸化得到产物,通过调ph、过离子交换树脂和重结晶等后处理得到烟酰胺单核苷酸。
[0008][0009]
但酶法合成方法所需酶价格昂贵,限制了其在工业生产的使用。化学法制备单独
使用三氯氧磷为磷酰化试剂,反应的选择性不高,容易对其他位点的羟基发生氯代,且产品在三氯氧磷下容易发生降解,由于杂质较多,后处理需要使用离子交换树脂来进一步纯化,操作繁琐,得到的产品纯度和收率偏低。
技术实现要素:
[0010]
本发明的主要目的在于提供一种烟酰胺单核苷酸的制备方法,以解决现有技术中烟酰胺单核苷酸合成方法存在的选择性低的问题。
[0011]
为了实现上述目的,根据本发明的一个方面,提供了一种烟酰胺单核苷酸的制备方法,该制备方法包括:步骤s1,将包含烟酰胺核苷盐、1,8-双二甲氨基萘、三氯氧磷及溶剂的原料进行磷酰化反应,得到反应后体系;步骤s2,将反应后体系进行水解,得到包含烟酰胺单核苷酸的反应液。
[0012]
进一步地,上述1,8-双二甲氨基萘、烟酰胺核苷盐与三氯氧磷的摩尔比为1~2:1:4~6,优选为1.5:1:5。
[0013]
进一步地,上述烟酰胺核苷盐中的阴离子为三氟甲磺酸根离子或氯离子。
[0014]
进一步地,上述溶剂为极性非质子溶剂,优选极性非质子溶剂为磷酸三甲酯或磷酸三乙酯。
[0015]
进一步地,上述磷酰化反应的温度为-20~0℃,优选为-10~0℃。
[0016]
进一步地,上述磷酰化反应的时间为12~48h,优选为18~36h。
[0017]
进一步地,上述制备方法还包括:将包含烟酰胺单核苷酸的反应液进行结晶处理,结晶处理的过程包括,将包含烟酰胺单核苷酸的反应液溶解于水中,得到水溶液;将水溶液与有机溶剂进行混合并搅拌,析出烟酰胺单核苷酸。
[0018]
进一步地,上述结晶处理的温度为-10~0℃,优选为-10~-5℃,优选结晶处理的时间为1~6h,进一步优选为2~4h。
[0019]
进一步地,上述水与有机溶剂的体积比为1:5~20,优选为1:10~15。
[0020]
进一步地,上述有机溶剂选自乙醇、正丙醇、异丙醇、乙腈、丙酮中的任意一种或多种。
[0021]
应用本发明的技术方案,烟酰胺核苷盐的五元杂环上的2位羟基为伯羟基,3、4位羟基属于仲羟基,由于伯羟基的反应活性强于仲羟基,当发生上述磷酰化反应时,1,8-双二甲氨基萘优先与烟酰胺核苷盐的2位羟基形成复合物,且一方面由于1,8-双二甲氨基萘为含有两个芳环的刚性结构,其体积较大,可抑制三氯氧磷继续对2位或3位羟基的进攻;另一方面在进行磷酰化反应时,1,8-双二甲氨基的一个氮原子有利于2位羟基氢的拔除,另一个氮原子有助于磷酰氯中氯的去除,在上述两个n原子的协同作用下有利于氯化氢的去除,同时,由于1,8-双二甲氨基萘中的两个氮原子距离较近,使得1,8-双二甲氨基萘在脱除氯化氢的过程中形成的过度中间体更稳定,从而使脱除氯化氢的过程倾向于分子内的反应,进一步地提高了磷酰化反应的选择性。
附图说明
[0022]
构成本技术的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:
[0023]
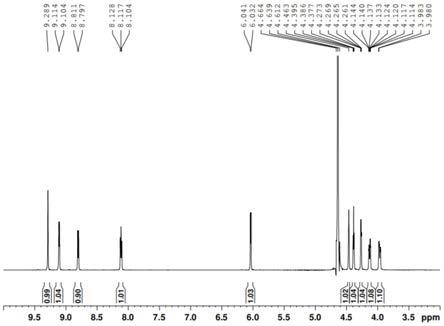
图1示出了根据本发明的实施例1提供的β-烟酰胺单核苷酸的核磁共振氢谱图;
[0024]
图2示出了根据本发明的实施例1提供的β-烟酰胺单核苷酸的红外光谱图。
具体实施方式
[0025]
需要说明的是,在不冲突的情况下,本技术中的实施例及实施例中的特征可以相互组合。下面将参考附图并结合实施例来详细说明本发明。
[0026]
如背景技术所分析的,现有技术中存在烟酰胺单核苷酸合成方法的选择性低的问题,为解决该问题,本发明提供了一种烟酰胺单核苷酸的制备方法。
[0027]
在本技术的一种典型的实施方式中,提供了一种烟酰胺单核苷酸的制备方法,该制备方法包括:步骤s1,将包含烟酰胺核苷盐、1,8-双二甲氨基萘、三氯氧磷及溶剂的原料进行磷酰化反应,得到反应后体系;步骤s2,将反应后体系进行水解,得到包含烟酰胺单核苷酸的反应液。
[0028]
烟酰胺核苷盐的五元杂环上的2位羟基为伯羟基,3、4位羟基属于仲羟基,由于伯羟基的反应活性强于仲羟基,当发生上述磷酰化反应时,1,8-双二甲氨基萘优先与烟酰胺核苷盐的2位羟基形成复合物,且一方面由于1,8-双二甲氨基萘为含有两个芳环的刚性结构,其体积较大,可抑制三氯氧磷继续对2位或3位羟基的进攻;另一方面在进行磷酰化反应时,1,8-双二甲氨基的一个氮原子有利于2位羟基氢的拔除,另一个氮原子有助于磷酰氯中氯的去除,在上述两个n原子的协同作用下有利于氯化氢的去除,同时,由于1,8-双二甲氨基萘中的两个氮原子距离较近,使得1,8-双二甲氨基萘在脱除氯化氢的过程中形成的过度中间体更稳定,从而使脱除氯化氢的过程倾向于分子内的反应,进一步地提高了磷酰化反应的选择性。
[0029]
具体地,上述反应的过程如下:
[0030][0031]
为尽可能地促进原料反应完全并提高上述反应的效率,优选上述1,8-双二甲氨基萘、烟酰胺核苷盐与三氯氧磷的摩尔比为1~2:1:4~6,优选为1.5:1:5。
[0032]
在本技术的一种施例中,上述烟酰胺核苷盐中的阴离子为三氟甲磺酸根离子或氯离子。
[0033]
本技术的烟酰胺核苷盐为烟酰胺单核苷酸的烟酰胺核苷部分的来源,本技术为提高烟酰胺核苷盐在溶剂中的溶解性,并降低成本,优选上述的烟酰胺核苷盐。
[0034]
上述烟酰胺核苷盐的制备方法可以参照现有技术进行合成,本技术为提高烟酰胺核苷盐的合成效率,优先采用下面的合成方法依次合成烟酰胺核苷三乙酸酯三氟甲磺酸盐
和烟酰胺核苷氯代物:
[0035]
取一个干净的反应瓶(1l),加入20g四乙酰核糖、11.2g烟酰胺、400ml乙腈,开启搅拌;保持温度25℃,加入27.6g三氟甲磺酸三甲基硅脂,溶液溶清;20min后,tlc检测,四乙酰核糖反应完全。向反应液加入8ml甲醇,5min后,减压浓缩,向浓缩油加入100ml二氯甲烷,减压抽滤,将母液减压浓缩,得到烟酰胺核苷三乙酸酯三氟甲磺酸盐,称重为37.5g。
[0036][0037]
将烟酰胺核苷三乙酸酯三氟甲磺酸盐(37.5g)加入到500ml反应瓶中,置于冰浴中,然后加入200ml氨甲醇溶液(4m),反应搅拌6h后,减压浓缩,即得13.5g烟酰胺核苷三氟甲磺酸盐。
[0038]
将10g烟酰胺核苷三氟甲磺酸盐溶于30ml水中,过氯型阴离子交换树脂,之后减压浓缩至干,加入50ml无水乙醇搅拌析晶,过滤,得到6.5g烟酰胺核苷氯代物。
[0039]
为提高上述原料在溶剂中的溶解性,从而提高反应的效率,优选上述溶剂为极性非质子溶剂,优选极性非质子溶剂为磷酸三甲酯或磷酸三乙酯。
[0040]
在本技术的一种实施例中,上述磷酰化反应的温度为-20~0℃,优选为-10~0℃。
[0041]
为降低上述反应中副反应的发生几率,优选上述反应在以上反应温度范围内进行。
[0042]
为兼顾反应的效率以及反应原料的转化率,优选上述磷酰化反应的时间为12~48h,优选为18~36h。
[0043]
在本技术的一种实施例中,上述制备方法还包括:将包含烟酰胺单核苷酸的反应液进行结晶处理,结晶处理的过程包括,将包含烟酰胺单核苷酸的反应液溶解于水中,得到水溶液;将水溶液与有机溶剂进行混合并搅拌,析出烟酰胺单核苷酸。
[0044]
本技术的上述反应由于1,8-双二甲氨基萘的添加,提高了磷酰化反应的选择性,因此直接对包含烟酰胺单核苷酸的反应液进行上述结晶处理即可得到烟酰胺单核苷酸,与现有技术相比,本技术的上述后处理的过程避免了对包含烟酰胺单核苷酸的反应液的离子交换树脂提纯的步骤,从而减少了反应步骤,降低了生产成本。
[0045]
为提高上述结晶处理的效率,优选结晶处理的温度为-10~0℃,优选为-10~-5℃,优选结晶处理的时间为1~6h,进一步优选为2~4h。
[0046]
在本技术的一种实施例中,上述水与有机溶剂的体积比为1:5~20,优选为1:10~15。
[0047]
优选上述比例的水与有机溶剂更有利于烟酰胺单核苷酸的析出。
[0048]
为提高结晶处理的效率,优选上述有机溶剂选自乙醇、正丙醇、异丙醇、乙腈、丙酮中的任意一种或多种。
[0049]
以下将结合具体实施例和对比例,对本技术的有益效果进行说明。
[0050]
实施例1
[0051]
称取10g烟酰胺核糖氯化物(34.4mmol),加入100ml反应瓶,加入50ml磷酸三甲酯,降温至-20~-10℃,加入11.06g 1,8-双二甲氨基萘(51.6mmol),然后滴加26.4g三氯氧磷
(172mmol),反应24h,将反应液减压抽滤并将滤液减压浓缩得到浓缩产物。
[0052]
于温度为-10~-5℃下,向浓缩产物中加入20ml纯化水,溶清后,缓慢滴加200ml乙腈,搅拌析晶4h,过滤,即得8.62gβ-烟酰胺单核苷酸,该β-烟酰胺单核苷酸产品的核磁共振氢谱见附图1,核磁共振氢谱数据为:1h-nmr(600mhz,d2o)δppm9.31(1h,s,ar),9.095-9.105(1h,d,ar),8.771-8.785(1h,d,ar),8.079-8.103(1h,t,ar),5.991-6.001(1h,d,h-1),4.405-4.420(1h,m,h-2),4.388-4.396(1h,t,h-3),4.249(1h,d,h-4),4.045-4.046(1h,d,h-5),3.876-3.896(1h,d,h-5).从附图1可以看出,结晶处理后的产物为β-烟酰胺单核苷酸,且几乎没有杂质。β-烟酰胺单核苷酸产品的红外光谱见附图2,其中,3437.15为糖环上羟基伸缩振动;3221.42为酰胺的氮氢伸缩振动;3118.9为磷酰基上羟基伸缩振动;3068.75为吡啶环上羟基伸缩振动;2873.94为糖环5号位上碳氢伸缩振动;1670.35为酰胺羰基上碳氧伸缩振动;1573.91为吡啶环上碳碳双键伸缩振动;1402.25为酰胺上碳氮伸缩振动;1215.15为磷酰基上磷氧双键伸缩振动;1105.21,1087.85为碳氧单键伸缩振动;775.38,765.74为吡啶环碳氢单键弯曲振动。
[0053]
实施例2
[0054]
实施例2与实施例1的区别在于,
[0055]
1,8-双二甲氨基萘、烟酰胺核糖氯化物(34.4mmol)与三氯氧磷的摩尔比为1:1:5,最终得到8.05gβ-烟酰胺单核苷酸。
[0056]
实施例3
[0057]
实施例3与实施例1的区别在于,
[0058]
1,8-双二甲氨基萘、烟酰胺核糖氯化物(34.4mmol)与三氯氧磷的摩尔比为2:1:5,最终得到8.03gβ-烟酰胺单核苷酸。
[0059]
实施例4
[0060]
实施例4与实施例1的区别在于,
[0061]
1,8-双二甲氨基萘、烟酰胺核糖氯化物(34.4mmol)与三氯氧磷的摩尔比为1.5:1:4,最终得到8.33gβ-烟酰胺单核苷酸。
[0062]
实施例5
[0063]
实施例5与实施例1的区别在于,
[0064]
1,8-双二甲氨基萘、烟酰胺核糖氯化物(34.4mmol)与三氯氧磷的摩尔比为1.5:1:6,最终得到8.60gβ-烟酰胺单核苷酸。
[0065]
实施例6
[0066]
实施例6与实施例1的区别在于,
[0067]
称取5g烟酰胺核糖三氟甲磺酸盐(12.4mmol),加入50ml反应瓶,加入25ml磷酸三甲酯,降温至-10~0℃,加入2.66g 1,8-双二甲氨基萘(12.4mmol),然后滴加10.5g三氯氧磷(68.6mmol),反应18h后,将反应液减压抽滤并将滤液减压浓缩得到浓缩产物。
[0068]
于温度为-10~-5℃下,向浓缩产物中加入10ml纯化水,溶清后,缓慢滴加100ml乙腈,搅拌析晶3h,过滤,即得8.05gβ-烟酰胺单核苷酸。
[0069]
实施例7
[0070]
实施例7与实施例1的区别在于,
[0071]
1,8-双二甲氨基萘、烟酰胺核糖氯化物(34.4mmol)与三氯氧磷的摩尔比为0.5:1:
5,最终得到7.97gβ-烟酰胺单核苷酸。
[0072]
实施例8
[0073]
实施例8与实施例1的区别在于,磷酰化反应的温度为-10~0℃,最终得到8.82gβ-烟酰胺单核苷酸。
[0074]
实施例9
[0075]
实施例9与实施例1的区别在于,磷酰化反应的时间为18h,最终得到8.59gβ-烟酰胺单核苷酸。
[0076]
实施例10
[0077]
实施例10与实施例1的区别在于,磷酰化反应的时间为36h,最终得到8.59gβ-烟酰胺单核苷酸。
[0078]
实施例11
[0079]
实施例11与实施例1的区别在于,磷酰化反应的时间为12h,最终得到8.30gβ-烟酰胺单核苷酸。
[0080]
实施例12
[0081]
实施例12与实施例1的区别在于,磷酰化反应的时间为48h,最终得到8.35gβ-烟酰胺单核苷酸。
[0082]
实施例13
[0083]
实施例13与实施例1的区别在于,磷酰化反应的时间为10h,最终得到8.07gβ-烟酰胺单核苷酸。
[0084]
实施例14
[0085]
实施例14与实施例1的区别在于,结晶处理的温度为-5~0℃,最终得到8.19gβ-烟酰胺单核苷酸。
[0086]
实施例15
[0087]
实施例15与实施例1的区别在于,结晶处理的时间为2h,最终得到8.64gβ-烟酰胺单核苷酸。
[0088]
实施例16
[0089]
实施例16与实施例1的区别在于,结晶处理的时间为1h,最终得到8.28gβ-烟酰胺单核苷酸。
[0090]
实施例17
[0091]
实施例17与实施例1的区别在于,结晶处理的时间为6h,最终得到8.34gβ-烟酰胺单核苷酸。
[0092]
实施例18
[0093]
实施例18与实施例1的区别在于,结晶处理的时间为0.5h,最终得到8.11gβ-烟酰胺单核苷酸。
[0094]
实施例19
[0095]
实施例19与实施例1的区别在于,水与乙腈的体积比为1:15,最终得到8.64gβ-烟酰胺单核苷酸。
[0096]
实施例20
[0097]
实施例20与实施例1的区别在于,水与丙酮的体积比为1:5,最终得到8.20gβ-烟酰
胺单核苷酸。
[0098]
实施例21
[0099]
实施例21与实施例1的区别在于,水与丙酮的体积比为1:20,最终得到8.23gβ-烟酰胺单核苷酸。
[0100]
实施例22
[0101]
实施例22与实施例1的区别在于,水与丙酮的体积比为1:3,最终得到8.03gβ-烟酰胺单核苷酸。
[0102]
对比例1
[0103]
对比例1与实施例1的区别在于,不加1,8-双二甲氨基萘,最终得到4.25gβ-烟酰胺单核苷酸。
[0104]
对比例2
[0105]
对比例2与实施例1的区别在于,采用三乙胺代替1,8-双二甲氨基萘,最终得到5.85gβ-烟酰胺单核苷酸。
[0106]
对比例3
[0107]
对比例3与实施例1的区别在于,采用二异丙基乙胺代替1,8-双二甲氨基萘,最终得到5.90gβ-烟酰胺单核苷酸。
[0108]
将上述实施例1至22、对比例1至3制备得到的β-烟酰胺单核苷酸的收率、纯度分别列于表1。
[0109]
表1
[0110]
[0111][0112]
从以上的描述中,可以看出,本发明上述的实施例实现了如下技术效果:
[0113]
烟酰胺核苷盐的五元杂环上的2位羟基为伯羟基,3、4位羟基属于仲羟基,由于伯羟基的反应活性强于仲羟基,当发生上述磷酰化反应时,1,8-双二甲氨基萘优先与烟酰胺核苷盐的2位羟基形成复合物,且一方面由于1,8-双二甲氨基萘为含有两个芳环的刚性结
构,其体积较大,可抑制三氯氧磷继续对2位或3位羟基的进攻;另一方面在进行磷酰化反应时,1,8-双二甲氨基的一个氮原子有利于2位羟基氢的拔除,另一个氮原子有助于磷酰氯中氯的去除,在上述两个n原子的协同作用下有利于氯化氢的去除,同时,由于1,8-双二甲氨基萘中的两个氮原子距离较近,使得1,8-双二甲氨基萘在脱除氯化氢的过程中形成的过度中间体更稳定,从而使脱除氯化氢的过程倾向于分子内的反应,进一步地提高了磷酰化反应的选择性。
[0114]
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1