一种具有降解BTK激酶的化合物及其制备方法和药学上的应用与流程
一种具有降解btk激酶的化合物及其制备方法和药学上的应用
技术领域
1.本发明涉及一种通式(i)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,及其中间体和制备方法,以及在btk相关疾病如肿瘤或自身免疫系统疾病中的用途。
背景技术:
2.布鲁顿酪氨酸蛋白激酶(btk,bruton’s tyrosine kinase)是非受体蛋白酪氨酸激酶tec家族的成员,是b细胞抗原受体(bcr)信号通路中的关键调节因子,分布在淋巴系统、造血及血液系统中。btk突变会引起下游肿瘤细胞的增殖、分化以及血管生成等信号通路的激活,会导致x连锁无丙种球蛋白血症、非霍奇金淋巴瘤(nhl)与许多b细胞恶性肿瘤,包括慢性淋巴细胞性白血病(cll)、套细胞淋巴瘤以及弥漫大b细胞淋巴瘤。由于主要在b细胞和髓细胞中表达,btk是一种靶向性和安全性较好的靶点。
3.protac(proteolysis targeting chimera)分子是一类能够同时结合靶向蛋白和e3泛素连接酶的双功能化合物,此类化合物能够被细胞的蛋白酶体识别,引起靶向蛋白的降解,能够有效地降低靶向蛋白在细胞中的含量。通过在protac分子引入能结合不同靶向蛋白的配体,使protac技术应用于各种疾病的治疗成为可能,该技术近年来同时得到了广泛的关注。
技术实现要素:
4.本发明开发了一种结构新颖的、药效好、生物利用度高、更安全的btk抑制剂,用于治疗与btk相关疾病如肿瘤或自身免疫系统疾病。
5.本发明开发了一种结构新颖的、药效好、生物利用度高、更安全、能抑制或降解btk的btk抑制剂与e3泛素连接酶的protac化合物,用于治疗与btk相关疾病如肿瘤或自身免疫系统疾病。
6.本发明涉及一种通式(i)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,其中
7.b-l-k
ꢀꢀꢀ
(i)
8.l选自-ak1-cy1-ak2-cy2-ak3-cy3-ak4-cy4-ak5-;
9.ak1、ak2、ak3、ak4和ak5各自独立的选自ch2、o、nh或者键;
10.cy1、cy2、cy3和cy4各自独立的选自3至12元杂环、3至12元环烷基、6至10元芳基或键,所述杂环、环烷基或芳基任选进一步被0至4个选自h、f、cl、br、i、oh、nh2、oxo、cf3、cooh、cn、c
1-4
烷基、卤素取代的c
1-4
烷基、羟基取代的c
1-4
烷基或c
1-4
烷氧基的取代基所取代,所述的杂环含有1至4个选自o、s、n的杂原子;
11.ak1、ak2、ak3、ak4或ak5为o时,不能直接与b连接;
12.ak1、ak2、ak3、ak4或ak5不为键时,互相不能直接连接;
13.当ak1、cy1、ak2、cy2、ak3、cy3、ak4、cy4、ak5有4个及以上不为键时,cy1、cy2、cy3和cy4中至少有一个不为哌啶、哌嗪、嘧啶或吡啶;
14.b选自b1-w1-b2-w2-b3-w3-b4;
15.b1选自6元杂芳环或苯基,所述的杂芳环或苯基进一步任选被0至4个r
b1
所取代,所述的杂芳环含有1至4个选自o、s、n的杂原子;
16.w1选自-o-、-s-、-nh-、-nhco-或-conh-;
17.w2选自键、-co-、-o-、-s-、-nh-、-nhco-或-conh-;
18.w3选自键、-co-、-o-、-s-、-nh-、-nhco-或-conh-;
19.b2选自6元杂芳环或苯基,所述的杂芳环或苯基任选进一步任选被0至4个r
b2
所取代,所述的杂芳环含有1至4个选自o、s、n的杂原子;
20.b3选自8-10元杂并环或5-6元杂芳环,所述的杂并环或杂芳环任选进一步任选被0至4个r
b3
所取代,所述的杂并环或杂芳环含有1至4个选自o、s、n的杂原子;
21.当b3选自8-10元杂并环时,w2不为键;
22.b4选自键或4-10元饱和杂环,所述的饱和杂环选自单环、并环或螺环,所述的饱和杂环、单环、并环或螺环任选进一步任选被0至4个r
b4
所取代,所述的饱和杂环含有1至2个选自o、s、n的杂原子;
23.r
b1
、r
b2
、r
b3
或r
b4
各自独立的选自h、f、cl、br、i、oh、nh2、cn、cf3、cooh、conh2、c
1-4
烷基、羟基取代的c
1-4
烷基、卤素取代的c
1-4
烷基或c
1-4
烷氧基,所述的烷基和烷氧基任选进一步被0至4个选自h、f、cl、br、i、oh、nh2、cn、conh2、c
1-4
烷基或c
1-4
烷氧基的取代基所取代;
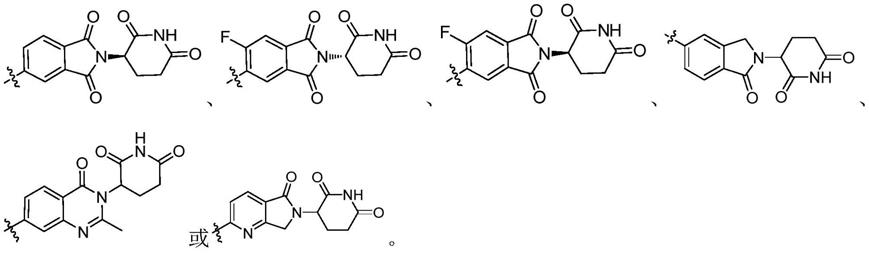
24.k选自
25.环e选自苯环或者5-6元的杂芳环,所述的杂芳环含有1至2个选自o、s、n的杂原子;
26.r
k2
选自ch2、c=o、s=o、so2;
27.r
k1
、r
k3
或r
k4
各自独立的选自h、f、cl、br、i、oh、nh2、cn、cooh、c
1-4
烷基或c
1-4
烷氧基;
28.r
k5
选自c=o或p1或p2各自独立的选自0、1、2、3或4。
29.本发明的一些实施例涉及一种通式(i)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,其中
30.cy1、cy2、cy3和cy4各自独立的选自3元杂环、4元杂环、5元杂环、6元杂环、7元杂环、8元杂环、9元杂环、10元杂环、11元杂环、12元杂环、3元环烷基、4元环烷基、5元环烷基、6元环烷基、7元环烷基、8元环烷基、9元环烷基、10元环烷基、11元环烷基、12元环烷基、6至10元芳基或键,优选键、4元杂单环、5元杂单环、6元杂单环、7元杂单环、5元杂并环、6元杂并环、7元杂并环、8元杂并环、9元杂并环、10元杂并环、6元杂螺环、7元杂螺环、8元杂螺环、9元杂螺环、10元杂螺环、11元杂螺环、12元杂螺环、7元杂桥环、8元杂桥环、9元杂桥环、10元杂桥环、4元单环烷基、5元单环烷基、6元单环烷基、7元单环烷基、5元并环烷基、6元并环烷基、7元并环烷基、8元并环烷基、9元并环烷基、10元并环烷基、6元螺环烷基、7元螺环烷基、8元
螺环烷基、9元螺环烷基、10元螺环烷基、11元螺环烷基、12元螺环烷基、7元桥环烷基、8元桥环烷基、9元桥环烷基、10元桥环烷基或6-10元芳基,所述芳基、环烷基、杂单环、杂并环、杂螺环或杂桥环任选进一步被0、1、2、3或4个选自h、f、cl、br、i、oh、nh2、oxo、cf3、cooh、cn、c
1-4
烷基、羟基取代的c
1-4
烷基、卤素取代的c
1-4
烷基或c
1-4
烷氧基的取代基所取代,所述的杂单环、杂并环、杂螺环或杂桥环含有1、2、3或4个选自o、s、n的杂原子;
31.b1选自6元杂芳环或苯基,优选苯基或吡啶基,所述的杂芳环、苯基或吡啶基进一步任选被0至4个r
b1
所取代,所述的杂芳环含有1至4个选自o、s、n的杂原子;
32.w1选自-o-、-nhco-或-conh-;
33.b2选自6元杂芳环或苯基,优选苯基或吡啶基,所述的杂芳环、苯基或吡啶基进一步任选被0至4个r
b2
所取代,所述的杂芳环含有1至4个选自o、s、n的杂原子;
34.b3选自8-10元杂并环或5-6元杂芳环,当被取代时,任选进一步任选被0至4个r
b3
所取代,所述的杂并环或杂芳环含有1至4个选自o、s、n的杂原子;
35.或者b3可以选自取代或未取代的如下基团之一:咪唑并嘧啶、吡唑并嘧啶、吡咯并嘧啶、咪唑并吡嗪、吡唑并吡嗪、咪唑并四氢嘧啶、吡唑并四氢嘧啶、吡唑或咪唑,当被取代时,任选进一步任选被0至4个r
b3
所取代;
36.b4选自键或4-10元饱和杂环,所述的饱和杂环选自单环、并环或螺环,所述的饱和杂环、单环、并环或螺环任选进一步任选被0至4个r
b4
所取代,所述的饱和杂环含有1至2个选自o、s、n的杂原子;
37.或者b4可以选自取代的或者未取代的如下基团之一:氮杂环丁基、氮杂环戊基、哌啶、环丙基并氮杂环丁基、环丙基并氮杂环戊基、环丙基并氮杂环己基、环丙基并哌啶、环丁基并氮杂环丁基、环丁基并氮杂环戊基、环丁基并氮杂环已基、环丁基并哌啶、环戊基并氮杂环丁基、环戊基并氮杂环戊基、环戊基并氮杂环已基、环戊基并哌啶、环已基并氮杂环丁基、环已基并氮杂环戊基、环已基并氮杂环已基、环己基并哌啶、环丁基螺氮杂环丁基、环丁基螺氮杂环戊基、环丁基螺氮杂环已基、环已基螺氮杂环丁基或环已基螺氮杂环戊基,当被取代时,任选被0至4个r
b4
所取代;
38.k选自
39.环e选自苯环或者5-6元的杂芳环,所述的杂芳环含有1至2个选自o、s、n的杂原子;
40.或者环e可以选自苯环、吡啶、噻吩、呋喃、吡咯、噻唑、恶唑、咪唑或吡唑;
41.r
k2
选自ch2、c=o、s=o、so2;
42.r
k1
、r
k3
或r
k4
各自独立的选自h、f、cl、br、i、oh、nh2、cn、cooh、c
1-4
烷基或c
1-4
烷氧基;
43.r
k5
选自c=o或p1或p2各自独立的选自0、1、2、3或4。
44.本发明的一些实施例涉及一种通式(i)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,其中
45.cy1、cy2、cy3和cy4各自独立的选自3元杂环、4元杂环、5元杂环、6元杂环、7元杂
环、8元杂环、9元杂环、10元杂环、11元杂环、12元杂环、3元环烷基、4元环烷基、5元环烷基、6元环烷基、7元环烷基、8元环烷基、9元环烷基、10元环烷基、11元环烷基、12元环烷基、6至10元芳基或键,优选键、4元杂单环、5元杂单环、6元杂单环、7元杂单环、5元杂并环、6元杂并环、7元杂并环、8元杂并环、9元杂并环、10元杂并环、6元杂螺环、7元杂螺环、8元杂螺环、9元杂螺环、10元杂螺环、11元杂螺环、12元杂螺环、7元杂桥环、8元杂桥环、9元杂桥环、10元杂桥环、4元单环烷基、5元单环烷基、6元单环烷基、7元单环烷基、5元并环烷基、6元并环烷基、7元并环烷基、8元并环烷基、9元并环烷基、10元并环烷基、6元螺环烷基、7元螺环烷基、8元螺环烷基、9元螺环烷基、10元螺环烷基、11元螺环烷基、12元螺环烷基、7元桥环烷基、8元桥环烷基、9元桥环烷基、10元桥环烷基或6-10元芳基,所述芳基、环烷基、杂单环、杂并环、杂螺环或杂桥环任选进一步被0、1、2、3或4个选自h、f、cl、br、i、oh、nh2、oxo、cf3、cooh、cn、c
1-4
烷基、羟基取代的c
1-4
烷基、卤素取代的c
1-4
烷基或c
1-4
烷氧基的取代基所取代,所述的杂单环、杂并环、杂螺环或杂桥环含有1、2、3或4个选自o、s、n的杂原子;
46.或者cy1、cy2、cy3和cy4可以各自独立的选自取代的或者未取代的如下基团之一:键、苯基、萘基、环丁基、环戊基、环己基、环丁基并环丁基、环丁基并环戊基、环丁基并环己基、环戊基并环戊基、环戊基并环己基、环己基并环己基、环丙基并环丁基、环丙基并环戊基、环丙基并环己基、环丁基螺环丁基、环丁基螺环戊基、环丁基螺环己基、环戊基螺环戊基、环戊基螺环己基、环己基螺环己基、环丙基螺环丁基、环丙基螺环戊基、环丙基螺环己基、氮杂环丁基、氮杂环戊基、哌啶、吗啉、哌嗪、吡咯、吡唑、咪唑、噻唑、吡啶、哒嗪、嘧啶、吡嗪、三氮唑、四氮唑、环丙基并氮杂环丁基、环丙基并氮杂环戊基、环丙基并氮杂环己基、环丙基并哌啶、环丁基并氮杂环丁基、环丁基并氮杂环戊基、环丁基并氮杂环已基、环丁基并哌啶、环戊基并氮杂环丁基、环戊基并氮杂环戊基、环戊基并氮杂环已基、环戊基并哌啶、环已基并氮杂环丁基、环已基并氮杂环戊基、环已基并氮杂环已基、环己基并哌啶、氮杂环丁基并氮杂环丁基、氮杂环丁基并氮杂环戊基、氮杂环丁基并氮杂环已基、氮杂环丁基并哌啶、氮杂环戊基并氮杂环丁基、氮杂环戊基并氮杂环戊基、氮杂环戊基并氮杂环已基、氮杂环戊基并哌啶、氮杂环已基并氮杂环丁基、氮杂环已基并氮杂环戊基、氮杂环已基并氮杂环已基、氮杂环己基并哌啶、环丁基螺氮杂环丁基、环丁基螺氮杂环戊基、环丁基螺氮杂环已基、环戊基螺氮杂环丁基、环戊基螺氮杂环戊基、环戊基螺氮杂环已基、环已基螺氮杂环丁基、环已基螺氮杂环戊基、环已基螺氮杂环已基、氮杂环丁基螺氮杂环丁基、氮杂环丁基螺氮杂环戊基、氮杂环丁基螺氮杂环已基、氮杂环戊基螺氮杂环丁基、氮杂环戊基螺氮杂环戊基、氮杂环戊基螺氮杂环已基、氮杂环已基螺氮杂环丁基、氮杂环已基螺氮杂环戊基、氮杂环已基螺氮杂环已基、环丁基螺哌啶、环戊基螺哌啶、环己基螺哌啶、氮杂环丁基螺哌啶、氮杂环戊基螺哌啶、氮杂环己基螺哌啶、当被取代时,任选被0至4个选自h、f、cl、br、i、oh、nh2、oxo、cf3、cooh、cn、c
1-4
烷基、羟基取代的c
1-4
烷基、卤素取代的c
1-4
烷基或c
1-4
烷氧基的取代基所取代;
47.b1选自苯基或吡啶基,所述的苯基或吡啶基进一步任选被0至4个r
b1
所取代;
48.w1选自-o-、-nhco-或-conh-;
49.b2选自苯基或吡啶基,所述的苯基或吡啶基进一步任选被0至4个r
b2
所取代;
50.b3选自取代或未取代的如下基团之一:咪唑并嘧啶、吡唑并嘧啶、吡咯并嘧啶、咪唑并吡嗪、吡唑并吡嗪、咪唑并四氢嘧啶、吡唑并四氢嘧啶、吡唑或咪唑,当被取代时,任选进一步任选被0至4个r
b3
所取代;
51.当b3选自8-10元杂并环时,w2不为键;
52.b4选自键或4-10元饱和杂环,所述的饱和杂环选自单环、并环或螺环,所述的饱和杂环、单环、并环或螺环任选进一步任选被0至4个r
b4
所取代,所述的饱和杂环含有1至2个选自o、s、n的杂原子;
53.或者b4可以选自取代的或者未取代的如下基团之一:氮杂环丁基、氮杂环戊基、哌啶、环丙基并氮杂环丁基、环丙基并氮杂环戊基、环丙基并氮杂环己基、环丙基并哌啶、环丁基并氮杂环丁基、环丁基并氮杂环戊基、环丁基并氮杂环已基、环丁基并哌啶、环戊基并氮杂环丁基、环戊基并氮杂环戊基、环戊基并氮杂环已基、环戊基并哌啶、环已基并氮杂环丁基、环已基并氮杂环戊基、环已基并氮杂环已基、环己基并哌啶、环丁基螺氮杂环丁基、环丁基螺氮杂环戊基、环丁基螺氮杂环已基、环已基螺氮杂环丁基或环已基螺氮杂环戊基,当被取代时,任选被0至4个r
b4
所取代;
54.或者b4可以选自或者b4可以选自
55.或者b可以选自或者b可以选自
56.或者b可以选自
57.r
b1
、r
b2
、r
b3
或r
b4
各自独立的选自h、f、cl、br、i、oh、nh2、cn、cf3、cooh、conh2、c
1-4
烷基、羟基取代的c
1-4
烷基、卤素取代的c
1-4
烷基或c
1-4
烷氧基,所述的烷基和烷氧基任选进一步被0至4个选自h、f、cl、br、i、oh、nh2、cn、conh2、c
1-4
烷基或c
1-4
烷氧基的取代基所取代;
58.或者r
b1
、r
b2
、r
b3
或r
b4
可以各自独立的选自h、f、cl、br、i、oh、nh2、cn、conh2、cf3、cooh、羟甲基、甲基或甲氧基,所述的甲基或甲氧基任选进一步被0至4选自h、f、cl、br、i的取代基所取代;
59.n1、n2、n3各自独立的选自0、1、2、3或4;
60.k选自
61.或者k可以选自
62.或者k可以选自或者k可以选自
63.或者k可以选自
64.r
k2
选自ch2、c=o、s=o、so2;
65.或者r
k2
可以选自ch2或c=o;
66.r
k1
、r
k3
或r
k4
各自独立的选自h、f、cl、br、i、oh、nh2、cn、cooh、c
1-4
烷基或c
1-4
烷氧基;
67.或者r
k1
、r
k3
或r
k4
各自独立的选自h、f、cl、br、i、oh或nh2;
68.r
k5
选自c=o或
69.p1或p2各自独立的选自0、1、2、3或4。
70.本发明的一些实施例涉及一种通式(i)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,其中
71.cy1、cy2、cy3和cy4各自独立的选自取代的或者未取代的如下基团之一:键、苯基、萘基、环丁基、环戊基、环己基、环丁基并环丁基、环丁基并环戊基、环丁基并环己基、环戊基并环戊基、环戊基并环己基、环己基并环己基、环丙基并环丁基、环丙基并环戊基、环丙基并环己基、环丁基螺环丁基、环丁基螺环戊基、环丁基螺环己基、环戊基螺环戊基、环戊基螺环己基、环己基螺环己基、环丙基螺环丁基、环丙基螺环戊基、环丙基螺环己基、氮杂环丁基、氮杂环戊基、哌啶、吗啉、哌嗪、吡咯、吡唑、咪唑、噻唑、吡啶、哒嗪、嘧啶、吡嗪、三氮唑、四氮唑、环丙基并氮杂环丁基、环丙基并氮杂环戊基、环丙基并氮杂环己基、环丙基并哌啶、环丁基并氮杂环丁基、环丁基并氮杂环戊基、环丁基并氮杂环已基、环丁基并哌啶、环戊基并氮杂环丁基、环戊基并氮杂环戊基、环戊基并氮杂环已基、环戊基并哌啶、环已基并氮杂环丁基、环已基并氮杂环戊基、环已基并氮杂环已基、环己基并哌啶、氮杂环丁基并氮杂环丁基、氮杂环丁基并氮杂环戊基、氮杂环丁基并氮杂环已基、氮杂环丁基并哌啶、氮杂环戊基并氮杂环丁基、氮杂环戊基并氮杂环戊基、氮杂环戊基并氮杂环已基、氮杂环戊基并哌啶、氮杂环已基并氮杂环丁基、氮杂环已基并氮杂环戊基、氮杂环已基并氮杂环已基、氮杂环己基并哌啶、环丁基螺氮杂环丁基、环丁基螺氮杂环戊基、环丁基螺氮杂环已基、环戊基螺氮杂环丁基、环戊基螺氮杂环戊基、环戊基螺氮杂环已基、环已基螺氮杂环丁基、环已基螺氮杂环戊基、环已基螺氮杂环已基、氮杂环丁基螺氮杂环丁基、氮杂环丁基螺氮杂环戊基、氮杂环
丁基螺氮杂环已基、氮杂环戊基螺氮杂环丁基、氮杂环戊基螺氮杂环戊基、氮杂环戊基螺氮杂环已基、氮杂环已基螺氮杂环丁基、氮杂环已基螺氮杂环戊基、氮杂环已基螺氮杂环已基、环丁基螺哌啶、环戊基螺哌啶、环己基螺哌啶、氮杂环丁基螺哌啶、氮杂环戊基螺哌啶、氮杂环己基螺哌啶、当被取代时,任选被0至4个选自h、f、cl、br、i、oh、nh2、oxo、cf3、cooh、cn、c
1-4
烷基、羟基取代的c
1-4
烷基、卤素取代的c
1-4
烷基或c
1-4
烷氧基的取代基所取代;
72.b选自b选自
73.或者b可以选自或者b可以选自
74.b4选自取代的或者未取代的如下基团之一:氮杂环丁基、氮杂环戊基、哌啶、环丙基并氮杂环丁基、环丙基并氮杂环戊基、环丙基并氮杂环己基、环丙基并哌啶、环丁基并氮杂环丁基、环丁基并氮杂环戊基、环丁基并氮杂环已基、环丁基并哌啶、环戊基并氮杂环丁基、环戊基并氮杂环戊基、环戊基并氮杂环已基、环戊基并哌啶、环已基并氮杂环丁基、环已基并氮杂环戊基、环已基并氮杂环已基、环己基并哌啶、环丁基螺氮杂环丁基、环丁基螺氮杂环戊基、环丁基螺氮杂环已基、环已基螺氮杂环丁基或环已基螺氮杂环戊基,当被取代时,任选被0至4个r
b4
所取代;
75.或者b4可以选自
76.r
b1
、r
b2
、r
b3
或r
b4
各自独立的选自h、f、cl、br、i、oh、nh2、cn、conh2、cf3、cooh、羟甲基、甲基或甲氧基,所述的甲基或甲氧基任选进一步被0至4选自h、f、cl、br、i的取代基所取代;
77.n1、n2、n3各自独立的选自0、1、2、3或4;
78.k选自
79.r
k2
选自ch2或c=o;
80.r
k1
、r
k3
或r
k4
各自独立的选自h、f、cl、br、i、oh或nh2;
81.p1或p2各自独立的选自0、1或2;
82.或者k可以选自或者k可以选自
83.或者k可以选自或者k可以选自
84.或者k可以选自
85.本发明的一些实施例涉及一种通式(i)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,其中
86.b选自b选自
87.或者b可以选自或者b可以选自
88.b4选自取代的或者未取代的如下基团之一:氮杂环丁基、氮杂环戊基、哌啶、环丙基并氮杂环丁基、环丙基并氮杂环戊基、环丙基并氮杂环己基、环丙基并哌啶、环丁基并氮杂环丁基、环丁基并氮杂环戊基、环丁基并氮杂环已基、环丁基并哌啶、环戊基并氮杂环丁基、环戊基并氮杂环戊基、环戊基并氮杂环已基、环戊基并哌啶、环已基并氮杂环丁基、环已基并氮杂环戊基、环已基并氮杂环已基、环己基并哌啶、环丁基螺氮杂环丁基、环丁基螺氮杂环戊基、环丁基螺氮杂环已基、环已基螺氮杂环丁基或环已基螺氮杂环戊基,当被取代时,任选被0至4个r
b4
所取代;
89.r
b1
、r
b2
、r
b3
或r
b4
各自独立的选自h、f、cl、br、i、oh、nh2、cn、conh2、cf3、cooh、羟甲基、甲基或甲氧基,所述的甲基或甲氧基任选进一步被0至4选自h、f、cl、br、i的取代基所取
代;
90.n1、n2、n3各自独立的选自0、1、2、3或4;
91.或者b4可以选自或者b4可以选自或者b4可以选自
92.l选自键、l选自键、
93.或者l选自
94.l左边与b连接,l右边与k连接;
95.k选自
96.或者k可以选自
97.r
k2
选自ch2或c=o;
98.r
k1
、r
k3
或r
k4
各自独立的选自h、f、cl、br、i、oh或nh2;
99.p1或p2各自独立的选自0、1或2;
100.或者k可以选自或者k可以选自
101.或者k可以选自或者k可以选自
102.或者k可以选自或者k可以选自
103.本发明的一些实施例涉及一种通式(i)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,其中
104.b选自
105.b4选自选自取代的或者未取代的如下基团之一:氮杂环丁基、氮杂环戊基、哌啶、环丙基并氮杂环丁基、环丙基并氮杂环戊基、环丙基并氮杂环己基、环丙基并哌啶、环丁基并氮杂环丁基、环丁基并氮杂环戊基、环丁基并氮杂环已基、环丁基并哌啶、环戊基并氮杂环丁基、环戊基并氮杂环戊基、环戊基并氮杂环已基、环戊基并哌啶、环已基并氮杂环丁基、环已基并氮杂环戊基、环已基并氮杂环已基、环己基并哌啶、环丁基螺氮杂环丁基、环丁基螺氮杂环戊基、环丁基螺氮杂环已基、环已基螺氮杂环丁基或环已基螺氮杂环戊基,当被取代时,任选被0至4个r
b4
所取代;
106.r
b4
各自独立的选自h、f、cl、br、i、oh、nh2、cn、conh2、cf3、cooh、羟甲基、甲基或甲氧基,所述的甲基或甲氧基任选进一步被0至4选自h、f、cl、br、i的取代基所取代;
107.或者b4可以选自或者b4可以选自
108.l选自键、l选自键、
109.或者l选自或者l选自
110.l左边与b连接,l右边与k连接;
111.k选自k选自
112.或者k可以选自或者k可以选自
113.或者k可以选自或者k可以选自
114.本发明的一些实施例涉及一种通式(i)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,其中
115.b选自
116.b4选自选自取代的或者未取代的如下基团之一:氮杂环丁基、氮杂环戊基、哌啶、环丙基并氮杂环丁基、环丙基并氮杂环戊基、环丙基并氮杂环己基、环丙基并哌啶、环丁基并氮杂环丁基、环丁基并氮杂环戊基、环丁基并氮杂环已基、环丁基并哌啶、环戊基并氮杂环丁基、环戊基并氮杂环戊基、环戊基并氮杂环已基、环戊基并哌啶、环已基并氮杂环丁基、环已基并氮杂环戊基、环已基并氮杂环已基、环己基并哌啶、环丁基螺氮杂环丁基、环丁基螺氮杂环戊基、环丁基螺氮杂环已基、环已基螺氮杂环丁基或环已基螺氮杂环戊基,当被取代时,任选被0至4个r
b4
所取代;
117.r
b4
各自独立的选自h、f、cl、br、i、oh、nh2、cn、conh2、cf3、cooh、羟甲基、甲基或甲氧基,所述的甲基或甲氧基任选进一步被0至4选自h、f、cl、br、i的取代基所取代;
118.或者b4可以选自或者b4可以选自或者b4可以选自
119.l选自键、
120.或者l选自或者l选自或者l选自
121.l左边与b连接,l右边与k连接;
122.k选自
123.或者k可以选自或者k可以选自
124.或者k可以选自或者k可以选自
125.本发明的一些实施例涉及一种通式(i)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,其中
126.b选自
127.b4选自选自取代的或者未取代的如下基团之一:氮杂环丁基、氮杂环戊基、哌啶、环丙基并氮杂环丁基、环丙基并氮杂环戊基、环丙基并氮杂环己基、环丙基并哌啶、环丁基并氮杂环丁基、环丁基并氮杂环戊基、环丁基并氮杂环已基、环丁基并哌啶、环戊基并氮杂环丁基、环戊基并氮杂环戊基、环戊基并氮杂环已基、环戊基并哌啶、环已基并氮杂环丁基、环已基并氮杂环戊基、环已基并氮杂环已基、环己基并哌啶、环丁基螺氮杂环丁基、环丁基螺氮杂环戊基、环丁基螺氮杂环已基、环已基螺氮杂环丁基或环已基螺氮杂环戊基,当被取代时,任选被0至4个r
b4
所取代;
128.r
b4
各自独立的选自h、f、cl、br、i、oh、nh2、cn、conh2、cf3、cooh、羟甲基、甲基或甲氧基,所述的甲基或甲氧基任选进一步被0至4选自h、f、cl、br、i的取代基所取代;
129.或者b4可以选自或者b4可以选自
130.l选自键、
131.或者l选自或者l选自或者l选自
132.l左边与b连接,l右边与k连接;
133.k选自
134.或者k可以选自或者k可以选自
135.或者k可以选自或者k可以选自
136.本发明的一些实施例涉及一种通式(ia)、(ib)、(ic)或(id)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,其中
137.b-cy1-k(ia)
138.b-cy1-cy2-k(ib)
139.b-cy1-cy2-cy3-k(ic)
140.b-cy1-cy2-cy3-cy4-k(id)
141.b选自
142.b4选自4至6元含氮杂单环、5至10元含氮杂并环、6至10元含氮杂螺环或4至6元单环烷基,所述的环烷基、杂单环、杂并环或杂螺环任选进一步被0至4个选自h、f、cl、br、i、oh、nh2、cn、cf3、cooh、conh2、c
1-4
烷基、羟基取代的c
1-4
烷基、卤素取代的c
1-4
烷基或c
1-4
烷氧基,所述的杂单环、杂并环或杂螺环含有1至4个选自o、s、n的杂原子;
143.cy1、cy2、cy3、cy4各自独立的选自取代的或者未取代的如下基团之一:4至6元含氮杂单环、5至10元含氮杂并环、6至10元含氮杂螺环、4至6元单环烷基或苯基,所述苯基、环烷基、杂单环、杂并环或杂螺环任选进一步被0至4个选自h、f、cl、br、i、oh、nh2、oxo、cf3、cooh、cn、c
1-4
烷基、卤素取代的c
1-4
烷基、羟基取代的c
1-4
烷基或c
1-4
烷氧基的取代基所取代,所述的杂单环、杂并环或杂螺环含有1至4个选自o、s、n的杂原子;
144.k选自
145.本发明的一些实施例涉及一种通式(ia)、(ib)、(ic)或(id)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,其中
146.b选自b4选自b4选自
147.cy1、cy2、cy3、cy4各自独立的选自cy1、cy2、cy3、cy4各自独立的选自
148.k选自k选自
149.本发明的一些实施例涉及一种通式(i)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,其中所述化合物选自如下结构之一:
150.151.152.153.154.155.[0156][0157]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0158]
k选自
[0159]
r
k2
选自ch2、c=o、s=o、so2;
[0160]
r
k1
、r
k3
或r
k4
各自独立的选自h、f、cl、br、i、oh、nh2、cn、cooh、c
1-4
烷基或c
1-4
烷氧基;
[0161]
r
k5
选自c=o或p1或p2各自独立的选自0、1、2、3或4。
[0162]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0163]
k选自
[0164]
r
k2
选自ch2或c=o;
[0165]
r
k1
、r
k3
或r
k4
各自独立的选自h、f、cl、br、i、oh或nh2;
[0166]
p1或p2各自独立的选自0、1或2。
[0167]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0168]
k选自k选自
[0169]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0170]
k选自k选自
[0171]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0172]
k选自k选自
[0173]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0174]
b4选自取代的或者未取代的如下基团之一:氮杂环丁基、氮杂环戊基、哌啶、环丙基并氮杂环丁基、环丙基并氮杂环戊基、环丙基并氮杂环己基、环丙基并哌啶、环丁基并氮杂环丁基、环丁基并氮杂环戊基、环丁基并氮杂环已基、环丁基并哌啶、环戊基并氮杂环丁基、环戊基并氮杂环戊基、环戊基并氮杂环已基、环戊基并哌啶、环已基并氮杂环丁基、环已基并氮杂环戊基、环已基并氮杂环已基、环己基并哌啶、环丁基螺氮杂环丁基、环丁基螺氮杂环戊基、环丁基螺氮杂环已基、环已基螺氮杂环丁基或环已基螺氮杂环戊基,当被取代时,任选被0至4个r
b4
所取代;
[0175]
r
b4
各自独立的选自h、f、cl、br、i、oh、nh2、cn、conh2、cf3、cooh、羟甲基、甲基或甲氧基,所述的甲基或甲氧基任选进一步被0至4选自h、f、cl、br、i的取代基所取代。
[0176]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0177]
b4选自b4选自
[0178]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0179]
b选自
[0180]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0181]
b选自
[0182]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0183]
b选自
[0184]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0185]
b选自
[0186]
本发明的一些实施例涉及一种通式(i)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0187]
l选自-cy1-、-cy1-cy2-、-cy1-cy2-cy3-或-cy1-cy2-cy3-cy4-。
[0188]
本发明的一些实施例涉及一种通式(i)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0189]
l选自-ch
2-cy1-、-cy1-ch
2-cy2-。
[0190]
本发明的一些实施例涉及一种通式(i)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0191]
l选自-ch
2-cy1-、-cy1-ch
2-cy2-;
[0192]
cy1、cy2各自独立的选自氮杂环丁基、氮杂环戊基、哌啶。
[0193]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0194]
cy1、cy2、cy3和cy4各自独立的选自取代的或者未取代的如下基团之一:键、苯基、萘基、环丁基、环戊基、环己基、环丁基并环丁基、环丁基并环戊基、环丁基并环己基、环戊基并环戊基、环戊基并环己基、环己基并环己基、环丙基并环丁基、环丙基并环戊基、环丙基并环己基、环丁基螺环丁基、环丁基螺环戊基、环丁基螺环己基、环戊基螺环戊基、环戊基螺环己基、环己基螺环己基、环丙基螺环丁基、环丙基螺环戊基、环丙基螺环己基、氮杂环丁基、氮杂环戊基、哌啶、吗啉、哌嗪、吡咯、吡唑、咪唑、噻唑、吡啶、哒嗪、嘧啶、吡嗪、三氮唑、四氮唑、环丙基并氮杂环丁基、环丙基并氮杂环戊基、环丙基并氮杂环己基、环丙基并哌啶、环丁基并氮杂环丁基、环丁基并氮杂环戊基、环丁基并氮杂环已基、环丁基并哌啶、环戊基并氮杂环丁基、环戊基并氮杂环戊基、环戊基并氮杂环已基、环戊基并哌啶、环已基并氮杂环丁基、环已基并氮杂环戊基、环已基并氮杂环已基、环己基并哌啶、氮杂环丁基并氮杂环丁基、氮杂环丁基并氮杂环戊基、氮杂环丁基并氮杂环已基、氮杂环丁基并哌啶、氮杂环戊基并氮杂环丁基、氮杂环戊基并氮杂环戊基、氮杂环戊基并氮杂环已基、氮杂环戊基并哌啶、氮杂环已基并氮杂环丁基、氮杂环已基并氮杂环戊基、氮杂环已基并氮杂环已基、氮杂环己基并哌啶、环丁基螺氮杂环丁基、环丁基螺氮杂环戊基、环丁基螺氮杂环已基、环戊基螺氮杂环丁基、环戊基螺氮杂环戊基、环戊基螺氮杂环已基、环已基螺氮杂环丁基、环已基螺氮杂环戊基、环已基螺氮杂环已基、氮杂环丁基螺氮杂环丁基、氮杂环丁基螺氮杂环戊基、氮杂环丁基螺氮杂环已基、氮杂环戊基螺氮杂环丁基、氮杂环戊基螺氮杂环戊基、氮杂环戊基螺氮杂环已基、氮杂环已基螺氮杂环丁基、氮杂环已基螺氮杂环戊基、氮杂环已基螺氮杂环已基、环丁基螺哌啶、环戊基螺哌啶、环己基螺哌啶、氮杂环丁基螺哌啶、氮杂环戊基螺哌啶、氮杂环己基螺哌啶、当被取代时,任选被0至4个选自h、f、cl、br、i、oh、nh2、oxo、cf3、cooh、cn、c
1-4
烷基、羟基取代的c
1-4
烷基、卤素取代的c
1-4
烷基或c
1-4
烷氧基的取代基所取代。
[0195]
本发明的一些实施例涉及一种通式(i)所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,
[0196]
l选自键、
[0197]
或者l选自或者l选自或者l选自
[0198]
l左边与b连接,l右边与k连接。
[0199]
本发明的一些实施例涉及一种通式(i)、(ia)、(ib)、(ic)或(id)所示的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,其中所述的盐选自三氟乙酸盐。
[0200]
本发明涉及一种药物组合物,包括本发明所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶,以及要学上可接受的载体。
[0201]
本发明涉及一种本发明所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶在用于制备治疗与btk活性或表达量相关疾病的药物中的应用。
[0202]
本发明涉及一种本发明所述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶在用于制备治疗与抑制或降解btk相关疾病的药物中的应用。
[0203]
本发明涉及的本发明述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶的应用,其特征在于,所述的疾病选自肿瘤或自身免疫疾病。
[0204]
本发明涉及的本发明述的化合物或者其立体异构体、溶剂化物、前药、代谢产物、药学上可接受的盐或共晶的应用,其特征在于,所述的肿瘤选自非霍奇金淋巴瘤、慢性淋巴细胞性白血病、套细胞淋巴瘤、b细胞淋巴瘤,自身免疫疾病选自内风湿关节炎或银屑病。
[0205]
除非有相反的陈述,在说明书和权利要求书中使用的术语具有下述含义。
[0206]
本发明所述基团和化合物中所涉及的碳、氢、氧、硫、氮或f、cl、br、i均包括它们的同位素情况,及本发明所述基团和化合物中所涉及的碳、氢、氧、硫或氮任选进一步被一个或多个它们对应的同位素所替代,其中碳的同位素包括
12
c、
13
c和
14
c,氢的同位素包括氕(h)、氘(d,又叫重氢)、氚(t,又叫超重氢),氧的同位素包括
16
o、
17
o和
18
o,硫的同位素包括
32
s、
33
s、
34
s和
36
s,氮的同位素包括
14
n和
15
n,氟的同位素包括
17
f和
19
f,氯的同位素包括
35
cl和
37
cl,溴的同位素包括
79
br和
81
br。
[0207]“烷基”是指1至20个碳原子的直链或支链饱和脂肪族烃基,优选为1至8个碳原子的烷基,更优选为1至6个碳原子的烷基,进一步优选为1至4个碳原子的烷基。非限制性实施例包括甲基、乙基、正丙基、异丙基、正丁基、仲丁基、新丁基、叔丁基、正戊基、异戊基、新戊基、正己基及其各种支链异构体;所述的烷基可以任选进一步被0至6个选自f、cl、br、i、羟基、巯基、硝基、氰基、氨基、烷基氨基、酰胺基、烯基、炔基、c
1-6
烷基、c
1-6
羟基烷基、c
1-6
烷氧基、3至8元碳环基、3至8元杂环基、3至8元碳环基氧基、3至8元杂环基氧基、羧基或者羧酸酯基的取代基所取代,本文中出现的烷基,其定义与本定义一致。
[0208]“烷氧基”是指-o-烷基。非限制性实施例包括甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、仲丁氧基、叔丁氧基、正戊氧基、正己氧基、环丙氧基和环丁氧基。所述的烷基可以任选进一步被0至5个选自f、cl、br、i、羟基、巯基、硝基、氰基、氨基、烷基氨基、烯基、炔基、烷基、羟基烷基、烷氧基、碳环基、杂环基、碳环基氧基、杂环基氧基、羧基或者羧酸酯基的取代基所取代。本文中出现的烷氧基,其定义与本定义一致。
[0209]“杂环基”或”杂环”是指取代的或未取代的饱和或不饱和的芳香环或者非芳香环,芳香环或者非芳香环可以是3至8元的单环、4至12元双环或者10至15元三环体系,且包含1至3个选自n、o或s的杂原子,优选3至8元杂环基,杂环基的环中选择性取代的n、s可被氧化成各种氧化态。杂环基可以连接在杂原子或者碳原子上,杂环基可以连接有桥环或者螺环,非限制性实施例包括环氧乙基、氮杂环丙基、氧杂环丁基、氮杂环丁基、1,3-二氧戊环基、1,4-二氧戊环基、1,3-二氧六环基、氮杂环庚基、吡啶基、呋喃基、噻吩基、吡喃基、n-烷基吡咯基、嘧啶基、吡嗪基、哒嗪基、咪唑基、哌啶基、哌叮基、吗啉基、硫代吗啉基、1,3-二噻基、二氢呋喃基、二氢吡喃基、二噻戊环基、四氢呋喃基、四氢吡咯基、四氢咪唑基、四氢噻唑基、四
氢吡喃基、苯并咪唑基、苯并吡啶基、吡咯并吡啶基、苯并二氢呋喃基、氮杂二环[3.2.1]辛烷基、氮杂二环[5.2.0]壬烷基、氧杂三环[5.3.1.1]十二烷基、氮杂金刚烷基和氧杂螺[3.3]庚烷基。所述的杂环基可以任选进一步被0至5个选自f、cl、br、i、=o、羟基、巯基、硝基、氰基、氨基、烷基氨基、酰胺基、烯基、炔基、烷基、羟基烷基、烷氧基、碳环基、杂环基、碳环基氧基、杂环基氧基、羧基或者羧酸酯基的取代基所取代。本文中出现的杂环基,其定义与本定义一致。
[0210]“螺环”是指取代的或未取代的单环之间共用一个碳原子(称螺原子)的5至20元多环基团,其可以包含0至5个双键,且可以含有0至5个选自n、o或s(=o)
n
的杂原子。优选为6至14元,进一步优选为6至12元,更优选6至10元,其非限定性实例包括:
[0211][0212]
当被取代时,取代基可以为1至5个选自f、cl、br、i、烷基、环烷基、烷氧基、卤代烷基、硫醇、羟基、硝基、巯基、氨基、氰基、异氰基、芳基、杂芳基、杂环基、桥环基、螺环基、并环基、羟基烷基、=o、羰基、醛、羧酸、甲酸酯、-(ch2)
m-c(=o)-r
a
、-o-(ch2)
m-c(=o)-r
a
、-(ch2)
m-c(=o)-nr
b
r
c
、-(ch2)
m
s(=o)
n
r
a
、-(ch2)
m-烯基-r
a
、or
d
或-(ch2)
m-炔基-r
a
(其中m、n为0、1或2)、芳基硫基、硫代羰基、硅烷基或-nr
b
r
c
等基团,其中r
b
与r
c
独立选自包括h、羟基、氨基、羰基、烷基、烷氧基、环烷基、杂环基、芳基、杂芳基、磺酰基、三氟甲磺酰基,作为选择,r
b
与r
c
可形成五或六元环烷基或杂环基。r
a
与r
d
各自独立选自芳基、杂芳基、烷基、烷氧基、环烷基、杂环基、羰基、酯基、桥环基、螺环基或并环基。本文中出现的杂环基,其定义与本定义一致。
[0213]“并环”是指系统中的每个环与体系中的其他环共享毗邻的一对碳原子的多环基团,其中一个或多个环可以含有0个或多个双键,且可以是取代的或未取代,并环体系中的各个环可以含0至5个选自n、s(=o)
n
或o的杂原子。优选为5至20元,进一步优选为5至14元,更有选5至12元,再进一步优选5至10元。非限定性实例包括:
[0214][0215]
当被取代时,取代基可以为1至5个选自f、cl、br、i、烷基、环烷基、烷氧基、卤代烷基、硫醇、羟基、硝基、巯基、氨基、氰基、异氰基、芳基、杂芳基、杂环基、桥环基、螺环基、并环基、羟基烷基、=o、羰基、醛、羧酸、甲酸酯、-(ch2)
m-c(=o)-r
a
、-o-(ch2)
m-c(=o)-r
a
、-(ch2)
m-c(=o)-nr
b
r
c
、-(ch2)
m
s(=o)
n
r
a
、-(ch2)
m-烯基-r
a
、or
d
或-(ch2)
m-炔基-r
a
(其中m、n为0、1或2)、芳基硫基、硫代羰基、硅烷基或-nr
b
r
c
等基团,其中r
b
与r
c
独立选自包括h、羟基、氨基、羰基、
烷基、烷氧基、环烷基、杂环基、芳基、杂芳基、磺酰基、三氟甲磺酰基,作为选择,r
b
与r
c
可形成五或六元环烷基或杂环基。r
a
与r
d
各自独立选自芳基、杂芳基、烷基、烷氧基、环烷基、杂环基、羰基、酯基、桥环基、螺环基或并环基。本文中出现的杂环基,其定义与本定义一致。
[0216]“桥环”是指任意两个不直接连接的碳原子的多环基团,可以含有0个或多个双键,且可以是取代的或未取代的,并环体系中的任意环可以含0至5个选自n、s(=o)
n
或o杂原子或基团(其中n为1、1、2)。环原子包含5至20个原子,优选为5至14个原子,进一步优选5至12个,在进一步优选5至10个。非限定性实例包括个,在进一步优选5至10个。非限定性实例包括和金刚烷。当被取代时,取代基可以为1至5个选自f、cl、br、i、烷基、环烷基、烷氧基、卤代烷基、硫醇、羟基、硝基、巯基、氨基、氰基、异氰基、芳基、杂芳基、杂环基、桥环基、螺环基、并环基、羟基烷基、=o、羰基、醛、羧酸、甲酸酯、-(ch2)
m-c(=o)-r
a
、-o-(ch2)
m-c(=o)-r
a
、-(ch2)
m-c(=o)-nr
b
r
c
、-(ch2)
m
s(=o)
n
r
a
、-(ch2)
m-烯基-r
a
、or
d
或-(ch2)
m-炔基-r
a
(其中m、n为0、1或2)、芳基硫基、硫代羰基、硅烷基或-nr
b
r
c
等基团,其中r
b
与r
c
独立选自包括h、羟基、氨基、羰基、烷基、烷氧基、环烷基、杂环基、芳基、杂芳基、磺酰基、三氟甲磺酰基,作为选择,r
b
与r
c
可形成五或六元环烷基或杂环基。r
a
与r
d
各自独立选自芳基、杂芳基、烷基、烷氧基、环烷基、杂环基、羰基、酯基、桥环基、螺环基或并环基。本文中出现的杂环基,其定义与本定义一致。
[0217]“杂单环”是指单环体系的“杂环基”或“杂环”,本文中出现的杂环基,其定义与本定义一致。
[0218]“杂并环”是指含有杂原子的“并环”。本文中出现的杂环基,其定义与本定义一致。
[0219]“杂螺环”是指含有杂原子的“螺环”。本文中出现的杂环基,其定义与本定义一致。
[0220]“杂桥环”是指含有杂原子的“桥环”。本文中出现的杂环基,其定义与本定义一致。
[0221]“杂芳基”或“杂芳环”是指取代或未取代的5至14元芳香环,且含有1至5个选自n、o或s(=o)
n
杂原子或基团,优选5至10元杂芳香环,进一步优选5至6元。杂芳基的非限制性实施例包括但不限于吡啶基、呋喃基、噻吩基、吡啶基、吡喃基、n-烷基吡咯基、嘧啶基、吡嗪基、哒嗪基、咪唑基、哌啶基、吗啉、硫代吗啉、1,3-二噻烷、苯并咪唑、哌叮基、苯并咪唑、苯并吡啶、吡咯并吡啶等。所述杂芳基环可以稠合于芳基、杂环基或环烷基环上,其中与母体结构连接在一起的环为杂芳基环,非限制性实施例包含
[0222]
当被取代时,取代基可以为1至5个选自f、cl、br、i、烷基、环烷基、烷氧基、卤代烷
基、硫醇、羟基、硝基、巯基、氨基、氰基、异氰基、芳基、杂芳基、杂环基、桥环基、螺环基、并环基、羟基烷基、=o、羰基、醛、羧酸、甲酸酯、-(ch2)
m-c(=o)-r
a
、-o-(ch2)
m-c(=o)-r
a
、-(ch2)
m-c(=o)-nr
b
r
c
、-(ch2)
m
s(=o)
n
r
a
、-(ch2)
m-烯基-r
a
、or
d
或-(ch2)
m-炔基-r
a
(其中m、n为0、1或2)、芳基硫基、硫代羰基、硅烷基或-nr
b
r
c
等基团,其中r
b
与r
c
独立选自包括h、羟基、氨基、羰基、烷基、烷氧基、环烷基、杂环基、芳基、杂芳基、磺酰基、三氟甲磺酰基,作为选择,r
b
与r
c
可形成五或六元环烷基或杂环基。r
a
与r
d
各自独立选自芳基、杂芳基、烷基、烷氧基、环烷基、杂环基、羰基、酯基、桥环基、螺环基或并环基。本文中出现的杂环基,其定义与本定义一致。
[0223]“任选”或“任选地”是指随后所描述的事件或环境可以但不必须发生,该说明包括该事件或环境发生或不发生的场合。如:“任选被f取代的烷基”指烷基可以但不必须被f取代,说明包括烷基被f取代的情形和烷基不被f取代的情形。
[0224]“药学上可接受的盐”或者“其药学上可接受的盐”是指本发明化合物保持游离酸或者游离碱的生物有效性和特性,且所述的游离酸通过与无毒的无机碱或者有机碱,所述的游离碱通过与无毒的无机酸或者有机酸反应获得的盐。
[0225]“药物组合物”是指一种或多种本发明所述化合物、其药学上可接受的盐或前药和其它化学组分形成的混合物,其中,“其它化学组分”是指药学上可接受的载体、赋形剂和/或一种或多种其它治疗剂。
[0226]“载体”是指不会对生物体产生明显刺激且不会消除所给予化合物的生物活性和特性的材料。
[0227]“赋形剂”是指加入到药物组合物中以促进化合物给药的惰性物质。非限制性实施例包括碳酸钙、磷酸钙、糖、淀粉、纤维素衍生物(包括微晶纤维素)、明胶、植物油、聚乙二醇类、稀释剂、成粒剂、润滑剂、粘合剂和崩解剂。
[0228]“前药”是指可经体内代谢转化为具有生物活性的本发明化合物。本发明的前药通过修饰本发明化合物中的氨基或者羧基来制备,该修饰可以通过常规的操作或者在体内被除去,而得到母体化合物。当本发明的前药被施予哺乳动物个体时,前药被割裂形成游离的氨基或者羧基。
[0229]“共晶”是指活性药物成分(api)和共晶形成物(ccf)在氢键或其他非共价键的作用下结合而成的晶体,其中api和ccf的纯态在室温下均为固体,并且各组分间存在固定的化学计量比。共晶是一种多组分晶体,既包含两种中性固体之间形成的二元共晶,也包含中性固体与盐或溶剂化物形成的多元共晶。
[0230]“动物”是指包括哺乳动物,例如人、陪伴动物、动物园动物和家畜,优选人、马或者犬。
[0231]“立体异构体”是指由分子中原子在空间上排列方式不同所产生的异构体,包括顺反异构体、对映异构体和构象异构体。
[0232]“任选”或“任选地”或“选择性的”或“选择性地”是指随后所述的事件或状况可以但未必发生,该描述包括其中发生该事件或状况的情况及其中未发生的情况。例如,“选择性地被烷基取代的杂环基”是指该烷基可以但未必存在,该描述包括其中杂环基被烷基取代的情况,及其中杂环基未被烷基取代的情况。
[0233]
ic
50
(被测量的抑制剂的半抑制浓度):通过测试受试化合物50%抑制gabapentin
与钙离子通道结合所需的浓度。
具体实施方式
[0234]
以下实施例详细说明本发明的技术方案,但本发明的保护范围包括但是不限于此。
[0235]
本文所述反应中使用的化合物是根据本领域技术人员已知的有机合成技术制备的,起始于市售化学品和(或)化学文献中所述的化合物。“市售化学品”是从正规商业来源获得的,供应商包括:泰坦科技、安耐吉化学、上海德默、成都科龙化工、韶远化学科技、南京药石、药明康德和百灵威科技等公司。
[0236]
本领域的参考书和专著,详细介绍了可用于制备本文所述化合物的反应物的合成,或提供了描述该制备方法的文章以供参考。这些参考书和专著包括:“synthetic organic chemistry”,john wiley&sons,inc.,new york;s.r.sandler et al.,“organic functional group preparations,”2nd ed.,academic press,new york,1983;h.o.house,“modern synthetic reactions”,2nd ed.,w.a.benjamin,inc.menlo park,calif.1972;t.l.gilchrist,“heterocyclic chemistry”,2nd ed.,john wiley&sons,new york,1992;j.march,“advanced organic chemistry:reactions,mechanisms and structure”,4th ed.,wiley-interscience,new york,1992;fuhrhop,j.and penzlin g.“organic synthesis:concepts,methods,starting materials”,second,revised and enlarged edition(1994)john wiley&sons isbn:3-527-29074-5;hoffman,r.v.“organic chemistry,an intermediate text”(1996)oxford university press,isbn 0-19-509618-5;larock,r.c.“comprehensive organic transformations:a guide to functional group preparations”2nd edition(1999)wiley-vch,isbn:0-471-19031-4;march,j.“advanced organic chemistry:reactions,mechanisms,and structure”4th edition(1992)john wiley&sons,isbn:0-471-60180-2;otera,j.(editor)“modern carbonyl chemistry”(2000)wiley-vch,isbn:3-527-29871-1;patai,s.“patai’s 1992guide to the chemistry of functional groups”(1992)interscience isbn:0-471-93022-9;solomons,t.w.g.“organic chemistry”7th edition(2000)john wiley&sons,isbn:0-471-19095-0;stowell,j.c.,“intermediate organic chemistry”2nd edition(1993)wiley-interscience,isbn:0-471-57456-2;“industrial organic chemicals:starting materials and intermediates:an ullmann’s encyclopedia”(1999)john wiley&sons,isbn:3-527-29645-x,in 8volumes;“organic reactions”(1942-2000)john wiley&sons,in over 55volumes;and“chemistry of functional groups”john wiley&sons,in 73volumes.
[0237]
通过美国化学会化学文摘社制备的已知化学物质的索引,可以选择性地识别特定和类似的反应物,这些索引可在大多数公共图书馆和大学图书馆以及在线获得。已知但在目录中不可商购的化学品可选地由定制化学合成工厂制备,其中许多标准化学供应工厂(例如,上面列出的那些)提供定制合成服务。制备和选择本文所述化合物的药用盐的参考文献是p.h.stahl&c.g.wermuth“handbook of pharmaceutical salts”,verlag helvetica chimica acta,zurich,2002.
[0238]
化合物的结构是通过核磁共振(nmr)或(和)质谱(ms)来确定的。nmr位移(δ)以10-6
(ppm)的单位给出。nmr的测定是用(bruker avance iii 400和bruker avance 300)核磁仪,测定溶剂为氘代二甲基亚砜(dmso-d6),氘代氯仿(cdcl3),氘代甲醇(cd3od),内标为四甲基硅烷(tms);
[0239]
ms的测定用(agilent 6120b(esi)和agilent 6120b(apci));
[0240]
hplc的测定使用agilent 1260dad高压液相色谱仪(zorbax sb-c18 100
×
4.6mm,3.5μm);
[0241]
薄层层析硅胶板使用烟台黄海hsgf254或青岛gf254硅胶板,薄层色谱法(tlc)使用的硅胶板采用的规格是0.15mm-0.20mm,薄层层析分离纯化产品采用的规格是0.4mm-0.5mm;
[0242]
柱层析一般使用烟台黄海硅胶200-300目硅胶为载体;
[0243]
dmso:二甲基亚砜;dipea:n,n'-二异丙基乙胺;ph:苯基;dcm:二氯甲烷;boc:叔丁基氧基羰基;
[0244]
中间体1:(2-氯-4-苯氧基苯基)(4-(哌啶-4-基氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(中间体1)
[0245]
(2-chloro-4-phenoxyphenyl)(4-(piperidin-4-ylamino)-7h-pyrrolo[2,3-d]pyrimidin-5-yl)methanone
[0246][0247]
第一步:2-氯-4-苯氧基苯甲酸甲酯(1b)
[0248]
methyl 2-chloro-4-phenoxybenzoate
[0249][0250]
向2-氯-4-氟苯甲酸甲酯(1a)(7.5g,40mmol)中加入100ml dmf,分别加入苯酚(4.5g,48mmol)和碳酸铯(20g,61mmol),加热至90℃反应3h。将反应液冷却至室温,向反应液中加入400ml乙酸乙酯,用400ml水洗涤,有机相用无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(石油醚/乙酸乙酯(v/v)=4:1),得2-氯-4-苯氧基苯甲酸甲酯(1b)(7.5g,收率:72%)。
[0251]
lcms m/z=263.1[m+1]
+
[0252]
第二步:(2-氯-4-苯氧基苯基)(4-氯-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(1c)
[0253]
(2-chloro-4-phenoxyphenyl)(4-chloro-7h-pyrrolo[2,3-d]pyrimidin-5-yl)methanone
[0254][0255]
在氮气氛围下向2-氯-4-苯氧基苯甲酸甲酯(1b)(4.5g,17mmol)中加入100ml无水四氢呋喃中,冷却至-70℃,缓慢滴加2.5mol/l正丁基锂的正己烷溶液(12ml,30mmol),滴加过程中保持反应体系温度低于-60℃,继续在此温度下搅拌1h。然后,将5-溴-4-氯-7h-吡咯并[2,3-d]嘧啶(3.2g,14mmol)的50ml四氢呋喃溶液缓慢滴加入上述反应体系中,滴加过程中保持体系温度低于-60℃,反应1h。反应完成后,在-60℃下缓慢滴加2n盐酸至反应液ph值为5,将反应液升至室温搅拌10分钟,将混合液直接浓缩至油状物,向该粗品中加入200ml乙酸乙酯,用300ml水洗涤,有机相用无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(石油醚/乙酸乙酯(v/v)=10:1),得(2-氯-4-苯氧基苯基)(4-氯-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(1c)(1.6g,收率:30%)。
[0256]1h nmr(400mhz,dmso-d6)δ13.41(s,1h),8.74(s,1h),8.12(s,1h),7.59(d,1h),7.53
–
7.44(m,2h),7.26(t,1h),7.22
–
7.14(m,3h),7.02(dd,1h).
[0257]
lcms m/z=384.1[m+1]
+
[0258]
第三步:4-[[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]哌啶-1-甲酸叔丁酯(1d)
[0259]
tert-butyl4-[[5-(2-chloro-4-phenoxy-benzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl]amino]piperidine-1-carboxylate
[0260][0261]
在高压反应釜中将(2-氯-4-苯氧基苯基)(4-氯-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(1c)(0.6g,1.56mmol)溶于15ml异丙醇中,加入1.5ml dipea和4-氨基哌啶-1-甲酸叔丁酯(310mg,1.55mmol),反应于130℃搅拌5小时。将反应液冷却至室温,加入50ml水,用100ml乙酸乙酯萃取,有机相用100ml水洗涤,无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=15:1),得4-[[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]哌啶-1-甲酸叔丁酯(1d)(0.72g,收率:85.0%)。
[0262]1h nmr(400mhz,dmso-d6)δ12.71(s,1h),8.81(d,1h),8.25(s,1h),7.62(s,1h),7.58(d,1h),7.52
–
7.44(m,2h),7.29
–
7.22(m,1h),7.21
–
7.15(m,3h),7.02(dd,1h),4.45
–
4.21(m,1h),3.89
–
3.78(m,2h),3.20
–
2.98(m,2h),2.08
–
1.97(m,2h),1.51
–
1.35(m,11h).
[0263]
第四步:(2-氯-4-苯氧基苯基)(4-(哌啶-4-基氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(中间体1)
[0264]
(2-chloro-4-phenoxyphenyl)(4-(piperidin-4-ylamino)-7h-pyrrolo[2,3-d]pyrimidin-5-yl)methanone
[0265][0266]
将4-[[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]哌啶-1-甲酸叔丁酯(1d)(720mg,1.31mmol)溶解到20ml dcm中,加入5ml三氟乙酸,室温搅拌4h。反应完后将体系直接旋干,再加入100ml饱和碳酸氢钠水溶液,用50ml二氯甲烷萃取三次,有机相用无水硫酸钠干燥,减压浓缩,得到粗品(2-氯-4-苯氧基苯基)(4-(哌啶-4-基氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(中间体1)(528mg)。
[0267]
lcms m/z=448.1[m+1]
+
[0268]
中间体2:5-氨基-3-(4-(2,4-二氟苯氧基)苯基)-1-(哌啶-4-基)-1h-吡唑-4-甲酰胺(中间体2)
[0269]
5-amino-3-(4-(2,4-difluorophenoxy)phenyl)-1-(piperidin-4-yl)-1h-pyrazole-4-carboxamide
[0270][0271]
第一步:4-(2-(叔丁氧基羰基)肼基)哌啶-1-甲酸苄酯(2b)
[0272]
benzyl 4-(2-(tert-butoxycarbonyl)hydrazinyl)piperidine-1-carboxylate
[0273][0274]
将4-氧代哌啶-1-甲酸苄酯(2a)(35g,0.15mol)和肼甲酸叔丁酯(20g,0.15mol)加入300ml四氢呋喃中,回流反应3h。将反应液冷却至室温,加入氰基硼氢化钠(10g,
0.16mol),继续搅拌5min,将一水合对甲基苯磺酸(29g,0.152mol)的100ml四氢呋喃缓慢加入上述反应液中,常温反应16h。将反应液浓缩至油状物,加入1000ml乙酸乙酯稀释反应液,用1000ml饱和碳酸氢钠溶液洗涤,有机相用无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(石油醚/乙酸乙酯(v/v)=2:1),得4-(2-(叔丁氧基羰基)肼基)哌啶-1-甲酸苄酯(2b)(33g,收率:63%)。
[0275]
lcms m/z=350.1[m+1]
+
[0276]
第二步:4-肼基哌啶-1-甲酸苄酯盐酸盐(2c)
[0277]
benzyl 4-hydrazinylpiperidine-1-carboxylate hydrochloride
[0278][0279]
将4-(2-(叔丁氧基羰基)肼基)哌啶-1-甲酸苄酯(2b)(33g,0.094mol)加入反应瓶中,加入200ml甲醇溶解,分批加入200ml 4n盐酸1,4-二氧六环溶液,常温反应16h。将反应液减压浓缩,得4-肼基哌啶-1-甲酸苄酯盐酸盐(2c)(20g)。
[0280]
lcms m/z=250.2[m+1]
+
[0281]
第三步:4-[5-氨基-4-氰基-3-[4-(2,4-二氟苯氧基)苯基]吡唑-1-基]哌啶-1-甲酸苄酯(2d)
[0282]
benzyl4-[5-amino-4-cyano-3-[4-(2,4-difluorophenoxy)phenyl]pyrazol-1-yl]piperidine-1-carboxylate
[0283][0284]
将2-((4-(2,4-二氟苯氧基)苯基)(甲氧基)亚甲基)丙二腈(合成方法见wo2014068527)(4.2g,13.5mmol)溶于50ml乙醇中,依次加入4-肼基哌啶-1-甲酸苄酯盐酸盐(2c)(3.7g)、dipea(2.6g,20mmol),室温搅拌16h。向反应液中缓慢加入20ml饱和氯化钠溶液,用100ml乙酸乙酯萃取两次,有机相用50ml饱和氯化钠洗涤,无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=20:1),得4-[5-氨基-4-氰基-3-[4-(2,4-二氟苯氧基)苯基]吡唑-1-基]哌啶-1-甲酸苄酯(2d)(5.0g,从化合物2b算两步总收率:54%)。
[0285]
lcms m/z=530.3[m+1]
+
[0286]
第四步:5-氨基-3-(4-(2,4-二氟苯氧基)苯基)-1-(哌啶-4-基)-1h-吡唑-4-甲酰胺(中间体2)
[0287]
5-amino-3-(4-(2,4-difluorophenoxy)phenyl)-1-(piperidin-4-yl)-1h-pyrazole-4-carboxamide
[0288][0289]
将4-[5-氨基-4-氰基-3-[4-(2,4-二氟苯氧基)苯基]吡唑-1-基]哌啶-1-甲酸苄酯(2d)(5.0g,9.43mmol)溶解在100ml乙醇中,加入100ml 4n氢氧化钠溶液,140℃搅拌回流24h。将反应液冷却至室温,减压浓缩,加入50ml水,用乙酸乙酯萃取(200mlx3),合并有机层,无水硫酸钠干燥,减压浓缩,得粗品5-氨基-3-(4-(2,4-二氟苯氧基)苯基)-1-(哌啶-4-基)-1h-吡唑-4-甲酰胺(中间体2)(2.6g)。
[0290]
lcms m/z=414.3[m+1]
+
[0291]
中间体3:5-氨基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-1-(哌啶-4-基)-1h-吡唑-4-甲酰胺(中间体3)
[0292]
5-amino-3-(4-((5-chloropyridin-2-yl)oxy)phenyl)-1-(piperidin-4-yl)-1h-pyrazole-4-carboxamide
[0293][0294]
第一步:4-(5-氨基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-4-氰基-1h-吡唑-1-基)哌啶-1-甲酸苄酯(3b)
[0295]
benzyl 4-(5-amino-3-(4-((5-chloropyridin-2-yl)oxy)phenyl)-4-cyano-1h-pyrazol-1-yl)piperidine-1-carboxylate
[0296]
[0297]
将2-((4-((5-氯吡啶-2-基)氧基)苯基)(乙氧基)亚甲基)丙二腈(3a)(合成方法见wo2019091441)(2.0g,6.15mmol)溶于30ml二氯甲烷中,室温下依次加入三乙胺(2.0ml)和4-肼基哌啶-1-甲酸苄酯盐酸盐(2c)(1.3g),室温搅拌6h。向反应液中加入150ml水,用二氯甲烷萃取(50ml
×
3),合并有机相,有机相用饱和食盐水洗涤(50ml
×
2),无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=20:1-10:1),得到4-(5-氨基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-4-氰基-1h-吡唑-1-基)哌啶-1-甲酸苄酯(3b)(1.8g,从化合物2b算两步总收率:56%)。
[0298]
lcms m/z=529.2[m+1]
+
[0299]
第二步:5-氨基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-1-(哌啶-4-基)-1h-吡唑-4-甲酰胺(中间体3)
[0300]
5-amino-3-(4-((5-chloropyridin-2-yl)oxy)phenyl)-1-(piperidin-4-yl)-1h-pyrazole-4-carboxamide
[0301][0302]
将4-(5-氨基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-4-氰基-1h-吡唑-1-基)哌啶-1-甲酸苄酯(3b)(1.8g,3.41mmol)溶于50ml质量分数为90%浓硫酸中,室温反应1h,升温至60℃搅拌2h。将反应液冷却至室温,将反应液缓慢倒入冰水中(300ml),用质量分数为28%氨水调ph至10,水相用二氯甲烷萃取(100ml
×
6),合并有机相,无水硫酸钠干燥,减压浓缩,得到粗品5-氨基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-1-(哌啶-4-基)-1h-吡唑-4-甲酰胺(中间体3)(1.1g)。
[0303]
lcms m/z=413.2[m+1]
+
[0304]
实施例1:
[0305]
5-[3-[3-[4-[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]-1-哌啶基]氮杂环丁-1-基]氮杂环丁-1-基]-2-(2,6-二氧代-3-哌啶基)异吲哚啉-1,3-二酮(化合物1)的三氟乙酸盐
[0306]
5-[3-[3-[4-[[5-(2-chloro-4-phenoxy-benzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl]amino]-1-piperidyl]azetidin-1-yl]azetidin-1-yl]-2-(2,6-dioxo-3-piperidyl)isoindoline-1,3-dione trifluoroacetate
5-yl]-(2-chloro-4-phenoxy-phenyl)methanone trifluoroacetate
[0315][0316]
将3-[4-[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]-1-哌啶基]氮杂环丁-1-甲酸叔丁酯(1a)(300mg,0.50mmol)溶解到20ml dcm中,加入8ml三氟乙酸,室温搅拌4小时。反应完后将体系直接旋干,即得粗品[4-[[1-(氮杂环丁-3-基)-4-哌啶基]氨基]-7h-吡咯并[2,3-d]嘧啶-5-基]-(2-氯-4-苯氧基-苯基)甲酮(1b)的三氟乙酸盐(450mg)。
[0317]
lcms m/z=503.2[m+1]
+
[0318]
第三步:3-[3-[4-[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]-1-哌啶基]氮杂环丁-1-基]氮杂环丁-1-甲酸叔丁酯(1c)
[0319]
tert-butyl 3-[3-[4-[[5-(2-chloro-4-phenoxy-benzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl]amino]-1-piperidyl]azetidin-1-yl]azetidine-1-carboxylate
[0320][0321]
将上述粗品[4-[[1-(氮杂环丁-3-基)-4-哌啶基]氨基]-7h-吡咯并[2,3-d]嘧啶-5-基]-(2-氯-4-苯氧基-苯基)甲酮(1b)的三氟乙酸盐(450mg)溶于30ml 1,2-二氯乙烷中,加入3-氧代氮杂环丁-1-甲酸叔丁酯(160mg,0.94mmol),室温搅拌10分钟后,加入三乙酰氧基硼氢化钠(400mg,1.89mmol),室温搅拌16h。向反应体系中缓慢加入30ml饱和碳酸氢钠溶液,用30ml dcm萃取三次,有机相用50ml水洗涤,无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=20:1),得3-[3-[4-[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]-1-哌啶基]氮杂环丁-1-基]氮杂环丁-1-甲酸叔丁酯(1c)(240mg,从化合物1a算两步总收率:73%)。
[0322]
lcms m/z=658.3[m+1]
+
[0323]
第四步:[4-[[1-[1-(氮杂环丁-3-基)氮杂环丁-3-基]-4-哌啶基]氨基]-7h-吡咯并[2,3-d]嘧啶-5-基]-(2-氯-4-苯氧基-苯基)甲酮(1d)的三氟乙酸盐
[0324]
[4-[[1-[1-(azetidin-3-yl)azetidin-3-yl]-4-piperidyl]amino]-7h-pyrrolo[2,3-d]pyrimidin-5-yl]-(2-chloro-4-phenoxy-phenyl)methanone trifluoroacetate
[0325][0326]
将3-[3-[4-[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]-1-哌啶基]氮杂环丁-1-基]氮杂环丁-1-甲酸叔丁酯(1c)(236mg,0.36mmol)溶解在20ml dcm中,加入8ml三氟乙酸,室温搅拌4小时。将反应体系直接旋干,即得粗品[4-[[1-[1-(氮杂环丁-3-基)氮杂环丁-3-基]-4-哌啶基]氨基]-7h-吡咯并[2,3-d]嘧啶-5-基]-(2-氯-4-苯氧基-苯基)甲酮(1d)的三氟乙酸盐(350mg)。
[0327]
lcms m/z=558.3[m+1]
+
[0328]
第五步:5-[3-[3-[4-[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]-1-哌啶基]氮杂环丁-1-基]氮杂环丁-1-基]-2-(2,6-二氧代-3-哌啶基)异吲哚啉-1,3-二酮(化合物1)的三氟乙酸盐
[0329]
5-[3-[3-[4-[[5-(2-chloro-4-phenoxy-benzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl]amino]-1-piperidyl]azetidin-1-yl]azetidin-1-yl]-2-(2,6-dioxo-3-piperidyl)isoindoline-1,3-dione trifluoroacetate
[0330][0331]
将上述粗品[4-[[1-[1-(氮杂环丁-3-基)氮杂环丁-3-基]-4-哌啶基]氨基]-7h-吡咯并[2,3-d]嘧啶-5-基]-(2-氯-4-苯氧基-苯基)甲酮(1d)的三氟乙酸盐(235mg)溶于15ml dmso中,加入1.5ml dipea和2-(2,6-二氧代哌啶-3-基)-5-氟异吲哚啉-1,3-二酮(合成方法见wo2017197056)(150mg,0.54mmol),反应于80℃搅拌5小时。将反应液冷却至室温,加入50ml水,用100ml乙酸乙酯萃取,有机相用100ml水洗涤,无水硫酸钠干燥,减压浓缩后粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=15:1),得5-[3-[3-[4-[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]-1-哌啶基]氮杂环丁-1-基]氮杂环丁-1-基]-2-(2,6-二氧代-3-哌啶基)异吲哚啉-1,3-二酮(化合物1)的三氟乙酸盐(97.4mg)。
[0332]1h nmr(400mhz,cdcl3)δ9.11(s,1h),8.34(s,1h),7.63(d,1h),7.46
–
7.37(m,3h),7.34(s,1h),7.25
–
7.20(m,1h),7.13
–
7.06(m,3h),6.96(dd,1h),6.77(d,1h),6.52(dd,1h),4.92(dd,1h),4.39
–
4.24(m,1h),4.08
–
3.99(m,2h),3.93
–
3.84(m,2h),3.78
–
3.67(m,1h),3.63
–
3.53(m,2h),3.34
–
3.04(m,3h),2.93
–
2.65(m,5h),2.48
–
2.06(m,5h),1.98
–
1.80(m,2h).
[0333]
lcms m/z=814.3[m+1]
+
[0334]
实施例1-1:
[0335]
5-[3-[3-[4-[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]-1-哌啶基]氮杂环丁-1-基]氮杂环丁-1-基]-2-(2,6-二氧代-3-哌啶基)异吲哚啉-1,3-二酮(化合物1)
[0336]
5-[3-[3-[4-[[5-(2-chloro-4-phenoxy-benzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl]amino]-1-piperidyl]azetidin-1-yl]azetidin-1-yl]-2-(2,6-dioxo-3-piperidyl)isoindoline-1,3-dione
[0337][0338]
将5-[3-[3-[4-[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]-1-哌啶基]氮杂环丁-1-基]氮杂环丁-1-基]-2-(2,6-二氧代-3-哌啶基)异吲哚啉-1,3-二酮(化合物1)的三氟乙酸盐(70mg)溶于10ml二氯甲烷,用质量分数为28%的浓氨水(10mlx5)洗涤,有机层用无水硫酸钠干燥,减压浓缩,得到5-[3-[3-[4-[[5-(2-氯-4-苯氧基-苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基]氨基]-1-哌啶基]氮杂环丁-1-基]氮杂环丁-1-基]-2-(2,6-二氧代-3-哌啶基)异吲哚啉-1,3-二酮(化合物1)(40mg)。
[0339]1h nmr(400mhz,cdcl3)δ9.10(s,1h),8.33(s,1h),7.63(d,1h),7.47
–
7.36(m,3h),7.33(s,1h),7.26
–
7.19(m,1h),7.14
–
7.05(m,3h),6.96(dd,1h),6.77(d,1h),6.52(dd,1h),4.92(dd,1h),4.38
–
4.20(m,1h),4.08
–
3.98(m,2h),3.93
–
3.82(m,2h),3.78
–
3.66(m,1h),3.63
–
3.52(m,2h),3.32
–
2.96(m,3h),2.93
–
2.64(m,5h),2.42
–
2.06(m,5h),1.96
–
1.80(m,2h).
[0340]
lcms m/z=814.3[m+1]
+
[0341]
实施例2:
[0342]
5-(3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-联哌啶]-1'-基)氮杂环丁-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物2)的三氟乙酸盐
[0343]
5-(3-(4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-[1,4'-bipiperidin]-1'-yl)azetidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dione trifluoroacetate
[0344]
[0345][0346]
第一步:4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-联哌啶]-1'-甲酸叔丁酯(2a)
[0347]
tert-butyl 4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-[1,4'-bipiperidine]-1'-carboxylate
[0348][0349]
将上述粗品(2-氯-4-苯氧基苯基)(4-(哌啶-4-基氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(中间体1)(300mg)溶于25ml 1,2-二氯乙烷中,加入4-氧代哌啶-1-甲酸叔丁酯(267mg,1.34mmol),室温搅拌10分钟后,加入三乙酰氧基硼氢化钠(568mg,2.68mmol),室温搅拌16h。向反应液中缓慢加入30ml饱和碳酸氢钠溶液,用30ml dcm萃取三次,有机相用50ml水洗涤,无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=20:1),得4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-联哌啶]-1'-甲酸叔丁酯(2a)(310mg,从化合物1d算两步总收率:66%)。
[0350]
lcms m/z=631.3[m+1]
+
[0351]
第二步:(4-([1,4'-联哌啶]-4-基氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(2b)的三氟乙酸盐
[0352]
(4-([1,4'-bipiperidin]-4-ylamino)-7h-pyrrolo[2,3-d]pyrimidin-5-yl)(2-chloro-4-phenoxyphenyl)methanone trifluoroacetate
[0353][0354]
将4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-联哌啶]-1'-甲酸叔丁酯(2a)(300mg,0.48mmol)溶解到20ml dcm中,加入8ml三氟乙酸,室温搅拌4小时。反应完后将体系直接旋干,即得粗品(4-([1,4'-联哌啶]-4-基氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(2b)的三氟乙酸盐(450mg)。
[0355]
lcms m/z=531.3[m+1]
+
[0356]
第三步:3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-联哌啶]-1'-基)氮杂环丁-1-甲酸叔丁酯(2c)
[0357]
tert-butyl 3-(4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-[1,4'-bipiperidin]-1'-yl)azetidine-1-carboxylate
[0358][0359]
将上述粗品(4-([1,4'-联哌啶]-4-基氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(2b)的三氟乙酸盐(430mg)溶于30ml 1,2-二氯乙烷中,加入3-氧代氮杂环丁-1-甲酸叔丁酯(160mg,0.93mmol),室温搅拌10分钟后,加入三乙酰氧基硼氢化钠(400mg,1.89mmol),室温搅拌16h。向反应体系中缓慢加入30ml饱和碳酸氢钠溶液,用30ml dcm萃取三次,有机相用50ml水洗涤,无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=20:1),得3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-联哌啶]-1'-基)氮杂环丁-1-甲酸叔丁酯(2c)(250mg,从化合物2a算两步总收率:80%)。
[0360]
lcms m/z=686.3[m+1]
+
[0361]
第四步:(4-(((1'-(氮杂环丁-3-基)-[1,4'-双哌啶]-4-基]氨基]-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(2d)的三氟乙酸盐
[0362]
(4-((1'-(azetidin-3-yl)-[1,4'-bipiperidin]-4-yl)amino)-7h-pyrrolo[2,3-d]pyrimidin-5-yl)(2-chloro-4-phenoxyphenyl)methanone trifluoroacetate
[0363][0364]
将3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-联哌啶]-1'-基)氮杂环丁-1-甲酸叔丁酯(2c)(250mg,0.36mmol)溶解在20ml dcm中,加入8ml三氟乙酸,室温搅拌4小时。将反应体系直接旋干,即得粗品(4-(((1'-(氮杂环丁-3-基)-[1,4'-双哌啶]-4-基]氨基]-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(2d)的三氟乙酸盐(350mg)。
[0365]
lcms m/z=586.3[m+1]
+
[0366]
第五步:5-(3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-联哌啶]-1'-基)氮杂环丁-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物2)的三氟乙酸盐
[0367]
5-(3-(4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-[1,4'-bipiperidin]-1'-yl)azetidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dione trifluoroacetate
[0368][0369]
将(4-(((1'-(氮杂环丁-3-基)-[1,4'-双哌啶]-4-基]氨基]-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(2d)的三氟乙酸盐(350mg)溶于15ml dmso中,加入1.5ml dipea和2-(2,6-二氧代哌啶-3-基)-5-氟异吲哚啉-1,3-二酮(合成方法见wo2017197056)(150mg,0.54mmol),反应于80℃搅拌5小时。将反应液冷却至室温,加入50ml水,用100ml乙酸乙酯萃取,有机相用100ml水洗涤,无水硫酸钠干燥,减压浓缩后粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=15:1),得5-(3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-联哌啶]-1'-基)氮杂环丁-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物2)的三氟乙酸盐(120mg)。
[0370]1h nmr(400mhz,cdcl3)δ9.09(s,1h),8.33(s,1h),7.63(d,1h),7.46
–
7.37(m,3h),7.32(s,1h),7.25
–
7.19(m,1h),7.13
–
7.05(m,3h),6.96(dd,1h),6.78(d,1h),6.51(dd,1h),4.92(dd,1h),4.35
–
4.17(m,1h),4.12
–
4.05(m,2h),3.92
–
3.82(m,2h),3.40
–
3.29(m,1h),3.09
–
2.39(m,10h),2.32
–
2.07(m,3h),2.01
–
1.77(m,6h),1.77
–
1.57(m,2h).
[0371]
lcms m/z=842.3[m+1]
+
[0372]
实施例3:
[0373]
5-氨基-3-[4-(2,4-二氟苯氧基)苯基]-1-[1-[1-[1-[2-(2,6-二氧代-3-哌啶基)-1,3-二氧代]-异吲哚啉-5-基]氮杂环丁-3-基]氮杂环丁-3-基]-4-哌啶基]吡唑-4-甲酰胺(化合物3)
[0374]
5-amino-3-[4-(2,4-difluorophenoxy)phenyl]-1-[1-[1-[1-[2-(2,6-dioxo-3-piperidyl)-1,3-dioxo-isoindolin-5-yl]azetidin-3-yl]azetidin-3-yl]-4-piperidyl]pyrazole-4-carboxamide
[0375][0376]
第一步:3-[4-[5-氨基-4-氨基甲酰基]-3-[4-(2,4-二氟苯氧基)苯基]吡唑-1-基]-1-哌啶基]氮杂环丁-1-甲酸叔丁酯(3a)
[0377]
tert-butyl 3-[4-[5-amino-4-carbamoyl-3-[4-(2,4-difluorophenoxy)phenyl]pyrazol-1-yl]-1-piperidyl]azetidine-1-carboxylate
[0378][0379]
将上述粗品5-氨基-3-(4-(2,4-二氟苯氧基)苯基)-1-(哌啶-4-基)-1h-吡唑-4-甲酰胺(中间体2)(400mg)溶于15ml dmf中,依次加入3-氧代氮杂环丁-1-甲酸叔丁酯(497mg,2.90mmol)、0.5ml乙酸以及2g无水硫酸镁,升温至70℃搅拌3小时后,将反应液冷却至室温,加入氰基硼氢化钠(304mg,4.84mmol),室温搅拌16h。向反应液中缓慢加入20ml饱和碳酸氢钠溶液,用60ml乙酸乙酯萃取两次,有机相用50ml饱和氯化钠洗涤,无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=20:1),得3-[4-[5-氨基-4-氨基甲酰基]-3-[4-(2,4-二氟苯氧基)苯基]吡唑-1-基]-1-哌啶基]氮杂环丁-1-甲酸叔丁酯(3a)(250mg,从化合物2d算两步总收率:30%)。
[0380]
lcms m/z=569.3[m+1]
+
[0381]
第二步:5-氨基-1-[1-(氮杂环丁-3-基)-4-哌啶基]-3-[4-(2,4-二氟苯氧基)苯基]吡唑-4-甲酰胺(3b)
[0382]
5-amino-1-[1-(azetidin-3-yl)-4-piperidyl]-3-[4-(2,4-difluorophenoxy)phenyl]pyrazole-4-carboxamide
[0383][0384]
将3-[4-[5-氨基-4-氨基甲酰基]-3-[4-(2,4-二氟苯氧基)苯基]吡唑-1-基]-1-哌啶基]氮杂环丁-1-甲酸叔丁酯(3a)(150mg,0.26mmol)溶解到5ml dcm中,加入2ml三氟乙酸,室温搅拌4小时。反应完后将体系直接旋干,再用50ml dcm溶解,用饱和碳酸氢钠溶液调ph至10,用50ml二氯甲烷萃取三次,无水硫酸钠干燥,减压浓缩,即得粗品5-氨基-1-[1-(氮杂环丁-3-基)-4-哌啶基]-3-[4-(2,4-二氟苯氧基)苯基]吡唑-4-甲酰胺(3b)(110mg)。
[0385]
lcms m/z=469.3[m+1]
+
[0386]
第三步:3-[3-[4-[5-氨基-4-氨基甲酰基]-3-[4-(2,4-二氟苯氧基)苯基]吡唑-1-基]-1-哌啶基]氮杂环丁-1-基]氮杂环丁-1-甲酸叔丁酯(3c)
[0387]
tert-butyl 3-[3-[4-[5-amino-4-carbamoyl-3-[4-(2,4-difluorophenoxy)phenyl]pyrazol-1-yl]-1-piperidyl]azetidin-1-yl]azetidine-1-carboxylate
[0388][0389]
将上述粗品5-氨基-1-[1-(氮杂环丁-3-基)-4-哌啶基]-3-[4-(2,4-二氟苯氧基)苯基]吡唑-4-甲酰胺(3b)(110mg)溶于10ml 1,2-二氯乙烷中,加入3-氧代氮杂环丁-1-甲酸叔丁酯(80mg,0.47mmol),室温搅拌60分钟后,加入三乙酰氧基硼氢化钠(249mg,1.17mmol),室温搅拌16h。向反应体系中缓慢加入30ml饱和碳酸氢钠溶液,用30ml dcm萃取三次,有机相用50ml水洗涤,无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=20:1),得3-[3-[4-[5-氨基-4-氨基甲酰基]-3-[4-(2,4-二氟苯氧基)苯基]吡唑-1-基]-1-哌啶基]氮杂环丁-1-基]氮杂环丁-1-甲酸叔丁酯(3c)(100mg,从化合物3a算两步总收率:62%)。
[0390]
lcms m/z=624.3[m+1]
+
[0391]
第四步:5-氨基-1-[1-[1-[1-(氮杂环丁-3-基)氮杂环丁-3-基]-4-哌啶基]-3-[4-(2,4-二氟苯氧基)苯基]吡唑-4-甲酰胺(3d)
[0392]
5-amino-1-[1-[1-(azetidin-3-yl)azetidin-3-yl]-4-piperidyl]-3-[4-(2,4-difluorophenoxy)phenyl]pyrazole-4-carboxamide
基)-1,3-二氧代异吲哚啉-5-基)-[1,4'-联哌啶]-4-基)-1h-吡唑-4-甲酰胺(化合物4)
[0404]
5-amino-3-(4-((5-chloropyridin-2-yl)oxy)phenyl)-1-(1'-(2-(2,6-dioxopiperidin-3-yl)-1,3-dioxoisoindolin-5-yl)-[1,4'-bipiperidin]-4-yl)-1h-pyrazole-4-carboxamide
[0405][0406][0407]
第一步:4-(5-氨基-4-氨基甲酰基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-1h-吡唑-1-基)-[1,4'-联哌啶]-1'-甲酸叔丁酯(4a)
[0408]
tert-butyl4-(5-amino-4-carbamoyl-3-(4-((5-chloropyridin-2-yl)oxy)phenyl)-1h-pyrazol-1-yl)-[1,4'-bipiperidine]-1'-carboxylate
[0409][0410]
将上述粗品5-氨基-3-(4-((5-氯吡啶-2-基)氧)苯基)-1-(哌啶-4-基)-1h-吡唑-4-甲酰胺(中间体3)(900mg)溶于30ml 1,2-二氯乙烷/dmso(v/v=10/1)中,室温下依次加入4-氧代哌啶-1-甲酸叔丁酯(1.3g,6.53mmol)、冰乙酸(0.32ml)和无水硫酸镁(1.4g),升温至70℃搅拌6h,将反应液冷却至室温,加入氰基硼氢化钠(545mg,8.67mmol),室温搅拌16h。将反应液进行抽滤,向滤液中加入50ml水,用2n氢氧化钠溶液调水相ph至10,用二氯甲烷萃取(40ml
×
3),合并有机相,有机相用水洗涤(20ml
×
2),无水硫酸钠干燥,减压浓缩,粗
品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=10:1-8:1),得到4-(5-氨基-4-氨基甲酰基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-1h-吡唑-1-基)-[1,4'-联哌啶]-1'-甲酸叔丁酯(4a)(410mg)。
[0411]
lcms m/z=596.3[m+1]
+
[0412]
第二步:1-([1,4'-联哌啶]-4-基)-5-氨基-3-(4-((5-氯吡啶基-2-基)氧基)苯基)-1h-吡唑-4-甲酰胺(4b)
[0413]
1-([1,4'-bipiperidin]-4-yl)-5-amino-3-(4-((5-chloropyridin-2-yl)oxy)phenyl)-1h-pyrazole-4-carboxamide
[0414][0415]
将4-(5-氨基-4-氨基甲酰基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-1h-吡唑-1-基)-[1,4'-联哌啶]-1'-甲酸叔丁酯(4a)(100mg,0.17mmol)溶于3ml二氯甲烷中,加入2ml三氟乙酸,室温反应2小时。反应液用2n氢氧化钠溶液调ph至10,水相用二氯甲烷萃取(10ml
×
3),合并有机相,用无水硫酸钠干燥,浓缩,得到1-([1,4'-联哌啶]-4-基)-5-氨基-3-(4-((5-氯吡啶基-2-基)氧基)苯基)-1h-吡唑-4-甲酰胺(4b)(74mg,产率:88%)。
[0416]
lcms m/z=496.2[m+1]
+
[0417]
第三步:5-氨基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-1-(1'-(2-(2,6-二氧代哌啶-3-基)-1,3-二氧代异吲哚啉-5-基)-[1,4'-联哌啶]-4-基)-1h-吡唑-4-甲酰胺(化合物4)
[0418]
5-amino-3-(4-((5-chloropyridin-2-yl)oxy)phenyl)-1-(1'-(2-(2,6-dioxopiperidin-3-yl)-1,3-dioxoisoindolin-5-yl)-[1,4'-bipiperidin]-4-yl)-1h-pyrazole-4-carboxamide
[0419][0420]
将1-([1,4'-联哌啶]-4-基)-5-氨基-3-(4-((5-氯吡啶基-2-基)氧基)苯基)-1h-吡唑-4-甲酰胺(4b)(73mg,0.15mmol)溶于5ml dmso中,室温下加入2-(2,6-二氧代哌啶-3-基)-5-氟异吲哚啉-1,3-二酮(合成方法见wo2017197056)(0.10g,0.36mmol)和二异丙基乙基胺(0.20g,1.55mmol),升温至80度反应4小时。将反应液倒入20ml水中,水相用二氯甲烷/
甲醇(v/v)=10:1萃取(30ml
×
3),合并有机相,有机相用50ml水洗涤,无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=10:1-5:1),得到5-氨基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-1-(1'-(2-(2,6-二氧代哌啶-3-基)-1,3-二氧代异吲哚啉-5-基)-[1,4'-联哌啶]-4-基)-1h-吡唑-4-甲酰胺(化合物4)(50mg,产率:44%)。
[0421]1h nmr(400mhz,dmso-d6)δ11.05(s,1h),8.25
–
8.20(m,1h),7.97(dd,1h),7.66(d,1h),7.57
–
7.50(m,2h),7.35
–
7.31(m,1h),7.28
–
7.18(m,3h),7.14(dd,1h),6.30(s,2h),5.06(dd,1h),4.18
–
4.03(m,3h),3.06
–
2.81(m,5h),2.70
–
2.53(m,3h),2.37
–
2.19(m,2h),2.07
–
1.75(m,7h),1.61
–
1.45(m,2h).
[0422]
lcms m/z=752.3[m+1]
+
[0423]
实施例5
[0424]
5-氨基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-1-(1'-(1-(2-(2,6-二氧代哌啶-3-基)-1,3-二氧代异吲哚啉-5-基)氮杂环丁-3-基)-[1,4'-联哌啶]-4-基)-1h-吡唑-4-甲酰胺(化合物5)
[0425]
5-amino-3-(4-((5-chloropyridin-2-yl)oxy)phenyl)-1-(1'-(1-(2-(2,6-dioxopiperidin-3-yl)-1,3-dioxoisoindolin-5-yl)azetidin-3-yl)-[1,4'-bipiperidin]-4-yl)-1h-pyrazole-4-carboxamide
[0426][0427]
第一步:3-(4-(5-氨基-4-氨基甲酰基-3-(4-((5-氯吡啶基-2-基)氧基)苯基)-1h-吡唑-1-基)-[1,4'-联哌啶]-1'-基)氮杂环丁-1-甲酸叔丁酯(5a)
[0428]
tert-butyl
[0429]
3-(4-(5-amino-4-carbamoyl-3-(4-((5-chloropyridin-2-yl)oxy)phenyl)-1h-pyrazol-1-yl)-[1,4'-bipiperidin]-1'-yl)azetidine-1-carboxylate
dioxopiperidin-3-yl)-1,3-dioxoisoindolin-5-yl)azetidin-3-yl)-[1,4'-bipiperidin]-4-yl)-1h-pyrazole-4-carboxamide
[0440][0441]
将5-氨基-1-(1'-(氮杂环丁-3-基)-[1,4'-联哌啶]-4-基)-3-(4-((5-氯吡啶-2-基)氧基)苯基)-1h-吡唑-4-甲酰胺(5b)(73mg,0.13mmol)溶于4ml dmso中,室温下加入2-(2,6-二氧代哌啶-3-基)-5-氟异吲哚啉-1,3-二酮(合成方法见wo2017197056)(53mg,0.19mmol)和二异丙基乙基胺(84mg,0.65mmol),升温至80℃反应4小时。将反应液倒入20ml水中,水相用二氯甲烷/甲醇(v/v)=10:1萃取(30ml
×
3),合并有机相,有机相用50ml水洗涤,无水硫酸钠干燥。粗产品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=10:1-5:1),得到5-氨基-3-(4-((5-氯吡啶-2-基)氧基)苯基)-1-(1'-(1-(2-(2,6-二氧代哌啶-3-基)-1,3-二氧代异吲哚啉-5-基)氮杂环丁-3-基)-[1,4'-联哌啶]-4-基)-1h-吡唑-4-甲酰胺(化合物5)(25mg,产率:24%)。
[0442]1h nmr(400mhz,dmso-d6)δ11.04(s,1h),8.23(d,1h),7.98(dd,1h),7.65(d,1h),7.58
–
7.50(m,2h),7.25
–
7.17(m,2h),7.14(d,1h),6.79(d,1h),6.65(dd,1h),6.30(s,2h),5.05(dd,1h),4.17
–
4.05(m,3h),3.88
–
3.78(m,2h),3.38
–
3.30(m,1h),3.08
–
2.80(m,5h),2.70
–
2.52(m,2h),2.38
–
2.19(m,3h),2.08
–
1.65(m,9h),1.58
–
1.41(m,2h).
[0443]
lcms m/z=404.3[m/2+1]
+
[0444]
实施例6:
[0445]
5-(3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)氮杂环丁-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物6)
[0446]
5-(3-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)piperidin-1-yl)methyl)azetidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dione
[0447][0448]
第一步:3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)氮杂环丁-1-甲酸叔丁酯(6a)
[0449]
tert-butyl3-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)piperidin-1-yl)methyl)azetidine-1-carboxylate
[0450][0451]
将上述粗品(2-氯-4-苯氧基苯基)(4-(哌啶-4-基氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(中间体1)(200mg)溶于10ml dce中,加入3-甲酰基氮杂环丁-1-甲酸叔丁酯(92mg,0.5mmol)和乙酸(0.05ml,0.875mmol),反应于室温搅拌1h,加入三乙酰氧基硼氢化钠(286mg,1.35mmol),反应于室温搅拌16h。向反应液中加入10ml水淬灭反应,分离出有机层,水层用二氯甲烷萃取(30ml
×
3),合并有机层,无水硫酸钠干燥,减压浓缩后粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=20:1),得3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)氮杂环丁-1-甲酸叔丁酯(6a)(220mg,从化合物1d算两步收率:72%)。
[0452]
第二步:(4-((1-(氮杂环丁-3-基甲基)哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(6b)
[0453]
(4-((1-(azetidin-3-ylmethyl)piperidin-4-yl)amino)-7h-pyrrolo[2,3-d]pyrimidin-5-yl)(2-chloro-4-phenoxyphenyl)methanone
[0454][0455]
将3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)氮杂环丁-1-甲酸叔丁酯(6a)(220mg,0.36mmol)溶于10ml dcm中,加入2.0ml三氟乙酸,反应于室温搅拌2h。将反应体系减压浓缩,将残余物溶于10ml dcm,加入10ml水后,滴加1mol/l naoh溶液调ph至12,分离出有机层,水层用二氯甲烷萃取(30ml
×
3),合并有机层,无水硫酸钠干燥,减压浓缩,得粗品(4-((1-(氮杂环丁-3-基甲基)哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(6b)(35mg)。
[0456]
第三步:5-(3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)氮杂环丁-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物6)
[0457]
5-(3-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)piperidin-1-yl)methyl)azetidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dione
[0458][0459]
将上述粗品(4-((1-(氮杂环丁-3-基甲基)哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(6b)(35mg)溶于2ml dmso中,加入0.2ml dipea和2-(2,6-二氧代哌啶-3-基)-5-氟异吲哚啉-1,3-二酮(合成方法见wo2017197056)(21mg,0.08mmol),反应于80℃搅拌5h。将反应液冷却至室温,加入5ml水,过滤,收集滤饼,用20ml水洗涤,固体用30ml二氯甲烷溶解,无水硫酸钠干燥,减压浓缩后粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=15:1),得5-(3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)氮杂环丁-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物6)(15mg,从化合物6a算两步收率:5%)。
[0460]1h nmr(400mhz,cdcl3)δ9.08(d,1h),8.39
–
8.30(m,1h),7.63(d,1h),7.47
–
7.36(m,3h),7.36
–
7.31(m,1h),7.26
–
7.19(m,1h),7.13
–
7.05(m,3h),6.96(dd,1h),6.80(d,1h),6.49(dd,1h),4.93(dd,1h),4.35
–
4.20(m,1h),4.20
–
4.11(m,2h),3.77
–
3.68(m,2h),3.15
–
3.00(m,1h),2.95
–
2.65(m,7h),2.51
–
2.34(m,2h),2.24
–
2.07(m,3h),1.90
–
1.76(m,2h).
[0461]
lcms m/z=773.3[m+1]
+
[0462]
实施例7:
[0463]
5-(3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)
吡咯并[2,3-d]嘧啶-5-基)甲酮(7b)
[0471]
(2-chloro-4-phenoxyphenyl)(4-((1-(pyrrolidin-3-ylmethyl)piperidin-4-yl)amino)-7h-pyrrolo[2,3-d]pyrimidin-5-yl)methanone
[0472][0473]
将3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)吡咯烷-1-甲酸叔丁酯(7a)(280mg,0.44mmol)溶于10ml dcm中,加入3.0ml三氟乙酸,反应于室温搅拌2h。将反应体系减压浓缩,将残余物溶于20ml dcm,加入20ml水,滴加1mol/l naoh溶液调ph至12,分离出有机层,水层用二氯甲烷萃取(30ml
×
3),合并有机层,无水硫酸钠干燥,减压浓缩,得粗品(2-氯-4-苯氧基苯基)(4-((1-(吡咯烷-3-基甲基)哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(7b)(200mg)。
[0474]
第三步:5-(3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)吡咯烷-1-基)-2-(2,6-二氧哌啶-3-基)异吲哚啉-1,3-二酮(化合物7)
[0475]
5-(3-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)piperidin-1-yl)methyl)pyrrolidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dione
[0476][0477]
将上述粗品(2-氯-4-苯氧基苯基)(4-((1-(吡咯烷-3-基甲基)哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(7b)(200mg)溶于10ml dmso中,加入1ml dipea和2-(2,6-二氧代哌啶-3-基)-5-氟异吲哚啉-1,3-二酮(合成方法见wo2017197056)(135mg,0.49mmol),反应于80℃搅拌5h。将反应液冷却至室温,加入10ml水,过滤,收集滤饼,用50ml水洗涤,固体用50ml二氯甲烷溶解,无水硫酸钠干燥,减压浓缩后粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=15:1),得5-(3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)吡咯烷-1-基)-2-(2,6-二氧哌啶-3-基)异吲哚啉-1,3-二酮(化合物7)(55mg,从化合物7a算两步收率:16%)。
[0478]1h nmr(400mhz,cdcl3)δ9.04(d,1h),8.34(s,1h),7.65(d,1h),7.49
–
7.35(m,3h),7.31(s,1h),7.26
–
7.19(m,1h),7.14
–
7.05(m,3h),6.99
–
6.93(m,2h),6.70(dd,1h),4.93(dd,1h),4.32
–
4.18(m,1h),3.63
–
3.54(m,1h),3.54
–
3.36(m,2h),3.25
–
3.16(m,1h),2.97
–
2.62(m,5h),2.54
–
2.27(m,4h),2.27
–
2.06(m,4h),1.92
–
1.72(m,4h).
[0479]
lcms m/z=787.3[m+1]
+
[0480]
实施例8:
[0481]
5-(4-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)哌啶-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物8)
[0482]
5-(4-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)piperidin-1-yl)methyl)piperidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dione
[0483][0484]
第一步:4-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)哌啶-1-甲酸叔丁酯(8a)
[0485]
tert-butyl4-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)piperidin-1-yl)methyl)piperidine-1-carboxylate
[0486][0487]
将上述粗品(2-氯-4-苯氧基苯基)(4-(哌啶-4-基氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(中间体1)(200mg)溶于10ml dce中,加入4-甲酰基哌啶-1-甲酸叔丁酯(106mg,0.5mmol)和乙酸(0.05ml,0.875mmol),反应于室温搅拌1h,加入三乙酰氧基硼氢化钠(286mg,1.35mmol),反应于室温搅拌16h。向反应液中加入10ml水淬灭反应,分离出有机层,水层用二氯甲烷萃取(30ml
×
3),合并有机层,无水硫酸钠干燥,减压浓缩后粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=20:1),得4-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)哌啶-1-甲酸叔丁酯(8a)(168mg,从
化合物1d算两步收率:52%)。
[0488]
第三步:(2-氯-4-苯氧基苯基)(4-((1-(哌啶-4-基甲基)哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(8b)
[0489]
(2-chloro-4-phenoxyphenyl)(4-((1-(piperidin-4-ylmethyl)piperidin-4-yl)amino)-7h-pyrrolo[2,3-d]pyrimidin-5-yl)methanone
[0490][0491]
将4-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)哌啶-1-甲酸叔丁酯(8a)(168mg,0.26mmol)溶于10ml dcm中,加入2.0ml三氟乙酸,反应于室温搅拌2h。将反应体系减压浓缩,将残余物溶于10ml dcm,加入10ml水,滴加1mol/lnaoh溶液调ph至12,分离出有机层,水层用二氯甲烷萃取(30ml
×
3),合并有机层,无水硫酸钠干燥,减压浓缩,得粗品(2-氯-4-苯氧基苯基)(4-((1-(哌啶-4-基甲基)哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(8b)(71mg)。
[0492]
第三步:5-(4-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)哌啶-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物8)
[0493]
5-(4-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)piperidin-1-yl)methyl)piperidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dione
[0494][0495]
将上述粗品(2-氯-4-苯氧基苯基)(4-((1-(哌啶-4-基甲基)哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(8b)(71mg)溶于5ml dmso中,加入0.5ml dipea和2-(2,6-二氧代哌啶-3-基)-5-氟异吲哚啉-1,3-二酮(合成方法见wo2017197056)(40mg,0.14mmol),反应于80℃搅拌5h。将反应液冷却至室温,加入10ml水,过滤,收集滤饼,用30ml水洗涤,固体用30ml二氯甲烷溶解,无水硫酸钠干燥,减压浓缩后粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=15:1),得5-(4-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)甲基)哌啶-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物8)(50mg,从化合物8a算两步收率:24%)。
[0496]1h nmr(400mhz,cdcl3)δ9.16
–
9.04(m,1h),8.33(s,1h),7.66(d,1h),7.46
–
7.37(m,3h),7.33(s,1h),7.29
–
7.26(m,1h),7.26
–
7.18(m,1h),7.13
–
7.06(m,3h),7.03(dd,1h),6.96(dd,1h),4.94(dd,1h),4.38
–
4.22(m,1h),3.99
–
3.89(m,2h),3.03
–
2.89(m,4h),2.89
–
2.65(m,3h),2.46
–
2.32(m,2h),2.32
–
2.17(m,2h),2.17
–
2.07(m,2h),2.03
–
1.83(m,
6h),1.40
–
1.28(m,2h).
[0497]
lcms m/z=801.3[m+1]
+
[0498]
实施例9:
[0499]
5-(3-((3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)氮杂环丁-1-基)甲基)氮杂环丁-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物9)的三氟乙酸盐
[0500]
5-(3-((3-(4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)piperidin-1-yl)azetidin-1-yl)methyl)azetidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dionetrifluoroacetate
[0501][0502]
第一步:3-((3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)氮杂环丁-1-基)甲基)氮杂环丁-1-甲酸叔丁酯(9a)
[0503]
tert-butyl3-((3-(4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)piperidin-1-yl)azetidin-1-yl)methyl)azetidine-1-carboxylate
[0504][0505]
将上述粗品[4-[[1-(氮杂环丁-3-基)-4-哌啶基]氨基]-7h-吡咯并[2,3-d]嘧啶-5-基]-(2-氯-4-苯氧基-苯基)甲酮(1b)的三氟乙酸盐(0.50g)溶解于20ml dce中,加入3-甲酰基氮杂环丁-1-甲酸叔丁酯(0.37g,2.0mmol),室温搅拌10min,加入三乙酰氧基硼氢化钠(0.42g,2.0mmol),室温搅拌反应12h。向反应液中缓慢滴加50ml饱和碳酸氢钠溶液,用30ml二氯甲烷萃取,无水硫酸钠干燥,减压浓缩后粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=20:1),得到3-((3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)氮杂环丁-1-基)甲基)氮杂环丁-1-甲酸叔丁酯(9a)(0.1g,从化合物1a算两步收率:27%)。
[0506]
lc-ms m/z=672.3[m+1]
+
[0507]
第二步:(4-((1-(1-(氮杂环丁-3-基甲基)氮杂环丁-3-基)哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(9b)
[0508]
(4-((1-(1-(azetidin-3-ylmethyl)azetidin-3-yl)piperidin-4-yl)amino)-7h-pyrrolo[2,3-d]pyrimidin-5-yl)(2-chloro-4-phenoxyphenyl)methanone
[0509][0510]
将3-((3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)氮杂环丁-1-基)甲基)氮杂环丁-1-甲酸叔丁酯(9a)(0.1g,0.15mmol)溶解到15ml dcm中,加入5ml三氟乙酸,室温搅拌3h。向反应液中缓慢滴加30ml饱和碳酸氢钠溶液,用30ml二氯甲烷萃取,无水硫酸钠干燥,减压浓缩,得粗品(4-((1-(1-(氮杂环丁-3-基甲基)氮杂环丁-3-基)哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(9b)(0.05g)。
[0511]
第三步:5-(3-((3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)氮杂环丁-1-基)甲基)氮杂环丁-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物9)的三氟乙酸盐
[0512]
5-(3-((3-(4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)piperidin-1-yl)azetidin-1-yl)methyl)azetidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dionetrifluoroacetate
[0513][0514]
将上述粗品(4-((1-(1-(氮杂环丁-3-基甲基)氮杂环丁-3-基)哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(9b)(0.05g)溶于5ml dmso中,加入1.0ml dipea和2-(2,6-二氧代哌啶-3-基)-5-氟异吲哚啉-1,3-二酮(合成方法见wo2017197056)(0.1g,0.36mmol),反应于90℃搅拌5h。将反应液冷却至室温,用50ml乙酸乙酯稀释,有机相用50ml水洗涤,无水硫酸钠干燥,减压浓缩后粗品过pre-hplc(仪器及制备柱:采用glison gx-281制备液相,制备柱型号是sunfire c18,5μm,内径
×
长度=30mm
×
150mm)。制备方法:粗品用甲醇和二甲亚砜溶解,并用0.45μm滤膜过滤,制备成样品液。流动相体系:乙腈/水(含0.1%tfa)。梯度洗脱方法:乙腈由5%梯度洗脱60%(洗脱时间15min),冻干得到5-(3-((3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)哌啶-1-基)氮杂环丁-1-基)甲基)氮杂环丁-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物9)的三氟乙酸盐(10mg)。
[0515]1h nmr(400mhz,dmso-d6)δ11.15
–
11.00(m,1h),8.91
–
8.82(m,1h),8.30
–
8.23(m,1h),7.97
–
7.87(m,1h),7.70
–
7.62(m,2h),7.58(d,1h),7.52
–
7.44(m,2h),7.30
–
7.22(m,1h),7.22
–
7.14(m,3h),7.04(d,1h),6.82
–
6.77(m,1h),6.66(d,1h),5.05(dd,1h),4.34
–
4.02(m,7h),3.86
–
3.78(m,2h),3.52
–
3.48(m,1h),3.08
–
2.80(m,6h),2.70
–
2.52(m,4h),2.25
–
2.10(m,2h),2.06
–
1.96(m,1h),1.80
–
1.60(m,2h).
[0516]
lcms m/z=828.3[m+1]
+
[0517]
实施例10:
[0518]
5-(3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-双哌啶]-1'-基)甲基)氮杂环丁-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物10)的三氟乙酸盐
[0519]
5-(3-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-[1,4'-bipiperidin]-1'-yl)methyl)azetidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dione trifluoroacetate
[0520][0521]
第一步:3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-双哌啶]-1'-基)甲基)氮杂环丁-1-甲酸叔丁酯(10a)
[0522]
tert-butyl3-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-[1,4'-bipiperidin]-1'-yl)methyl)azetidine-1-carboxylate
[0523][0524]
将粗品(4-([1,4'-联哌啶]-4-基氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(2b)的三氟乙酸盐(0.3g)溶解于20ml dce中,加入3-甲酰基氮杂环丁-1-甲酸叔丁酯(0.2g,1.08mmol),室温搅拌10min,加入三乙酰氧基硼氢化钠(0.21g,1.0mmol),室温搅拌反应12h。向反应液中缓慢滴加50ml饱和碳酸氢钠溶液,用30ml二氯甲烷萃取,无水硫酸钠干燥,减压浓缩后粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=15:1),得到3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-双哌啶]-1'-基)甲基)氮杂环丁-1-甲酸叔丁酯(10a)(0.35g,从化合物2a算两步收率:>99%)。
[0525]
lc-ms m/z=700.3[m+1]
+
[0526]
第二步:(4-((1'-(氮杂环丁-3-基甲基)-[1,4'-双哌啶]-4-基]氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(10b)
[0527]
(4-((1'-(azetidin-3-ylmethyl)-[1,4'-bipiperidin]-4-yl)amino)-7h-pyrrolo[2,3-d]pyrimidin-5-yl)(2-chloro-4-phenoxyphenyl)methanone
[0528][0529]
将3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-双哌啶]-1'-基)甲基)氮杂环丁-1-甲酸叔丁酯(10a)(0.35g,0.50mmol)溶解到15ml dcm中,加入5ml三氟乙酸,室温搅拌3h。向反应液中缓慢滴加30ml饱和碳酸氢钠溶液,用30ml二氯甲烷萃取,无水硫酸钠干燥,减压浓缩,得粗品(4-((1'-(氮杂环丁-3-基甲基)-[1,4'-双哌啶]-4-基]氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(10b)(0.45g)。
[0530]
第三步:5-(3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-双哌啶]-1'-基)甲基)氮杂环丁-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物10)的三氟乙酸盐
[0531]
5-(3-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-[1,4'-bipiperidin]-1'-yl)methyl)azetidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dione trifluoroacetate
[0532][0533]
将上述粗品(4-((1'-(氮杂环丁-3-基甲基)-[1,4'-双哌啶]-4-基]氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(10b)(0.1g)溶于10ml dmso中,加入1.0ml dipea和2-(2,6-二氧代哌啶-3-基)-5-氟异吲哚啉-1,3-二酮(合成方法见wo2017197056)(0.1g,0.36mmol),反应于90℃搅拌5h。将反应液冷却至室温,用50ml乙酸乙酯稀释,有机相用50ml水洗涤,无水硫酸钠干燥,减压浓缩后粗品过pre-hplc(仪器及制备柱:采用glison gx-281制备液相,制备柱型号是sunfire c18,5μm,内径
×
长度=30mm
×
150mm)。制备方法:粗品用甲醇和二甲亚砜溶解,并用0.45μm滤膜过滤,制备成样品液。流动相体系:乙腈/水(含0.1%tfa)。梯度洗脱方法:乙腈由5%梯度洗脱60%(洗脱时间15min),冻干得到5-(3-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-双哌啶]-1'-基)甲基)氮杂环丁-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物10)的三氟乙酸盐(8mg)。
[0534]1h nmr(400mhz,dmso-d6)δ12.84(br.s,1h),11.06(s,1h),8.81(br.s,1h),8.29
(s,1h),7.73
–
7.64(m,2h),7.58(d,1h),7.53
–
7.45(m,2h),7.30
–
7.23(m,1h),7.22
–
7.15(m,3h),7.04(dd,1h),6.81(s,1h),6.71
–
6.64(m,1h),5.06(dd,1h),4.48
–
4.30(m,1h),4.30
–
4.16(m,2h),3.89
–
3.79(m,2h),3.70
–
3.53(m,6h),3.32
–
3.18(m,4h),3.11
–
2.95(m,2h),2.95
–
2.82(m,1h),2.70
–
2.52(m,2h),2.46
–
2.22(m,4h),2.08
–
1.71(m,5h).
[0535]
lcms m/z=856.3[m+1]
+
[0536]
实施例11:
[0537]
5-(4-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-双哌啶]-1'-基)甲基)哌啶-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物11)的三氟乙酸盐
[0538]
5-(4-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-[1,4'-bipiperidin]-1'-yl)methyl)piperidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dione trifluoroacetate
[0539][0540]
第一步:4-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-双哌啶]-1'-基)甲基)哌啶-1-甲酸叔丁酯(11a)
[0541]
tert-butyl4-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-[1,4'-bipiperidin]-1'-yl)methyl)piperidine-1-carboxylate
[0542][0543]
将上述粗品(4-([1,4'-联哌啶]-4-基氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(2b)的三氟乙酸盐(0.3g)溶解于20ml dce中,加入4-甲酰基哌啶-1-甲酸叔丁酯(0.3g,1.4mmol),室温搅拌10min,加入三乙酰氧基硼氢化钠(0.42g,2.0mmol),室温搅拌反应12h。向反应液中缓慢滴加50ml饱和碳酸氢钠溶液,用30ml二氯甲烷萃取,无水硫酸钠干燥,减压浓缩后粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=
20:1),得到4-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-双哌啶]-1'-基)甲基)哌啶-1-甲酸叔丁酯(11a)(0.3g,从化合物2a算两步收率:>99%)。
[0544]
lc-ms m/z=728.4[m+1]
+
[0545]
第二步:(2-氯-4-苯氧基苯基)(4-((1'-(哌啶-4-基甲基)-[1,4'-双哌啶]-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(11b)
[0546]
(2-chloro-4-phenoxyphenyl)(4-((1'-(piperidin-4-ylmethyl)-[1,4'-bipiperidin]-4-yl)amino)-7h-pyrrolo[2,3-d]pyrimidin-5-yl)methanone
[0547][0548]
将4-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-双哌啶]-1'-基)甲基)哌啶-1-甲酸叔丁酯(11a)(0.3g,0.41mmol)溶解到15ml dcm中,加入5ml三氟乙酸,室温搅拌3h。向反应液中缓慢滴加30ml饱和碳酸氢钠溶液,用30ml二氯甲烷萃取,无水硫酸钠干燥,减压浓缩,得粗品(2-氯-4-苯氧基苯基)(4-((1'-(哌啶-4-基甲基)-[1,4'-双哌啶]-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(11b)(0.2g)。
[0549]
第三步:5-(4-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-双哌啶]-1'-基)甲基)哌啶-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物11)的三氟乙酸盐
[0550]
5-(4-((4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-[1,4'-bipiperidin]-1'-yl)methyl)piperidin-1-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dione trifluoroacetate
[0551][0552]
将上述粗品(2-氯-4-苯氧基苯基)(4-((1'-(哌啶-4-基甲基)-[1,4'-双哌啶]-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(11b)(0.2g)溶于10ml dmso中,加入1.0ml dipea和2-(2,6-二氧代哌啶-3-基)-5-氟异吲哚啉-1,3-二酮(合成方法见wo2017197056)(0.2g,0.72mmol),反应于90℃搅拌5h。将反应液冷却至室温,用50ml乙酸乙酯稀释,有机相用50ml水洗涤,无水硫酸钠干燥,减压浓缩后粗品过pre-hplc(仪器及制备柱:采用glison gx-281制备液相,制备柱型号是sunfire c18,5μm,内径
×
长度=30mm
×
150mm)。制备方法:粗品用甲醇和二甲亚砜溶解,并用0.45μm滤膜过滤,制备成样品液。流动相体系:乙腈/水(含0.1%tfa)。梯度洗脱方法:乙腈由5%梯度洗脱60%(洗脱时间15min),冻干得到5-(4-((4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-[1,4'-双哌啶]-1'-基)甲基)哌啶-1-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物11)
的三氟乙酸盐(150mg)。
[0553]1h nmr(400mhz,dmso-d6)δ11.07(s,1h),8.31(s,1h),7.74
–
7.64(m,2h),7.60(d,1h),7.53
–
7.45(m,2h),7.39
–
7.33(m,1h),7.31
–
7.23(m,2h),7.23
–
7.15(m,3h),7.05(dd,1h),5.08(dd,1h),4.48
–
4.32(m,1h),4.18
–
4.08(m,2h),3.80
–
3.67(m,2h),3.66
–
3.46(m,3h),3.39
–
3.21(m,2h),3.10
–
2.96(m,5h),2.96
–
2.83(m,1h),2.66
–
2.52(m,2h),2.48
–
2.24(m,4h),2.24
–
1.96(m,5h),1.96
–
1.78(m,4h),1.36
–
1.20(m,2h).
[0554]
lcms m/z=884.3[m+1]
+
[0555]
实施例12:
[0556]
trans-5-(3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-3-氟哌啶-1-基)-[1,3'-双氮杂环丁]-1'-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物12)的三氟乙酸盐
[0557]
trans-5-(3-(4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-3-fluoropiperidin-1-yl)-[1,3'-biazetidin]-1'-yl)-2-(2,6-dioxopiperidin-3-yl)isoindoline-1,3-dionetrifluoroacetate
[0558][0559]
第一步:trans-4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-3-氟哌啶-1-甲酸叔丁酯(12a)
[0560]
trans-tert-butyl4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-3-fluoropiperidine-1-carboxylate
[0561][0562]
将trans-4-氨基-3-氟哌啶-1-甲酸叔丁酯(393mg,1.80mmol)(合成方法见wo2016127358)与(2-氯-4-苯氧基苯基)(4-氯-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(1c)(576mg,1.50mmol)溶于30ml异丙醇中,加入1ml dipea,回流反应5h。将反应液冷却至室温,加入50ml水,用100ml乙酸乙酯萃取,有机相用100ml水洗涤,无水硫酸钠干燥,减压浓缩后粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=15:1),得trans-4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-3-氟哌啶-1-甲酸叔丁酯(12a)(700mg,从化合物1c算收率:83%)。
[0563]
lcms m/z=566.2[m+1]
+
[0564]
第二步:trans-(2-氯-4-苯氧基苯基)(4-((3-氟哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(12b)的三氟乙酸盐
[0565]
trans-(2-chloro-4-phenoxyphenyl)(4-((3-fluoropiperidin-4-yl)amino)-7h-pyrrolo[2,3-d]pyrimidin-5-yl)methanone trifluoroacetate
[0566][0567]
将trans-4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-3-氟哌啶-1-甲酸叔丁酯(12a)(700mg,1.24mmol)溶解到30ml dcm中,加入10ml三氟乙酸,室温搅拌4h。将反应体系减压浓缩,得粗品trans-(2-氯-4-苯氧基苯基)(4-((3-氟哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(12b)的三氟乙酸盐(810mg)。
[0568]
lcms m/z=466.2[m+1]
+
[0569]
第三步:trans-3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-3-氟哌啶-1-基)氮杂环丁-1-甲酸叔丁酯(12c)
[0570]
trans-tert-butyl3-(4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-3-fluoropiperidin-1-yl)azetidine-1-carboxylate
[0571][0572]
将上述粗品trans-(2-氯-4-苯氧基苯基)(4-((3-氟哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)甲酮(12b)的三氟乙酸盐(0.8g)溶于35ml dce中,加入3-氧代氮杂环
丁-1-甲酸叔丁酯(423mg,2.47mmol),室温搅拌20min,加入三乙酰氧基硼氢化钠(1.02g,4.81mmol),室温搅拌18h。向反应液中缓慢加入50ml饱和碳酸氢钠溶液,用80ml dcm萃取3次,有机相用50ml水洗涤,无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=20:1),得trans-3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-3-氟哌啶-1-基)氮杂环丁-1-甲酸叔丁酯(12c)(700mg,从化合物12a算两步收率:92%)。
[0573]
lcms m/z=621.3[m+1]
+
[0574]
第四步:trans-(4-((1-(氮杂环丁-3-基)-3-氟哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(12d)的三氟乙酸盐
[0575]
trans-(4-((1-(azetidin-3-yl)-3-fluoropiperidin-4-yl)amino)-7h-pyrrolo[2,3-d]pyrimidin-5-yl)(2-chloro-4-phenoxyphenyl)methanone trifluoroacetate
[0576][0577]
将trans-3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-3-氟哌啶-1-基)氮杂环丁-1-甲酸叔丁酯(12c)(500mg,0.81mmol)溶解到25ml二氯甲烷中,加入10ml三氟乙酸,室温搅拌2h。将反应体系减压浓缩,得粗品trans-(4-((1-(氮杂环丁-3-基)-3-氟哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(12d)的三氟乙酸盐(0.61g)。
[0578]
lcms m/z=521.3[m+1]
+
[0579]
第五步:trans-3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)氨基)-3-氟哌啶-1-基)-[1,3'-双氮杂环丁]-1'-甲酸叔丁酯(12e)
[0580]
trans-tert-butyl3-(4-((5-(2-chloro-4-phenoxybenzoyl)-7h-pyrrolo[2,3-d]pyrimidin-4-yl)amino)-3-fluoropiperidin-1-yl)-[1,3'-biazetidine]-1'-carboxylate
[0581][0582]
将上述粗品trans-(4-((1-(氮杂环丁-3-基)-3-氟哌啶-4-基)氨基)-7h-吡咯并[2,3-d]嘧啶-5-基)(2-氯-4-苯氧基苯基)甲酮(12d)的三氟乙酸盐(0.6g)溶于40ml dce中,加入固体碳酸氢钠(202mg,2.40mmol),室温搅拌20min,加入3-氧代氮杂环丁-1-甲酸叔丁酯(329mg,1.92mmol),室温搅拌10min,加入三乙酰氧基硼氢化钠(814mg,3.84mmol),室温搅拌16h。向反应体系中缓慢加入60ml碳酸氢钠溶液,用dcm萃取(80ml
×
3),有机相用50ml水洗涤,无水硫酸钠干燥,减压浓缩,粗品用硅胶柱色谱分离提纯(二氯甲烷/甲醇(v/v)=10:1),得trans-3-(4-((5-(2-氯-4-苯氧基苯甲酰基)-7h-吡咯并[2,3-d]嘧啶-4-基)
[1,3'-双氮杂环丁]-1'-基)-2-(2,6-二氧代哌啶-3-基)异吲哚啉-1,3-二酮(化合物12)的三氟乙酸盐(120mg)。
[0593]1h nmr(400mhz,cdcl3)δ9.26
–
9.14(m,1h),8.35(s,1h),7.62(d,1h),7.46
–
7.38(m,3h),7.35(s,1h),7.25
–
7.19(m,1h),7.13
–
7.06(m,3h),6.96(dd,1h),6.77(d,1h),6.51(dd,1h),4.92(dd,1h),4.86
–
4.63(m,1h),4.62
–
4.46(m,1h),4.08
–
3.98(m,2h),3.91
–
3.81(m,2h),3.74
–
3.64(m,1h),3.61
–
3.51(m,2h),3.24
–
3.15(m,1h),3.13
–
3.03(m,2h),3.03
–
2.91(m,1h),2.91
–
2.64(m,4h),2.43
–
2.21(m,3h),2.17
–
2.06(m,1h),1.87
–
1.72(m,1h).
[0594]
lcms m/z=832.3[m+1]
+
[0595]
七:效果(必填)
[0596]
1.细胞增殖抑制实验
[0597]
当su-dhl-4细胞生长至5
×
106个/ml,mino细胞生长至2
×
106个/ml时,细胞铺板。
[0598]
用移液管将培养皿/瓶中的细胞混匀,转移至15ml(50ml)无菌离心管中,1500rpm离心3分钟,离心完毕取出,弃去上清液。离心管加入5ml培养基重悬细胞,计数。根据计数的结果将su-dhl-4细胞稀释成20000个/90μl,mino细胞稀释成5000个/90μl,用排枪进行细胞铺板,每孔90μl,铺板同时注意将加样槽的细胞混均匀,在96孔板上标注好细胞信息。
[0599]
su-dhl-4细胞:p13i与受试化合物母液10mm,起始给药浓度10000nm,3倍稀释9个梯度。化合物浓度:10000、3333.33、1111.11、370.37、123.46、41.15、13.72、4.57、1.52nm。稀释方式:第1孔5μl化合物母液+495μl培养基,第2孔-第9孔加80μl含dmso 1%的培养基+前一孔稀释液40μl。
[0600]
mino细胞:p13i与受试化合物母液10mm,起始给药浓度10000nm,5倍稀释6个梯度。给药浓度:10000、2000、400、80、16、3.2nm。稀释方式:第1孔5μl化合物母液+495μl培养基,第2孔-第6孔加80μl含dmso 1%的培养基+前一孔稀释液20μl。
[0601]
在铺好细胞的96孔板上加入10μl/孔化合物。每个浓度设3复孔,最后一列为dmso溶媒对照组,在37℃、5%co2条件下继续培养72小时。
[0602]
72小时后,每孔加入100μl检测试剂(cell viability assay,promega,g7573),混匀2分钟,室温孵育10分钟,酶标仪检测化学发光读数。
[0603]
细胞增殖抑制检测(ic
50
):使用origin9.2软件,计算化合物抑制细胞增殖的ic
50
值。
[0604]
表1抑制mino细胞增殖的ic
50
值
[0605]
序号化合物编号ic50(nm)1化合物1的三氟乙酸盐672化合物31023化合物4434化合物9的三氟乙酸盐1095化合物11的三氟乙酸盐1266化合物12的三氟乙酸盐19
[0606]
抑制su-dhl-4细胞增殖的ic
50
值结果见表2。
[0607]
表2抑制su-dhl-4细胞的ic
50
值
[0608]
序号化合物编号ic
50
(nm)
1化合物1679
[0609]
结论:运用本发明技术所合成的化合物对mino细胞(套细胞淋巴瘤细胞)和su-dhl-4细胞(人b淋巴瘤细胞)增殖有显著的抑制作用,本发明的实施例化合物2的三氟乙酸盐、化合物10的三氟乙酸盐、化合物6~7对mino细胞(套细胞淋巴瘤细胞)细胞的活性抑制ic
50
为10-1000nm,本发明的实施例化合物对su-dhl-4细胞(人b淋巴瘤细胞)的活性抑制ic
50
为100-1500nm,部分化合物的活性具体数值见表1和表2。
[0610]
2.大鼠药代动力学测试
[0611]
实验目的:本试验通过单剂量静脉和灌胃给予受试物于sd大鼠,测定大鼠血浆中受试物的浓度,评价受试物在大鼠体内药代特征。
[0612]
试验动物:雄性sd大鼠,200g左右,6~8周龄,6只/化合物。购于成都达硕实验动物有限公司。
[0613]
试验方法:试验当天,6只sd大鼠按体重随机分组。给药前1天禁食不禁水12~14h,给药后4h给食。
[0614][0615][0616]
*剂量以游离碱计。
[0617]
取样
[0618]
于给药前及给药后异氟烷麻醉经眼眶取血0.1ml,置于edtak2离心管中。5000rpm,4℃离心10min,收集血浆。
[0619]
g1&g2组采集血浆时间点:0,5min,15min,30min,1,2,4,6,8,24h。
[0620]
分析检测前,所有样品存于-80℃。用hplc-ms/ms对样品进行检测。
[0621]
*注:i.g.(灌胃)给予化合物。
[0622]
结论:运用本发明技术所合成的化合物在大鼠中具有一定的口服生物利用度。
[0623]
3.大鼠药代动力学测试
[0624]
实验目的:本试验通过单剂量静脉和灌胃给予受试物于sd大鼠,测定大鼠血浆中受试物的浓度,评价受试物在大鼠体内药代特征和生物利用度。
[0625]
试验动物:雄性sd大鼠,200g左右,6~8周龄,6只/化合物。购于成都达硕实验动物有限公司。
[0626]
试验方法:试验当天,6只sd大鼠按体重随机分组。给药前1天禁食不禁水12~14h,给药后4h给食。
[0627][0628]
*剂量以游离碱计。
[0629]
取样
[0630]
于给药前及给药后异氟烷麻醉经眼眶取血0.1ml,置于edtak2离心管中。5000rpm,4℃离心10min,收集血浆。
[0631]
g1&g2组采集血浆时间点:0,5min,15min,30min,1,2,4,6,8,24h。
[0632]
分析检测前,所有样品存于-80℃。用hplc-ms/ms对样品进行检测。
[0633]
表3化合物在大鼠血浆中药代动力学参数
[0634]
受试化合物给药方式*auc
0-t
(ng/ml
·
h)f(%)化合物1i.g.(20mg/kg)6801
±
30416.0
±
0.72
[0635]
*注:i.g.(灌胃)给予化合物。
[0636]
结论:运用本发明技术所合成的化合物在大鼠体内具有一定的口服生物利用度。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1