与肺癌疗效相关的SNP位点、引物组、试剂盒及应用的制作方法
与肺癌疗效相关的snp位点、引物组、试剂盒及应用
技术领域
[0001]
本发明属于生物基因技术领域,尤其涉及一种与肺癌疗效相关的snp位点、引物组、试剂盒及应用。
背景技术:
[0002]
随着工业的发展和环境污染的日趋严重,我国肺癌发病率和死亡率逐年上升,严重危害人们的身心健康,其中非小细胞肺癌(non small cell lung cancer,nsclc)约占80%。nsclc起病隐匿,早期无明显特异性症状,使得75%以上的nsclc患者在确诊时已属中、晚期,无法依靠定量某些肿瘤组织rna水平和蛋白表达水平来预测疗效和预后。
[0003]
自从rosenberg等人首次发现铂类药物的抗肿瘤活性后,铂类药物的研究得到迅速发展,铂类药物通过细胞膜上的铜转运蛋白ctr1发挥作用。铂类药物进入人体细胞后与dna链上的碱基形成交叉联结,生成dna加合物,从而起到破坏肿瘤细胞dna结构和功能的作用。铂类药物发挥抗肿瘤作用机制的主要途径是其可与很多胞内物质结合,限制dna的解旋从而抑制dna的复制,其中大部分结合物能够产生细胞毒性或者毒副作用。
[0004]
regulome dna是在细胞内能调节基因、mrna、蛋白质和代谢产物等重要调控成分的dna序列,包括转录因子结合位点(tanscription factor binding site)、表达数量性状基因座(expression quantitative trait loci,eqtl)、转录因子识别序列(tanscription factor motif)、脱氧核糖核酸酶足迹(dnase footprint)和dnase峰(dnase peak)等,在细胞的新陈代谢、发育、病理和组织演化等过程中起关键作用。
[0005]
regulome-db是一个整合的庞大数据库,包括encode研究数据、高通量测序数据、计算机预测软件数据和其他重要实验研究来源的数据等。regulome-db作为一个新技术,预测单核苷酸多态性(single nucleotide polymorphism,snp)位点是否可影响转录因子的调控作用以及基因表达,并根据其作用程度对功能性snp进行排序,分为i-vi量级(数值越小,snps影响转录因子和基因表达可能性越大。因此,利用regulome-db筛选功能性基因帮助研究者找到疾病相关性基因及其功能对疾病的精准诊断具有重要作用。到目前为止,利用该数据库研究功能性snp与疾病相关性还处于肺癌研究领域。
技术实现要素:
[0006]
本发明实施例的目的在于提供一种与肺癌疗效相关的snp位点,旨在解决背景技术中提出的问题。
[0007]
本发明实施例是这样实现的,一种与肺癌疗效相关的snp位点,其包括parp1基因的rs17573756位点和/或xrcc3基因的rs7142555位点。
[0008]
作为本发明实施例的一个优选方案,所述rs17573756位点的周围的核苷酸序列如序列表seq id no:1所示,其中s碱基为g或c。
[0009]
作为本发明实施例的另一个优选方案,所述rs7142555位点的周围的核苷酸序列如序列表seq id no:2所示,其中k碱基为g或t。
[0010]
本发明实施例的另一目的在于提供一种用于检测上述的snp位点的引物组,其包括rs17573756位点的检测引物对和/或rs7142555位点的检测引物对;
[0011]
其中,所述rs17573756位点的检测引物对包括:
[0012]
rs17573756上游引物,其核苷酸序列如序列表seq id no:3所示;以及
[0013]
rs17573756下游引物,其核苷酸序列如序列表seq id no:4所示。
[0014]
所述rs7142555位点的检测引物对包括:
[0015]
rs7142555上游引物,其核苷酸序列如序列表seq id no:5所示;以及
[0016]
rs7142555下游引物,其核苷酸序列如序列表seq id no:6所示。
[0017]
本发明实施例的另一目的在于提供一种试剂盒,其包括pcr缓冲液以及上述的引物组。
[0018]
作为本发明实施例的另一个优选方案,所述试剂盒用于检测所述snp位点的基因型。
[0019]
本发明实施例的另一目的在于提供一种上述的snp位点在制备用于判定非小细胞肺癌疗效的试剂盒中的应用。
[0020]
本发明实施例的另一目的在于提供一种上述的引物组在制备用于判定非小细胞肺癌疗效的试剂盒中的应用。
[0021]
本发明实施例提供的一种与nsclc疗效相关的regulome区域内的基因序列,通过snp位点parp1-rs17573756和xrcc3-rs7142555的序列研究,提出一种疗效相关的nsclc疗效相关人群的筛查的方法,以利于判断nsclc疗效。具体的,本发明通过提取受试者基因组dna进行snp位点rs17573756和rs7142555的基因分型,其次,组合为危险因子组合比较,随着危险基因型增加肺癌疗效差的危险度越高。相比于现有技术,本发明具有以下优点:
[0022]
(1)本发明提供的引物组可以特异、高效检测出rs17573756和rs7142555多态性位点。
[0023]
(2)本发明通过检测snp位点rs17573756和rs7142555的基因分型结果,可以对nsclc疗效进行判定,从而有利于预测肺癌疾病的疗效。
附图说明
[0024]
图1为携带危险基因型时的危险度和95%的可信区间的统计结果图。
具体实施方式
[0025]
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
[0026]
实施例1
[0027]
该实施例提供了一种与肺癌疗效相关的snp位点,为regulome-snp位点,其包括parp1基因的rs17573756位点和xrcc3基因的rs7142555位点;其中,rs17573756和rs7142555的序列通过www.ncbi.nlm.nih.gov/projects/snp和http://regulome.stanfri.edu/index数据库获得。具体的,rs17573756位点周围的核苷酸序列如序列表seq id no:1所示,具体为:
[0028]
caggtcgctcatgttctctcctcagttaaggaccatggagcaaaggctcgaggctggtctgacactcgttgggagggtagcaggggtccgattgtttgcattgtcccagcatgaggaaccaccagtctggctgagccctgcccctcagacccaccatggcttggtttacatgtttctgtgtagcaagccaaggaggtcttsgttgaacctagcggtcattagaggtatgggagtgggggaccatatcagcagtttccactttattctgaagacagtgggatttctgagactgtcatggtttgaaaagctcgctcatcagccttgtggggaatggaggaaaggaggccaggaggagtggcctctgtggtcacacagaagaaa。
[0029]
其中,s碱基(即rs17573756位点碱基)为g或c;根据该rs17573756位点的基因型可以用于判定nsclc疗效,具体的,rs17573756位点的cc基因型和gc基因型的个体为nsclc疗效差的人群。
[0030]
rs7142555位点周围的核苷酸序列如序列表seq id no:2所示,具体为:
[0031]
gtgctgggattataggcatgggccaccatgcctggccaattgaaatattttaatccagcttttctagttgtgttcagtggaagagttggtcctagtcactaatctgctacttatggacagagacatctcctattttctgttgtaaggacaggaaaaagcagaaaatatagaaaaggaaataaagagcaaccatctctcagakagtactgctgcccaacaagaacactgctgacatttggaaactgttttccaatttgattcttattggaaagcataacaaccagccagggcctgtgctgctggagcgggcagttatgtgcagggagacagctggttacggctggctcctggcctcgacggagcttctcagcctcttggagcctctgtcccctcagctgctgaaggaacacatctcctgcacttctcaagttgctgccggtgcgaaggtgactccagattctgcagtttgggctccgtagctgctcagcaaatgtcagcaggtccagaagcaaggctcctcagctgcagagtgaatgcaaatgtccccattgtaaatggccgt。
[0032]
其中,k碱基(即rs7142555位点碱基)为g或t;根据该rs7142555位点的基因型可以用于判定nsclc疗效,具体的,rs7142555位点的gg基因型和gt基因型的个体为nsclc疗效差的人群。
[0033]
实施例2
[0034]
该实施例提供一种用于检测上述rs17573756位点和rs7142555位点的引物组,其包括包括rs17573756位点的检测引物对和rs7142555位点的检测引物对;
[0035]
其中,rs17573756位点的检测引物对包括:
[0036]
rs17573756上游引物,其核苷酸序列如序列表seq id no:3所示,具体为:accatggcttggtttacatg,其gc比值为45%,tm值为49.7℃;以及
[0037]
rs17573756下游引物,其核苷酸序列如序列表seq id no:4所示,具体为:cgagcttttcaaaccatgac,其gc比值为45%,tm值为49.7℃。
[0038]
另外,rs7142555位点的检测引物对包括:
[0039]
rs7142555上游引物,其核苷酸序列如序列表seq id no:5所示,具体为:ataaagagcaaccatctctcga,其gc比值为41%,tm值为51.1℃;以及
[0040]
rs7142555下游引物,其核苷酸序列如序列表seq id no:6所示,具体为:acatttgcattcactctgcag,其gc比值为43%,tm值为50.5℃。
[0041]
另外,该实施例还提供了一种试剂盒,其包括pcr缓冲液以及上述的引物组。此外,该试剂盒还可包括dna聚合酶(可采用市售hotstartaq dna聚合酶)、三蒸水、脱氧核糖核苷三磷酸混合物(dntp mix)、xcmi限制性内切酶、xhoi限制性内切酶、neb2缓冲液、neb4缓冲液等试剂,但不限于此。
[0042]
实施例3
[0043]
该实施例提供了一种上述试剂盒的应用,其中,上述2个位点经上述引物组pcr扩增后,各pcr产物分别利用限制性内切酶xcmi(对应rs17573756位点)和xhoi(对应rs7142555位点)消化pcr产物,便可根据被切断的条带大小判断基因型。具体的,通过提取受试者基因组dna进行snp位点rs17573756和rs7142555的基因分型,其包括以下步骤:
[0044]
s1、基因组dna的提取:抽取受试者外周静脉血2ml,利用现有技术中市售的全血dna提取试剂盒提取外周静脉血中的基因组dna,并置于-20℃保存,备用。
[0045]
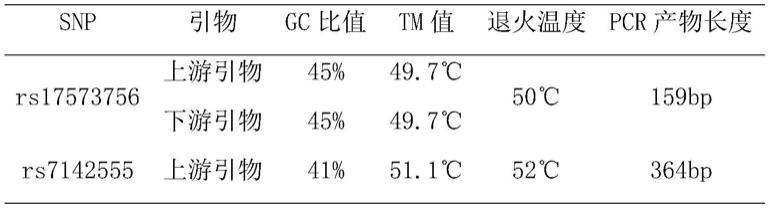
s2、snp基因分型:根据上述2个snp位点rs17573756和rs7142555的序列信息,设计聚合酶链式反应(polymerase chain reaction,pcr),并在生物工程有限公司进行引物组的合成,其中引物组的序列与实施例2提供的相同。合成后的引物与上述基因组dna进行pcr反应,可得到pcr产物;接着,将pcr产物与限制性内切酶进行rflp(限制性内切酶片段长度多态性,restriction fragment length polymorphism)反应,得到反应产物;然后,将反应物置于37℃孵育后,再置于聚丙酰胺凝胶或微芯片电泳系统(mce-202multina)中,根据被切断的条带大小来判断基因型。其中,引物组的gc比值、tm值、退火温度、pcr产物长度如表1所示,被切断的条带大小及其对应的基因型如表2所示。
[0046]
表1
[0047][0048][0049]
表2
[0050][0051]
另外,pcr反应体系如下:将2μl的10
×
pcr缓冲液,2μl的dntp mix,1μl各位点对应的上游引物,1μl各位点对应的下游引物,0.3μl的hotstar taq dna聚合酶,1μl的基因组dna进行混匀,并用三蒸水补足至20μl,即可得到pcr反应体系。其中,dntp的终浓度为200μm,上游引物的终浓度为0.25μm,下游引物的终浓度为0.25μm,dna聚合酶的终浓度为2.5units/20μl,基因组dna的终浓度为1μg/20μl。
[0052]
pcr反应的循环条件如表3所示:
[0053]
表3
[0054][0055]
此外,rflp反应体系如下:将1μl含有bsa或不含bsa的10
×
neb缓冲液,0.3units各位点对应的限制性内切酶,3μl上述得到的pcr产物进行混匀,并用三蒸水补足10μl,即可得到rflp反应体系。neb缓冲液可参考现有的限制性内切酶工具书(new england biolabs)。其中,各位点的限制性内切酶孵育条件如表4所示。
[0056]
表4
[0057][0058][0059]
需要说明的是,上述实验所用的试剂、耗材和和限制性内切酶均为市售常见。
[0060]
实施例4
[0061]
该实施例提供了一种上述试剂盒的应用,其中,上述2个位点经上述引物组pcr扩增后,各pcr产物分别利用限制性内切酶xcmi(对应rs17573756位点)和xhoi(对应rs7142555位点)消化pcr产物,便可根据被切断的条带大小判断基因型。具体的,通过提取受试者基因组dna进行snp位点rs17573756和rs7142555的基因分型,其包括以下步骤:
[0062]
s1、基因组dna的提取:抽取受试者外周静脉血2ml,利用现有技术中市售的全血dna提取试剂盒提取外周静脉血中的基因组dna,并置于-20℃保存,备用。
[0063]
s2、snp基因分型:根据上述2个snp位点rs17573756和rs7142555的序列信息,设计聚合酶链式反应(polymerase chain reaction,pcr),并在生物工程有限公司进行引物组的合成,其中引物组的序列与实施例2提供的相同。合成后的引物与上述基因组dna进行pcr反应,可得到pcr产物;接着,将pcr产物与限制性内切酶进行rflp(限制性内切酶片段长度多态性,restriction fragment length polymorphism)反应,得到反应产物;然后,将反应物置于37℃孵育后,再置于聚丙酰胺凝胶或微芯片电泳系统(mce-202multina)中,根据被切断的条带大小来判断基因型。其中,引物组的gc比值、tm值、退火温度、pcr产物长度如上表1所示,被切断的条带大小及其对应的基因型如上表2所示。
[0064]
另外,pcr反应体系如下:将2μl的10
×
pcr缓冲液,1μl的dntp mix,0.4μl各位点对应的上游引物,0.4μl各位点对应的下游引物,0.24μl的hotstartaq dna聚合酶,0.5μl的基因组dna进行混匀,并用三蒸水补足至20μl,即可得到pcr反应体系。其中,dntp的终浓度为100μm,上游引物的终浓度为0.1μm,下游引物的终浓度为0.1μm,dna聚合酶的终浓度为2units/20μl,基因组dna的终浓度为0.5μg/20μl。
[0065]
pcr反应的循环条件如上表3所示。
[0066]
此外,rflp反应体系如下:将1μl含有bsa或不含bsa的10
×
neb缓冲液,0.2units各位点对应的限制性内切酶,2μl上述得到的pcr产物进行混匀,并用三蒸水补足10μl,即可得到rflp反应体系。neb缓冲液可参考现有的限制性内切酶工具书(new england biolabs)。其中,各位点的限制性内切酶孵育条件如上表4所示。
[0067]
需要说明的是,上述实验所用的试剂、耗材和和限制性内切酶均为市售常见。
[0068]
实施例5
[0069]
该实施例提供了一种上述试剂盒的应用,其中,上述2个位点经上述引物组pcr扩增后,各pcr产物分别利用限制性内切酶xcmi(对应rs17573756位点)和xhoi(对应rs7142555位点)消化pcr产物,便可根据被切断的条带大小判断基因型。具体的,通过提取受试者基因组dna进行snp位点rs17573756和rs7142555的基因分型,其包括以下步骤:
[0070]
s1、基因组dna的提取:抽取受试者外周静脉血2ml,利用现有技术中市售的全血dna提取试剂盒提取外周静脉血中的基因组dna,并置于-20℃保存,备用。
[0071]
s2、snp基因分型:根据上述2个snp位点rs17573756和rs7142555的序列信息,设计聚合酶链式反应(polymerase chain reaction,pcr),并在生物工程有限公司进行引物组的合成,其中引物组的序列与实施例2提供的相同。合成后的引物与上述基因组dna进行pcr反应,可得到pcr产物;接着,将pcr产物与限制性内切酶进行rflp(限制性内切酶片段长度多态性,restriction fragment length polymorphism)反应,得到反应产物;然后,将反应物置于37℃孵育后,再置于聚丙酰胺凝胶或微芯片电泳系统(mce-202multina)中,根据被切断的条带大小来判断基因型。其中,引物组的gc比值、tm值、退火温度、pcr产物长度如上表1所示,被切断的条带大小及其对应的基因型如上表2所示。
[0072]
另外,pcr反应体系如下:将2μl的10
×
pcr缓冲液,3μl的dntp mix,2μl各位点对应的上游引物,2μl各位点对应的下游引物,0.36μl的hotstartaq dna聚合酶,3μl的基因组dna进行混匀,并用三蒸水补足至20μl,即可得到pcr反应体系。其中,dntp的终浓度为300μm,上游引物的终浓度为0.5μm,下游引物的终浓度为0.5μm,dna聚合酶的终浓度为3units/20μl,基因组dna的终浓度为3μg/20μl。
[0073]
pcr反应的循环条件如上表3所示。
[0074]
此外,rflp反应体系如下:将1μl含有bsa或不含bsa的10
×
neb缓冲液,0.4units各位点对应的限制性内切酶,4μl上述得到的pcr产物进行混匀,并用三蒸水补足10μl,即可得到rflp反应体系。neb缓冲液可参考现有的限制性内切酶工具书(new england biolabs)。其中,各位点的限制性内切酶孵育条件如上表4所示。
[0075]
需要说明的是,上述实验所用的试剂、耗材和和限制性内切酶均为市售常见。
[0076]
试验例:
[0077]
选取若干名肺癌患者,分别按照上述实施例3提供的方法进行snp位点rs17573756和rs7142555基因型鉴定,并利用excel表格统计病例和对照组的携带危险基因型个数,其中spss22.0统计软件统计携带危险基因型时的危险度和95%的可信区间如表5和附图1所示。
[0078]
表5
[0079][0080]
*adjusted for age,gender,sm,histology,py,stage.
[0081]
ci,confidence interval;or,adjusted odds ratio.
[0082]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1