一种4的制作方法
一种4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐的纯化方法
技术领域
1.本发明涉及农用化学品及制备技术领域,尤其涉及一种4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐的纯化方法。
背景技术:
2.阿维菌素为发酵组分的混合物,共有8个组分:a1a、a1b、a2a、a2b、b1a、b1b、b2a、b2b。通过对阿维菌素进行多次分离纯化可得到阿维菌素b2a/2b。阿维菌素b2a与阿维菌素b2b结构如式(ii)和式(iii)所示:
[0003][0004]
近年来甲氨基阿维菌素b2a/2b逐渐被重视,大量文献报道了甲氨基阿维菌素b2a/2b的合成方法、阿维菌素b2a/2b相关衍生物、以及相关制剂方法。甲氨基阿维菌素b2a苯甲酸盐是其中应用较多的一种物质。但是,目前合成方法制备所得的甲氨基阿维菌素b2a苯甲酸盐的纯度较低,含有较多的杂质,因此,影响后续制剂的杀虫活性。因此,有必要寻求一种收率和纯度较高的甲氨基阿维菌素b2a苯甲酸盐异构体的分离纯化方法。
技术实现要素:
[0005]
针对目前合成方法制备所得的甲氨基阿维菌素b2a苯甲酸盐的纯度较低的问题,本发明提供一种4
″
位为s构型甲氨基阿维菌素b2a苯甲酸盐的纯化方法。
[0006]
为解决上述技术问题,本发明提供的技术方案是:
[0007]
一种4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐的纯化方法,包括以下步骤:
[0008]
将甲氨基阿维菌素b2a/2b苯甲酸盐粗品加入甲基叔丁基醚中,加热溶解,然后滴加叔丁醇和正丁醚混合溶液,滴加结束后降温过滤,将所得滤液降温析晶,得到4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐产品。
[0009]
相对于现有技术,本发明提供的4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐的纯化方法,通过选择甲基叔丁基醚、叔丁醇和正丁醚的混合溶液作为结晶溶剂,并配合两次降温析晶的方式,得到单一构型的含量98%以上的4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐产品,有利于提高其相关制剂的杀虫活性,为后续研发人员开发高活性的甲氨基阿维菌素b2a苯甲酸盐产品提供了可能。
[0010]4″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐的结构式如式(i)所示:
[0011][0012]
本发明中所述s构型指的是反应活性位点4
″
位的甲胺基是s构型。
[0013]
优选的,所述甲基叔丁基醚、叔丁醇和正丁醚的质量比为1:1~1.5:1.5~4。
[0014]
优选的,所述甲氨基阿维菌素b2a/2b苯甲酸盐粗品与甲基叔丁基醚、叔丁醇和正丁醚总量的质量比为1:3~5。
[0015]
优选的结晶溶剂以及溶剂的加入量,有利于去除甲氨基阿维菌素b2a/2b苯甲酸盐粗品中的杂质,并有利于获得高纯度的4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐产品。
[0016]
优选的,降温过滤的温度为0~5℃。
[0017]
优选的降温过滤的温度有利于充分去除甲氨基阿维菌素b2a/2b苯甲酸盐粗品中的氨基阿维菌素b2b苯甲酸盐和其他杂质,从而有利于后续得到高纯度的4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐。
[0018]
优选的,降温析晶的温度为
‑
10~
‑
5℃。
[0019]
优选的,降温析晶的时间为2~3h。
[0020]
优选的,所述叔丁醇和正丁醚混合溶液的滴加时间为1.5~2.5h。
[0021]
优选的降温析晶温度和时间,以及叔丁醇和正丁醚混合溶液的滴加时间,有利于增大4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐与其他物质在体系中的溶解度差异,从而获得高纯度的单一构型的4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐产品。
[0022]
优选的,所述甲氨基阿维菌素b2a/2b苯甲酸盐粗品中甲氨基阿维菌素b2a苯甲酸盐的含量不小于70%。
[0023]
优选的,加热溶解的温度为35~45℃。
[0024]
优选的加热温度有利于使甲氨基阿维菌素b2a/2b苯甲酸盐粗品充分溶解,从而有利于通过降温过滤除去杂质。
[0025]
优选的,采用核磁共振表征所得的1h
‑
nmr、
13
c
‑
nmr、dept135、dept90、cosy、hsqc和hmbc谱图对所得4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐产品进行结构鉴定。
[0026]
本发明采用核磁共振中的1h
‑
nmr、
13
c
‑
nmr、dept135、dept90、cosy、hsqc和hmbc谱图进行综合分析,证明了纯化所得的甲氨基阿维菌素b2a苯甲酸盐为s
‑
构型。
[0027]
本发明提供的甲氨基阿维菌素b2a苯甲酸盐的纯化方法,通过选择甲基叔丁基醚、
叔丁醇和正丁醚的混合溶液作为结晶溶剂,并配合两次降温析晶的方式,得到含量98%以上的4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐产品,产品收率可达62%以上,且纯化方法简单,为后续研发人员开发高活性的甲氨基阿维菌素b2a苯甲酸盐产品提供了可能。
附图说明
[0028]
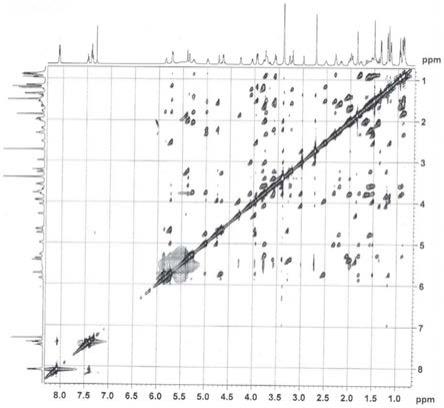
图1为实施例1制备的4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐的noesy谱;
[0029]
图2为图1中noesy谱的局部放大图。
具体实施方式
[0030]
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
[0031]
以下实施例中所用甲氨基阿维菌素b2a/2b苯甲酸盐粗品的含量为70%。
[0032]
实施例1
[0033]
一种4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐的纯化方法,包括以下步骤:
[0034]
将50g甲氨基阿维菌素b2a/2b苯甲酸盐粗品加入50g甲基叔丁基醚中,加热至40℃使其完全溶解,然后缓慢滴加50g叔丁醇和150g正丁醚的混合溶液,滴加时间为2h,滴加结束后降温至0℃过滤,将所得滤液降温至
‑
5℃搅拌析晶3h,过滤,烘干,得到类白色4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐产品22.24g,hplc含量98.5%,收率62.6%。
[0035]
制备所得4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐的核磁谱图解析过程如下:
[0036]
仪器:aviii
‑
500兆核磁共振仪,德国bruker公司,产地:瑞士。
[0037]
溶剂:氘代氯仿。
[0038]
测试条件:常温下,取制备所得4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐溶于适量cdcl3中,在303k温度下,对样品1h
‑
nmr、
13
c
‑
nmr、dept135、dept90、cosy、hsqc、hmbc谱进行测试,结果如图1
‑
图2所示。
[0039]4″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐核磁共振氢谱数据:
[0040]
l
h nmr(400.0mhz):8.13(s,1h),7.55(d,j=6.1,2h),7.45(d,j=7.5,2h),5.43(m,3h),5.00(m,lh),4.76(br d,j=3.0,lh),4.69(m,2h),4.30(br d,j=6.1,lh),4.03(br q,j=6.7,lh),3.98(d,j=6.2,lh),3.94(br s,lh),3.88(m,2h),3.85(s,1h),3.82(dq,j=9.1,6.2,lh),3.74(ddd,j=11.5,5.0,3.8,lh),3.68(s,lh),3.58(m,lh),3.48(dd,j=9.9,1.3,lh),3.398(s,3h),3.395(s,3h),3.38(m,lh),3.32(s,1h),3.30(q,j=2.2,lh),3.23(dd,j=9.1,8.7,lh),2.87(br d,j=3.8,lh),2.67(s,3h),2.52(m,lh),2.31
‑
2.25(m,3h),2.21(dd,j=12.7,5.0,lh),2.05
‑
1.90(m,2h),1.87(br s,3h),1.78(m,lh),1.72(d,j=4.1,2h),1.63
‑
1.46(m,6h),1.49(brs,3h),1.369(d,j=6.7,3h),1.355(d,j=6.7,3h),1.230(d,j=6.2,3h),1.218(d,j=7.0,3h),1.11(d,j=7.6,3h),0.96
‑
0.91(m,9h),0.89(m,1h)。
[0041]4″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐核磁共振碳谱数据:
[0042]
13
c nmr(400.0mhz):174.98,170.30,139.56,138.15,136.31,135.15,133.90,130.50,130.30,130.20,130.10,128.60,128.40,126.03,120.57,118.42,118.13,98.68,
95.90,95.33,81.39,80.99,80.53,79.18,74.99,74.20,71.10,68.62,68.48,68.46,67.83,67.35,65.65,60.58,56.43,55.62,47.50,45.82,41.60,40.55,36.80,36.35,35.20,34.63,34.44,30.83,30.70,27.61,26.27,20.11,18.05,17.56,16.50,15.20,13.11,12.33,12.32。
[0043]
核磁共振氢谱(1h
‑
nmr)中,由于分子式中氢质子个数较多,造成许多氢质子峰交叉重叠。为了验证甲氨基阿维菌素b2a苯甲酸盐结构式中4
″‑
甲胺基所在的含氧六元环中三个甲基的成键方向,下面只归属了相关联的甲基氢和甲基碳,以便确定相关甲基的成键方向,结果如表1
‑
表2所示。
[0044]
表1 氢谱测试结果
[0045]
化学位移(ppm)多重性氢质子数归属1.355,1.369d3h
‑5″
2.723s3h
‑4″
3.398s3h
‑3″
3.395s3h
‑
3'1.218,1.230d3h
‑
5'
[0046]
表2 碳谱测试结果
[0047]
化学位移(ppm)碳类型dept归属17.56伯碳正峰c
‑5″
36.35伯碳正峰c
‑4″
55.62伯碳正峰c
‑3″
56.43伯碳正峰c
‑
3'18.05叔碳正峰c
‑
5'
[0048]
上表中,δ3.398和δ3.395的积分值为3,出峰位置为甲氧基化学位移范畴,故归属为c
‑
3和c
‑
4。氮与氧相比,氮的去屏蔽效应稍弱,即与n相连的甲基应处在甲氧基的高场,δ36.35归属为h
‑4″
,δ1.355和δ1.218均有cosy相关,被相邻ch偶合为双峰,分别与甲氧基有较弱hmbc远程相关,应归属于h
‑5″
和h
‑
5'。
[0049]
核磁共振碳谱(
13
c
‑
nmr)中,δ55.62和δ56.43在dept135为负峰,并在dept90谱图中消失,证明为甲基碳峰,且与h
‑3″
和h
‑
3'有hsqc近程相关,故归属c
‑3″
和c
‑
3'。同理δ17.56、δ18.05和δ36.35均在dept135为负峰,并在dept90中消失,证明为甲基碳峰,且与h
‑5″
、h
‑
5'和h
‑4″
有hsqc近程相关,故依次归属c
‑5″
、c
‑
5'和c
‑
4'。
[0050]
在二维noesy谱中,h
‑4″
与h
‑3″
有相关峰、h
‑4″
与h
‑5″
有相关峰,说明他们之间空间距离小于表明这三个基团在空间上为同一方向,进而证明4
″
位甲胺基为s构型。
[0051]
综合上述分析,证明了本实施例制备所得的产品为4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐。
[0052]
在谱图中并未发现r构型相关出峰。
[0053]
实施例2
[0054]
一种4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐的纯化方法,包括以下步骤:
[0055]
将50g甲氨基阿维菌素b2a/2b苯甲酸盐粗品加入23g甲基叔丁基醚中,加热至45℃
使其完全溶解,然后缓慢滴加35g叔丁醇和92g正丁醚的混合溶液,滴加时间为2h,滴加结束后降温至2℃过滤,将所得滤液降温至
‑
8℃搅拌析晶2.5h,过滤,烘干,得到类白色4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐产品21.97g,hplc含量98.9%,收率62.1%。
[0056]
实施例3
[0057]
一种4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐的纯化方法,包括以下步骤:
[0058]
将50g甲氨基阿维菌素b2a/2b苯甲酸盐粗品加入54g甲基叔丁基醚中,加热至35℃使其完全溶解,然后缓慢滴加65g叔丁醇和81g正丁醚的混合溶液,滴加时间为2h,滴加结束后降温至5℃过滤,将所得滤液降温至
‑
10℃搅拌析晶2h,过滤,烘干,得到类白色4
″‑
(s)
‑
甲氨基阿维菌素b2a苯甲酸盐产品22.34g,hplc含量98.2%,收率62.7%。
[0059]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换或改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1