一种新型哌啶衍生物及其药物用途的制作方法
1.本公开属于医药领域,涉及一种新型哌啶衍生物及其药物用途。
背景技术:
2.作为细胞内信号转导物(第二信使)的3’,5
’‑
环腺苷酸(camp)、3’,5
’‑
环鸟苷酸(cgmp)通过称为磷酸二酯酶(pde)的水解酶类被分别分解为无活性的5
’‑
amp、5
’‑
gmp。使它们失活的pde同工酶不是均匀地存在于生物体内,而是在细胞分布、组织分布等方面显示出差异,以器官的特有位置存在于生物体内。
3.迄今为止已确认存在pde1
‑
pde11的11个种类族(currentopinion in cell biology,12,174
‑
179(2000)),而依据不同的基团编码,pde4家族可以分为4个亚型pde4a、pde4b、pde4c和pde4d,每个亚型又有多个次亚型,如pde4b有3种次亚型。其中以3种pde4亚型pde4a、pde4b和pde4d表达最多,而pde4c表达很少或不表达。pde4b是已知最强的pde4致炎因子,抑制pde4d则与副作用密切相关。
4.已知pde4抑制剂大体分为非选择性pde4抑制剂和选择性pde4抑制剂。
5.非选择性pde4抑制剂如茶碱,虽然茶碱能有效地扩张支气管,但是茶碱的一些不良反应如中枢神经刺激、心律失常和利尿效应等也与腺苷受体拮抗作用有关。
6.选择性pde4抑制剂分为第一代选择性抑制剂如洛利普兰、第二代选择性抑制如罗氟司特、西洛司特和其他选择性抑制,其中罗氟司特除了对pde4c的抑制效稍低外,对pde4a、pde4b和pde4d三种亚型的活性相当。罗氟司特可以降低肺部的炎症、抵抗氧应激、有效的缓解肺部的纤维化、增强粘膜的清除能力以及气道的重塑等等,然后其也存在严重的不良反应,主要表现为腹泻、体重下降、恶心、心房纤颤及精神方面疾病加重等,不良反应发生与pde4抑制剂对不同pde4亚型选择抑制性相关。
7.截止目前,pde4选择性抑制剂仍不能实现绝对的特异性抑制pde4b,极大地限制了该类药物的临床用。另一方面,基于camp进行结构修饰,构建出与camp高度同源性pde4抑制剂,提高pde4抑制剂的选择性,增加药效的同时降低毒副作用是药化研究者所追求的。
8.另外,已知pde4抑制剂专利文献有cn1468219a、cn1203058c、us5602173、us7649095、wo93/19747和wo93/19749等。
技术实现要素:
9.本公开(the disclosure)提供了式(i)所示化合物,
10.或其可药用的盐或其立体异构体、旋转异构体或互变异构体,
11.其中,r1选自氢或腈基;
12.r2选自c3‑7环烷基,所述c3‑7环烷基被卤素或卤代烷基所取代;
13.r3选自烷基、环烷基、杂环基、芳基、杂芳基,所述烷基、烷氧基、环烷基、杂环基、芳基或杂芳基任选被一个或多个选自烷基、烷氧基、环烷基、杂环基、烷氧基、烯基、炔基、芳基、杂芳基、硝基、腈基、羟基或卤素所取代;
14.r4和r5各自独立选自氢、卤素、羟基、烷基、烷氧基、环烷基、杂环基、芳基、杂芳基,所述烷基、烷氧基、环烷基、杂环基、芳基或杂芳基任选被一个或多个选自烷基、烷氧基、环烷基、杂环基、烷氧基、烯基、炔基、芳基、杂芳基、硝基、腈基、羟基、卤素所取代,或者,r4、r5与其相邻碳原子一起形成5元至12元碳环、杂环、芳环或杂芳环,优选6元至8元碳环、杂环、芳环或杂芳环,所述碳环、杂环、芳环或杂芳环任选被选自烷基、卤素、羟基、氨基、氧代基、羧基、硝基、氰基、烷氧基、环烷基、杂环基、芳基和杂芳基中的一个或多个取代基所取代;
15.r6选自羟基、烷基、烷氧基、环烷基、杂环基、芳基、杂芳基或
‑
nhoh基,所述烷基、烷氧基、环烷基、杂环基、芳基或杂芳基任选被一个或多个选自烷基、烷氧基、环烷基、杂环基、烷氧基、烯基、炔基、芳基、杂芳基、硝基、腈基、羟基或卤素所取代;
16.x为亚甲基,所述亚甲基任选被一个或多个选自卤素、羟基、烷基、烷氧基或环烷基所取代;
17.n、m=1
‑
4的整数(包括1、2、3或4)。
18.一些实施方案提供式(i)所示化合物中r6选自羟基、c1‑8烷基(例如甲基、乙基、异丙基、苯基、被c1‑4烷基所取代的苯基等)、c1‑8烷氧基(例如甲氧基、乙氧基、异丙基氧等)或
‑
nhoh基,所述c1‑8烷基或c1‑8烷氧基任选被选自芳基、杂芳基中的一个或多个取代基所取代。
19.在一些实施方案中,式(i)所示化合物如下所示:
[0020][0021]
其中,r1~r5、m如式(i)化合物中所定义,
[0022]
一些实施方案提供式(i)所示化合物中r2为被1
‑
3氟原子取代的c3‑7环烷基。
[0023]
一些实施方案提供式(i)所示化合物中r2为卤代烷基所取代的c3‑7环烷基,所述卤代烷基为二氟甲基、三氟甲基或1,1
‑
二氟乙基。
[0024]
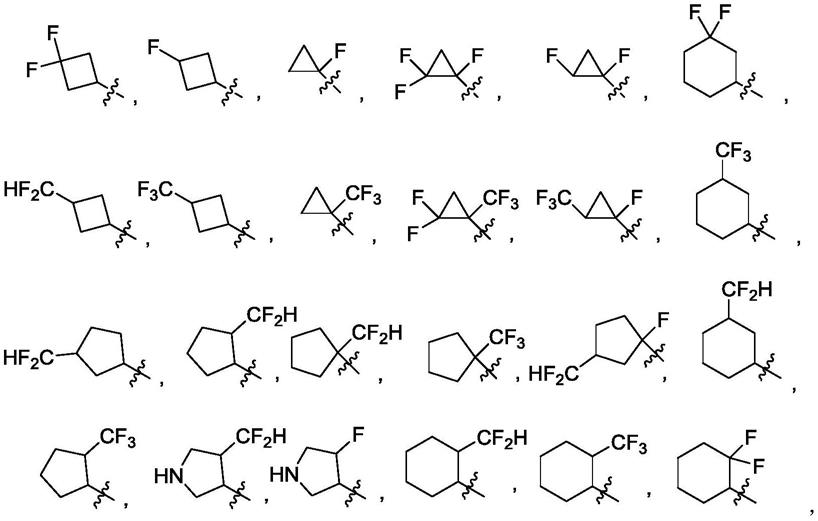
一些实施方案提供式(i)所示化合物中r2选自但不限于:
[0025][0026]
进一步地,其可以在环碳原子上任选且独立地被选自c1‑6烷基(包括甲基、乙基、异丙基等)、c1‑6烷基氧基(包括甲氧基、乙氧基、异丙氧基等)、c3‑7环烷基(包括环丙烷基、环戊烷基、环己烷基等)所取代,可以在环氮原子上任选且独立地被选自c1‑6烷基、
‑
cor'、
‑
s(o)2r'、
‑
con(r')2、c3‑7环烷基所取代,
[0027]
r'选自氢、羟基、烷基(例如c1‑8烷基)、烷氧基(例如c1‑8烷氧基)、酰基(c3‑6烷酰基,包括但不限于乙酰基、甲酰基)、芳基(例如苯基、甲基苯基)或杂芳基(例如吡啶基),所述烷基、烷氧基、芳基或杂芳基任选被一个或多个选自卤素(如氟、氯或溴)、烷基(例如c1‑8烷基,包括不限于甲基、乙基或异丙基)、环烷基(例如c3‑7环烷基,包括但不限于环丙基或环戊基)、烷氧基(例如c1‑8烷氧基,包括但不限于甲氧基、乙氧基、异丙基氧等)、氧基、羟基、硝基、腈基所取代。
[0028]
另一方面,一些实施方案提供式(i)所示化合物中r3选自c1‑8烷基(例如甲基、乙基或异丙基)或c3‑7环烷基(例如环丙基或环戊基),所述c1‑8烷基或c3‑7环烷基任选被一个或多个选自c1‑8烷基(例如甲基、乙基或异丙基)、c3‑7环烷基(例如环丙基或环戊基)、卤素(如氟、氯或溴)、c1‑8烷氧基(例如甲氧基、乙氧基、异丙基氧等)、c3‑7杂环基(例如派啶基、吡咯基)、芳基(如苯基、甲基苯基)或杂芳基(如吡啶基)中的一个或多个取代基所取代。
[0029]
在一些实施方案中,式(i)所示化合物中r3选自二氟甲基、三氟甲基、1,1
‑
二氟乙基。
[0030]
在一些实施方案中,式(i)化合物如下所示:
[0031][0032]
其中,r1~r2,r4~r5、m如式(i)化合物中所定义。
[0033]
另一些实施方案提供式(i)所示化合物中r4和r5各自独立选自氢、c1‑8烷基(例如甲基、乙基、异丙基、苯基、被c1‑4烷基所取代的苯基等),或者r4、r5与其相邻碳原子一起形成6元至8元碳环或杂环,所述碳环或杂环任选被选自烷基(例如甲基、乙基、异丙基)、卤素(如氟、氯或溴)、羟基(
‑
oh)、硝基、氰基、烷氧基(如c1‑8烷氧基,包括不限于甲氧基、乙氧基、异丙基氧等)中的一个或多个取代基所取代。
[0034]
在一些实施方案中,式(i)所示化合物中r4和r5选自氢。
[0035]
在一些实施方案中,式(i)所示化合物中r4和r5各自独立选自甲基、乙基或异丙基,所述甲基、乙基或异丙基任选被卤素所取代,如氟、氯或溴。
[0036]
在一些实施方案中,式(i)所示化合物中r4和r5与其相邻碳原子一起形成6元至8元碳环,包括但限于环丙烷基、环丁烷基、环戊烷基。
[0037]
式(i)所示典型化合物,包括但不限于:
[0038]
[0039][0040]
或其可药用的盐或其立体异构体、旋转异构体或互变异构体。
[0041]
在一些实施方案中,本公开提供式(i)所示化合物选自:
[0042]
或其可药用的盐。
[0043]
本公开中还提供了一种药物组合物,包括至少一种治疗有效量的前述式(i)所示化合物或其可药用的盐或其立体异构体、旋转异构体或互变异构体以及药学上可接受的载体、稀释剂或赋形剂。
[0044]
在一些实施方案中,所述的药物组合物的单位剂量为0.001mg
‑
1000mg。
[0045]
在某些实施方式中,基于组合物的总重量,所述的药物组合物含有0.01
‑
99.99%的前述化合物。在某些实施方式中,所述的药物组合物含有0.1
‑
99.9%的前述化合物。在某些实施方式中,所述的药物组合物含有0.5%
‑
99.5%的前述化合物。在某些实施方式中,所述的药物组合物含有1%
‑
99%的前述化合物。在某些实施方式中,所述的药物组合物含有2%
‑
98%的前述化合物。
[0046]
在某些实施方式中,基于组合物的总重量,所述的药物组合物含有0.01%
‑
99.99%的药学上可接受的载体、稀释剂或赋形剂。在某些实施方式中,所述的药物组合物含有0.1%
‑
99.9%的药学上可接受的载体、稀释剂或赋形剂。在某些实施方式中,所述的药物组合物含有0.5%
‑
99.5%的药学上可接受的载体、稀释剂或赋形剂。在某些实施方式中,所述的药物组合物含有1%
‑
99%的药学上可接受的载体、稀释剂或赋形剂。在某些实施方式中,所述的药物组合物含有2%
‑
98%的药学上可接受的载体、稀释剂或赋形剂。
[0047]
另一方面,本公开中还提供了一种治疗或预防气喘、阻塞性肺病、败血病、肾炎、糖尿病、变应性鼻炎、变应性结膜炎、溃疡性肠炎或风湿病疾病的方法,其通过向所述患者施用治疗有效量的前述式(i)所示化合物或前述的药物组合物。
[0048]
进一步地,所述气喘、阻塞性肺病、败血病、肾炎、糖尿病、变应性鼻炎、变应性结膜炎、溃疡性肠炎或风湿病等疾病是与磷酸二酯酶4(pde4)相关的。
[0049]
本公开中还提供了一种治疗或预防与pde4相关疾病的方法,其通过向所述患者施用治疗有效量的前述式(i)所示化合物或前述的药物组合物。
[0050]
在一些实施方案中,与pde4相关疾病包括有炎症性疾病(气喘、阻塞性肺病、败血
病、肾炎等)、糖尿病、变应性疾病(变应性鼻炎、变应性结膜炎等)、自体免疫疾病(溃疡性肠炎、风湿病)等。
[0051]
本公开中还涉及上述方案中所述化合物或前述的药物组合物在制备治疗或预防气喘、阻塞性肺病、败血病、肾炎、糖尿病、变应性鼻炎、变应性结膜炎、溃疡性肠炎或风湿病疾病的疾病的药物中的用途。
[0052]
进一步地,所述气喘、阻塞性肺病、败血病、肾炎、糖尿病、变应性鼻炎、变应性结膜炎、溃疡性肠炎或风湿病等疾病是与磷酸二酯酶4(pde4)相关的。
[0053]
本公开中还涉及上述方案中所述化合物或前述的药物组合物在制备治疗或预防与pde4相关疾病的药物中的用途。
[0054]
在一些实施方案中,与pde4相关疾病包括有炎症性疾病(气喘、阻塞性肺病、败血病、肾炎等)、糖尿病、变应性疾病(变应性鼻炎、变应性结膜炎等)、自体免疫疾病(溃疡性肠炎、风湿病)等。
[0055]
另一方面,本公开中所述化合物可药用盐选自无机盐或有机盐,本公开所述化合物与酸如三氟乙酸反应成相应盐,所述酸选自但不限于乙酸、盐酸、水杨酸、苹果酸、抗坏血酸、磷酸、柠檬酸、苯甲酸或富马酸。
[0056]
在一些实施方案中,式(i)所示化物的可药用盐为其盐酸盐。
[0057]
本公开化合物可以存在特定的几何或立体异构体形式。本公开设想所有的这类化合物,包括顺式和反式异构体、(
‑
)
‑
和(+)
‑
对对映体、(r)
‑
和(s)
‑
对映体、非对映异构体、(d)
‑
异构体、(l)
‑
异构体,及其外消旋混合物和其他混合物,例如对映异构体或非对映体富集的混合物,所有这些混合物都属于本公开的范围之内。烷基等取代基中可存在另外的不对称碳原子。所有这些异构体以及它们的混合物,均包括在本公开的范围之内。本公开的含有不对称碳原子的化合物可以以光学活性纯的形式或外消旋形式被分离出来。光学活性纯的形式可以从外消旋混合物拆分,或通过使用手性原料或手性试剂合成。
[0058]
可以通过的手性合成或手性试剂或者其他常规技术制备光学活性的(r)
‑
和(s)
‑
异构体以及d和l异构体。如果想得到本公开某化合物的一种对映体,可以通过不对称合成或者具有手性助剂的衍生作用来制备,其中将所得非对映体混合物分离,并且辅助基团裂开以提供纯的所需对映异构体。或者,当分子中含有碱性官能团(如氨基)或酸性官能团(如羧基)时,与适当的光学活性的酸或碱形成非对映异构体的盐,然后通过本领域所公知的常规方法进行非对映异构体拆分,然后回收得到纯的对映体。此外,对映异构体和非对映异构体的分离通常是通过使用色谱法完成的,所述色谱法采用手性固定相,并任选地与化学衍生法相结合(例如由胺生成氨基甲酸盐)。
[0059]
本公开所述化合物的化学结构中,键表示未指定构型,即如果化学结构中存在手性异构体,键可以为或或者同时包含和两种构型。
[0060]
另一方面,本公开所述化合物的官能团中氢被氘代,获得相应氘代化合物,氘代化合物保留了与氢类似物相当的选择性和潜力;氘键更稳定,使得“adme”即“毒药物动力学”不同,从而提供临床上有益效果。
[0061]
毒药物动力学,指机体对外源化学物的吸收(absorption)、分布(distribution)、代谢(metabolism)及排泄(excretion)过程。制备式i所示化合物的方法
[0062]
根据有机合成领域技术人员已知的方法,由已知或容易制备的起始原料制备式i
所示的化合物制备式i所示的化合物的方法如下所示,并概括在下面的方案中。对于有机合成领域的技术人员来说,替代的合成途径和类似结构是显而易见。
[0063]
方案:
[0064][0065]
术语解释:
[0066]“可药用载体、稀释剂或赋形剂”包括但不限于任何已经被美国食品和药物管理局批准对于人类或家畜动物使用可接受的任何助剂、载体、赋形剂、助流剂、甜味剂、稀释剂、防腐剂、染料/着色剂、增香剂、表面活性剂、润湿剂、分散剂、助悬剂、稳定剂、等渗剂、溶剂或乳化剂。
[0067]“烷基”指饱和的脂族烃基团,包括1至20个碳原子的直链和支链基团。优选含有1至12个碳原子的烷基,更优选含有1至6个碳原子的烷基。非限制性实施例包括甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、仲丁基、正戊基、1,1
‑
二甲基丙基、1,2
‑
二甲基丙基、2,2
‑
二甲基丙基、1
‑
乙基丙基、2
‑
甲基丁基、3
‑
甲基丁基,及其各种支链异构体等。烷基可以是取代的或未取代的,当被取代时,取代基可以在任何可使用的连接点上被取代,优选为一个或多个以下基团,独立地选自烷基、烷氧基、环烷基、杂环基、烯基、炔基、芳基、杂芳基、硝基、腈基、羟基或卤素所取代。
[0068]“烯基”包括具有2至12个碳原子的支链和直链烯烃或含有脂族烃基团的烯烃。例如“c2‑6烯基”表示具有2、3、4、5或6个碳原子的烯基。烯基的实例包括但不限于,乙烯基、烯丙基、1
‑
丙烯基、1
‑
丁烯基、2
‑
丁烯基、3
‑
丁烯基、2
‑
甲基丁
‑2‑
烯基、3
‑
甲基丁
‑1‑
烯基、1
‑
戊烯基、3
‑
戊烯基及4
‑
己烯基。烯基可以是取代的或未取代的,当被取代时,取代基可以在任何可使用的连接点上被取代,优选为一个或多个以下基团,独立地选自烷基、烷氧基、环烷基、杂环基、烯基、炔基、芳基、杂芳基、硝基、腈基、羟基或卤素所取代。
[0069]
术语“环烷基”指饱和或部分不饱和单环或多环环状烃取代基,环烷基环包含3至20个碳原子,优选包含3至12个碳原子,更优选包含3至6个碳原子。单环环烷基的非限制性实例包括环丙基、环丁基、环戊基、环戊烯基、环己基、环己烯基、环己二烯基、环庚基、环庚
三烯基、环辛基等;多环环烷基包括螺环、稠环和桥环的环烷基。
[0070]
所述环烷基环可以稠合于芳基、杂芳基或杂环烷基环上,其中与母体结构连接在一起的环为环烷基,非限制性实例包括茚满基、四氢萘基、苯并环庚烷基等。环烷基可以是任选取代的或非取代的,当被取代时,取代基优选为一个或多个以下基团,其独立地选自烷基、卤素、羟基、氨基、氧代基、羧基、硝基、氰基、烷氧基、环烷基、杂环基、芳基和杂芳基。
[0071]
术语“杂环基”指饱和或部分不饱和单环或多环环状烃取代基,其包含3至20个环原子,其中一个或多个环原子为选自氮、氧或s(o)
m
(其中m是整数0至2)的杂原子,但不包括―o―o―、―o―s―或―s―s―的环部分,其余环原子为碳。优选包含3至12个环原子,其中1~4个是杂原子;更优选包含3至8个环原子。单环杂环基的非限制性实例包括吡咯烷基、咪唑烷基、四氢呋喃基、四氢噻吩基、二氢咪唑基、二氢呋喃基、二氢吡唑基、二氢吡咯基、哌啶基、哌嗪基、吗啉基、硫代吗啉基、高哌嗪基等。多环杂环基包括螺环、稠环和桥环的杂环基。“杂环基”非限制性实例包括:
[0072][0072]
等等。
[0073]
所述杂环基环可以稠合于芳基、杂芳基或环烷基环上,其中与母体结构连接在一起的环为杂环基,其非限制性实例包括:
[0074]
等。
[0075]
杂环烷基的环碳原子可以被氧代(官能化为羰基)。这种杂环烷基的示例性实例是:.
[0076][0077]
术语“5至8元单环环烷基”是指具有5至8个环原子的单环环烷基,包括5元、6元、7元或8元环原子。术语“5至8元单环杂环烷基”是指具有5至8个环原子的单环杂环烷基,包括5元、6元、7元或8元环原子,至少一个环原子选自除碳原子以外的,如氮、氧或硫。术语“8至12元双环环烷基”是指具有8至12个环原子的双环环烷基,包括8元、10元或12元环原子。术语“8至12元双环杂环烷基”是指具有8至12个环原子的双环杂环烷基,包括8元、10元或12元环原子,至少一个环原子选自除碳原子以外的,如氮、氧或硫。除非另有说明,环烷基、杂环烷基可以被取代的。
[0078]
杂环基可以是任选取代的或非取代的,当被取代时,取代基优选为一个或多个以下基团,其独立地选自烷基、卤素、羟基、氨基、氧代基、羧基、硝基、氰基、烷氧基、环烷基、杂
环基、芳基和杂芳基。
[0079]“炔基”包括具有2至12个碳原子的支链和直链炔基或含有脂族烃基的烯烃,或若规定指定碳原子数,则意指该特定数目。例如乙炔基、丙炔基(例如1
‑
丙炔基、2
‑
丙炔基)、3
‑
丁炔基、戊炔基、己炔基及1
‑
甲基戊
‑2‑
炔基。
[0080]
术语“芳基”指具有共轭的π电子体系的6至14元全碳单环或稠合多环(也就是共享毗邻碳原子对的环)基团,优选为6至12元,例如苯基和萘基。所述芳基环可以稠合于杂芳基、杂环基或环烷基环上,其中与母体结构连接在一起的环为芳基环,其非限制性实例包括:
[0081][0082]
芳基可以是取代的或非取代的,当被取代时,取代基优选为一个或多个以下基团,其独立地选自烷基、卤素、羟基、氨基、氧代基、氧基、羧基、硝基、氰基、烷氧基、环烷基、杂环基、芳基和杂芳基,优选苯基。
[0083]
术语“杂芳基”指包含1至4个杂原子、5至14个环原子的杂芳族体系,其中杂原子选自氧、硫和氮。杂芳基优选为6至12元,更优选为5元或6元。例如。其非限制性实例包括:咪唑基、呋喃基、噻吩基、噻唑基、吡唑基、噁唑基、吡咯基、四唑基、吡啶基、嘧啶基、吡嗪,噻二唑等等。
[0084]
所述杂芳基环可以稠合于芳基、杂环基或环烷基环上,其中与母体结构连接在一起的环为杂芳基环,其非限制性实例包括:
[0085][0086]
杂芳基可以是任选取代的或非取代的,当被取代时,取代基优选为一个或多个以下基团,其独立地选自烷基、卤素、羟基、氨基、氧代基、羧基、硝基、氰基、烷氧基、环烷基、杂环基、芳基和杂芳基。
[0087]
术语“烷氧基”指―o―(烷基)和―o―(非取代的环烷基),其中烷基的定义如上所述。烷氧基的非限制性实例包括:甲氧基、乙氧基、丙氧基、丁氧基、环丙氧基、环丁氧基、环戊氧基、环己氧基。烷氧基可以是任选取代的或非取代的,当被取代时,取代基优选为一个或多个以下基团,其独立地选自烷基、卤素、羟基、氨基、氧代基、羧基、硝基、氰基、烷氧基、
环烷基、杂环基、芳基和杂芳基。
[0088]
术语“卤代烷基”是指被一个或多个如上文定义的卤素原子取代的如上定义的烷基。优选地,卤代烷基可以是单卤代烷基、二卤代烷基或包括全卤代烷基的多卤代烷基。单卤代烷基可以具有一个碘原子、溴原子、氯原子或氟原子。二卤代烷基和多卤代烷基可被两个或更多个相同的卤素原子或不同的卤素原子的组合所取代。除非有相反的阐述或叙述,本公开所描述或要求保护的所有卤代烷基可以是直链的或支链的,取代的或未取代的。
[0089]
术语“羟基”指
‑
oh基团。
[0090]
术语“卤素”指氟、氯、溴或碘。
[0091]
术语“氨基”指
‑
nh2。
[0092]
术语“氰基”指
‑
cn。
[0093]
术语“硝基”指
‑
no2。
[0094]
术语“氧代基”指=o取代基。
[0095]“任选”或“任选地”意味着随后所描述地事件或环境可以但不必发生,该说明包括该事件或环境发生或不发生地场合。例如,“任选被烷基取代的杂环基团”意味着烷基可以但不必须存在,该说明包括杂环基团被烷基取代的情形和杂环基团不被烷基取代的情形。
[0096]“取代的”指基团中的一个或多个氢原子,优选为最多5个,更优选为1~3个氢原子彼此独立地被相应数目的取代基取代。不言而喻,取代基仅处在它们的可能的化学位置,本领域技术人员能够在不付出过多努力的情况下确定(通过实验或理论)可能或不可能的取代。例如,具有游离氢的氨基或羟基与具有不饱和(如烯属)键的碳原子结合时可能是不稳定的。
[0097]
本领域已知其在合成过程期间保护反应基团(包括而不限于羟基和氨基)免于副反应。用保护基保护的羟基和氨基在本文中分别称为“保护的羟基”和“保护的氨基”。保护基通常选择性地和/或正交性地使用以在其他反应性位点反应期间保护位点且然后可以被除去而留下无保护的基团保持原状或参与进一步的反应。如本领域已知的保护基一般描述在greene and wuts,protective groups in organic synthes is,3rd edition,john wiley&sons,new york(1999)中。“羟基保护基”的实例包括但不限于叔丁基、叔
‑
丁氧基甲基、甲氧基甲基、四氢吡喃基、1
‑
乙氧基乙基、1
‑
(2
‑
氯乙氧基)乙基、2
‑
三甲基甲硅烷基乙基、对
‑
氯苯基、2,4
‑
二硝基苯基、苄基、2,6
‑
二氯苄基、二苯基
‑
甲基、对
‑
硝基苄基、三苯基甲基、三甲基甲硅烷基、三乙基甲硅烷基、叔丁基二甲基甲硅烷基、叔丁基
‑
二苯基甲硅烷基(tbdps)、三苯基甲硅烷基、苯甲酰基甲酸酯、乙酸酯、氯乙酸酯、三氯乙酸酯、三氟乙酸酯、特戊酸酯(pivaloate)、苯甲酸酯、对
‑
苯甲酸苯酯、9
‑
芴基甲基碳酸酯、甲磺酸酯和甲苯磺酸酯。“氨基保护基”的实例包括但不限于氨基甲酸酯保护基,比如2
‑
三甲基
‑
甲硅烷基乙氧基羰基(teoc)、1
‑
甲基
‑1‑
(4
‑
联苯基)
‑
乙氧基
‑
羰基(bpoc)、叔
‑
丁氧基羰基(boc)、烯丙氧基羰基(al loc)、9
‑
芴基甲基氧基羰基(fmoc)和苄基氧基羰基(cbz);酰胺保护基,比如甲酰基、乙酰基、三氯乙酰基、苯甲酰基和硝基苯基乙酰基;磺酰胺
‑
保护基,比如2
‑
硝基苯磺酰基;和亚胺和环状亚胺保护基,比如苯二甲酰亚氨基和二硫杂丁二酰基。
[0098]“药物组合物”表示含有一种或多种本文所述化合物或其生理学上可药用的盐或前体药物与其他化学组分的混合物,以及其他组分例如生理学可药用的载体和赋形剂。药物组合物的目的是促进对生物体的给药,利于活性成分的吸收进而发挥生物活性。
[0099]
本公开中化合物可以含有一个或多个不对称中心,因此可以产生对映异构体、非对映异构体、及可以根据绝对立体化学定义为(r)
‑
或(s)
‑
或用于氨基酸的(d)
‑
或(l)
‑
的其它立体异构形式。本公开包括所有可能异构体以及其外消旋的和光学纯的形式。光学活性的(+)和(
‑
)、(r)
‑
和(s)
‑
或(d)
‑
和(l)
‑
异构体可以使用手性合成子或手性试剂制备,或者可以使用常规方法例如色谱法和分级结晶制备。用于制备/分离各个对映体的常规方法包括从合适的的光学纯前体手性合成或使用例如手性高压液相色谱法(hplc)的外消旋物(或盐或衍生物的外消旋物)拆分。当本文描述的化合物含有烯双键或其它几何不对称性中心,除非另有说明,否则其意味着所述化合物包括e和z几何异构体。而且,所有的互变异构形式也意味着包括在内。
[0100]“立体异构体”指通过相同的键键合但具有不同的三维结构的相同原子组成的化合物,其不可互换。本公开中预期各种立体异构体及其混合物,并且包括“对映异构体”,其指其分子彼此为不能重叠的镜像的两种立体异构体。
[0101]“互变异构体”指质子从分子的一个原子转移到同一分子的另一个原子。本公开中包括任何所述化合物的互变异构体。
具体实施方式
[0102]
以下结合实施例进一步描述本公开中,但这些实施例并非限制本公开中的范围。
[0103]
本公开中实施例中未注明具体条件的实验方法,通常按照常规条件,或按照原料或商品制造厂商所建议的条件。未注明具体来源的试剂,为市场购买的常规试剂。
[0104]
化合物的结构是通过核磁共振(nmr)或/和质谱(ms)来确定的。nmr位移(δ)以10
‑6(ppm)的单位给出。nmr的测定是用bruker avance
‑
400核磁仪,测定溶剂为氘代二甲基亚砜(dmso
‑
d6),氘代氯仿(cdcl3),氘代甲醇(methanol
‑
d4),内标为四甲基硅烷(tms)。
[0105]
hplc的测定使用waters 2795 allianceht lc高压液相色谱仪,waters 2996 photodiode array detector紫外检测器,thermo accucore polar premium c18 50*4.6mm 2.6um色谱柱。
[0106]
ms的测定用waters micromass quattro micro api三重四级杆质谱仪,以正/负离子模式扫描,质量扫描范围为120~1300。
[0107]
薄层层析硅胶板使用烟台黄海hsgf254硅胶板,薄层色谱法(tlc)使用硅胶板采用规格是0.2mm
±
0.03mm,薄层层析分离纯化产品采用的规格是0.4mm
‑
0.5mm。
[0108]
快速柱纯化系统使用combiflash rf150(teledyne isco)或者isolara one(biotage)。
[0109]
正向柱层析一般使用烟台黄海硅胶200~300目或300~400目硅胶为载体,或者使用常州三泰预填预填超纯正相硅胶柱(40
‑
63μm,60g,24g,40g,120g或其它规格)。
[0110]
本公开中的已知的起始原料可以采用或按照本领域已知的方法来合成,或可购买自上海泰坦科技,abcr gmbh&co.kg,acros organics,aldrich chemical company,韶远化学科技(accela chembio inc),毕得医药等公司。
[0111]
实施例中无特殊说明,反应能够均在氮气氛下进行。
[0112]
氮气氛是指反应瓶连接一个约1l容积的氮气气球。
[0113]
氢气氛是指反应瓶连接一个约1l容积的氢气气球。
[0114]
氢气是由上海全浦科学仪器公司qph
‑
1l型氢气发生仪制得。
[0115]
氮气氛或氢化氛通常抽真空,充入氮气或氢气,反复操作3次。
[0116]
实施例中无特殊说明,溶液是指水溶液。
[0117]
实施例中无特殊说明,反应的温度为室温,为20℃~30℃。
[0118]
实施例中的反应进程的监测采用薄层色谱法(tlc),反应所使用的展开剂,纯化化合物采用的柱层析的洗脱剂的体系和薄层色谱法的展开剂体系包括:a:二氯甲烷/甲醇体系,b:正庚烷/乙酸乙酯体系,c:石油醚/乙酸乙酯体系,溶剂的体积比根据化合物的极性不同而进行调节,也可以加入少量的三乙胺和醋酸等碱性或酸性试剂进行调节。
[0119]
下面简写词的使用贯穿本发明:
[0120]
下面简写词的使用贯穿本发明:
[0121]
dmso
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
二甲基亚砜
[0122]
dmf
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
二甲基甲酰胺
[0123]
dipea
ꢀꢀꢀꢀꢀꢀꢀꢀ
n,n
‑
二异丙基乙基胺
[0124]
hobt
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ1‑
羟基苯并三唑
[0125]
edci
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ1‑
乙基
‑
3(3
‑
二甲基丙胺)碳二亚胺
[0126]
thf
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
四氢呋喃
[0127]
tmscn
ꢀꢀꢀꢀꢀꢀꢀꢀ
三甲基氰硅烷
[0128]
pph3ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三苯基膦
[0129]
ni(cod)2ꢀꢀꢀꢀꢀ
双
‑
(1,5
‑
环辛二烯)镍
[0130]
实施例
[0131]
关键中间体的制备
[0132]
中间体3
‑
(苄氧基)
‑4‑
(二氟甲氧基)苯甲醛(1)的制备
[0133]4‑
(二氟甲氧基)
‑3‑
羟基苯甲醛(37.60g,200.0mmol)溶于四氢呋喃(200ml)中,室温下先后加入碳酸钾(55.28g,400.0mmol)及溴化苄(44.19g,260.0mmol),70℃搅拌至反应完毕,冷却,过滤,滤液减压浓缩,再经硅胶柱层析(正庚烷/乙酸乙酯体系=5:1)得到中间体1(52.89g,收率95.1%),无色油状物,ms(esi)m/z 279.1[m+h]
+
。
[0134]
中间体(3
‑
(苄氧基)
‑4‑
(二氟甲氧基)苯基)甲醇(2)的制备
[0135]
中间体3
‑
(苄氧基)
‑4‑
(二氟甲氧基)苯甲醛(1,52.89g,190.2mmol)溶于甲醇(250ml),0℃下分批加入硼氢化钠(7.20g,190.2mmol),0℃搅拌至反应完毕,加入饱和氯化铵溶液淬灭反应,乙酸乙酯萃取,饱和氯化钠溶液洗涤,无水硫酸钠干燥,过滤,滤液减压浓缩,再经硅胶柱层析(正庚烷/乙酸乙酯体系=2:1)得到中间体2(49.23g,收率92.4%),无色油状物,ms(esi)m/z 281.1[m+h]
+
。
[0136]
中间体2
‑
(3
‑
(苄氧基)
‑4‑
(二氟甲氧基)苯基)乙腈(3)的制备
[0137]
中间体(3
‑
(苄氧基)
‑4‑
(二氟甲氧基)苯基)甲醇(2,28.00g,100.0mmol)溶于二氯甲烷(150ml),室温下缓慢滴加氯化亚砜(16.65g,140.0mmol),室温搅拌至反应完毕,减压浓缩得到中间体3。中间体3溶于无水甲苯(150ml)中,室温氮气保护下分别加入tmscn(39.68,400.0mmol),pph3(5.24g,20.0mmol)和ni(cod)2(5.50g,20.0mmol),60℃搅拌反应,冷却,减压浓缩,再经硅胶柱层析(正庚烷/乙酸乙酯体系=2:1)得到中间体3(26.25g,收率90.8%),白色固体粉末,ms(esi)m/z 290.2[m+h]
+
。
[0138]
中间体4
‑
(3
‑
(苄氧基)
‑4‑
(二氟甲氧基)苯基)
‑4‑
氰基哌啶
‑1‑
甲酸叔丁酯(4)的制备
[0139]
中间体2
‑
(3
‑
(苄氧基)
‑4‑
(二氟甲氧基)苯基)乙腈(3,26.25g,90.8mmol)溶于n,n
‑
二甲基甲酰胺(250ml),0℃下分批加入60%氢钠(5.45g,227.0mmol),搅拌0.5小时,接着加入n,n
‑
双(2
‑
氯乙基)氨基甲酸叔丁酯(32.98g,136.2mmol),缓慢升到室温继续搅拌至反应完毕,加入饱和氯化铵溶液淬灭反应,乙酸乙酯萃取,合并有机相,饱和氯化钠溶液洗涤,无水硫酸钠干燥,过滤,滤液减压浓缩,再经硅胶柱层析(正庚烷/乙酸乙酯体系=2:1)得到中间体4(31.54g,收率75.8%),白色固体粉末,ms(esi)m/z 459.2[m+h]
+
。
[0140]
中间体4
‑
(3
‑
(苄氧基)
‑4‑
甲氧基苯基)
‑4‑
氰基哌啶
‑1‑
甲酸叔丁酯(5)的制备
[0141]
参照中间体4的合成方法,以2
‑
(3
‑
(苄氧基)
‑4‑
甲氧基苯基)乙腈为原料得到中间体5(收率76.3%),白色固体粉末,ms(esi)m/z 423.5[m+h]
+
。
[0142]
中间体2
‑
(4
‑
(3
‑
(苄氧基)
‑4‑
(二氟甲氧基)苯基)
‑4‑
氰基哌啶
‑1‑
基)乙酸乙酯(6)的制备
[0143]
中间体4
‑
(3
‑
(苄氧基)
‑4‑
(二氟甲氧基)苯基)
‑4‑
氰基哌啶
‑1‑
甲酸叔丁酯(4,31.54g,68.8mmol)溶于二氯甲烷(300ml),室温下缓慢滴加三氟乙酸(67ml),室温搅拌0.5小时,反应液减压浓缩得到固体。将固体溶于乙腈(300ml),室温分别加入溴乙酸乙酯(22.84g,137.6mmol)和碳酸钾(38.04g,275.2mmol),搅拌至反应完毕,过滤,滤液减压浓缩,再经硅胶柱层析(正庚烷/乙酸乙酯体系=2:1)得到中间体5(26.92g,收率88.1%),白色固体粉末,ms(esi)m/z 445.2[m+h]
+
。
[0144]
中间体2
‑
(4
‑
(3
‑
(苄氧基)
‑4‑
甲氧基苯基
‑4‑
氰基哌啶
‑1‑
基)乙酸乙酯(7)的制备
[0145]
参照中间体6的合成方法,以中间体5为原料得到中间体7(收率85.7%),白色固体粉末,ms(esi)m/z 409.2[m+h]
+
。
[0146]
中间体2
‑
(4
‑
氰基
‑4‑
(4
‑
(二氟甲氧基)
‑3‑
羟基苯基)哌啶
‑1‑
基)乙酸乙酯(8)的制备
[0147]
中间体2
‑
(4
‑
(3
‑
(苄氧基)
‑4‑
(二氟甲氧基)苯基)
‑4‑
氰基哌啶
‑1‑
基)乙酸乙酯(6,26.92g,60.6mmol)溶于甲醇(300ml),室温下加入10%钯碳(2.69g),1atm下搅拌至反应完毕,过滤,滤液减压浓缩,再经硅胶柱层析(二氯甲烷/甲醇体系=20:1)得到中间体6(18.45g,收率85.7%),白色固体粉末,ms(esi)m/z 355.3[m+h]
+
。
[0148]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
羟基
‑4‑
甲氧基苯基)哌啶
‑1‑
基)乙酸乙酯(9)的制备
[0149]
参照中间体8的合成方法,以中间体7为原料得到中间体9(收率88.2%),白色固体粉末,ms(esi)m/z 319.4[m+h]
+
。
[0150]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
((3,3
‑
二氟环丁基)甲氧基)
‑4‑
(二氟甲氧基)苯基)哌啶
‑1‑
基)乙酸乙酯(10)的制备
[0151]
中间体2
‑
(4
‑
氰基
‑4‑
(4
‑
(二氟甲氧基)
‑3‑
羟基苯基)哌啶
‑1‑
基)乙酸乙酯(8,1.78g,5.0mmol)溶于n,n
‑
二甲基甲酰胺(15ml),室温下分别加入1
‑
(3,3
‑
二氟环丁基)
‑4‑
甲基苯磺酸甲酯(2.07g,7.5mmol)和碳酸钾(2.10g,15.0mmol),100℃搅拌至反应完毕,冷却,加入饱和氯化钠溶液淬灭反应,乙酸乙酯萃取,合并有机相,饱和氯化钠溶液洗涤,无水硫酸钠干燥,过滤,滤液减压浓缩,再经硅胶柱层析(正庚烷/乙酸乙酯体系=5:1)得到中间体10(2.05g,收率88.5%),无色油状物,ms(esi)m/z 459.2[m+h]
+
。
[0152]
中间体(11):2
‑
(4
‑
氰基
‑4‑
(4
‑
(二氟甲氧基)
‑3‑
((1
‑
氟环丙基)甲氧基)苯基)哌啶
‑1‑
基)乙酸乙酯的制备
[0153]
参照中间体10的合成方法,以中间体8和4
‑
甲基
‑1‑
氟环丙基苯磺酸甲酯为原料得到中间体11(收率72.1%),无色油状物,ms(esi)m/z 427.2[m+h]
+
。
[0154]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
(2
‑
环丙基乙氧基)
‑4‑
(二氟甲氧基)苯基)哌啶
‑1‑
基)乙酸乙酯(12)的制备
[0155]
参照中间体10的合成方法,以中间体8和4
‑
甲基苯磺酸
‑2‑
环丙基乙酯为原料得到中间体12(收率95.3%),无色油状物,ms(esi)m/z 423.5[m+h]
+
。
[0156]
中间体2
‑
(4
‑
氰基
‑4‑
(4
‑
(二氟甲氧基)
‑3‑
(4
‑
苯氧基丁氧基)苯基)哌啶
‑1‑
基)乙酸乙酯(13)的制备
[0157]
参照中间体10的合成方法,以中间体8和4
‑
溴丁氧基苯为原料得到中间体13(收率91.9%),无色油状物,ms(esi)m/z 503.6[m+h]
+
。
[0158]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
(((1
‑
氟环丙基)甲氧基)
‑4‑
甲氧基苯基)哌啶
‑1‑
基)乙酸乙酯(14)的制备
[0159]
参照中间体10的合成方法,以中间体9和4
‑
甲基
‑1‑
氟环丙基苯磺酸甲酯为原料得到中间体14(收率89.1%),无色油状物,ms(esi)m/z 391.5[m+h]
+
。
[0160]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
(((3,3
‑
二氟环丁基)甲氧基)
‑4‑
甲氧基苯基)哌啶
‑1‑
基)乙酸乙酯(15)的制备
[0161]
参照中间体10的合成方法,以中间体9和1
‑
(3,3
‑
二氟环丁基)
‑4‑
甲基苯磺酸甲酯为原料得到中间体15(收率90.4%),无色油状物,ms(esi)m/z 423.4[m+h]
+
。
[0162]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
((3,3
‑
二氟环丁基)甲氧基)
‑4‑
(二氟甲氧基)苯基)哌啶
‑1‑
基)乙酸(16)的制备
[0163]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
((3,3
‑
二氟环丁基)甲氧基)
‑4‑
(二氟甲氧基)苯基)哌啶
‑1‑
基)乙酸乙酯(10,2.05g,4.5mmol)溶于甲醇/四氢呋喃/水混合溶液中(150ml,v
甲醇
/v
四氢呋喃
/v
水
=3:1:1),室温下加入氢氧化锂(0.95g,22.5mmol),搅拌至反应完毕,减压浓缩至无甲醇和四氢呋喃,接着加水至固体溶解后加入1n hcl溶液至ph=3,过滤,滤饼干燥得到中间体16(1.75g,收率90.3%),白色固体粉末。
[0164]1h nmr(400mhz,dmso
‑
d6)δ7.32(d,j=2.2hz,1h),7.30
‑
7.25(m,1h),7.19(dd,j=8.4,2.2hz,1h),7.09(s,0.43h),6.91(s,0.20h),4.19(d,j=5.7hz,2h),3.36(s,2h),3.11(d,j=12.0hz,2h),2.80
‑
2.53(m,8h),2.29
‑
2.05(m,3h)。ms(esi)m/z 429.4[m
‑
h]
+
。
[0165]
中间体2
‑
(4
‑
氰基
‑4‑
(4
‑
(二氟甲氧基)
‑3‑
((1
‑
氟环丙基)甲氧基)苯基)哌啶
‑1‑
基)乙酸(17)的制备
[0166]
参照中间体16的合成方法,以中间体11为原料得到中间体17(收率87.5%),白色固体粉末。
[0167]1h nmr(400mhz,dmso
‑
d6)δ7.35
‑
7.27(m,2h),7.20(dd,j=8.4,2.2hz,1h),7.13(s,0.47h),6.94(s,0.22h),4.47(d,j=22.6hz,2h),3.21(s,2h),3.10
‑
3.00(m,2h),2.67
‑
2.54(m,2h),2.16
‑
2.10(m,4h),1.25
‑
1.07(m,2h),1.01
‑
0.81(m,2h)。ms(esi)m/z 397.3[m
‑
h]
+
。
[0168]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
(2
‑
环丙基乙氧基)
‑4‑
(二氟甲氧基)苯基)哌啶
‑1‑
基)乙
酸(18)的制备
[0169]
参照中间体16的合成方法,以中间体12为原料得到中间体18(收率90.7%),白色固体粉末,1h nmr(400mhz,dmso
‑
d6)δ7.33
‑
7.22(m,2h),7.15(dd,j=8.4,2.2hz,1h),7.09(s,0.45h),6.91(s,0.21h),4.18(t,j=6.5hz,2h),3.28(s,2h),3.28
‑
3.02(m,2h),2.67
‑
2.60(m,2h),2.21
‑
2.04(m,4h),1.68(q,j=6.6hz,2h),0.94
‑
0.80(m,1h),0.52
‑
0.41(m,2h),0.21
‑
0.12(m,2h)。ms(esi)m/z 393.4[m
‑
h]
+
。
[0170]
中间体2
‑
(4
‑
氰基
‑4‑
(4
‑
(二氟甲氧基)
‑3‑
(4
‑
苯氧基丁氧基)苯基)哌啶
‑1‑
基)乙酸(19)的制备
[0171]
参照中间体16的合成方法,以中间体13为原料得到中间体19(收率95.1%),白色固体粉末,1h nmr(400mhz,dmso
‑
d6)δ7.37
‑
7.22(m,4h),7.16(dd,j=8.4,2.1hz,1h),7.11(s,0.45h),6.99
‑
6.89(m,3h),4.19(d,j=5.8hz,2h),4.10
‑
4.03(m,2h),3.28(s,2h),3.16
‑
2.96(m,2h),2.66
‑
2.62(m,2h),2.20
‑
2.01(m,4h),1.94
‑
1.88(m,4h)。ms(esi)m/z 473.2[m
‑
h]
+
。
[0172]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
(((1
‑
氟环丙基)甲氧基)
‑4‑
甲氧基苯基)哌啶
‑1‑
基)乙酸(20)的制备
[0173]
参照中间体16的合成方法,以中间体14为原料得到中间体20(收率83.4%),白色固体粉末。
[0174]1h nmr(400mhz,dmso
‑
d6)δ7.11(dd,j=6.3,2.3hz,2h),7.07
‑
7.03(m,1h),4.34(d,j=22.7hz,2h),3.82(s,3h),3.27(s,2h),3.10
‑
3.00(m,3h),2.66
‑
2.58(m,2h),2.17
‑
1.97(m,4h),1.21
‑
1.06(m,2h),0.95
‑
0.84(m,2h)。ms(esi)m/z 361.4[m
‑
h]
+
。
[0175]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
(((3,3
‑
二氟环丁基)甲氧基)
‑4‑
甲氧基苯基)哌啶
‑1‑
基)乙酸(21)的制备
[0176]
参照中间体16的合成方法,以中间体15为原料得到中间体21(收率86.1%),白色固体粉末。
[0177]1h nmr(400mhz,methanol
‑
d4)δ7.20
‑
7.07(m,3h),4.17(d,j=6.9hz,2h),4.05(s,2h),3.86(s,3h),3.55
‑
3.45(m,1h),2.85
‑
2.80(m,2h),2.80
‑
2.68(m,2h),2.65
‑
2.55(m,4h),2.55
‑
2.35(m,4h)。ms(esi)m/z 393.3[m
‑
h]
+
。
[0178]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
((3,3
‑
二氟环丁基)甲氧基)
‑4‑
(二氟甲氧基)苯基)哌啶
‑1‑
基)
‑
n
‑
(2
‑
甲氧基丙烷
‑2‑
基)氧基乙酰胺(22)的制备
[0179]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
((3,3
‑
二氟环丁基)甲氧基)
‑4‑
(二氟甲氧基)苯基)哌啶
‑1‑
基)乙酸(16,1.75g,4.1mmol)溶于n,n
‑
二甲基甲酰胺(60ml),室温下分别加入o
‑
(2
‑
甲氧基丙烷
‑2‑
基)羟胺(0.78g,6.2mmol),hobt(1.11g,8.2mmol),edci(1.57g,8.2mmol)和dipea(2.65g,20.5mmol),搅拌至反应完毕,加入饱和氯化钠溶液淬灭反应,乙酸乙酯萃取3次,合并有机相,饱和氯化钠溶液洗涤,无水硫酸钠干燥,过滤,滤液减压浓缩,再经硅胶柱层析(乙酸乙酯体系)得到中间体22(1.26g,收率59.8%),无色油状物,ms(esi)m/z 518.5[m+h]
+
。
[0180]
中间体2
‑
(4
‑
氰基
‑4‑
(4
‑
(二氟甲氧基)
‑3‑
((1
‑
氟环丙基)甲氧基)苯基)哌啶
‑1‑
基)
‑
n
‑
(((2
‑
甲氧基丙烷
‑2‑
基)氧基)乙酰胺(23)的制备
[0181]
参照中间体22的合成方法,以中间体17为原料得到中间体23(收率62.1%),无色
油状物,ms(esi)m/z 486.5[m+h]
+
。
[0182]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
(2
‑
环丙基乙氧基)
‑4‑
(二氟甲氧基)苯基)哌啶
‑1‑
基)
‑
n
‑
((2
‑
甲氧基丙烷
‑2‑
基)氧基)乙酰胺(24)的制备
[0183]
参照中间体22的合成方法,以中间体18为原料得到中间体24(收率65.6%),无色油状物,ms(esi)m/z 482.5[m+h]
+
。
[0184]
中间体2
‑
(4
‑
氰基
‑4‑
(4
‑
(二氟甲氧基)
‑3‑
(4
‑
苯氧基丁氧基)苯基)哌啶
‑1‑
基)
‑
n
‑
((2
‑
甲氧基丙烷
‑2‑
基)氧基)乙酰胺(25)的制备
[0185]
参照中间体22的合成方法,以中间体19为原料得到中间体25(收率84.3%),无色油状物,ms(esi)m/z 562.6[m+h]
+
。
[0186]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
(((1
‑
氟环丙基)甲氧基)
‑4‑
甲氧基苯基)哌啶
‑1‑
基)
‑
n
‑
((2
‑
甲氧基丙烷
‑2‑
基)氧基)乙酰胺(26)的制备
[0187]
参照中间体22的合成方法,以中间体20为原料得到中间体26(收率73.8%),无色油状物,ms(esi)m/z 450.2[m+h]
+
。
[0188]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
((3,3
‑
二氟环丁基)甲氧基)
‑4‑
甲氧基苯基)哌啶
‑1‑
基)
‑
n
‑
((2
‑
甲氧基丙烷
‑2‑
基)氧基)乙酰胺(27)的制备
[0189]
参照中间体22的合成方法,以中间体21为原料得到中间体27(收率70.8%),无色油状物,ms(esi)m/z 482.5[m+h]
+
。
[0190]
实施例1:2
‑
(4
‑
氰基
‑4‑
(3
‑
((3,3
‑
二氟环丁基)甲氧基)
‑4‑
(二氟甲氧基)苯基)哌啶
‑1‑
基)
‑
n
‑
羟基乙酰胺盐酸盐
[0191][0192]
中间体2
‑
(4
‑
氰基
‑4‑
(3
‑
((3,3
‑
二氟环丁基)甲氧基)
‑4‑
(二氟甲氧基)苯基)哌啶
‑1‑
基)
‑
n
‑
(2
‑
甲氧基丙烷
‑2‑
基)氧基乙酰胺(22,1.26g,2.4mmol)溶于乙醇(20ml),室温下滴加2n hcl溶液(20ml),搅拌至反应完毕,过滤,滤饼干燥得到目标化合物1(0.74g,收率69.4%)。
[0193]1h nmr(400mhz,dmso
‑
d6)δ7.43
‑
7.26(m,2h),7.24
‑
7.10(m,1.35h),6.95(s,0.17h),4.40(s,0.43h),4.19(d,j=5.7hz,2h),4.02(s,1h),3.87
‑
3.57(m,2h),2.85
‑
2.53(m,10h)。
[0194]
ms(esi)m/z 446.2[m+h]
+
。
[0195]
实施例2:2
‑
(4
‑
氰基
‑4‑
(4
‑
(二氟甲氧基)
‑3‑
((1
‑
氟环丙基)甲氧基)苯基)哌啶
‑1‑
基)
‑
n
‑
羟基乙酰胺盐酸盐
[0196][0197]
参照实施例1的合成方法,以中间体23为原料得到目标化合物2(收率85.8%)。
[0198]1h nmr(400mhz,dmso
‑
d6)δ7.40
‑
7.30(m,2h),7.25
‑
7.15(m,1.46h),6.98(s,
0.23h),4.53
‑
4.38(m,2h),4.11
‑
3.61(m,5h),3.46
‑
3.29(m,2h),1.21
‑
1.13(m,2h),0.94
‑
0.89(m,2h)。
[0199]
ms(esi)m/z 414.3[m+h]
+
。
[0200]
实施例3:2
‑
(4
‑
氰基
‑4‑
(3
‑
(((1
‑
氟环丙基)甲氧基)
‑4‑
甲氧基苯基)哌啶
‑1‑
基)
‑
n
‑
羟基乙酰胺
[0201][0202]
参照实施例1的合成方法,以中间体26为原料得到目标化合物5(收率69.8%)。
[0203]1h nmr(400mhz,methanol
‑
d4)δ7.37(d,j=2.3hz,1h),7.32(d,j=8.4hz,1h),7.25(dd,j=8.5,2.3hz,1h),6.86(t,j=75.0hz,1h),4.53
‑
4.41(m,3h),4.09(s,1h),4.00
‑
3.80(m,2h),3.70
‑
3.48(m,2h),2.68
‑
2.48(m,4h),1.26
‑
1.14(m,2h),0.96
‑
0.91(m,2h)。
[0204]
ms(esi)m/z 378.4[m+h]
+
。
[0205]
实施例4:2
‑
(4
‑
氰基
‑4‑
(3
‑
((3,3
‑
二氟环丁基)甲氧基)
‑4‑
甲氧基苯基)哌啶
‑1‑
基)
‑
n
‑
羟基乙酰胺
[0206][0207]
参照实施例1的合成方法,以中间体27为原料得到目标化合物6(收率70.1%)。
[0208]1h nmr(400mhz,methanol
‑
d4)δ7.32(d,j=8.2hz,2h),7.23(dd,j=8.5,2.3hz,1h),6.81(t,j=74.5hz,1h),4.45(s,0.59h),4.21(d,j=5.3hz,2h),4.08(s,1h),4.00
‑
3.80(m,2h),3.70
‑
3.50(m,2h),2.83
‑
2.65(m,3h),2.65
‑
2.50(m,6h)。
[0209]
ms(esi)m/z 410.1[m+h]
+
。
[0210]
生物学评价
[0211]
以下结合测试例进一步描述解释本公开中,但这些测试例并非意味着限制本公开中的范围。
[0212]
测试例1体外pde4b酶活性检测实验:基于imap fp的分析方法检测
[0213]
1、实验材料
[0214]
材料品牌货号/型号pde4b1bps60041trequinsinsigmat2057384
‑
well plateperkin elmer6007279imap fp ipp explorer kitmolecular devicesr8124
[0215]
2、实验步骤
[0216]
将化合物用dmso进行5倍的梯度稀释得到其不同的浓度(10000nm,2000nm,400nm,80nm,16nm,3.2nm,0.64nm,0.128nm,0.0256nm,0.005nm)。取200μl不同浓度的化合物加到
384孔板中(n=2),并同时加入2份200μl dmso到384孔板中(n=2)作为空白对照;接着向384孔板中加入10μl 0.025μg/ml pde4b1酶溶液(用1mm的5*imap reaction buffer和1mm的dtt配制),及向其中一份空白对照中加入10μl不含pde4b1酶的空白buffer,室温震荡孵育15分钟,接着向其中加入10μl 0.1μm fam
‑
camp溶液(用1mm的5*imap reaction buffer和1mm的dtt配制),室温震荡孵育30分钟后加入60μl检测溶液(用0.5625mm的5*imap progressive binding buffer a,0.1875mm的5*imap progressive binding buffer b和0.75mm的beads配制),室温震荡孵育60分钟后搜集数据。抑制率计算公式是:抑制率=m/(m
‑
m
control
)*100;根据浓度和抑制率拟合曲线计算出ic
50
值。本实验用罗氟斯特和an
‑
2728作为阳性对照。
[0217]
本公开的实施例在体外对pde4b1酶活性抑制通过以上的试验进行测定,测得的ic
50
值见表1。
[0218]
表1
[0219][0220]
测试例2细胞体外活性实验:利用lps诱导pbmc细胞,检测tnf
‑
α释放
[0221]
1、实验材料
[0222]
材料品牌货号/型号lpssigmal4391human tnf
‑
αelisa kitneobioscienceehc103a.96celltiter
‑
glo cell viability assaypromegag7572多功能酶标仪perkinelmerenvision 2105自动细胞计数仪上海睿钰countstar medical台式冷冻离心机thermost40r二氧化碳培养箱thermo3111生物安全柜escoac2
‑
6s1显微镜olympusckx53
[0223]
2、实验步骤
[0224]
取10μl不同浓度的化合物(10mm,1mm,0.1mm,0.01mm,0.001mm,0.0001mm,0.00001mm)dmso溶液用pbmc完全培养基(rpmi 1640medium+10%灭活的fbs+1*penicillin streptomycin)稀释10倍,dmso作为空白对照。将新鲜的pbmc 400g离心7分钟,弃上清,用14ml pbmc完全培养基重悬至细胞密度为1.25e6/ml,取160μl加入到96孔板中(n=2),接着
加入20μl不同浓度的化合物稀释液,震荡混均,37℃孵育1小时,接着加入20μl lps(40ng/ml),混匀,37℃孵育18小时。细胞培养结束后,400g离心5分钟,取100μl上清液加入到96孔板中,
‑
80℃保存,待测tnf
‑
α的含量。剩余的细胞加入100μl celltiter
‑
glo试剂,室温下400g离心10分钟,利用envision读取数值来计算细胞的存活率。
[0225]
取20μl复苏后的细胞上清液加入到96孔板中(n=2),加入140μl标准品稀释液,标准品稀释液作为空白对照,标准品作为标准对照,封住板子,37℃孵育90分钟,洗板5次,加入100μl生物素化抗体工作液(空白孔加生物素化抗体稀释液),封住板子,37℃孵育60分钟,洗板5次,加入100μl酶结合物工作液(空白孔加酶结合物稀释液),封住板子,37℃孵育30分钟,洗板5次,加入100μl显色底物tmb,避光37℃孵育15分钟,接着加入100μl反应终止液,震荡混匀,利用酶标仪读取od
450
值。本实验用罗氟斯特和an
‑
2728作为阳性对照。
[0226]
本公开的实施例对lps诱导的pbmc细胞的tnf
‑
α释放的影响通过以上的试验进行测定,测得的ic
50
值见表2。
[0227]
表2
[0228]
编号ic
50
(nm)an
‑
2728470.6罗氟司特1.004实施例10.636实施例20.384实施例32.189实施例42.641
[0229]
测试例3细胞体外活性实验:利用prostaglandin e2诱导抑制后的pbmc细胞,检测camp的含量
[0230]
1、实验材料
[0231][0232][0233]
2、实验步骤
[0234]
取10μl不同浓度的化合物(10mm,1mm,0.1mm,0.01mm,0.001mm,0.0001mm,0.00001mm)dmso溶液用pbmc完全培养基(rpmi 1640medium+10%灭活的fbs+1*penicillin streptomycin)稀释10倍,dmso作为空白对照。将新鲜的pbmc 400g离心7分钟,弃上清,用
14ml pbmc完全培养基重悬至细胞密度为1.25e6/ml,取160μl加入到96孔板中(n=2),接着加入20μl不同浓度的化合物稀释液,震荡混均,37℃孵育1小时,接着加入20μl peg2(100μm),混匀,37℃孵育1小时,细胞培养结束后,400g离心5分钟,取10μl上清液加入到384孔板中(n=2),接着加入5μl的anti
‑
camp
‑
cryptate工作液(1.1ml的ddh2o溶解anti
‑
camp
‑
cryptate进行配制),再次加入5μl的camp
‑
d2工作液(1.1ml的ddh2o溶解camp
‑
d2进行配制),封住板子,室温孵育1小时,读取665nm和620nm波长下的数值。本实验用罗氟斯特和an
‑
2728作为阳性对照。
[0235]
测得的ic
50
值见表3。
[0236]
表3
[0237]
编号ic
50
(μm)an
‑
272831.66罗氟司特0.0977实施例10.36实施例21.95实施例30.11实施例40.13
[0238]
结论:本公开的实施例在细胞实验中都展现了与阳性化合物罗氟司特相当或者好的生物活性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1