一种检测APOE和SLCO1B1基因多态性位点的引物、探针及其试剂盒的制作方法
本发明涉及基因检测
技术领域:
,更具体地,涉及一种检测apoe和slco1b1基因多态性位点的引物、探针及其试剂盒。
背景技术:
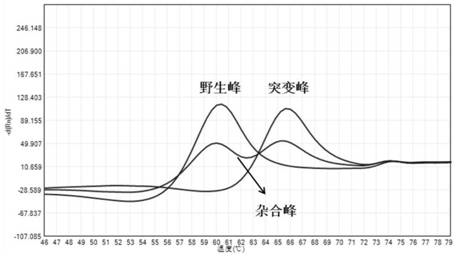
:近30年来,中国人群的血脂水平逐步升高,血脂异常患病率明显增加。《中国居民营养与慢性病状况报告(2015年)》显示,中国成人血脂异常总体患病率高达40.40%。《中国成人血脂异常防治指南(2016年修订版)》指出ldl-c是调脂治疗干预的首要靶点,降低ldl-c水平可显著减少ascvd的发病及死亡危险。他汀类药物可通过抑制hmg-coa还原酶活性来减少胆固醇的合成,有研究表明,他汀类药物可降低55%的ldl-c的水平,降低20-30%的心血管事件,ascvd一级和二级预防中均能显著降低心血管事件风险,是防治此类疾病最为重要的药物。而他汀类药物是临床使用疗效和不良反应个体差异较大的药物,这些个体差异与药物基因多态性有关,apoe和slco1b1基因则是近年来研究最多的热点基因。apoe通过多种途径参与机体的脂质代谢调节,是影响机体血脂水平的重要内在因素。apoe多态性被认为是高脂蛋白血症及动脉粥样硬化性血管病的易感候选基因,可以形成3种单倍型分别是apoe3(388t-526c)、apoe2(388t-526t)、apoe4(388c-526c),其中apoe4携带者患冠心病的风险要高40%,并且他汀类药物对apoe4携带者疗效往往不佳或无疗效,而对apoe2携带者的降脂作用最强。slco1b1编码的oatp1b1有机阴离子转运多肽,是运输他汀类药物进入肝脏的主要运载蛋白,slco1b1的基因多态性会影响他汀类药物的血药浓度。slco1b1*5基因型能够减少他汀转运到肝脏的水平,而使他汀类药物的血药浓度增加,从而增加他汀的不良反应,导致横纹肌溶解和肌病的风险增加。因此,cpic药物遗传学指南和国家卫计委颁布的《药物代谢酶和药物作用靶点基因检测技术指南(试行)》中指出:slco1b1和apoe基因多态性影响他汀类药物的代谢水平,医生可根据其基因多态性,指导病人他汀类服用剂量,降低发生肌病的风险。目前针对基因多态性的检测方法主要包括:高分辨率熔解曲线法、芯片法、荧光pcr法、snpshot法、直接测序法。其中,高分辨率熔解曲线法对设备的温度分辨率要求较高,各个样品孔间的差异必须小于0.1℃,而大部分常规的定量pcr仪孔间温度差异在0.3℃~0.5℃之间,常规定量pcr仪器无法胜任高分辨率熔解曲线(hrm)的分析,临床推广困难;芯片法操作复杂,耗时长,且自动化程度较低;普通荧光pcr法由于荧光通道的限制,检测通量受限,且现有同类试剂盒一管混合液仅检测一个位点的一种基因型,操作繁琐;snpshot和直接测序法需要使用测序仪,该仪器昂贵,难以推广普及。因此,目前亟需开发一种准确度高、成本低的apoe和slco1b1基因多态性位点检测试剂盒。技术实现要素:本发明的目的是为了克服现有技术中对基因多态性位点检测的不足,提供一种检测成本低、检测时间短、特异性强,不同基因型区分度高的apoe和slco1b1基因多态性位点检测试剂盒。本发明的第一个目的是提供一种检测apoe基因多态性位点的引物组。本发明的第二个目的是提供一种检测slco1b1基因多态性位点的引物组。本发明的第三个目的是提供一种检测apoe基因多态性位点的探针。本发明的第四个目的是提供一种检测slco1b1基因多态性位点的探针。本发明的第五个目的是提供以上任一所述引物组和/或探针在制备apoe和/或slco1b1基因多态性位点的检测试剂盒中的应用。本发明的第六个目的是提供一种apoe和/或slco1b1基因多态性位点检测试剂盒。为了实现上述目的,本发明是通过以下技术方案予以实现的:本发明提供一种检测apoe基因多态性位点的引物组,包括:检测位点apoec.388t>c的引物组,其核苷酸序列如seqidno.1~2所示;检测位点apoec.526c>t的引物组,其核苷酸序列如seqidno.3~4所示。一种检测slco1b1基因多态性位点的引物组,包括:检测位点slco1b1c.521t>c的引物组,其核苷酸序列如seqidno.5~6所示;检测位点slco1b1c.388a>g的引物组,其核苷酸序列如seqidno.7~8所示。优选地,以上所述引物组分为上游引物和下游引物,上游引物的核苷酸序列为seqidno.1、seqidno.3、seqidno.5、seqidno.7;下游引物的核苷酸序列为seqidno.2、seqidno.4、seqidno.6、seqidno.8。更优选地,以上所述序列如seqid1~8所示的引物的长度在16~28bp之间。进一步更优选地,以上所述序列如seqid1~8所示的引物的长度优选在20~24bp之间。一种检测apoe基因多态性位点的探针,包括:检测位点apoec.388t>c的探针,其核苷酸序列如seqidno.9所示;检测位点apoec.526c>t的探针,其核苷酸序列如seqidno.10所示。一种检测slco1b1基因多态性位点的探针,包括:检测位点slco1b1c.521t>c的探针,其核苷酸序列如seqidno.11所示;检测位点slco1b1c.388a>g的探针,其核苷酸序列如seqidno.12所示。优选地,以上所述序列如seqidno.9~12所示的探针的长度在16~24bp之间。更优选地,以上所述序列如seqidno.9~12所示的探针的长度优选在20~22bp之间。优选地,以上所述探针的5’端由fam、rox、vic或cy5中的任意一种荧光基团所修饰,3’端由bhq1或bhq2中的任意一种淬灭基团所修饰。更优选地,检测位点apoec.388t>c的探针的5’端由fam荧光基团所修饰,3’端由bhq1淬灭基团所修饰;检测位点apoec.526c>t的探针的5’端由rox荧光基团所修饰,3’端由bhq2淬灭基团所修饰;检测位点slco1b1c.521t>c的探针的5’端由vic荧光基团所修饰,3’端由bhq2淬灭基团所修饰;检测位点slco1b1c.388a>g的探针的5’端由cy5荧光基团所修饰,3’端由bhq2淬灭基团所修饰。以上所述引物组和/或所述探针在制备apoe和/或slco1b1基因多态性位点的检测试剂盒中的应用,也属于本发明的保护范围。本发明还要求保护一种apoe和/或slco1b1基因多态性位点检测试剂盒,包含以上所述引物组和所述探针。优选地,所述检测试剂盒包括pcr反应液、taq酶、质控品对照质粒。优选地,所述检测试剂盒,pcr反应液包括pcr扩增缓冲液、0.1~1μm以上所述引物组、0.1μm以上所述探针、1×gcbuffer、ddh2o。更优选地,pcr反应液中的引物组,上游引物为0.1μm,下游引物为1μm。优选地,质控品对照质粒包括野生型apoe基因的质粒和突变型apoe基因的质粒、野生型slco1b1基因的质粒和突变型slco1b1基因的质粒。优选地,质控品对照质粒的浓度为1×105copies/μl。与现有技术相比,本发明具有如下有益效果:(1)本发明的基因多态性位点检测试剂盒采用熔解曲线法,与传统的荧光pcr法相比,节省了一半的探针,操作简单,仅用4个探针就可以一管检测四个基因位点,检测成本低、检测时间短、特异性强、重复性好,检测的最低检测限为1ng/μl,且同一位点不同基因型之间区分度高(野生型和突变型对应的熔解峰的tm值差异大于5)。(2)本发明的基因多态性位点检测试剂盒采用普通荧光pcr仪即可满足,且操作简便,同一反应管中检测两个基因、一个待检测位点的8种型别,可更快出结果;同一通道、不同型别间的熔解峰对应的tm值差异大于5℃,易于区分判断;搭配自动判读软件,检测结果易判读;操作过程均为闭管反应,显著降低污染,保证结果真实可信;该检测试剂盒通过对apoe和slco1b1基因多态性位点的检测,不但可以用于预测疾病风险和健康管理,也可指导他汀类药物的合理使用。附图说明图1为apoe基因位点apoec.388t>c基因扩增熔解曲线结果。图2为apoe基因位点apoec.526c>t基因扩增熔解曲线结果。图3为slco1b1基因位点slco1b1c.521t>c基因扩增熔解曲线结果。图4为slco1b1基因位点slco1b1c.388a>g基因扩增熔解曲线结果。具体实施方式下面结合说明书附图和具体实施例对本发明作出进一步地详细阐述,所述实施例只用于解释本发明,并非用于限定本发明的范围。下述实施例中所使用的试验方法如无特殊说明,均为常规方法;所使用的材料、试剂等,如无特殊说明,为可从商业途径得到的试剂和材料。实施例1apoe和slco1b1基因多态性位点检测试剂盒一、检测试剂盒的制备1、引物和探针设计针对apoe基因的c.526c>t、c.388t>c位点和slco1b1基因的c.388a>g、c.521t>c位点设计各自的引物和探针,其序列如表2所示:表1检测apoe和slco1b1基因多态性位点的引物和探针2、质控品质粒的制备质控品对照质粒包括apoe基因野生型质粒和apoe基因突变型质粒、slco1b1基因野生型质粒和slco1b1基因突变型质粒,具体成分如表2所示:表2质控品组成其制备方法如下:(1)收集apoec.526c>t、apoec.388t>c和slco1b1c.388a>g、slco1b1c.521t>c4个基因位点的野生型、纯合突变型的临床样本,采用凯普血液基因组dna提取试剂盒提取dna,具体操作参照试剂盒内所提供的说明书。(2)分别取2μl以上dna为模板,采用对应的引物对(seqidno.1~8)进行扩增。(3)使用omega胶回收试剂盒对pcr产物进行切胶回收,将纯化后的pcr产物与pmdvector于16℃连接2小时。(4)取连接产物10μl转化大肠杆菌dh5α感受态细胞,涂lb(amp+)平板,37℃培养过夜。(5)转化好的培养皿上挑取白色单菌落接种于5mllb(amp+)液体培养基的试管中,37℃过夜培养。(6)细菌培养好以后,利用omega质粒提取试剂盒提取质粒dna,并溶于te缓冲液中,并进行凝胶电泳检测,紫外分光光度法测定浓度,然后用te缓冲液将其稀释,分装后置于-15℃以下保存。(7)将提取的质粒dna进行测序,确定所得质粒型别正确。3、试剂盒的组成一种简单、快速、准确度高的apoe和slco1b1基因多态性位点检测试剂盒,可以一管同时检测apoec.526c>t、apoec.388t>c和slco1b1c.388a>g、slco1b1c.521t>c基因位点;该试剂盒主要组成如表3所示:表3试剂盒主要组成成分及含量其中,pcr反应液的组成为:dntps、缓冲液、以上设计的引物和探针,反应液各组分的终浓度及含量具体如表4所示:表4pcr反应液各组分终浓度及含量各组分名称终浓度pcr扩增缓冲液1×dntps(datp、dgtp、dctp、dttp)375μmseqidno.10.1μmseqidno.21μmseqidno.90.1μmseqidno.30.1μmseqidno.41μmseqidno.100.1μmseqidno.50.1μmseqidno.61μmseqidno.110.1μmseqidno.70.1μmseqidno.81μmseqidno.120.1μmgcbuffer1×ddh2o/二、apoe和slco1b1基因多态性位点检测试剂盒的使用方法1、检测样本准备(标本制备区)(1)取静脉全血、口腔拭子临床样本,参考所购买的商用基因组dna提取试剂盒说明书的操作进行dna提取。(2)取2μl抽提好的dna样本作为模板进行pcr扩增;剩余dna样品存储于-15℃以下备用,冻融次数不超过5次。2、扩增试剂准备(试剂准备区)(1)从制备好的检测试剂盒中取出pcr反应液,室温下避光解冻,上下颠倒混匀后,6000转/分钟离心10秒;从试剂盒中取出dna聚合酶,6000转/分钟离心10秒;取17μlpcr反应液和1μldna聚合酶混合配制成18μl的扩增试剂。(2)将配制好的扩增试剂充分混匀,6000转/分钟离心1分钟,向pcr反应管中加入18μl配制好的扩增试剂,转移到样品处理区。3、加样(标本制备区)(1)在pcr反应管中分别加入处理好的样本dna、野生型对照、突变型对照各2μl,盖紧管盖,稍做离心(反应总体积为24μl/人份)。(2)转移到检测区,放入相应的荧光pcr检测仪内,记录样本摆放顺序。4、pcr扩增与熔解曲线分析(扩增区)扩增与熔解曲线分析步骤程序的设定见表5,荧光信号采集通道为fam通道、vic通道、rox通道和cy5通道。以上海宏石slan-96s的检测模式为标准熔解曲线,以rochelightcycler480ii的检测模式为monocolorhydrolysisprobe/uplprobe。表5扩增程序的设定5、检测结果的判定(1)参考范围以表6中的各tm值的常见值作为参考值(在上海宏石slan-96s仪器上所测得,当使用rochelightcycler480ii时,tm值可能略有变动,以当次试验野生型对照和突变型对照的tm值为准)。当仪器给出1个或1个以上tm值时,参考野生型对照、突变型对照的峰型选择有效tm值;当出现仪器无法自动给出tm值的情况时,可通过调整基线或直接人工判读的方法获得tm值。表6tm值参考(2)结果判定野生型对照的检测结果为4个检测位点的野生型;突变型对照的检测结果为4个检测位点的纯合突变型。当野生型对照和突变型对照的熔解峰tm值符合表6所示的tm值范围,即可对待测样本进行分析:①通过比较待测样本在pcr体系中各通道的熔解峰与相应位点野生型对照、突变型对照熔解峰之间熔点(tm值)的差异,判断样本是否发生突变:a.当样本熔解峰为单峰,且样本熔解峰与野生型对照熔解峰差异(样本峰-野生峰)在±1.0℃以内的即为野生型;b.当样本熔解峰为单峰,且样本熔解峰与突变型对照熔解峰差异(样本峰-突变峰)在±1.0℃以内的即为纯合突变型;c.当样本熔解峰为双峰,且左侧样本熔解峰与突变型对照熔解峰差异(样本峰-突变峰)在±1.0℃以内,右侧样本熔解峰与野生型对照熔解峰差异(样本峰-野生峰)在±1.0℃以内即为杂合突变型。②若检测结果无熔解峰,该样本需重新检测,必要时重新提取dna进行检测。6、检测结果对检测基因扩增熔解曲线结果进行分析,本试剂盒对样本的检测结果如图1~4和表7所示:表7样本检测结果分析实施例2试剂盒的检测准确性采用实施例1中的检测试剂盒和检测方法,检测下列已知型别样本p1~p7来验证本发明试剂盒的检测准确性,最终每个位点的三种型别(野生型、杂合突变型、纯合突变型)均被检测至少一次。已知样本的型别组成如表8所示:表8验证样本的组成对验证样本的检测结果如表9所示:表9准确性检验结果以上结果显示,7份已知样品的基因型均与试剂盒对样品检测得到的基因型一致,准确性为100%。实施例3试剂盒的检测特异性及最低检测限一、实验方法1、特异性验证:使用实施例1的试剂盒和检测方法检测非人类基因组样本及试剂盒检测范围外的样本4份(表10),检测结果如表11所示。表10特异性检测所用样本注:“-”表示此参考品不含该位点的检测区域表11特异性检测结果2、最低检测限验证:使用实施例1的试剂盒和检测方法检测不高于1ng/μl的样本7份(涵盖检测位点的野生型、纯合突变、杂合突变,表12),检测结果如表13所示。表12最低检测限验证样本表13最低检测限验证结果二、实验结果1、特异性:检测非人类基因组样本及试剂盒检测范围外的样本,检测结果均为未检出突变,说明本发明的检测试剂盒和检测方法特异性强。2、最低检测限:检测最低检测限参考品(1ng/μl),检测结果符合相应位点的型别,说明本发明的检测试剂盒和检测方法灵敏度较高,值得推广。实施例4试剂盒的重复性检验使用实施例1的试剂盒和检测方法对样品(涵盖所有检测位点杂合突变,表14)重复检测10次,检测结果如表15所示。表14重复性验证样本表15重复性验证结果以上结果显示,对样品进行重复检测10次,检测结果均一致,说明本发明的检测试剂盒和检测方法稳定性好。最后应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,对于本领域的普通技术人员来说,在上述说明及思路的基础上还可以做出其它不同形式的变化或变动,这里无需也无法对所有的实施方式予以穷举。凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。序列表<110>广州凯普医药科技有限公司郑州凯普医学检验所(有限合伙)北京凯普医学检验实验室有限公司<120>一种检测apoe和slco1b1基因多态性位点的引物、探针及其试剂盒<160>12<170>siposequencelisting1.0<210>1<211>20<212>dna<213>人工序列(2ambystomalateralexambystomajeffersonianum)<400>1ggctgtccaaggagctgcag20<210>2<211>20<212>dna<213>人工序列(2ambystomalateralexambystomajeffersonianum)<400>2ctggccgagcatggcctgca20<210>3<211>20<212>dna<213>人工序列(2ambystomalateralexambystomajeffersonianum)<400>3caagctgcgtaagcggctcc20<210>4<211>18<212>dna<213>人工序列(2ambystomalateralexambystomajeffersonianum)<400>4tcgcggatggcgctgagg18<210>5<211>22<212>dna<213>人工序列(2ambystomalateralexambystomajeffersonianum)<400>5agccccaatggtactatgggag22<210>6<211>22<212>dna<213>人工序列(2ambystomalateralexambystomajeffersonianum)<400>6tttaaaggaatctgggtcatac22<210>7<211>22<212>dna<213>人工序列(2ambystomalateralexambystomajeffersonianum)<400>7ccactatctcaggtgatgctct22<210>8<211>22<212>dna<213>人工序列(2ambystomalateralexambystomajeffersonianum)<400>8gtgatgttcttacagttacagg22<210>9<211>21<212>dna<213>人工序列(2ambystomalateralexambystomajeffersonianum)<400>9ggcggccgcacacgtcctcca21<210>10<211>20<212>dna<213>人工序列(2ambystomalateralexambystomajeffersonianum)<400>10tgccaggcgcttctgcaggt20<210>11<211>22<212>dna<213>人工序列(2ambystomalateralexambystomajeffersonianum)<400>11gatatatgcgttcatgggtaat22<210>12<211>20<212>dna<213>人工序列(2ambystomalateralexambystomajeffersonianum)<400>12aactaatatcgattcatcag20当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1