一种全人源抗体酵母展示技术的设计与构建的制作方法
1.本申请涉及基因工程技术领域,具体的涉及一种用于酵母展示文库的构建体、表达载体、宿主细胞及其构建方法与应用。
背景技术:
2.目前应用较普遍的抗体筛选技术包括体内筛选和体外筛选的两大类,而体外筛选技术由于其简便和快速的特点备受青睐。体外筛选技术以抗体文库的构建为基础,目前比较成熟的技术又主要包括噬菌体展示技术和酵母展示技术。噬菌体展示技术作为最早的抗体体外筛选技术已被广泛用于抗体药物的研发,目前已有大量的上市药物被批准使用。其原理为将b淋巴细胞的抗体重链可变区(vh)和轻链可变区(vl)采用pcr方法进行扩增,将扩增的片段插入到噬菌体载体中,抗体分子与单链噬菌体外壳蛋白以融合蛋白的形式展示在噬菌体表面,再将噬菌体转染至宿主细胞中进行增殖,待成熟后释放出来,最后利用抗原筛选的方法经过亲和吸附
‑
洗脱
‑
扩增等步骤后即可获得靶抗原特异性的单克隆噬菌体抗体。
3.噬菌体展示技术作为第一代的抗体体外筛选技术,有着体内抗体筛选难以比拟的优势,但其自身缺点也同样明显。第一,由于噬菌体的生长繁殖是在原核生物细菌中进行的,使得抗体的表达和生产处于一个完全不同的系统中,很难模拟抗体在哺乳动物中所拥有的各种翻译后修饰。而这些修饰在某些时候对于抗体的功能却是至关重要的。第二,噬菌体抗体库的多样性在细菌的不断扩增中易丢失。由于抗体是持续的在细菌中进行表达,其中的一部分抗体会影响到细菌的分裂增殖,故这部分抗体就很容易在细菌不断分裂增殖的过程中丢失。同时,也不是所有的抗体序列都能在噬菌体中获得很好的表达,这同样影响抗体库的多样性。这些缺点也促使着科学家不断地寻找更好的抗体体外筛选技术。
4.酵母展示技术就是后续发展起来的一个被认为更优于噬菌体展示的抗体体外筛选技术。其基本原理是将外源靶蛋白基因(外源蛋白)与特定的载体基因序列融合后导入酵母细胞,融合蛋白含有可锚定在酵母细胞壁上的结构,经转录翻译后可将外源蛋白固定化表达在酵母细胞表面。其优点包括了以下几个:第一,酵母表达系统不但具有原核生物细菌表达系统的特点,如操作简单,繁殖快等,同时由于其属于真核生物系统,具备了对蛋白进行加工和修饰的功能,使得表达出来的抗体更接近真实情况。第二,酵母的个体比细菌大很多,这使得酵母展示技术的筛选可以和流式细胞仪有机的结合起来。利用流式细胞仪来进行筛选有着非常大的优势,不但筛选的通量和速度大大地提高,同时可以非常直观跟踪和预估抗体亲和力,极大地提高筛选效率。第三,利用流式细胞仪进行筛选,可以对抗体的很多特性进行不同的设置,如结合抗体或是阻断抗体,种属选择性,以及不同亚型间特异性等等。第四,抗体的多样性能在酵母系统中得到很好的保真。实验结果表明即使在超过200代的酵母培育后,抗体库的多样性保持不变。
5.酵母展示技术相比噬菌体展示技术有着非常突出的优点,但同时也有其缺点。如目前的抗体库容量相对较低,对抗体的多样性有较大的影响。酵母表达质粒和抗体片段间的相对低效的重组也同样限制了抗体的多样性。
6.因此,本领域亟需一种具有高转化效率和丰富多样性的酵母展示文库的构建方法。
技术实现要素:
7.本申请提供了一种具有高转化效率和丰富多样性的酵母展示文库。
8.在本发明的第一方面,提供了一种构建体,其中包括启动子、多克隆位点区域、人igg重链恒定区的ch1片段、接头序列、酵母表面定位序列以及任选的标签序列。
9.在一个具体实施方式中,所述构建体包含表达式(i)所述的结构:
10.表达式(i):
[0011]5’‑
a
‑
b
‑
c
‑
d
‑
e
‑
f
‑3’ꢀꢀꢀ
(i);
[0012]
其中,
[0013]
a代表启动子;
[0014]
b代表多克隆位点区域;
[0015]
c代表人igg重链恒定区的ch1片段;
[0016]
d代表接头序列;
[0017]
e代表酵母表面定位序列;和
[0018]
f代表无或标签序列。
[0019]
在一个具体实施方式中,所述启动子选自:酵母gal1启动子、酵母gal10启动子和酵母gal1/gal10双向启动子。
[0020]
在一个具体实施方式中,所述接头序列为富含甘氨酸和丝氨酸的接头。
[0021]
在一个具体实施方式中,所述接头选自(gly4ser)3和(glyser)5。
[0022]
在一个具体实施方式中,所述酵母表面定位序列选自:aga1p多肽或其片段、aga2p多肽或其片段和sag1p多肽或其片段。
[0023]
在一个具体实施方式中,所述标签序列选自:c
‑
myc、v5、六组氨酸、谷胱甘肽
‑
s
‑
转移酶、链霉亲合素、生物素、血凝素、flag标签和e标签。
[0024]
在一个具体实施方式中,所述构建体包含seq id no:1所示的核酸序列。
[0025]
在本发明的第二方面,提供了所述构建体在制备重组载体的用途。
[0026]
在一个具体实施方式中,所述重组载体能够在细菌和酵母宿主细胞中复制和表达。
[0027]
在本发明的第三方面,提供了一种重组载体,其包括所述构建体。
[0028]
在一个具体实施方式中,其包括seq id no:1所示核酸序列。
[0029]
在一个具体实施方式中,所述载体选自:质粒、载体、噬菌体、粘粒和病毒。
[0030]
在一个具体实施方式中,所述质粒为酵母质粒。
[0031]
在一个具体实施方式中,所述酵母质粒选自下组:酵母整合质粒、酵母复制质粒、引入着丝粒元件的酵母复制质粒、酵母游离质粒和酵母线性质粒。
[0032]
在一个具体实施方式中,所述重组载体包含如seq id no:2所示的核酸序列。
[0033]
在本发明的第四方面,提供了一种试剂盒,其包含第三方面所述重组载体。
[0034]
在一个具体实施方式中,所述试剂盒还包括选自一种或多种下组的试剂:引物、核酸内切酶、和核酸连接酶。
[0035]
在一个具体实施方式中,所述引物用于扩增靶蛋白序列。
[0036]
在一个具体实施方式中,所述引物包括seq id no:3
‑
seq id no:20所示序列的引物。
[0037]
在一个具体实施方式中,所述重组载体包含如seq id no:2所示的核酸序列。
[0038]
在一个具体实施方式中,所述试剂盒用于在所述重组载体中插入靶蛋白序列。
[0039]
在本发明的第五方面,提供了第四方面所述试剂盒在用于制备靶蛋白表达载体中的用途。
[0040]
在本发明的第六方面,提供了一种表达载体,所述表达载体为在第三方面所述重组载体中插入靶蛋白序列得到的表达载体。
[0041]
在一个具体实施方式中,所述靶蛋白序列包含抗原结合序列。
[0042]
在一个具体实施方式中,所述抗原结合序列选自下组:重链、轻链、重链
‑
轻链二聚体、fab片段、f(ab’)2片段、fv片段、单链fv(scfv)和dab。
[0043]
在一个具体实施方式中,所述抗原结合序列为人源抗体基因序列。
[0044]
在一个具体实施方式中,所述人源抗体基因序列包括:人源抗体基因重链序列、人源抗体基因轻链序列、或其组合。
[0045]
在一个具体实施方式中,所述人源抗体基因轻链序列选自:人kappa轻链基因序列和人lambda轻链基因序列。
[0046]
在一个具体实施方式中,所述表达载体使用第四方面所述试剂盒制备。
[0047]
在本发明的第七方面,提供了所述表达载体在用于制备酵母展示细胞的用途。
[0048]
在本发明的第八方面,提供了一种细胞构建方法,其包括:
[0049]
a)在第三方面所述载体v0中插入靶蛋白序列,得到表达载体v1;和
[0050]
b)将步骤a)中得到的表达载体v1导入宿主细胞中,得到重组宿主细胞。
[0051]
在一个具体实施方式中,其中所述载体v0包含如seq id no:2所示的核酸序列。
[0052]
在一个具体实施方式中,所述宿主细胞为酵母细胞。
[0053]
在一个具体实施方式中,所述酵母细胞选自:酿酒酵母、毕赤酵母、及其衍生物。
[0054]
在一个具体实施方式中,所述步骤b)中得到的所述重组宿主细胞的表面表达靶蛋白。
[0055]
在本发明的第九方面,提供了一种宿主细胞,其包含第三方面所述表达载体。
[0056]
在一个具体实施方式中,所述宿主细胞根据第八方面所述方法构建。
[0057]
在一个具体实施方式中,所述宿主细胞表达至少102、至少103、至少104或者至少105种靶蛋白。
[0058]
在一个具体实施方式中,所述靶蛋白为抗体或抗原结合蛋白。
[0059]
在一个具体实施方式中,所述抗体或抗原结合蛋白为人源抗体或抗原结合蛋白。
[0060]
在一个具体实施方式中,所述宿主细胞为表达全人源抗体或抗原结合蛋白的酵母细胞。
[0061]
在一个具体实施方式中,所述酵母细胞为表达全人源抗体或抗原结合蛋白的酵母展示细胞。
[0062]
在本发明的第十方面,提供了一种宿主细胞展示文库,其包括至少两种第九方面所述宿主细胞。
[0063]
在一个具体实施方式中,所述宿主细胞展示文库为酵母细胞展示文库。
[0064]
在一个具体实施方式中,所述宿主细胞展示文库用于提供抗体展示库。
[0065]
在一个具体实施方式中,所述宿主细胞展示文库展示至少102、至少104、至少106或者至少108种全人源抗体或抗原结合蛋白。
[0066]
本领域技术人员能够从下文的详细描述中容易地洞察到本申请的其它方面和优势。下文的详细描述中仅显示和描述了本申请的示例性实施方式。如本领域技术人员将认识到的,本申请的内容使得本领域技术人员能够对所公开的具体实施方式进行改动而不脱离本申请所涉及发明的精神和范围。相应地,本申请的附图和说明书中的描述仅仅是示例性的,而非为限制性的。
附图说明
[0067]
本申请所涉及的发明的具体特征如所附权利要求书所显示。通过参考下文中详细描述的示例性实施方式和附图能够更好地理解本申请所涉及发明的特点和优势。对附图简要说明书如下:
[0068]
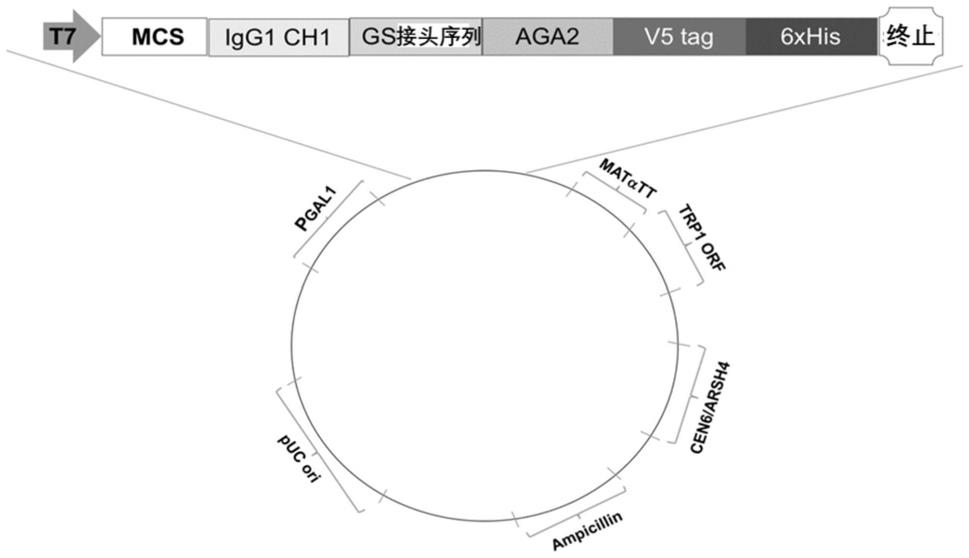
图1显示的是本申请所述构建体的示意图。
[0069]
图2显示的是本申请所述的重组载体pan
‑
hc表达的抗体验证实验中,fitc标记的酵母细胞的流式分析结果。
[0070]
图3显示的是本申请所述重组载体pan
‑
hc表达的抗体结合能力实验中,fitc和pe标记的酵母细胞的流式分析结果。
[0071]
图4显示的是本申请所述引物对特异性扩增得到人源抗体片段的电泳结果。
[0072]
图5显示的是本申请所述酵母展示库的示意图。
[0073]
图6显示的是本申请所述酵母展示库中随机挑选的酵母克隆的测序结果。
具体实施方式
[0074]
以下由特定的具体实施例说明本申请发明的实施方式,熟悉此技术的人士可由本说明书所公开的内容容易地了解本申请发明的其他优点及效果。
[0075]
术语定义
[0076]
在本申请中,术语“构建体”和“核酸构建体”可以互换,通常指包含一个或多个功能单元的核酸序列。所述构建体可以是一段dna序列,但在同一个质粒上可提供多个构建体;构建体的实例可以包括但不限于,环状、线性或双链的染色体外dna分子、粘粒、包含非天然核酸序列的病毒基因组等。本发明提供了一种构建体,其中包括启动子、多克隆位点区域、人igg重链恒定区的ch1片段、接头序列、酵母表面定位序列以及任选的标签序列,例如,一种包含seq id no:1所示的核酸序列的构建体。
[0077]
在本申请中,术语“启动子”通常是指一段dna序列,其可以调节与启动子其操作性连接的所述dna序列的表达,从而影响细胞中所述dna序列的表达。启动子通常将适合于靶基因正在其中表达的宿主细胞。例如,所述启动子为在细菌和酵母细胞中均表达的启动子。所述启动子可以来自于酵母启动子数据库scpd。
[0078]
在本申请中,术语“多克隆位点区域”、“多克隆位点”、“多克隆位点区”和“mcs”可以互换,通常是指载体中一段dna序列,其上含有多个酶切位点,是可作为外源dna的插入部
位。mcs可以是包含多个限制性酶切位点的一段很短的dna序列。其中,每个限制性酶切位点通常是唯一的,即它们在一个特定的载体质粒中常常只出现一次;不同酶的酶切位点可有重叠。
[0079]
在本申请中,术语“接头”和“接头序列”可以互换,通常是指连接2个或更多个离散的结构域的部分。接头可以使离散的结构域独立存在。接头部分可以是线性的。合适的接头包括多肽、多核酸、肽核酸等。示例性的接头包括编码多肽、或氨基酸的多肽或其它非天然发生的部分的多核苷酸。接头可以是天然序列的一部分、其变体或合成的序列。例如,本申请提供的构建体中的接头序列可以为富含甘氨酸和丝氨酸的接头,例如(gly4ser)3和(glyser)5。
[0080]
在本申请中,术语“酵母表面定位序列”通常是指载体中的一段蛋白基因序列,其与靶蛋白序列融合后,可以利用酵母细胞内蛋白转运机制(如gpi锚定),使所述靶蛋白能够定位于酵母细胞表面。酵母表面定位序列的实例包括但不限于,酵母细胞壁甘露糖蛋白基因、凝集素基因、絮凝素flo1p基因、agα1、aga1、aga2、flo1、sed1p、cwp1p、cwp2p、tip1p、tir1p、srp1p等。
[0081]
在本申请中,术语“标签”通常是指可以插入表达载体中可使构建体的一种或多种表达产物被检测到或易于纯化的功能肽。所述标签是本领域众所周知,且可以包括放射性标记的氨基酸或与生物素基部分的多肽的连接。实例包括但不限于,c
‑
myc、v5、六组氨酸、谷胱甘肽
‑
s
‑
转移酶、链霉亲合素、生物素、血凝素、flag标签、e标签等。在本申请中,所述构建体中的标签还可以包括酵母选择标记。所述酵母选择标记包括抗药性标记和允许酵母宿主细胞合成必需的细胞营养素(例如氨基酸)的遗传功能。在酵母中常用的抗药性标记包括氯霉素、卡那霉素、甲氨蝶呤、g418(遗传霉素)等。允许酵母宿主细胞合成必需的细胞营养素的遗传功能与可得到的具有在对应的基因组功能中的营养缺陷型突变的酵母菌株一起使用。典型的酵母选择标记包括leu2、trp1、his3、his4、ura3、ura5、sfa1、ade2、met15、lys5、lys2、ilv2、fba1、pse1、pdi1和pgk1。使载体整合进酵母中的方法是众所周知的,例如,参见美国专利号7,479,389、w02007136865和pct/us2008/13719。
[0082]
在本申请中,术语“载体”用来指能转运与之连接的构建体的核酸分子,其可以包括质粒、载体、噬菌体、粘粒或病毒,以及细菌人工染色体(bac)和酵母人工染色体(yac)。某些载体能在它所导入的宿主细胞中自主复制,如具有在宿主细胞中起作用的复制起点的载体;其他的载体可在导入宿主细胞后整合入宿主细胞的基因组中,并且由此随着宿主基因组一起复制。本发明提供了一种包括所述构建体的重组载体,例如,一种包含如seq id no:1所示的核酸序列的重组载体,其具有seq id no:2所示的核酸序列。
[0083]
在本申请中,所述“载体”是可以使一种酵母载体。基于其在酵母中的复制模式,所述酵母载体包括五种的酵母载体:yip(酵母整合质粒)、yrp(酵母复制质粒)、ycp(引入着丝粒元件cen的酵母复制质粒)、yep(酵母游离质粒)和ylp(酵母线性质粒)。其中,除ylp质粒之外,所有这些质粒都可以在大肠杆菌以及酿酒酵母中维持,因此也被称作酵母穿梭载体。酵母载体的实例可以包括酵母2μm环及其衍生物、编码酵母自主复制序列的酵母载体、酵母微型染色体或酵母整合载体等。
[0084]
在本申请中,术语“重组表达载体”和“表达载体”可以互换,通常指能指导与之连接的基因的表达的载体;所述表达载体可包括用于在细胞中表达靶蛋白的任何核酸分子。
表达载体可以是本领域技术人员已知的任何质粒或载体,其适合于在特定宿主细胞中表达蛋白质,包括但不限于哺乳动物细胞、细菌细胞和酵母细胞。本发明提供了一种在所述的重组载体中插入靶蛋白序列得到的表达载体。
[0085]
在本申请中,术语“重组”是指通过人为干预而改变的材料(例如,核酸、基因、多核苷酸、多肽)。例如,重组分子中的元件可能不是天然的,或一级序列上所述重组分子中的元件的排列可能发生改变,以优化其表达和/或活性。用于产生重组分子(例如,重组核酸)的试剂是本领域常见的。术语“重组”在本文中还可以指包含重组分子的细胞或生物体。例如,含有重组核酸的宿主细胞。本发明提供了一种含有所述构建体的重组载体,一种插入了靶蛋白编码序列的表达载体,以及一种含有所述表达载体的宿主细胞。例如,一种含有所述表达载体的酵母细胞。
[0086]
在本发明的一些实施方案中,所述酵母选自酿酒酵母、己氏酵母(saccharomyces pastorianus)、贝酵母(saccharomyces bayanus)、乳酸克鲁维酵母(kluyveromyces lactis)、马克斯克鲁维酵母(kluyveromyces marxianus)、粟酒裂殖酵母(schizosaccharomyces pombe)、白色假丝酵母(candida albicans)、毕赤酵母(pichia pastoris)、树干毕赤酵母(pichia stipitis)、解脂耶氏酵母(yarrowia lipoidica)、多形汉逊酵母(hansenula polymorpha)、红法夫酵母(phaffia rhodozyma)、产航假丝酵母(candida utilis)、耐盐酵母(arxula adeninivorans)、汉逊德己利酵母(debaryomyces hansenii)、多形德己利酵母(debaryomyces polymorphus)、粟酒裂殖酵母(schizosaccharomyces pombe)、西方许旺酵母(schwanniomyces occidentalis)或其衍生物。
[0087]
在本申请中,术语“文库”通常指集合、或组合物。所述文库可以指所编码的蛋白质的集合,也可以指表达所述蛋白质的细胞的集合。例如,“抗体展示文库”可以指大量抗体蛋白组成的合集合。“宿主细胞展示文库”可以指表达重组靶蛋白的大量宿主细胞组成的合集合,例如酵母展示文库。
[0088]
在本申请中,术语“展示”通常指表达所述蛋白的行为,有时还指其表达的蛋白可以被检测。例如,重组宿主细胞可以展示修饰多肽,可以理解为所述细胞中存在所述修饰多肽的表达,且所述表达的修饰多肽可以被检测到,例如使用细胞免疫沉淀法或免疫杂交方法检测细胞中或表面上有所述修饰多肽的存在。
[0089]
在本申请中,术语“包含”通常是指包括明确指定的特征,但不排除其他要素。
[0090]
在本申请中,术语“约”通常是指在指定数值以上或以下0.5%
‑
10%的范围内变动,例如在指定数值以上或以下0.5%、1%、1.5%、2%、2.5%、3%、3.5%、4%、4.5%、5%、5.5%、6%、6.5%、7%、7.5%、8%、8.5%、9%、9.5%、或10%的范围内变动。
[0091]
在本申请中,术语“富含”通常其含有的某一种或几种物质的含量不低于50%,例如不低于60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%、99.5%。
[0092]
发明详述
[0093]
重组载体
[0094]
本申请提供了一种包括本发明提供的构建体的重组载体。例如所述重组载体可以为一种包含seq id no:1所示序列的构建体的载体。在本申请的一个具体实施方式中,使用限制性内切酶agei和pmei酶切商业化酵母质粒pyd1,然后通过筛选得到了一段长度相对较
短,但保留质粒的复制功能和在大肠杆菌和酵母细胞中稳定转录的能力的载体;将上述载体与合成的上述构建体,具体是具有seq id no:1所示序列的dna片段结合;得到了seq id no:2所示序列的重组载体pan
‑
hc。得到的重组载体可以进而感染感受态细胞,得到具有上述重组质粒的菌株。
[0095]
本申请提供的重组载体可以作为一种工具载体,可用于酵母展示技术。在所述重组载体的多克隆位点区域中插入具有靶蛋白的编码序列,可以得到可表达修饰多肽的载体,且所述修饰多肽中融合有能将靶蛋白定位到酵母细胞表面的蛋白序列、方便检测的标签序列、人igg重链恒定区的ch1片段和接头序列。例如,在本发明的一个实施例中,通过设计引物,扩增得到人源抗体基因片段,将所述抗体基因片段连接或插入所述载体pan
‑
hc的多克隆位点区域中,得到重组载体。
[0096]
表达载体
[0097]
本申请提供了一种通过在所述的重组载体中插入靶蛋白序列得到的表达载体。当所述靶蛋白序列包含抗原结合序列,尤其是人源抗体基因时,所述表达载体为一种可用于表达全人源抗体的表达载体。所述人源抗体基因序列可以包括人源抗体基因重链序列、人源抗体基因轻链序列、或其组合。
[0098]
在本申请的一个具体实施方式中,可以根据人源抗体基因设计引物,用以扩增所述人源抗体基因片段,然后将所述人源抗体基因片段插入所述重组载体pan
‑
hc中,得到可以表达人源抗体的表达载体。通过抗体结合能力实验验证,本申请提供的表达载体可以导入酵母细胞中,并表达出能够与抗原结合的抗体蛋白。
[0099]
宿主细胞
[0100]
将上述含有靶蛋白编码序列的重组载体导入宿主细胞中,通过筛选,可以得到能表达修饰多肽的重组宿主细胞。若表达的修饰多肽能定位在宿主细胞表面,则所述重组宿主细胞可以作为一种表面展示性宿主细胞。
[0101]
在本申请的一个具体实施方式中,在载体pan
‑
hc中插入人源tigit蛋白抗体序列,导入上述tigit抗体表达载体的酵母细胞可以产生tigit抗体,而且产生的tigit抗体能够与加入的人tigit重组蛋白结合。说明含有载体pan
‑
hc的重组酵母细胞能够发挥抗体表达载体的功能,产生的抗体有抗原亲和性。
[0102]
宿主细胞展示文库
[0103]
一个宿主细胞中可以有一种或多种修饰多肽。例如所述重组宿主细胞可以展示至少102、至少103、至少104或者至少105种所述修饰多肽序列。多种上述重组宿主细胞可以组成一个宿主细胞展示文库。所述宿主细胞展示文库中可以展示大量修饰多肽。例如所述宿主细胞展示文库可以展示至少102、至少104、至少106或者至少108种所述修饰多肽。
[0104]
在本申请的一个具体实施方式中,在载体pan
‑
hc中插入人源抗体基因重链家族h1、h2、h3、h4和h5,kappa轻链家族的κ1、κ2、κ3及lambda轻链家族的λ1、λ2、λ3片段;且在同一个重组酵母细胞中同时导入重链片段表达载体和轻链片段表达载体。通过不同重链片段和轻链片段的组合配对,可以得到具有抗体基因多样性的抗体库。而由于本实施例中使用的载体pan
‑
hc表达的修饰多肽能够定位到细胞膜外表面上,因此形成了酵母展示抗体库。
[0105]
构建方法与试剂盒
[0106]
本申请提供了一种细胞构建方法,其包括:a)在载体v0中插入靶蛋白的编码序列,
得到重组载体v1;和b)将重组载体v1导入细胞中。其中,所述载体v0可以具有如seq id no:2所示的核酸序列;所述细胞为细菌细胞和/或酵母细胞;所得到的细胞产生修饰多肽且所述修饰多肽为靶蛋白的融合蛋白。将重组载体导入细胞中、筛选得到导入重组载体的阳性细胞的方法是本领域技术人员所熟知的。
[0107]
本申请还提供了可用于上述构建重组表达载体的试剂盒。所述试剂盒中可包括上述重组载体;可以还包括含有靶蛋白编码序列的核酸,或可以扩增得到所述靶蛋白编码序列的引物。试剂盒中可以还含有其他用于将所述靶核酸插入载体中的试剂,例如限制性内切酶、核酸连接酶等。
[0108]
本申请还包括以下的实施方式:
[0109]
1.一种构建体,其中包括启动子、多克隆位点区域、人igg重链恒定区的ch1片段、接头序列、酵母表面定位序列以及任选的标签序列。
[0110]
2.根据实施方式1所述的构建体,所述构建体包含表达式(i)所述的结构:
[0111]
表达式(i):
[0112]5’‑
a
‑
b
‑
c
‑
d
‑
e
‑
f
‑3’ꢀꢀꢀ
(i);
[0113]
其中,
[0114]
a代表启动子;
[0115]
b代表多克隆位点区域;
[0116]
c代表人igg重链恒定区的ch1片段;
[0117]
d代表接头序列;
[0118]
e代表酵母表面定位序列;和
[0119]
f代表无或标签序列。
[0120]
3.根据实施方式1或2中所述的构建体,所述启动子选自:酵母gal1启动子、酵母gal10启动子和酵母gal1/gal10双向启动子。
[0121]
4.根据实施方式1
‑
3中任一项所述的构建体,所述接头序列为富含甘氨酸和丝氨酸的接头。
[0122]
5.根据实施方式1
‑
4中任一项所述的构建体,所述接头选自(gly4ser)3和(glyser)5。
[0123]
6.根据实施方式1
‑
5中任一项所述的构建体,所述酵母表面定位序列选自:aga1p多肽或其片段、aga2p多肽或其片段和sag1p多肽或其片段。
[0124]
7.根据权利求1
‑
6中任一项所述的构建体,所述标签序列选自:c
‑
myc、v5、六组氨酸、谷胱甘肽
‑
s
‑
转移酶、链霉亲合素、生物素、血凝素、flag标签和e标签。
[0125]
8.根据实施方式1
‑
7中任一项所述的构建体,其包含seq id no:1所示的核酸序列。
[0126]
9.根据实施方式1
‑
8中所述的构建体在制备重组载体的用途。
[0127]
10.根据实施方式9中所述的用途,所述重组载体能够在细菌和酵母宿主细胞中复制和表达。
[0128]
11.一种重组载体,其包括实施方式1
‑
8中所述的构建体。
[0129]
12.根据实施方式11中所述的重组载体,其包括seq id no:1所示核酸序列。
[0130]
13.根据实施方式11或12中所述的重组载体,所述载体选自下组:质粒、载体、噬菌
体、粘粒和病毒。
[0131]
14.根据实施方式13中所述的重组载体,所述质粒为酵母质粒。
[0132]
15.根据实施方式14中所述的重组载体,所述酵母质粒选自下组:酵母整合质粒、酵母复制质粒、引入着丝粒元件的酵母复制质粒、酵母游离质粒和酵母线性质粒。
[0133]
16.根据实施方式11
‑
15中任一项所述的重组载体,其包含如seq id no:2所示的核酸序列。
[0134]
17.一种试剂盒,其包含根据实施方式11
‑
16中所述的重组载体。
[0135]
18.根据实施方式17中任一项所述的试剂盒,还包括选自一种或多种下组的试剂:引物、核酸内切酶、和核酸连接酶。
[0136]
19.根据实施方式18中所述的试剂盒,所述引物用于扩增靶蛋白序列。
[0137]
20.根据实施方式18或19中所述的试剂盒,所述引物包括seq id no:3
‑
seq id no:20所示序列的引物。
[0138]
21.根据实施方式17
‑
20中任一项所述的试剂盒,所述重组载体包含如seq id no:2所示的核酸序列。
[0139]
22.根据实施方式19
‑
21中任一项所述的试剂盒,其用于在所述重组载体中插入所述靶蛋白序列。
[0140]
23.根据实施方式17
‑
22中所述的试剂盒在用于制备靶蛋白表达载体中的用途。
[0141]
24.一种表达载体,所述表达载体为在根据实施方式17
‑
22中任一项所述的重组载体中插入靶蛋白序列得到的表达载体。
[0142]
25.根据实施方式24中所述的表达载体,所述靶蛋白序列包含抗原结合序列。
[0143]
26.根据实施方式25中所述的表达载体,所述抗原结合序列选自下组:重链、轻链、重链
‑
轻链二聚体、fab片段、f(ab')2片段、fv片段、单链fv(scfv)和dab。
[0144]
27.根据实施方式25或26中所述的表达载体,所述抗原结合序列为人源抗体基因序列。
[0145]
28.根据实施方式27中所述的表达载体,所述人源抗体基因序列包括:人源抗体基因重链序列、人源抗体基因轻链序列、或其组合。
[0146]
29.根据实施方式28中所述的表达载体,所述人源抗体基因轻链序列选自:人kappa轻链基因序列和人lambda轻链基因序列。
[0147]
30.根据实施方式24
‑
29中任一项所述的表达载体,其使用根据实施方式17
‑
22中任一项所述的试剂盒制备。
[0148]
31.根据实施方式24
‑
30中所述的表达载体在用于制备酵母展示细胞的用途。
[0149]
32.一种细胞构建方法,其包括:
[0150]
a)在实施方式24
‑
30中任一项所述载体v0中插入靶蛋白序列,得到表达载体v1;和
[0151]
b)将步骤a)中得到的表达载体v1导入宿主细胞中,得到重组宿主细胞。
[0152]
33.根据实施方式32中所述的方法,其中所述载体v0包含如seq id no:2所示的核酸序列。
[0153]
34.根据实施方式32或33中所述的方法,所述宿主细胞为酵母细胞。
[0154]
35.根据实施方式34中所述的方法,所述酵母细胞选自:酿酒酵母、毕赤酵母、及其衍生物。
[0155]
36.根据实施方式32
‑
35中任一项所述的方法,所述步骤b)中得到的所述重组宿主细胞的表面表达所述靶蛋白。
[0156]
37.一种宿主细胞,其包含根据实施方式24
‑
29中所述的表达载体。
[0157]
38.根据实施方式37中所述的宿主细胞,其根据实施方式32
‑
36中任一项所述的方法构建。
[0158]
39.根据实施方式36或37中所述的宿主细胞,其表达至少102、至少103、至少104或者至少105种靶蛋白。
[0159]
40.根据实施方式39中所述的宿主细胞,所述靶蛋白为抗体或抗原结合蛋白。
[0160]
41.根据实施方式40中所述的宿主细胞,所述抗体或抗原结合蛋白为人源抗体或抗原结合蛋白。
[0161]
42.根据实施方式37
‑
41中任一项所述的宿主细胞,其为表达全人源抗体或抗原结合蛋白的酵母细胞。
[0162]
43.根据实施方式42中所述的宿主细胞,所述酵母细胞为表达全人源抗体或抗原结合蛋白的酵母展示细胞。
[0163]
44.一种宿主细胞展示文库,其包括至少两种根据实施方式37
‑
43中所述的宿主细胞。
[0164]
45.根据实施方式44中所述的宿主细胞展示文库,其为酵母细胞展示文库。
[0165]
46.根据实施方式44或45中所述的宿主细胞展示文库,其用于提供抗体展示库。
[0166]
47.根据实施方式44
‑
46中任一项所述的宿主细胞展示文库,其展示至少102、至少104、至少106或者至少108种全人源抗体或抗原结合蛋白。
[0167]
不欲被任何理论所限,下文中的实施例仅仅是为了阐释本申请的融合蛋白、制备方法和用途等,而不用于限制本申请发明的范围。
[0168]
实施例
[0169]
实施例1构建重组表达载体pan
‑
hc
[0170]
使用商业化质粒pyd1(购自invitrogen)构建具有人igg重链恒定区的重组表达载体。简要操作如下所示:
[0171]
(1)使用核酸内切酶agei和pmei酶切处理商业化质粒pyd1,在37℃进行一个小时;然后用琼脂糖胶回收较大片段。
[0172]
(2)人工合成一段如seq id no:2所示的核酸序列(购自thermofisher)。此序列所含的元件如图1所示。
[0173]
(3)使用in
‑
fusion cloning试剂盒(购自takara生物技术公司),将步骤(1)中回收纯化的载体片段和步骤(2)所合成的片段进行连接。
[0174]
(4)把步骤(3)中的连接产物转化到细菌中,并进行阳性克隆的筛选及测序鉴定。
[0175]
通过测序筛选得到序列中没有任何突变的重组表达载体pan
‑
hc,其序列如seq id no:2所示。
[0176]
实施例2使用重组载体pan
‑
hc构建的表达载体以表达抗体
[0177]
使用已知的tigit抗体序列来测试实施例1中得到的pan
‑
hc重组载体,以评估此重组载体的抗体表达能力。
[0178]
(1)提供一段人tigit抗体的核酸序列(购自thermofisher)。
[0179]
(2)用dna限制性内切酶nhei和eco47iii对重组载体pan
‑
hc进行酶切,并回收大片段。
[0180]
(3)用酵母电转的方法把步骤(1)和(2)中的抗体及载体序列转到酵母菌株eby100。
[0181]
(4)用100毫升色氨酸缺陷的培养基sd
‑
caa(酪氨酸5g/l,葡萄糖20g/l,无氨基酸无硫酸铵的酵母氮源基础1.7g/l,硫酸铵5.3g/l,na2hpo4‑
7h2o 10.2g/l,nah2po4‑
h2o 8.6g/l)进行培养过夜,筛选出含有重组质粒的酵母。
[0182]
(5)从步骤(4)中取出2毫升的酵母培养液,3000rpm离心5分钟后并去除上清,然后用5ml诱导培养基sgr
‑
caa(酪氨酸5g/l,葡萄糖1g/l,棉子糖20g/l,半乳糖20g/l,无氨基酸无硫酸铵的酵母氮源基础1.7g/l,硫酸铵5.3g/l,na2hpo4‑
7h2o 10.2g/l,nah2po4‑
h2o 8.6g/l)对抗体进行诱导过夜。
[0183]
(6)从步骤(5)中取出500μl的酵母培养液,3000rpm离心5分钟后去除上清,保留酵母沉淀物。然后用含有fitc标记的v5抗体溶液重悬酵母沉淀物,并在4℃冰箱中放置30分钟。
[0184]
(7)用pbs清洗一遍,把最终的酵母沉淀物用1ml的pbs重悬起来,用流式细胞仪检测抗体表达的情况
[0185]
结果:如图2所示,在无表达载体的eby100酵母中没有任何fitc的信号,而在电转含有tigit抗体表达载体的酵母中,则有fitc信号。说明了重组表达载体pan
‑
hc可以进行抗体的表达,且表达出来的抗体可以很好地展示在酵母的表面。
[0186]
实施例3使用重组载体pan
‑
hc构建的表达载体表达的抗体的结合能力验证实验使用pan
‑
hc表达抗体,验证其能否与目的蛋白tigit结合。
[0187]
(1)从上述实施例2步骤(5)取出500μl诱导过夜的酵母培养液,3000rpm离心5分钟后去除上清,保留酵母沉淀物。用500μl的pbs重悬酵母,并加入100nm生物素标记的人源tigit重组蛋白,在室温孵育1个小时。
[0188]
(2)用同样的条件离心,沉淀酵母,然后用1ml的pbs重悬。重复上述洗涤3次。
[0189]
(3)由于实施例2中的抗体有v5标签,用含有fitc标记的v5抗体和pe标记的链霉亲和素溶液重悬酵母沉淀物,并在4℃冰箱中放置30分钟。
[0190]
(4)重复步骤(2)。
[0191]
(5)用500μl pbs重悬酵母沉淀物。
[0192]
结果:由于fitc可以标记展示在酵母表面的抗体,pe可以标记tigit重组蛋白,因此如果fitc和pe可以同时存在酵母表面的话,就说明酵母展示的抗体可以结合tigit重组蛋白。结果对照为左图,实施例2中的酵母培养液如图3右图所示。对照组显示了没有fitc信号即酵母没有抗体的表达,也没有pe的信号即没有tigit连接到细胞膜;而实验组中酵母表面同时存在fitc和pe信号,证明了在酵母表面被检测到有tigit蛋白通过结合酵母表面的抗体上。
[0193]
实施例4酵母展示抗体库的构建与分析
[0194]
使用重组表达载体pan
‑
hc构建酵母展示抗体库。
[0195]
4.1分别根据人源抗体基因重链家族h1、h2、h3、h4和h5,kappa轻链家族的κ1、κ2、κ3及lambda轻链家族的λ1、λ2、λ3,设计用于连接到重组表达载体pan
‑
hc上pcr克隆人源抗体
基因的引物(具体参见表1)。
[0196]
表1
[0197]
序号扩增片段引物序列1人源抗体重链h1seq id no:3和seq id no:42人源抗体重链h2seq id no:5和seq id no:43人源抗体重链h3seq id no:6和seq id no:74人源抗体重链h4seq id no:8和seq id no:95人源抗体重链h5seq id no:10和seq id no:96人源抗体kappa轻链κ1seq id no:13和seq id no:147人源抗体kappa轻链κ2seq id no:13和seq id no:148人源抗体kappa轻链κ3seq id no:15和seq id no:169人源抗体lambda轻链λ1seq id no:17和seq id no:1810人源抗体lambda轻链λ2seq id no:19和seq id no:1811人源抗体lambda轻链λ3seq id no:20和seq id no:18
[0198]
4.2以富含免疫细胞mrna(购自takara),作为抗体基因的来源。使用smarter pcr cdna synthesis kit试剂盒(购自clontech),按照其说明书把mrna反转录为cdna。使用得到的cdna为模板,利用上述引物,通过pcr扩增,得到抗体基因核酸片段。
[0199]
pcr的反应体系为:总体积为100μl,其中cdna模板为2μl,20μm的引物(正向和反向两条引物)各2μl,accuprime pfx dna polymerase(100μl,2.5u/μl)为1μl,10x accuprime reaction mix为10μl,以及83μl纯化的去离子水。pcr的反应条件为:94℃,30秒/56℃,30秒/68℃,45秒,循环30次。
[0200]
结果:如图4所示,所有测试的重链基因(h1到h5)和轻链基因(κ1、κ2、κ3和λ1、λ2、λ3)都能特异性被扩增出来,同时pcr产物的大小与预期一致,显示了所设计的引物达到预期目的。
[0201]
4.3构建酵母展示库的示意图如图5所示,具体步骤如下:
[0202]
(1)用dna限制性内切酶nhei和ecor47 iii对重组载体pan
‑
hc进行酶切,并回收载体。
[0203]
(2)用步骤2中的pcr反应和扩增条件分别对重链基因和轻链基因进行扩增,并纯化pcr扩增产物。
[0204]
(3)酵母的电转转化。整个酵母展示库含有10个小的抗体库,其中每个重链将分别与两种不同类型的轻链来配对。如重链h1会跟轻链κ1、2、3配对,同时重链h1也跟轻链λ1、2、3配对,以此类推(总共5个重链则可以形成10个抗体小库)。每个抗体小库由50个电转组成,每次电转使用10μg载体、10μg重链基因和10μg轻链基因混合物(比例为1:1:1)。
[0205]
(4)为了检测这个酵母展示库是否成功地把抗体基因引入到表达载体,以及对抗体库中抗体基因多样性有个初步的了解,随机挑选一些酵母菌株,使用yeast dna extract kit(购自thermofisher)对酵母体内的dna进行提取,并对抗体基因进行测序。
[0206]
结果:测序结果如图6所示,随机挑选的14个酵母克隆中,都含有序列正确的抗体基因,且没有任何的重复性,证明了酵母展示库构建成功,也证明本方案的抗体库具有很好的多样性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1