具有与生物材料的相容性的聚合物的制造方法与流程
1.本发明涉及不引起凝胶化问题的含有共聚物的清漆的制造方法、涂覆膜形成用组合物的制造方法、涂覆膜的制造方法、优选具有与生物材料的相容性(例如具有抑制生物材料附着的能力、细胞培养促进性)的涂覆膜的制造方法。
背景技术:
2.已提出了具有用于抑制人工透析器、人工脏器、医疗器具等医疗用器具、器材等生物材料附着的各种抑制生物材料附着的能力的涂覆材料、或用于促进细胞培养的涂覆材料。
3.专利文献1中公开了具有生物材料附着控制能力的离子复合材料及其制造方法。专利文献2中公开了防污性等特性优异的表面处理剂。
4.现有技术文献
5.专利文献
6.专利文献1:国际公开第2014/196650号
7.专利文献2:国际公开第2018/008663号
技术实现要素:
8.发明所要解决的课题
9.对于具有不饱和键的磷酸酯系单体而言,利用通常的合成方法时,包含大量的磷酸二酯等杂质。将包含大量磷酸二酯成分的具有不饱和键的磷酸酯系单体、与其他具有不同的不饱和键的单体用于共聚反应的情况下,存在下述问题:磷酸二酯生成了成为交联部的三维网状结构而引发凝胶化,从而无法制作聚合物溶解或分散在溶剂中而得的清漆。
10.本技术的发明人进行了深入研究,结果发现,使一定纯度以上的具有特定结构式的磷酸酯单体与其他具有不同的不饱和键的单体通过自身已知的方法进行共聚,由此可在不发生凝胶化的情况下制造含有共聚物的清漆。
11.本发明提供不发生凝胶化问题的含有共聚物的清漆的制造方法、组合物的制造方法、涂覆膜的制造方法、优选具有与生物材料的相容性(例如,具有抑制生物材料附着的能力、细胞培养促进性)的涂覆膜的制造方法。
12.用于解决课题的手段
13.本发明包含以下内容。
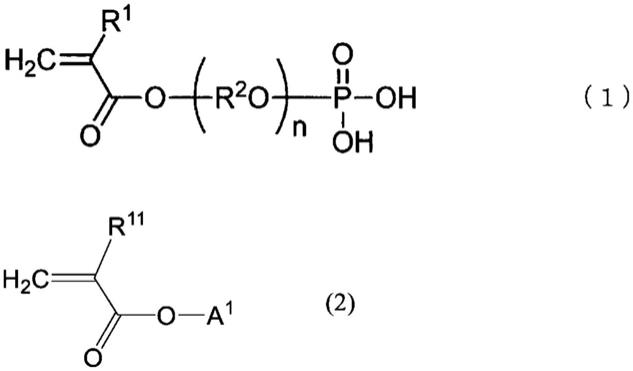
14.[1]含有共聚物的清漆的制造方法,其包括:使包含由下述式(1)及式(2)表示的化合物的单体混合物在聚合用溶剂中、在自由基聚合引发剂存在下共聚的工序,
[0015]
[化学式1]
[0016][0017]
[化学式2]
[0018][0019]
(式(1)中,r1表示氢原子或甲基,r2表示碳原子数为1~6的亚烷基,n表示1~30的整数,式(2)中,r
11
表示氢原子或甲基,a1表示具有阳离子性的1价有机基团),
[0020]
上述单体混合物包含的含磷化合物中的、由式(1)表示的化合物的质量%为70质量%以上。
[0021]
[2]如[1]所述的含有共聚物的清漆的制造方法,其中,上述a1包含由下述式(2
‑
1)表示的结构,
[0022]
[化学式3]
[0023][0024]
(u
b1
、u
b2
及u
b3
各自独立地表示氢原子或碳原子数为1~5的直链或者支链烷基,an
‑
表示选自由卤化物离子、无机酸根离子、氢氧化物离子及异硫氰酸根离子组成的组中的阴离子)。
[0025]
[3]如[1]所述的含有共聚物的清漆的制造方法,其中,上述a1由下述式(2
‑
2)表示,
[0026]
[化学式4]
[0027][0028]
(r
21
表示可以被磷酸二酯键中断的碳原子数为1~6的亚烷基,u
b1
、u
b2
及u
b3
各自独立地表示氢原子或碳原子数为1~5的直链或者支链烷基,an
‑
表示选自由卤化物离子、无机酸根离子、氢氧化物离子及异硫氰酸根离子组成的组中的阴离子)。
[0029]
[4]涂覆膜形成用组合物的制造方法,其包括下述工序:
[0030]
使包含由下述式(1)及式(2)表示的化合物的单体混合物在聚合用溶剂中、在自由基聚合引发剂存在下共聚的工序;
[0031]
接下来添加溶剂的工序,
[0032]
[化学式5]
[0033][0034]
[化学式6]
[0035][0036]
(式(1)中,r1表示氢原子或甲基,r2表示碳原子数为1~6的亚烷基,n表示1~30的整数,式(2)中,r
11
表示氢原子或甲基,a1表示具有阳离子性的1价有机基团。)
[0037]
上述单体混合物包含的含磷化合物中的、由式(1)表示的化合物的质量%为70质量%以上。
[0038]
[5]如[4]所述的涂覆膜形成用组合物的制造方法,其中,所述涂覆膜具有与生物材料的相容性。
[0039]
[6]涂覆膜的制造方法,其包括将[4]或[5]所述的涂覆膜形成用组合物涂布于基板的工序。
[0040]
发明的效果
[0041]
根据本发明的方法,可以提供不发生凝胶化问题的含有共聚物的清漆的制造方法、涂覆膜形成用组合物的制造方法、涂覆膜的制造方法、优选具有与生物材料的相容性(例如,具有抑制生物材料附着的能力、细胞培养促进性)的涂覆膜的制造方法。
附图说明
[0042]
[图1]为示出试验例1中用实施例1的涂覆膜形成用组合物所涂覆的孔的细胞附着抑制效果的显微镜照片。
[0043]
[图2]为示出试验例1中用实施例2的涂覆膜形成用组合物所涂覆的孔的细胞附着抑制效果的显微镜照片。
[0044]
[图3]为示出试验例1中用实施例3的涂覆膜形成用组合物所涂覆的孔的细胞附着抑制效果的显微镜照片。
[0045]
[图4]为示出试验例1中用阳性对照(参考例1)的涂覆膜形成用组合物所涂覆的孔的细胞附着抑制效果的显微镜照片。
[0046]
[图5]为示出试验例1中阴性对照(未涂覆)的孔的细胞附着抑制效果的显微镜照
片。
具体实施方式
[0047]
《术语的说明》
[0048]
对于本发明中使用的术语而言,只要没有特别说明,具有以下的定义。
[0049]
作为“碳原子数为1~6的亚烷基”,可举出:亚甲基、亚乙基、正亚丙(三亚甲)基、亚丙基、环亚丙基、正亚丁基、异亚丁基、仲亚丁基、叔亚丁基、环亚丁基、1
‑
甲基
‑
环亚丙基、2
‑
甲基
‑
环亚丙基、正亚戊基、1
‑
甲基
‑
正亚丁基、2
‑
甲基
‑
正亚丁基、3
‑
甲基
‑
正亚丁基、1,1
‑
二甲基
‑
正亚丙基、1,2
‑
二甲基
‑
正亚丙基、2,2
‑
二甲基
‑
正亚丙基、1
‑
乙基
‑
正亚丙基、环亚戊基、1
‑
甲基
‑
环亚丁基、2
‑
甲基
‑
环亚丁基、3
‑
甲基
‑
环亚丁基、1,2
‑
二甲基
‑
环亚丙基、2,3
‑
二甲基
‑
环亚丙基、1
‑
乙基
‑
环亚丙基、2
‑
乙基
‑
环亚丙基、正亚己基、1
‑
甲基
‑
正亚戊基、2
‑
甲基
‑
正亚戊基、3
‑
甲基
‑
正亚戊基、4
‑
甲基
‑
正亚戊基、1,1
‑
二甲基
‑
正亚丁基、1,2
‑
二甲基
‑
正亚丁基、1,3
‑
二甲基
‑
正亚丁基、2,2
‑
二甲基
‑
正亚丁基、2,3
‑
二甲基
‑
正亚丁基、3,3
‑
二甲基
‑
正亚丁基、1
‑
乙基
‑
正亚丁基、2
‑
乙基
‑
正亚丁基、1,1,2
‑
三甲基
‑
正亚丙基、1,2,2
‑
三甲基
‑
正亚丙基、1
‑
乙基
‑1‑
甲基
‑
正亚丙基、1
‑
乙基
‑2‑
甲基
‑
正亚丙基、环亚己基、1
‑
甲基
‑
环亚戊基、2
‑
甲基
‑
环亚戊基、3
‑
甲基
‑
环亚戊基、1
‑
乙基
‑
环亚丁基、2
‑
乙基
‑
环亚丁基、3
‑
乙基
‑
环亚丁基、1,2
‑
二甲基
‑
环亚丁基、1,3
‑
二甲基
‑
环亚丁基、2,2
‑
二甲基
‑
环亚丁基、2,3
‑
二甲基
‑
环亚丁基、2,4
‑
二甲基
‑
环亚丁基、3,3
‑
二甲基
‑
环亚丁基、1
‑
正丙基
‑
环亚丙基、2
‑
正丙基
‑
环亚丙基、1
‑
异丙基
‑
环亚丙基、2
‑
异丙基
‑
环亚丙基、1,2,2
‑
三甲基
‑
环亚丙基、1,2,3
‑
三甲基
‑
环亚丙基、2,2,3
‑
三甲基
‑
环亚丙基、1
‑
乙基
‑2‑
甲基
‑
环亚丙基、2
‑
乙基
‑1‑
甲基
‑
环亚丙基、2
‑
乙基
‑2‑
甲基
‑
环亚丙基及2
‑
乙基
‑3‑
甲基
‑
环亚丙基等。
[0050]
另外,所谓“可以被磷酸二酯键中断的碳原子数为1~6的亚烷基”,是指“碳原子数为1~6的亚烷基”或者“被磷酸二酯键中断的碳原子数为1~6的亚烷基”。
[0051]“碳原子数为1~6的亚烷基”的例子如上所述。“被磷酸二酯键中断的、碳原子数为1~6的亚烷基”是指上述“碳原子数为1~6的亚烷基”中的至少一个亚甲基(
‑
ch2‑
)被磷酸二酯键置换的2价基团。
[0052]
作为“碳原子数为1~5的直链或者支链烷基”,可举出甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、1
‑
甲基丁基、2
‑
甲基丁基、3
‑
甲基丁基、1,1
‑
二甲基丙基、1,2
‑
二甲基丙基、2,2
‑
二甲基丙基或1
‑
乙基丙基。
[0053]
作为“卤化物离子”,可举出氟化物离子、氯化物离子、溴化物离子或碘化物离子。
[0054]
作为“无机酸根离子”,可举出碳酸根离子、硫酸根离子、磷酸根离子、磷酸氢根离子、磷酸二氢根离子、硝酸根离子、高氯酸根离子或硼酸根离子。
[0055]
作为“聚合用溶剂”,是指本发明的2种以上的单体的自身已知的共聚反应中使用的溶剂,可以为水、磷酸缓冲液或乙醇等醇、或将它们组合的混合溶剂,优选包含水或乙醇。进一步优选包含10质量%以上100质量%以下的水或乙醇。进一步优选包含50质量%以上100质量%以下的水或乙醇。进一步优选包含80质量%以上100质量%以下的水或乙醇。进一步优选包含90质量%以上100质量%以下的水或乙醇。优选水和乙醇的合计为100质量%。
[0056]
作为“自由基聚合引发剂”,可以为“热自由基聚合引发剂”或“光自由基聚合引发
剂”。
[0057]
作为“热自由基聚合引发剂”,可使用2,2
’‑
偶氮双(异丁腈)、2,2
’‑
偶氮双(2
‑
甲基丁腈)、2,2
’‑
偶氮双(2,4
‑
二甲基戊腈)(fujifilm wako pure chemical corporation制品名;v
‑
65,10小时半衰期温度:51℃)、4,4
’‑
偶氮双(4
‑
氰基戊酸)、2,2
’‑
偶氮双(4
‑
甲氧基
‑
2,4
‑
二甲基戊腈)、1,1
’‑
偶氮双(环己烷
‑1‑
甲腈)、1
‑
[(1
‑
氰基
‑1‑
甲基乙基)偶氮]甲酰胺、2,2
’‑
偶氮双[2
‑
(2
‑
咪唑啉
‑2‑
基)丙烷]二盐酸盐(fujifilm wako pure chemical corporation;va
‑
044,10小时半衰期温度:44℃)、2,2
’‑
偶氮双[2
‑
(2
‑
咪唑啉
‑2‑
基)丙烷](fujifilm wako pure chemical corporation;va
‑
061,10小时半衰期温度:61℃)、2,2
’‑
偶氮双(2
‑
甲基丙脒)二盐酸盐、2,2
’‑
偶氮(2
‑
甲基
‑
n
‑
(2
‑
羟基乙基)丙酰胺(fujifilm wako pure chemical corporation制品名;va
‑
086,10小时半衰期温度:86℃)、过氧化苯甲酰(bpo)、2,2
’‑
偶氮双(n
‑
(2
‑
羧基乙基)
‑2‑
甲基丙脒)n
‑
水合物(fujifilm wako pure chemical corporation制品名;va
‑
057,10小时半衰期温度:57℃)、4,4
’‑
偶氮双(4
‑
氰基戊酸)(fujifilm wako pure chemical corporation制品名;va
‑
501)、2,2
’‑
偶氮双[2
‑
(2
‑
咪唑啉
‑2‑
基)丙烷]二硫酸盐二水合物(fujifilm wako pure chemical corporation制品名;va
‑
046b,10小时半衰期温度:46℃)、2,2
’‑
偶氮双(2
‑
脒基丙烷)二盐酸盐(fujifilm wako pure chemical corporation制品名;v
‑
50,10小时半衰期温度:56℃)、过二硫酸或叔丁基过氧化氢、二甲基1,1
’‑
偶氮双(1
‑
环己烷甲酸酯)(fujifilm wako pure chemical corporation制品名;ve
‑
073)等。
[0058]
作为“光自由基聚合引发剂”,可举出苯乙酮、氯苯乙酮、羟基苯乙酮、2
‑
氨基苯乙酮、二烷基氨基苯乙酮、2,2
‑
二乙氧基苯乙酮、2,2
‑
二甲氧基
‑2′‑
苯基苯乙酮(basf公司制品名;irgacure651)、2
‑
羟基
‑2‑
甲基1
‑
苯基丙酮(basf公司制品名;irgacure1173)、1
‑
[4
‑
(2
‑
羟基乙氧基)
‑
苯基]
‑2‑
羟基甲基丙酮(basf公司制品名;irgacure2959)、2
‑
羟基
‑1‑
{4
‑
[4
‑
(2
‑
羟基
‑2‑
甲基丙酰基)苄基]苯基}
‑2‑
甲基
‑1‑
丙烷
‑1‑
酮(basf公司制品名;irgacure127)、2
‑
甲基
‑1‑
[4
‑
(甲硫基)苯基]
‑2‑
吗啉基丙烷
‑1‑
酮(basf公司制品名;irgacure907)、2
‑
苄基
‑2‑
(二甲基氨基)
‑4‑
吗啉基丁酰苯(basf公司制品名;irgacure369)等苯乙酮类;苯偶姻、苯偶姻甲基醚、苯偶姻乙基醚、苯偶姻异丙基醚、苯偶姻异丁基醚、1
‑
羟基环己基苯基酮(basf公司制品名;irgacure184)等苯偶姻类;二苯甲酮、苯甲酰基苯甲酸、苯甲酰基苯甲酸甲酯、甲基
‑
邻苯甲酰基苯甲酸酯、4
‑
苯基二苯甲酮、羟基二苯甲酮、羟基丙基二苯甲酮、丙烯酰基二苯甲酮、4,4
′‑
双(二甲基氨基)二苯甲酮、4,4
′‑
二氯二苯甲酮等二苯甲酮类;噻吨酮、2
‑
氯噻吨酮、2
‑
甲基噻吨酮、二乙基噻吨酮、二甲基噻吨酮等噻吨酮类;2,4,6
‑
三甲基苯甲酰基
‑
二苯基膦氧化物(basf公司制品名;irgacure tpo)、双(2,4,6
‑
三甲基苯甲酰基)
‑
苯基氧化膦(basf公司制品名;irgacure819)等酰基氧化膦类;氧基苯基乙酸、2
‑
[2
‑
氧代
‑2‑
苯基乙酰氧基乙氧基]乙酯与氧基苯基乙酸、2
‑
(2
‑
羟基乙氧基)乙酯的混合物(basf公司制品名;irgacure754)、苯甲酰基甲酸甲酯(basf公司制品名;irgacure mbf)、α
‑
酰基肟酯、苄基
‑
(邻乙氧基羰基)
‑
α
‑
单肟、乙醛酸酯、2
‑
乙基蒽醌、樟脑醌、四甲基秋兰姆硫化物、偶氮二异丁腈、过氧化苯甲酰、二烷基过氧化物、过氧化新戊酸叔丁酯;等等。
[0059]
所谓“溶剂”,为本发明的涂覆膜形成用组合物中使用的溶剂,可举出水、磷酸缓冲生理盐水(pbs)、醇。作为醇,可举出碳原子数为2~6的醇,例如,乙醇、丙醇、异丙醇、1
‑
丁
醇、2
‑
丁醇、异丁醇、叔丁醇、1
‑
戊醇、2
‑
戊醇、3
‑
戊醇、1
‑
庚醇、2
‑
庚醇、2,2
‑
二甲基
‑1‑
丙醇(=新戊醇)、2
‑
甲基
‑1‑
丙醇、2
‑
甲基
‑1‑
丁醇、2
‑
甲基
‑2‑
丁醇(=叔戊醇)、3
‑
甲基
‑1‑
丁醇、3
‑
甲基
‑3‑
戊醇、环戊醇、1
‑
己醇、2
‑
己醇、3
‑
己醇、2,3
‑
二甲基
‑2‑
丁醇、3,3
‑
二甲基
‑1‑
丁醇、3,3
‑
二甲基
‑2‑
丁醇、2
‑
乙基
‑1‑
丁醇、2
‑
甲基
‑1‑
戊醇、2
‑
甲基
‑2‑
戊醇、2
‑
甲基
‑3‑
戊醇、3
‑
甲基
‑1‑
戊醇、3
‑
甲基
‑2‑
戊醇、3
‑
甲基
‑3‑
戊醇、4
‑
甲基
‑1‑
戊醇、4
‑
甲基
‑2‑
戊醇、4
‑
甲基
‑3‑
戊醇及环己醇,可单独使用或使用它们组合而成的混合溶剂,但从共聚物的溶解性的观点考虑,优选从水、pbs、乙醇及丙醇中选择。
[0060]
作为“生物材料”,可举出蛋白质、糖、核酸、细胞或它们的组合。例如,作为蛋白质,可举出纤维蛋白原、牛血清白蛋白(bsa)、人白蛋白、各种球蛋白、β
‑
脂蛋白、各种抗体(igg、iga、igm)、过氧化物酶、各种补体、各种凝集素、纤连蛋白、溶菌酶、冯
·
维勒布兰德因子(vwf,von willebrand’s factor)、血清γ
‑
球蛋白、胃蛋白酶、卵清白蛋白、胰岛素、组蛋白、核糖核酸酶、胶原蛋白、细胞色素c;例如,作为糖,可举出葡萄糖、半乳糖、甘露糖、果糖、肝素、透明质酸;例如,作为核酸,可举出脱氧核糖核酸(dna)、核糖核酸(rna);例如,作为细胞,可举出成纤维细胞、骨髓细胞、β淋巴细胞、τ淋巴细胞、嗜中性粒细胞、红细胞、血小板、巨噬细胞、单核细胞、骨细胞、周皮细胞、树突状细胞、角质形成细胞、脂肪细胞、间质细胞、上皮细胞、表皮细胞、内皮细胞、血管内皮细胞、肝实质细胞、软骨细胞、卵丘细胞、神经细胞、神经胶质细胞、神经元、少突胶质细胞、小胶质细胞、星形胶质细胞、心脏细胞、食道细胞、肌肉细胞(例如,平滑肌细胞或骨骼肌细胞)、胰岛β细胞、黑色素细胞、定向造血干细胞、单核细胞、胚胎干细胞(es细胞)、胚胎肿瘤细胞、胚胎生殖干细胞、诱导多能干细胞(ips细胞)、神经干细胞、造血干细胞、间充质干细胞、肝干细胞、胰干细胞、肌肉干细胞、生殖干细胞、肠干细胞、癌干细胞、毛囊干细胞、及各种细胞株(例如,hct116、huh7、hek293(人源胚胎肾细胞)、hela(人宫颈癌细胞株)、hepg2(人肝癌细胞株)、ut7/tpo(人白血病细胞株)、cho(中国仓鼠卵巢细胞株)、mdck、mdbk、bhk、c
‑
33a、ht
‑
29、ae
‑
1、3d9、ns0/1、jurkat、nih3t3、pc12、s2、sf9、sf21、high five、vero);等等。
[0061]
所谓“具有抑制生物材料附着的能力”,例如,生物材料为血小板时,是指:通过利用日本再表2016/093293的实施例中记载的方法实施的血小板附着试验与无涂覆膜进行比较的情况下的相对血小板附着数(%)((实施例的血小板附着数(个))/(比较例的血小板附着数(个)))为50%以下,优选为30%以下,进一步优选为20%以下;
[0062]
生物材料为蛋白质时,是指:通过利用实施例中记载的方法进行的qcm
‑
d测定与无涂覆膜进行比较的情况下的相对每单位面积的质量(%)((实施例的每单位面积的质量(ng/cm2)/(比较例的每单位面积的质量(ng/cm2)))为50%以下,优选为30%以下,进一步优选为20%以下;
[0063]
生物材料为细胞时,是指:通过利用日本再表2016/093293的实施例中记载的方法进行的荧光显微镜观察与无涂覆膜进行比较的情况下的相对吸光度(wst o.d.450nm)(%)((实施例的吸光度(wst o.d.450nm))/(比较例的吸光度(wst o.d.450nm)))为50%以下,优选为30%以下,进一步优选为20%以下。
[0064]
<含有共聚物的清漆的制造方法>
[0065]
本发明涉及含有共聚物的清漆的制造方法,其包括:使包含由下述式(1)及式(2)表示的化合物的单体混合物的单体混合物在聚合用溶剂中、在自由基聚合引发剂存在下共
聚的工序,
[0066]
[化学式7]
[0067][0068]
[化学式8]
[0069][0070]
(式(1)中,r1表示氢原子或甲基,r2表示碳原子数为1~6的亚烷基,n表示1~30的整数;式(2)中,r
11
表示氢原子或甲基,a1表示具有阳离子性的1价有机基团)
[0071]
上述单体混合物包含的含磷化合物中的、由式(1)表示的化合物的质量%(纯度)为70质量%以上。
[0072]
本发明中“单体混合物”是指上述由式(1)及式(2)表示的化合物全部、以及包含供于共聚反应工序的全部化合物的混合物。即,换言之,所谓“单体混合物包含的含磷化合物中的、由式(1)表示的化合物的质量%(绝对质量%)”,是指相对于供于共聚反应工序的单体混合物所包含的含磷化合物的总量而言,由式(1)表示的化合物的纯度(含量)为70质量%以上。
[0073]
所谓上述含磷化合物,是指化合物一分子中包含至少1个以上的磷原子的化合物,为由式(1)表示的化合物、以及源自由式(1)表示的化合物的杂质(例如,相当于由式(1)表示的化合物的二聚体的磷酸二酯化合物等)。
[0074]
n表示1~30的整数,优选为1~20的整数、1~10的整数、1~7的整数、2~6的整数、3~5的整数。
[0075]
由式(1)表示的化合物也可以使用日本特开2018
‑
27927号公报中记载的单体。
[0076]
上述共聚物制造中使用的单体混合物所包含的含磷化合物中的、由式(1)表示的化合物的质量%(绝对质量%)例如可通过实施例中记载的含磷化合物的组成分析来求出。
[0077]
由式(1)表示的化合物的、含磷化合物中的质量%(绝对质量%)优选为70质量%以上、75质量%以上、80质量%以上、85质量%以上、90质量%以上、95质量%以上。最优选为100质量%。
[0078]
在后述的式(2)表示的化合物的r
21
为被磷酸二酯键中断的碳原子数为1~6的亚烷基的情况下,本发明涉及的共聚物中的由式(1)表示的化合物衍生的重复单元的比例为5摩尔%~80摩尔%,优选为7摩尔%~70摩尔%,优选为8摩尔%~65摩尔%,进一步优选为10摩尔%~60摩尔%。
[0079]
在后述的式(2)表示的化合物的r
21
未被磷酸二酯键中断(即,r
21
为碳原子数为1~6的亚烷基)的情况下,本发明涉及的共聚物中的由式(1)表示的化合物衍生的重复单元的
比例为10摩尔%~80摩尔%,优选为30摩尔%~70摩尔%,进一步优选为40摩尔%~60摩尔%。
[0080]
需要说明的是,本发明中涉及的共聚物也可以包含2种以上的由式(1)表示的化合物衍生的重复单元,优选为1种或2种,优选为1种。
[0081]
就本发明涉及的共聚物中的由式(2)表示的化合物衍生的重复单元的比例而言,可以是相对于全部共聚物减去上述式(1)后的剩余部分全体,也可以是减去上述式(1)和下述记载的第3成分的合计比例后的剩余部分。需要说明的是,本发明涉及的共聚物也可以包含2种以上的由式(2)表示的化合物衍生的重复单元。
[0082]
本发明涉及的单体混合物可进一步包含烯键式不饱和单体、或者多糖类或其衍生物作为任意的第3成分。作为烯键式不饱和单体的例子,可以举出选自由(甲基)丙烯酸及其酯;乙酸乙烯酯;乙烯基吡咯烷酮;乙烯;乙烯醇;以及它们的亲水性的官能性衍生物组成的组中的1种或2种以上的烯键式不饱和单体。作为多糖类或其衍生物的例子,可以举出羟烷基纤维素(例如,羟乙基纤维素或羟丙基纤维素)等纤维素系高分子、淀粉、葡聚糖、凝胶多糖。
[0083]
所谓亲水性的官能性衍生物,是指具有亲水性的官能团或结构的烯键式不饱和单体。作为亲水性的官能性基团或结构的例子,可举出酰胺结构;亚烷基二醇残基;氨基;以及亚磺酰基;等等。
[0084]
酰胺结构是指下述式表示的基团,
[0085]
[化学式9]
[0086][0087]
[其中,r
16
、r
17
及r
18
相互独立为氢原子或有机基团(例如,甲基、羟基甲基或羟基乙基等)]。
[0088]
作为具有这样的结构的烯键式不饱和单体的例子,可以举出(甲基)丙烯酰胺、n
‑
(羟基甲基)(甲基)丙烯酰胺等。此外,具有这样的结构的单体或聚合物例如已经在日本特开2010
‑
169604号公报等中公开。
[0089]
亚烷基二醇残基是指亚烷基二醇(ho
‑
alk
‑
oh;其中alk为碳原子数1~10的亚烷基)的单侧末端或两末端的羟基与其他化合物进行缩合反应后所残留的亚烷基氧基(
‑
alk
‑
o
‑
),也包括重复亚烷基氧基单元而成的聚(亚烷基氧基)基团。作为具有这样的结构的烯键式不饱和单体的例子,可举出(甲基)丙烯酸2
‑
羟基乙酯、甲氧基聚乙二醇(甲基)丙烯酸酯等。此外,具有这样的结构的单体或聚合物例如已经在日本特开2008
‑
533489号公报等中公开。
[0090]
氨基是指由式:
‑
nh2、
‑
nhr
19
或
‑
nr
20
r
21
[其中,r
19
、r
20
及r
21
相互独立地为有机基团(例如,碳原子数为1~5的直链或者支链烷基等)]表示的基团。本发明中的氨基包括经季铵化或氯化的氨基。作为具有这样的结构的烯键式不饱和单体的例子,可举出(甲基)丙烯酸二甲基氨基乙酯、(甲基)丙烯酸2
‑
(叔丁基氨基)乙酯、甲基丙烯酰基胆碱氯化物
(methacroylcholine chloride)等。
[0091]
亚磺酰基是指下述式表示的基团,
[0092]
[化学式10]
[0093][0094]
[其中,r
22
为有机基团(例如,碳原子数为1~10的有机基团,优选为具有一个以上羟基的碳原子数1~10的烷基等]。
[0095]
作为具有这样的结构的聚合物,可举出在日本特开2014
‑
48278号公报等中公开的共聚物。
[0096]
(共聚物的重均分子量)
[0097]
本发明涉及的共聚物的重量分子量只要为数千至数百万左右即可,优选为5,000~5,000,000。进一步优选为10,000~2,000,000。另外,为无规共聚物、嵌段共聚物、接枝共聚物均可,对用于制造该共聚物的共聚反应自身没有特别限制,可使用自由基聚合、离子聚合、光聚合、利用了大分子单体、乳液聚合的聚合等已知的在溶液中进行合成的方法。根据它们的目标用途,可单独使用本发明的共聚物中的任一种,也可将多种共聚物混合并改变其比率而使用。
[0098]
(共聚反应)
[0099]
本发明的含有共聚物的清漆可以通过包括如下工序的制造方法来制造:在聚合用溶剂中,使包含由上述式(1)及(2)表示的化合物的单体混合物以两化合物的合计浓度0.01质量%~20质量%进行反应(聚合)。
[0100]
作为自由基聚合引发剂的添加量,相对于用于聚合的单体的合计重量而言为0.05质量%~10质量%。
[0101]
对于反应条件而言,通过油浴等将反应容器加热至50℃~200℃并进行1小时~48小时搅拌,更优选加热至80℃~150℃并进行5小时~30小时搅拌,使得聚合反应进行,可得到本发明的共聚物。反应气氛可以大气下,优选为氮气氛。
[0102]
作为反应步骤,可以将由式(1)及式(2)表示的化合物、以及根据需要的第3成分单体全部加入到室温的聚合用溶剂后,加热至上述温度而使其聚合;也可以将由式(1)及式(2)表示的化合物、以及根据需要的第3成分单体的混合物的全部或一部分逐次少量地滴加到预先经加热的聚合用溶剂中。
[0103]
根据后者的反应步骤,对于本发明的含有共聚物的清漆而言,可以通过包括如下工序的制造方法来制备:将含有包含上述由式(1)及式(2)表示的化合物的单体混合物、聚合用溶剂及聚合引发剂的混合物滴加到保持在比聚合引发剂的10小时半衰期温度高的温度的溶剂中,使其发生反应(聚合)。
[0104]
对于上述a1而言,具有阳离子性的1价有机基团为具有阳离子性的有机基团,例如可举出包含叔胺、季铵盐的基团。或者,上述a1也可以为包含芳香环的阳离子性基团,例如可举出包含吡啶骨架的基团等。
[0105]
上述a1优选包含由下述式(2
‑
1)表示的结构,
[0106]
[化学式11]
[0107][0108]
(u
b1
、u
b2
及u
b3
各自独立地表示氢原子或碳原子数为1~5的直链或者支链烷基,an
‑
表示选自由卤化物离子、无机酸根离子、氢氧化物离子及异硫氰酸根离子组成的组的阴离子)。
[0109]
作为上述an
‑
,优选为卤化物离子、硫酸根离子、磷酸根离子、氢氧化物离子及异硫氰酸根离子,特别优选为卤化物离子。
[0110]
上述a1优选由下述式(2
‑
2)表示,
[0111]
[化学式12]
[0112][0113]
(r
21
表示可以被磷酸二酯键中断的碳原子数为1~6的亚烷基,u
b1
、u
b2
及u
b3
各自独立地表示氢原子或碳原子数为1~5的直链或者支链烷基,an
‑
表示选自由卤化物离子、无机酸根离子、氢氧化物离子及异硫氰酸根离子组成的组的阴离子)。
[0114]
由上述式(2
‑
2)表示的结构可以为甜菜碱结构。甜菜碱结构是指具有季铵型的阳离子结构和酸性的阴离子结构的两性中心的化合物的一价或二价的基团,例如可以举出磷酰胆碱基。
[0115]
[化学式13]
[0116][0117]
作为具有这样的结构的式(2)表示的化合物的例子,可以举出2
‑
甲基丙烯酰氧基乙基磷酰胆碱(mpc)等。
[0118]
<涂覆膜形成用组合物的制造方法>
[0119]
涂覆膜形成用组合物的制造方法,其包括下述工序:
[0120]
使包含由下述式(1)及式(2)表示的化合物的单体混合物在聚合用溶剂中、在自由基聚合引发剂存在下共聚的工序;
[0121]
接下来添加溶剂的工序,
[0122]
[化学式14]
[0123][0124]
[化学式15]
[0125][0126]
(式(1)中,r1表示氢原子或甲基,r2表示碳原子数为1~6的亚烷基,n表示1~30的整数,式(2)中,r
11
表示氢原子或甲基,a1表示具有阳离子性的1价有机基团)
[0127]
包含上述单体混合物的磷化合物中的、由式(1)表示的化合物的质量%(纯度)为70质量%以上。根据本发明的方法,可以制造不发生共聚物的凝胶化等、共聚物稳定地溶解于溶剂中或均匀地分散的涂覆膜形成用组合物。
[0128]
对于本发明的涂覆膜形成用组合物而言,可通过使包含如上所述的各化合物的单体混合物共聚后、用自身已知的方法添加上述溶剂来制造。
[0129]
本发明的涂覆膜形成用组合物的制造方法优选为具有与生物材料的相容性的涂覆膜形成用组合物的制造方法。
[0130]
所谓与生物材料的相容性,是指具有上述的抑制生物材料附着的能力、以及细胞培养促进性(例如为日本特开2014
‑
162865号公报中记载的细胞培养容器被覆用聚合物、日本特愿2018
‑
157444号公报记载的细胞培养的基底膜形成用)。
[0131]
作为本发明涉及的涂覆膜形成用组合物中的固态成分的浓度,为了均匀地形成涂覆膜,优选为0.01~50质量%。另外,作为涂覆膜形成用组合物中的共聚物的浓度,优选为0.01~4质量%,更优选为0.01~3质量%,特别优选为0.01~2质量%,进一步优选为0.01~1质量%。共聚物的浓度为0.01质量%以下时,得到的涂覆膜形成用组合物的共聚物的浓度过低,无法形成膜厚充分的涂覆膜,为4质量%以上时,涂覆膜形成用组合物的保存稳定性变差,可能发生溶解物的析出、凝胶化。
[0132]
为了调节本发明涉及的涂覆膜形成用组合物中的共聚物的离子平衡,在得到本发明的涂覆膜时,还可包括预先调节涂覆膜形成用组合物中的ph的工序。ph调节例如可通过下述方式实施:向含有上述共聚物和溶剂的组合物中添加ph调节剂,使该组合物的ph成为3.0~13.5、优选3.5~8.5、进一步优选3.5~7.0、或者优选8.5~13.5、进一步优选10.0~13.5。可使用的ph调节剂的种类及其量可根据上述共聚物的浓度、其阴离子与阳离子的存在比等适当选择。
[0133]
作为ph调节剂的例子,可举出氨、二乙醇胺、吡啶、n
‑
甲基
‑
d
‑
葡萄糖胺、三(羟基甲基)氨基甲烷等有机胺;氢氧化钾、氢氧化钠等碱金属氢氧化物;氯化钾、氯化钠等碱金属卤化物;硫酸、磷酸、盐酸、碳酸等无机酸或其碱金属盐;胆碱等季铵阳离子;或者它们的混合物(例如,磷酸缓冲生理盐水等缓冲液)。这些中,优选氨、二乙醇胺、氢氧化钠、胆碱、n
‑
甲基
‑
d
‑
葡萄糖胺、三(羟基甲基)氨基甲烷,特别优选氨、二乙醇胺、氢氧化钠及胆碱。
[0134]
因此,本发明涉及下述涂覆膜形成用组合物的制造方法,所述涂覆膜形成用组合物包含:(i)共聚物,所述共聚物包含由上述式(1)表示的化合物衍生的重复单元、和由上述式(2)表示的化合物衍生的重复单元;(ii)溶剂;及根据情况的(iii)ph调节剂。共聚物、溶剂及ph调节剂的具体例子如上所述。
[0135]
此外,对于本发明的涂覆膜形成用组合物而言,除了上述共聚物和溶剂之外,根据需要,也可在不损害得到的涂覆膜的性能的范围内添加其他物质。作为其他物质,可举出防腐剂、表面活性剂、提高与基材的密合性的底漆、防霉剂及糖类等。
[0136]
<涂覆膜的制造方法>
[0137]
本发明的涂覆膜的制造方法为包含将上述的涂覆膜形成用组合物涂布于基板的工序的涂覆膜的制造方法。
[0138]
将本发明涉及的涂覆膜形成用组合物涂布于基体并使其干燥而形成涂覆膜。
[0139]
作为用于形成本发明的涂覆膜的基体,可举出玻璃、含有金属的化合物或含有准金属的化合物、活性炭或树脂。关于含有金属的化合物或含有准金属的化合物,例如,可举出基本成分为金属氧化物、经高温下的热处理烧结而成的烧结体即陶瓷、硅这样的半导体、金属氧化物或准金属氧化物(硅氧化物、氧化铝等)、金属碳化物或准金属碳化物、金属氮化物或准金属氮化物(硅氮化物等)、金属硼化物或准金属硼化物等无机化合物的成型体等无机固体材料、铝、镍钛、不锈钢(sus304、sus316、sus316l等)。
[0140]
作为树脂,可以是天然树脂或合成树脂中的任意,作为天然树脂,可优选使用纤维素、三乙酸纤维素(cta)、固定了硫酸葡聚糖的纤维素等,作为合成树脂,可优选使用聚丙烯腈(pan)、聚酯系聚合物合金(pepa)、聚苯乙烯(ps)、聚砜(psf)、聚对苯二甲酸乙二醇酯(pet)、聚甲基丙烯酸甲酯(pmma)、聚乙烯醇(pva)、聚氨酯(pu)、乙烯
‑
乙烯醇(eval)、聚乙烯(pe)、聚酯(pe)、聚丙烯(pp)、聚偏二氟乙烯(pvdf)、聚醚砜(pes)、聚碳酸酯(pc)、聚氯乙烯(pvc)、聚四氟乙烯(ptfe)、超高分子量聚乙烯(uhpe)、聚二甲基硅氧烷(pdms)、丙烯腈
‑
丁二烯
‑
苯乙烯树脂(abs)、teflon(注册商标)、环烯烃聚合物(cop)(例如,zeonor(注册商标)、zeonex(注册商标)(日本zeon corporation制))或各种离子交换树脂等,更优选聚苯乙烯(ps)、聚醚砜(pes)、聚丙烯(pp)及环烯烃聚合物(cop),特别优选聚苯乙烯(ps)及聚醚砜(pes)。由于本发明的涂覆膜可在低温干燥下形成,因此也可应用于耐热性低的树脂等。
[0141]
为了形成本发明的涂覆膜,将上述的涂覆膜形成用组合物涂覆于基体的表面的至少一部分。作为涂布方法,没有特别限制,可使用通常的旋涂法、浸涂法、溶剂浇铸法等涂布法。
[0142]
本发明涉及的涂覆膜的干燥工序在大气下或真空下、优选在
‑
200℃~200℃的温度范围内进行。通过干燥工序将上述涂覆膜形成用组合物中的溶剂去除,并且本发明涉及的共聚物的由式(1)表示的化合物的磷酸部分及由式(2)表示的化合物的阳离子性部分形成离子键而完全固着于基体。
[0143]
涂覆膜例如也可利用室温(10℃~35℃,例如25℃)的干燥而形成,为了更快速地形成涂覆膜,例如可于40℃~50℃进行干燥。另外,也可利用基于冷冻干燥(freeze drying)法的极低温~低温(
‑
200℃~
‑
30℃左右)下的干燥工序。冷冻干燥被称为真空冷冻干燥,通常是用制冷剂将想要干燥的物体冷却并在真空状态下通过升华而将溶剂除去的方法。关于冷冻干燥中可使用的常规的制冷剂,可举出干冰与甲醇的混合介质(
‑
78℃)、液氮
(
‑
196℃)等。
[0144]
干燥温度为
‑
200℃以下时,必须使用非常规的制冷剂,欠缺通用性,并且,为了使溶剂升华,干燥需要长时间,效率差。干燥温度为200℃以上时,涂覆膜表面的离子键合反应过度进行,该表面丧失亲水性,无法发挥抑制生物材料附着的能力。更优选的干燥温度为10℃~190℃、10℃~180℃、10℃~170℃、10℃~160℃、20℃~180℃、20℃~170℃、20℃~160℃、20℃~150℃、25℃~150℃。
[0145]
干燥后,为了消除在该涂覆膜上残留的杂质、未反应的单体等、以及为了调节膜中的共聚物的离子平衡,可实施利用选自水和含有电解质的水溶液中的至少1种的溶剂进行洗涤的工序。洗涤优选为流水洗涤或超声波洗涤等。上述水和含有电解质的水溶液例如可以是在40℃~95℃的范围内经加热的水或含有电解质的水溶液。含有电解质的水溶液优选为pbs、生理盐水(仅含有氯化钠的水溶液)、杜氏磷酸盐缓冲生理盐水、tris缓冲生理盐水、hepes缓冲生理盐水及veronal缓冲生理盐水,特别优选为pbs。固着后,即使用水、pbs及醇等洗涤,涂覆膜也不溶出,牢固地固着于基体。即使在形成的涂覆膜上附着有生物材料,也可随后通过水洗等容易地将其除去,形成有本发明的涂覆膜的基体表面具有抑制生物材料附着的能力。
[0146]
作为本发明的涂覆膜的应用实例,例如有人工透析器的过滤器用涂覆膜,对于本发明的涂覆膜而言,涂覆膜固着于被用于过滤器的合成树脂(例如pes、ps及psf等)的固着性、固着后的耐久性也良好。基体的形态没有特别限制,可举出基板、纤维、粒子、凝胶形态、多孔质形态等,形状可以是平板也可以是曲面。
[0147]
例如,在制作人工透析器的过滤器用涂覆膜时,可向由上述原材料制作的例如形成为直径0.1~500μm的中空纤维形状的过滤器的内侧,通入本发明涉及的涂覆膜形成用组合物,然后经干燥工序、洗涤工序(热水(例如40℃~95℃)洗涤等)而制作。
[0148]
根据需要,为了进行灭菌,有时也可进行γ射线、环氧乙烷、高压釜等的处理。
[0149]
本发明的涂覆膜的膜厚优选为进一步优选为10~最优选为
[0150]
本发明的涂覆膜由于具有抑制生物材料附着的能力,因而可作为医疗用基材用涂覆膜而合适地使用。例如,可在去白细胞过滤器、输血过滤器、去病毒过滤器、除微小凝血块过滤器、血液净化用组件、人工心脏、人工肺、血液回路、人工血管、血管旁路管、医疗用管、人工瓣膜、套管(canula)、支架、导管、血管内导管、气囊导管、导丝、缝合线、留置针、分流器(shunt)、人工关节、人工髋关节、血袋、血液保存容器、手术用辅助器具、防粘连膜、创伤被覆材料等中合适地使用。其中,所谓血液净化用组件,是指使血液在体外循环、具有去除血中的废物、有害物质的功能的组件,可举出人工肾脏、毒素吸附过滤器或柱等。
[0151]
另外,本发明的涂覆膜作为烧瓶、培养皿、培养板等细胞培养容器、抑制蛋白质附着的各种研究用器具的涂覆膜是有用的。
[0152]
另外,本发明的涂覆膜形成用组合物作为化妆品用材料、隐形眼镜护理用品用材料、皮肤护理用纤维加工剂、生物化学研究用诊断剂用材料、用于抑制临床诊断法中广泛使用的酶联免疫吸附测定(elisa)法、乳胶凝集法中的非特异性吸附的封闭剂(blocking agent)、用于使酶、抗体等蛋白质稳定化的稳定化剂也是有用的。
[0153]
此外,本发明的涂覆膜作为用于化妆用品(toiletry)、个人护理用品、洗剂、医药
品、准医药品、纤维、用于防污材料的涂覆膜也是有用的。
[0154]
实施例
[0155]
以下参照实施例等而更详细地说明本发明,但本发明不受以下实施例等的任何限制。
[0156]
<单体的纯度测定方法>
[0157]
对于下述合成例所用的酸式磷酰氧基聚丙二醇单甲基丙烯酸酯(环氧丙烷的平均加成摩尔数为5)(制品名;ppm
‑
5p,东邦化学株式会社制)的质量%(纯度)而言,使用
31
p
‑
nmr测定进行含磷化合物的组成分析后,使用将酸式磷酰氧基聚丙二醇单甲基丙烯酸酯(环氧丙烷的平均加成摩尔数为5)的加成摩尔数设为5时的分子量进行换算而求出。
[0158]
(
31
p
‑
nmr测定条件)
[0159]
·
装置:avance iii hd(500mhz)
[0160]
·
溶剂:氘代丙酮
[0161]
·
测定温度:室温(23℃)
[0162]
·
测定条件:非解耦法(non
‑
decoupling)
[0163]
·
测定数据点:131072(128k)
[0164]
·
脉冲宽度:90
°
脉冲(14μ秒)
[0165]
·
测定范围:
‑
50~10ppm
[0166]
·
累积次数:256次
[0167]
<共聚物的分子量测定方法>
[0168]
下述合成例所示的共聚物的重均分子量是基于凝胶过滤色谱法(gel filtration chromatography)(以下,简称为gfc)的测定结果。
[0169]
(测定条件)
[0170]
·
装置:hlc
‑
8320gpc(东曹株式会社制)
[0171]
·
gfc柱:tskgel gmpwxl(7.8mmi.d.
×
30cm)
×
2~3根
[0172]
·
洗脱液:含离子性物质水溶液、或者etoh(乙醇)的混合溶液
[0173]
·
柱温:40℃
[0174]
·
检测器:ri
[0175]
·
进样浓度:聚合物固态成分为0.05~0.5%
[0176]
·
进样量:100μl
[0177]
·
标准曲线:三次近似曲线
[0178]
·
标准试样:聚环氧乙烷(agilent公司制)
×
10种
[0179]
<合成例1>
[0180]
向酸式磷酰氧基聚丙二醇单甲基丙烯酸酯(环氧丙烷的平均加成摩尔数为5)(制品名;ppm
‑
5p,东邦化学株式会社制,质量%(纯度)95.6质量%)2.27g中添加乙醇16.70g,充分地溶解。接下来,添加甲基丙烯酸2
‑
(二甲基氨基)乙酯(东京化成工业株式会社制)0.80g、纯水11.23g,充分搅拌后,添加二甲基1,1
′‑
偶氮双(1
‑
环己烷甲酸酯)(制品名;ve
‑
073,fujifilm wako pure chemical corporation制)15.7mg。充分地搅拌直至均匀,将加入了上述所有物质的混合溶液加入到100ml烧瓶内并进行氮置换,一边搅拌一边升温至回流温度(油浴温度:设定为95℃)。在维持24小时上述环境的状态下进行加热搅拌,由此得到
固态成分约10.60质量%的含有共聚物的清漆。得到的透明液体的利用gfc测得的重均分子量为约310,000。
[0181]
<合成例2>
[0182]
向纯水10.46g与乙醇10.14g的混合溶剂中添加2
‑
甲基丙烯酰氧基乙基磷酰胆碱(mpc,东京化成工业株式会社制)0.89g及酸式磷酰氧基聚丙二醇单甲基丙烯酸酯(环氧丙烷的平均加成摩尔数为5)(制品名;ppm
‑
5p,东邦化学株式会社制,质量%(纯度)95.6质量%)1.37g,并进行充分搅拌。接下来,添加二甲基1,1
′‑
偶氮双(1
‑
环己烷甲酸酯)(制品名;ve
‑
073,fujifilm wako pure chemical corporation制)6mg,充分地搅拌直至均匀。使加入有该混合溶液的100ml烧瓶内进行氮置换,升温至70℃后加热搅拌7小时,由此得到固态成分约9.93质量%的含有共聚物的清漆。得到的透明液体的利用gfc测得的重均分子量为约750,000。
[0183]
<合成例3>
[0184]
向纯水8.51g与乙醇8.59g的混合溶剂中添加2
‑
甲基丙烯酰氧基乙基磷酰胆碱(mpc,东京化成工业株式会社制)1.25g及酸式磷酰氧基聚丙二醇单甲基丙烯酸酯(环氧丙烷的平均加成摩尔数为5)(制品名;ppm
‑
5p,东邦化学株式会社制,质量%(纯度)95.6质量%)0.84g,进行充分搅拌。接下来,添加二甲基1,1
′‑
偶氮双(1
‑
环己烷甲酸酯)(制品名;ve
‑
073,fujifilm wako pure chemical corporation制)6mg,充分地搅拌直至均匀。使加入有该混合溶液的100ml烧瓶内进行氮置换,升温至70℃后加热搅拌7小时,由此得到固态成分约11.20质量%的含有共聚物的清漆。得到的透明液体的利用gfc测得的重均分子量为约710,000。
[0185]
<合成例4>
[0186]
向纯水8.60g与乙醇8.52g的混合溶剂中添加2
‑
甲基丙烯酰氧基乙基磷酰胆碱(mpc,东京化成工业株式会社制)1.62g及酸式磷酰氧基聚丙二醇单甲基丙烯酸酯(环氧丙烷的平均加成摩尔数为5)(制品名;ppm
‑
5p,东邦化学株式会社制,质量%(纯度)95.6质量%)0.28g,进行充分搅拌。接下来,添加二甲基1,1
′‑
偶氮双(1
‑
环己烷甲酸酯)(制品名;ve
‑
073,fujifilm wako pure chemical corporation制)6mg,充分地搅拌直至均匀。使加入有该混合溶液的100ml烧瓶内进行氮置换,升温至70℃后加热搅拌7小时,由此得到固态成分约10.36质量%的含有共聚物的清漆。得到的透明液体的利用gfc测得的重均分子量为约390,000。
[0187]
<合成例5~12>
[0188]
根据合成例1,使用表中所示的单体及组成比的单体组合物来得到聚合物。将得到的聚合物的分子量与合成例1同样地进行分析的结果示于表1。
[0189]
需要说明的是,分别地,表1中的pem5p表示酸式磷酰氧基乙二醇单甲基丙烯酸酯(环氧乙烷的平均加成摩尔数为5)(制品名;pem
‑
5p,东邦化学株式会社制,质量%(纯度)87.4质量%),mhp表示单甲基丙烯酸(酸式磷酰氧基)己酯(制品名;mhp,东邦化学株式会社制,质量%(纯度)94.2质量%),dmma表示甲基丙烯酸2
‑
(二甲基氨基)乙酯(东京化成工业株式会社制),dema表示甲基丙烯酸2
‑
(二乙基氨基)乙酯(东京化成工业株式会社制),macc表示甲基丙烯酰基氯化胆碱约80%水溶液(东京化成工业株式会社制)。
[0190]
另外,pem5p、mhp的质量%(纯度)通过与合成例1~4中记载的ppm5p同样的方法进
行组成分析。针对pem5p而言,通过使用将环氧乙烷的加成摩尔数设为5时的分子量进行换算而求出。
[0191]
[表1]
[0192][0193]
<比较合成例1>
[0194]
下述记载的甲基丙烯酸(酸式磷酰氧基)乙酯的含磷化合物的质量%为日本再表2016/093293号中记载的、通过
31
p
‑
nmr测定求得的值。
[0195]
甲基丙烯酸(酸式磷酰氧基)乙酯(制品名;phosmer m,uni chemical株式会社制,干固法100℃
·
1小时条件下的非挥发成分:91.8%,各成分的质量%:甲基丙烯酸(酸式磷酰氧基)乙酯(44.2质量%)、磷酸双[2
‑
(甲基丙烯酰基氧基)乙基]酯(28.6质量%)、其他物质(27.2质量%)的混合物)1.06g中添加乙醇9.22g,将其充分溶解。接下来,添加甲基丙烯酸2
‑
(二甲基氨基)乙酯(东京化成工业株式会社制)0.72g、纯水6.00g,进行充分搅拌后,添加二甲基1,1
’‑
偶氮双(1
‑
环己烷甲酸酯)(制品名;ve
‑
073,fujifilm wako pure chemical corporation制)8.6mg。进行充分地搅拌直至均匀,将加入了上述所有物质的混合溶液加入到50ml烧瓶内并进行氮置换,一边搅拌一边升温至回流温度(油浴温度:设定为95℃)。维持该状态而进行加热搅拌,1小时以内产生白色沉淀。
[0196]
<比较合成例2>
[0197]
向纯水7.26g与乙醇7.24g的混合溶剂中添加2
‑
甲基丙烯酰氧基乙基磷酰胆碱(mpc,东京化成工业株式会社制)0.90g及甲基丙烯酸(酸式磷酰氧基)乙酯(制品名;phosmer m,uni chemical株式会社制,干固法100℃
·
1小时条件下的非挥发成分:91.8%,各成分的质量%:甲基丙烯酸(酸式磷酰氧基)乙酯(44.2质量%)、磷酸双[2
‑
(甲基丙烯酰基氧基)乙基]酯(28.6质量%)、其他物质(27.2质量%)的混合物)0.73g,进行充分搅拌。接下来,添加二甲基1,1
′‑
偶氮双(1
‑
环己烷甲酸酯)(制品名;ve
‑
073,fujifilm wako pure chemical corporation制)6mg,充分地搅拌直至均匀。使加入该混合溶液的50ml烧瓶内进行氮置换,升温至70℃后维持该状态而进行加热搅拌,3小时以内产生白色沉淀。
[0198]
<实施例1>
[0199]
向由上述合成例1得到的含有共聚物的清漆0.80g中添加纯水5.05g、乙醇1.94g、0.1mol/l盐酸(将1n盐酸(关东化学株式会社制)以纯水稀释10倍来使用)0.20g并充分地搅
拌,制备涂覆膜形成用组合物。ph为4.6。将得到的涂覆膜形成用组合物以1500rpm/60秒旋涂于经hmds处理过的硅晶片,作为干燥工序,在50℃的烘箱干燥24小时。然后,用磷酸缓冲液(以下,简称pbs)进行充分洗涤后,在50℃的烘箱中干燥1小时,在经hmds处理过的硅晶片上得到涂覆膜。用椭圆偏光仪确认hmds处理过的硅晶片上的涂覆膜的膜厚时,为3.9nm。
[0200]
<实施例2>
[0201]
向由上述合成例1得到的含有共聚物的清漆0.80g中添加纯水5.26g、乙醇1.94g并充分地搅拌,制备涂覆膜形成用组合物。ph为5.9。将得到的涂覆膜形成用组合物以1500rpm/60秒旋涂于经hmds处理过的硅晶片,作为干燥工序,在50℃的烘箱干燥24小时。然后,用磷酸缓冲液(以下,简称为pbs)进行充分洗涤后,在50℃的烘箱中干燥1小时,在经hmds处理过的硅晶片上得到涂覆膜。用椭圆偏光仪确认经hmds处理过的硅晶片上的涂覆膜的膜厚时,为4.0nm。
[0202]
<实施例3>
[0203]
向由上述合成例1得到的含有共聚物的清漆0.80g中添加纯水4.84g、乙醇1.95g并充分地搅拌,添加0.1mol/l氢氧化钠水溶液(将1n氢氧化钠(关东化学株式会社制)以纯水稀释10倍来使用)0.26g并充分地搅拌,制备涂覆膜形成用组合物。ph为7.0。将得到的涂覆膜形成用组合物以1500rpm/60秒旋涂于经hmds处理过的硅晶片,作为干燥工序,在50℃的烘箱干燥24小时。然后,用磷酸缓冲液(以下,简称pbs)进行充分洗涤后,在50℃的烘箱中干燥1小时,在经hmds处理过的硅晶片上得到涂覆膜。用椭圆偏光仪确认经hmds处理过的硅晶片上的涂覆膜的膜厚时,为3.9nm。
[0204]
<实施例4>
[0205]
向由上述合成例2得到的含有共聚物的清漆2.00g中添加纯水9.00g、乙醇9.00g并充分地搅拌,制备涂覆膜形成用组合物。ph为2.8。将得到的涂覆膜形成用组合物以1500rpm/60秒旋涂于经hmds处理过的硅晶片,作为干燥工序,在50℃的烘箱干燥24小时。然后,用pbs进行充分地洗涤后,在50℃的烘箱中干燥1小时,在经hmds处理过的硅晶片上得到涂覆膜。用椭圆偏光仪确认经hmds处理过的硅晶片上的涂覆膜的膜厚时,为3.9nm。
[0206]
<实施例5>
[0207]
向由上述合成例3得到的含有共聚物的清漆2.00g中添加纯水9.00g、乙醇9.00g并充分地搅拌,制备涂覆膜形成用组合物。ph为3.1。将得到的涂覆膜形成用组合物以1500rpm/60秒旋涂于经hmds处理过的硅晶片,作为干燥工序,在50℃的烘箱干燥24小时。然后,用pbs进行充分地洗涤后,在50℃的烘箱中干燥1小时,在经hmds处理过的硅晶片上得到涂覆膜。用椭圆偏光仪确认经hmds处理过的硅晶片上的涂覆膜的膜厚时,为3.5nm。
[0208]
<实施例6>
[0209]
向由上述合成例4得到的含有共聚物的清漆2.00g中添加纯水9.00g、乙醇9.00g并充分地搅拌,制备涂覆膜形成用组合物。ph为3.3。将得到的涂覆膜形成用组合物以1500rpm/60秒旋涂于经hmds处理过的硅晶片,作为干燥工序,在50℃的烘箱干燥24小时。然后,用pbs进行充分地洗涤后,在50℃的烘箱中干燥1小时,在经hmds处理过的硅晶片上得到涂覆膜。用椭圆偏光仪确认hmds处理过的硅晶片上的涂覆膜的膜厚时,为3.1nm。
[0210]
<实施例7>
[0211]
向由上述合成例5得到的含有共聚物的清漆1.00g中添加纯水2.60g、乙醇6.40g并
充分地搅拌,制备涂覆膜形成用组合物。ph为3.6。将得到的涂覆膜形成用组合物以1500rpm/60秒旋涂于经hmds处理过的硅晶片,作为干燥工序,在50℃的烘箱干燥24小时。然后,用pbs进行充分地洗涤后,在50℃的烘箱中干燥1小时,在经hmds处理过的硅晶片上得到涂覆膜。用椭圆偏光仪确认经hmds处理过的硅晶片上的涂覆膜的膜厚时,为3.5nm。
[0212]
<实施例8>
[0213]
向由上述合成例8得到的含有共聚物的清漆1.00g中添加纯水2.60g、乙醇6.40g并充分地搅拌,制备涂覆膜形成用组合物。ph为6.8。将得到的涂覆膜形成用组合物以1500rpm/60秒旋涂于经hmds处理过的硅晶片,作为干燥工序,在50℃的烘箱干燥24小时。然后,用pbs进行充分地洗涤后,在50℃的烘箱中干燥1小时,在经hmds处理过的硅晶片上得到涂覆膜。用椭圆偏光仪确认经hmds处理过的硅晶片上的涂覆膜的膜厚时,为3.8nm。
[0214]
<实施例9>
[0215]
向由上述合成例10得到的含有共聚物的清漆1.00g中添加纯水2.50g、乙醇6.40g并充分地搅拌,添加0.1mol/l氢氧化钠水溶液(将1n氢氧化钠(关东化学株式会社制)以纯水稀释10倍来使用)0.11g并充分地搅拌,制备涂覆膜形成用组合物。ph为4.2。将得到的涂覆膜形成用组合物以1500rpm/60秒旋涂于经hmds处理过的硅晶片,作为干燥工序,在50℃的烘箱干燥24小时。然后,用pbs进行充分地洗涤后,在50℃的烘箱中干燥1小时,在经hmds处理过的硅晶片上得到涂覆膜。用椭圆偏光仪确认经hmds处理过的硅晶片上的涂覆膜的膜厚时,为3.7nm。
[0216]
<参考例1>
[0217]
向lipidure
‑
cm5206(日油株式会社制)0.25g中添加乙醇49.75g并充分地搅拌而制备涂覆膜形成用组合物。将得到的涂覆膜形成用组合物以1500rpm/60秒旋涂于经hmds处理过的硅晶片,作为干燥工序,在50℃的烘箱干燥24小时。然后,用pbs进行充分地洗涤后,在50℃的烘箱中干燥1小时,在经hmds处理过的硅晶片上得到涂覆膜。用椭圆偏光仪确认经hmds处理过的硅晶片上的涂覆膜的膜厚时,为25.4nm。
[0218]
<试验例1:细胞附着抑制效果>
[0219]
(涂覆板的制备)
[0220]
将由实施例1~3、8、9制备的涂覆膜形成用组合物以成为200μl/孔的方式添加到96孔细胞培养板(corning公司制,#351172,容积0.37ml,聚苯乙烯制)的各个孔中,于室温静置1小时后,除去过量的清漆。使用烘箱在50℃干燥24小时。然后,将涂覆的各孔用250μl的纯水各洗涤3次,使用50℃的烘箱干燥1小时后,用于试验。作为阳性对照,使用将参考例1中制备的涂覆膜形成用组合物利用与上述相同的方法而涂覆到96孔细胞培养板(corning公司制,#351172,容积0.37ml,聚苯乙烯制)的孔中而成的培养板。作为阴性对照,使用未实施涂覆的96孔细胞培养板(corning公司制,#351172,容积0.37ml,聚苯乙烯制)。
[0221]
(细胞的制备)
[0222]
作为细胞,使用小鼠胚胎成纤维细胞(ds pharma biomedical公司制)。作为细胞的培养中使用的培养基,使用包含10%fbs(sigma
‑
aldrich公司制)和l
‑
谷氨酰胺
‑
青霉素
‑
链霉素稳定化溶液(thermo fisher scientific公司制)的bme培养基(thermo fisher scientific公司制)。使用直径为10cm的培养皿(10ml培养基),在37℃/co2培养箱内,在保持5%二氧化碳浓度的状态下,将细胞静置培养2天以上。接下来,用pbs 5ml洗涤该细胞,然
后添加1ml的0.25w/v%胰蛋白酶
‑
1mmol/l edta溶液(fujifilm wako pure chemical corporation制),将细胞剥离,利用上述的培养基10ml分别进行悬浮。将该悬浮液进行离心分离(tomy seiko co.,ltd.制,型号lc
‑
200,1000rpm/3min,室温),然后,除去上清液,添加上述的培养基,制备细胞悬浮液。
[0223]
(细胞附着实验)
[0224]
向上述制备的板的各孔、阳性对照、阴性对照中,将各细胞悬浮液以成为1
×
104细胞/孔的方式各添加150μl。然后,在保持5%二氧化碳浓度的状态下,于37℃在co2培养箱内静置3天。
[0225]
(细胞附着的观察)
[0226]
培养3天后,利用倒置型显微镜(奥林巴斯公司制,ckx31)观察(倍率:4倍)细胞对上述制备的板的各孔、阳性对照及阴性对照附着的情况,并基于此进行比较。在用实施例1~3、8、9及阳性对照的涂覆剂(参考例1)进行了涂覆的板的各孔中,未观察到细胞的附着,在阴性对照的孔中,观察到细胞的附着。实施例1~3、阳性对照及阴性对照的结果分别示于图1~5。
[0227]
<试验例2:蛋白质吸附抑制效果>
[0228]
(qcm传感器(ps)的制作)
[0229]
使用软蚀刻装置(meiwafosis株式会社制,sede
‑
ge),对蒸镀有au的晶体振荡器(q
‑
sence,qsx301)进行50ma/3min洗涤,然后立即在将2
‑
氨基乙烷硫醇(东京化成工业株式会社制)0.0772g溶解于乙醇1000ml而成的溶液中浸渍24小时。用乙醇洗涤传感器表面,然后自然干燥,利用旋涂机以3500rpm/30秒将使聚苯乙烯(ps)(sigma
‑
aldrich公司制)1.00g溶解于甲苯99.00g而成的清漆旋涂于膜传感器侧,进行150℃/1min干燥,由此制作qcm传感器(ps)。
[0230]
(qcm传感器(sio2)的制作)
[0231]
使用软蚀刻装置(meiwafosis株式会社制,sede
‑
ge),对蒸镀有sio2的晶体振荡器(q
‑
sence,qsx303)进行50ma/3min洗涤,直接使用。
[0232]
(经表面处理的qcm传感器(ps)及经表面处理的qcm传感器(sio2)的制备)
[0233]
以3500rpm/30秒将由实施例1~4、7~9、参考例1得到的涂覆膜形成用组合物旋涂于qcm传感器(ps),作为干燥工序,在50℃的烘箱中烧成24小时。然后,作为洗涤工序,用pbs和纯水对过量的涂覆膜形成用组合物分别进行各2次洗涤,得到经表面处理的qcm传感器(ps)(基板no.1~5、11~13)。同样地,以3500rpm/30秒将由实施例4~6得到的涂覆膜形成用组合物旋涂于qcm传感器(sio2),作为干燥工序,在50℃的烘箱中烧成24小时。然后,作为洗涤工序,用pbs和纯水对过量的涂覆膜形成用组合物分别进行各2次洗涤,得到经表面处理的qcm传感器(sio2)(基板no.7~9)。作为阳性对照,使用涂覆了由参考例1得到的涂覆膜形成用组合物的经表面处理的qcm传感器(ps)(基板no.5)。作为阴性对照,使用qcm传感器(ps)(基板no.6)及qcm传感器(sio2)(基板no.10)。
[0234]
(蛋白质吸附实验)
[0235]
将使用涂覆膜形成用组合物并通过上述方法制作的经表面处理的qcm传感器(ps)(基板no.1~5、11~13)及经表面处理的qcm传感器(sio2)(基板no.7~9)安装于耗散型石英晶体微天平qcm
‑
d(e4,q
‑
sence),使pbs流通直至确立了频率的变化在1小时内成为1hz以
下的稳定的基线。接下来,将稳定的基线的频率作为0hz,使pbs流通约10分钟。接下来,使源自人血清的γ
‑
球蛋白的100μg/ml pbs溶液流通约30分钟,然后再次使pbs流通约20分钟,然后读取9次谐波的吸附诱导频率的位移(δf)。为了进行分析,使用q
‑
tools(q
‑
sence),针对吸附诱导频率的位移(δf),将由sauerbrey式说明的吸附诱导频率的位移(δf)换算为每单位面积的质量(ng/cm2),将所得值作为生物材料的附着量示于下述的表2。对于将本发明涉及的实施例1~9的涂覆膜形成用组合物进行涂覆而使用的基板no.1~4、基板no.7~9及基板no.11~13而言,与未涂覆的基板no.6、no.10相比,显示出低蛋白质吸附量。
[0236]
[表2]
[0237]
基板no.qcm传感器涂覆剂蛋白质附着量(ng/cm2)1ps实施例1212ps实施例21063ps实施例3204ps实施例43335ps参考例1296ps无9467sio2实施例458sio2实施例5199sio2实施例6710sio2无32311ps实施例713012ps实施例84813ps实施例9235
[0238]
产业上的可利用性
[0239]
根据本发明,可以提供不发生凝胶化问题的含有共聚物的清漆的制造方法、组合物的制造方法、涂覆膜的制造方法、优选具有与生物材料的相容性(具有抑制生物材料附着的能力、细胞培养促进性)的涂覆膜的制造方法。
[0240]
本发明的涂覆膜具有抑制生物材料附着的能力,因此可作为医疗用基材用涂覆膜而合适地使用。例如,可在去白细胞过滤器、输血过滤器、除病毒过滤器、除微小凝血块过滤器、血液净化用组件、人工心脏、人工肺、血液回路、人工血管、血管旁路管、医疗用管、人工瓣膜、套管(canula)、支架、导管、血管内导管、气囊导管、导丝、缝合线、留置针、分流器(shunt)、人工关节、人工髋关节、血袋、血液保存容器、手术用辅助器具、防粘连膜、创伤被覆材料等中合适地使用。其中,所谓血液净化用组件,是指使血液在体外循环而具有去除血中的废物、有害物质的功能的组件,可举出人工肾脏、毒素吸附过滤器或柱等。
[0241]
另外,本发明的涂覆膜作为烧瓶、培养皿、培养板等细胞培养容器、抑制蛋白质附着的各种研究用器具的涂覆膜是有用的。
[0242]
另外,对于本发明的涂覆膜而言,作为化妆品用材料、隐形眼镜护理用品用材料、皮肤护理用纤维加工剂、生物化学研究用诊断剂用材料、用于抑制临床诊断法中广泛使用的酶联免疫吸附测定(elisa)法、乳胶凝集法中的非特异性吸附的封闭剂(blocking agent)、用于使酶、抗体等蛋白质稳定化的稳定化剂也是有用的。
[0243]
此外,本发明的涂覆膜作为用于化妆用品(toiletry)、个人护理用品、洗剂、医药品、准医药品、纤维、用于防污材料的涂覆膜也是有用的。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1