FXR激动剂的固体形式的制作方法
fxr激动剂的固体形式
1.相关申请的交叉引用
2.本技术要求于2019年2月19日提交的美国临时专利申请号62/807,542的优先权益,通过引用全文将其内容并入本文中。
技术领域
3.本公开内容涉及fxr激动剂的新型固体形式,及其药物制剂和治疗用途。
背景技术:
4.本公开内容涉及化合物的固体形式,其结合nr1h4受体(fxr)并充当fxr的激动剂或调节剂。本公开内容还涉及此类化合物的固体形式用于治疗和/或预防通过所述化合物与所述核受体的结合来调节的疾病和/或病症。
5.与nr1h4受体(fxr)结合的化合物可以充当fxr的激动剂或调节剂。fxr激动剂通过结合nr1h4受体用于治疗和/或预防疾病和病症。一种这样的fxr激动剂是式i的化合物:
[0006][0007]
尽管已知多种fxr激动剂,但是本领域中需要的是式i的化合物或其药学上可接受的盐的物理稳定形式,其具有需要的性质(例如良好的物理和化学稳定性、良好的水溶性和良好的生物利用度)。例如,需要解决稳定性、可变药效学响应、药物
‑
药物相互作用、ph效应、食物效应和口服生物利用度的挑战的药物组合物。
[0008]
因此,需要式i化合物的稳定形式,其具有针对化合物的制剂、治疗用途、制造和储存的化学和物理稳定性。
[0009]
此外,需要开发可以用于式i的合成的式i的固体形式。固体形式,例如式i的化合物的结晶形式可以是式i的合成的中间体。固体形式在某些条件下可以具有例如生物利用度、稳定性、纯度和/或可制造性的性质,这些性质可以适用于医疗用途或制药用途。
[0010]
发明概述
[0011]
在一些实施方案中,本公开内容涉及式i的化合物的新型固体形式及其药学上可接受的盐、溶剂合物和水合物:
[0012][0013]
例如,这些新型形式用于治疗患有肝病(如非酒精性脂肪性肝炎(“nash”))的人类患者。本公开内容的新型固体形式可以用于制备治疗肝病的药物。本公开内容的新型固体形式可以用作fxr激动剂。
[0014]
在一些实施方案中,本公开内容涉及式i的两性离子形式的固体形式
[0015][0016]
在一些实施方案中,本公开内容涉及两性离子形式i。
[0017]
在一些实施方案中,本公开内容涉及两性离子形式ii。
[0018]
在一些实施方案中,本公开内容涉及两性离子水合物。
[0019]
在一些实施方案中,本公开内容涉及两性离子无定形形式。
[0020]
在一些实施方案中,本公开内容涉及式i的氨丁三醇盐的固体形式。在一些实施方案中,式i的氨丁三醇盐具有以下结构:
[0021][0022]
在一些实施方案中,本公开内容涉及氨丁三醇盐形式i。
[0023]
在一些实施方案中,本公开内容涉及氨丁三醇盐形式ii。
[0024]
在一些实施方案中,本公开内容涉及氨丁三醇盐水合物i。
[0025]
在一些实施方案中,本公开内容涉及氨丁三醇盐水合物ii。
[0026]
在一些实施方案中,本公开内容涉及氨丁三醇盐水合物iii。
[0027]
在一些实施方案中,本公开内容涉及氨丁三醇盐水合物iv。
[0028]
在一些实施方案中,本公开内容涉及氨丁三醇盐甲醇溶剂合物i。
[0029]
在一些实施方案中,本公开内容涉及氨丁三醇盐甲醇溶剂合物ii。
[0030]
在一些实施方案中,本公开内容涉及氨丁三醇盐甲醇溶剂合物iii。
[0031]
在一些实施方案中,本公开内容涉及氨丁三醇盐甲基叔丁基醚(“mtbe”)溶剂合
物。
[0032]
在一些实施方案中,本公开内容涉及氨丁三醇盐无定形形式。
[0033]
在一些实施方案中,本公开内容涉及氨丁三醇盐乙醇溶剂合物。
[0034]
在一些实施方案中,本公开内容涉及式i的对甲苯磺酸盐的固体形式。
[0035]
在一些实施方案中,本公开内容涉及对甲苯磺酸盐形式i。
[0036]
在一些实施方案中,本公开内容涉及对甲苯磺酸盐形式ii。
[0037]
在一些实施方案中,本公开内容涉及对甲苯磺酸盐形式iii。
[0038]
在一些实施方案中,本公开内容涉及对甲苯磺酸盐水合物。
[0039]
在一些实施方案中,药物组合物包含治疗有效量的式i的固体形式。
附图说明
[0040]
图1显示了式i的两性离子化合物形式i的xrpd谱图。
[0041]
图2显示了式i的两性离子化合物形式i的dsc热谱图。
[0042]
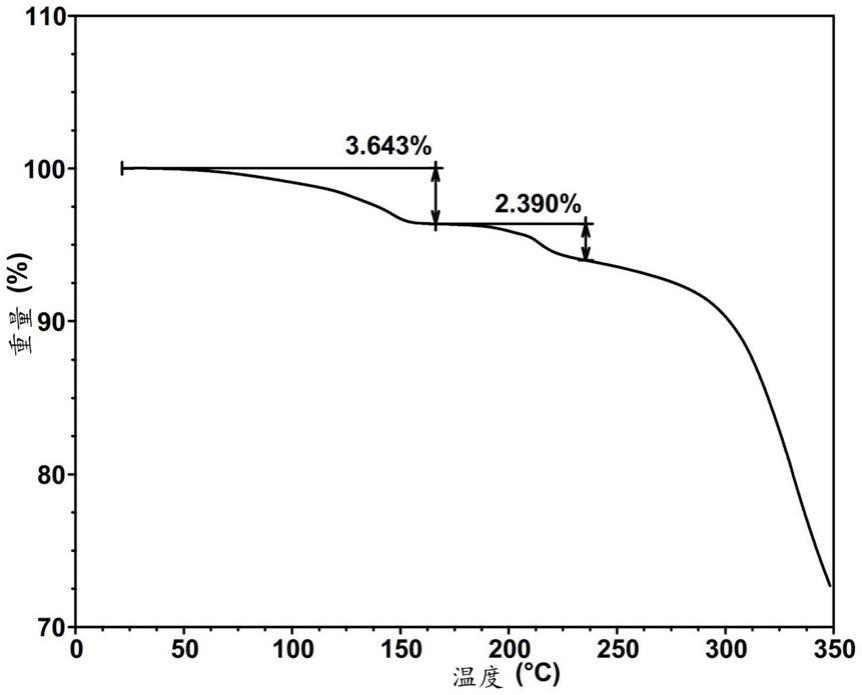
图3显示了式i的两性离子化合物形式i的tga热谱图。
[0043]
图4显示了式i的两性离子化合物形式ii的xrpd谱图。
[0044]
图5显示了式i的两性离子化合物形式ii的dsc热谱图。
[0045]
图6显示了式i的两性离子化合物形式ii的tga热谱图。
[0046]
图7显示了式i的两性离子化合物水合物的xrpd谱图。
[0047]
图8显示了式i的两性离子化合物水合物的dsc热谱图。
[0048]
图9显示了式i的两性离子化合物水合物的tga热谱图。
[0049]
图10显示了式i的无定形两性离子化合物的xrpd谱图。
[0050]
图11显示了式i氨丁三醇盐形式i的xrpd谱图。
[0051]
图12显示了式i氨丁三醇盐形式i的dsc热谱图。
[0052]
图13显示了式i氨丁三醇盐形式i的tga热谱图。
[0053]
图14显示了式i氨丁三醇盐形式ii的xrpd谱图。
[0054]
图15显示了式i氨丁三醇盐水合物i的xrpd谱图。
[0055]
图16显示了式i氨丁三醇盐水合物i的dsc热谱图。
[0056]
图17显示了式i氨丁三醇盐水合物i的tga热谱图。
[0057]
图18显示了式i氨丁三醇盐水合物ii的xrpd谱图。
[0058]
图19显示了式i氨丁三醇盐水合物ii的dsc热谱图。
[0059]
图20显示了式i氨丁三醇盐水合物ii的tga热谱图。
[0060]
图21显示了式i氨丁三醇盐水合物iii的xrpd谱图。
[0061]
图22显示了式i氨丁三醇盐水合物iii的dsc热谱图。
[0062]
图23显示了式i氨丁三醇盐水合物iii的tga热谱图。
[0063]
图24显示了式i氨丁三醇盐水合物iv的xrpd谱图。
[0064]
图25显示了式i氨丁三醇盐水合物iv的dsc热谱图。
[0065]
图26显示了式i氨丁三醇盐水合物iv的tga热谱图。
[0066]
图27显示了式i氨丁三醇盐甲醇溶剂合物i的xrpd谱图。
[0067]
图28显示了式i氨丁三醇盐甲醇溶剂合物ii的xrpd谱图。
[0068]
图29显示了式i氨丁三醇盐甲醇溶剂合物iii的xrpd谱图。
[0069]
图30显示了式i氨丁三醇盐甲醇溶剂合物iii的dsc热谱图。
[0070]
图31显示了式i氨丁三醇盐甲醇溶剂合物iii的tga热谱图。
[0071]
图32显示了式i氨丁三醇盐mtbe溶剂合物的xrpd谱图。
[0072]
图33显示了式i氨丁三醇盐mtbe溶剂合物的dsc热谱图。
[0073]
图34显示了式i氨丁三醇盐mtbe溶剂合物的tga热谱图。
[0074]
图35显示了式i氨丁三醇盐无定性形式的xrpd谱图。
[0075]
图36显示了式i氨丁三醇盐乙醇溶剂合物的xrpd谱图。
[0076]
图37显示了式i对甲苯磺酸盐形式i的xrpd谱图。
[0077]
图38显示了式i对甲苯磺酸盐形式i的dsc热谱图。
[0078]
图39显示了式i对甲苯磺酸盐形式i的tga热谱图。
[0079]
图40显示了式i对甲苯磺酸盐形式ii的xrpd谱图。
[0080]
图41显示了式i对甲苯磺酸盐形式ii的dsc热谱图。
[0081]
图42显示了式i对甲苯磺酸盐形式ii的tga热谱图。
[0082]
图43显示了式i对甲苯磺酸盐形式iii的xrpd谱图。
[0083]
图44显示了式i对甲苯磺酸盐形式iii的dsc热谱图。
[0084]
图45显示了式i对甲苯磺酸盐形式iii的tga热谱图。
[0085]
图46显示了式i对甲苯磺酸盐水合物的xrpd谱图。
[0086]
图47显示了式i对甲苯磺酸盐水合物dsc热谱图。
[0087]
图48显示了式i对甲苯磺酸盐水合物的tga热谱图。
[0088]
发明详述
[0089]
在以下描述中,为了提供对本公开内容的各种实施方案的透彻理解,阐述了某些具体的细节。然而,本领域技术人员将理解,可以在没有这些细节的情况下实践本公开内容。以下若干个实施方案的描述是在理解本公开内容被视为所要求保护的主题的示例,并不旨在将所附权利要求限制为所示的特定的实施方案下进行的。提供本公开内容通篇使用的标题仅为了方便起见,并不被解释为以任何方式限制权利要求。在任何标题下说明的实施方案可以与在任何其它标题下说明的实施方案组合。
[0090]
定义
[0091]
除非上下文另有要求,否则在整个说明书和权利要求书中,词语“包括”及其变体,例如“包括”和“包含”应被解释为开放的、包括性的意义,即“包括,但不限于”。
[0092]
在整个说明书中对“一个(one)实施方案”或“一种(an)实施方案”的引用意味着结合该实施方案描述的特定的特征、结构或特性包括在本公开内容的至少一个实施方案中。因此,在整个说明书中的不同地方出现的短语“在一个实施方案中”或“在一种实施方案中”不一定都指的是相同的实施方案。此外,特定的特征、结构或特性可以在一个或多个实施方案中以任何合适的方式组合。
[0093]
在整个说明书中提及“化合物”的实施方案包括本文公开的式和/或化合物的结晶、盐、共晶、两性离子、水合物、溶剂合物和/或无定形形式。因此,陈述(appearance)或短语“式i的化合物”可以包括式i两性离子形式i;式i两性离子形式ii;式i水合物;式i两性离子无定形;式i氨丁三醇盐形式i;式i氨丁三醇盐形式ii;式i氨丁三醇盐水合物i;式i氨丁
三醇盐水合物ii;式i氨丁三醇盐水合物iii;式i氨丁三醇盐水合物iv;式i氨丁三醇盐甲醇溶剂合物i;式i氨丁三醇盐甲醇溶剂合物ii;式i氨丁三醇盐甲醇溶剂合物iii;式i氨丁三醇盐mtbe溶剂合物;式i氨丁三醇盐无定形形式;式i氨丁三醇盐乙醇溶剂合物;式i对甲苯磺酸盐形式i;式i对甲苯磺酸盐形式ii;式i对甲苯磺酸盐形式iii;和/或式i对甲苯磺酸盐水合物。
[0094]
本文公开的公开内容也意欲涵盖所有药学上可接受的式i的化合物,其通过具有一个或多个原子被具有不同原子量或质量数的原子代替被同位素标记。可以掺入所述公开的化合物中的同位素的实例包括氢、碳、氮、氧、磷、氟、氯和碘的同位素,例如分别为2h、3h、
11
c、
13
c、
14
c、
13
n、
15
n、
15
o、
17
o、
18
o、
31
p、
32
p、
35
s、
18
f、
36
cl、
123
i和
125
i。这些放射性标记的化合物可以用于帮助确定或测量化合物的有效性,例如通过表征作用的作用位点或作用模式或与药理学上重要的作用位点的结合亲和力。式i的某些放射性标记的化合物,例如掺入放射性同位素的那些,用于药物和/或底物组织分布研究。由于放射性同位素氚(即3h)和碳
‑
14(即
14
c)容易加入和检测手段容易,因此它们尤其适用于这一目的。
[0095]
用较重的同位素如氘(即2h)进行取代可能会由于更大的代谢稳定性而产生某些治疗优点。例如,体内半衰期可能增加或剂量要求可能降低。因此,在某些情况下,较重的同位素可能是优选的。
[0096]
用正电子发射同位素(如
11
c、
18
f、
15
o和
13
n)进行取代可以用于在正电子发射测量(pet)研究中用于检查底物受体占据率(occupancy)。同位素标记的式i的化合物通常可以通过本领域技术人员已知的常规技术或通过与下文描述的方法类似的方法使用适当的同位素标记试剂代替先前使用的未标记试剂。
[0097]“稳定化合物”和“稳定结构”意在表示足够稳定的化合物,以便能够以有用的纯度从反应混合物中分离并配制成有效的治疗剂。
[0098]“任选的”或“任选地”意指随后描述的事件或情况可能发生也可能不发生,并且该描述包括所述事件或情况发生的实例和不发生的实例。例如,“任选取代的芳基”意指芳基可以被取代或可以不被取代,并且该描述包括取代的芳基和没有取代的芳基。
[0099]“药学上可接受的赋形剂”包括但不限于任何经美国食品和药物管理局批准的可以用于人或家养动物的辅料、载体、赋形剂、助流剂、甜味剂、稀释剂、防腐剂、染料/着色剂、风味增强剂、表面活性剂、润湿剂、分散剂、混悬剂、稳定剂、等渗剂、溶剂和/或乳化剂,或以上一种或多种的组合。
[0100]“药物组合物”是指本公开内容的化合物(例如,式i的化合物)与本领域中普遍接受的用于将生物活性化合物递送到哺乳动物(例如人类)的介质的制剂。这种介质包括所有药学上可接受的赋形剂。
[0101]“有效量”或“治疗有效量”是指根据本公开内容的化合物的量,其在向有需要的患者施用时足以实现对所述化合物有效的疾病状态、病症或障碍的治疗。这样的量足以引起由研究人员或临床医生寻求的组织系统或患者的生物或医学响应。构成治疗有效量的根据本公开内容的化合物的量将根据如化合物及其生物活性、用于施用的组合物、施用时间、施用途径、化合物的排泄速率、治疗的持续时间、所治疗的疾病状态或障碍的类型及其严重程度、与本公开内容的化合物组合或同时使用的药物、以及患者的年龄、体重、整体健康状况、性别和饮食来变化。这样的治疗有效量可以由本领域技术人员考虑到他们自己的知识、现
有技术和本公开内容来常规确定。
[0102]“阻止”或“防止”或“预防”意指对导致疾病或病症的临床症状不发展的对疾病或病症的任何治疗。在一些实施方案中,化合物可以向处于疾病或病症风险或具有疾病或病症家族史的受试者(包括人)施用。
[0103]“治疗”疾病或疾病的“治疗”包括以下内容:
[0104]
(i)预防或降低发展该疾病的风险,即,使该疾病的临床症状不会在可能暴露于或易患该疾病但尚未经历或表现该疾病的症状的受试者中发展,
[0105]
(ii)抑制该疾病,即,阻止或减少该疾病或其临床症状的发展;和
[0106]
(iii)缓解该疾病,即,引起该疾病或其临床症状的消退。
[0107]
术语“受试者”或“患者”是指已经或将成为治疗、观察或实验对象的动物,例如哺乳动物(包括人)。本文描述的方法可以用于人类治疗和/或兽医应用。在一些实施方案中,受试者(或患者)是哺乳动物。在一些实施方案中,受试者(或患者)是人、家养动物(例如狗和猫)、农场动物(例如牛、马、绵羊、山羊和猪)和/或实验室动物(例如小鼠、大鼠、仓鼠、豚鼠、猪、兔子、狗和猴子)。在一些实施方案中,受试者(或患者)是人。“有需要的人(或患者)”是指可能患有或怀疑患有可以从某些治疗中受益的疾病或病症的人;例如,用根据本技术的本文公开的化合物治疗的人。
[0108]
本文对“约”一个值或参数的提及包括(和描述)涉及该值或参数本身的实施方案。例如,提及“约x”的描述包括“x”的描述。此外,除非上下文另有明确规定,否则单数形式“一个”和“该”包括复数个提及物。因此,例如,对“化合物”的提及包括复数个此化合物并且提及“试验”包括对本领域技术人员知晓的一种或多种试验及其等效物的提及。
[0109]“药学上可接受的”或“生理学上可接受的”是指化合物、盐、组合物、剂型和其它的物质,其用于制备适用于兽用(veterinary)或人用(human)制药用途的药物组合物。
[0110]“单位剂型”是适合作为用于受试者(例如,人类受试者和其它哺乳动物)的单位剂量的物理离散单位,每个单位包含经计算以产生所需治疗效果的预定量的活性物质,以及合适的药学上的赋形剂。
[0111]
当提及例如xrpd谱图、dsc热谱图、dvs等温线或tga热谱图时,术语“基本上如
…
中所示”包括不一定与本文描述的那些相同的谱图、热谱图或光谱,但是在本领域普通技术人员考虑时落入实验误差或偏差的限度内的那些。
[0112]
在一些实施方案中,就化合物的特定结晶形式而言,术语“基本上纯的”或“基本上不含”意指包含该结晶形式的组合物含有按重量计少于99%、少于95%、少于90%、少于85%、少于80%、少于75%、少于70%、少于65%、少于60%、少于55%、少于50%、少于40%、少于30%、少于20%、少于15%、少于10%、少于5%或少于1%的其它物质,所述物质包括其它的结晶形式和/或杂质。在某些实施方案中,“基本上纯的”或“基本上不含”是指不含其它物质,所述物质包括其它的结晶形式和/或杂质。例如,杂质可能包括来自化学反应的副产物或残留试剂、污染物、降解产物、其它的结晶形式、水和溶剂。
[0113]
术语“药学上可接受的盐”是指由药学上可接受的无毒碱或酸制备的盐,包括无机碱或酸和有机碱或酸。在本公开内容的化合物含有一个或多个酸性或碱性基团的情况下,本公开内容还包括它们相应的药学上或毒理学上可接受的盐,特别是它们的药学上可使用的盐。因此,包含酸性基团的本公开内容的化合物可以存在于这些基团上并且可以根据本
公开内容,例如以碱金属盐、碱土金属盐或铵盐使用。此类盐的更精确的实例包括钠盐、钾盐、钙盐、镁盐或与氨或有机胺(例如乙胺、乙醇胺、三乙醇胺或氨基酸)形成的盐。包含一个或多个碱性基团(即可以被质子化的基团)的本公开内容的化合物可以存在并且可以根据本公开内容以其与无机或有机酸的加成盐的形式使用。合适的酸的实例包括盐酸、氢溴酸、磷酸、硫酸、硝酸、甲磺酸、对甲苯磺酸、萘二磺酸、草酸、乙酸、酒石酸、乳酸、水杨酸、苯甲酸、甲酸、丙酸、新戊酸、二乙基乙酸、丙二酸、琥珀酸、庚二酸、富马酸、马来酸、苹果酸、氨基磺酸、苯基丙酸、葡萄糖酸、抗坏血酸、异烟酸、柠檬酸、己二酸,以及本领域技术人员已知的其它酸。如果本公开内容的化合物在分子中同时含有酸性基团和碱性基团,则本公开内容除了提到的盐形式外,还包括内盐或内铵盐(betaines)(两性离子)。相应的盐可以通过本领域技术人员已知的常规方法获得,例如,通过将它们与有机或无机酸或有机或无机碱在溶剂或分散剂中接触,或通过与其它盐进行阴离子交换或阳离子交换。本公开内容还包括本公开内容的化合物的所有盐,这些盐由于生理相容性低,不直接适用于药物,但可以用作,例如化学反应的中间体或用于制备药学上可接受的盐。
[0114]
此外,本公开内容的化合物可以以溶剂合物的形式存在,例如包括作为溶剂合物水的那些,或药学上可接受的溶剂合物,例如醇,特别是乙醇。“溶剂合物”是通过将溶剂与化合物相互作用形成的。当溶剂是水时,所述“溶剂合物”是“水合物”。
[0115]
在某些实施方案中,提供了本文描述的化合物或其药学上可接受的盐或它们的混合物的旋光异构体、外消旋体,或上述物质的其它混合物。如果需要,异构体可以通过本领域公知的方法分离,例如通过液相色谱法分离。在这些情况下,单一对映异构体或非对映异构体(即光学活性形式),可以通过不对称合成或拆分获得。拆分可以通过,例如常规方法实现,如存在拆分剂时进行结晶,或例如,使用手性高压液相色谱(hplc)柱进行色谱法。
[0116]“立体异构体”是指由通过相同键键合的相同原子组成但具有不同的三维结构的化合物,且所述不同的三维结构间不可互换。本发明考虑了各种立体异构体及其混合物并且包括“对映异构体”,其是指两种立体异构体,其分子是彼此不可重叠的镜像。“非对映异构体”是具有至少两个不对称原子但彼此不成镜像的立体异构体。
[0117]
本文公开的化合物及其药学上可接受的盐可以包括不对称中心,因此可以产生对映异构体、非对映异构体和其它立体异构形式,它们可以根据绝对的立体化学定义为(r)
‑
或(s)
‑
,或者对于氨基酸,定义为(d)
‑
或(l)
‑
。本发明意在包括所有这些可能的异构体,以及它们的外消旋形式和光学纯形式。光学活性(+)和(
‑
)、(r)
‑
和(s)
‑
或(d)
‑
和(l)
‑
异构体可以使用手性合成子或手性试剂来制备,或使用常规技术,例如色谱法和分级结晶进行拆分。用于制备/分离单个对映体的常规技术包括从合适的光学纯的前体进行手性合成或使用,例如手性高压液相色谱(hplc)拆分外消旋物(或盐或衍生物的外消旋物)。当本文描述的化合物包含烯双键或其它几何不对称中心时,并且除非另有说明,否则意指该化合物包括e和z几何异构体。
[0118]
包含本文描述的化合物或其药学上可接受的盐、异构体,或它们的混合物的本文提供的组合物可以包括外消旋混合物,或含有一种对映异构体过量的对映异构体的混合物,或单一非对映异构体,或非对映异构体混合物。这些化合物的所有这些异构体形式明确地包括在本文中,如同每个和每种异构体形式被具体地和单独地列出一样。
[0119]“互变异构体”是指化合物的异构体,其在平衡状态下与另一种异构体一起存在,
其中两种异构体可以通过分子内原子或基团的迁移而相互转换。
[0120]
式i的固体形式
[0121]
式i的固体形式(包括结晶形式和基本上纯的形式)可以提供生物利用度和稳定性的优点,适于用作药物组合物中的活性成分。例如,式i氨丁三醇盐形式i具有有利的物理性质,如良好的物理和化学稳定性、良好的水溶性和良好的生物利用度。药物原料药(drug substance)或活性成分的晶体结构的变化可能影响药学药品或活性成分的溶出速率(这可能影响生物利用度等)、可制造性(例如,易于处理、始终如一地制备已知强度的剂量的能力)和稳定性(例如,热稳定性、保质期等)。这种变化可能影响不同剂量或递送形式的药物组合物的制剂(preparation/formulation),例如溶液或固体口服剂型(包括片剂和胶囊剂)。与其它形式(例如非结晶形式或无定形形式)相比,结晶形式可以提供所需或合适的吸湿性、粒径控制、溶出速率、溶解度、纯度、物理和化学稳定性、可制造性、产率和/或工艺控制。因此,式i的化合物的固体形式可以提供优势,例如改善:化合物的制造工艺、化合物的药品形式的稳定性或可储存性、化合物的原料药的稳定性或可储存性和/或化合物作为活性剂的生物利用度和/或稳定性。
[0122]
已经发现使用某些溶剂和/或方法来制备本文描述的化合物式i的不同固体形式,其可以表现出一种或多种上述有利特征。下文详细描述了本文描述的固体形式的制备方法和这些固体形式的特征。
[0123]
在特定的实施方式中,公开了新型固体形式,例如式i的结晶形式。在一些实施方案中,公开了式i的化合物的两性离子固体形式。在一些实施方案中,公开了式i的氨丁三醇盐的固体形式。在一些实施方案中,公开了式i的对甲苯磺酸盐的固体形式。
[0124]
式i两性离子形式i
[0125]
在一些实施方案中,本文提供的是式i的两性离子固体化合物(式i形式i),其中所述固体形式表现出基本上如图1中所示的x射线粉末衍射(xrpd)谱图。两性离子结晶式i形式i可以表现出基本上如图2中所示的差示扫描量热法(dsc)热谱图。结晶式i形式i可以表现出基本上如图3中所示的热重分析(tga)热谱图。
[0126]
在结晶式i形式i的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式i形式i具有基本上如图1中所示的xrpd谱图;(b)结晶式i形式i具有基本上如图2中所示的dsc热谱图;(c)结晶式i形式i具有基本上如图3中所示的tga热谱图。
[0127]
在一些实施方案中,结晶式i形式i具有至少一种、至少两种或至少三种以下性质:
[0128]
(a)基本上如图1中所示的xrpd谱图
[0129]
(b)基本上如图2中所示的dsc热谱图
[0130]
(c)基本上如图3中所示的tga热谱图。
[0131]
在一些实施方案中,结晶式i形式i具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图1中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0132]
在某些实施方案中,两性离子结晶式i形式i具有包含在6.7、13.3和16.6度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,两性离子式i形式i具有包含在6.7、13.3和16.6度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在12.3、16.2和20.0度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,两性离子式i形式i具有包含在6.7、
13.3和16.6度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在15.3、22.4和26.6度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,两性离子式i形式i具有包含在6.7、13.3、16.6、12.3、16.2、20.0、15.3、22.4和26.6度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0133]
在一些实施方案中,两性离子式i形式i具有包含在约265℃处开始吸热的差示扫描量热法热谱图。
[0134]
式i两性离子形式ii
[0135]
在一些实施方案中,本文提供的是式i的两性离子结晶化合物(式i形式ii),其中晶体结构表现出基本上如图4中所示的x射线粉末衍射(xrpd)谱图。两性离子结晶式i形式ii可以表现出基本上如图5中所示的差示扫描量热法(dsc)热谱图。结晶式i形式i可以表现出基本上如图6中所示的热重分析(tga)热谱图。
[0136]
在结晶式i形式ii的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式i形式ii具有基本上如图4中所示的xrpd谱图;(b)结晶式i形式ii具有基本上如图5中所示的dsc热谱图;(c)结晶式i形式ii具有基本上如图6中所示的tga热谱图。
[0137]
在一些实施方案中,结晶式i形式ii具有至少一种、至少两种或至少三种以下性质:
[0138]
(a)基本上如图4中所示的xrpd谱图
[0139]
(b)基本上如图5中所示的dsc热谱图
[0140]
(c)基本上如图6中所示的tga热谱图。
[0141]
在一些实施方案中,结晶式i形式ii具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图4中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0142]
在某些实施方案中,两性离子结晶式i形式ii具有包含在7.3、18.1和24.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,两性离子式i形式ii具有包含在7.3、18.1和24.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个、三个或四个在14.5、25.0、25.4和29.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,两性离子式i形式ii具有包含在7.3、18.1、24.1、14.5、25.0、25.4和29.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0143]
在一些实施方案中,两性离子式i形式ii具有有着在约135℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,两性离子式i形式ii具有有着在约271℃处开始吸热的差示扫描量热法热谱图。
[0144]
式i两性离子水合物
[0145]
在一些实施方案中,本文提供的是式i的两性离子结晶化合物(式i水合物),其中晶体结构表现出基本上如图7中所示的x射线粉末衍射(xrpd)谱图。两性离子结晶式i水合物可以表现出基本上如图8中所示的差示扫描量热法(dsc)热谱图。结晶式i水合物可以表现出基本上如图9中所示的热重分析(tga)热谱图。
[0146]
在结晶式i水合物的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式i水合物具有基本上如图7中所示的xrpd谱图;(b)结晶式i水合物具有基本上如图8中所示的dsc热谱图;(c)结晶式i水合物具有基本上如图9中所示的tga热谱图。
[0147]
在一些实施方案中,结晶式i水合物具有至少一种、至少两种或至少三种以下性质:
[0148]
(a)基本上如图7中所示的xrpd谱图
[0149]
(b)基本上如图8中所示的dsc热谱图
[0150]
(c)基本上如图9中所示的tga热谱图。
[0151]
在一些实施方案中,结晶式i水合物具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图7中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0152]
在某些实施方案中,两性离子结晶式i水合物具有包含在10.2、15.4、19.7和23.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,两性离子式i水合物具有包含在10.2、15.4、19.7和23.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个、三个或四个在16.4、17.9、21.7和25.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,两性离子式i水合物具有包含在10.2、15.4、19.7和23.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在10.8、25.0和26.4度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,两性离子式i水合物具有包含在10.2、15.4、19.7、23.1、16.4、17.9、21.7、25.8、10.8、25.0和26.4度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0153]
在一些实施方案中,两性离子式i水合物具有有着在约46℃处开始的宽吸热的差示扫描量热法热谱图。在一些实施方案中,两性离子式i水合物具有有着在约157℃处开始放热的差示扫描量热法热谱图。在一些实施方案中,两性离子式i水合物具有有着在约268℃处开始吸热的差示扫描量热法热谱图。
[0154]
式i两性离子无定形
[0155]
在一些实施方案中,本文提供的是式i的固体两性离子化合物(式i无定形),其中所述固体形式表现出基本上如图10中所示的x射线粉末衍射(xrpd)谱图。
[0156]
式i氨丁三醇盐形式i
[0157]
在一些实施方案中,本文提供的是式i氨丁三醇盐形式i的结晶化合物(式i氨丁三醇盐形式i),其中晶体结构表现出基本上如图11中所示的x射线粉末衍射(xrpd)谱图。式i氨丁三醇盐形式i可以表现出基本上如图12中所示的差示扫描量热法(dsc)热谱图。结晶式i氨丁三醇盐形式i可以表现出基本上如图13中所示的热重分析(tga)热谱图。.
[0158]
在结晶式i氨丁三醇盐形式i的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式i氨丁三醇盐形式i具有基本上如图11中所示的xrpd谱图;(b)结晶式i氨丁三醇盐形式i具有基本上如图12中所示的dsc热谱图;(c)结晶式i氨丁三醇盐形式i具有基本上如图13中所示的tga热谱图。
[0159]
在一些实施方案中,结晶式i氨丁三醇盐形式i具有至少一种、至少两种或至少三种以下性质:
[0160]
(a)基本上如图11中所示的xrpd谱图
[0161]
(b)基本上如图12中所示的dsc热谱图
[0162]
(c)基本上如图13中所示的tga热谱图。
[0163]
在一些实施方案中,结晶式i氨丁三醇盐形式i具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图11中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0164]
在某些实施方案中,结晶式i氨丁三醇盐形式i具有包含在5.2、16.8和25.6度处
的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0165]
在一些实施方案中,式i氨丁三醇盐形式i具有包含在5.2、16.8和25.6度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在10.9、15.3和21.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0166]
在一些实施方案中,式i氨丁三醇盐形式i具有包含在5.2、16.8和25.6度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个、三个、四个或五个在13.3、20.1、20.4、21.0和24.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0167]
在一些实施方案中,式i氨丁三醇盐形式i具有包含在5.2、16.8、25.6、10.9、15.3、21.8和13.3、20.1、20.4、21.0和24.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0168]
在一些实施方案中,式i氨丁三醇盐形式i具有有着在约129℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,式i氨丁三醇盐形式i具有有着在约150℃处开始放热的差示扫描量热法热谱图。
[0169]
式i氨丁三醇盐形式ii
[0170]
在一些实施方案中,本文提供的是式i氨丁三醇盐形式ii的结晶化合物(式i氨丁三醇盐形式ii),其中晶体结构表现出基本上如图14中所示的x射线粉末衍射(xrpd)谱图。
[0171]
在一些实施方案中,结晶式i氨丁三醇盐形式ii具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图14中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0172]
在某些实施方案中,结晶式i氨丁三醇盐形式ii具有包含在9.2、15.9和17.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐形式ii具有包含在9.2、15.9和17.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个、三个或四个在12.9、20.4、24.5和25.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐形式ii具有包含在9.2、15.9、17.3、12.9、20.4、24.5和25.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0173]
式i氨丁三醇盐水合物i
[0174]
在一些实施方案中,本文提供的是式i氨丁三醇盐水合物i的结晶化合物(式i氨丁三醇盐水合物i),其中晶体结构表现出基本上如图15中所示的x射线粉末衍射(xrpd)谱图。式i氨丁三醇盐水合物i可以表现出基本上如图16中所示的差示扫描量热法(dsc)热谱图。结晶式i氨丁三醇盐水合物i可以表现出基本上如图17中所示的热重分析(tga)热谱图。
[0175]
在结晶式i氨丁三醇盐水合物i的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式i氨丁三醇盐水合物i具有基本上如图15中所示的xrpd谱图;(b)结晶式i氨丁三醇盐水合物i具有基本上如图16中所示的dsc热谱图;(c)结晶式i氨丁三醇盐水合物i具有基本上如图17中所示的tga热谱图。
[0176]
在一些实施方案中,结晶式i氨丁三醇盐水合物i具有至少一种、至少两种或至少三种以下性质:
[0177]
(a)基本上如图15中所示的xrpd谱图
[0178]
(b)基本上如图16中所示的dsc热谱图
[0179]
(c)基本上如图17中所示的tga热谱图。
[0180]
在一些实施方案中,结晶式i氨丁三醇盐水合物i具有显示至少两个、至少三个、至
少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图15中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0181]
在某些实施方案中,结晶式i氨丁三醇盐水合物i具有包含在5.9、13.9和23.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐水合物i具有包含在5.9、13.9和23.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在在7.1、12.7和20.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐水合物i具有包含在5.9、13.9和23.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个、三个或四个在在9.8、17.4、22.7和25.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐水合物i具有包含在5.9、13.9、23.3、7.1、12.7、20.3、9.8、17.4、22.7和25.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0182]
在一些实施方案中,式i氨丁三醇盐水合物i具有有着在约74℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,式i氨丁三醇盐水合物i具有在约123℃处开始的吸热。在一些实施方案中,式i氨丁三醇盐水合物i具有有着在约145℃处开始放热的差示扫描量热法热谱图。
[0183]
式i氨丁三醇盐水合物ii
[0184]
在一些实施方案中,本文提供的是式i氨丁三醇盐水合物ii的结晶化合物(式i氨丁三醇盐水合物ii),其中晶体结构表现出基本上如图18中所示的x射线粉末衍射(xrpd)谱图。式i氨丁三醇盐水合物ii可以表现出基本上如图19中所示的差示扫描量热法(dsc)热谱图。结晶式i氨丁三醇盐水合物ii可以表现出基本上如图20中所示的热重分析(tga)热谱图。
[0185]
在结晶式i氨丁三醇盐水合物ii的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式i氨丁三醇盐水合物ii具有基本上如图18中所示的xrpd谱图;(b)结晶式i氨丁三醇盐水合物ii具有基本上如图19中所示的dsc热谱图;(c)结晶式i氨丁三醇盐水合物ii具有基本上如图20中所示的tga热谱图。
[0186]
在一些实施方案中,结晶式i氨丁三醇盐水合物ii具有至少一种、至少两种或至少三种以下性质:
[0187]
(a)基本上如图18中所示的xrpd谱图
[0188]
(b)基本上如图19中所示的dsc热谱图
[0189]
(c)基本上如图20中所示的tga热谱图。
[0190]
在一些实施方案中,结晶式i氨丁三醇盐水合物ii具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图18中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0191]
在某些实施方案中,结晶式i氨丁三醇盐水合物ii具有包含在10.5、16.1和21.5度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐水合物ii具有包含在10.5、16.1和21.5度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在9.0、17.2和18.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐水合物ii具有包含在10.5、16.1和21.5度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个、三个或四个在13.4、20.1、24.9和26.9度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐水合物ii具有包含在10.5、16.1、21.5、9.0、17.2、18.8、13.4、20.1、24.9和26.9度处
的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0192]
在一些实施方案中,式i氨丁三醇盐水合物ii具有有着在约48℃处开始的宽吸热的差示扫描量热法热谱图。在一些实施方案中,式i氨丁三醇盐水合物ii具有有着在约130℃处开始吸热的差示扫描量热法热谱图。
[0193]
式i氨丁三醇盐水合物iii
[0194]
在一些实施方案中,本文提供的是式i氨丁三醇盐水合物iii的结晶化合物(式i氨丁三醇盐水合物iii),其中晶体结构表现出基本上如图21中所示的x射线粉末衍射(xrpd)谱图。式i氨丁三醇盐水合物iii可以表现出基本上如图22中所示的差示扫描量热法(dsc)热谱图。结晶式i氨丁三醇盐水合物iii可以表现出基本上如图23中所示的热重分析(tga)热谱图。
[0195]
在结晶式i氨丁三醇盐水合物iii的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式i氨丁三醇盐水合物iii具有基本上如图21中所示的xrpd谱图;(b)结晶式i氨丁三醇盐水合物iii具有基本上如图22中所示的dsc热谱图;(c)结晶式i氨丁三醇盐水合物iii具有基本上如图23中所示的tga热谱图。
[0196]
在一些实施方案中,结晶式i氨丁三醇盐水合物iii具有至少一种、至少两种或至少三种以下性质:
[0197]
(a)基本上如图21中所示的xrpd谱图
[0198]
(b)基本上如图22中所示的dsc热谱图
[0199]
(c)基本上如图23中所示的tga热谱图。
[0200]
在一些实施方案中,结晶式i氨丁三醇盐水合物iii具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图21中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0201]
在某些实施方案中,结晶式i氨丁三醇盐水合物iii具有包含在10.2、16.0和23.2度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐水合物iii具有包含在10.2、16.0和23.2度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在9.1、15.2和23.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐水合物iii具有包含在10.2、16.0和23.2度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在11.2、12.3、19.0、21.6和26.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐水合物iii具有包含在10.2、16.0、23.2、9.1、15.2、23.8、11.2、12.3、19.0、21.6和26.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0202]
在一些实施方案中,式i氨丁三醇盐水合物iii具有有着在约82℃处开始的宽吸热的差示扫描量热法热谱图。在一些实施方案中,式i氨丁三醇盐水合物iii具有有着在约120℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,式i氨丁三醇盐水合物iii具有有着在约154℃处开始放热的差示扫描量热法热谱图。
[0203]
式i氨丁三醇盐水合物iv
[0204]
在一些实施方案中,本文提供的是式i氨丁三醇盐水合物iv的结晶化合物(式i氨丁三醇盐水合物iv),其中晶体结构表现出基本上如图24中所示的x射线粉末衍射(xrpd)谱图。式i氨丁三醇盐水合物iv可以表现出基本上如图25中所示的差示扫描量热法(dsc)热谱图。结晶式i氨丁三醇盐水合物iv可以表现出基本上如图26中所示的热重分析(tga)热谱
图。
[0205]
在结晶式i氨丁三醇盐水合物iv的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式i氨丁三醇盐水合物iv具有基本上如图24中所示的xrpd谱图;(b)结晶式i氨丁三醇盐水合物iv具有基本上如图25中所示的dsc热谱图;(c)结晶式i氨丁三醇盐水合物iv具有基本上如图26中所示的tga热谱图。
[0206]
在一些实施方案中,结晶式i氨丁三醇盐水合物iv具有至少一种、至少两种或至少三种以下性质:
[0207]
(a)基本上如图24中所示的xrpd谱图
[0208]
(b)基本上如图25中所示的dsc热谱图
[0209]
(c)基本上如图26中所示的tga热谱图。
[0210]
在一些实施方案中,结晶式i氨丁三醇盐水合物iv具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图24中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0211]
在某些实施方案中,结晶式i氨丁三醇盐水合物iv具有包含在11.4、16.9和22.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0212]
在一些实施方案中,式i氨丁三醇盐水合物iv具有包含在11.4、16.9和22.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在14.2、15.3和20.5度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0213]
在一些实施方案中,式i氨丁三醇盐水合物iv具有包含在11.4、16.9和22.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个、三个或四个在13.7、15.8、19.4和21.9度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0214]
在一些实施方案中,式i氨丁三醇盐水合物iv具有包含在11.4、16.9、22.8、14.2、15.3、20.5、13.7、15.8、19.4和21.9度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0215]
在一些实施方案中,式i氨丁三醇盐水合物iv具有有着在约48℃处开始的宽吸热的差示扫描量热法热谱图。在一些实施方案中,式i氨丁三醇盐水合物iv具有有着在约117℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,式i氨丁三醇盐水合物iv具有有着在约148℃处开始吸热的差示扫描量热法热谱图。
[0216]
式i氨丁三醇盐甲醇溶剂合物i
[0217]
在一些实施方案中,本文提供的是式i氨丁三醇盐甲醇溶剂合物i的结晶化合物(式i氨丁三醇盐甲醇溶剂合物i),其中晶体结构表现出基本上如图27中所示的x射线粉末衍射(xrpd)谱图。
[0218]
在一些实施方案中,结晶式i氨丁三醇盐甲醇溶剂合物i具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图27中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0219]
在某些实施方案中,结晶式i氨丁三醇盐甲醇溶剂合物i具有包含在10.8、13.3和22.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0220]
在一些实施方案中,式i氨丁三醇盐甲醇溶剂合物i具有包含在10.8、13.3和22.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在14.5、20.0和21.4度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0221]
在一些实施方案中,式i氨丁三醇盐甲醇溶剂合物i具有包含在10.8、13.3、14.5、20.0、21.4和22.3度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0222]
式i氨丁三醇盐甲醇溶剂合物ii
[0223]
在一些实施方案中,本文提供的是式i氨丁三醇盐甲醇溶剂合物ii的结晶化合物(式i氨丁三醇盐甲醇溶剂合物ii),其中晶体结构表现出基本上如图28中所示的x射线粉末衍射(xrpd)谱图。
[0224]
在一些实施方案中,结晶式i氨丁三醇盐甲醇溶剂合物ii具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图28中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0225]
在某些实施方案中,结晶式i氨丁三醇盐甲醇溶剂合物ii具有包含在5.4、12.9和22.7度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐甲醇溶剂合物ii具有包含在5.4、12.9和22.7度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在10.7、14.3和15.9度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐甲醇溶剂合物ii具有包含在5.4、12.9和22.7度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个或两个在21.2和26.6度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。在一些实施方案中,式i氨丁三醇盐甲醇溶剂合物ii具有包含在5.4、10.7、12.9、14.3、15.9、21.2、22.7和26.6度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0226]
式i氨丁三醇盐甲醇溶剂合物iii
[0227]
在一些实施方案中,本文提供的是式i氨丁三醇盐甲醇溶剂合物iii的结晶化合物(式i氨丁三醇盐甲醇溶剂合物iii),其中晶体结构表现出基本上如图29中所示的x射线粉末衍射(xrpd)谱图。式i氨丁三醇盐甲醇溶剂合物iii可以表现出基本上如图30中所示的差示扫描量热法(dsc)热谱图。结晶式i氨丁三醇盐甲醇溶剂合物iii可以表现出基本上如图31中所示的热重分析(tga)热谱图。
[0228]
在结晶式i氨丁三醇盐甲醇溶剂合物iii的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式i氨丁三醇盐甲醇溶剂合物iii具有基本上如图29中所示的xrpd谱图;(b)结晶式i氨丁三醇盐甲醇溶剂合物iii具有基本上如图30中所示的dsc热谱图;(c)结晶式i氨丁三醇盐甲醇溶剂合物iii具有基本上如图31中所示的tga热谱图。
[0229]
在一些实施方案中,结晶式i氨丁三醇盐甲醇溶剂合物iii具有至少一种、至少两种或至少三种以下性质:
[0230]
(a)基本上如图29中所示的xrpd谱图
[0231]
(b)基本上如图30中所示的dsc热谱图
[0232]
(c)基本上如图31中所示的tga热谱图。
[0233]
在一些实施方案中,结晶式i氨丁三醇盐甲醇溶剂合物iii具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图29中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0234]
在某些实施方案中,结晶式i氨丁三醇盐甲醇溶剂合物iii具有包含在12.6、13.3和13.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0235]
在一些实施方案中,式i氨丁三醇盐甲醇溶剂合物iii具有包含在12.6、13.3和13.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在14.3、17.4和23.2度处的
°
2θ
‑
反射
(
±
0.2
°
2θ)的xrpd谱图。
[0236]
在一些实施方案中,式i氨丁三醇盐甲醇溶剂合物iii具有包含在12.6、13.3和13.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在20.2、24.2、25.2和29.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0237]
在一些实施方案中,式i氨丁三醇盐甲醇溶剂合物iii具有包含在12.6、13.3、13.8、14.3、17.4、20.2、23.2、24.2、25.2和29.1度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0238]
在一些实施方案中,式i氨丁三醇盐甲醇溶剂合物iii具有有着在约80℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,式i氨丁三醇盐甲醇溶剂合物iii具有有着在约110℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,式i氨丁三醇盐甲醇溶剂合物iii具有有着在约127℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,式i氨丁三醇盐水合物iv具有有着在约145℃处开始放热的差示扫描量热法热谱图。
[0239]
式i氨丁三醇盐mtbe溶剂合物
[0240]
在一些实施方案中,本文提供的是式i氨丁三醇盐甲基叔丁基醚(mtbe)溶剂合物的结晶化合物(式i氨丁三醇盐mtbe溶剂合物),其中晶体结构表现出基本上如图32中所示的x射线粉末衍射(xrpd)谱图。式i氨丁三醇盐mtbe溶剂合物可以表现出基本上如图33中所示的差示扫描量热法(dsc)热谱图。结晶式i氨丁三醇盐mtbe溶剂合物可以表现出基本上如图34中所示的热重分析(tga)热谱图。
[0241]
在结晶式i氨丁三醇盐mtbe溶剂合物的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式i氨丁三醇盐mtbe溶剂合物具有基本上如图32中所示的xrpd谱图;(b)结晶式i氨丁三醇盐mtbe溶剂合物具有基本上如图33中所示的dsc热谱图;(c)结晶式i氨丁三醇盐mtbe溶剂合物具有基本上如图34中所示的tga热谱图。
[0242]
在一些实施方案中,结晶式i氨丁三醇盐mtbe溶剂合物具有至少一种、至少两种或至少三种以下性质:
[0243]
(a)基本上如图32中所示的xrpd谱图
[0244]
(b)基本上如图33中所示的dsc热谱图
[0245]
(c)基本上如图34中所示的tga热谱图。
[0246]
在一些实施方案中,结晶式i氨丁三醇盐mtbe溶剂合物具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图32中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0247]
在某些实施方案中,结晶式i氨丁三醇盐mtbe溶剂合物具有包含在5.8、11.4、15.6和20.4度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0248]
在一些实施方案中,式i氨丁三醇盐mtbe溶剂合物具有包含在5.8、11.4、15.6和20.4度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个、三个或四个在14.5、18.4、23.4和25.9度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0249]
在一些实施方案中,式i氨丁三醇盐mtbe溶剂合物具有包含在5.8、11.4、15.6和20.4度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在12.7、19.0和24.7度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0250]
在一些实施方案中,式i氨丁三醇盐mtbe溶剂合物具有包含在5.8、11.4、12.7、14.5、15.6、18.4、19.0、20.4、23.4、24.7和25.9度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0251]
在一些实施方案中,式i氨丁三醇盐mtbe溶剂合物具有有着在约85℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,式i氨丁三醇盐mtbe溶剂合物具有有着在约147℃处开始吸热的差示扫描量热法热谱图。
[0252]
式i氨丁三醇不定形
[0253]
在一些实施方案中,本文提供的是式i氨丁三醇盐不定形形式的化合物(式i氨丁三醇不定形形式),其中所述固体形式表现出基本上如图35中所示的x射线粉末衍射(xrpd)谱图。
[0254]
式i氨丁三醇盐乙醇溶剂合物
[0255]
在一些实施方案中,本文提供的是式i氨丁三醇盐乙醇溶剂合物的结晶化合物(式i氨丁三醇盐乙醇溶剂合物),其中晶体结构表现出基本上如图36中所示的x射线粉末衍射(xrpd)谱图。
[0256]
在一些实施方案中,结晶式i氨丁三醇盐乙醇溶剂合物形式具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图36中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。在一些实施方案中,氨丁三醇盐乙醇溶剂合物具有四个或更多以下特征峰:5.3、10.7、12.1、12.9、21.0、21.6、22.3、22.6、23.8和26.3
°
2θ。
[0257]
式i对甲苯磺酸(p
‑
tsa)盐形式i
[0258]
在一些实施方案中,本文提供的是式ip
‑
tsa盐形式i的结晶化合物(式ip
‑
tsa盐形式i),其中晶体结构表现出基本上如图37中所示的x射线粉末衍射(xrpd)谱图。式i p
‑
tsa盐形式i可以表现出基本上如图38中所示的差示扫描量热法(dsc)热谱图。结晶式i p
‑
tsa盐形式i可以表现出基本上如图39中所示的热重分析(tga)热谱图。
[0259]
在结晶式i p
‑
tsa盐形式i的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式i p
‑
tsa盐形式i具有基本上如图37中所示的xrpd谱图;(b)结晶式ip
‑
tsa盐形式i具有基本上如图38中所示的dsc热谱图;(c)结晶式ip
‑
tsa盐形式i具有基本上如图39中所示的tga热谱图。
[0260]
在一些实施方案中,结晶式i p
‑
tsa盐形式i具有至少一种、至少两种或至少三种以下性质:
[0261]
(a)基本上如图37中所示的xrpd谱图
[0262]
(b)基本上如图38中所示的dsc热谱图
[0263]
(c)基本上如图39中所示的tga热谱图。
[0264]
在一些实施方案中,结晶式i p
‑
tsa盐形式i具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图37中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0265]
在某些实施方案中,结晶式i p
‑
tsa盐形式i具有包含在16.6、20.9、22.3和23.4度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0266]
在一些实施方案中,式ip
‑
tsa盐形式i具有包含在16.6、20.9、22.3和23.4度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在3.0、13.1和21.5度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0267]
在一些实施方案中,式ip
‑
tsa盐形式i具有包含在16.6、20.9、22.3和23.4度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在9.0、15.0、17.5和26度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0268]
在一些实施方案中,式i p
‑
tsa盐形式i具有包含在16.6、20.9、22.3、23.4、3.0、13.1、21.5、9.0、15.0、17.5和26度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0269]
在一些实施方案中,式ip
‑
tsa盐形式i具有有着在约198℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,式i p
‑
tsa盐形式i具有有着在约208℃处开始放热的差示扫描量热法热谱图。
[0270]
式i对甲苯磺酸(p
‑
tsa)盐形式ii
[0271]
在一些实施方案中,本文提供的是式i p
‑
tsa盐形式ii的结晶化合物(式ip
‑
tsa盐形式ii),其中晶体结构表现出基本上如图40中所示的x射线粉末衍射(xrpd)谱图。式ip
‑
tsa盐形式ii可以表现出基本上如图41中所示的差示扫描量热法(dsc)热谱图。结晶式i p
‑
tsa盐形式ii可以表现出基本上如图42中所示的热重分析(tga)热谱图。
[0272]
在结晶式ip
‑
tsa盐形式ii的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式ip
‑
tsa盐形式ii具有基本上如图40中所示的xrpd谱图;(b)结晶式i p
‑
tsa盐形式ii具有基本上如图41中所示的dsc热谱图;(c)结晶式i p
‑
tsa盐形式ii具有基本上如图42中所示的tga热谱图。
[0273]
在一些实施方案中,结晶式ip
‑
tsa盐形式ii具有至少一种、至少两种或至少三种以下性质:
[0274]
(a)基本上如图40中所示的xrpd谱图
[0275]
(b)基本上如图41中所示的dsc热谱图
[0276]
(c)基本上如图42中所示的tga热谱图。
[0277]
在一些实施方案中,结晶式ip
‑
tsa盐形式ii具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图40中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0278]
在某些实施方案中,结晶式ip
‑
tsa盐形式ii具有包含在14.8、20.8、23.2和23.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0279]
在一些实施方案中,式i p
‑
tsa盐形式ii具有包含在14.8、20.8、23.2和23.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在21.6、22.1和24.4度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0280]
在一些实施方案中,式i p
‑
tsa盐形式ii具有包含在14.8、20.8、23.2和23.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在3.0、11.8和16.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0281]
在一些实施方案中,式i p
‑
tsa盐形式i具有包含在14.8、20.8、23.2、23.8、21.6、22.1、24.4、3.0、11.8和16.8度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0282]
在一些实施方案中,式i p
‑
tsa盐形式ii具有有着在约202℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,式ip
‑
tsa盐形式ii具有有着在约155℃处开始放热的差示扫描量热法热谱图。在一些实施方案中,式i p
‑
tsa盐形式ii具有有着在约209℃处放热开始的差示扫描量热法热谱图。
[0283]
式i对甲苯磺酸(p
‑
tsa)盐形式iii
[0284]
在一些实施方案中,本文提供的是式i p
‑
tsa盐形式iii的结晶化合物(式ip
‑
tsa盐形式i),其中晶体结构表现出基本上如图43中所示的x射线粉末衍射(xrpd)谱图。式ip
‑
tsa盐形式iii可以表现出基本上如图44中所示的差示扫描量热法(dsc)热谱图。结晶式ip
‑
tsa盐形式iii可以表现出基本上如图45中所示的热重分析(tga)热谱图。
[0285]
在结晶式ip
‑
tsa盐形式iii的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式i p
‑
tsa盐形式iii具有基本上如图43中所示的xrpd谱图;(b)结晶式i p
‑
tsa盐形式iii具有基本上如图44中所示的dsc热谱图;(c)结晶式ip
‑
tsa盐形式iii具有基本上如图45中所示的tga热谱图。
[0286]
在一些实施方案中,结晶式ip
‑
tsa盐形式iii具有至少一种、至少两种或至少三种以下性质:
[0287]
(a)基本上如图43中所示的xrpd谱图
[0288]
(b)基本上如图44中所示的dsc热谱图
[0289]
(c)基本上如图45中所示的tga热谱图。
[0290]
在一些实施方案中,结晶式ip
‑
tsa盐形式iii具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图43中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0291]
在某些实施方案中,结晶式i p
‑
tsa盐形式iii具有包含在11.9、14.8、16.9和23.2度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0292]
在一些实施方案中,式ip
‑
tsa盐形式iii具有包含在11.9、14.8、16.9和23.2度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在17.6、20.8、22.1和24.6度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0293]
在一些实施方案中,式ip
‑
tsa盐形式iii具有包含在11.9、14.8、16.9和23.2度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在12.3、18.8和26.6度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0294]
在一些实施方案中,式i p
‑
tsa盐形式i具有包含在11.9、14.8、16.9、23.2、17.6、20.8、22.1、24.6、12.3、18.8和26.6度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0295]
在一些实施方案中,式ip
‑
tsa盐形式iii具有有着在约156℃处开始放热的差示扫描量热法热谱图。在一些实施方案中,式ip
‑
tsa盐形式iii具有有着在约205℃处开始吸热的差示扫描量热法热谱图。
[0296]
式i对甲苯磺酸(p
‑
tsa)盐水合物
[0297]
在一些实施方案中,本文提供的是式ip
‑
tsa盐形式i的结晶化合物(式i p
‑
tsa盐水合物),其中晶体结构表现出基本上如图46中所示的x射线粉末衍射(xrpd)谱图。式i p
‑
tsa盐水合物可以表现出基本上如图47中所示的差示扫描量热法(dsc)热谱图。结晶式i p
‑
tsa盐水合物可以表现出基本上如图48中所示的热重分析(tga)热谱图。
[0298]
在结晶式ip
‑
tsa盐水合物的一些实施方案中,以下(a)
‑
(c)的至少一个、至少两个或全部适用:(a)结晶式ip
‑
tsa盐水合物具有基本上如图46中所示的xrpd谱图;(b)结晶式ip
‑
tsa盐水合物具有基本上如图47中所示的dsc热谱图;(c)结晶式ip
‑
tsa盐水合物具有基本上如图48中所示的tga热谱图。
[0299]
在一些实施方案中,结晶式ip
‑
tsa盐水合物具有至少一种、至少两种或至少三种
以下性质:
[0300]
(a)基本上如图46中所示的xrpd谱图
[0301]
(b)基本上如图47中所示的dsc热谱图
[0302]
(c)基本上如图48中所示的tga热谱图。
[0303]
在一些实施方案中,结晶式ip
‑
tsa盐水合物具有显示至少两个、至少三个、至少四个、至少五个、至少六个、至少七个、至少八个或至少九个基本上如图46中所示的xrpd谱图的具有最大强度的
°
2θ
‑
反射的xrpd谱图。
[0304]
在某些实施方案中,结晶式ip
‑
tsa盐水合物具有包含在6.6、8.6、19.8和25.5度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0305]
在一些实施方案中,式i p
‑
tsa盐水合物具有包含在6.6、8.6、19.8和25.5度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个、三个或四个在11.3、17.1、22.5和28.4度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0306]
在一些实施方案中,式i p
‑
tsa盐水合物具有包含在6.6、8.6、19.8和25.5度处的
°
2θ
‑
反射(
±
0.2
°
2θ)和一个、两个或三个在15.6、17.7和26.9度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0307]
在一些实施方案中,式i p
‑
tsa盐水合物具有包含在6.6、8.6、19.8、25.5、11.3、17.1、22.5和28.4、15.6、17.7和26.9度处的
°
2θ
‑
反射(
±
0.2
°
2θ)的xrpd谱图。
[0308]
在一些实施方案中,式ip
‑
tsa盐水合物具有有着在约144℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,式ip
‑
tsa盐水合物具有有着在约192℃处开始吸热的差示扫描量热法热谱图。在一些实施方案中,式i p
‑
tsa盐水合物具有有着在约214℃处开始放热的差示扫描量热法热谱图。
[0309]
药物组合物
[0310]
出于施用的目的,在某些实施方案中,本文描述的化合物作为原料化学品施用或配制成药物组合物。本公开内容的药物组合物可以包含治疗有效量的式i的化合物和至少一种药学上可接受的载体和/或赋形剂。式i的化合物以有效治疗具有感兴趣的特定疾病或病症的量存在于组合物中。本公开内容的药物组合物可以另外包含一种或多种其它的,作为活性成分的化合物,包括例如前药、其它的核受体调节剂或其它的活性药物成分,例如用于治疗肝病的活性药物成分,如acc抑制剂或ask1抑制剂。在一些实施方案中,本公开内容的药物组合物另外包含acc抑制剂和ask1抑制剂。
[0311]
在一些实施方案中,药物组合物包含式i两性离子形式i;式i两性离子形式ii;式i水合物;式i两性离子无定形;式i氨丁三醇盐形式i;式i氨丁三醇盐形式ii;式i氨丁三醇盐水合物i;式i氨丁三醇盐水合物ii;式i氨丁三醇盐水合物iii;式i氨丁三醇盐水合物iv;式i氨丁三醇盐甲醇溶剂合物i;式i氨丁三醇盐甲醇溶剂合物ii;式i氨丁三醇盐甲醇溶剂合物iii;式i氨丁三醇盐mtbe溶剂合物;式i氨丁三醇无定形形式;式i氨丁三醇盐乙醇溶剂合物;式i对甲苯磺酸盐形式i;式i对甲苯磺酸盐形式ii;式i对甲苯磺酸盐形式iii;和/或式i对甲苯磺酸盐水合物。在一些实施方案中,药物组合物包含式i两性离子形式i;式i两性离子形式ii;式i水合物;式i两性离子无定形;式i氨丁三醇盐形式i;式i氨丁三醇盐形式ii;式i氨丁三醇盐水合物i;式i氨丁三醇盐水合物ii;式i氨丁三醇盐水合物iii;式i氨丁三醇盐水合物iv;式i氨丁三醇盐甲醇溶剂合物i;式i氨丁三醇盐甲醇溶剂合物ii;式i氨丁三醇
盐甲醇溶剂合物iii;式i氨丁三醇盐mtbe溶剂合物;式i氨丁三醇无定形形式;式i氨丁三醇盐乙醇溶剂合物;式i对甲苯磺酸盐形式i;式i对甲苯磺酸盐形式ii;式i对甲苯磺酸盐形式iii;和/或式i对甲苯磺酸盐水合物和药学上可接受的载体。
[0312]
在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是两性离子形式i,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是两性离子形式ii,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是水合物,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i两性离子无定形,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i氨丁三醇盐形式i,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i氨丁三醇盐形式ii,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i氨丁三醇盐水合物i,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i氨丁三醇盐水合物ii,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i氨丁三醇盐水合物iii,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i氨丁三醇盐水合物iv,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i氨丁三醇盐甲醇溶剂合物i,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i氨丁三醇盐甲醇溶剂合物ii,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i氨丁三醇盐甲醇溶剂合物iii,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i氨丁三醇盐mtbe溶剂合物,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i氨丁三醇无定形形式,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i氨丁三醇盐乙醇溶剂合物,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i对甲苯磺酸盐形式i,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离
子、水合物、盐或溶剂合物),其中至少95%的式i是式i对甲苯磺酸盐形式ii,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i对甲苯磺酸盐形式iii,以及不超过5%、4%、3%、2%或1%的其它形式。在一些实施方案中,药物组合物包含式i的化合物(或其两性离子、水合物、盐或溶剂合物),其中至少95%的式i是式i对甲苯磺酸盐水合物,以及不超过5%、4%、3%、2%或1%的其它形式。在任何此类实施方案中,所述药物组合物包含药学上可接受的载体。
[0313]
式i的化合物的活性可以由本领域技术人员确定,例如,如本文所述。本领域技术人员可以容易地确定合适的治疗有效浓度和剂量。
[0314]
在某些实施方案中,本文描述的结晶、盐和/或溶剂合物形式可以展现出改善的性质。例如,在某些实施方案中,本文描述的结晶和/或盐形式可以展现出改善的稳定性。这种改善的稳定性可以对制造式i的化合物具有潜在的有益影响,例如提供长时间储存过程中间体的能力。改善的稳定性也可以有益于式i的化合物的组合物或药物组合物。在某些实施方案中,本文描述的结晶、盐和/或溶剂合物形式也可以潜在地导致式i的化合物的产率提高,或式i的化合物的质量提高。在某些实施方案中,本文描述的结晶、盐和/或溶剂合物形式也可以展现出改善的药代动力学性质和/或潜在改善的生物利用度。
[0315]
所述组合物适用于口服、直肠、局部、肠胃外(包括皮下、肌肉内和静脉内)、眼(眼用的)、肺(鼻或口腔吸入)或鼻给药,尽管任何给定情况下的最合适的途径将取决于所治疗的病症的性质和严重程度,以及将取决于所述活性成分的性质。它们可以方便地以单位剂型存在并通过药学领域熟知的任何方法制备。
[0316]
在实际使用中,本公开内容的化合物可以作为活性成分根据常规的药物混合技术与药学上的载体密切地混合来组合。根据给药所需的制剂形式,例如口服或肠胃外(包括静脉内),所述载体可以采用多种形式。在制备用于口服剂型的组合物时,在口服液体制剂(例如混悬液、酏剂和溶液)的情况下,可以使用任何常用药学上的媒介,例如,水、二醇类(glycols)、油、醇类、调味剂、防腐剂、着色剂等;或在口服固体制剂(例如粉末、硬与软胶囊剂和片剂)的情况下,可以使用载体,例如淀粉、糖、微晶纤维素、稀释剂、造粒剂、润滑剂、粘合剂、崩解剂等,固体口服制剂优选于液体制剂。
[0317]
由于给药方便,片剂和胶囊剂代表最有利的口服剂量单位形式,在这种情况下采用固体药学上的载体。如果需要,片剂可以通过标准的水性或非水性技术进行包衣。这种组合物和制剂应含有至少0.1%的活性化合物。当然,这些组合物中的活性化合物的百分比可以变化并且可以方便地在单位重量的约2%至约60%之间。此类治疗上有用的组合物中的活性化合物的量使得将获得有效剂量。所述活性化合物也可以鼻内给药,例如作为液滴或喷雾剂。
[0318]
片剂、丸剂、胶囊剂等也可以含有粘合剂如黄蓍胶、阿拉伯树胶、玉米淀粉或明胶;赋形剂如磷酸二钙、微晶纤维素、乳糖一水合物、甘露醇或胶体二氧化硅;崩解剂如玉米淀粉、马铃薯淀粉、海藻酸、交联羧甲基纤维素钠或交聚维酮;润滑剂如硬脂酸镁;和甜味剂如蔗糖、乳糖或糖精。当剂量单位形式是胶囊剂时,除了上述类型的材料之外,它可以含有液体载体如脂肪油或药学上的媒介例如水、乙二醇(例如聚乙二醇400)或醇类。
[0319]
各种其它材料可以作为涂层存在或改变剂量单位的物理形式。例如,片剂可以用
虫胶、糖、聚乙烯醇、聚乙二醇3350、二氧化钛、滑石粉、着色剂,或它们的组合包衣。除了活性成分之外,糖浆或酏剂可以含有作为甜味剂的蔗糖、作为防腐剂的对羟基苯甲酸甲酯和对羟基苯甲酸丙酯、染料和调味剂如樱桃味或橙味调味剂。
[0320]
本公开内容的化合物也可以肠胃外给药。这些活性化合物的溶液或混悬液可以在与在与有机物、添加剂或它们的组合适当混合的水中制备。有机物的实例包括但不限于n
‑
甲基吡咯烷酮、二甲亚砜、聚乙二醇,和它们的组合。添加剂的实例包括但不限于羟丙基纤维素、聚乙烯吡咯烷酮、泊洛沙姆、聚(乳酸
‑
共
‑
乙醇酸)、聚山梨醇酯、聚维酮、羧甲基纤维素,和它们的组合。分散剂也可以在甘油、液体聚乙二醇,和它们在油中的混合物中制备。在通常的储存和使用条件下,这些制剂可以含有防腐剂以,例如防止微生物的生长。在一些实施方案中,肠胃外给药包括用包含有机物和水性介质混合物的溶液的制剂进行静脉内给药。在一些实施方案中,所述静脉给药以100%有机溶液给药。
[0321]
适用于可注射用途的药物形式包括无菌水性溶液或分散剂以及用于临时制备无菌可注射溶液或分散剂的无菌粉末。在所有情况下,所述形式必须是无菌的,并且必须是流体,以达到存在易注射性的程度。例如,所述形式可以在制造和储存的条件下是稳定的。所述形式可以防止微生物如细菌和真菌的污染作用(例如,通过使用防腐剂)。载体可以是溶剂或分散介质,其含有例如水、乙醇、多元醇(例如甘油、丙二醇和液体聚乙二醇),它们的合适的混合物和植物油。
[0322]
为了向哺乳动物,尤其是人类提供有效剂量的本公开内容的化合物,可以使用任何合适的给药途径。例如,可以使用口服、直肠、局部、肠胃外、眼、肺、鼻等。剂型包括片剂、锭剂、分散剂、混悬剂、溶液剂、胶囊剂、霜剂、软膏剂、气雾剂等。在一些实施方案中,本公开内容的化合物是口服给药的。
[0323]
在一些实施方案中,所述组合物包含式i或其药学上可接受的盐的结晶形式。在一些实施方案中,所述组合物含有式i的化合物的两性离子的结晶形式。在一些实施方案中,所述组合物含有式i的化合物的氨丁三醇盐的结晶形式。在某些实施方案中提供了包含如本文描述的结晶形式的组合物,其中所述组合物中的式i基本上是纯的(即基本上纯的式i两性离子形式i;式i两性离子形式ii;式i水合物;式i两性离子无定形;式i氨丁三醇盐形式i;式i氨丁三醇盐形式ii;式i氨丁三醇盐水合物i;式i氨丁三醇盐水合物ii;式i氨丁三醇盐水合物iii;式i氨丁三醇盐水合物iv;式i氨丁三醇盐甲醇溶剂合物i;式i氨丁三醇盐甲醇溶剂合物ii;式i氨丁三醇盐甲醇溶剂合物iii;式i氨丁三醇盐mtbe溶剂合物;式i氨丁三醇无定形形式;式i氨丁三醇盐乙醇溶剂合物;式i;式i对甲苯磺酸盐形式i;式i对甲苯磺酸盐形式ii;式i对甲苯磺酸盐形式iii;或式i对甲苯磺酸盐水合物)。
[0324]
在包含式i或其药学上可接受的盐的结晶形式的组合物的具体的实施方案中,所述组合物中存在的至少约50%、至少约60%、至少约70%、至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%或至少约99%的式i是一种本文公开的结晶形式。在某些实施方案中,所述组合物含有至少约50%、至少约60%、至少约70%、至少约80%、至少约85%、至少约90%、至少约95%、至少约96%、至少约97%、至少约98%或至少约99%的一种式i的结晶形式。
[0325]
在包含本文公开的结晶形式的组合物的其它的实施方案中,所述组合物中存在的低于约50%、低于约40%、低于约30%、低于约20%、低于约10%、低于约5%、低于约4%、低
于约3%、低于约2%或低于约1%的式i是式i的其它的无定形或晶体形式和/或杂质。
[0326]
在包含本文公开的结晶形式的组合物的其它的实施方案中,相对于存在的结晶形式的质量,杂质占低于约5%、低于约4%、低于约3%、低于约2%或低于约1%的总质量。杂质可以,例如,包括来自合成式i的副产物、污染物、降解产物、其它的结晶形式、无定形形式、水和溶剂。在某些实施方案中,杂质包括来自合成式i的方法的副产物。在某些实施方案中,杂质包括来自合成式i的方法的污染物。在某些实施方案中,杂质包括式i的降解产物。在某些实施方案中,杂质包括式i的其它的结晶形式。在某些实施方案中,杂质包括式i的其它的结晶形式和/或式i的其它的无定形形式。在某些实施方案中,杂质包括水和溶剂。在包含本文公开的结晶形式的组合物的某些实施方案中,杂质选自合成式i的副产物、污染物、降解产物、其它的结晶形式、无定形形式、水、溶剂,和它们的组合。
[0327]
剂量
[0328]
所用活性成分的有效剂量可以根据所用的具体化合物、给药方式、所治疗的病症和所治疗病症的严重程度而变化。本领域技术人员可以容易地确定这种剂量。
[0329]
当治疗或预防本公开内容的化合物所针对的fxr介导的病症时,当本公开内容的化合物以每千克动物体重约0.1毫克至约100毫克的日剂量施用时,通常获得令人满意的结果。在一些实施方案中,本公开内容的化合物作为单次日剂量或以每天两至六次的分剂量或以缓释形式给予。对于大多数大型哺乳动物,总日剂量可以是约1毫克至约1000毫克。在70kg成人的情况下,总日剂量将通常为约7毫克至约350毫克。可以调整该给药方案以提供最佳的治疗反应。在一些实施方案中,所述总日剂量为约1毫克至约900毫克、约10毫克至约800毫克、约20毫克至约700毫克、约30毫克至约600毫克、约40毫克至约550毫克或约50毫克至约400毫克。在一些实施方案中,所述总日剂量为约10毫克至约50毫克、约20毫克至约40毫克、约25毫克至约35毫克、约50毫克至约150毫克、约70毫克至约130毫克、约80毫克至约120毫克、约90毫克至约100毫克、约1毫克至约150毫克、约1毫克至约75毫克、约1毫克至约50毫克、约25毫克至约125毫克、约125毫克至约275毫克、约275毫克至约425毫克、约425毫克至约575毫克、约575毫克至约725毫克、约725毫克至约875毫克、或约875毫克至约1000毫克。
[0330]
本技术的化合物或其组合物可以使用上述任何合适的模式每天给药一次、两次、三次或四次。另外,化合物的给药或治疗可以持续数天;例如,对于一个治疗周期,通常治疗将持续至少7天、14天或28天。治疗周期在癌症化疗中是公知的,并且经常在周期之间以约1至28天,通常约7天或约14天的休息期交替。在一些实施方案中,所述治疗周期是30天。在其它的实施方案中,所述治疗周期也可为连续的。
[0331]
在具体的实施方案中,本文提供的方法包括向受试者给药约1mg至约800mg的本文描述的化合物的初始日剂量并以增量增加剂量直至实现临床功效。可以使用约5、10、25、30、40、50或100mg的增量来增加剂量。剂量可以每天、每隔一天、每周两次、每周一次或每四周一次增加。
[0332]
治疗方法和用途
[0333]“治疗”或“处置”是用于得到有益的或者希望的结果(包括临床结果)的方法。有益的或者希望的临床结果可以包括以下中的一个或者多个:(a)抑制疾病或者病症(例如,减少由疾病或者病症导致的一个或者多个症状和/或减轻疾病或者病症的程度);(b)减慢或
者阻止与疾病或者病症相关的一个或者多个临床症状的发展(例如,稳定疾病或者病症,防止或者延缓疾病或者病症的恶化或者进程,和/或防止或者延缓疾病或者病症的扩散(例如,转移));和/或(c)减轻疾病,即,导致临床症状消退(例如,改善疾病状态,提供疾病或者病症的部分或者全部缓解,增强其它药物的效果,延缓疾病进程,提高生命质量和/或延长存活率)。
[0334]
本公开内容另外涉及所述化合物通过所述化合物与所述核受体的结合来治疗和/或预防疾病和/或病症的用途。此外,本公开内容涉及所述化合物在制备用于通过所述化合物与所述核受体结合来治疗和/或预防疾病和/或病症的药物中的用途。
[0335]
本文还提供治疗患有fxr介导的病症的患者的方法。在一些实施方案中,所述方法包括施用本文公开的化合物或组合物。在一些实施方案中,治疗患有fxr介导的病症的患者的方法包括施用治疗有效量的式i两性离子形式i;式i两性离子形式ii;式i水合物;式i两性离子无定形;式i氨丁三醇盐形式i;式i氨丁三醇盐形式ii;式i氨丁三醇盐水合物i;式i氨丁三醇盐水合物ii;式i氨丁三醇盐水合物iii;式i氨丁三醇盐水合物iv;式i氨丁三醇盐甲醇溶剂合物i;式i氨丁三醇盐甲醇溶剂合物ii;式i氨丁三醇盐甲醇溶剂合物iii;式i氨丁三醇盐mtbe溶剂合物;式i氨丁三醇无定形形式;式i氨丁三醇盐乙醇溶剂合物;式i;式i对甲苯磺酸盐形式i;式i对甲苯磺酸盐形式ii;式i对甲苯磺酸盐形式iii;和/或式i对甲苯磺酸盐水合物。
[0336]
本文还提供在有需要的患者中治疗或预防疾病或病症的方法,包括施用治疗有效量的fxr激动剂,其中所述疾病或病症是先天性肝纤维化,并且其中所述fxr激动剂是式i的化合物。
[0337][0338]
在一些实施方案中,治疗患有先天性肝纤维化的患者的方法包括施用式i的化合物。在一些实施方案中,治疗患有先天性肝纤维化的患者的方法包括施用式i的化合物的固体形式。
[0339]
在一些实施方案中,提供本文公开的化合物或组合物用于治疗fxr介导的病症。
[0340]
在一些实施方案中,提供本文公开的化合物或组合物用于制造用于治疗fxr介导的病症的药物。
[0341]
在一些实施方案中,所述fxr介导的病症是:慢性肝内或者一些形式的肝外胆汁郁积性病症;肝纤维化;肝脏的梗阻性炎性障碍;肝脏的慢性炎性障碍;肝硬化;肝脏脂肪变性或相关综合征;与酒精诱发性肝硬化或与病毒传播形式的肝炎相关的胆汁淤积或纤维化效应;大型肝切除术后肝衰竭或肝缺血;化疗相关脂肪性肝炎(cash);急性肝衰竭;或炎性肠病。
[0342]
在一些实施方案中,所述fxr介导的病症是脂质障碍或脂蛋白障碍;i型糖尿病;ii
型糖尿病;选自糖尿病性肾病、糖尿病性神经病变、糖尿病性视网膜病的i型和ii型糖尿病的临床并发症,以及其它观察到的临床显现出长期糖尿病的效应;非酒精性脂肪性肝病(nafld);非酒精性脂肪性肝炎(nash);肥胖症;选自血脂异常、糖尿病和异常高的体重指数的组合病症的代谢综合征;急性心肌梗塞;急性中风;或作为慢性阻塞性动脉粥样硬化的终点出现的血栓形成。
[0343]
在一些实施方案中,所述fxr介导的病症是:非恶性过度增殖性障碍;和选自肝细胞癌、结肠腺瘤和息肉病的恶性过度增殖性障碍;结肠腺癌;乳腺癌;胰腺腺癌;巴雷特食管;或其它形式的胃肠道和肝脏的肿瘤性疾病。
[0344]
在一些实施方案中,所述fxr介导的病症是非酒精性脂肪性肝炎(nash)、原发性硬化性胆管炎(psc)或原发性胆汁性肝硬化(pbc)。
[0345]
在一些实施方案中,所述fxr介导的病症是先天性肝纤维化。
[0346]
在一些实施方案中,本公开内容涉及本文公开的化合物和组合物在制备用于预防和/或治疗下列疾病的药物中的用途:慢性肝内或者一些形式的肝外胆汁郁积性病症、肝纤维化、急性肝内胆汁郁积性病症、由胆汁组成不当引起的梗阻性或者慢性炎性障碍、具有减少的膳食脂肪和脂溶性膳食维生素摄入的胃肠病症、炎性肠病、脂质和脂蛋白障碍、ii型糖尿病以及i型和ii型糖尿病的临床并发症、由器官的慢性脂肪性和纤维性变性产生的病症和疾病,所述器官的慢性脂肪性和纤维性变性由于强制的脂质并且具体为甘油三酯积累和随后促纤维化途径的活化所导致,肥胖症和代谢综合征(血脂障碍、糖尿病和异常高的体重指数的合并病症)、急性心肌梗塞、急性中风、作为慢性阻塞性动脉粥样硬化的终点出现的血栓形成、细胞内细菌或者寄生原生动物的持续感染、非恶性过度增殖性性障碍、恶性过度增殖性性障碍、结肠腺癌并且具体为肝细胞癌、肝脏脂肪变性和相关综合征、作为慢性肝病或者外科肝切除的结果的肝功能衰竭或者肝功能失常、乙型肝炎感染、丙型肝炎感染、与酒精诱发性肝硬化或者与病毒传播型肝炎相关的胆汁郁积性和纤维变性影响和/或先天性肝纤维化。
[0347]
本文所指的药物可以通过常规方法制备,所述药物包括根据本公开内容的化合物和药学上可接受的载体的组合。
[0348]
试剂盒
[0349]
本文还提供了试剂盒,其包括本文描述的化合物或组合物,以及合适的包装。在一个实施方案中,试剂盒还包括使用说明书。在一个方面,试剂盒包括本公开内容的结晶形式,或包括本公开内容的结晶形式的组合物,和标签和/或使用化合物治疗本文描述的适应症(包括疾病或病症)的说明书。
[0350]
本文还提供了制品,其在合适容器中包含本文描述的化合物或组合物。所述容器可以是小瓶、罐子、安瓿、预装注射器和静脉袋。
[0351]
组合疗法
[0352]
在一些实施方案中,本文公开了口服剂型(例如,片剂),其包含式i的化合物或其药学上可接受的盐的新型结晶形式和至少一种额外的治疗剂,所述化合物为下式:
[0353][0354]
在一些实施方案中,本文公开的口服剂型包含新型晶体形式式i或其药学上可接受的盐和一种、两种或三种额外的治疗剂。
[0355]
在一些实施方案中,所述治疗剂或治疗剂的组合是ace抑制剂、乙醛脱氢酶抑制剂、乙酰辅酶a羧化酶抑制剂、乙酰辅酶a羧化酶抑制剂、二酰基甘油o
‑
酰基转移酶2抑制剂、腺苷a3受体激动剂、脂联素受体激动剂、乙醛脱氢酶2刺激物、akt蛋白激酶抑制剂、amp激活蛋白激酶(ampk)、amp激酶激活剂、atp柠檬酸裂解酶抑制剂、amp激活蛋白激酶刺激物、内皮型一氧化氮合酶刺激物、nad依赖性脱乙酰酶沉默调节蛋白
‑
1刺激物、雄激素受体激动剂、胰淀素受体激动剂、血管紧张素ii at
‑
1受体拮抗剂、自噬蛋白调节剂、自毒素抑制剂、axl酪氨酸激酶受体抑制剂、bax蛋白刺激物、生物活性脂质、降钙素激动剂、大麻素受体调节剂、胱天蛋白酶抑制剂、胱天蛋白酶3刺激物、组织蛋白酶抑制剂、小窝蛋白1抑制剂、ccr2趋化因子拮抗剂、ccr2趋化因子拮抗剂、血管紧张素ii at
‑
1受体拮抗剂、ccr3趋化因子拮抗剂、ccr5趋化因子拮抗剂、cd3拮抗剂、氯离子通道刺激物、cnr1抑制剂、细胞周期蛋白d1抑制剂、细胞色素p450 7a1抑制剂、dgat1/2抑制剂、二酰基甘油o
‑
酰基转移酶1抑制剂(dgat1)、细胞色素p450 2e1抑制剂(cyp2e1)、cxcr4趋化因子拮抗剂、二肽基肽酶iv抑制剂、内皮唾酸蛋白调节剂、嗜酸性粒细胞趋化因子配体抑制剂、细胞外基质蛋白调节剂、法尼醇x受体激动剂、脂肪酸合酶抑制剂、fgf1受体激动剂、成纤维细胞生长因子(fgf
‑
15、fgf
‑
19、fgf
‑
21)配体、半乳凝集素
‑
3抑制剂、胰高血糖素受体激动剂、胰高血糖素样肽1激动剂、g蛋白偶联胆汁酸受体1激动剂、g蛋白偶联受体84拮抗剂、hedgehog(hh)调节剂、丙型肝炎病毒ns3蛋白酶抑制剂、肝细胞核因子4α调节剂(hnf4a)、肝细胞生长因子调节剂、组蛋白脱乙酰酶抑制剂、stat
‑
3调节剂、hmg辅酶a还原酶抑制剂、低氧诱导因子2α抑制剂、il
‑
10激动剂、il
‑
17拮抗剂、回肠胆酸钠协同转运蛋白抑制剂、胰岛素增敏剂、胰岛素配体激动剂、胰岛素受体激动剂、整合素调节剂、整合素拮抗剂、白介素
‑
1受体
‑
相关激酶4(irak4)抑制剂、il
‑
6受体激动剂、jak2酪氨酸激酶抑制剂、己酮糖激酶(khk)抑制剂、克洛索β刺激物、5
‑
脂氧合酶抑制剂、脂蛋白脂酶抑制剂、肝脏x受体、lpl基因刺激物、溶血磷脂
‑
1受体拮抗剂、赖氨酰氧化酶同系物2抑制剂、巨噬细胞甘露糖受体1调节剂、基质金属蛋白酶(mmp)抑制剂、mekk
‑
5蛋白激酶抑制剂、mch受体
‑
1拮抗剂、膜铜胺氧化酶(vap
‑
1)抑制剂、甲硫氨酸氨肽酶
‑
2抑制剂、甲基cpg结合蛋白2调节剂、微小rna
‑
21(mir
‑
21)抑制剂、线粒体解偶联剂、混合谱系激酶
‑
3抑制剂、髓鞘碱性蛋白刺激物、nacht lrr pyd结构域蛋白3(nlrp3)抑制剂、nad
‑
依赖性脱乙酰酶沉默调节蛋白(sirtuin)刺激物、nadph氧化酶抑制剂(nox)、烟酸受体1激动剂、p2y13嘌呤受体刺激物、核受体调节剂、p2x7嘌呤受体调节剂、pde 3抑制剂、pde 4抑制剂、pde 5抑制剂、pdgf受体β调节剂、苯基丙氨酸羟化酶刺激物、磷脂酶c抑制剂、pparα激动剂、pparδ激动剂、pparγ激动剂、肽基脯氨酰基顺反异构酶a抑制剂、pparγ调节剂、蛋白酶激活受体
‑
2拮抗剂、蛋白激酶调节剂、rho相关蛋白激酶抑制剂、s
‑
亚硝基谷
胱甘肽还原酶(gsnor)酶抑制剂、钠葡糖转运子
‑
2抑制剂、srebp转录因子抑制剂、stat
‑
1抑制剂、硬脂酰辅酶a去饱和酶
‑
1抑制剂、stk25抑制剂、细胞因子信号传导抑制因子
‑
1刺激物、细胞因子信号传导抑制因子
‑
3刺激物、转化生长因子β(tgf
‑
β)、转化生长因子β活化激酶1(tak1)、甲状腺激素受体β激动剂、tlr
‑
4拮抗剂、转谷氨酰胺酶抑制剂、酪氨酸激酶受体调节剂、gpcr调节剂、核激素受体调节剂、wnt调节剂、yap/taz调节剂和连蛋白抑制剂。
[0356]
一种或多种额外治疗剂的非限制性实例包括:
[0357]
ace抑制剂,例如依那普利;
[0358]
乙醛脱氢酶抑制剂,例如adx
‑
629;
[0359]
乙酰辅酶a羧化酶(acc)抑制剂,例如ndi
‑
010976(firsocostat)、drm
‑
01、吉卡宾、pf
‑
05175157、qlt
‑
091382、pf
‑
0522 1304;
[0360]
乙酰辅酶a羧化酶/二酰基甘油o
‑
酰基转移酶2抑制剂,例如pf
‑
07055341;
[0361]
腺苷受体激动剂,例如cf
‑
102(namodenoson)、cf
‑
101、cf
‑
502、cgs21680;
[0362]
脂联素受体激动剂,例如adp
‑
355、adp
‑
399;
[0363]
乙醛脱氢酶2刺激物,例如fp
‑
045;
[0364]
胰淀素/降钙素受体激动剂,例如kbp
‑
042、kbp
‑
089;
[0365]
amp激活蛋白激酶刺激物,例如、pxl
‑
770、o
‑
304;
[0366]
amp激酶激活剂/atp柠檬酸裂解酶抑制剂,例如贝培多酸(bempedoic acid)(etc
‑
1002、esp
‑
55016)
[0367]
amp激活蛋白激酶/内皮型一氧化氮合酶/nad依赖性脱乙酰酶沉默调节蛋白
‑
1刺激物,例如ns
‑
0200;
[0368]
雄激素受体激动剂,例如lpcn
‑
1144;
[0369]
血管紧张素ii at
‑
1受体拮抗剂,例如厄贝沙坦;血管生成素相关蛋白
‑
3抑制剂,例如ionis
‑
angptl3
‑
lrx;
[0370]
自噬蛋白调剂剂,例如a
‑
2906;
[0371]
自毒素抑制剂,例如pat
‑
505、pat
‑
048、glpg
‑
1690、x
‑
165、pf
‑
8380、am
‑
063、bbt
‑
877;
[0372]
axl酪氨酸激酶受体抑制剂,例如bemcentinib(bgb
‑
324、r
‑
428);
[0373]
bax蛋白刺激物,例如cbl
‑
514;
[0374]
生物活性脂质,例如ds
‑
102;
[0375]
大麻素受体调节剂,例如namacizumab、gwp
‑
42004、rev
‑
200、crb
‑
4001;
[0376]
胱天蛋白酶抑制剂,例如恩利卡生;
[0377]
泛(pan)组织蛋白酶b抑制剂,例如vby
‑
376;
[0378]
泛组织蛋白酶抑制剂,例如vby
‑
825;
[0379]
ccr2/ccr5趋化因子拮抗剂,例如西尼韦罗、马拉韦罗、ccx
‑
872、wxsh
‑
0213;
[0380]
ccr2趋化因子拮抗剂,例如丙帕锗;
[0381]
ccr2趋化因子/血管紧张素ii at
‑
1受体拮抗剂,例如dmx
‑
200、dmx
‑
250;
[0382]
ccr3趋化因子拮抗剂,例如柏替木单抗;
[0383]
cd3拮抗剂,例如ni
‑
0401;
[0384]
氯离子通道刺激物,例如考前列酮;
[0385]
cxcr4趋化因子拮抗剂,例如ad
‑
214;
[0386]
二脂酰甘油脂酰基转移酶2(dgat2)抑制剂,例如ionis
‑
dgat2rx、pf
‑
06865571;
[0387]
二脂酰甘油脂酰基转移酶1(dgat1)抑制剂,例如gsk
‑
3008356;
[0388]
二酰基甘油o
‑
酰基转移酶1(dgat1)/细胞色素p450 2e1抑制剂(cyp2e1),例如snp
‑
610;
[0389]
二肽基肽酶iv抑制剂,例如利拉利汀、依格列汀;
[0390]
嗜酸性粒细胞趋化因子配体抑制剂,例如柏替木单抗、cm
‑
101;
[0391]
细胞外基质蛋白调节剂,例如cnx
‑
024;
[0392]
法尼醇x受体(fxr)激动剂,例如agn
‑
242266、agn
‑
242256、ep
‑
024297、rdx
‑
023、bwl
‑
200、akn
‑
083、edp
‑
305、gnf
‑
5120、gs
‑
9674、lmb
‑
763、奥贝胆酸、px
‑
102、px
‑
103、m790、m780、m450、m
‑
480、(met
‑
409)、px20606、eyp
‑
001、tern
‑
101、tc
‑
100、int
‑
2228;
[0393]
法尼醇x受体(fxr)/g蛋白偶联胆汁酸受体1(tgr5)激动剂,例如int
‑
767;
[0394]
脂肪酸合酶抑制剂,例如tvb
‑
2640;
[0395]
成纤维细胞生长因子19(rhfgf19)/细胞色素p450(cyp)7a1抑制剂,例如ngm
‑
282;
[0396]
成纤维细胞生长因子21(fgf
‑
21)配体,例如bms
‑
986171、bio89
‑
100、bms
‑
986036、b
‑
1344;
[0397]
成纤维细胞生长因子21(fgf
‑
21)/胰高血糖素样肽1(glp
‑
1)激动剂,例如yh
‑
25723akr
‑
001;
[0398]
半乳凝集素
‑
3抑制剂,例如gr
‑
md
‑
02、gb
‑
1107;
[0399]
胰高血糖素样肽1(glp1r)激动剂,例如ac
‑
3174、利拉鲁肽、cotadutide(medi
‑
0382)、sar
‑
425899、ly
‑
3305677、hm
‑
15211、yh
‑
25723、yh
‑
glp1、rpc
‑
8844、pb
‑
718、索马鲁肽;
[0400]
g蛋白偶联胆汁酸受体1(tgr5)激动剂,例如rdx
‑
009、int
‑
777;
[0401]
热激蛋白47(hsp47)抑制剂,例如nd
‑
l02
‑
s0201;
[0402]
组蛋白脱乙酰酶抑制剂/stat
‑
3调节剂,例如sfx
‑
01;
[0403]
hmg辅酶a还原酶抑制剂,例如阿托伐他汀、氟伐他汀、匹伐他汀、普伐他汀、瑞舒伐他汀和辛伐他汀;
[0404]
低氧诱导因子2α抑制剂,例如pt
‑
2567;
[0405]
il
‑
10激动剂,例如peg
‑
伊洛白介素;
[0406]
回肠胆酸钠协同转运蛋白抑制剂,例如odevixibat(a
‑
4250)、volixibat乙醇钾水合物(shp
‑
262)、gsk2330672、cj
‑
14199、依洛昔巴特/(a
‑
3309);
[0407]
胰岛素增敏剂,例如、kbp
‑
042、msdc
‑
0602k、msdc
‑
5514、px
‑
102、rg
‑
125(azd4076)、vvp
‑
100x、cb
‑
4211、eti
‑
101;
[0408]
胰岛素配体/胰岛素受体激动剂(insulin ligand/dsinsulin receptor agonists),
[0409]
例如ormd
‑
0801;
[0410]
整合素拮抗剂,例如idl
‑
2965;
[0411]
il
‑
6受体激动剂,例如km
‑
2702;
[0412]
己酮糖激酶(khk)抑制剂,例如pf
‑
06835919;
[0413]
β克洛索(klb)
‑
fgf1c激动剂,例如mk
‑
3655(ngm
‑
313);
[0414]5‑
脂氧合酶抑制剂,例如泰鲁司特(mn
‑
001)、ds
‑
102(af
‑
102);
[0415]
脂蛋白脂酶抑制剂,例如cat
‑
2003;
[0416]
lpl基因刺激物,例如替帕阿立泊基;
[0417]
肝脏x受体(lxr)抑制剂,例如px
‑
l603、px
‑
l493、bms
‑
852927、t
‑
0901317、gw
‑
3965、sr
‑
9238;
[0418]
溶血磷脂
‑
1受体拮抗剂,例如bmt
‑
053011、ud
‑
009(cp
‑
2090)、ar
‑
479、itmn
‑
10534、bms
‑
986020、ki
‑
16198;
[0419]
赖氨酰氧化酶同系物2抑制剂,例如simtuzumab、pxs
‑
5382a(pxs
‑
5338);
[0420]
巨噬细胞甘露糖受体1调节剂,例如tilmanocept
‑
cy3(technetium tc 99m tilmanocept);
[0421]
膜铜胺氧化酶(vap
‑
1)抑制剂,例如tern
‑
201;
[0422]
mekk
‑
5蛋白激酶(ask
‑
1)抑制剂,例如gs
‑
4997、srt
‑
015、gs
‑
444217、gst
‑
hg
‑
151;
[0423]
mch受体
‑
1拮抗剂,例如csti
‑
100(alb
‑
127158);
[0424]
氨基脲敏感的胺氧化酶/血管粘附蛋白
‑
1(ssao/vap
‑
1)抑制剂,例如pxs
‑
4728a;
[0425]
甲硫氨酸氨肽酶
‑
2抑制剂,例如zgn
‑
1061、zgn
‑
839、zn
‑
1345;
[0426]
甲基cpg结合蛋白2调节剂,例如巯乙胺;
[0427]
盐皮质激素受体拮抗剂(mcra),例如mt
‑
3995;
[0428]
线粒体解偶联剂,例如2,4
‑
二硝基酚;
[0429]
混合谱系激酶
‑
3抑制剂,例如urmc
‑
099
‑
c;
[0430]
髓鞘碱性蛋白刺激物,例如奥索来肟;
[0431]
髓过氧化物酶抑制剂,例如pf
‑
06667272、azm
‑
198;
[0432]
nadph氧化酶抑制剂,例如gkt
‑
831、apx
‑
311;
[0433]
烟酸受体1激动剂,例如ari
‑
3037mo;
[0434]
nacht lrr pyd结构域蛋白3(nlrp3)抑制剂,例如kddf
‑
201406
‑
03、nbc
‑
6、ifm
‑
514、jt
‑
194(jt
‑
349);
[0435]
核受体调节剂,例如dur
‑
928(dv
‑
928);
[0436]
p2x7嘌呤受体调节剂,例如sgm
‑
1019;
[0437]
p2y13嘌呤受体刺激物,例如cer
‑
209;
[0438]
pde 3/4抑制剂,例如泰鲁司特(mn
‑
001);
[0439]
pde 5抑制剂,例如西地那非、mstm
‑
102;
[0440]
pdgf受体β调节剂,例如bot
‑
191、bot
‑
509;
[0441]
肽基脯氨酰基顺反异构酶抑制剂,例如crv
‑
431(cpi
‑
432
‑
32)、nvp
‑
018、nv
‑
556(nvp
‑
025);
[0442]
苯基丙氨酸羟化酶刺激物,例如hepastem;
[0443]
ppar激动剂,例如elafibranor(gft
‑
505)、seladelpar lysine(mbx
‑
8025)、氘代吡格列酮r
‑
对映异构体、吡格列酮、drx
‑
065、赛格列扎(saroglitazar)、lanifibranor(iva
‑
337)、chs
‑
131;
[0444]
蛋白酶激活受体
‑
2拮抗剂,例如pz
‑
235;
[0445]
蛋白激酶调节剂,例如cnx
‑
014;
[0446]
rho相关蛋白激酶(rock)抑制剂,例如redx
‑
10178(redx
‑
10325)、kd
‑
025;
[0447]
s
‑
亚硝基谷胱甘肽还原酶(gsnor)酶抑制剂,例如sl
‑
891;
[0448]
钠葡糖转运子
‑
2(sglt2)抑制剂,例如依格列净、依碳酸瑞格列净、埃格列净、达格列净、托格列净和索格列净(sotagliflozin);
[0449]
钠葡糖转运子
‑
1/2(sglt 1/2)抑制剂,例如利可格列净二(脯氨酸盐);srebp转录因子抑制剂,例如cat
‑
2003、mdv
‑
4463;
[0450]
硬脂酰辅酶a去饱和酶
‑
1抑制剂,例如aramchol;
[0451]
甲状腺激素受体β激动剂,例如resmetirom(mgl
‑
3196)、mgl
‑
3745、
[0452]
vk
‑
2809;
[0453]
tlr
‑
2/tlr
‑
4拮抗剂,例如vb
‑
201(ci
‑
201);
[0454]
tlr
‑
4拮抗剂,例如jkb
‑
121;
[0455]
酪氨酸激酶受体调节剂,例如cnx
‑
025;
[0456]
gpcr调节剂,例如cnx
‑
023;
[0457]
核激素受体调节剂,例如px
‑
102;
[0458]
黄嘌呤氧化酶/尿素阴离子交换剂1(urat1)抑制剂,例如rlbn
‑
1001、
[0459]
rlbn
‑
1127;和
[0460]
连蛋白抑制剂,例如lorazotide acetate(inn
‑
202)。
[0461]
在某些特定的实施方案中,一种或多种额外的治疗剂选自a
‑
4250、ac
‑
3174、乙酰水杨酸、ak
‑
20、替帕阿立泊基、amx
‑
342、an
‑
3015、aramchol、ari
‑
3037mo、asp
‑
8232、azd
‑
2693、柏替木单抗、无水甜菜碱、bi
‑
1467335、bms
‑
986036、bms
‑
986171、bmt
‑
053011、bot
‑
191、btt
‑
1023、cat
‑
2003、西尼韦罗、cbw
‑
511、cer
‑
209、cf
‑
102、cgs21680、cnx
‑
014、cnx
‑
023、cnx
‑
024、cnx
‑
025、考前列酮、考来维仑、达格列净、dcr
‑
liv1、氘代吡格列酮r
‑
对映异构体、2,4
‑
二硝基酚、drx
‑
065、ds
‑
102、dur
‑
928、edp
‑
305、elafibranor(gft
‑
505)、恩利卡生、依那普利、艾格列净、依格列汀(evogliptin)、f
‑
351、fluasterone(st
‑
002)、ft
‑
4101、gkt
‑
831、gnf
‑
5120、gri
‑
0621、gr
‑
md
‑
02、gs
‑
300、gs
‑
4997、gs
‑
9674、htd
‑
1801、hst
‑
202、hst
‑
201、氢氯噻嗪、icosabutate(prc
‑
4016)、二十碳五烯酸乙酯、imm
‑
124
‑
e、int
‑
767、inv
‑
240、ionis
‑
dgat2rx、依格列净、厄贝沙坦、丙帕锗、iva
‑
337、jkb
‑
121、kb
‑
ge
‑
001、kbp
‑
042、kd
‑
025、m790、m780、m450、二甲双胍、西地那非、lc
‑
280126、利拉利汀、利拉鲁肽、ljn
‑
452、lm
‑
011、lm
‑
002(cvi
‑
lm
‑
002)、lmb
‑
763、lyn
‑
100、mbx
‑
8025、mdv
‑
4463、巯乙胺、mgl
‑
3196、mgl
‑
3745、mp
‑
301、msdc
‑
0602k、namacizumab、nc
‑
101、ndi
‑
010976、nd
‑
l02
‑
s0201、ngm
‑
282、ngm
‑
313、ngm
‑
386、ngm
‑
395、np
‑
160、去甲熊去氧胆酸、nvp
‑
022、o
‑
304、奥贝胆酸、25hc3s、奥利索西、pat
‑
505、pat
‑
048、pb
‑
4547、peg
‑
伊洛白介素、吡格列酮、吡非尼酮、pri
‑
724、px20606、px
‑
102、px
‑
l603、px
‑
l493、pxs
‑
4728a、pz
‑
235、rdx
‑
009、依碳酸瑞格列净、rg
‑
125(azd4076)、rpi
‑
500、saroglitazar、司美鲁肽、simtuzumab、索利霉素、索格列净、他汀类药物(阿托伐他汀、氟伐他汀、匹伐他汀、普伐他汀、瑞舒伐他汀、辛伐他汀)、tcm
‑
606f、tev
‑
45478,tqa
‑
3526、泰鲁司特(mn
‑
001)、tly
‑
012、trx
‑
318、tvb
‑
2640、ud
‑
009、熊去氧胆酸、vby
‑
376、vby
‑
825、vk
‑
2809、维莫德吉、volixibat乙醇钾水合物(shp
‑
626)、vvp
‑
100x、wav
‑
301、wnt
‑
974、xrx
‑
117、zgn
‑
839、zg
‑
5216、zsym
‑
008、zysm
‑
007。
[0462]
在一些实施方案中,方法和组合物包括治疗有效量的细胞凋亡信号调节激酶1(ask1)抑制剂和治疗有效量的法尼醇x受体(fxr)激动剂,其中所述fxr激动剂是本文描述的固体形式。
[0463]
在本文公开的方法和药物组合物的某些实施方案中,ask1抑制剂是式ii的化合物或其药学上可接受的盐、立体异构体、立体异构体的混合物或互变异构体:
[0464][0465]
ask1抑制剂,例如式(ii)的化合物,可以使用本领域技术人员已知的方法合成和表征,例如在u.s.2007/0276050、u.s.2011/0009410和u.s.2013/0197037中描述的那些。
[0466]
在一些实施方案中,方法和组合物包括治疗有效量的乙酰辅酶a羧化酶抑制剂和治疗有效量的法尼醇x受体(fxr)激动剂,其中所述fxr激动剂是本文描述的固体形式。
实施例
[0467]
方法
[0468]
根据已知方法合成式i的化合物,例如美国专利号9,139,539中公开的那些。
[0469]
x射线粉末衍射(xrpd)
[0470]
在pananalytical xpert
‑
pro衍射仪上,在以下实验设置下在环境条件下采集xrpd图谱:45kv,40ma,扫描范围2至40
°
2θ,步长0.0084或0.0167
°
2θ,测量时间:5min。
[0471]
一些x射线粉末衍射数据是在环境条件下在rigaku miniflex 600衍射仪上使用cu kα(1.5406埃)辐射收集的。在40kv和15ma,于具有0.1mm凹痕的零背景支架上从2至40
°
2θ的2θ以2
°
2θ每分钟的扫描速率收集粉末谱图。
[0472]
差示扫描量热法(dsc)
[0473]
在配备有50位自动取样器的ta instruments q2000系统上采集dsc热谱图。使用合乎标准的铟进行能量和温度校准。典型地,将1
‑
5mg的各样品在带针孔铝盘中以10c/min从25℃加热至300℃。在整个测量中,在样品上维持50ml/min的干燥氮气吹扫。熔融吸热的起始记录为熔点。
[0474]
一些dsc分析是使用ta discovery series dsc实施的,在tzero铝盘中使用几毫克的材料,该盘用包含两个针孔的tzero密封盖密封。在50ml每分钟的氮气流下,以10℃每分钟扫描样品。
[0475]
热重分析(tga)
[0476]
在配备有25位自动取样器的ta instruments q5000系统上采集tga热谱图。典型地,将1
‑
5mg的各样品装载到预配衡的铝盘中并且以10℃/min从25℃加热至350℃。在整个测量中,在样品上维持25ml/min的氮气吹扫。
[0477]
一些热重分析数据是用ta discovery series tga收集的。在铝制样品盘中分析
了几毫克的材料。以10℃每分钟的扫描速率收集从室温到300℃的数据。
[0478]
式i两性离子形式i
[0479]
式i两性离子形式i是非溶剂合物形式。它通过在ph 3.5
‑
4.0从etoh中结晶式i首次获得。
[0480]
进行了xrpd分析。图1显示了式i的两性离子化合物形式i的xrpd谱图。鉴定了xrpd峰并将其包括在下表1中。
[0481]
表1.
[0482][0483][0484]
进行了dsc分析。图2显示了式i的两性离子化合物形式i的dsc热谱图。所述dsc分析显示在约265℃处开始的吸热,随后对应于分解的放热。
[0485]
进行了tga分析。图3显示了式i的两性离子化合物形式i的tga热谱图。所述tga分析表明在低于约150℃,固体损失约0.9%的重量。
[0486]
式i两性离子形式ii
[0487]
式i的两性离子化合物形式ii是非溶剂合物形式。它是通过将式i两性离子形式i溶解在dmso(4倍体积)中,然后加入反溶剂(40倍体积的ipac、etoac或mecn)并在室温搅拌而获得。式i两性离子形式ii还在式i氨丁三醇盐在meoh/水(0.4
‑
0.6水活度)中歧化后获
得。
[0488]
进行了xrpd分析。图4显示了式i的两性离子化合物形式ii的xrpd谱图。鉴定了xrpd峰并将其包括在下表2中。
[0489]
表2.
[0490][0491][0492]
进行了dsc分析。图5显示了式i的两性离子化合物形式ii的dsc热谱图。如图所示,dsc提供在约135℃处开始的小吸热和在约271℃处开始的吸热,随后是对应于分解的放热。
[0493]
进行了tga分析。图6显示了式i的两性离子化合物形式ii的tga热谱图。如图所示,在低于约100℃,固体损失约0.7%的重量,在约100
‑
150℃,固体损失约1.1%的重量。
[0494]
式i两性离子水合物
[0495]
式i两性离子水合物是结晶形式。由于式i氨丁三醇盐的歧化,它从式i氨丁三醇盐在水中的浆液中获得。
[0496]
进行了xrpd分析。图7显示了式i的两性离子化合物水合物的xrpd谱图。鉴定了xrpd峰并将其包括在下表3中。
[0497]
表3.
[0498][0499]
进行了dsc分析。图8显示了式i的两性离子化合物水合物的dsc热谱图。可以看出,dsc提供了在约46℃处开始的宽吸热,在约157℃处开始的小放热,和在约268℃处开始的熔融吸热,随后对应于分解的放热。
[0500]
进行了tga分析。图9显示了式i的两性离子化合物水合物的tga热谱图。如图所示,在约低于约100℃,固体损失约2.4%的重量,在约100
‑
250℃,固体损失约1.1%的重量。
[0501]
式i两性离子无定形
[0502]
式i的无定形两性离子化合物通过在含有不锈钢球的不锈钢舱中球磨式i(约1.1g)约5分钟来首次获得。无定形两性离子式i还使用以下方法获得:将式i(1.0当量)、水(20.0v)和50%naoh(1.5当量)装入反应器,然后搅拌直至实现溶解。然后将反应混合物精过滤(polish
‑
filtered),用1.0m hcl(1.5当量)酸化,搅拌约20秒,并过滤以分离所得固体。将固体用水(20v)洗涤并转移到充满氮气的手套袋中,然后在氮气下干燥过夜。
[0503]
进行了xrpd分析。图10显示式i的无定形两性离子化合物的xrpd谱图。
[0504]
式i氨丁三醇盐形式i
[0505]
式i氨丁三醇盐(tris盐)形式i通过干燥式i氨丁三醇盐乙醇溶剂合物(在0%rh和25℃)获得。式i氨丁三醇盐形式i也通过在50℃真空下干燥式i氨丁三醇盐水合物i来获得。式i氨丁三醇盐形式i也从在50℃真空下干燥式i氨丁三醇盐甲醇溶剂合物获得。
[0506]
图11显示了式i氨丁三醇盐形式i的xrpd谱图。鉴定了xrpd峰,如下表4所示。
[0507]
表4.
[0508][0509][0510]
进行了dsc分析。图12显示了式i氨丁三醇盐形式i的dsc热谱图。熔融在约129℃处开始,然后在约150℃处开始放热并分解。
[0511]
进行了tga分析。图13显示了式i氨丁三醇盐形式i的tga热谱图。可以看出,在分解之前,在低于约150℃,固体没有显示任何重量损失。
[0512]
式i氨丁三醇盐形式ii
[0513]
式i氨丁三醇盐形式ii通过在约80
‑
120℃脱水式i氨丁三醇盐水合物ii,以及在
0%rh和25℃脱水后来获得的。式i氨丁三醇盐形式ii还通过在约50
‑
80℃真空干燥式i甲醇溶剂合物i、式i甲醇溶剂合物ii或式i甲醇溶剂合物iii而获得。式i氨丁三醇盐形式ii是非溶剂合物形式,其在约>20%rh快速吸收水分并转化为式i氨丁三醇盐水合物ii。
[0514]
进行了xrpd分析。图14显示了式i氨丁三醇盐形式ii的xrpd谱图。xrpd峰的鉴定如下表5所示。
[0515]
表5.
[0516][0517][0518]
式i氨丁三醇盐水合物i
[0519]
式i氨丁三醇盐水合物i是通过在环境条件和约98%rh、约20
‑
25℃平衡式i氨丁三醇盐乙醇溶剂合物来获得。式i氨丁三醇盐水合物i还通过在环境条件和约98%rh、约20
‑
25℃平衡式i氨丁三醇盐甲醇溶剂合物来获得。式i氨丁三醇盐水合物i还通过在约80
‑
98%
rh,在约20
‑
25℃平衡式i氨丁三醇盐形式i来获得。
[0520]
进行了xrpd分析。图15显示了式i氨丁三醇盐水合物i的xrpd谱图。鉴定了xrpd峰并将其包括在下表6中。
[0521]
表6.
[0522][0523][0524]
进行了dsc分析。图16显示了式i氨丁三醇盐水合物i的dsc热谱图。在约74℃处开始的宽吸热对应于水的损失。熔融是在约123℃处开始,然后在约145℃处开始放热并分解。在约100℃脱水后,式i氨丁三醇盐水合物i转化为非溶剂合物的式i氨丁三醇盐形式i。
[0525]
进行了tga分析。图17显示了式i氨丁三醇盐水合物i的tga热谱图。在低于约100℃,固体损失约6.2%的重量,这对应于约2.4当量的水。
[0526]
式i氨丁三醇盐水合物ii
[0527]
式i氨丁三醇盐水合物ii是在环境条件,通过从空气(>10%rh)中吸附水分,将式i氨丁三醇盐乙醇溶剂合物和式i氨丁三醇盐形式i在乙腈中浆化来获得。式i氨丁三醇盐水合物ii还通过在环境条件平衡式i氨丁三醇盐形式ii来获得。
[0528]
进行了xrpd分析。图18显示了式i氨丁三醇盐水合物ii的xrpd谱图。鉴定了xrpd峰并将其包括在下表7中。
[0529]
表7.
[0530][0531]
进行了dsc分析。图19显示了式i氨丁三醇盐水合物ii的dsc热谱图。在约48℃处开始的宽吸热对应于水的损失。在约130℃处开始熔融,然后放热和分解。在约80℃脱水后,式i氨丁三醇盐水合物ii转化为非溶剂合物形式,即式i氨丁三醇盐形式ii。
[0532]
进行了tga分析。图20显示了式i氨丁三醇盐水合物ii的tga热谱图。在低于约100℃,固体损失约4.3%的重量,这相当于约1.8当量的水。
[0533]
式i氨丁三醇盐水合物iii
[0534]
式i氨丁三醇盐水合物iii是通过将220mg式i和约1.1当量tris(50mg)和6ml mecn/10%水装入20ml小瓶中来获得。将浆液在约50℃搅拌过夜,然后在室温搅拌约3天。分离出的固体用2ml乙腈洗涤,并在约40℃真空下干燥过夜。
[0535]
进行了xrpd分析。图21显示了式i氨丁三醇盐水合物iii的xrpd谱图。鉴定了xrpd峰并将其包括在下表8中。
[0536]
表8.
[0537][0538]
进行了dsc分析。图22显示了式i氨丁三醇盐水合物iii的dsc热谱图。在约20
‑
110℃处的宽吸热,其中在约82℃开始的吸热对应于水的损失。在约120℃处开始熔融,然后在
约154℃处开始的放热和分解。
[0539]
进行了tga分析。图23显示了式i氨丁三醇盐水合物iii的tga热谱图。在低于约125℃,固体损失约4.8%的重量,相当于约2当量的水。
[0540]
式i氨丁三醇盐水合物iv
[0541]
式i氨丁三醇盐水合物iv是通过将式i氨丁三醇盐形式i与丙酮、dcm和甲苯混合并在环境条件平衡获得的固体来获得。
[0542]
进行了xrpd分析。图24显示了式i氨丁三醇盐水合物iv的xrpd谱图。鉴定了xrpd峰并将其包括在下表9中。
[0543]
表9.
[0544][0545][0546]
进行了dsc分析。图25显示了式i氨丁三醇盐水合物iv的dsc热谱图。在约20
‑
90℃处的宽吸热,其中在约48℃处开始的吸热对应于水的损失,然后在约117℃处开始的小吸热。在约148℃处开始熔融,然后放热和分解。
[0547]
进行了tga分析。图26显示了式i氨丁三醇盐水合物iv的tga热谱图。在低于约100℃,固体损失约2.6%的重量,这相当于约1当量的水。
[0548]
式i氨丁三醇盐甲醇溶剂合物i
[0549]
式i氨丁三醇盐甲醇溶剂合物i是通过将6g式i、约1.1当量tris(1.36g)和60ml meoh装入100ml夹套反应器来获得。将浆液在约50℃搅拌过夜以提供非常大的meoh溶剂合物i颗粒,这通过单晶x射线分析得到证实。单晶x射线分析显示每分子式i氨丁三醇盐两个甲醇分子。式i氨丁三醇盐甲醇溶剂合物i在环境条件非常迅速地失去甲醇并转化为氨丁三醇盐甲醇溶剂合物iii,其进一步转化为氨丁三醇盐水合物i。式i氨丁三醇盐甲醇溶剂合物i也在thf和mtbe浆液中转化为甲醇溶剂合物ii。式i氨丁三醇盐甲醇溶剂合物i也通过在环境条件,平衡式i氨丁三醇盐形式i、式i氨丁三醇盐水合物i、式i氨丁三醇盐水合物ii、式i氨丁三醇盐水合物iii、式i氨丁三醇盐水合物iv、式i氨丁三醇盐甲醇溶剂合物ii、式i氨丁三醇盐甲醇溶剂合物iii、式i氨丁三醇盐乙醇溶剂合物和式i氨丁三醇盐mtbe溶剂合物在高达10%的水/meoh混合物中来获得。
[0550]
进行了xrpd分析。图27显示了式i氨丁三醇盐甲醇溶剂合物i的xrpd谱图。鉴定了xrpd峰并将其包括在下表10中。
[0551]
表10.
[0552][0553][0554]
式i氨丁三醇盐甲醇溶剂合物ii
[0555]
如上所述,式i氨丁三醇盐甲醇溶剂合物ii是从式i氨丁三醇meoh溶剂合物i在thf中的浆液里获得。它也从在meoh/mtbe和meoh/5%水/mtbe中的式i氨丁三醇盐形成来获得。
[0556]
进行了xrpd分析。图28显示了式i氨丁三醇盐甲醇溶剂合物ii的xrpd谱图。鉴定了xrpd峰并将其包括在下表11中。
[0557]
表11.
[0558][0559][0560]
式i氨丁三醇盐甲醇溶剂合物iii
[0561]
式i氨丁三醇盐甲醇溶剂合物iii是通过在环境条件平衡式i氨丁三醇盐甲醇溶剂合物i约5
‑
10分钟而获得。它还通过在环境条件平衡式i氨丁三醇盐甲醇溶剂合物ii约5
‑
10分钟而获得。在环境条件,氨丁三醇甲醇溶剂合物iii在约1小时内(取决于%rh)完全转化为式i氨丁三醇盐水合物i。
[0562]
进行了xrpd分析。图29显示了式i氨丁三醇盐甲醇溶剂合物iii的xrpd谱图。鉴定了xrpd峰并将其包括在下表12中。
[0563]
表12.
[0564][0565][0566]
进行了dsc分析。图30显示了式i氨丁三醇盐甲醇溶剂合物iii的dsc热谱图。观察到在约80和110℃处开始的两个吸热。这些可能对应于甲醇和水的损失。在约127℃处开始熔融,然后在约145℃处开始放热并分解。去溶剂化后,式i氨丁三醇甲醇溶剂合物iii转化为非溶剂合物形式——式i氨丁三醇盐形式i。
[0567]
进行了tga分析。图31显示了式i氨丁三醇盐甲醇溶剂合物iii的tga热谱图。在低于约120℃,固体损失约6.0%的重量。卡尔费休(kf)分析显示约1.1%的水。进行了1h nmr
分析,并且所得频谱显示约1.1当量甲醇,这相当于约4.7重量%。
[0568]
式i氨丁三醇盐mtbe溶剂合物
[0569]
式i氨丁三醇盐mtbe溶剂合物是通过在50℃,将式i氨丁三醇盐形式i(50mg)在mtbe(1ml)中浆化而获得。通过xrpd分析湿固体。所述mtbe溶剂合物在环境条件并在50℃真空干燥后转化为无序材料。
[0570]
进行了xrpd分析。图32显示了式i氨丁三醇盐mtbe溶剂合物的xrpd谱图。鉴定了xrpd峰并将其包括在下表13中。
[0571]
表13.
[0572][0573][0574]
进行了dsc分析。图33显示了式i氨丁三醇盐mtbe溶剂合物的dsc热谱图。在约85℃处开始的宽吸热对应于溶剂的损失。在约147℃处开始熔融,然后放热和分解。
[0575]
进行了tga分析。图34显示了式i氨丁三醇盐mtbe溶剂合物的tga热谱图。在低于约120℃,固体显示约6.2%的重量损失,其对应于约0.5当量的mtbe。
[0576]
式i氨丁三醇盐无定形
[0577]
式i氨丁三醇盐无定形形式是通过在高温(约65℃),将式i氨丁三醇盐(约0.89mg)在约5ml thf中,然后在约40℃(浴温),于旋转蒸发仪上快速蒸发得到泡沫,然后在约50℃真空下干燥约2小时而获得。
[0578]
进行了xrpd分析。图35显示了式i氨丁三醇盐无定形形式的xrpd谱图。
[0579]
式i氨丁三醇盐乙醇溶剂合物
[0580]
式i氨丁三醇盐乙醇溶剂合物是通过将52.5mg两性离子式i、约1.1当量tris(12mg)和1ml乙醇装入4ml小瓶而获得。将浆液在约50℃搅拌约5小时并在室温搅拌过夜。通过xrpd分析湿固体样品并提供乙醇溶剂合物的独特的xrpd谱图,其在环境条件转化为式i氨丁三醇盐水合物i。
[0581]
进行了xrpd分析。图36显示了所述式i氨丁三醇盐乙醇溶剂合物的xrpd谱图。获得xrpd峰并在下表14中描述。
[0582]
表14
[0583][0584]
式i p
‑
tsa盐形式i
[0585]
式ip
‑
tsa盐形式i是通过在50℃,将52.7mg式i形式i用1.1当量对甲苯磺酸一水合物(18.8mg)在1ml etoh中溶解,然后冷却至室温并在该温度搅拌约16小时来获得。式ip
‑
tsa盐形式i也在以下溶剂中使用类似方法获得:thf、methf、mecn、ipac、ipa、etoac。式ip
‑
tsa盐形式i也由式i形式i在mecn/水或etoh/水混合物(9:1或8:2)中与naoh(1.1当量)和对甲苯磺酸一水合物(2.2当量)来制备或由式i氨丁三醇盐形式i在mecn/水或etoh/水混合物(9:1或8:2)中与naoh(1.1当量)和对甲苯磺酸一水合物(3.2当量)来制备。式ip
‑
tsa盐形式i还通过在20、35、55和70℃将式i p
‑
tsa盐水合物在mecn中浆化来制备。
[0586]
进行了xrpd分析。图37显示了式i p
‑
tsa盐形式i的xrpd谱图。鉴定了xrpd峰并将其包括在下表15中。
[0587]
表15.
[0588][0589]
进行了dsc分析。图38显示了式i p
‑
tsa盐形式i的dsc热谱图。dsc提供了在约198℃处开始的熔融吸热,然后在约208℃处开始的放热与分解。
[0590]
进行了tga分析。图39显示式ip
‑
tsa盐形式i的tga热谱图。在低于约170℃,固体损失约0.6%的重量,在约170
‑
235℃,固体损失约3.0%的重量,这对应于由于分解而损失的水。
[0591]
式i p
‑
tsa盐形式ii
[0592]
式i p
‑
tsa盐形式ii是通过在室温,将式i p
‑
tsa盐形式i在以下溶剂中搅拌3周获得:mecn、meoh、etoh、ipa、丙酮、mek、mibk、thf、methf、etoac、ipac、mtbe、甲苯和庚烷。
[0593]
进行了xrpd分析。图40显示了式i p
‑
tsa盐形式ii的xrpd谱图。鉴定了xrpd峰并将其包括在下表16中。
[0594]
表16.
[0595][0596]
进行了dsc分析。图41显示式ip
‑
tsa盐形式ii的dsc热谱图。dsc提供了在约155℃处开始的宽放热,在约202℃处开始的熔融吸热,然后在约209℃处开始的放热和分解。
[0597]
进行了tga分析。图42显示式i p
‑
tsa盐形式ii的tga热谱图。在低于约175℃,固体损失约0.7%的重量,和在约175
‑
238℃,固体损失约3.0%的重量,这对应于由于分解而损失的水。
[0598]
式i p
‑
tsa盐形式iii
[0599]
式ip
‑
tsa盐形式iii是通过在室温,搅拌在下列溶剂中搅拌式ip
‑
tsa盐形式i约3周后获得的式i p
‑
tsa盐形式i来获得的:etoac、甲苯和在mecn/水(其中0.6、0.7和0.95的水活度)。
[0600]
进行了xrpd分析。图43显示了式i p
‑
tsa盐形式iii的xrpd谱图。鉴定了xrpd峰并将其包括在下表17中。
[0601]
表17.
[0602][0603][0604]
进行了dsc分析。图44显示式ip
‑
tsa盐形式iii的dsc热谱图。dsc提供了在约156℃处开始的宽放热,在约205℃处开始的熔融吸热,然后在立即放热和分解。
[0605]
进行了tga分析。图45显示式ip
‑
tsa盐形式iii的tga热谱图。在低于约175℃,固体损失约0.5%的重量,和在约175
‑
235℃,固体损失约2.5%的重量,这对应于由于分解而损失的水。
[0606]
式i p
‑
tsa盐水合物
[0607]
式i p
‑
tsa盐水合物是通过在50℃和室温,将式i氨丁三醇盐在水中与2当量的对甲苯磺酸一水合物搅拌来获得。式i p
‑
tsa盐水合物也在70℃,≥0.4水活度,从式ip
‑
tsa盐形式i和水合物在mecn/水混合物中的竞争浆液中获得。式i p
‑
tsa盐水合物也由式i形式i在有或没有p
‑
tsa盐水合物晶种的情况下,在mecn/水混合物(9:1或8:2)中,与naoh(1.1当量)和对甲苯磺酸一水合物(2.2当量)来制备或由式i氨丁三醇盐形式i在mecn/水混合物(9:1或8:2)中与naoh(1.1当量)和对甲苯磺酸一水合物(3.2当量)来制备。
[0608]
进行了xrpd分析。图46显示式i p
‑
tsa盐水合物的xrpd谱图。鉴定了xrpd峰并将其
包括在下表18中。
[0609]
表18.
[0610][0611][0612]
进行了dsc分析。图47显示式ip
‑
tsa盐水合物的dsc热谱图。dsc提供在约144℃处开始的宽吸热,然后是在约192℃处开始的宽熔融吸热,在约214℃处开始的放热,以及分解。
[0613]
进行了tga分析。图48显示式i p
‑
tsa盐水合物的tga热谱图。在低于约166℃,固体损失约3.6%的重量,和在约166
‑
236℃,固体损失约2.4%的重量,这对应于由于分解而损失的水。
[0614]
***
[0615]
除非另有定义,否则本文使用的所有技术术语和科学术语都具有与本公开内容所属领域的普通技术人员通常理解的相同的含义。
[0616]
因此,应当理解,尽管本公开内容已经由优选的实施方案和任选的特征具体地公
开,但是可以由本领域的技术人员对本文公开的其中所体现的公开内容进行修改、改进和变化,并且认为此类修改、改进和变化在本公开内容的范围之内。本文提供的材料、方法和实施例是优选的实施方案的代表,且为示例性的,并且不旨在限制本公开的范围。
[0617]
本公开内容已经在本文中进行了广泛地和一般性地描述。落入一般公开内容之内的较窄物类和亚类分组中的每者也构成本公开内容的一部分。这包括具有从种类物移除任何主题的附带条件或负面限制的本公开内容的一般性描述,而不管所删除的材料是否在本文中具体叙述。
[0618]
此外,在根据马库什组描述本公开内容的特征或方面的情况下,本领域技术人员将认识到,本公开内容也由此根据马库什组的任何单独成员或成员亚组进行描述。
[0619]
应当理解,尽管已经结合上述实施方案描述了本公开内容,但是前述描述和实施例旨在说明而不是限制本公开内容的范围。本公开内容范围内的其它方面、优点和修改对于本公开内容所属领域的技术人员将是明显的。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1