用于预防和治疗单纯疱疹病毒感染的单克隆抗体
用于预防和治疗单纯疱疹病毒感染的单克隆抗体
相关申请的交叉引用本技术要求2019年3月19日提交的美国临时申请序列号62/820,495的优先权,该申请的内容通过引用以其全文并入本文。政府支持的声明
1.本发明是根据由美国国立卫生研究院(national institutes of health)授予的基金号ai117321在政府支持下进行的。政府拥有本发明的某些权利。
背景技术:
2.疱疹病毒感染是人类的主要健康问题。目前有一些小分子抗病毒治疗对活动性感染有一定的疗效,但没有针对hsv
‑
1或hsv
‑
2感染的市售疫苗。此外,尚无有效的用于hsv治疗的单克隆抗体。
技术实现要素:
3.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gysfttyd(seq id no:1),iypregst(seq id no:2),和atygssryytmdy(seq id no:3);和/或轻链可变区,该轻链可变区包括esvdnfgisf(seq id no:4),aas(seq id no:5),和qqskevplt(seq id no:6)。
4.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gysitngnh(seq id no:7),irssgss(seq id no:8),和arggglrhyfdy(seq id no:9);和/或轻链可变区,该轻链可变区包括gnihny(seq id no:10),hae(seq id no:11),和qhfwstpyt(seq id no:12)。
5.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gftftdyy(seq id no:13),irnkangytt(seq id no:14),和acgnyvgyamdy(seq id no:15);和/或
轻链可变区,该轻链可变区包括qsllnsrtrkny(seq id no:16),was(seq id no:17),和kqsynlyt(seq id no:18)。
6.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gfslsrhd(seq id no:79),iwgdgst(seq id no:80),和akedygifpy(seq id no:81);和/或轻链可变区,该轻链可变区包括qdissy(seq id no:82),ran(seq id no:83),和lqydefplt(seq id no:84)。
7.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gytftnyd(seq id no:87),iyprdgst(seq id no:88),和argifyvnydvy(seq id no:89);和/或轻链可变区,该轻链可变区包括dhinnw(seq id no:90),gaa(seq id no:91),和qqywssplt(seq id no:92)。
8.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括eyefpshd(seq id no:93),insdggst(seq id no:94),和arhssgyvldy(seq id no:95);和/或轻链可变区,该轻链可变区包括dhinhw(seq id no:96),gat(seq id no:97),和qqywstpyt(seq id no:98)。
9.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括eyefpshd(seq id no:85),insdggst(seq id no:80),和arhssgyvldy(seq id no:81);和/或轻链可变区,该轻链可变区包括dhinhw(seq id no:86),gat(seq id no:83),和
qqywstpyt(seq id no:84)。
10.一种药物组合物,该药物组合物包含如本文所述的抗体或抗原结合片段,以及药学上可接受的载体或赋形剂。
11.一种编码抗体的重链可变区的核酸,其中该重链可变区具有氨基酸序列,该氨基酸序列包括:gysfttyd(seq id no:1),iypregst(seq id no:2),和atygssryytmdy(seq id no:3);或gysitngnh(seq id no:7);irssgss(seq id no:8),和arggglrhyfdy(seq id no:9);或gftftdyy(seq id no:13),irnkangytt(seq id no:14),和acgnyvgyamdy(seq id no:15);或gfslsrhd(seq id no:79),iwgdgst(seq id no:80),和akedygifpy(seq id no:81);或gfslnnyd(seq id no:85),iwgdgst(seq id no:80),和akedygifpy(seq id no:81);或gytftnyd(seq id no:87),iyprdgst(seq id no:88),和argifyvnydvy(seq id no:89);或eyefpshd(seq id no:93),insdggst(seq id no:94),和arhssgyvldy(seq id no:95)。
12.一种编码抗体的轻链可变区的核酸,其中该轻链可变区具有氨基酸序列,该氨基酸序列包括:esvdnfgisf(seq id no:4);aas(seq id no:5);和qqskevplt(seq id no:6),或gnihny(seq id no:10);
hae(seq id no:11);和qhfwstpyt(seq id no:12),或qsllnsrtrkny(seq id no:16);was(seq id no:17);和kqsynlyt(seq id no:18);或qdissy(seq id no:82),ran(seq id no:83),和lqydefplt(seq id no:84);或qdinsy(seq id no:86),ran(seq id no:83),和lqydefplt(seq id no:84);或dhinnw(seq id no:90),gaa(seq id no:91),和qqywssplt(seq id no:92);或dhinhw(seq id no:96),gat(seq id no:97),和qqywstpyt(seq id no:98)。
13.一种核酸,该核酸编码如本文所述的抗体的轻链的轻链互补决定区(lcdr)lcdr1、lcdr2和lcdr3。
14.一种核酸,该核酸编码如本文所述的抗体的重链的重链互补决定区(hcdr)hcdr1、hcdr2和hcdr3。
15.一种宿主细胞,该宿主细胞包含一种或多种本文所述的核酸。
16.一种如本文所述的抗体或抗原结合片段,该抗体或抗原结合片段与治疗剂连接或偶联。
17.一种抑制受试者单纯疱疹病毒
‑
2(hsv
‑
2)活性的方法,该方法包括以有效抑制受试者的hsv
‑
2活性的量施用本文所述的抗体或抗原结合片段。
18.一种激活感染单纯疱疹病毒
‑
2(hsv
‑
2)的细胞的抗体依赖性细胞毒性(adcc)的方法,该方法包括:使细胞与本文所述的分离的抗体或抗原结合片段以影响细胞adcc的量接触。
19.有效量的本文所述的抗体或抗原结合片段,或本文所述的药物组合物,在治疗或预防受试者中与单纯疱疹病毒
‑
2(hsv
‑
2)感染相关的疾病或病症中的用途。
附图说明
20.本领域技术人员将理解,以下描述的附图仅是出于说明目的。附图并不旨在以任
何方式限制本传授内容的范围。
21.本专利或申请文件含有至少一幅彩色附图。应请求并且支付必要的费用后,具有一幅或多幅彩色附图的本专利或专利申请披露的副本将由专利局提供。
22.图1:elisa结果显示培养物上清液与hsv
‑
2g感染的细胞裂解物和未感染的vero细胞裂解物的结合。将来自接种了δgd
‑
2的小鼠的腹股沟淋巴结的生发中心(gc)b细胞直接分选到96孔板中(1个细胞/孔)。然后在nb
‑
21.2d9饲养细胞的存在下培养这些gc b细胞。培养后,首先通过elisa测定igg的存在,然后通过elisa检测培养物上清液igg对hsv
‑
2g感染的细胞裂解物(hsv
‑
2g)和未感染的vero裂解物(对照)的反应性。
23.图2:从d16
‑
d17 gc b细胞获得的vh基因片段的分布。
24.图3a
‑
3b:重组抗体(22d10、32h6、33b8和35h7)对hsv
‑
2g裂解物结合的保留。通过elisa检测重组抗体与hsv
‑
2g裂解物的结合。通过标准rt
‑
pcr,从选定的单个b细胞培养孔(22d10、32h6、33b8和35h7)中扩增重链和轻链v(d)j重排。将这些克隆的v(d)j重排引入表达载体。通过将这些表达载体共转染到expi293f细胞中获得重组抗体。获得了≥4mg的纯化的igg(未显示)。这些抗体未与对照、未感染的vero裂解物结合。
25.图4:单个mab的igg1和igg2c同种型对fcγriv的激活。使用promega fcγriv adcc报告基因生物活性检测试剂盒(promega fcγriv adcc reporter bioassay)以1mg/ml的浓度测定fcγriv活化。统计分析是通过anova,**p<0.01,****p<0.0001。
26.图5a
‑
5b显示了分别从单个骨髓浆细胞和gc b细胞克隆的重组抗体(bmpc
‑
23和19g7)与hsv
‑
2g裂解物的结合。通过elisa检测重组抗体与hsv
‑2‑
g感染的细胞裂解物和未感染的细胞裂解物的结合。
27.图6a
‑
6c:具有克隆的hsv反应性igg2c抗体(bmpc
‑
23、33b8和22d10)的小鼠的被动转移在总生存期(图6a)以及上皮(图6b)和神经检测(图6c)方面提供了针对致死性hsv
‑
2攻击的保护。
28.图7a
‑
7b。进行免疫沉淀质谱(ip
‑
ms)以鉴定22d10、33b8和bmpc
‑
23抗体的结合靶标。结果将人类疱疹病毒糖蛋白b(gb)确定为靶标。
29.图8:显示了重组抗体与hsv
‑
1的糖蛋白b(gb
‑
1)的结合,如通过luminex多重测定所测量的。
30.图9a和9b是中值荧光强度(mfi)对igg浓度(ng/ml)的图,显示了通过luminex多重测定测量的各种重组抗体与gb
‑
1的结合。
31.图10a
‑
10g显示了gb
‑
1特异性小鼠单克隆igg抗体抑制bmpc
‑
23人igg抗体与gb
‑
1结合的能力。
具体实施方式
32.使用抗呼吸道合胞病毒(rsv)f中和单克隆抗体(mab)(帕利珠单抗)进行预防性治疗,已证明可有效预防高危婴幼儿rsv感染的严重并发症,现已获得许可并经常用于此目的。市售的抗hsv
‑
2或抗hsv
‑
1抗体治疗将非常有用,但以前不存在。这种产品将特别适用于免疫功能低下的患者或免疫反应未发育的早产患者。
33.本文披露了抗体、抗原结合片段和编码抗体和抗原结合片段的核酸。该抗体或抗原结合片段与单纯疱疹病毒
‑
2(hsv
‑
2)抗原结合。该抗体或抗原结合片段包含重链可变区,
该重链可变区具有包含三个重链互补决定区(hcdr)的氨基酸序列;并包含轻链可变区,该轻链可变区具有包含三个轻链互补决定区(lcdr)的氨基酸序列,或其组合。该抗体或抗原结合片段包含重链可变区,该重链可变区具有包含重链hcdr1、hcdr2和hcdr3的氨基酸序列;轻链可变区,该轻链可变区具有包含轻链lcdr1、lcdr2和lcdr3的氨基酸序列;或其组合。
34.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gysfttyd(seq id no:1),iypregst(seq id no:2),和atygssryytmdy(seq id no:3);和/或轻链可变区,该轻链可变区包括esvdnfgisf(seq id no:4),aas(seq id no:5),和qqskevplt(seq id no:6)。
35.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gysitngnh(seq id no:7),irssgss(seq id no:8),和arggglrhyfdy(seq id no:9);和/或轻链可变区,该轻链可变区包括gnihny(seq id no:10),hae(seq id no:11),和qhfwstpyt(seq id no:12)。
36.提供了一种抗体或其抗原结合片段,该抗体或其抗原结合片段包括:重链可变区,该重链可变区包括gftftdyy(seq id no:13),irnkangytt(seq id no:14),和acgnyvgyamdy(seq id no:15)和/或轻链可变区,该轻链可变区包括qsllnsrtrkny(seq id no:16),was(seq id no:17),和kqsynlyt(seq id no:18)。
37.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gfslsrhd(seq id no:79),iwgdgst(seq id no:80),和akedygifpy(seq id no:81);和/或轻链可变区,该轻链可变区包括qdissy(seq id no:82),
ran(seq id no:83),和lqydefplt(seq id no:84)
38.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gfslnnyd(seq id no:85),iwgdgst(seq id no:80),和akedygifpy(seq id no:81);和/或轻链可变区,该轻链可变区包括qdinsy(seq id no:86),ran(seq id no:83),和lqydefplt(seq id no:84)。
39.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gytftnyd(seq id no:87),iyprdgst(seq id no:88),和argifyvnydvy(seq id no:89);和/或轻链可变区,该轻链可变区包括dhinnw(seq id no:90),gaa(seq id no:91),和qqywssplt(seq id no:92)。
40.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括eyefpshd(seq id no:93),insdggst(seq id no:94),和arhssgyvldy(seq id no:95);和/或轻链可变区,该轻链可变区包括dhinhw(seq id no:96),gat(seq id no:97),和qqywstpyt(seq id no:98)。
41.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gytftnyw(seq id no:99),ihpnigit(seq id no:100),和argsdsgsawfay(seq id no:101);和/或轻链可变区,该轻链可变区包括dhinnw(seq id no:90),gat(seq id no:97),和qqywstplt(seq id no:102)。
42.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:
重链可变区,该重链可变区包括gytftsyw(seq id no:103),ihpnsgit(seq id no:104),和argsnsgsawfay(seq id no:105);和/或轻链可变区,该轻链可变区包括dhinnw(seq id no:90),gat(seq id no:97),和qqywstplt(seq id no:102)。
43.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gytftsyw(seq id no:103),ihpnsgit(seq id no:104),和argsnsgsawfay(seq id no:105);和/或轻链可变区,该轻链可变区包括dhinnw(seq id no:90),gaa(seq id no:91),和qqywssplt(seq id no:92)。
44.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gytfttyg(seq id no:107),intysgvs(seq id no:108),和aqlnygmdy。(seq id no:109);和/或轻链可变区,该轻链可变区包括qdvsts(seq id no:110),sas(seq id no:111),和hqhysiprt(seq id no:112)。
45.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gytfttyg(seq id no:107),intysgvs(seq id no:108),和aqvnyamdy(seq id no:113);和/或轻链可变区,该轻链可变区包括qdvsta(seq id no:114),sas(seq id no:111),和qqhystprt(seq id no:115)。
46.提供了一种抗体或抗原结合片段,该抗体或抗原结合片段包括:重链可变区,该重链可变区包括gysitsgyd(seq id no:116),isysglt(seq id no:117),和
argppwyfdv(seq id no:118);轻链可变区,该轻链可变区包括qivrat(seq id no:119),las(seq id no:120),和lqywnypyt(seq id no:121)。
47.在一些实施例中,抗体或其抗原结合片段是igg抗体。在一些实施例中,抗体或其抗原结合片段是具有igg2c同种型的igg抗体。
48.在一些实施例中,抗体或其片段是人源化抗体。
49.在一些实施例中,提供了抗体。在一些实施例中,提供了抗原结合片段。在一些实施例中,抗原是单纯疱疹病毒
‑
2(hsv
‑
2)抗原。例如,hsv
‑
2抗原是糖蛋白b(gb)。
50.在一些实施例中,抗体或其片段包含结合fcγ受体riii(fcγriii)的fc区。在一些实施例中,抗体或其片段包含当结合人fcγriii时激活人fcγriii的fc区。在一些实施例中,人fcγriii受体是fcγriiia。
51.在一些实施例中,抗体或其片段结合fcγ受体riv(fcγriv)。
52.在一些实施例中,抗体或其片段结合hsv
‑
2抗原。
53.在一些实施例中,轻链和/或重链的框架区是人框架区,或与其具有85%或更高的同一性。在一些实施例中,轻链和/或重链的框架区是人框架区。
54.在一些实施例中,重链v(d)j重排源自ighv1
‑
85的种系vh、ighd1
‑
1的种系d和ighj4的种系jh。在一些实施例中,重链v(d)j重排与ighv1
‑
85的种系vh、ighd1
‑
1的种系d和ighj4的种系jh具有95%或更高的同一性。在一些实施例中,轻链源自igkv3
‑
2的种系vl和igkj5的种系jl。在一些实施例中,轻链与igkv3
‑
2的种系vl和igkj5的种系jl具有95%或更高的同一性。
55.在一些实施例中,重链v(d)j重排源自ighv3
‑
4的种系vh、ighd2的种系d和ighj4的种系jh。在一些实施例中,重链v(d)j重排与ighv3
‑
4的种系vh、ighd2的种系d和ighj4的种系jh具有95%或更高的同一性。在一些实施例中,轻链源自igkv12
‑
41的种系vl和igkj2的种系jl。在一些实施例中,轻链与igkv12
‑
41的种系vl和igkj2的种系jl具有95%或更高的同一性。
56.在一些实施例中,重链v(d)j重排源自ighv7
‑
3的种系vh、ighd2
‑
1的种系d和ighj4的种系jh。在一些实施例中,重链v(d)j重排与ighv7
‑
3的种系vh、ighd2
‑
1的种系d和ighj4的种系jh具有95%或更高的同一性。在一些实施例中,轻链源自igkv8
‑
21的种系vl和igkj2的种系jl。在一些实施例中,轻链与igkv8
‑
21的种系vl和igkj2的种系jl具有95%或更高的同一性。
57.在一些实施例中,重链v(d)j重排源自ighv2
‑
3的种系vh、ighd2
‑
1的种系d和ighj3的种系jh。在一些实施例中,重链v(d)j重排与ighv2
‑
3的种系vh、ighd2
‑
1的种系d和ighj3的种系jh具有95%或更高的同一性。在一些实施例中,轻链源自igkv14
‑
111的种系vl和igkj5的种系jl。在一些实施例中,轻链与igkv14
‑
111的种系vl和igkj5的种系jl具有95%或更高的同一性。
58.在一些实施例中,重链v(d)j重排源自ighv1
‑
85的种系vh、ighd2
‑
1的种系d和ighj3的种系jh。在一些实施例中,重链v(d)j重排与ighv1
‑
85的种系vh、ighd2
‑
1的种系d和
ighj3的种系jh具有95%或更高的同一性。在一些实施例中,轻链源自igkv13
‑
85的种系vl和igkj5的种系jl。在一些实施例中,轻链与igkv13
‑
85的种系vl和igkj5的种系jl具有95%或更高的同一性。
59.在一些实施例中,重链v(d)j重排源自ighv5
‑
2的种系vh、ighd3
‑
2的种系d和ighj4的种系jh。在一些实施例中,重链v(d)j重排与ighv5
‑
2的种系vh、ighd3
‑
2的种系d和ighj4的种系jh具有95%或更高的同一性。在一些实施例中,轻链源自igkv13
‑
85的种系vl和igkj2的种系jl。在一些实施例中,轻链与igkv13
‑
85的种系vl和igkj2的种系jl具有95%或更高的同一性。
60.在一些实施例中,重链v(d)j重排源自ighv1
‑
64的种系vh、ighd3
‑
2的种系d和ighj3的种系jh。在一些实施例中,重链v(d)j重排与ighv1
‑
64的种系vh、ighd3
‑
2的种系d和ighj3的种系jh具有95%或更高的同一性。在一些实施例中,轻链源自igkv13
‑
85的种系vl和igkj5的种系jl。在一些实施例中,轻链与igkv13
‑
85的种系vl和igkj5的种系jl具有95%或更高的同一性。
61.在一些实施例中,重链v(d)j重排源自ighv9
‑
3的种系vh、ighd2
‑
12的种系d和ighj4的种系jh。在一些实施例中,重链v(d)j重排与ighv9
‑
3的种系vh、ighd2
‑
12的种系d和ighj4的种系jh具有95%或更高的同一性。在一些实施例中,轻链源自igkv6
‑
17的种系vl和igkj1的种系jl。在一些实施例中,轻链与igkv6
‑
17的种系vl和igkj1的种系jl具有95%或更高的同一性。
62.在一些实施例中,重链v(d)j重排源自ighv3
‑
1的种系vh、ighd6
‑
3的种系d和ighj1的种系jh。在一些实施例中,重链v(d)j重排与ighv3
‑
1的种系vh、ighd6
‑
3的种系d和ighj1的种系jh具有95%或更高的同一性。在一些实施例中,轻链源自igkv6
‑
14的种系vl和igkj2的种系jl。在一些实施例中,轻链与igkv6
‑
14的种系vl和igkj2的种系jl具有95%或更高的同一性。
63.还提供了一种药物组合物,该药物组合物包含如本文所述的抗体或抗原结合片段,以及药学上可接受的载体或赋形剂。在一些实施例中,药物组合物进一步包含抗病毒小分子药物。抗病毒小分子包括泛昔洛韦、喷昔洛韦、伐昔洛韦或其组合。在一些实施例中,小分子抗病毒药物是阿昔洛韦。
64.以下是抗hsv抗体的示例性核苷酸序列和氨基酸序列。相应的重链或轻链cdr(例如,hcdr1、hcdr2、hcdr3、lcdr1、lcdr2、lcdr3)以连续顺序加下划线。表4提供了示例性抗hsv抗体的核苷酸序列和氨基酸序列的总结,包括相应的hcdr1、hcdr2、hcdr3、lcdr1、lcdr2和lcdr3。
65.bmpc
‑
23_igh核苷酸:caggttcagctgcagcagtctggacctgagctggtgaagcctggggcttcagtgaagttgtcctgcaaggcttctggctacagtttcacaacctacgatataaactgggtgaaggagaggcctggacagggacttgagtggattgggtggatttatcctagagagggtagtacgaattacaatgagaagttcaggggcaaggccacattgactgcagacacatcctccagtacagcgtacatggagctccacagcctgacatctgaggactctgcggtctatttctgtgcaacctacggtagtagtcgctactatactatggactactggggtcaaggaacctcagtcaccgtctcctcagcc(seq id no:19)
氨基酸:qvqlqqsgpelvkpgasvklsckasgysfttydinwvkerpgqglewigwiypregstnynekfrgkatltadtssstaymelhsltsedsavyfcatygssryytmdywgqgtsvtvssa(seq id no:20)
66.bmpc
‑
23_igl核苷酸gacattgtgctgacccaatctccaacttctttggctgtgtctctagggcagagggccaccatctcctgcagagccagcgaaagtgttgataattttggcattagttttatgaactggttccagcagaaaccaggacagccacccaaactcctcatctacgctgcatccaacctaggatccggggtccctgccaggtttagtggcagtgggtctgggacagacttcagcctcaacatccatcctatggaggatgatgatactgcaatgtatttctgtcagcaaagtaaggaggttccgctcacgttcggtgctgggaccaagctggagctgaaacgg(seq id no:21)氨基酸:divltqsptslavslgqratiscrasesvdnfgisfmnwfqqkpgqppklliyaasnlgsgvparfsgsgsgtdfslnihpmedddtamyfcqqskevpltfgagtklelkr(seq id no:22)
67.22d10_igh核苷酸gatgtacagcttcaggagtcaggacctgccctggtgaagccttctcagacagtgtccctcacctgcactgtcactggctactctatcactaatggtaatcattggtggaactggatccggcaggtttcaggaagcaaactggagtggttagggtacataaggtccagtggtagctctgacagcaatccatctctcaaaagtcgaatctccatcactagagacacttccaagaaccagttattcctgcacttgaactctatgactactgaagatatagccacatattactgtgcaagaggggggggattacggcactactttgactactggggccaaggcaccactctcacagtctcctcagcc(seq id no:23)氨基酸:dvqlqesgpalvkpsqtvsltctvtgysitngnhwwnwirqvsgsklewlgyirssgssdsnpslksrisitrdtsknqlflhlnsmttediatyycarggglrhyfdywgqgttltvssa(seq id no:24)
68.22d10_igl核苷酸gacatccagatgactcagtctccagcctccctatctgcatctgtgggagatactgtcaccatcacatgtcgagcaagtgggaatattcacaattatttagcatggtatcaccagaaacagggaaaatctcctcaactcctggtctatcatgcagaaaccttaacagatggtgtgccatcaaggttcagtggcagtggatcaggaacacaatattctctcaagatcaacagcctgcagcctgaagattttgggagttattactgtcaacatttttggagtactccgtacacattcggaggggggaccaagctggaaataaaacgg(seq id no:25)氨基酸:diqmtqspaslsasvgdtvtitcrasgnihnylawyhqkqgkspqllvyhaetltdgvpsrfsgsgsgtqyslkinslqpedfgsyycqhfwstpytfgggtkleikr(seq id no:26)
69.33b8_igh核苷酸gaggtgaagctggtggagtctggaggaggcttggtacagcctgggggttctctgagtctctcctgtgcaacttctggattcaccttcactgattactacatgaactgggtccgccagcctccagggaaggcacttgagtggttgggttttattagaaacaaagctaatggttacacaacagagtacagtgcatctgtgaagggtcggttcaccatctcca
gagataattcccaaagcatcctctatcttcaaatgaattccctgagagctgaggacagtgccacttattactgtgcttgtggtaactacgtaggctatgctatggactactggggtcaaggaacctcagtcaccgtctcctcagcc(seq id no:27)氨基酸:evklvesggglvqpggslslscatsgftftdyymnwvrqppgkalewlgfirnkangytteysasvkgrftisrdnsqsilylqmnslraedsatyycacgnyvgyamdywgqgtsvtvssa(seq id no:28)
70.33b8_igl核苷酸gacattgtgatgtcacagtctccatcctccctggctgtgtcagcaggagagaaggtcactatgagctgcaaatccagtcagagtctgctcaacagtagaacccgaaagaactacttggcttggtaccagcagaaaccagggcagtctcctaaactgctgatctactgggcatccactagggaatctggggtccctgatcgcttcacaggcagtggatctgggacagatttcactctcaccatcagcagtgtgcaggctgaagacctggcagtttattactgcaagcaatcttataatctgtacacgttcggaggggggaccaagctggaaataaaacgg(seq id no:29)氨基酸:divmsqspsslavsagekvtmsckssqsllnsrtrknylawyqqkpgqspklliywastresgvpdrftgsgsgtdftltissvqaedlavyyckqsynlytfgggtkleikr(seq id no:30)
71.hsv010
‑
4_igh核苷酸caggtgcagctgaaggagtcaggacctggcctggtggcgccctcacagagcctgtccatcacatgcactgtctcagggttctcattaagcagacatgatgtaagctgggttcgccagcctccaggaaagggtctggagtggctgggagtaatatggggtgacgggagcacaaattatcattcagctctcatatccagactgagcatcagcaaagataactccaagagccaagttttcttaaaactgaacagtctgcaaaatgatgacacagccacgtactactgtgccaaagaagactatggtatttttccttactggggccaagggactctggtcactgtctctgcagcc(seq id no:31)氨基酸qvqlkesgpglvapsqslsitctvsgfslsrhdvswvrqppgkglewlgviwgdgstnyhsalisrlsiskdnsksqvflklnslqnddtatyycakedygifpywgqgtlvtvsaa(seq id no:32)
72.hsv010
‑
4_igl核苷酸gacatcaagatgacccagtctccatcttccatgtatgcatctctaggagagaaagtcactatcacttgcaaggcgagtcaggacattagtagctatttaagctggttccagcagaaaccagggaaatctcctaagaccctgatctatcgtgcaaacagattggtagatggggtcccatcaaggttcagtggcagtggatctgggcaagattattctctctccatcagcagcctggactatgaagatatgggaatttattattgtctacagtatgatgagtttccgctcacgttcggtgctgggaccaagctggagctgaaacgg(seq id no:33)氨基酸dikmtqspssmyaslgekvtitckasqdissylswfqqkpgkspktliyranrlvdgvpsrfsgsgsgqdyslsissldyedmgiyyclqydefpltfgagtklelkr(seq id no:34)
73.hsv010
‑
7_igh核苷酸caggttcagctgcagcagtctggacctgagctggtgaagcctggggcttcagtgaagttgtcctgcaaggcttctggctacaccttcacaaactacgatataaactgggtgaagcagaggcctggacagggacttgagtggatt
ggatggatttatcctagagatggtagcactaaatacaatgagaaattcaagggcaaggccacattgactattgacacatcctccagcacagcgtacatggagctccacagcctgacatctgaggactctgcggtctatttctgtgcaagagggatcttctatgttaactacgacgtttactggggccaagggactctggtcactgtctctgcagcc(seq id no:35)氨基酸qvqlqqsgpelvkpgasvklsckasgytftnydinwvkqrpgqglewigwiyprdgstkynekfkgkatltidtssstaymelhsltsedsavyfcargifyvnydvywgqgtlvtvsaa(seq id no:36)
74.hsv010
‑
7_igl核苷酸gacatccagatgacacaatcttcatccttcttgtctgtatctctaggaggcagagtcaccattacttgcaaggcaagtgaccacattaataattggttagcctggtatcagcagaaaccaggacatgctcctaggctcttaatatctggtgcagccagtttggaaactggggttccttcaagattcagtggcagtggatctggaaaggattacactctcaccattaccagtcttcagactgaagatgttgctacttattactgtcaacagtattggagtagtccgctcacgttcggtggtgggaccaagctggagctgaaacgg(seq id no:37)氨基酸diqmtqsssflsvslggrvtitckasdhinnwlawyqqkpghaprllisgaasletgvpsrfsgsgsgkdytltitslqtedvatyycqqywsspltfgggtklelkr(seq id no:38)
75.hsv010
‑
34_igh核苷酸gaggtgcagctggtggagtctgggggaggcttagtgcagcctggagagtccctgaaactctcctgtgaatccaatgaatacgaattcccttcccatgacatgtcttgggtccgcaagactccggagaagaggctggagttggtcgcagccattaatagtgatggtggtagcacctactatccagacaccatggagagacgattcatcatctccagagacaataccaagaagaccctgtacctgcaaatgagcagtctgaggtctgaggacacagccttgtattactgtgcaagacatagctcaggctatgttttggactactggggtcaaggaacctcagtcaccgtctcctcagcc(seq id no:39)氨基酸evqlvesggglvqpgeslklscesneyefpshdmswvrktpekrlelvaainsdggstyypdtmerrfiisrdntkktlylqmsslrsedtalyycarhssgyvldywgqgtsvtvssa(seq id no:40)
76.hsv010
‑
34_igl核苷酸gacatccagatgacacaatcttcatcctacttgtctgtatctctaggaggcagagtcaccattacttgcaaggcaagtgaccacattaatcattggttagcctggtatcagcagaaaccaggaaatgctcctaggctcttaatatctggtgcaaccagtttggaaactggggttccttcaagattcagtggcagtggatctggaaaggattacactctcagcattgccagtcttcagactgaagatgttgctacttattactgtcaacagtattggagtactccgtacacgttcggaggggggaccaagctggaaataaaacgg(seq id no:41)氨基酸diqmtqsssylsvslggrvtitckasdhinhwlawyqqkpgnaprllisgatsletgvpsrfsgsgsgkdytlsiaslqtedvatyycqqywstpytfgggtkleikr(seq id no:42)
77.hsv010
‑
6_igh核苷酸
caggtccaactgcagcagcctggggctgagctggtaaagcctggggcttcagtgaagttgtcctgcaaggcttctggctacactttcaccaactactggatacactgggtgaagcagaggcctggacaaggccttgagtggattggaatgattcatcctaatattggtattactcactacagtgagaggttcaagagcaaggccacactgactgtagacaaatcctccaccacagcctacatgcaactcagcagcctgacatctgaggactctgcggtctattactgtgcaagagggtcggactcaggctccgcctggtttgcttactggggccaagggactctggtcactgtctctgcagcc(seq id no:43)氨基酸qvqlqqpgaelvkpgasvklsckasgytftnywihwvkqrpgqglewigmihpnigithyserfkskatltvdkssttaymqlssltsedsavyycargsdsgsawfaywgqgtlvtvsaa(seq id no:44)
78.hsv010
‑
6_igl核苷酸gacatccagatgacacaatcttcatcctacttgtctgtttctctaggaggcagagtcaccattacttgcaaggcaagtgaccacattaataattggttagcctggtatctgcagaaaccaggaaatgctcctagactcttaatgtctggtgcaaccagtttggaaactggggttccttcaagattcagtggcagtggatctggaaaggattacactctcagcattaccagtcttcagactgaagatgttgctacttattactgtcaacagtattggagtactccgctcacgttcggtgctgggaccaagctggagctgaaacgg(seq id no:45)氨基酸diqmtqsssylsvslggrvtitckasdhinnwlawylqkpgnaprllmsgatsletgvpsrfsgsgsgkdytlsitslqtedvatyycqqywstpltfgagtklelkr(seq id no:46)
79.hsv010
‑
9_igh核苷酸caggtccaactgcagcagcctggggctgagttggtaaagcctggggcttcagtgaagttgtcctgcaagtcttctggctacactttcaccagctactggatgcactgggtgaagcagaggcctggacaaggccttgagtggattggaatgattcatcctaatagtggtattactcactacaatgagaagttcaagaccaaggccacactgactgtagacaaatcctccagcacagcctacatgcaactcagcagcctgacatctgaggactctgcggtctcttactgtgcaagagggtcgaactcaggctccgcctggtttgcttactggggccaagggactctggtcactgtctctgcagcc(seq id no:47)氨基酸qvqlqqpgaelvkpgasvklsckssgytftsywmhwvkqrpgqglewigmihpnsgithynekfktkatltvdkssstaymqlssltsedsavsycargsnsgsawfaywgqgtlvtvsaa(seq id no:48)
80.hsv010
‑
9_igl核苷酸gacatccagatgacacaatcttcatcctacttgtctgtatctctaggaggcagagtcaccattacttgcaaggcaagtgaccacattaataattggttagcctggtatcagcagaaaccaggaaatgctcctaggctcttaatatctggtgcaaccagtttggaaactggggttccttcaagattcagtggcagtggatctggaaaggattacactctcagcattaccagtcttcagactgaagatgttgctacttattactgtcaacagtattggagtactccgctcacgttcggtgctgggaccaagctggagctgaaacgg(seq id no:49)氨基酸diqmtqsssylsvslggrvtitckasdhinnwlawyqqkpgnaprllisgatsletgvpsrfsgsgsg
kdytlsitslqtedvatyycqqywstpltfgagtklelkr(seq id no:50)
81.hsv010
‑
13_igh核苷酸caggtccaactgcagcagcctggggctgagctggtaaagcctggggcttcagtgaagttgtcctgcaaggcttctggctacactttcaccagctactggatacactgggtgaagcaggggcctggacaaggccttgagtggattggaatgattcatcctaatagtggtattactcactacaatgagaagttcaagaccaaggccacactgactgtagacaaatcctccagcacagcctacatgcaactcagcagcctgacatctgaggactctgcggtctgttactgtgcaagagggtcgagctcaggctccgcctggtttgcttactggggccaagggactctggtcactgtctctgcagcc(seq id no:51)氨基酸qvqlqqpgaelvkpgasvklsckasgytftsywihwvkqgpgqglewigmihpnsgithynekfktkatltvdkssstaymqlssltsedsavcycargsssgsawfaywgqgtlvtvsaa(seq id no:52)
82.hsv010
‑
13_igl核苷酸gacatccagatgacacaatcttcatcctacttgtctgaatctctaggaggcagagtcaccattacttgcaaggcaagtgaccacattaataattggttagcctggtatcagcagaaaccaggaaatgctcccaggctcttaatatctggtgcaaccagtttggaaactggggttccttcaagattcagtggcagtggatctggaaaggattacactctcagcattaccagtcttcagactgaagatgttgctacttattactgtcaacagtattggagtagtccgctcacgttcggtgctgggaccaagctggagctgaaacgg(seq id no:53)氨基酸diqmtqsssylseslggrvtitckasdhinnwlawyqqkpgnaprllisgatsletgvpsrfsgsgsgkdytlsitslqtedvatyycqqywsspltfgagtklelkr(seq id no:54)
83.hsv010
‑
14_igh核苷酸caggtccaactgcagcagcctggggctgagctggtaaagcctggggcttcagtgaagttgtcctgcaaggcttctggctacactttcaccagctactggatacactgggtgaagcagaggcctggccaaggccttgagtggattggaatgattcatcctaatagtggtattgctcactacagtgagaagttcaagagcacggccacactgactgtagacaaatcctccagcacagcctacatgcaactcagcagcctgacatctgaggactcttcggtctattactgtgcaagagggtcgagctcaggctccgcctggtttgcttattggggccaagggactctggtcactgtctctgcagcc(seq id no:55)氨基酸qvqlqqpgaelvkpgasvklsckasgytftsywihwvkqrpgqglewigmihpnsgiahysekfkstatltvdkssstaymqlssltsedssvyycargsssgsawfaywgqgtlvtvsaa(seq id no:56)
84.hsv010
‑
14_igl核苷酸gacatccagatgacacaatcttcatcctacttgtctgtttctctaggaggcagagtcaccattacttgcaaggcaggtgaccacattaataattggttagcctggtatcagcagaaaccaggaaatgctcctaggctcttaatatctggtgcaaccagtttggaaactggggttccttcaagattcagtggcagtggatctggaaaggattacactctcagcattaccagtcttcagactgaagatgttgctacttattactgtcaacagtattggagtactccgctcacgttcgg
tgctgggaccaagctggagctgaaacgg(seq id no:57)氨基酸diqmtqsssylsvslggrvtitckagdhinnwlawyqqkpgnaprllisgatsletgvpsrfsgsgsgkdytlsitslqtedvatyycqqywstpltfgagtklelkr(seq id no:58)
85.hsv010
‑
28_igh核苷酸cagatccagttggtacagtctggacctgagctgaagaagcctggagagacagtcaagatctcctgcaaggcttctgggtataccttcacaacctatggaatgagctgggtgaaacaggctccaggaaagggtttaaagtggatgggctggataaacacctactctggagtgtcaacatatgctgatgacttcaagggacggtttgccttctctttggaaacctctgccagcactgcctatttgcagatcaacaacctcaaaaatgaggacacggctacatatttctgtgctcaggtaaactatgctatggactactggggtcaaggaacctcagtcaccgtctcctcagcc(seq id no:59)氨基酸qiqlvqsgpelkkpgetvkisckasgytfttygmswvkqapgkglkwmgwintysgvstyaddfkgrfafsletsastaylqinnlknedtatyfcaqvnyamdywgqgtsvtvssa(seq id no:60)
86.hsv010
‑
28_igl核苷酸gacattgtgatgacccagtctcacaaattcttgtccacatcagtaggagactgggtcaccatcacctgcaaggccagtcaggatgtgagtactgctgtagcctggtttcagcagaaaccaggacaatctcctaaagtactgatttactcggcatcctaccggtacactggagtccctgatcgcttcactggcagtggatctgggacggatttcactttcaccatcagcagtgtgcaggctgaagacctggcagtttattactgtcagcaacattatagtactcctcggacgttcggtggaggcaccaagctggaaatcaaacgg(seq id no:61)氨基酸divmtqshkflstsvgdwvtitckasqdvstavawfqqkpgqspkvliysasyrytgvpdrftgsgsgtdftftissvqaedlavyycqqhystprtfgggtkleikr(seq id no:62)
87.hsv010
‑
20_igh核苷酸gatgtgcagcttcaggagtcaggacctggcatggtgagaccttctcagtcactttccctcacctgcactgtcactggctactccatcaccagtggttatgactggcactggatccgacattttccaggaaacaaactggagtggatgggctacataagctacagtggtctcactaactacaacccatccctcagaagtcgattctccatcactcatgacacatctaagaaccatttcttcctgaagttgaattctgtgactactgaggacacagccacatattactgtgcaagaggtcctccctggtacttcgatgtctggggcacagggaccacggtcaccgtctcctcagcc(seq id no:63)氨基酸dvqlqesgpgmvrpsqslsltctvtgysitsgydwhwirhfpgnklewmgyisysgltnynpslrsrfsithdtsknhfflklnsvttedtatyycargppwyfdvwgtgttvtvssa(seq id no:64)
88.hsv010
‑
20_igl核苷酸gacattgtgatgacccagtctcaaaaattcatgtccacatcagtaggaggcagggtcagcatcacctgcaaggccagtcagattgttcgtgctactgtagcctggtatcaacagaaaccagggcagtctcctaaaccactaatttacttggcatccaaccggcacactggagtccctgatcgcttcacaggcagtggatctgggacagatttcactctcaccattagcaatgtgcaatctgaagacctggcagattatttctgtctgcaatattggaattatccgtacacgttcgg
aggggggaccaagctggaaataaaacgg(seq id no:65)氨基酸divmtqsqkfmstsvggrvsitckasqivratvawyqqkpgqspkpliylasnrhtgvpdrftgsgsgtdftltisnvqsedladyfclqywnypytfgggtkleikr(seq id no:66)
89.hsv010
‑
8_igh核苷酸caggtgcagctgaaggagtcaggacctggcctggtggcgccctcacagagcctgtcgatcacatgcactgtctcagggttctcattaaacaactatgatgtaagctgggttcgccagcctccaggaaagggtctggagtggctgggagtaatatggggtgacgggagcacaaattatcattcagctctcatatccagactgagcatcagcaaggataactccaagagccaagttttcttaaaactgaacagtctgcaaactgatgacacagccacgtactactgtgccaaagaagactatggtatttttccttactggggccaagggactctggtcactgtctctgcagcc(seq id no:67)氨基酸qvqlkesgpglvapsqslsitctvsgfslnnydvswvrqppgkglewlgviwgdgstnyhsalisrlsiskdnsksqvflklnslqtddtatyycakedygifpywgqgtlvtvsaa(seq id no:68)
90.hsv010
‑
8_igl核苷酸gacatcaagatgacccagtctccatcttccatgtatgcatctctaggagagagagtcactatcacttgcaaggcgagtcaggacattaatagctatttaagctggttccagcagaaaccagggaaatctcctaagaccctgatctatcgtgcaaacagattggtagatggggtcccatcaaggttcagtggcagtggatctgggcaagattattctctcaccatcagcagcctggaatatgaaaatatgggaatttattattgtctacagtatgatgagtttccgctcacgttcggtgctgggaccaagctggagctgaaacgg(seq id no:69)氨基酸dikmtqspssmyaslgervtitckasqdinsylswfqqkpgkspktliyranrlvdgvpsrfsgsgsgqdysltissleyenmgiyyclqydefpltfgagtklelkr(seq id no:70)
91.hsv010
‑
15_igh核苷酸caggtccaactgcagcagcctggggctgagctggtaaagcctggggcttcagtgaagttgtcctgcaaggcttctggctacactttcaccagctactggatacactgggtgcagcagaggcctggacaaggccttgagtggattggaatgattcatcctaatagtggtattactaactacagtgagaagttcaagagcaaggccacactgactttagacaagtcctccagcacagcctacatgcaactcatcagcctgacatctgaggactctgcggtctattactgtgcaagagggtcgagttcaggctccgcctggtttgcttactggggccaagggactctggtcactgtctctgcagcc(seq id no:71)氨基酸qvqlqqpgaelvkpgasvklsckasgytftsywihwvqqrpgqglewigmihpnsgitnysekfkskatltldkssstaymqlisltsedsavyycargsssgsawfaywgqgtlvtvsaa (seq id no:72)
92.hsv010
‑
15_igl核苷酸gacatccagatgacacaatcttcatcctacttgtctgtttctctaggaggcagagtcaccattacttgcaaggcaagtgaccacattaataattggttaccttggtatcagcagaaaccaggaaatgctcctaggctcttaatt
tctggtgcaaccagtttggaaactggggttccttcaagattcagtggcagtggatctggaaaggattacactctcagcattaccagtcttcagactgaagatgttgctacttattactgtcaacagtattggagttctccgctcacgttcggtgctgggaccaagctggagctgaaacgg(seq id no:3)氨基酸diqmtqsssylsvslggrvtitckasdhinnwlpwyqqkpgnaprllisgatsletgvpsrfsgsgsgkdytlsitslqtedvatyycqqywsspltfgagtklelkr(seq id no:74)
93.hsv010
‑
16_igh核苷酸cagatccagttggtacagtctggacctgagctgaagaagcctggagagacagtcaagatctcctgcaaggcttctgggtataccttcacaacctatggaatgagctgggtgaaacaggctccaggaaaggatttaaagtggatgggctggataaacacctactctggagtgtcaacatatggtgatgacttcaagggacggtttgccttgtctttggaaacctctgccagcactgcctatttacaaatcaacaacctcaaaaatgaggacacggctacatatttctgtgctcagttaaactatggtatggactactggggtcaaggaacctcagtcaccgtctcctcagcc(seq id no:75)氨基酸qiqlvqsgpelkkpgetvkisckasgytfttygmswvkqapgkdlkwmgwintysgvstygddfkgrfalsletsastaylqinnlknedtatyfcaqlnygmdywgqgtsvtvssa(seq id no:76)
94.hsv010
‑
16_igl核苷酸gacattgtgatgacccagtctcacaaattcatgtccacatcagtaggagacagggtcagcatcacctgcaaggccagtcaggatgtgagtacttctttagcctggtatcaacagaaaccaggacaatctcctaaactactgatttattcggcatcctaccggtacactggagtccctgatcgcttcactggcagtggatctgggacggatttcactttcaccatcagcagtgtgcaggctgaagacctggcagtttattactgtcaccaacattatagtattcctcggacgttcggtggaggcaccaagctggaaatcaaacgg(seq id no:77)氨基酸divmtqshkfmstsvgdrvsitckasqdvstslawyqqkpgqspklliysasyrytgvpdrftgsgsgtdftftissvqaedlavyychqhysiprtfgggtkleikr(seq id no:78)
95.在一些实施例中,提供了一种抗体,该抗体具有上文所列重链氨基酸序列之一的重链hcdr1、hcdr2和hcdr3以及上文所列轻链氨基酸序列中的任一个的轻链lcdr1、lcdr2和lcdr3。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与bmpc
‑
23的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与33b8的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与22d10的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与hsv010
‑
4的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与hsv010
‑
8的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与hsv010
‑
7的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与hsv010
‑
34的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与hsv010
‑
6的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻
链lcdr1、lcdr2和lcdr3与hsc010
‑
9的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与hsv010
‑
13的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与hsv010
‑
14的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与hsv010
‑
15的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与hsv010
‑
16的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与hsv010
‑
28的重链hcdr和轻链lcdr相同。在一些实施例中,重链hcdr1、hcdr2和hcdr3以及轻链lcdr1、lcdr2和lcdr3与hsv010
‑
20的重链hcdr和轻链lcdr相同。
96.提供了一种编码抗体或其抗原结合片段的核酸。还提供了一种编码抗体或抗原结合片段的分离的核酸分子。
97.在一些实施例中,提供了一种编码抗体的轻链的核酸。具体地,核酸编码抗体的轻链可变区。轻链是λ链或κ链。在一些实施例中,核酸还编码人框架区。核酸可以是分离的核酸分子。
98.在一些实施例中,该核酸编码抗体的轻链可变区,该轻链具有核酸序列,该核酸序列包括:seq id no:21、seq id no:25、seq id no:29、seq id no:33、seq id no:69、seq id no:37、seq id no:41、seq id no:45、seq id no:49、seq id no:53、seq id no:57、seq id no:73、seq id no:77、seq id no:61或seq id no:66。在一些实施例中,该核酸编码抗体的轻链可变区,其中该轻链具有核酸序列,该核酸序列与seq id no:21、seq id no:25、seq id no:29、seq id no:33、seq id no:69、seq id no:37、seq id no:41、seq id no:45、seq id no:49、seq id no:53、seq id no:57、seq id no:73、seq id no:77、seq id no:61或seq id no:66具有95%或更高的同一性。
99.在一些实施例中,核酸编码抗体的轻链可变区,该轻链可变区具有氨基酸序列,该氨基酸序列包括(按各自顺序列出的lcdr1、lcdr2和lcdr3):esvdnfgisf(seq id no:4);aas(seq id no:5);和qqskevplt(seq id no:6),或gnihny(seq id no:10);hae(seq id no:11);和qhfwstpyt(seq id no:12),或qsllnsrtrkny(seq id no:16);was(seq id no:17);和kqsynlyt(seq id no:18)或qdissy(seq id no:82);ran(seq id no:83);和lqydefplt(seq id no:84)
或qdinsy(seq id no:86);ran(seq id no:83);和lqydefplt(seq id no:84)或dhinnw(seq id no:90);gaa(seq id no:91);和qqywssplt(seq id no:92)或dhinhw(seq id no:96)gat(seq id no:97)qqywstpyt(seq id no:98)或dhinnw(seq id no:90);gat(seq id no:97);和qqywstplt(seq id no:102)或dhinnw(seq id no:90);gat(seq id no:97);和qqywssplt(seq id no:92)或qdvsts(seq id no:110);sas(seq id no:111);和hqhysiprt(seq id no:112)或qdvsta(seq id no:114);sas(seq id no:111);和qqhystprt(seq id no:115)或qivrat(seq id no:119);las(seq id no:120);和lqywnypyt(seq id no:122)。
100.在一些实施例中,核酸还编码人框架区。在一些实施例中,轻链是λ链或κ链。
101.提供了一种编码抗体的重链的核酸。具体地,核酸编码抗体的轻链可变区。在一些实施例中,核酸还编码人框架区。核酸可以是分离的核酸分子。
102.在一些实施例中,核酸编码抗体的重链可变区,其中该重链具有核酸序列,该核酸序列包括:seq id no:19、seq id no:23、seq id no:27、seq id no:31、seq id no:67、seq id no:35、seq id no:39、seq id no:43、seq id no:47、seq id no:51、seq id no:55、seq id no:71、seq id no:75、seq id no:59或seq id no:63。在一些实施例中,核酸编码抗体
的重链可变区,其中该重链具有核酸序列,该核酸序列与seq id no:19、seq id no:23、seq id no:27、seq id no:31、seq id no:67、seq id no:35、seq id no:39、seq id no:43、seq id no:47、seq id no:51、seq id no:55、seq id no:71、seq id no:75、seq id no:59或seq id no:63具有95%或更高的同一性。
103.在一些实施例中,核酸编码抗体的重链可变区,该重链可变区具有氨基酸序列,该氨基酸序列包括(按各自顺序列出的hcdr1、hcdr2和hcdr3):gysfttyd(seq id no:1);iypregst(seq id no:2);和atygssryytmdy(seq id no:3)或gysitngnh(seq id no:7),irssgss(seq id no:8);和arggglrhyfdy(seq id no:9),或gftftdyy(seq id no:13);irnkangytt(seq id no:14);和acgnyvgyamdy(seq id no:15)或gfslsrhd(seq id no:79);iwgdgst(seq id no:80);和akedygifpy(seq id no:81)或gfslnnyd(seq id no:85);iwgdgst(seq id no:80);和akedygifpy(seq id no:81)或gytftnyd(seq id no:87);iyprdgst(seq id no:88);和argifyvnydvy(seq id no:89)或eyefpshd(seq id no:93);insdggst(seq id no:94);和arhssgyvldy(seq id no:95)或gytftnyw(seq id no:99);ihpnigit(seq id no:100);和argsdsgsawfay(seq id no:101)或gytftsyw(seq id no:103);
ihpnsgit(seq id no:104);和argsnsgsawfay(seq id no:105)或gytfttyg(seq id no:107);intysgvs(seq id no:108);和aqlnygmdy(seq id no:109)或gytfttyg(seq id no:107);intysgvs(seq id no:108);和aqvnyamdy(seq id no:113)或gysitsgyd(seq id no:116);isysglt(seq id no:117);和argppwyfdv(seq id no:118)。
104.在一些实施例中,核酸编码具有seq id no:19的核酸序列的抗体的重链可变区和具有seq id no:21的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:23的核酸序列的抗体的重链可变区和具有seq id no:25的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:27的核酸序列的抗体的重链可变区和具有seq id no:29的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:31的核酸序列的抗体的重链可变区和具有seq id no:33的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:67的核酸序列的抗体的重链可变区和具有seq id no:69的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:35的核酸序列的抗体的重链可变区和具有seq id no:37的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:39的核酸序列的抗体的重链可变区和具有seq id no:41的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:43的核酸序列的抗体的重链可变区和具有seq id no:45的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:47的核酸序列的抗体的重链可变区和具有seq id no:49的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:51的核酸序列的抗体的重链可变区和具有seq id no:53的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:55的核酸序列的抗体的重链可变区和具有seq id no:57的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:71的核酸序列的抗体的重链可变区和具有seq id no:73的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:75的核酸序列的抗体的重链可变区和具有seq id no:77的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:59的核酸序列的抗体的重链可变区和具有seq id no:61的核酸序列的抗体的轻链可变区。在一些实施例中,核酸编码具有seq id no:63的核酸序列的抗体的重链可变区和具有seq id no:65的核酸序列的抗体的轻链可变区。
105.在一些实施例中,核酸还编码人fc区。在一些实施例中,核酸还编码与fcγriii结合的人fc区。在一些实施例中,抗体或抗原结合片段包含在结合人fcγriii时激活人fcγ
riii的fc区。在一些实施例中,人fcγriii受体是fcγriiia。在一些实施例中,重链是γ链。
106.在一些实施例中,本披露的核酸编码长度小于500个氨基酸、长度小于250个氨基酸或长度小于120个氨基酸的多肽。在一些实施例中,本披露的核酸编码长度为70至100个氨基酸的多肽。
107.在核酸的实施例中,核酸是dna。在一些实施例中,核酸是cdna。在一些实施例中,核酸是rna。
108.本文披露的核酸适用于本文披露的抗体或抗原结合片段的重组生产。因此,本发明还涉及含有编码抗体或抗原结合片段的核酸序列的载体和宿主细胞。
109.提供了编码本文所述的核酸分子的载体。还提供了包含一种或多种本文所述的核酸或本文所述的载体的宿主细胞。
110.抗体或抗原结合片段可以与异源分子连接或偶联。异源分子可以是治疗剂,例如细胞毒性药物、放射性同位素、免疫调节剂、第二抗体、抗病毒小分子或其组合。在一些实施例中,抗体或抗原结合片段可以与治疗剂连接或偶联。
111.一种抑制受试者的hsv
‑
2活性的方法,包括以有效抑制受试者的hsv
‑
2活性的量施用抗体或抗原结合片段。抗体或抗原结合片段可以通过从受试者中清除病毒、防止hsv
‑
2在受试者中的传播、防止在受试者中建立潜伏期和/或预防受试者感染hsv
‑
2来抑制受试者中的hsv
‑
2活性。
112.在一些实施例中,受试者感染了hsv
‑
2。在一些实施例中,受试者尚未感染hsv
‑
2。在一些实施例中,受试者免疫功能低下。在一些实施例中,免疫功能低下的患者患有癌症、接受过移植或正在服用免疫抑制药物。在一些实施例中,受试者正处于妊娠期。在一些实施例中,受试者是新生儿。
113.在一些实施例中,受试者正在接受或已经接受抗病毒疗法。抗病毒疗法包括向受试者施用抗病毒小分子。抗病毒小分子包括泛昔洛韦、喷昔洛韦、伐昔洛韦或其组合。在一些实施例中,抗病毒疗法包括向受试者施用阿昔洛韦。
114.一种激活被hsv
‑
2感染的细胞的抗体依赖性细胞毒性(adcc)的方法,包括将细胞与分离的抗体或抗原结合片段以影响细胞adcc的量接触。
115.在一些实施例中,该细胞位于感染了hsv
‑
2的受试者体内。
116.提供了本文所述的抗体或抗原结合片段,或包含该抗体或抗原结合片段的药物组合物,用于治疗或预防受试者中与单纯疱疹病毒
‑
2(hsv
‑
2)感染相关的疾病或病症。
117.有效量的本文所述的抗体或抗原结合片段在生产用于治疗或预防受试者中与hsv
‑
2感染相关的疾病或病症的药物中的用途。
118.本文所述的一种或多种抗体可以是分离的一种或多种抗体。类似地,本文所述的一种或多种抗原结合片段可以是分离的一种或多种抗原结合片段。
119.在一些实施例中,抗体或其抗原结合片段是嵌合的或人源化的。在一些实施例中,抗体或其抗原结合片段具有人序列fc区。
120.在一些实施例中,抗体或抗原结合片段包括单克隆抗体、scfv、fab片段、fab'片段、f(ab')2片段或其组合。
121.在一些实施例中,分离的抗体、分离的抗原结合片段、抗体或抗原结合片段包含单
克隆抗体、scfv、fab片段、fab'片段、f(ab')2片段,或其组合。应注意,尽管scfv并非严格意义上的抗体片段,而是融合蛋白,但如本文所用,除非另有说明,否则抗体的抗原结合片段包括scfv。
122.在一些实施例中,这些方法用于治疗和预防受试者的神经性hsv
‑
2感染症状。
123.在一些实施例中,该方法用于治疗和预防上皮hsv
‑
2感染症状。
124.在一些实施例中,抗体或其抗原结合片段包含如表2或表4中命名的人种系的框架序列的vh框架和/或(ii)包含如表2或表4中命名的人种系的框架序列的vl框架。在一些实施例中,抗体或其抗原结合片段包含与表2或表4中命名的人种系的框架序列具有95%或更高同一性的vh框架和/或(ii)包含与表2或表4中命名的人种系的框架序列的具有95%或更高同一性的vl框架。
125.在一些实施例中,抗体或其片段以约1x 10
‑9摩尔(m)至约1x 10
‑
12
m的结合亲和力(k
d
)结合hsv
‑
2表面抗原。
126.提供了一种产生如本文所述的抗体或其抗原结合片段的方法,该方法包括在其中由宿主细胞产生抗体或其抗原结合片段的条件下培养宿主细胞。术语“宿主细胞”是指已引入编码抗体或抗原结合片段的外源核酸的细胞,包括此类细胞的子代。宿主细胞包括“转化体”、“转化细胞”、“转染体”、“转染细胞”和“转导细胞”,包括原代转化/转染/转导细胞和由其衍生的子代,不考虑传代次数。子代在核酸含量上可能与亲代细胞不完全相同,但可能包含突变。还包括与在最初转化的细胞中筛选或选择的具有相同功能或生物活性的突变子代。
127.宿主细胞可以是哺乳动物宿主细胞。用于表达本文提供的抗体或其抗原结合片段的哺乳动物宿主细胞的实例包括中国仓鼠卵巢(cho细胞),例如cho
‑
k1、cho
‑
s、cho
‑
k1sv、nso骨髓瘤细胞、cos细胞、hek293细胞、hkb11细胞、bhk21细胞、cap细胞、eb66细胞、sp2细胞和expi293f细胞。在一些实施例中,宿主细胞是中国仓鼠卵巢(cho)细胞。在一些实施例中,宿主细胞是expi293f细胞。
128.如本文所用,术语“抗体”是指完整的(全部的)抗体,即具有完全的fc和fv区。完整抗体是包含由二硫键相互连接的至少两条重(h)链及两条轻(l)链的糖蛋白。每条重链由一个重链可变区(v
h
)和一个重链恒定区构成。重链恒定区由三个结构域(ch1、ch2和ch3)构成。每条轻链由一个轻链可变区(v
l
)和一个轻链恒定区构成。轻链恒定区由一个结构域(cl)构成。v
h
及v
l
区进一步细分成高变区(称为互补决定区(cdr))及更保守区(称为框架区(fr)),二者散布排列。每个v
h
及v
l
由三个cdr及四个fr构成,其自氨基
‑
末端至羧基
‑
末端按下列顺序排列:fr1,cdr1,fr2,cdr2,fr3,cdr3,fr4。重链和轻链的可变区含有与抗原相互作用的结合结构域或结合部分。
129.如本文所用,术语“抗原结合片段”或“抗原结合部分”是指抗体的任何部分,或连接在一起的抗体部分,其小于完整抗体,但保留了与抗原特异性结合的能力。抗原结合片段与完整抗体的片段竞争特异性结合。在这种情况下,抗原是hsv
‑
2抗原。抗原也可以是hsv
‑
1抗原。“抗体”或其“片段”可包含任何类别的免疫球蛋白,例如igg、igm、iga、igd和ige。示例性类别是igg,示例性同种型是igg2c。
130.抗体的术语“抗原结合片段”或“抗原结合部分”所涵盖的实例包括fab片段(由v
l v
h
、c
l
和c
h1
结构域组成的单价片段)、f(ab')2片段(一个二价片段,其包含两个通过铰链区二
硫键连接的fab片段)、fab'片段(通过还原f(ab')2片段产生的单价片段,具有游离巯基)、由抗体单臂的v
l
和v
h
结构域组成的片段、fv片段(由抗体单臂的v
l
和v
h
结构域组成的片段)、单链片段(scfv,轻链可变结构域(vl)和重链可变结构域(vh)通过肽接头连接)、dab片段(由v
h
结构域组成);分离的互补决定区(cdr)、纳米抗体(包含单个可变结构域和两个恒定结构域的重链可变区)、其突变体、天然存在的变体、包含具有所需特异性抗原识别位点的抗体部分的融合蛋白、人源化抗体、嵌合抗体和包含所需特异性的抗原识别位点的免疫球蛋白分子的任何其他修饰构型。
131.例如,可以通过切割完整抗体或通过重组方式来制备抗原结合片段。一般参见,fundamental immunology,ch.7(paul,w.,ed.,2nd ed.raven press,n.y.(1989))[基本免疫学,第七章(paul,w.,编辑,第二版,渡鸦出版社,纽约(1989))],通过引用以其全文并入本文。抗原结合片段可以通过重组dna技术或通过完整抗体的酶促或化学裂解或通过分子生物学技术产生。在一些实施例中,片段是fab、fab'、f(ab')2、fd、fv、互补决定区(cdr)片段或单链抗体(scfv)。在scfv片段的情况下,v
l
和v
h
由单独的基因编码,并且通过重组方式通过合成接头连接在一起,这使得它们能够制备为单条蛋白质链,其中vl和vh区配对形成单价分子。在一些实施例中,scfv包含具有与人可变结构域fr1、fr2、fr3或fr4相同的序列的可变结构域框架序列。在一些实施例中,scfv包含合成接头,该接头是长度为5至30个氨基酸残基的肽。例如,scfv包含接头肽,该接头肽含有一个或多个甘氨酸、丝氨酸和苏氨酸残基。在一些实施例中,scfv的接头长度为10
‑
25个氨基酸。在一些实施例中,肽接头包含甘氨酸、丝氨酸和/或苏氨酸残基。(例如,参见bird et al.,science,242:423
‑
426(1988)and huston et al.,proc.natl.acad.sci.usa,85:5879
‑
5883(1988)[bird等人,科学,242:423
‑
426(1988)和huston等人,美国科学院院刊,85:5879
‑
5883(1988)],每篇文献都通过引用以其全文并入本文)。
[0132]
抗原结合片段可以是包含抗体的至少一部分的多肽,该抗体足以将hsv
‑
2抗原特异性结合到该多肽上,该多肽包括双功能抗体。从n端到c端,成熟的轻链和重链可变结构域均包含区域结构域fr1、cdr1、fr2、cdr2、fr3、cdr3和fr4。每个结构域的氨基酸分配符合kabat,sequences of proteins of immunological interest(national institutes of health,bethesda,md.(1987and 1991))[kabat,具有免疫学意义的蛋白质序列(美国国立卫生研究院,贝塞斯达,马里兰州(1987年和1991年))],chothia&lesk,j.mol.biol.196:901
‑
917(1987)[chothia&lesk,分子生物学杂志,196:901
‑
917(1987)],或chothia et al.(nature 342:878
‑
883(1989))[chothia等人(自然,342:878
‑
883(1989))],每篇文献均通过引用以其全文并入本文。如本文所用,术语“多肽”包括天然或人工蛋白质、蛋白质片段和/或蛋白质序列的多肽类似物。多肽可以是单体的或聚合的。如本文所用,fd片段是指由vh和ch1结构域组成的抗体片段;由抗体单臂的vl和vh结构域组成的fv片段;和由vh结构域组成的dab片段(ward et al.,nature 341:544
‑
546(1989)[ward等人,自然341:544
‑
546(1989)]通过引用以其全文并入本文)。在一些实施例中,片段的长度为至少5、6、8或10个氨基酸。在其他实施例中,抗原结合片段的长度为至少14、至少20、至少50或至少70、80、90、100、150或200个氨基酸。
[0133]
如在此使用的术语“单克隆抗体”(monoclonal antibody或mab)是指获得自基本上均一的抗体群体的抗体成员,即包括该群体的单独抗体是相同的,除了可能的突变,例如
天然存在的突变,可能以较小的量存在。因此,修饰语“单克隆”指示抗体的特征,而并不是离散抗体的混合物。与典型地包括针对不同抗原决定簇(表位)的不同抗体的多克隆抗体制品相比,单克隆抗体制品的每个单克隆抗体是针对抗原上单个决定簇。除了它们的特异性之外,单克隆抗体制品还在它们典型地不被其他免疫球蛋白污染方面是有优势的。因此,一旦鉴定出单克隆抗体的序列,就可以通过非杂交瘤技术,例如通过适当的重组方式产生确定的单克隆抗体。
[0134]
在本文描述的本发明的实施例中,抗体是分离的。如本文所用,术语“分离的抗体”是指由于其起源或衍生来源而具有以下至少一种(例如,一种、两种、三种或四种)的抗体:(1)与在其天然状态下伴随它的天然相关成分不相关,(2)不含来自同一物种的其他蛋白质,(3)由来自不同物种的细胞表达,或(4)没有人为操作在自然界中不会发生。
[0135]
在一些实施例中,抗体是人源化的。如本文所用,“人源化抗体”是指包含来自人类和非人类(例如,鼠类、大鼠)抗体的序列的抗体形式。人源化形式的非人类的(例如,鼠类)抗体是嵌合抗体,包含从非人类免疫球蛋白衍生的最小序列。在一个实施例中,人源化抗体是具有人免疫球蛋白序列(受体抗体)但具有来自鼠高变区(hvr)(或cdr)的残基的抗体。在一些实施例中,鼠类mab的框架(fr)残基被相应的人免疫球蛋白可变结构域框架(fr)残基替换。这些人源化抗体可以进一步修饰以改善抗体性能。人源化抗体可以包括未在受体抗体或供体抗体中发现的残基。或者,人源化抗体不包括在受体抗体或供体抗体中未发现的残基。通常,人源化抗体将包括基本上至少一个、并且典型地两个可变结构域的全部,其高变环的全部或基本上全部对应于非人类免疫球蛋白的那些,并且fr的全部或基本上全部是人类免疫球蛋白序列的那些。人源化抗体可任选地还将包括(典型地人类免疫球蛋白的)免疫球蛋白恒定区(fc)的至少一部分。参见,例如,jones et al.,nature 321:522
‑
525(1986)[jones等人,自然321:522
‑
525(1986)];riechmann et al.,nature 332:323
‑
329(1988)[riechmann等人,自然332:323
‑
329(1988)];presta,curr.op.struct.biol.2:593
‑
596(1992)[presta,当前结构生物学观点2:593
‑
596(1992)];vaswani and hamilton,ann.allergy,asthma&immunol.1:105
‑
115(1998)[vaswani和hamilton,过敏性哮喘和免疫学年鉴1:105
‑
115(1998)];harris,biochem.soc.transactions23:1035
‑
1038(1995)[harris,生化学会会刊23:1035
‑
1038(1995)];hurle and gross,curr.op.biotech.5:428
‑
433(1994)[hurle和gross,当前生物技术观点5:428
‑
433(1994)];和美国专利第6,982,321和7,087,409号,它们各自的内容通过引用以其全文并入本文。在一个实施例中,人源化抗体包含在受体抗体或供体抗体中未发现的残基,并且人源化抗体的fc区如wo 99/58572中所述进行修饰,其内容通过引用以其全文并入本文。
[0136]
将单克隆抗体人源化的技术是众所周知的,并且描述于例如美国专利号4,816,567、5,807,715、5,866,692、6,331,415、5,530,101、5,693,761、5,693,762、5,585,089和6,180,370中,每个专利的内容通过引用以其全文并入本文。已经描述了许多包含源自非人类免疫球蛋白的抗原结合位点的“人源化”抗体分子,包括具有与人恒定结构域融合的啮齿动物或修饰的啮齿动物v区及其相关互补决定区(cdr)的抗体。例如,参见winter et al.nature 349:293
‑
299(1991)[winter等人,自然349:293
‑
299(1991)],lobuglio et al.proc.nat.acad.sci.usa 86:4220
‑
4224(1989)[lobuglio等人,美国科学院院刊86:4220
‑
4224(1989)],shaw et al.j.immunol.138:4534
‑
4538(1987)[shaw等人,免疫学杂志
138:4534
‑
4538(1987)]和brown et al.cancer res.47:3577
‑
3583(1987)[brown等人,癌症研究47:3577
‑
3583(1987)],每篇文献的内容通过引用以其全文并入本文。其他参考文献描述了啮齿动物高变区或cdr在与合适的人类抗体恒定结构域融合之类支持框架区(fr)中的情况。例如,参见riechmann et al.nature 332:323
‑
327(1988)[riechmann等人,自然332:323
‑
327(1988)],verhoeyen et al.science 239:1534
‑
1536(1988)[verhoeyen等人,科学239:1534
‑
1536(1988)]和jones et al.nature 321:522
‑
525(1986)[jones等人,自然321:522
‑
525(1986)],每篇文献的内容通过引用以其全文并入本文。另一篇参考文献描述了由重组贴面的啮齿动物框架区支持的啮齿动物cdr—欧洲专利公开号0519596(通过引用以其全文并入本文)。这些“人源化”分子旨在最大限度地减少对啮齿动物抗人类抗体分子的不想要的免疫反应,这限制了这些部分在人类受体中的治疗应用的持续时间和有效性。可以对抗体恒定区进行工程改造,使其在免疫学上是惰性的(例如,不会触发补体裂解)。例如,参见pct公开号wo 99/58572;英国专利申请号9809951.8。daugherty et al.,nucl.acids res.19:2471
‑
2476(1991)[daugherty等人,核酸研究19:2471
‑
2476(1991)]和美国专利号6,180,377、6,054,297、5,997,867、5,866,692、6,210,671和6,350,861以及pct公开号wo 01/27160披露了也可以利用的人源化抗体的其他方法(均通过引用以其全文并入本文)。
[0137]
在一些实施例中,本文的抗体或片段可以重组产生,例如使用转染到宿主细胞中的重组表达载体表达的抗体,从重组、组合人抗体文库中分离的抗体,从人免疫球蛋白基因的转基因动物(例如小鼠)中分离的抗体。
[0138]
抗体的“可变区”或“可变结构域”是指抗体的重链或轻链的氨基末端结构域。重链的可变结构域可称为“vh”。轻链的可变结构域可称为“vl”。这些结构域通常是抗体最可变的部分,包含抗原结合位点。术语“可变的”是指可变结构域的某些部分在抗体之间在序列上有很大差异,并且用于每个特定抗体对其特定抗原的结合和特异性。然而,变异性并非均匀分布在整个抗体的可变结构域中。它集中在轻链和重链可变结构域中称为高变区(hvr)(或结构域cdr)的三个部分中。可变结构域的高度保守部分称为框架区(fr)。天然重链和轻链的可变结构域各包含四个fr区,主要采用β
‑
折叠结构,由三个cdr连接,形成环连接,在某些情况下形成β
‑
折叠结构的一部分。每条链中的cdr由fr区紧密地连接在一起,并且与来自另一条链的cdr一起有助于形成抗体的抗原结合位点(参见kabat et al.,sequences of proteins of immunological interest,fifth edition,national institute of health,bethesda,md.(1991)[kabat等人,免疫学感兴趣的蛋白质序列,第五版,国立卫生研究院,贝塞斯达,马里兰州(1991)])。恒定结构域不直接参与抗体与抗原的结合,但表现出多种效应子功能,例如抗体参与抗体依赖性细胞毒性。
[0139]
来自任何脊椎动物物种的抗体(免疫球蛋白)的“轻链”基于其恒定结构域的氨基酸序列可以归为两种明显不同的类型之一,称为kappa(κ)和lambda(λ)。
[0140]“框架”或“fr”残基是指除了本文所定义的hvr残基以外的那些可变结构域残基。
[0141]
在一些实施例中,本文的抗体具有人fc区。本文中的术语“fc区”用于定义免疫球蛋白重链的c端区,包括天然序列fc区和变体fc区。尽管免疫球蛋白重链fc区的边界可能不同,但人igg重链fc区通常定义为从cys226或pro230位置的氨基酸残基延伸至其羧基末端。例如,在抗体的生产或纯化过程中,或通过重组工程化编码抗体的重链的核酸,可去除fc区
的c端赖氨酸。因此,如本文所用的完整抗体可以是具有或不具有另外的c端赖氨酸的抗体。
[0142]
包含本文披露的抗体、scfv或抗体片段的组合物或药物组合物优选地包含稳定剂,以防止在使用前的储存和运输过程中,由于在一段时间内变性、氧化或聚集的影响,使蛋白质失去活性或结构完整性。组合物或药物组合物可包含可有助于克服聚集问题的盐、表面活性剂、ph调节剂和张力剂(例如糖)的任何组合中的一种或多种。当本发明的组合物或药物组合物用作注射剂时,理想的是将ph值保持在近似中性的ph范围内,将表面活性剂水平降至最低也有利于避免制剂中的气泡,气泡对注射入受试者是有害的。在一些实施例中,组合物或药物组合物为液体形式,并且稳定地支持溶液中的高浓度生物活性抗体,并且适合于吸入或肠胃外施用。在一些实施例中,组合物或药物组合物配制用于哺乳动物受试对象,特别是人类受试者。在一些实施例中,组合物或药物组合物配制用于静脉内、肌肉内、腹膜内、皮内和/或皮下注射。在一些实施例中,组合物或药物组合物可以是液体形式,并且将气泡形成和过敏样副作用的风险降至最低。在一些实施例中,组合物或药物组合物是等渗的。在一个实施例中,组合物或药物组合物的ph值为6.8至7.4。
[0143]
在一些实施例中,本文披露的scfv或抗体片段是冻干的和/或冷冻干燥,并且复溶后使用。
[0144]
药学上可接受的载体的实例包括但不限于磷酸盐缓冲液、无菌水(包括注射用水usp)、乳剂例如油/水乳剂和各种类型的润湿剂。用于气雾剂或肠胃外给药的示例性稀释剂是磷酸盐缓冲液或生理(0.9%)盐水,例如0.9%氯化钠溶液(usp)。包含此类载体的组合物通过众所周知的常规方法配制(参见,例如,remington's pharmaceutical sciences,18th edition,a.gennaro,ed.,mack publishing co.,easton,pa.,1990[雷明顿制药科学,第18版,a.gennaro编辑,麦克出版社公司,伊斯顿,宾夕法尼亚州,1990];和remington,the science and practice of pharmacy 20th ed.mack publishing,2000[雷明顿,药学的科学与实践,第20版,麦克出版社,2000],其每一个的内容通过引用以其全文并入本文)。在非限制性实例中,其可包含磷酸氢二钠、氯化钾、磷酸二氢钾、聚山梨醇酯80(例如2
‑
[2
‑
[3,5
‑
双(2
‑
羟基乙氧基)氧杂环戊
‑2‑
基]
‑2‑
(2
‑
羟基乙氧基)乙氧基]乙基(e)
‑
十八碳
‑9‑
烯酸乙酯)、依地酸二钠脱水物、蔗糖、磷酸二氢钠一水合物和磷酸氢二钠二水合物中的一种或多种。
[0145]
本文所述的抗体、或抗体片段、或组合物、或药物组合物也可冻干或以任何合适的形式提供,包括但不限于可注射溶液或可吸入溶液、凝胶形式和片剂形式。
[0146]
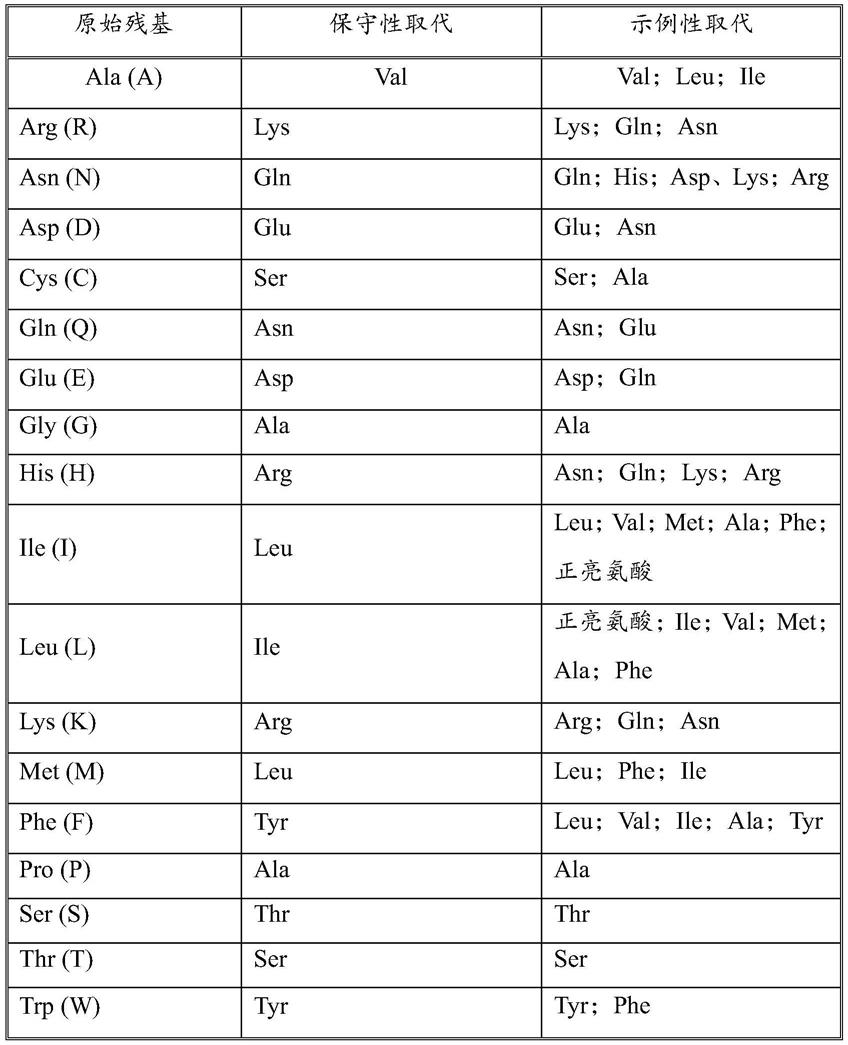
本发明涵盖抗体的取代变体。取代变体去除抗体分子中的至少一个氨基酸残基,并在其位置插入不同的残基。取代突变最感兴趣的位点包括高变区,但也考虑了框架改变。这些保守取代显示于表1中的“保守性取代”的标题下。如果此类取代导致生物活性的改变,则可以引入在表1中命名为“示例性取代”的、或如在下文进一步参考氨基酸类别所述的更多实质性改变,并且筛选产物。表1:氨基酸取代
[0147]
抗体的生物学特性中的实质性修饰是通过选择它们在维持以下作用上显著不同的取代来完成:(a)取代区域中多肽骨架的结构,例如β
‑
片层或螺旋构象;(b)靶位点处分子的电荷或疏水性;或(c)侧链的体积。基于共同侧链性质,将天然存在的残基分为以下的组:(1)非极性:正亮氨酸、met、ala、val、leu、ile;
(2)极性不带电:cys、ser、thr、asn、gln;(3)酸性(带负电):asp、glu;(4)碱性(带正电):lys、arg;(5)影响链取向的残基:gly、pro;和(6)芳族的:trp、tyr、phe、his。
[0148]
通过将这些类别之一的成员交换为另一类来进行非保守取代。
[0149]
例如,可以进行的一种类型的取代是将抗体中的一个或多个半胱氨酸(其可能具有化学反应性)改变为另一残基,例如但不限于丙氨酸或丝氨酸。例如,可以取代非典型半胱氨酸。可以在可变结构域的cdr或框架区或抗体的恒定区中进行取代。在一些实施例中,半胱氨酸是典型的。通常还可用丝氨酸取代不参与维持抗体正确构象的任何半胱氨酸残基,以改善分子的氧化稳定性并防止异常交联。相反,可以将一个或多个半胱氨酸键添加到抗体中以提高其稳定性,特别是当抗体是抗体片段(例如fv片段)时。
[0150]
抗体也可以被修饰,例如在重链和/或轻链的可变结构域中,例如以改变抗体的结合特性。可变区的变化可以改变结合亲和力和/或特异性。在一些实施例中,在cdr结构域内进行不超过一到五个保守氨基酸取代。在其他实施例中,在cdr结构域内进行不超过一到三个保守氨基酸取代。
[0151]
本文所述的抗体可以重组产生。在真核表达系统中产生的抗体在对应于asn297的fc部分的残基处包含糖基化。
[0152]
在一些实施例中,包含本文所述的抗体或其抗原结合片段的组合物或药物组合物就抗体或其抗原结合片段而言是基本上纯的。当组合物或药物组合物的至少60%至75%的样品表现出单一物种的抗体或其抗原结合片段时,包含本文所述的抗体或其抗原结合片段的组合物或药物组合物就抗体或片段而言是“基本纯的”。包含本文所述的抗体或其抗原结合片段的基本纯的组合物或药物组合物可以在其作为抗体或抗原结合片段的部分中包含单一物种的抗体或抗原结合片段的60%、70%、80%或90%,更通常为约95%,优选超过99%。纯度或均一性可以通过本领域公知的多种方法来检测,例如聚丙烯酰胺凝胶电泳或hplc。
[0153]
在这些方法的实施例中,受试者是哺乳动物。
[0154]
在一些实施例中,该哺乳动物是人类。
[0155]
除非本文另有说明或另外与上下文明显矛盾,否则本文描述的各种要素的所有组合均在本发明的范围内。
[0156]
本文所使用的术语仅出于描述特定实施例的目的,而并非旨在进行限制。如本文所使用的,除非内容另外明确指出,否则单数形式“一(a和an)”和“该”旨在包括复数形式,包括“至少一个”。“至少一个”不应被解释为限制“一个”(a和an)。“或”的意思是“和/或”。在此使用的,术语“和/或”包括相关列出项目中的一个或多个的任何和所有组合。术语“包含”、“包括”和“具有”旨在为包括在内的并且意指可存在除所列要素之外的另外的要素。
[0157]
药学上可接受的:如本文所用,术语“药学上可接受的”是指经联邦或州政府的监管机构批准或列于美国药典、除可安全用于动物(更特别地用于人类和/或非人类哺乳动物)的其他制剂之外的其他公认药典。药学上可接受的载体;如本文所用,术语“药学上可接受的载体”是指赋形剂、稀释剂、防腐剂、增溶剂、乳化剂、佐剂和/或赋形剂,与本发明的抗
体或片段一起施用。此类载体可以是无菌液体,如水和油,包括来自石油、动物、植物或合成来源的那些油,如花生油、大豆油、矿物油、芝麻油等、聚乙二醇、甘油、丙二醇或其他合成溶剂。抗细菌剂,如苄醇或对羟苯甲酸甲酯;抗氧化剂,如抗坏血酸或亚硫酸氢钠;螯合剂,如乙二胺四乙酸;以及用于调节张力的试剂,如氯化钠或葡萄糖也可以是载体。生产与载体组合的组合物的方法是本领域技术人员已知的。在一些实施例中,词语“药学上可接受的载体”旨在包括与药物施用相容的任何和所有溶剂、分散介质、包衣、等渗剂以及吸收延迟剂等。用于药物活性物质的此类介质和试剂的使用是本领域熟知的。参见,例如,remington,the science and practice of pharmacy.20"'ed.[雷明顿,制药科学与实践,第20"'版],(lippincott,williams和wilkins 2003)。除非任何常规介质或试剂与活性化合物不相容,否则考虑在组合物中的此种用途。
[0158]
应理解,本文所述的本发明的方面和实施例包括“由多个方面和实施例组成”和/或“基本上由多个方面和实施例组成”。
[0159]
贯穿本披露,本发明的各个方面可以以范围的格式呈现。应当理解,在范围格式内的描述仅为了方便和简洁,并且不应当解释为是对本发明的范围的硬性限制。因此,应当将范围的描述视为已明确披露所有可能的子范围以及该范围内的单独数值。例如,对诸如1至6的范围的描述应当被视为已经明确披露诸如1至3、1至4、1至5、2至4、2至6、3至6等子范围,以及该范围内的单独数字,例如1、2、3、4、5和6。无论范围的宽度如何,这都适用。
[0160]
本发明的其他目标、优点和特征将根据以下说明结合附图而变得清楚。
[0161]
虽然已经参考各种实施例描述了本披露,但是本领域技术人员将理解,在不脱离本披露的范围的情况下,可以做出各种改变并且能以多种等效物替代其元素。此外,在不脱离其本质范围的情况下,可以进行许多修改以使特定情况或材料适应本披露的指导。因此,其目的是,本披露不限于作为实施本披露考虑的最佳模式所披露的特定实施例,而是本披露将包括落入所附权利要求书的范围内的所有实施例。
[0162]
所有引用的专利、专利申请和其他参考文献均通过引用以其全文而并入本文。然而,如果本技术中的术语与并入的参考文献中的术语矛盾或冲突,则来自本技术的术语优先于来自并入的参考文献的冲突术语。
[0163]
从下面的实验细节可以更好地理解本发明。实验细节
[0164]
在免疫显性包膜糖蛋白d(指定为δgd
‑
2)中缺失的候选hsv
‑
2单周期病毒疫苗诱导高滴度抗体,这些抗体能够在鼠模型中主动和被动地保护小鼠免受hsv疾病。这些抗体具有弱中和作用,但可有效激活鼠fcγ受体iv(fcγriv)以激活抗体依赖性细胞介导的细胞毒性(adcc)。本披露已经分析、克隆、测序和测试了从免疫小鼠的生发中心b细胞中分离的单克隆抗体(mab),并且鉴定了几种被动保护小鼠免受病毒性疾病侵害的单克隆抗体。某些mab具有足够的活性,可用于预防和治疗带有hsv(例如人源化形式)或有播散性疾病风险的患者(例如新生儿、免疫功能低下的宿主)。
[0165]
用δgd
‑
2对小鼠进行初免
‑
加强免疫,并分离脾脏、引流淋巴结或骨髓。然后在nb
‑
21.2d9细胞(nojima培养物)上培养生发中心(gc)b细胞。培养后,通过elisa筛选上清液中是否存在结合hsv裂解物的igg。对从选定的gc b细胞培养物中扩增的v(d)j重排进行了测序,用于在单个小鼠的gc b细胞克隆中进行b细胞抗原受体(bcr)谱分析。然后,评估来自选
定的单个gc b细胞培养物和单个骨髓浆细胞的重建抗体在体外激活mfcγriv和在被动转移模型中保护小鼠的能力。
[0166]
简而言之,小鼠用δgd
‑
2接种,然后在接种后16天,取引流的腹股沟淋巴结。从这些组织中分离出gc b细胞并在nojima培养物中培养。尽管来自这些(运输)组织的gc b细胞的总体克隆效率低于来自新鲜分离组织的那些(6%结构域对结构域20%),但获得了50个对hsv
‑
2g菌株(hsv
‑
2g或hsv2
‑
g)裂解物具有特异性的gc克隆。对hsv
‑
2g裂解物和未感染的vero裂解物(对照)进行elisa分析,结果示于图1中。将来自接种了δgd
‑
2的小鼠的腹股沟淋巴结的gc b细胞直接分选到96孔板中(1个细胞/孔)。然后在nb
‑
21.2d9饲养细胞的存在下培养这些gc b细胞。培养后,首先通过elisa测定igg的存在,然后通过elisa检测培养上清液igg对hsv
‑
2g裂解物(hsv
‑
2g)和未感染的vero裂解物的反应性。
[0167]
分析了gc b细胞的分子遗传学(图2)。从hsv
‑
2g裂解物反应性、igg+的培养物的cdna中扩增v(d)j重排,然后进行克隆和测序。使用imgt v
‑
quest(参见万维网imgt.org/)测定重排的v、d和j基因片段。hsv2特异性gc b细胞使用了不同组的vh基因片段。vh1
‑
64和vh1
‑
26比其他基因片段出现的频率更高(~10%)。
[0168]
基于从每个b细胞培养物中获得的v(d)j序列,成对的重链和轻链在expi293f细胞中重新表达(作为重组小鼠igg1和igg2c抗体)(kuraoka et al.immunity2016;dilillo et al.nature medicine 2013[kuraoka等人,免疫2016;dilillo等人,自然医学2013])。然后,从第16天的gc b细胞中选择4个独立的、hsv
‑
2g裂解物反应的igg+单个b细胞培养物。正如预期的那样,所有重组抗体都与hsv
‑
2g裂解物发生特异性反应(图3)。克隆32h6与裂解物结合最紧密,其次是35h7、22d10和33b8。图3显示了重组抗体对hsv
‑
2g裂解物结合的保留。通过elisa检测重组抗体与hsv
‑
2g裂解物的结合。通过标准rt
‑
pcr,从选定的单个b细胞培养孔(22d10、32h6、33b8和35h7)中扩增重链和轻链v(d)j重排。将这些克隆的v(d)j重排引入表达载体。通过将这些表达载体共转染到expi293f细胞中获得重组抗体。获得了≥4mg的纯化的igg(未显示)。这些抗体未与对照、未感染的vero裂解物结合。在体外fcγriv激活测定(promega fcγriv adcc报告基因生物检测试剂盒)(图4)和体内保护测定中,检测了这些重组抗体(每种≥4mg)的反应抗原的同一性。
[0169]
δgd
‑
2初免
‑
加强疫苗接种在小鼠中建立了持久的、hsv反应性的(和保护性的)血清igg反应,结果表明加强后8个月,小鼠仍然受到保护免受hsv攻击。这些结果表明疫苗接种成功地建立了长寿命的浆细胞。假设可以分离出hsv反应性浆细胞,这些浆细胞可以从已接受初免
‑
加强疫苗接种的小鼠的骨髓中产生保护性igg。在从δgd
‑
2接种小鼠中分离骨髓浆细胞的实验中,与未接种小鼠相比,接种δgd
‑
2的小鼠在骨髓中含有频率高4倍的表面igm
‑
cd138hib220lo/
‑
fschi浆细胞。
[0170]
为了分析骨髓浆细胞的分子遗传学,从单个sigm
‑
cd138
hi
b220
lo/
‑
fsc
hi
浆细胞的cdna中扩增v(d)j重排,然后对扩增产物进行克隆和测序。使用imgt v
‑
quest(可在万维网imgt.org/上获得)测定重排的v、d和j基因片段。我们从96个单个细胞中回收了21对重链和轻链以及4个仅重链的克隆(表1)。25条重链序列由四个igg3(16%)、九个igg1(36%)、七个igg2b(28%)、四个igg2c(16%)和一个iga(4%)同种型组成。20个单独的克隆(80%)在v
h
基因片段中携带至少一个核苷酸取代(平均4.4个v
h
突变)。从δgd的骨髓浆细胞中回收的v(d)j重排总结:下表2中提供了接种hsv的小鼠。如表2所示,cdr3显示保守残基(c、w表示
hdcr,c、f表示lcdr)。除了bmpc
‑
7,igg2b或igg2c克隆(表2中的灰色行)携带v
h
和v
l
突变,表明这些浆细胞克隆是通过gc反应产生的。
[0171]
由δgd
‑
2疫苗接种引发的血清抗体的保护取决于fcγriv的激活。重点关注优先结合活化fcγr的igg2c抗体。基于从每个浆细胞获得的v(d)j序列,如上所述在expi293f细
胞中重新表达成对的重链和轻链(作为重组小鼠igg1和igg2c抗体)。选择了九个带有igg2b和igg2c恒定区的克隆(bmpc
‑
1、bmpc
‑
12、bmpc
‑
7、bmpc
‑
8、bmpc
‑
9、bmpc
‑
23、bmpc
‑
26、bmpc
‑
57和bmpc
‑
61)。在这九种抗体中,bmpc
‑
23,而不是其他抗体,与hsv
‑
2g裂解物反应(图5a和5b,数据未显示)。bmpc
‑
23的结合与19g7的结合相当,后者是另一种从δgd
‑
2接种小鼠的gc b细胞克隆的hsv
‑
2g裂解物反应性igg。bmpc
‑
23的igg1和igg2c同种型在体外fcγriv激活测定(图4)和体内保护测定(参见下文描述,图6a至6c)中进行分析。如图4所示,bmpc
‑
23igg2c显示出最高水平的fcγr活化。
[0172]
评估了igg1和igg2c形式的22d10、33b8和bmpc
‑
23抗体(每种≥4mg)的体内保护测定的重现性,以及对ig同种型保护的任何依赖性。代表性实验示于图6a
‑
6c中。简而言之,来自2个独立实验的总体结果表明bmpc
‑
23的igg2c版本保护8/10小鼠,22d10保护5/10小鼠,而33b8保护4/10小鼠免受致命攻击。三种单克隆抗体bmpc
‑
23、22d10和33b8(作为igg2c)提供了针对hsv
‑
2的显著保护。为了测试ig同种型对提供保护能力的作用,生成了这三种抗体的igg1和igg2c同种型,并评估了激活mfcγriv信号传导的能力(作为adcc的测量),以及用于体内保护测定。结果示于图4中。
[0173]
进行ip
‑
ms以鉴定22d10、33b8和bmpc
‑
23抗体的靶标。结果示于图7a和7b中,鉴定人类疱疹病毒糖蛋白b(gb)作为靶标。
[0174]
bmpc
‑
23结合hsv
‑
1gb(gb
‑
1)。抗体的gb
‑
1结合通过luminex多重分析测定。将抗原(gb
‑
1)偶联微球的混合物(每个1,000个计数)添加到96孔过滤板(millipore)的每个孔中。用含1%bsa、0.05%tween 20和0.05%nan3的pbs洗涤后,连续稀释重组抗体(5e7、19g7、18g4、22e10、3a2、17g3、22d10、32h6、33b8、25h7、bmpc
‑
23和s5v2
‑
29)加入板中并在室温下孵育2小时,同时轻轻搅动板。样品在含有1%牛奶、1%bsa、0.05%tween 20和0.05%nan3的pbs中稀释。洗涤后,将pe山羊抗小鼠igg加入板中并在室温下温和搅拌孵育1小时。洗涤后,将微球重新悬浮在含有1%bsa、0.05%tween 20和0.05%nan3的pbs中,并在3d机器中测量来自每个微球的荧光信号。如图8所示,唯一证明与gb
‑
1有实质性结合的抗体是bmpc
‑
23。
[0175]
寻找gb
‑
1特异性hsv抗体。在nojima培养(单b细胞培养)后,从生发中心b细胞中克隆出hsv特异性抗体,并通过如上所述的luminex多重分析检测该抗体与hsv
‑
1gb
‑
1的结合。图9a和9b显示了与bmpc
‑
23相比的10种抗体的gb
‑
1结合结果。所检测抗体的细胞来源和分离方法见表3。除bmpc
‑
23外,表3中的抗体来自于初次接种δgd
‑
2后15
‑
17天采集的生发中心b细胞(淋巴结)。bmpc
‑
23来源于用δgd
‑
2加强后2周采集的骨髓浆细胞。表4中显示了重链和轻链的核苷酸序列和氨基酸序列,以及轻链和重链cdr1、cdr2和cdr3的氨基酸序列。
[0176]
寻找bmpc样抗体。检测了图3中10种gb
‑
1特异性小鼠单克隆igg抗体中的9种抑制bmpc
‑
23人igg抗体与gb
‑
1结合的能力。连续稀释的gb
‑
1特异性小鼠单克隆抗体或无关的对照小鼠抗体(h33lγ1)与gb
‑
1偶联的luminex珠一起孵育。孵育后,将固定浓度(2ng/ml)的bmpc
‑
23人igg抗体加入每个孔中。洗涤后,加入小鼠抗人igg
‑
pe以检测人bmpc
‑
23抗体的结合。y轴表示最大结合的mfi百分比,确定为存在不与gb
‑
1结合的对照igg、h33lγ1时的平均mfi。图10a显示bmpc
‑
23小鼠igg(222ng/ml)抑制人bmpc>99%。hsv010
‑
4(在222ng/ml时>95%)、hsv010
‑
7(在222ng/ml时>90%)和hsv010
‑
34(在222ng/ml时>80%)的强烈抑制,如图10b、10f和10g分别表明这些抗体结合gb
‑
1上的表位,与bmpc
‑
23识别的表位紧密重叠。因
此,预计这些抗体具有与bmpc
‑
23类似的保护功效(实验在进行中)。hsv010
‑
28(图10d中222ng/ml时30%抑制)和hsv010
‑
6、9、13、14(图10e中222ng/ml时32%
‑
48%)的轻度抑制表明,这些抗体识别的gb
‑
1上的表位与bmpc
‑
23识别的表位部分地重叠。如图10c所示,hsv010
‑
20没有抑制作用,表明该抗体识别的表位与bmpc
‑
23识别的表位不重叠。需要检测这些抗体的保护功效(实验在进行中)。上述数据也总结在下表3中。
[0177]
追加的实验。抗体22d10和33b8的目标抗原的测定将使用类似于用于bmpc
‑
23抗体的抗原测定的那些方法的方法进行。例如,可以使用诸如由22d10或33b8抗体结合的蛋白质的质谱和/或针对来自hsv
‑
1的其他非gb纯化抗原筛选22d10或33b8的方法。
[0178]
将使用上述方法评估表3中12种未经检测的抗体防止hsv
‑
1引起的眼部感染的能力。
[0179]
将进行表3中hsv
‑
1结合抗体的表位的结构测定。此类方法包括抗体的fab片段与hsv
‑
1蛋白(例如gb
‑
1)的共结晶、x
‑
射线衍射和通过xds的分析。(参见例如watanabe et al,2019,cell,177,1124
‑
1135[watanabe等人,2019,细胞,177:1124
‑
1135])。表3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1