具有降低的免疫原性的抗体的制作方法
具有降低的免疫原性的抗体
1.相关申请的交叉引用
2.本技术要求2019年7月9日提交的美国临时专利申请号62/871,856的优先权权益,其内容全部通过引用并入本文。
技术领域
3.本发明属于抗体工程领域。
背景技术:
4.已经很好地确立了使用治疗性抗体来治疗多种病症,其中数百种治疗性抗体靶向数十种已经批准用于人类使用的靶标。具有细胞毒性作用、阻断作用、活化作用和更多种作用的抗体是已知的并已被充分表征。然而,许多治疗性抗体在施用它们的患者中引发免疫反应。
5.具有与人类序列不同的氨基酸序列的外源蛋白质被免疫系统识别为病原体。这导致产生与外源蛋白质结合并靶向它们以降解的抗药物抗体(ada)。当外源蛋白是治疗剂时,ada可以阻断治疗性分子的功能,减少循环半衰期,并导致治疗剂在达到治疗效果之前从受试者体内消除。通常,ada反应会严重降低分子的治疗效果。
6.已知许多众所周知和充分表征的抗体可诱导ada。根据所调查的研究,据报道,接受修美乐(humira)治疗的患者中有9-89%出现ada。据报道,抗ctla抗体伊匹单抗在约25%的患者中产生ada。降低ada的一种可能方法是降低治疗性分子的免疫原性,然而,非常需要设计具有降低的免疫原性的治疗剂,特别是抗体的方法。
技术实现要素:
7.本发明提供了从第一抗体产生第二抗体的方法和降低抗体的免疫原性的方法。还提供了包括非免疫原性或低免疫原性序列的多肽、抗体和抗原结合片段。
8.根据第一方面,提供了包括三条重链cdr(cdr-h)和三条轻链cdr(cdr-l)的抗体或其抗原结合片段,其中:
9.cdr-h1包括如seq id no:114(dyamh)中所列的氨基酸序列,cdr-h2包括如seq id no:115(aitw)中所列的氨基酸序列,cdr-h3包括如seq id no:116(x
12
sx
13
x
14
x
15
x
16
x
17
x
18
x
19
ldx
30
)所列的氨基酸序列且不包括seq id no:6,cdr-l1包括如seq id no:117(rasqgirnyla)中所列的氨基酸序列,cdr-l2包括如seq id no:118(aastlqs)中所列的氨基酸序列,并且cdr-l3包括如seq id no:119(qrynrapyx
31
)中所列的氨基酸序列,其中
10.x
12
选自d、e和v,
11.x
13
选自d、e、g、n、q、t、v、w、f、l和y,
12.x
14
选自a、e、h、l、n、p、q、s、t、v和w,
13.x
15
选自e、s和g,
14.x
16
选自e、g、h、k、p、r和t,
15.x
17
选自a、s和g,
16.x
18
选自e、s、g和d,
17.x
19
选自d、n、g和s,
18.x
30
选自y和n,
19.x
31
选自t和a。
20.根据另一方面,提供了一种抗体或抗原结合片段,其包括包含seq id no:133且不包含seq id no:1的重链。
21.根据另一方面,提供了一种抗体或抗原结合片段,其包括包含seq id no:134且不包含seq id no:1的重链。
22.根据一些实施方式,cdr-l3由seq id no:120(qrynrapyt)组成。
23.根据一些实施方式,cdr-h3包括seq id no:121(x
12
sx
13
x
14
x
15
x
16
x
17
x
18
x
19
ld y)。
24.根据一些实施方式,其中seq id no:116包括x
12
sx
20
x
21
x
15
x
16
x
22
x
23
x
24
ld x
31
(seq id no:122),其中
25.x
12
选自d、e和v,
26.x
20
选自d、e、g、n、q、t、v、w和y,
27.x
21
选自a、e、h、l、n、p、q、s、t和w,
28.x
15
选自e、s和g,
29.x
16
选自e、g、h、k、p、r和t,
30.x
22
选自a和g,
31.x
23
选自e、s和d,
32.x
24
选自d和s,和
33.x
31
选自t和a。
34.根据一些实施方式,seq id no:116包括vsx
25
x
26
stx
27
x
28
x
29
ldx
31
(seq id no:123),其中
35.x
25
选自w、y、g、q、f、l和v,
36.x
26
选自l、v、h和p,
37.x
27
选自a和s,
38.x
28
选自e、s和g,
39.x
29
选自n、s、d和g,
40.x
31
选自t和a。
41.根据一些实施方式,seq id no:116包括选自seq id no:97-112的氨基酸序列。
42.根据一些实施方式,本发明的抗体或抗原结合片段进一步包括cdr-h2和cdr-h3之间的lx1lx2mnx3lx4x5(seq id no:2)。
43.根据一些实施方式,seq id no:2不包括lylqmnslra(seq id no:1)。
44.根据一些实施方式,seq id no:2包括seq id no:3、seq id no:4或seq id no:5。
45.根据一些实施方式,seq id no:2由选自seq id no:10-26、37-96和113的序列组成。
46.根据一些实施方式,重链包括选自seq id no:132和133的序列。
47.根据一些实施方式,抗体或抗原结合片段包括包含seq id no:128的轻链。
48.根据一些实施方式,重链包括seq id no:131。
49.根据一些实施方式,seq id no:133从氨基酸79-88包括seq id no:3、seq id no:4或seq id no:5。
50.根据一些实施方式,seq id no:133在氨基酸79-88处包括选自seq id no:10-26、37-96和113的序列。
51.根据一些实施方式,抗体或抗原结合片段结合肿瘤坏死因子α(tnfa)。
52.根据一些实施方式,抗体或抗原结合片段包括包含seq id no:130的轻链。
53.根据一些实施方式,seq id no:134从氨基酸79-88包括seq id no:3、seq id no:4或seq id no:5。
54.根据一些实施方式,seq id no:134在氨基酸79-88处包括选自seq id no:10-26、37-96和113的序列。
55.根据一些实施方式,抗体或抗原结合片段结合细胞毒性t淋巴细胞相关蛋白4(ctla4)。
56.根据另一方面,提供了一种包括seq id no:2的多肽,其中seq id no:2不包括seq id no:1、seq id no:12、seq id no:38、seq id no:60、seq id no:71和seq id no:94中的任一者。
57.根据另一方面,提供了一种抗体或抗原结合结构域,其包括本发明的多肽。
58.根据另一方面,提供了一种抗体或抗原结合结构域,其包括包含seq id no:2的多肽,其中seq id no:2不包括seq id no:1并且不包括seq id no:12。
59.根据另一方面,提供一种药物组合物,其包括本发明的多肽或本发明的抗体或抗原结合片段以及药学上可接受的载体、赋形剂或佐剂。
60.根据一些实施方式,多肽在人类中是非免疫原性的。
61.根据一些实施方式,seq id no:2是seq id no:3。
62.根据一些实施方式,seq id no:2是seq id no:4。
63.根据一些实施方式,seq id no:2是seq id no:5。
64.根据一些实施方式,seq id no:2由选自seq id no:10-11、13-26、37、39-59、61-70、72-93、95-96和113的序列组成。
65.根据一些实施方式,seq id no:2由选自seq id no:10-11、13-26、37、39-59、61-70、72-93、95-96和113的序列组成。
66.根据一些实施方式,抗体或其抗原结合片段的重链包括seq id no:2。
67.根据一些实施方式,重链的氨基酸79-88是seq id no:2。
68.根据另一方面,提供了由第一抗体产生第二抗体的方法,该方法包括:
69.a.提供包括编码第一抗体的氨基酸序列的编码序列的第一核酸分子,其中氨基酸序列包括lylqmnslra(seq id no:1),
70.b.提供编码第二抗体的氨基酸序列的第二核酸分子,其中氨基酸序列包括lx1lx2mnx3lx4x5(seq id no:2),而不是seq id no:1,其中:
71.x1选自d、h、n、s、y、a、f和t,
72.x2选自e和q,
73.x3选自d、g和s,
74.x4选自a、g、r、s和t,
75.x5选自a、d、e、n、p、t和k,
76.其中seq id no:1和seq id no:2包括不同的氨基酸序列;
77.c.由第二核酸分子产生第二抗体;
78.从而产生第二抗体。
79.根据一些实施方式,产生第二抗体包括降低第一抗体的免疫原性。
80.根据一些实施方式,第一抗体的重链包括seq id no:1。
81.根据一些实施方式,seq id no:1是第一抗体的重链的氨基酸79-88。
82.根据一些实施方式,seq id no:2由选自seq id no:10-26、37-96和113的序列组成。
83.根据一些实施方式,本发明的方法进一步包括确认第二抗体与第一抗体的靶标或表位的结合。
84.根据一些实施方式,确认的结合包括通过结合测定测量第二抗体与靶标或表位的结合值,并确认第二抗体的结合值是第一抗体与靶标或表位的结合值的至少70%。
85.根据一些实施方式,第一抗体选自表2。
86.根据一些实施方式,第一抗体选自:阿法西库单抗(afasevikumab)、阿达木单抗(adalimumab)、苏替木单抗(sutimlimab)、壬托鲁单抗(remtolumab)、特雷克单抗(terextumab)、埃罗妥珠单抗(elotuzumab)、比美克珠单抗(bimekizumab)、索非妥珠单抗(sofituzumab vedotin)、洛利昔珠单抗(rozanolixizumab)、拉那鲁单抗(lanadelumab)、苏维妥昔单抗(suvratoxumab)、戈奈单抗(gosuranemab)、伊匹单抗(ipilimumab)、度匹鲁单抗(dupliumab)、依法利珠单抗(efalizumab)、弗洛西单抗(frovocimab)、依玛鲁单抗(emapalumab)、阿利库单抗(alirocumab)、英克勒库单抗(inclacumab)、克罗特度单抗(crotedumab)、阿维鲁单抗(avelumab)、奥匹努单抗(opicinumab)、艾米珠单抗(emicizumab)、杜伐鲁单抗(durvalumab)、索拉尼单抗(solanexumab)、雷莫卢单抗(ramucirumab)、托维单抗(tovetumab)、帕妥珠单抗(pertuzumab)、舒他伏单抗(suptavumab)、奈伐苏单抗(nesvacumab)、奎利珠单抗(quilizumab)、布拉齐单抗(brazikumab)、地诺单抗(denosumab)、伐立鲁单抗(varlilumab)、曲美木单抗(tremelimumab)、伊妥珠单抗(igatuzumab)、罗妥木单抗(robatumumab)、普瑞鲁单抗(prezalumab)、prasinezumab、帕诺库单抗(panobacumab)、奥替利单抗(otilimab)、奥昔组单抗(otelixizumab)、奥索西单抗(osocimab)、莫星-洛沃妥珠单抗(lorvotuzumab mertansine)、来沙木单抗(lexatumumab)、艾芦库单抗(icrucumab)、fremanexumab、埃吉姆单抗(elgemtumab)、daratumumb、corncizumab、巴匹珠单抗(bapineuzumab)和安芦珠单抗(anrukinzumab)。
87.根据一些实施方式,第一抗体是阿达木单抗或伊匹单抗。
88.从下文给出的详细描述中,本发明的其他实施方式和应用的全部范围将变得显而易见。然而,应该理解的是,虽然详细描述和具体实例指示了本发明的优选实施方式,但是其仅以说明的方式给出,因为从该具体描述,在本发明的精神和范围内的各种变化和修改对于本领域技术人员来说是显而易见的。
no:2不包括seq id no:94。在一些实施方式中,seq id no:2不包括选自seq id no:1、seq id no:12、seq id no:38、seq id no:60、seq id no:71和seq id no:94的序列。在一些实施方式中,seq id no:2不包括seq id no:1、seq id no:12、seq id no:38、seq id no:60、seq id no:71和seq id no:94。在一些实施方式中,seq id no:2不包括seq id no:1、seq id no:12、seq id no:38、seq id no:60、seq id no:71和seq id no:94中的任一者。在一些实施方式中,seq id no:2不含seq id no:1、seq id no:12、seq id no:38、seq id no:60、seq id no:71和seq id no:94。在一些实施方式中,seq id no:2不含seq id no:1、seq id no:12、seq id no:38、seq id no:60、seq id no:71和seq id no:94的全部。
99.在一些实施方式中,多肽包括至少10、20、30、40、50、60、70、80、90、100、110、120、130、140、150、160、170、180、190、200、210、220、230、240、250、260、270、280、290、300、310、320、330、340、350、360、370、380、390、400、410、420、430、440、450、460、470、480、490或500个氨基酸。每种可能性代表本发明的单独实施方式。在一些实施方式中,多肽包括至少120个氨基酸。在一些实施方式中,多肽包括至少220个氨基酸。在一些实施方式中,多肽包括至少330个氨基酸。在一些实施方式中,多肽包括至少440个氨基酸。在一些实施方式中,多肽包括至多100、110、120、130、140、150、160、170、180、190、200、210、220、230、240、250、260、270、280、290、300、310、320、330、340、350、360、370、380、390、400、410、420、430、440、450、460、470、480、490、500、550、600、650、700、750、800、850、900、950或1000个氨基酸。每种可能性代表本发明的单独实施方式。在一些实施方式中,多肽包括至多130个氨基酸。在一些实施方式中,多肽包括至多230个氨基酸。在一些实施方式中,多肽包括至多450个氨基酸。在一些实施方式中,多肽包括至多500个氨基酸。
100.在一些实施方式中,多肽是治疗剂或包括在治疗剂中。在一些实施方式中,多肽是药物或包括在药物中。在一些实施方式中,多肽、治疗剂或药物适合施用于受试者。在一些实施方式中,多肽治疗剂或药物被配制用于施用于受试者。在一些实施方式中,受试者是哺乳动物。在一些实施方式中,受试者是人。在一些实施方式中,施用是全身施用。在一些实施方式中,多肽是非免疫原性肽。在一些实施方式中,多肽为低免疫原性肽。在一些实施方式中,多肽不会在受试者中诱导免疫反应。在一些实施方式中,与包括seq id no:1的多肽相比,多肽在受试者中产生降低的免疫反应。在一些实施方式中,治疗剂是抗体。在一些实施方式中,治疗剂是抗原结合结构域。
101.在一些实施方式中,抗体或抗原结合结构域包括多肽。在一些实施方式中,抗体或抗原结合片段的重链包括seq id no:2。在一些实施方式中,seq id no:2是抗体或抗原结合片段的重链的氨基酸79-88。
102.在一些实施方式中,抗体是阿达木单抗(修美乐(humira))。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中阿达木单抗的重链的氨基酸79-88已被seq id no:2替代。在一些实施方式中,抗体是伊匹单抗(yervoy)。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中阿达木单抗的重链的氨基酸79-88已被seq id no:2替代。
103.在一些实施方式中,seq id no:2包括氨基酸序列lx6lx2mnx3lx4x7(seq id no:3),其中x6选自n、s、y、a和h,x2选自e和q,x3选自d、g和s,x4选自a、g、r、s和t,和x7选自e、p、t和a。在一些实施方式中,seq id no:2由seq id no:3组成。在一些实施方式中,seq id no:2包括氨基酸序列lx8lx2mnx3lx4x9(seq id no:4),其中x8选自n、s、y、d和h,x2选自e和q,x3选自
d、g和s,x4选自a、g、r、s和t,和x9选自d、e、p、n和a。在一些实施方式中,seq id no:2由seq id no:4组成。在一些实施方式中,seq id no:2包括氨基酸序列lx
10
lx2mnx3lx4x
11
(seq id no:5),其中x
10
选自t、d和y,x2选自e和q,x3选自d、g和s,x4选自a、g、r、s和t,和x
11
选自e、p和d。在一些实施方式中,seq id no:2由seq id no:5组成。
104.在一些实施方式中,抗体或抗原结合片段的重链选自表1。在一些实施方式中,抗体或抗原结合片段的重链选自seq id no:27-36。
105.表1
[0106][0107]
在一些实施方式中,seq id no:2由lnlemndltp(seq id no:10)组成。在一些实施方式中,seq id no:2由lnlqmndltp(seq id no:11)组成。在一些实施方式中,seq id no:2由lylqmnslrp(seq id no:12)组成。在一些实施方式中,seq id no:2由lylemnglsp(seq id no:13)组成。在一些实施方式中,seq id no:2由lslqmndltt(seq id no:14)组成。在一些实施方式中,seq id no:2由lhlemnglte(seq id no:15)组成。在一些实施方式中,seq id no:2由lylemndlgt(seq id no:16)组成。在一些实施方式中,seq id no:2由lylemnglap(seq id no:17)组成。在一些实施方式中,seq id no:2由lalemnsltp(seq id no:18)组成。在一些实施方式中,seq id no:2由lslemndlga(seq id no:19)组成。在一些实施方式中,seq id no:2由ltlemnsltp(seq id no:20)组成。在一些实施方式中,seq id no:2由ltlemnslte(seq id no:21)组成。在一些实施方式中,seq id no:2由ltlemnglgp(seq id no:22)组成。在一些实施方式中,seq id no:2由ltlemnglap(seq id no:23)组成。在一些实施方式中,seq id no:2由lylemndlsd(seq id no:24)组成。在一些实施方式
中,seq id no:2由ltlemnglsp(seq id no:25)组成。在一些实施方式中,seq id no:2由ltlemnglrp(seq id no:26)组成。在一些实施方式中,seq id no:2由选自seq id no:10-19的序列组成。在一些实施方式中,seq id no:2由选自seq id no:10-26的序列组成。在一些实施方式中,seq id no:2由选自表4的序列组成。在一些实施方式中,seq id no:2由选自表6的序列组成。在一些实施方式中,seq id no:2不由seq id no:12组成。
[0108]
在一些实施方式中,多肽进一步包括氨基酸序列x
12
sx
13
x
14
x
15
x
16
x
17
x
18
x
19
ld(seq id no:7),其中x
12
选自d、e和v;x
13
选自d、e、g、n、q、t、v、w、f、l和y;x
14
选自a、e、h、l、n、p、q、s、t、v和w;x
15
选自e、s和g;x
16
选自e、g、h、k、p、r和t;x
17
选自a、s和g;x
18
选自e、s、g和d;和x
19
选自d、n、g和s。在一些实施方式中,seq id no:7不包括氨基酸序列vsylstassld(seq id no:6)。在一些实施方式中,seq id no:6和seq id no:7包括不同的氨基酸序列。在一些实施方式中,seq id no:6和seq id no:7不相同。
[0109]
在一些实施方式中,seq id no:7包括氨基酸序列x
12
sx
20
x
21
x
15
x
16
x
22
x
23
x
24
ld(seq id no:8),其中x
12
选自d、e和v,x
20
选自d、e、g、n、q、t、v、w和y,x
21
选自a、e、h、l、n、p、q、s、t和w,x
15
选自e、s和g,x
16
选自e、g、h、k、p、r和t,x
22
选自a和g,x
23
选自e、s和d,和x
24
选自d和s。在一些实施方式中,seq id no:7由seq id no:8组成。在一些实施方式中,seq id no:7包括氨基酸序列vsx
25
x
26
stx
27
x
28
x
29
ld(seq id no:9),其中x
25
选自w、y、g、q、f、l和v,x
26
选自l、v、h和p,x
27
选自a和s,x
28
选自e、s和g,和x
29
选自n、s、d和g。在一些实施方式中,seq id no:7由seq id no:9组成。在一些实施方式中,seq id no:7由选自seq id no:97-100的序列组成。在一些实施方式中,seq id no:7由选自seq id no:97-112的序列组成。在一些实施方式中,seq id no:7由vswvstsssld(seq id no:97)组成。在一些实施方式中,seq id no:7由vswlstsgsld(seq id no:98)组成。在一些实施方式中,seq id no:7由vsgpstsgnld(seq id no:99)组成。在一些实施方式中,seq id no:7由vswlstsgnld(seq id no:100)组成。
[0110]
在一些实施方式中,seq id no:2由选自表6的序列组成。在一些实施方式中,seq id no:2由选自seq id no:37-96的序列组成。在一些实施方式中,抗体或抗原结合片段包括seq id no:7和seq id no:2由选自表6的序列组成。在一些实施方式中,抗体或抗原结合片段包括seq id no:7和seq id no:2由选自seq id no:37-96的序列组成。
[0111]
在一些实施方式中,抗体或抗原结合片段包括阿达木单抗的抗原结合结构域,其中重链的氨基酸79-88被替代。在一些实施方式中,抗体或抗原结合片段包括伊匹单抗的抗原结合结构域,其中重链的氨基酸79-88被替代。
[0112]
在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:3、seq id no:4和seq id no:10-19的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:10-19的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:10-26的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:10-26和113的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:10-26和37-96的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:10-19和37-96的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:10-26、37-96和113的
序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中重链的氨基酸79-88被选自表4的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中重链的氨基酸79-88被选自表6的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中重链的氨基酸79-88被选自表4和6的序列替代。在一些实施方式中,抗体重链的氨基酸79-88不包括seq id no:12。
[0113]
在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:3和seq id no:4的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:3、seq id no:4和seq id no:5的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:10-26的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:10-26和113的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:20-26的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:20-26和113的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:20-26的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:20-26和113的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:10-26的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:10-26和113的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被ldlqmnglgp(seq id no:113)替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自seq id no:10-26、37-96和113的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自表4的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自表6的序列替代。在一些实施方式中,抗体包括伊匹单抗的氨基酸序列,其中重链的氨基酸79-88被选自表4和6的序列替代。
[0114]
在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:7替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被选自seq id no:7和seq id no:97-100的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被选自seq id no:7和seq id no:97-112的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:7替代,并且重链的氨基酸79-88被选自表6的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:7替代,并且重链的氨基酸79-88被选自seq id no:10-26和37-96的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:7替代,并且重链的氨基酸79-88被选自seq id no:10-26、37-96和113的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:7替代,并且重链的氨基酸79-88被选自seq id no:37-96的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:7替代,并且重链的氨基酸79-88被选自表4和6的序列替代。在一些实施方式中,抗体或抗原结合结构域不包括seq id no:12。
[0115]
在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:97替代,并且氨基酸79-88被来自库3.1的表6中提供的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:98替代,并且氨基酸79-88被来自库3.2的表6中提供的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:99替代,并且氨基酸79-88被来自库3.3的表6中提供的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:100替代,并且氨基酸79-88被来自库3.4的表6中提供的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:97替代,并且氨基酸79-88被选自seq id no:37-54的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:98替代,并且氨基酸79-88被选自seq id no:38、47、49和55-74的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:99替代,并且氨基酸79-88被选自seq id no:37、40、43、46和74-93的序列替代。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中氨基酸99-109被seq id no:100替代,并且氨基酸79-88被选自seq id no:37-38、42-43、46-47、49、70-71和94-96的序列替代。
[0116]
在一些实施方式中,阿达木单抗的重链的氨基酸序列是evqlvesggglvqpgrslrlscaasgftfddyamhwvrqapgkglewvsaitwnsghidyadsvegrftisrdnaknslylqmnslraedtavyycakvsylstassldywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrd(seq id no:127)。在一些实施方式中,阿达木单抗的轻链的氨基酸序列是diqmtqspsslsasvgdrvtitcrasqgirnylawyqqkpgkapklliyaastlqsgvpsrfsgsgsgtdftltisslqpedvatyycqrynrapytfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgeceltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:128)。在一些实施方式中,具有降低的免疫原性的阿达木单抗的重链包括seq id no:131或由其组成。在一些实施方式中,具有降低的免疫原性的阿达木单抗的重链包括seq id no:132或由其组成。在一些实施方式中,具有降低的免疫原性的阿达木单抗的重链包括seq i d no:133或由其组成。
[0117]
在一些实施方式中,伊匹单抗的重链的氨基酸序列是qvqlvesgggvvqpgrslrlscaasgftfssytmhwvrqapgkglewvtfisydgnnkyyadsvkgrftisrdnskntlylqmnslraedtaiyycartgwlgpfdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkrvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:129)。在一些实施方式中,伊匹单抗的轻链的氨基酸序列是eivltqspgtlslspgeratlscrasqsvgssylawyqqkpgqaprlliygafsratgipdrfsgsgsgtdftltisrlepedfavyycqqygsspwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacev
thqglsspvtksfnrgec(seq id no:130)。在一些实施方式中,具有降低的免疫原性的伊匹单抗的重链包括qvqlvesgggvvqpgrslrlscaasgftfssytmhwvrqapgkglewvtfisydgnnkyyadsvkgrftisrdnskntlx1lx2mnx3lx4x5edtaiyycartgwlgpfdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkrvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:134)或由其组成。在一些实施方式中,seq id no:134不包括seq id no:1。
[0118]
在一些实施方式中,包括用seq id no:2替代seq id no:1的抗体或抗原结合片段选自表2。表2中的所有抗体都包含seq id no:1,并且因此由于免疫原性降低,表2中的所有抗体都将受益于seq id no:1到seq id no:2的转化。实际上,任何含有seq id no:1的抗体(只要它不在cdr中)都会受益于seq id no:1到seq id no:2的转化。
[0119]
表2:fw3中含有免疫原性核心hc:79:88的临床治疗ab列表
[0120]
[0121]
[0122][0123]
在一些实施方式中,抗体包括已知抗体的序列,其中seq id no:1被seq id no:2替代。在一些实施方式中,抗体包括用seq id no:2替代seq id no:1。在一些实施方式中,包括用seq id no:2替代seq id no:1的抗体选自:阿法西库单抗、阿达木单抗、苏替木单抗、壬托鲁单抗、特雷克单抗、埃罗妥珠单抗、比美克珠单抗、索非妥珠单抗、洛利昔珠单抗、拉那鲁单抗、苏维妥昔单抗、戈奈单抗、伊匹单抗、度匹鲁单抗、依法利珠单抗、弗洛西单抗、依玛鲁单抗、阿利库单抗、英克勒库单抗、克罗特度单抗、阿维鲁单抗、奥匹努单抗、艾米珠单抗、杜伐鲁单抗、索拉尼单抗、雷莫卢单抗、托维单抗、帕妥珠单抗、舒他伏单抗、奈伐苏单
抗、奎利珠单抗、布拉齐单抗、地诺单抗、伐立鲁单抗、曲美木单抗、伊妥珠单抗、罗妥木单抗、普瑞鲁单抗、prasinezumab、帕诺库单抗、奥替利单抗、奥昔组单抗、奥索西单抗、莫星-洛沃妥珠单抗、来沙木单抗、艾芦库单抗、fremanexumab、埃吉姆单抗、daratumumb、corncizumab、巴匹珠单抗和安芦珠单抗。在一些实施方式中,包括用seq id no:2替代seq id no:1的抗体选自阿达木单抗或伊匹单抗。
[0124]
另一方面,提供了包括seq id no:7的抗体或抗原结合片段。
[0125]
在一些实施方式中,抗体或抗原结合片段的重链包括seq id no:7。在一些实施方式中,seq id no:7是抗体或抗原结合片段的重链的氨基酸99-109。在一些实施方式中,seq id no:7不是seq id no:6。
[0126]
在一些实施方式中,抗体是阿达木单抗(修美乐(humira))。在一些实施方式中,抗体包括阿达木单抗的氨基酸序列,其中阿达木单抗的重链的氨基酸99-109已被seq id no:7替代。在一些实施方式中,抗体或抗原结合片段包括阿达木单抗的抗原结合结构域,其中重链的氨基酸99-109已被seq id no:7替代。
[0127]
在一些实施方式中,抗体或抗原结合片段进一步包括seq id no:2。在一些实施方式中,抗体或抗原结合片段的氨基酸79-88是seq id no:2。
[0128]
另一方面,提供了包括三条重链cdr(cdr-h)和三条轻链cdr(cdr-l)的抗体或其抗原结合片段,其中:
[0129]
cdr-h1包括seq id no:114(dyamh)中所列的氨基酸序列,cdr-h2包括如seq id no:115(aitw)中所列的氨基酸序列,cdr-h3包括如seq id no:116(x
12
sx
13
x
14
x
15
x
16
x
17
x
18
x
19
ldx
30
)所列的氨基酸序列且不包括seq id no:6,cdr-l1包括如seq id no:117(rasqgirnyla)中所列的氨基酸序列,cdr-l2包括如seq id no:118(aastlqs)中所列的氨基酸序列,并且cdr-l3包括如seq id no:119(qrynrapyx
31
)中所列的氨基酸序列,其中
[0130]
x
12
选自d、e和v,
[0131]
x
13
选自d、e、g、n、q、t、v、w、f、l和y,
[0132]
x
14
选自a、e、h、l、n、p、q、s、t、v和w,
[0133]
x
15
选自e、s和g,
[0134]
x
16
选自e、g、h、k、p、r和t,
[0135]
x
17
选自a、s和g,
[0136]
x
18
选自e、s、g和d,
[0137]
x
19
选自d、n、g和s,
[0138]
x
30
选自y和n,
[0139]
x
31
选自t和a。
[0140]
在一些实施方式中,抗体或抗原结合片段结合tnfa。在一些实施方式中,抗体与阿达木单抗相当地结合tnfa。在一些实施方式中,抗体或抗原结合片段是具有降低的免疫原性的修饰的阿达木单抗。在一些实施方式中,抗体或抗原结合片段是具有修饰的cdr-h3的阿达木单抗。
[0141]
在一些实施方式中,cdr-l3由seq id no:120(qrynrapyt)组成。在一些实施方式中,cdr-l3由seq id no:124(qrynrapya)组成。
[0142]
在一些实施方式中,cdr-h3包括seq id no:121(x
12
sx
13
x
14
x
15
x
16
x
17
x
18
x
19
ld y)。在一些实施方式中,cdr-h3包括seq id no:125(x
12
sx
13
x
14
x
15
x
16
x
17
x
18
x
19
ld n)。在一些实施方式中,seq id no:116包括x
12
sx
20
x
21
x
15
x
16
x
22
x
23
x
24
ldx
31
(seq id no:122),其中
[0143]
x
12
选自d、e和v,
[0144]
x
20
选自d、e、g、n、q、t、v、w和y,
[0145]
x
21
选自a、e、h、l、n、p、q、s、t和w,
[0146]
x
15
选自e、s和g,
[0147]
x
16
选自e、g、h、k、p、r和t,
[0148]
x
22
选自a和g,
[0149]
x
23
选自e、s和d,
[0150]
x
24
选自d和s,和
[0151]
x
31
选自t和a。
[0152]
在一些实施方式中,seq id no:116包括vsx
25
x
26
stx
27
x
28
x
29
ld x
31
(seq id no:123),其中
[0153]
x
25
选自w、y、g、q、f、l和v,
[0154]
x
26
选自l、v、h和p,
[0155]
x
27
选自a和s,
[0156]
x
28
选自e、s和g,
[0157]
x
29
选自n、s、d和g,
[0158]
x
31
选自t和a。
[0159]
在一些实施方式中,seq id no:116由选自seq id no:97-112的氨基酸序列组成。
[0160]
在一些实施方式中,抗体或抗原结合片段的重链选自表1。在一些实施方式中,抗体或抗原结合片段的重链选自seq id no:27-36。在一些实施方式中,抗体或抗原结合片段的重链包括选自表1的序列。在一些实施方式中,抗体或抗原结合片段的重链包括选自seq id no:27-36的序列。
[0161]
在一些实施方式中,抗体或抗原结合片段进一步包括seq id no:2。在一些实施方式中,抗体或抗原结合片段包括用seq id no:2替代seq id no:1。
[0162]
在一些实施方式中,抗体或抗原结合片段的轻链包括seq id no:128或由其组成。在一些实施方式中,抗体或抗原结合片段的重链包括seq id no:127,其中seq id n o:1已被seq id no:2替代。在一些实施方式中,抗体或抗原结合片段的重链包括seq id no:127,其中seq id no:6已被seq id no:7替代。在一些实施方式中,抗体或抗原结合片段的重链包括seq id no:127,其中seq id no:1已被seq id no:2替代和seq id no:6已被seq id no:7替代。
[0163]
在一些实施方式中,抗体或抗原结合片段的重链包括evqlvesggglvqpgrslrlscaasgftfddyamhwvrqapgkglewvsaitwnsghidyadsvegrftisrdnaknslx1lx2mnx3lx4x5edtavyycakvsylstassldywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrd(seq id no:131)或由其组成。在一些实施方式
中,抗体或抗原结合片段的重链包括evqlvesggglvqpgrslrlscaasgftfddyamhwvrqapgkglewvsaitwnsghidyadsvegrftisrdnaknslylqmnslraedtavyycakx
12
sx
13
x
14
x
15
x
16
x
17
x
18
x
19
ldywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrd(seq id no:132)或由其组成。在一些实施方式中,抗体或抗原结合片段的重链包括evqlvesggglvqpgrslrlscaasgftfddyamhwvrqapgkglewvsaitwnsghidyadsvegrftisrdnaknslx1lx2mnx3lx4x5edtavyycakx
12
sx
13
x
14
x
15
x
16
x
17
x
18
x
19
ldywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrd(seq id no:133)或由其组成。
[0164]
在一些实施方式中,抗体或抗原结合片段结合肿瘤坏死因子α(tnfa)。
[0165]
另一方面,提供了一种抗体或抗原结合片段,其包括包含seq id no:133且不包含seq id no:1的重链。
[0166]
在一些实施方式中,抗体或抗原结合片段包括包含seq id no:128的轻链。在一些实施方式中,重链包括seq id no:131。在一些实施方式中,seq id no:133包括seq id no:2。在一些实施方式中,seq id no:133包括seq id no:3。在一些实施方式中,seq id no:133包括seq id no:4。在一些实施方式中,seq id no:133包括seq id no:5。在一些实施方式中,seq id no:131包括seq id no:2、3、4或5。每种可能性代表本发明的单独实施方式。在一些实施方式中,seq id no:2、3、4或5是seq id no:133的氨基酸79-88。在一些实施方式中,seq id no:2、3、4或5是seq id no:131的氨基酸79-88。在一些实施方式中,seq id no:133包括选自seq id no:10-26、37-96和113的序列。在一些实施方式中,seq id no:131包括选自seq id no:10-26、37-96和113的序列。在一些实施方式中,选自seq id no:10-26、37-96和113的序列是seq id no:133的氨基酸79-88。在一些实施方式中,选自seq id no:10-26、37-96和113的序列是seq id no:131的氨基酸79-88。
[0167]
在一些实施方式中,抗体或抗原结合片段结合肿瘤坏死因子α(tnfa)。
[0168]
另一方面,提供了一种抗体或抗原结合片段,其包括包含seq id no:134且不包含seq id no:1的重链。
[0169]
在一些实施方式中,具有降低的免疫原性的伊匹单抗包括轻链,该轻链包括seq id no:130或由其组成。在一些实施方式中,抗体或抗原结合片段包括轻链,该轻链包括seq id no:130或由其组成。
[0170]
在一些实施方式中,seq id no:134包括seq id no:2。在一些实施方式中,seq id no:134包括seq id no:3。在一些实施方式中,seq id no:134包括seq id no:4。在一些实施方式中,seq id no:134包括seq id no:5。在一些实施方式中,seq id no:2、3、4或5是seq id no:134的氨基酸79-88。在一些实施方式中,seq id no:134包括选自seq id no:10-26、37-96和113的序列。在一些实施方式中,选自seq id no:10-26、37-96和113的序列是seq id no:134的氨基酸79-88。
[0171]
在一些实施方式中,抗体或抗原结合片段结合细胞毒性t淋巴细胞相关蛋白4
(ctla4)。
[0172]
另一方面,提供了一种药物组合物,其包括本发明的多肽。
[0173]
另一方面,提供了一种药物组合物,其包括本发明的抗体或抗原结合片段。
[0174]
在一些实施方式中,药物组合物进一步包括药学上可接受的载体、赋形剂或佐剂。如本文所使用的,术语“载体”、“赋形剂”或“佐剂”是指药物组合物中不是活性剂的任何组分。如本文所使用的,术语“药学上可接受的载体”是指无毒、惰性固体、半固体液体填充剂、稀释剂、包封材料、任何类型的制剂助剂,或简单的无菌水性介质,比如盐水。可以用作药学上可接受的载体的材料的一些实例是糖,例如乳糖、葡萄糖和蔗糖,淀粉例如玉米淀粉和马铃薯淀粉,纤维素及其衍生物例如羧甲基纤维素钠、乙基纤维素和醋酸纤维素;粉状黄蓍胶;麦芽、明胶、滑石粉;赋形剂,例如可可脂和栓剂蜡;油类比如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;二醇类比如丙二醇,多元醇类,例如甘油、山梨糖醇、甘露糖醇和聚乙二醇;酯类如油酸乙酯和月桂酸乙酯,琼脂;缓冲剂比如氢氧化镁和氢氧化铝;海藻酸;无热原水;等渗盐水,林格溶液(ringer's solution);乙醇和磷酸盐缓冲溶液,以及药物制剂中使用的其他无毒相容物质。可用作本文载体的物质的一些非限制性实例包括糖、淀粉、纤维素及其衍生物、粉末黄蓍胶、麦芽、明胶、滑石、硬脂酸、硬脂酸镁、硫酸钙、植物油、多元醇、海藻酸、无热原水、等渗盐水、磷酸盐缓冲溶液、可可脂(栓剂基体)、乳化剂以及用于其他药物制剂的其他无毒药物相容物质。还可能存在润湿剂和润滑剂比如十二烷基硫酸钠,以及着色剂、调味剂、赋形剂、稳定剂、抗氧化剂和防腐剂。任何无毒、惰性和有效的载体都可用于配制本文所考虑的组合物。在这方面合适的药学上可接受的载体、赋形剂和稀释剂是本领域技术人员众所周知的,比如在merck index,第十三版,budavari等人,eds.,merck&co.,inc.,rahway,n.j.(2001);the ctfa(cosmetic,toiletry,and fragrance association)international cosmetic ingredient dictionary and handbook,第十版(2004);和“inactive ingredient guide,”u.s.food and drug administration(fda)center for drug evaluation and research(cder)office of management中描述的那些,所有这些内容通过引用以其整体并入本文。可用于本发明组合物的药学上可接受的赋形剂、载体和稀释剂的实例包括蒸馏水、生理盐水、林格溶液、葡萄糖溶液、汉克溶液和dmso。这些额外的非活性成分以及有效的制剂和施用程序在本领域中是众所周知的,并且在标准教科书中进行了描述,比如goodman和gillman’s:the pharmacological bases of therapeutics,第8版,gilman等人,eds.pergamon press(1990);remington’s pharmaceutical sciences,第18版,mack publishing co.,easton,pa.(1990);和remington:the science and practice of pharmacy,第21版,lippincott williams&wilkins,philadelphia,pa.,(2005),其每一篇通过引用以其整体并入本文。目前描述的组合物也可以包含在人工产生的结构中,比如脂质体、iscoms、缓释颗粒和其他增加血清中的肽或多肽半衰期的载体。脂质体包括乳液、泡沫、胶束、不溶性单层、液晶、磷脂分散体、层状层等。与目前描述的肽一起使用的脂质体由标准囊泡形成的脂质形成,该脂质通常包括中性和带负电荷的磷脂和固醇,比如胆固醇。脂质的选择通常由诸如脂质体大小和血液中的稳定性等因素决定。有多种方法可用于制备脂质体,如coligan,j.e等人,current protocols in protein science,1999,john wiley&sons,inc.,new york中所综述的,并且还参见美国专利号4,235,871、4,501,728、4,837,028和5,019,369。
[0175]
载体总共可以占本文所述的药物组合物重量的约0.1%至约99.99999%
[0176]
在一些实施方式中,药物组合物被配制用于施用于受试者。在一些实施方式中,药物组合物被配制用于全身施用。在一些实施方式中,受试者是哺乳动物。在一些实施方式中,受试者是人。
[0177]
如本文所使用的,术语“施用(administering)”、“施用(administration)”和类似术语是指在合理的医学实践中以提供治疗效果的方式将含有活性剂的组合物递送至受试者的任何方法。在一些实施方式中,施用是向有需要的患者施用治疗有效量的本主题的组合物。合适的施用途径可以包括口服、肠胃外、皮下、静脉内、肌肉内或腹膜内。
[0178]
施用的剂量将取决于接受者的年龄、健康和体重、同时治疗的种类(如果有的话)、治疗的频率以及期望的效果的性质。
[0179]
另一方面,提供了一种从第一抗体产生第二抗体的方法,该方法包括:
[0180]
a.提供包括编码所述第一抗体的氨基酸序列的编码序列的第一核酸分子,其中所述氨基酸序列包括seq id no:1;
[0181]
b.提供编码第二抗体的氨基酸序列的第二核酸分子,其中所述氨基酸序列包括seq id no:2,而不是seq id no:1;和
[0182]
c.由第二核酸分子产生第二抗体;
[0183]
从而由第一抗体产生第二抗体。
[0184]
在一些实施方式中,该方法是用于产生与第一抗体相比具有降低的免疫原性的第二抗体的方法。在一些实施方式中,该方法用于降低抗体的免疫原性。在一些实施方式中,产生第二抗体包括降低第一抗体的免疫原性。
[0185]
在一些实施方式中,降低的免疫原性包括降低至少5、10、20、25、30、40、50、60、70、75、80、85、90、95、97、99或100%。每种可能性代表本发明的单独实施方式。在一些实施方式中,该方法进一步包括确认第二抗体的免疫原性降低。在一些实施方式中,通过计算免疫原性评分来测量免疫原性。计算免疫原性在本领域中是众所周知的,并且许多程序可用于该计算。计算免疫原性的方法可以在下文的方法部分中找到。
[0186]
在一些实施方式中,提供第二核酸分子包括选择第一核酸分子并将编码seq id no:1的序列替代为编码seq id no:2的序列。在一些实施方式中,除了编码seq id no:1和seq id no:2的区域之外,第二核酸分子与所述第一核酸分子相同。在一些实施方式中,除了seq id no:1和seq id no:2区域之外,第二核酸分子编码与由第一核酸分子编码的氨基酸序列相同的氨基酸序列。在一些实施方式中,替代是突变。在一些实施方式中,替代是生成新序列。在一些实施方式中,序列在电子文件中。在一些实施方式中,该方法是计算机化方法。
[0187]
在一些实施方式中,第二抗体的重链包含seq id no:2。在一些实施方式中,seq id no:2是第二抗体的重链的氨基酸79-88。在一些实施方式中,第一抗体的重链包含seq id no:1。在一些实施方式中,seq id no:1是第一抗体重链的氨基酸79-88。在一些实施方式中,seq id no:1不在第一抗体的cdr中。在一些实施方式中,seq id no:1不与第一抗体的cdr重叠。在一些实施方式中,seq id no:1不在决定第一抗体结合的区域中。在一些实施方式中,seq id no:1不与决定第一抗体结合的区域重叠。
[0188]
在一些实施方式中,核酸分子是载体。在一些实施方式中,核酸分子是表达载体。
在一些实施方式中,表达载体被配置用于在靶细胞中表达抗体。在一些实施方式中,编码抗体的区域与至少一种调节元件可操作地连接。在一些实施方式中,调节元件被配置用于在靶细胞中表达抗体。在一些实施方式中,元件是启动子。在一些实施方式中,所述产生包括培养包括载体的宿主细胞。在一些实施方式中,所述产生包括在宿主细胞中表达抗体。
[0189]
在细胞内表达编码抗体的核酸分子是本领域技术人员众所周知的。它可以通过转染、病毒感染或直接改变细胞基因组等许多方法来进行。在一些实施方式中,该基因在诸如质粒或病毒载体的表达载体中。含有p16-ink4a的表达载体的一个这样的实例是可获自addgene的哺乳动物表达载体pcmv p16 ink4a。
[0190]
载体核酸序列通常至少包含用于在细胞中繁殖的复制起点和任选的附加元件,比如异源多核苷酸序列、表达控制元件(例如,启动子、增强子)、选择标记(例如,抗生素抗性)、聚腺嘌呤序列。
[0191]
载体可以是经由非病毒方法或经由病毒方法递送的dna质粒。病毒载体可以是逆转录病毒载体、疱疹病毒载体、腺病毒载体、腺相关病毒载体或痘病毒载体。启动子可以在哺乳动物细胞中具有活性。启动子可以是病毒启动子。
[0192]
术语“可操作地连接”旨在表示感兴趣的核苷酸序列以允许核苷酸序列表达的方式(例如在体外转录/翻译系统中或当将载体引入宿主细胞时在宿主细胞中)连接至一个或多个调节元件。
[0193]
在一些实施方式中,通过标准方法将载体引入细胞,包括电穿孔(例如,如from等人,proc.natl.acad.sci.usa 82,5824(1985)中所述)、热休克、病毒载体感染、小颗粒高速弹道穿透小珠或颗粒基质内或表面上的核酸(klein等人,nature 327.70-73(1987))等。
[0194]
如本文所使用的,术语“启动子”是指一组转录控制模块,它们聚集在rna聚合酶即rna聚合酶ii的起始位点周围。启动子由离散的功能模块组成,每个模块由大约7-20bp的dna组成,并且含有一个或多个转录激活蛋白或阻遏蛋白的识别位点。
[0195]
在一些实施方式中,核酸序列由rna聚合酶ii(rnap ii和pol ii)转录。rnap ii是一种存在于真核细胞中的酶。它催化dna的转录以合成mrna和大多数snrna和microrna的前体。
[0196]
在一些实施方式中,哺乳动物表达载体包括但不限于可获得自invitrogen的pcdna3、pcdna3.1(
±
)、pgl3、pzeosv2(
±
)、psectag2、pdisplay、pef/myc/cyto、pcmv/myc/cyto、pcr3.1、psinrep5、dh26s、dhbb、pnmt1、pnmt41、pnmt81,可获得自promega的pci,可获得自strategene的pmbac、ppbac、pbk-rsv和pbk-cmv,可获得自clontech的ptres,及其衍生物。
[0197]
在一些实施方式中,本发明使用含有来自真核病毒比如逆转录病毒的调节元件的表达载体。sv40载体包括psvt7和pmt2。在一些实施方式中,源自牛乳头状瘤病毒的载体包括pbv-1mtha,和源自epstein bar病毒的载体包括phebo和p2o5。其他示例性载体包括pmsg、pav009/a+、pmto10/a+、pmamneo-5、杆状病毒pdsve和任何其他允许在sv-40早期启动子、sv-40晚期启动子、金属硫蛋白启动子、鼠乳腺肿瘤病毒启动子、劳斯肉瘤病毒启动子、多角体蛋白启动子或其他显示对在真核细胞中表达有效的启动子的指导下表达蛋白质的载体。
[0198]
在一些实施方式中,提供诸如横向感染和靶向特异性等优点的重组病毒载体用于
体内表达。在一个实施方式中,横向感染在例如逆转录病毒的生命周期中是固有的,并且是单个受感染细胞产生许多子代病毒粒子的过程,这些子代病毒粒子萌芽并感染相邻细胞。在一个实施方式中,结果是大面积被迅速感染,其中大部分最初没有被原始病毒粒子感染。在一个实施方式中,产生了不能横向扩散的病毒载体。在一个实施方式中,如果期望的目的是将特定基因引入仅局部数量的靶细胞中,则该特征可能是有用的。
[0199]
可以使用多种方法将本发明的表达载体引入细胞中。这种方法通常描述于sambrook等人,molecular cloning:a laboratory manual,cold springs harbor laboratory,new york(1989,1992);ausubel等人,current protocols in molecular biology,john wiley and sons,baltimore,md.(1989);chang等人,somatic gene therapy,crc press,ann arbor,mich.(1995);vega等人,gene targeting,crc press,ann arbor mich.(1995),vectors:a survey of molecular cloning vectors and their uses,butterworths,boston mass.(1988)和gilboa等人,[biotechniques 4(6):504-512,1986]中,并且包括例如稳定或瞬时转染、脂转染、电穿孔和重组病毒载体感染。此外,正负选择方法参见美国专利号5,464,764和5,487,992。
[0200]
应当理解,除了包含插入的编码序列(编码多肽)的转录和翻译所必需的元件之外,本发明的表达构建体还可以包括经工程改造以优化稳定性、生产、纯化、表达的多肽的产量或活性。
[0201]
在一些实施方式中,本发明的方法进一步包括测量第二抗体与第一抗体的靶标或表位的结合。在一些实施方式中,本发明的方法进一步包括确认第二抗体与第一抗体的靶标或表位的结合。在一些实施方式中,本发明的方法进一步包括选择具有与第一抗体相当的与靶标或表位结合的抗体。在一些实施方式中,通过结合测定来测量与靶标或表位的结合。在一些实施方式中,结合测定是facs测定。在一些实施方式中,通过结合测定测量产生结合值。在一些实施方式中,结合值是结合的表位或靶标的百分比,即表达结合的靶蛋白的细胞数。在一些实施方式中,结合的亲和力是结合值。在一些实施方式中,ec50是结合值。
[0202]
在一些实施方式中,第二抗体的结合值是第一抗体的结合值的至少50、55、60、65、70、75、80、85、90、95、97、99或100%。每种可能性代表本发明的单独实施方式。在一些实施方式中,与第一抗体相比,第二抗体具有小于20、15、10、9、8、7、6、5、4、3、2或1%的降低的结合。每种可能性代表本发明的单独实施方式。在一些实施方式中,第一和第二抗体结合的facs直方图是相当的。
[0203]
在一些实施方式中,第一抗体选自表2。在一些实施方式中,第一抗体选自:阿法西库单抗、阿达木单抗、苏替木单抗、壬托鲁单抗、特雷克单抗、埃罗妥珠单抗、比美克珠单抗、索非妥珠单抗、洛利昔珠单抗、拉那鲁单抗、苏维妥昔单抗、戈奈单抗、伊匹单抗、度匹鲁单抗、依法利珠单抗、弗洛西单抗、依玛鲁单抗、阿利库单抗、英克勒库单抗、克罗特度单抗、阿维鲁单抗、奥匹努单抗、艾米珠单抗、杜伐鲁单抗、索拉尼单抗、雷莫卢单抗、托维单抗、帕妥珠单抗、舒他伏单抗、奈伐苏单抗、奎利珠单抗、布拉齐单抗、地诺单抗、伐立鲁单抗、曲美木单抗、伊妥珠单抗、罗妥木单抗、普瑞鲁单抗、prasinezumab、帕诺库单抗、奥替利单抗、奥昔组单抗、奥索西单抗、莫星-洛沃妥珠单抗、来沙木单抗、艾芦库单抗、fremanexumab、埃吉姆单抗、daratumumb、corncizumab、巴匹珠单抗和安芦珠单抗。在一些实施方式中,第一抗体选自阿达木单抗或伊匹单抗。
[0204]
如本文所使用的,术语“抗体”是指包含至少一个结合结构域的多肽或多肽组,该结合结构域由具有三维结合空间的多肽链折叠形成,其中内表面形状和电荷分布与抗原的抗原决定簇的特征(feature)互补。抗体通常具有四聚体形式,包括两对相同的多肽链,每对具有一条“轻”链和一条“重”链。每个轻/重链对的可变区形成抗体结合位点。抗体可以是寡克隆的、多克隆的、单克隆的、嵌合的、骆驼化的(camelised)、cdr移植的、多特异性的、双特异性的、催化的、人源化的、完全人的、抗独特型的,以及可以以可溶性或结合形式标记的抗体以及片段,包括其单独或与其他氨基酸序列组合的表位结合片段、变体或衍生物。抗体可以来自任何物种。术语抗体还包括结合片段,包括但不限于fv、fab、fab'、f(ab')2单链抗体(svfc)、二聚体可变区(双抗体)和二硫键连接的可变区(dsfv)。具体而言,抗体包括免疫球蛋白分子和免疫球蛋白分子的免疫活性片段,即,含有抗原结合位点的分子。抗体片段可以融合或不融合至另一个免疫球蛋白结构域,包括但不限于fc区或其片段。本领域技术人员将进一步理解,可以产生其他融合产物,包括但不限于scfv-fc融合体、可变区(例如,vl和vh)-fc融合体和scfv-scfv-fc融合体。
[0205]
免疫球蛋白分子可以是任何类型(例如,igg、ige、igm、igd、iga和igy)、类别(例如,iggl、igg2、igg3、igg4、iga1和iga2)或亚类。在一些实施方式中,抗体包括igg2或igg4。在一些实施方式中,抗体包括igg2。在一些实施方式中,抗体包括igg4。
[0206]
天然存在的抗体结构的基本单元是约150,000道尔顿的异四聚体糖蛋白复合物,由通过非共价缔合且通过二硫键连接在一起的两条相同的轻(l)链和两条相同的重(h)链组成。每条重链和轻链还具有规则间隔的链内二硫桥键。存在五种人类抗体类别(igg、iga、igm、igd和ige),并且在这些类别中,基于结构差异比如单个抗体分子中免疫球蛋白单元的数量、单个单元的二硫键结构以及链长和序列的差异识别出各种亚类。抗体的类别和亚类是其同种型。
[0207]
重链和轻链的氨基末端区域在序列上比羧基末端区域更多样化,并且因此被称为可变结构域。抗体结构的这一部分赋予了抗体的抗原结合特异性。重可变(vh)结构域和轻可变(vl)结构域一起形成单个抗原结合位点,因此,基本免疫球蛋白单元具有两个抗原结合位点。认为特定的氨基酸残基在轻链和重链可变结构域之间形成界面(chothia等人,j.mol.biol.186,651-63(1985);novotny和haber,(1985)proc.natl.acad.sci.usa 82 4592-4596)。
[0208]
重链和轻链的羧基末端部分形成恒定结构域,即,ch1、ch2、ch3、cl。虽然这些结构域的多样性要少得多,但是在动物物种之间相互存在差异,并且此外,在同一个体中有几种不同的抗体同种型,每种具有不同的功能。
[0209]
术语“框架区”或“fr”是指抗体可变结构域中的氨基酸残基,其不同于本文定义的高变区氨基酸残基。如本文所使用的,术语“高变区”是指抗体可变结构域中负责抗原结合的氨基酸残基。高变区包括来自“互补决定区”或“cdr”的氨基酸残基。cdr主要负责与抗原的表位结合。fr和cdr的范围已被精确定义(参见kabat等人)。
[0210]
还可以使用imgt信息系统(www://imgt.cines.fr/)(/v-quest)分析免疫球蛋白可变结构域以鉴定可变区片段,包括cdr。参见,例如,brochet,x等人,nucl.acids res.j6:w503-508(2008)。
[0211]
chothia等人还定义了适用于任何抗体的可变结构域序列的编号系统。本领域普
通技术人员可以明确地将这种“chothia编号”系统分配给任何可变结构域序列,而不依赖于序列本身之外的任何实验数据。如本文所使用的,“chothia编号”是指由chothia等人,journal of molecular biology,"canonical structures for the hypervariable regions of immunoglobulins"(1987)和chothia等人,nature,“conformations of immunoglobulin hypervariable regions”所陈述的编号系统。
[0212]
如本文所使用的,术语“人源化抗体”是指来自非人类物种的抗体,其蛋白质序列已被修饰以增加与人类抗体的相似性。人源化抗体可以通过产生编码被类似人类抗体的序列包围的非人类抗体的cdr的重组dna而产生。在一些实施方式中,人源化抗体是嵌合抗体。在一些实施方式中,人源化包括将本发明的cdr插入人类抗体支架或骨架中。人源化抗体在本领域中是众所周知的,并且可以使用任何产生它们的保留本发明的cdr的方法。
[0213]
如本文所使用的,术语“单克隆抗体”或“mab”是指从基本上同质的抗体群体中获得的抗体,即构成该群体的个体抗体是相同的和/或结合相同的表位,除非可能在单克隆抗体生产过程中可能出现的变体,这种变体通常以少量存在。与通常包括针对不同决定簇(表位)的不同抗体的多克隆抗体制剂相比,每种单克隆抗体针对抗原上的单个决定簇。除了它们的特异性之外,单克隆抗体的优势在于它们不受其他免疫球蛋白的污染。修饰语“单克隆”表示抗体的特征是从基本上同质的抗体群体中获得的,并且不应解释为通过任何特定的制备方法产生。根据本文提供的方法使用的单克隆抗体可以通过由kohler等人,nature256:495(1975)中首次描述的杂交瘤方法制备,或者可以通过重组dna方法制备(参见,例如,美国专利号4,816,567)。“单克隆抗体”还可以使用例如clackson等人,nature 352:624-628(1991)和marks等人,j.mol.biol.222:581-597(1991)中描述的技术从噬菌体抗体库分离。
[0214]
本发明的mab可以是任何免疫球蛋白类别,包括igg、igm、igd、ige或iga。可以在体外或体内培养产生mab的杂交瘤。可以在体内生产中获得高滴度的mab,其中将来自单个杂交瘤的细胞腹膜内注射到原始的balb/c小鼠中,以产生含有高浓度所需mab的腹水。可以使用本领域技术人员众所周知的柱色谱方法从这种腹水或培养上清液中纯化同种型igm或igg的mab。
[0215]“抗体片段”包括完整抗体的一部分,优选地包括其抗原结合区。抗体片段的实例包括fab、fab'、f(ab')2和fv片段;双抗体;串联双抗体(tadb)、线性抗体(例如,美国专利号5,641,870,实施例2;zapata等人,protein eng.8(10):1057-1062(1995));单臂抗体、单可变结构域抗体、微抗体、单链抗体分子;由抗体片段(例如,包括但不限于db-fc、tadb-fc、tadb-ch3、(scfv)4-fc、di-scfv、bi-scfv或串联(di,tri)-scfv)形成的多特异性抗体;和双特异性t细胞接合剂(bite)。
[0216]
抗体的木瓜蛋白酶消化产生两个相同的抗原结合片段,称为“fab”片段,每个片段具有单个抗原结合位点,以及残留的“fc”片段,其名称反映了其容易结晶的能力。胃蛋白酶处理产生具有两个抗原结合位点并且仍然能够交联抗原的f(ab')2片段。
[0217]“fv”是包含完整抗原识别和抗原结合位点的最小抗体片段。该区域由紧密、非共价结合的一条重链和一条轻链可变结构域的二聚体组成。其为vh-vl二聚体的三个表面的这种构型。六个高变区共同赋予抗体抗原结合特异性。然而,即使是单个可变结构域(或仅包括对抗原特异的三个高变区的fv的一半)也具有识别和结合抗原的能力,尽管亲和力低
于整个结合位点。
[0218]
fab片段还包含轻链的恒定结构域和重链的第一恒定结构域(ch1)。fab'片段与fab片段的不同之处在于在重链ch1结构域的羧基末端添加了几个残基,包括来自抗体铰链区的一个或多个半胱氨酸。fab'-sh是本文对fab'的名称,其中恒定结构域的半胱氨酸残基(一个或多个)带有至少一个游离硫醇基团。f(ab')2抗体片段最初是作为在其之间具有铰链半胱氨酸的成对的fab'片段产生的。抗体片段的其他化学偶联也是已知的。
[0219]
来自任何脊椎动物物种的抗体(免疫球蛋白)的“轻链”可以基于其恒定结构域的氨基酸序列被归为两种明显不同的类型之一,称为κ和λ。
[0220]
根据其重链恒定结构域的氨基酸序列,可以将抗体分配到不同的类别。完整抗体有五种主要类别:iga、igd、ige、igg和igm,并且其中一些可进一步分为亚类(同种型),例如iggl、igg2、igg3、igg4、iga和iga2。对应于不同类别抗体的重链恒定结构域分别称为a、δ、e、γ和μ(micro)。不同类别的免疫球蛋白的亚基结构和三维构型是众所周知的。
[0221]“单链fv”或“scfv”抗体片段包括抗体的vh和vl结构域,其中这些结构域存在于单个多肽链中。在一些实施方式中,fv多肽进一步包括位于vh和vl结构域之间的多肽接头,其使得scfv能够形成用于抗原结合的所需结构。有关scfv的评论,请参阅pluckthun in the pharmacology of monoclonal antibodies,vol.113,rosenburg和moore eds.,springer-verlag,new york,pp.269-315(1994)。
[0222]
术语“双抗体”是指具有两个抗原结合位点的小抗体片段,该片段包括与同一多肽链(vh-vl)中的轻链可变结构域(vl)连接的重链可变结构域(vh))。通过使用太短而无法在同一条链上的两个结构域之间配对的接头,这些结构域被迫与另一条链的互补结构域配对并产生两个抗原结合位点。双抗体生产在本领域中是已知的并且描述于natl.acad.sci.usa,90:6444-6448(1993)。
[0223]
术语“多特异性抗体”以最广含义使用,并且具体涵盖具有多表位特异性的抗体。这种多特异性抗体包括但不限于包含重链可变结构域(vh)和轻链可变结构域(vl)的抗体(其中vhvl单元具有多表位特异性)、具有两个或更多个vl和vh结构域的抗体(其中每个vhvl单元与不同的表位结合)、具有两个或多个单可变结构域的抗体(其中每个单可变结构域与不同的表位结合)、全长抗体、抗体片段比如fab、fv、dsfv、scfv、双抗体、双特异性双抗体、三抗体,三功能抗体、共价或非共价连接的抗体片段。“多表位特异性”是指特异性结合相同或不同靶标(一个或多个)上的两个或更多个不同表位的能力。
[0224]
本发明的单克隆抗体可以使用本领域熟知的方法制备。实例包括各种技术,比如kohler,g.和milstein,c,nature 256:495-497(1975);kozbor等人,immunology today 4:72(1983);cole等人,monoclonal antibodies and cancer therapy,alan r.liss,inc.(1985)第77-96页中的那些。
[0225]
除了在体内产生抗体的常规方法之外,还可以使用噬菌体展示技术在体外产生抗体。与常规的抗体生产相比,这种重组抗体的生产速度要快得多,并且可以针对大量抗原产生它们。此外,当使用常规方法时,许多抗原被证明是非免疫原性的或剧毒的,并且因此不能用于在动物体内产生抗体。此外,重组抗体的亲和力成熟(即增加亲和力和特异性)非常简单且相对较快。最后,可以在一个选定程序中产生大量针对特定抗原的不同抗体。为了生成重组单克隆抗体,可以使用各种基于展示库的方法来生成大量(a large pool of)具有
不同抗原识别位点的抗体。这样的库可以通过多种方式制作:一种可以通过在重链种系基因库中克隆合成的cdr3区域来生成合成的库(repertoire),从而生成大的抗体库,从中可以选择具有各种特异性的重组抗体片段。可以使用人类的淋巴细胞库(pool)作为构建抗体库的起始材料。可以构建人类igm抗体的原始库,并且因此创建一个具有大量多样性的人类库。这种方法已被广泛成功地用于选择大量针对不同抗原的抗体。噬菌体库构建和重组抗体选择的方案在众所周知的参考文本current protocols in immunology,colligan等人(eds.),john wiley&sons,inc.(1992-2000),第17章,第17.1节中提供。
[0226]
非人类抗体可以通过本领域已知的任何方法进行人源化。在一种方法中,将非人互补决定区(cdr)插入人类抗体或共有抗体框架序列中。然后可以将进一步的变化引入抗体框架以调节亲和力或免疫原性。
[0227]
在一些实施方式中,抗体及其部分包括:抗体、抗体片段、fab和f(ab')2、单域抗原结合重组片段和天然纳米抗体。在一些实施方式中,抗原结合片段选自fv、fab、f(ab')2、scfv或scfv2片段。
[0228]
在一些实施方式中,本发明提供了编码本发明的抗体或抗原结合部分的核酸序列。
[0229]
例如,多核苷酸可以编码整个免疫球蛋白分子链,比如轻链或重链。完整的重链不仅包括重链可变区(vh),而且还包括重链恒定区(ch),其通常包括三个恒定结构域:ch1、ch2和ch3;和一个“铰链”区。在一些情况下,存在恒定区是期望的。
[0230]
可以由多核苷酸编码的其他多肽包括抗原结合抗体片段,例如单域抗体(“dabs”)、fv、scfv、fab'和chi,并且ck或cl结构域已被切除。由于微抗体比传统抗体小,它们应该在临床/诊断应用中实现更好的组织穿透,但是是二价的,它们应该比单价抗体片段(比如dab)保持更高的结合亲和力。因此,除非上下文另有说明,否则本文所用的术语“抗体”不仅包括完整的抗体分子,而且还包括上述类型的抗原结合抗体片段。存在于编码多肽中的每个框架区可以包括相对于相应的人受体框架的至少一个氨基酸取代。因此,例如,相对于受体框架区,框架区可以总共包含三个、四个、五个、六个、七个、八个、九个、十个、十一个、十二个、十三个、十四个或十五个氨基酸取代。鉴于构成所公开蛋白质产物的单个氨基酸的特性,本领域技术人员将认识到一些合理的取代。例如,可以基于所涉及残基的极性、电荷、溶解性、疏水性、亲水性和/或两亲性质的相似性进行氨基酸取代,即“保守取代”。
[0231]
如本文所使用的,当与值组合时,术语“约”是指提及值
±
10%。例如,约1000纳米(nm)的长度是指1000nm
±
100nm的长度。
[0232]
注意,如本文和所附权利要求中使用的,除非上下文另有明确规定,否则单数形式“一(a)”、“一(an)”和所述(the)包括复数指示物。因此,例如,提及“多核苷酸”包括多个此类多核苷酸,提及“多肽”包括提及本领域技术人员已知的一种或多种多肽及其等同物等。还应注意,可以撰写权利要求以排除任何可选的要素。因此,本声明旨在作为这种排他性术语如“唯一”、“仅”等结合权利要求要素使用或使用“否定”限制时的引用基础。
[0233]
在类似于“a、b和c等中的至少一个”的惯例(convention)的那些情况下,在使用这种结构时,一般来说,这种结构意在本领域技术人员会理解惯例的意义(例如,“具有a、b和c中的至少一个的系统”将包括但不限于以下系统:仅a、仅b、仅c、a和b一起、a和c一起、b和c一起、和/或a、b和c一起等)。本领域技术人员将进一步理解,无论是在说明书、权利要求书
或附图中,实际上呈现两个或多个可选术语的任何分离词和/或短语都应被理解为考虑包括这些术语中的一个、术语中的任一个或两个术语的可能性。例如,短语“a或b”将被理解为包括“a”或“b”或“a和b”的可能性。
[0234]
应当理解,为了清楚起见,在单独实施方式的上下文中描述的本发明的某些特征也可以在单个实施方式中组合地提供。相反,为了简洁起见,在单个实施方式的上下文中描述的本发明的各种特征也可以单独提供或以任何合适的子组合提供。属于本发明的实施方式的所有组合都被本发明特别地包含并且在本文中被公开,就好像每个组合被单独地且明确地公开一样。此外,各种实施方式及其要素的所有子组合也被本发明具体涵盖并在本文中公开,就好像每个这样的子组合在本文中被单独且明确地公开一样。
[0235]
通过检查以下实施例,本发明的其他目的、优点和新颖特征对于本领域普通技术人员将变得显而易见,这些实施例不旨在限制性的。此外,如上文所述和如在以下权利要求部分中所要求保护的本发明的各种实施方式和方面中的每一个在以下实施例中找到实验依据。
[0236]
如上文所描述和在以下权利要求部分中要求保护的本发明的各种实施方式和方面在以下实施例中找到实验依据。
[0237]
实施例
[0238]
通常,本文使用的命名法和本发明使用的实验室程序包括分子、生物化学、微生物学和重组dna技术。这些技术在文献中得到了详尽的解释。参见,例如,“molecular cloning:a laboratory manual”sambrook等人,(1989);“current protocols in molecular biology"volumes i-iii ausubel,r.m.,ed.(1994);ausubel等人,“current protocols in molecular biology”,john wiley and sons,baltimore,maryland(1989);perbal,“a practical guide to molecular cloning”,john wiley&sons,new york(1988);watson等人,“recombinant dna”,scientific american books,new york;birren等人(eds)“genome analysis:a laboratory manual series”,第1-4卷,cold spring harbor laboratory press,new york(1998);美国专利号4,666,828;4,683,202;4,801,531;5,192,659和5,272,057中阐述的方法;“cell biology:a laboratory handbook”,volumes i-iii cellis,j.e.,ed.(1994);freshney的“culture of animal cells-a manual of basic technique”,wiley-liss,n.y.(1994),第3版;“current protocols in immunology”volumes i-iii coligan j.e.,ed.(1994);stites等人(eds),“basic and clinical immunology”(第8版),appleton&lange,norwalk,ct(1994);mishell和shiigi(eds),“strategies for protein purification and characterization-a laboratory course manual”cshl press(1996);其所有通过引用并入。本文档通篇提供了其他一般参考资料。
[0239]
方法:
[0240]
‘
免疫分数’计算:首先使用netmhciipan算法分析蛋白质序列,该算法识别具有可结合my mhc ii类分子的9聚体核心表位的15聚体肽。对蛋白质序列中的每个15聚体和我们数据集中的27个等位基因中的每一个进行预测。如果15聚体表位在iedb肽中排名前2%,则被标记为cd4+表位。然后根据两个参数对原始预测值进行加权:(1)群体中的等位基因频率。(2)鉴定的核心表位在15聚体肽内位置的依赖性。这两个参数通过以下方式组合成每个
残基的
‘
免疫原性评分’:
[0241]
其中:
[0242]
wi–
是等位基因i的hla频率
[0243]bi
–
是等位基因i的hla结合ic50值,和
[0244]fj
–
是位置j所属的15聚体中长度为9的表位频率(范围1-7)
[0245]
同时核心位置依赖性计算为:核心位置依赖性=在已识别的15聚体表位内9聚体核心的出现次数/7
[0246]
'自我相似性'计算:从uniprotkb下载具有大约20,000个人类蛋白质序列的人类蛋白质组。我们使用了查询:蛋白质组:up000005640与审查:是的。每个蛋白质序列被一个残基划分为9聚体肽缩进。该数据集包含人类蛋白质组中呈现的大约1000万个9聚体序列。然后使用参数:-gapopen 100-gapextend 10-endweight y-endopen 100-endextend 10,通过emboss针针对人类9聚体肽的数据集分析修美乐序列中的每个9聚体肽。计算与自身的相似性作为人类蛋白质组中相同的9聚体肽的数量。
[0247]
实施例1:阿达木单抗可变区免疫热点的计算映射
[0248]
抗药物抗体(ada)的开发是现代生物制剂的一个常见问题,因为许多治疗性蛋白质会在患者体内引发免疫反应,从而降低生物制剂的功效。ada的发展依赖于cd4+t细胞的诱导,cd4+t细胞激活血浆b细胞产生abs。cd4+t细胞在t细胞上的t细胞受体(tcr)和与抗原呈递细胞(apc)上的外源肽结合的hla ii类分子之间形成免疫复合物时被激活。因此,为了识别免疫热点,计算了两个参数:(i)
‘
免疫评分’——蛋白质序列中每个9聚体肽由hla ii类分子呈递的概率和(ii)蛋白质序列中每个9聚体肽的
‘
自相似性’,即人类蛋白质组中相同肽的数量。有关详细信息,请参阅方法。自相似性程度与在人类t细胞库中找到可以识别特定mhc-肽复合物的tcr的概率呈负相关,因为表达结合mhc-自身肽复合物的tcr的t细胞是在胸腺t细胞发育过程中通过负选择消除的。
[0249]
人类抗体阿达木单抗(修美乐(humira),一种抗-tnfa抗体)是一种广泛使用的治疗性单克隆抗体。根据所检查的研究,接受修美乐治疗的患者中有9-89%产生ada。同样,据报道,接受伊匹单抗(一种抗ctla4抗体)治疗的患者中约有25%产生ada。酶替代疗法,例如用于治疗溶酶体贮积病(50-97%ada)和血友病(5-88%ada)的那些,也被发现会产生ada,证明了这个问题的范围。由于阿达木单抗的广泛分布和ada的高发病率(尤其是在以色列人群中,~40%),它被选中进行研究。
[0250]
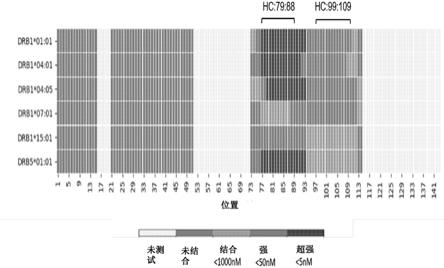
修美乐可变区中潜在免疫原性热点的图总结在图1a中。vl结构域显示位于位置47-57和71-81的两个区域,具有中等免疫评分,因此结合mhc ii类分子的可能性中等。然而,这些区域与自身值(self-value)具有高度相似性(图1b)。因此,这些区域没有被定义为预测热点。
[0251]
vh结构域(重链)显示四个表位。最高的免疫评分是位于位置79至88的残基lylqmnslra,该表位称为hc:79:88。由于其高免疫评分,该表位被归类为潜在的免疫原性热点,尽管它与自身值具有高度相似性(图1c)。位于99至109位的另一个表位呈现中等免疫评分,人类基因组中的9聚体肽与该区域中的肽相同,或者甚至没有鉴定出具有一个氨基酸取代的肽(图1c)。因此,该表位也被预测为免疫热点,并且该表位被称为hc:99:109。在vh结构
域的开头还有另外两个潜在的表位,然而,这些热点呈现出低到中等的免疫评分和与自身的中等相似性(图1c)。这些区域未被归类为潜在的免疫原性热点。
[0252]
具体地,vh序列中的残基根据它们在以下范围内的出现分为5类:(1)未测试hla结合的肽。(2)不与被测hla等位基因结合的肽,ic50》1000nm。(3)1000nm》ic50》50nm的结合肽。(4)显示强结合力的肽,50nm》ic50》5nm和(5)以ic50《5nm紧密结合jla的超肽。根据具有最低ic50的肽定义来自两个或多个类别的肽内的残基。如图1a所示,表位hc:79:88内或附近的残基是肽的一部分,这些肽对六个测试的hla等位基因中的四个显示出超结合力,并对另外两个hla分子显示出强到中等结合力。位于表位hc:99:109中或附近的残基是关于四个等位基因的强结合肽和关于另外两个等位基因的结合肽的一部分。对于在1-15位和21-51位的残基,没有鉴定到任何测试等位基因的结合肽。未测试vh结构域中的其他位置。总体而言,两个表位hc:79:88和hc:88:109由不同的hla等位基因分子呈递,表明这些表位在全世界人群中的免疫原性潜力。
[0253]
实施例2:产生具有降低的抗原性和与靶标的保守结合的表位。
[0254]
产生具有降低的抗原性但与靶标的结合保守的表位的方法如下。简而言之,表位hc79:88和99:109被改变以降低免疫原性。这是通过比对同源序列,然后计算位置频率矩阵来完成的。对产生的突变进行免疫原性分析和结构分析,产生了750个可能的hc79:88替代的序列和1.4
×
10^5个hc99:109替代的序列。酵母表面展示库用于表达这些突变序列,并通过facs分析测试与它们的靶标的保留结合。具有与野生型抗体相当结合的靶标被保留为具有降低的免疫原性但功能保守的突变序列。这个过程总结在图2中。
[0255]
已经在修美乐的重链中确定了两个免疫原性热点之后,创建了两个库(每个热点一个),其中包含用于替代热点的可选序列。覆盖hc:79-88的库被指定为库1,覆盖hc 99:109的库被指定为库2。库1覆盖10聚体,并且因此具有1x10^13个可能序列的总多样性。库2涵盖11聚体,并且因此具有1x10^14个可能序列的总多样性。然而,这些可能的序列中的许多都具有亲本序列的免疫原性问题,因此第一步是去除具有高免疫评分和与自身相似性低的序列。图3a显示了库1中在hc:79-88区域几乎没有或没有免疫原性的代表性克隆,图3b显示了库2中在hc:99-109区域几乎没有或没有免疫原性的克隆。库1和库2的保守表位分别显示在图3c和3d中。
[0256]
产生编码具有突变以包括来自库1和库2的序列的修美乐的重组scfv的载体,并在酵母高通量展示系统中表达。通过facs进行三个连续的富集以产生高度表达重组突变体修美乐的富集群体。
[0257]
现在测试突变抗体与细胞表面上表达的tnfa的结合。将表达tnfa的酵母细胞与突变抗体一起温育,并通过facs检查表面结合(图4a-4b)。选择了至少与wt修美乐一样能够结合tnfa的突变体。然后针对存在的特定突变区域对每个富集克隆进行测序。在此功能测试之后,库1仅包含750个序列,和库2仅包含1.4
×
10^5个序列。
[0258]
基于与tnfa的结合、低数量的突变和零免疫原性评分,选择来自库2的四个最佳表位(vswvstsssld、vswlstsgsld、vsgpstsgnld和vswlstsgnld;seq id no:97-100)用于进一步研究。将这四个表位插入库1,产生4个库,命名为库3.1、3.2、3.3和3.4(库3.1包含seq id no:97,3.2包含seq id no:98,3.3包含seq id no:99,3.4包含seq id no:100)。这些库在两个热点都显示出降低的免疫原性(图5a)。再次选择了至少与wt修美乐一样能够结合tnfa
的突变体(图5b,表6)。
[0259]
接下来测试各种突变表位与各种hla的结合。五个hla等位基因已用于识别热点。其中4个是非常强的结合剂,和一个是结合剂,尽管强度较低(hla-drb3*02:02)(表3)。还测试了未在初始分析中的第六个hla等位基因,并且发现它与两个wt热点序列都强烈结合(参见表3)。这强调了这样一个事实,即,预测的免疫原性是该区域的普遍方面。
[0260]
表3
[0261][0262]
即使这些等位基因结合库中的许多单独的表位,特定肽与各种hla的结合也大大降低。图6a显示了所选肽与六种hla的结合。还测试了表位两侧的氨基酸的作用。图6a显示了c2和c3库,它们包含相同的突变肽,但具有不同的侧翼序列。库c2。这些侧翼序列的影响是最小的。图6b显示了与wt修美乐相比结合降低的程度,如通过ic50的降低倍数测量的。几种肽的hla结合显著降低,并且因此免疫原性显著降低。
[0263]
在表4中提供了来自库1的、被发现具有降低的免疫原性并且发现仍然允许与tnfa结合的wt水平的靠前(top)肽。表4还包括当测定与ctla4的结合以降低伊匹单抗的免疫原性时的靠前命中(top hit)(见下文)。表5中提供了来自库2的靠前命中。来自库1和库2的选定序列的共同表位分别显示在图3e和3f中。表6中提供了来自3.1-3.4组合库的hc:79-88内的靠前表位。在多于一个库中发现了一些表位。在组合库中也发现了表4中发现的序列。尽管本文的表格中提供了靠前命中,但它们仅是示例性的。共同表位更准确地代表了发现的功能肽的广度。事实上,还发现修美乐的靠前命中在插入伊匹单抗时会降低免疫原性并发挥作用,反之亦然。
[0264]
表4:来自库1的修美乐和伊匹单抗的靠前命中
[0265]
序列seq id no:修美乐/伊匹单抗lnlemndltp10修美乐lnlqmndltp11修美乐lylqmnslrp12修美乐lylemnglsp13修美乐lslqmndltt14修美乐
lhlemnglte15修美乐lylemndlgt16修美乐lylemnglap17修美乐lalemnsltp18修美乐lslemndlga19修美乐ltlemnsltp20伊匹单抗ltlemnslte21伊匹单抗ltlemnglgp22伊匹单抗ltlemnglap23伊匹单抗lylemndlsd24伊匹单抗ltlemnglsp25伊匹单抗ltlemnglrp26伊匹单抗ldlqmnglgp113伊匹单抗
[0266]
表5:来自库2的靠前命中
[0267]
序列seq id no:用于vswvstsssld97生成库3.1vswlstsgsld98生成库3.2vsgpstsgnld99生成库3.3vswlstsgnld100生成库3.4vsfhstsegld101 vswlstsssld102 vsylstsgnld103 vsylstsgsld104 vsqlstsgdld105 vsqlstsgsld106 vswlstsgsld107 vsqlstsgdld108 vsvlstsgsld109 vsllstsgsld110 vsvlstsgdld111 vsgvstsgsld112 [0268]
表6:来自库3.1-3.4的靠前命中
[0269]
[0270][0271]
最后,表位经由t细胞功能测定使用从修美乐治疗的发生ada的患者收集的pbmc进行验证。收集的pbmc与产生的突变修美乐抗体混合,并通过分泌促炎细胞因子来测量t细胞活化。已确认变体抗体不会激活来自发生ada的患者的t细胞。
[0272]
实施例3:包括hc:79:88热点的市售抗体
[0273]
对hc:79:88热点检查了462种不同的治疗性抗体。hc99:109热点位于阿达木单抗的cdr3区域,并且因此预计不会在其他抗体中发现。这些中的118种被发现具有hc:79:88热点的确切序列。上述表3中提供了这118种抗体。该表位(lylqmnslra,seq id no:1)是在462种抗体中发现的最常见的共享表位之一。
[0274]
实施例4:工程化免疫原性降低的伊匹单抗
[0275]
118种抗体之一是伊匹单抗。伊匹单抗是一种治疗性抗ctla4单克隆抗体。据报道,施用该抗体可诱导ada。因此,使用上文描述的方案,设计了具有降低的免疫原性的伊匹单抗变体。对伊匹单抗序列的扫描显示它还共享核心hc:79:88热点。因此,库1被转移到伊匹单抗的序列中,因为这也可以预测会降低免疫原性(图7a)。如前所述,对于抗体变体,与酵母细胞表面上的ctla4结合得到证实(图7b)。如前所述,通过测试与六个hla等位基因的结合来证实免疫原性降低(图7c)。正如预期的那样,几种变体显示测试的hla的ic50显著降低(图7d)。因此,这种替代策略对于降低阿达木单抗和伊匹单抗二者的免疫原性是有效的,并且对共享这些共同热点的任何抗体确实是有效的。图7e中提供了伊匹单抗热点区域的选定变体的表位。
[0276]
尽管已经结合其特定实施方式描述了本发明,但是显然,许多替代、修改和变化对于本领域技术人员来说将是显而易见的。因此,旨在涵盖落入所附权利要求的精神和广泛范围内的所有这些替代、修改和变化。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1