用于制备E-选择素抑制剂中间体的方法与流程
用于制备e-选择素抑制剂中间体的方法
1.本技术根据35u.s.c.
§
119(e)要求2019年8月20日提交的美国临时申请第62/889,326号的权益,所述申请通过引用以其整体并入本文。
2.提供了用于合成中间体的方法,所述中间体可用于e-选择素抑制剂的合成。还提供了由所述方法获得的有用中间体。这类化合物描述于例如美国专利第9,796,745号和第9,867,841号、美国专利申请第15/025,730号、第15/531,951号、第16/081,275号、第16/323,685号和第16/303,852号以及pct国际申请号pct/us2018/067961。
3.选择素是一组结构相似的对于介导白细胞与内皮细胞的结合重要的细胞表面受体。这些蛋白是1型膜蛋白,并且由氨基末端凝集素结构域、表皮生长因子(egf)样结构域、可变数目的补体受体相关重复、疏水结构域跨越区和胞质结构域组成。结合相互作用似乎是通过选择素的凝集素结构域和各种碳水化合物配体的接触介导的。
4.存在三种已知的选择素:e-选择素、p-选择素和l-选择素。e-选择素见于活化的内皮细胞的表面,所述内皮细胞排列在毛细血管的内壁上。e-选择素结合碳水化合物唾液酸化-路易斯
x
(sle
x
),其作为某些白细胞(单核细胞和嗜中性粒细胞)表面上的糖蛋白或糖脂呈现,并且帮助这些细胞粘附到周围组织被感染或损伤的区域中的毛细管壁;以及e-选择素还结合在许多肿瘤细胞上表达的唾液酸化-路易斯a(slea)。p-选择素在发炎的内皮和血小板上表达,并且还识别sle
x
和slea,但还含有与硫酸化酪氨酸相互作用的第二个位点。当邻近毛细血管的组织被感染或损伤时,e-选择素和p-选择素的表达通常增加。l-选择素在白细胞上表达。选择素介导的细胞间粘附是选择素介导的功能的一个实例。
5.尽管需要选择素介导的细胞粘附来抵抗感染和破坏外来物质,但存在以下情况,其中这样的细胞粘附是不希望的或过度的,导致组织损伤而不是修复。例如,许多病理(如自身免疫病和炎症性疾病、休克和再灌注损伤)涉及白细胞的异常粘附。这种异常的细胞粘附也可能在移植和移植物排斥中起作用。此外,一些循环癌细胞似乎利用炎症性机制结合活化的内皮。在这种情况下,可能需要调节选择素介导的细胞间粘附。
6.本文提供了用于制备化合物15(一种可用于合成e-选择素抑制剂的中间体)的新方法。附图简述
7.图1a和1b说明了化合物15的合成。
8.图2显示了结晶化合物14的观察到的x-射线粉末衍射(xrpd)谱图。
9.图3显示了结晶化合物14的热重分析(tga)曲线。
10.图4显示了结晶化合物14的差示扫描量热法(dsc)热谱图。
11.在一些实施方案中,提供了用于制备化合物15的方法,其中所述方法包括化合物14的氢化。
12.在一些实施方案中,化合物14的氢化包括使用h2和pd/c。在一些实施方案中,化合物14的氢化在至少一种溶剂的存在下进行。在一些实施方案中,所述至少一种溶剂选自醇。在一些实施方案中,所述至少一种溶剂是2-丙醇。在一些实施方案中,所述至少一种溶剂选自酯和醚。在一些实施方案中,所述至少一种溶剂是thf。在一些实施方案中,所述至少一种溶剂是水。在一些实施方案中,化合物14的氢化在至少两种溶剂的存在下进行。在一些实施方案中,所述至少两种溶剂是2-丙醇和thf。在一些实施方案中,化合物14的氢化在至少三种溶剂的存在下进行。在一些实施方案中,所述至少三种溶剂是2-丙醇、thf和水。
13.在一些实施方案中,用于制备化合物15的方法包括化合物13的meo-三苯甲基裂解以提供化合物14。
14.在一些实施方案中,化合物13的meo-三苯甲基裂解包括使用至少一种酸。在一些实施方案中,所述至少一种酸选自无机酸。在一些实施方案中,所述至少一种酸选自有机酸。在一些实施方案中,所述至少一种酸是盐酸。在一些实施方案中,至少一种酸选自三氟乙酸、三氯乙酸、甲酸、对甲苯磺酸和甲磺酸。在一些实施方案中,所述至少一种酸是三氯乙酸。
15.在一些实施方案中,化合物13的meo-三苯甲基裂解在至少一种溶剂的存在下进行。在一些实施方案中,所述至少一种溶剂选自醇。在一些实施方案中,所述至少一种溶剂是甲醇。在一些实施方案中,所述至少一种溶剂是水。在一些实施方案中,所述至少一种溶剂是二氯甲烷。在一些实施方案中,化合物13的meo-三苯甲基裂解在至少两种溶剂的存在下进行。在一些实施方案中,所述至少两种溶剂是二氯甲烷和甲醇。
16.在一些实施方案中,化合物14通过包括硅胶色谱法的方法纯化。在一些实施方案中,硅胶色谱法在正庚烷的存在下进行。在一些实施方案中,硅胶色谱法在乙酸乙酯的存在下进行。在一些实施方案中,硅胶色谱法在正庚烷和乙酸乙酯的存在下进行。
17.在一些实施方案中,化合物14是结晶的。在一些实施方案中,化合物14的结晶在至少一种溶剂的存在下进行。在一些实施方案中,所述至少一种溶剂选自醇。在一些实施方案中,所述至少一种溶剂是2-丙醇。在一些实施方案中,结晶化合物14的特征在于棒状形态。
18.在一些实施方案中,结晶化合物14的特征在于包含在一个或多个以下位置处的信
号的xrpd谱图:
19.在一些实施方案中,结晶化合物14的特征在于包含选自在13.9
±
0.2、11.1
±
0.2、12.2
±
0.2、7.1
±
0.2、4.6
±
0.2和4.9
±
0.2的d-间距处的信号的至少一个信号的xrpd谱图。在一些实施方案中,结晶化合物14的特征在于包含选自在13.9
±
0.2、11.1
±
0.2、12.2
±
0.2、7.1
±
0.2、4.6
±
0.2和4.9
±
0.2的d-间距处的信号的至少两个信号的xrpd谱图。在一些实施方案中,结晶化合物14的特征在于包含选自在13.9
±
0.2、11.1
±
0.2、12.2
±
0.2、7.1
±
0.2、4.6
±
0.2和4.9
±
0.2的d-间距处的信号的至少三个信号的xrpd谱图。在一些实施方案中,结晶化合物14的特征在于包含选自在13.9
±
0.2、11.1
±
0.2、12.2
±
0.2、7.1
±
0.2、4.6
±
0.2和4.9
±
0.2的d-间距处的信号的至少四个信号的xrpd谱图。在一些实施方案中,结晶化合物14的特征在于包含至少在13.9
±
0.2、11.1
±
0.2、12.2
±
0.2、7.1
±
0.2、4.6
±
0.2和4.9
±
0.2的d-间距处的信号的xrpd谱图。
20.在一些实施方案中,结晶化合物14的特征在于包含选自在19.2
±
0.2、18.0
±
0.2、12.4
±
0.2、7.9
±
0.2、7.3
±
0.2和6.4
±
0.2度2θ处的信号的至少一个信号的xrpd谱图。在一些实施方案中,结晶化合物14的特征在于包含选自在19.2
±
0.2、18.0
±
0.2、12.4
±
0.2、7.9
±
0.2、7.3
±
0.2和6.4
±
0.2度2θ处的信号的至少两个信号的xrpd谱图。在一些实施方案中,结晶化合物14的特征在于包含选自在19.2
±
0.2、18.0
±
0.2、12.4
±
0.2、7.9
±
0.2、7.3
±
0.2和6.4
±
0.2度2θ处的信号的至少三个信号的xrpd谱图。在一些实施方案中,结晶化合物14的特征在于包含选自在19.2
±
0.2、18.0
±
0.2、12.4
±
0.2、7.9
±
0.2、7.3
±
0.2和6.4
±
0.2度2θ处的信号的至少四个信号的xrpd谱图。在一些实施方案中,结晶化合物14的特征在于包含至少在19.2
±
0.2、18.0
±
0.2、12.4
±
0.2、7.9
±
0.2、7.3
±
0.2和6.4
±
0.2度2θ处的信号的xrpd谱图。
21.在一些实施方案中,结晶化合物14的特征在于在约170℃具有吸热起始的dsc曲线。在一些实施方案中,结晶化合物14的特征在于在约171℃具有吸热峰的dsc曲线。在一些实施方案中,结晶化合物14的特征在于在约170℃具有吸热起始和在约171℃具有峰的dsc曲线。在一些实施方案中,结晶化合物14的特征在于在169.7℃具有吸热起始和在171.4℃具有峰的dsc曲线。在一些实施方案中,当通过热重分析进行分析时,直到140℃,结晶化合物14具有约小于2重量%的质量损失。在一些实施方案中,当通过热重分析进行分析时,直至140℃,结晶化合物14具有约小于1重量%的质量损失。在一些实施方案中,当通过热重分析进行分析时,直至140℃,结晶化合物14具有约0.7重量%的质量损失。
22.在一些实施方案中,用于制备化合物15的方法包括化合物12的烯丙氧羰基裂解和酰化以提供化合物13。
23.在一些实施方案中,化合物12的烯丙氧羰基裂解/酰化包括使用至少一种碱。在一些实施方案中,所述至少一种碱是4-甲基吗啉。在一些实施方案中,化合物12的烯丙氧羰基裂解/酰化包括使用至少一种酸。在一些实施方案中,所述至少一种酸是乙酸。在一些实施方案中,化合物12的烯丙氧羰基裂解/酰化包括使用至少一种酸酐。在一些实施方案中,所述至少一种酸酐是乙酸酐。
24.在一些实施方案中,化合物12的烯丙氧羰基裂解/酰化包括使用至少一种膦。在一些实施方案中,所述至少一种膦是三苯基膦。在一些实施方案中,化合物12的烯丙氧羰基裂解/酰化包括使用至少一种催化剂。在一些实施方案中,所述至少一种催化剂是pd[(c6h5)3p]4。
[0025]
在一些实施方案中,化合物12的烯丙氧羰基裂解/酰化在至少一种溶剂的存在下进行。在一些实施方案中,所述至少一种溶剂是二氯甲烷。在一些实施方案中,所述至少一种溶剂是甲苯。
[0026]
在一些实施方案中,用于制备化合物15的方法包括化合物9与化合物11的o-烷基化以提供化合物12。
[0027]
在一些实施方案中,化合物9的o-烷基化包括使用至少一种烷基锡。在一些实施方案中,所述至少一种烷基锡是氧化二丁基锡(iv)。在一些实施方案中,化合物9的o-烷基化
在至少一种溶剂的存在下进行。在一些实施方案中,所述至少一种溶剂是乙腈。在一些实施方案中,所述至少一种溶剂是甲醇。在一些实施方案中,所述至少一种溶剂是甲苯。在一些实施方案中,化合物9的o-烷基化在至少两种溶剂的存在下进行。在一些实施方案中,所述至少两种溶剂是甲苯和乙腈。在一些实施方案中,化合物9的o-烷基化包含至少一种氟化物。在一些实施方案中,所述至少一种氟化物是氟化铯。
[0028]
在一些实施方案中,用于制备化合物15的方法包括化合物8的甲氧基-三苯甲基化以提供化合物9。
[0029]
在一些实施方案中,化合物8的甲氧基-三苯甲基化包括使用4-meo-三苯甲基-cl。在一些实施方案中,化合物8的甲氧基-三苯甲基化包括使用至少一种碱。在一些实施方案中,所述至少一种碱选自dabco、吡啶和2,6-二甲基吡啶。在一些实施方案中,化合物8的甲氧基-三苯甲基化在至少一种溶剂的存在下进行。在一些实施方案中,所述至少一种溶剂是二氯甲烷。在一些实施方案中,所述至少一种溶剂是me-thf。在一些实施方案中,化合物8的甲氧基-三苯甲基化在至少两种溶剂的存在下进行。在一些实施方案中,所述至少两种溶剂是methf和二氯甲烷。
[0030]
在一些实施方案中,沉淀化合物9。在一些实施方案中,在至少一种溶剂的存在下沉淀化合物9。在一些实施方案中,所述至少一种溶剂是methf。在一些实施方案中,所述至少一种溶剂是正庚烷。在一些实施方案中,在至少两种溶剂的存在下沉淀化合物9。在一些实施方案中,所述至少两种溶剂是methf和正庚烷。
[0031]
在一些实施方案中,用于制备化合物15的方法包括化合物7的脱乙酰化以提供化合物8。
[0032]
在一些实施方案中,化合物7的脱乙酰化包括使用至少一种碱。在一些实施方案中,所述至少一种碱选自醇盐。在一些实施方案中,所述至少一种碱为naome。在一些实施方案中,化合物7的脱乙酰化在至少一种溶剂的存在下进行。在一些实施方案中,所述至少一种溶剂是甲醇。在一些实施方案中,所述至少一种溶剂是乙酸甲酯。在一些实施方案中,化合物7的脱乙酰化在至少两种溶剂的存在下进行。在一些实施方案中,所述至少两种溶剂是
甲醇和乙酸甲酯。
[0033]
在一些实施方案中,化合物8是结晶的。在一些实施方案中,化合物8在至少一种溶剂的存在下结晶。在一些实施方案中,所述至少一种溶剂是2-甲基-2-丁醇。在一些实施方案中,所述至少一种溶剂是正庚烷。在一些实施方案中,化合物8在至少两种溶剂的存在下结晶。在一些实施方案中,所述至少两种溶剂是2-甲基-2-丁醇和正庚烷。
[0034]
在一些实施方案中,化合物8作为乙醇溶剂化物结晶。在一些实施方案中,化合物8在至少一种溶剂的存在下作为乙醇溶剂化物结晶。在一些实施方案中,所述至少一种溶剂是乙醇。在一些实施方案中,化合物8在至少两种溶剂的存在下作为乙醇溶剂化物结晶。在一些实施方案中,所述至少两种溶剂是乙醇和水。在一些实施方案中,结晶化合物8为乙醇溶剂化物。在一些实施方案中,结晶化合物8乙醇溶剂化物的特征在于棒状晶体。
[0035]
在一些实施方案中,用于制备化合物15的方法包括化合物4与化合物6的糖基化以提供化合物7。
[0036]
在一些实施方案中,化合物4的糖基化在至少一种溶剂的存在下进行。在一些实施方案中,所述至少一种溶剂是甲苯。在一些实施方案中,所述至少一种溶剂是二氯甲烷。在一些实施方案中,化合物4的糖基化在至少两种溶剂的存在下进行。在一些实施方案中,所述至少两种溶剂是甲苯和二氯甲烷。在一些实施方案中,化合物4的糖基化包括使用至少一种酸。在一些实施方案中,所述至少一种酸是三氟甲磺酸。
[0037]
在一些实施方案中,用于制备化合物6的方法包括化合物5的活化。
[0038]
在一些实施方案中,化合物5的活化包括使用至少一种亚磷酸酯。在一些实施方案中,所述至少一种亚磷酸酯选自氯亚磷酸酯。在一些实施方案中,所述至少一种亚磷酸酯是氯亚磷酸二乙酯。在一些实施方案中,化合物5的活化在至少一种溶剂的存在下进行。在一些实施方案中,所述至少一种溶剂是甲苯。在一些实施方案中,化合物5的活化在至少一种有机碱的存在下进行。在一些实施方案中,所述至少一种有机碱是三乙胺。
[0039]
在一些实施方案中,用于制备化合物15的方法包括化合物3的tbdms-去保护以提
供化合物4。
[0040]
在一些实施方案中,化合物3的tbdms-去保护包括使用至少一种氟化物。在一些实施方案中,所述至少一种氟化物是tbaf。在一些实施方案中,化合物3的tbdms-去保护在至少一种溶剂的存在下进行。在一些实施方案中,所述至少一种溶剂是thf。在一些实施方案中,所述至少一种溶剂是acn。在一些实施方案中,化合物3的tbdms-去保护在至少两种溶剂的存在下进行。在一些实施方案中,所述至少两种溶剂是thf和acn。
[0041]
在一些实施方案中,化合物4是结晶的。在一些实施方案中,化合物4在至少一种溶剂的存在下结晶。在一些实施方案中,所述至少一种溶剂是二氯甲烷。在一些实施方案中,所述至少一种溶剂是甲醇。在一些实施方案中,所述至少一种溶剂是水。在一些实施方案中,化合物4在至少两种溶剂的存在下结晶。在一些实施方案中,所述至少两种溶剂是水和甲醇。
[0042]
在一些实施方案中,用于制备化合物15的方法包括化合物1与化合物2b的岩藻糖基化以提供化合物3。
[0043]
在一些实施方案中,化合物1的岩藻糖基化包括使用tbabr。在一些实施方案中,化合物1的岩藻糖基化包括使用至少一种碱。在一些实施方案中,所述至少一种碱是dipea。在一些实施方案中,化合物1的岩藻糖基化在至少一种溶剂的存在下进行。在一些实施方案中,所述至少一种溶剂是methf。在一些实施方案中,所述至少一种溶剂是二氯甲烷。在一些实施方案中,化合物1的岩藻糖基化在至少两种溶剂的存在下进行。在一些实施方案中,所述至少两种溶剂是methf和二氯甲烷。
[0044]
在一些实施方案中,制备化合物2b的方法包括使化合物2a与br2反应。在一些实施方案中,化合物2a与br2的反应在至少一种溶剂的存在下进行。在一些实施方案中,所述至少一种溶剂是环己烷。
[0045]
在一些实施方案中,用于制备化合物15的方法包括以下步骤中的至少一个:(a)化合物14的氢化;(b)化合物13的meo-三苯甲基裂解;(c)化合物12的烯丙氧羰基裂解/酰化;(d)化合物9的o-烷基化;(e)化合物8的甲氧基-三苯甲基化;(f)化合物7的脱乙酰化;
chemistry”,2nd ed.,john wiley&sons,new york,1992;j.march,“advanced organic chemistry:reactions,mechanisms and structure,”4th ed.,wiley interscience,new york,1992。详述用于制备本公开内容的化合物的反应物的合成或提供对描述制备的文章的参考的另外合适的参考书籍和论文包括例如fuhrhop,j.和penzlin g.“organic synthesis:concepts,methods,starting materials”,second,revised and enlarged edition(1994)john wiley&sons isbn:3-527-29074-5;hoffman,r.v.“organic chemistry,an intermediate text”(1996)oxford university press,isbn 0-19-509618-5;larock,r.c.“comprehensive organic transformations:a guide to functional group preparations”2nd edition(1999)wiley-vch,isbn:0-471-19031-4;march,j.“advanced organic chemistry:reactions,mechanisms,and structure”4th edition(1992)john wiley&sons,isbn:0-471-60180-2;otera,j.(编辑)“modern carbonyl chemistry”(2000)wiley-vch,isbn:3-527-29871-1;patai,s.“patai’s 1992guide to the chemistry of functional groups”(1992)interscience isbn:0-471-93022-9;quin,l.d.等人,“a guide to organophosphorus chemistry”(2000)wiley-interscience,isbn:0-471-31824-8;solomons,t.w.g.“organic chemistry”7th edition(2000)john wiley&sons,isbn:0-471-19095-0;stowell,j.c.,“intermediate organic chemistry”2nd edition(1993)wiley-interscience,isbn:0-471-57456-2;“industrial organic chemicals:starting materials and intermediates:an ullmann’s encyclopedia”(1999)john wiley&sons,isbn:3-527-29645-x,在8卷中(in 8volumes);“organic reactions”(1942-2000)john wiley&sons,在多于55卷中(in over 55volumes);以及“chemistry of functional groups”john wiley&sons,在73卷中(in 73volumes)。
实施例
实施例1:化合物15的合成步骤1
[0052]
化合物3:将39.34g化合物2a(1.30当量)溶解在环己烷(8体积)中,在ta=55℃/200mbar下汽提(去掉6体积),加入环己烷(5体积),并在ta=55℃/230-210mbar下再次汽提(去掉5体积)。加入dcm(2.2体积)并将溶液冷却至ti=0℃。在ti=0-5℃下历经67分钟加入溴(1.20当量)在dcm(0.4体积)中的溶液,并在0℃的ti下再搅拌55分钟,然后在ti=0-5℃下历经55min加入环己烯(1.5当量)。将混合物(dcm中的化合物2b)在0℃下再搅拌40分钟。
[0053]
在ti=0℃下加入dipea(3.0当量)、tbabr(1.0当量)和methf(2体积)。然后在ti=0-1℃下历经10分钟加入化合物1(20.02g/1.0当量)在dcm(2体积)中的溶液。用dcm(1体积)漂洗加料罐并将洗涤液加入到反应混合物中。历经120min将反应混合物升温至ti=25℃,并在ti=25℃下保持搅拌120h。
[0054]
在ti=25℃下加入水(7体积),分离各相,并用dcm(2体积)再萃取水相(ap的ph~7)。将合并的有机层用15%柠檬酸水溶液(5体积)、7.4%nahco3水溶液(5体积)和水(5体积)依次洗涤(最终ap的ph~7)。测定有机层的体积(op 4#1~260ml),并在ta=45℃/500mbar下浓缩至10vol。控制浓缩物的ph(ph 4-5)并加入dipea(0.2当量),导致ph~9。在ph调节之后,重新开始蒸馏,并且在ta=60℃/500-190mbar下蒸馏掉4体积的溶剂。加入乙腈(7体积),并在ta=55℃/200-190mbar下蒸馏掉6体积。步骤2
[0055]
化合物4:在ti~20℃下历经10min加入在thf中的1m tbaf(2.2当量),将反应混合物(红色溶液)加热至ti=55℃,并在ti=55℃下搅拌19h。
[0056]
在ta=55℃/240-190mbar下蒸馏掉4体积溶剂。加入dcm(5体积)和水(5体积),分离各相,并用dcm(2体积)再萃取水相。将合并的有机层用3.7%的nahco3(5体积)和水(5体积)依次洗涤。测定有机层的体积(230ml)并在ta=55℃/580-420mbar(
→
溶液)下浓缩至6体积的浓缩体积。加入甲醇(12体积),得到浓稠悬浮液。在ta=58℃-70℃/480-430mbar下蒸馏掉4体积。在ta=80℃/atm下将悬浮液加热回流。(ti~60℃),获得澄清溶液。在ta=75℃下历经17分钟加入水(1体积)。将悬浮液在大约85分钟内冷却至ti=20℃
[0057]
将悬浮液在ti=20℃下搅拌4小时20分钟,然后过滤。用meoh/水6:1(3体积)、meoh/水4:1(1体积)和甲基-环己烷(4体积)洗涤滤饼。在真空中在吸滤器(nutsch filter)上干燥并在ta=45℃下旋转蒸发至99.56%dc的干重含量。28.36g n.校正(n.corr.)/28.24g lod校正(y lod校正:72.1%)。
[0058]1h nmr(氯仿-d)δ:7.27-7.42(m,15h),4.95-5.02(m,2h),4.94-5.03(m,2h),4.73-4.87(m,2h),4.67(dd,j=14.1,11.5hz,2h),4.62-4.72(m,2h),4.06-4.14(m,2h),3.96(dd,j=10.1,2.8hz,1h),3.64-3.73(m,4h),3.38-3.47(m,1h),2.98(dd,j=10.3,8.5hz,1h),2.35(tt,j=12.6,3.2hz,1h),2.23(tdd,j=7.9,4.7,2.9hz,1h),1.99-2.10(m,2h),1.33-1.56(m,2h),1.07-1.20(m,5h),0.79(t,j=7.5hz,3h)。ms:c
37h46
o8的计算值=618.76,实测值m/z=641.3(m+na
+
)。步骤3
[0059]
化合物6:向化合物5(1.50当量校正,45.32g n.校正/42.47g校正)中加入甲苯(8体积),然后在ta=55℃/130-60mbar下蒸馏掉5体积的溶剂。加入甲苯(2体积),并在ta=55℃下蒸馏掉2体积的溶剂。用甲苯(5.5体积)稀释浓缩物。在冷却至ti=0-5℃之后,加入三乙胺(2.05当量)。在ti=0-3℃下历经30分钟将氯亚磷酸二乙酯(0.93当量)加入到反应混合物中(放热)。将混合物在ti=0℃下搅拌30分钟。在ti=0-5℃下历经10分钟加入第二部分的氯亚磷酸二乙酯(0.13当量)。将混合物在ti=0℃下搅拌30分钟。在ti=0-5℃下历经7分钟加入第三部分的氯亚磷酸二乙酯(0.09当量)。将混合物在ti=0℃下搅拌30分钟。
[0060]
在ti=1℃下在氮气气氛下将反应混合物从固体(teaxhcl)中滤出,并用冷甲苯(3体积)洗涤。滤液经0.2μm尖端过滤器精细过滤。滤液经0.2μm尖端过滤器进行第二次精细过滤。将滤液在ta=4℃下储存过夜,随后经0.2μm尖端过滤器进行第三次过滤。将亚磷酸酯溶液储存在冰箱中,用于随后的糖基化实验。
[0061]
化合物7:将126.41g糖基亚磷酸酯溶液(33.1mmol化合物6,1.28当量)置于500ml烧瓶中,并装入16.03g化合物4(15.95g,25.78mmol)和32ml(2体积)甲苯。将溶液在旋转蒸发仪上在tj=50℃/100
–
4mbar下浓缩,除去175ml(~11体积)的甲苯。将所得固体残余物溶解在96ml(6体积)dcm中并将其转移至三颈烧瓶中。
[0062]
通过在ti=-30℃下历经30分钟定量给料3.53g(23.5mmol,0.91当量)三氟甲磺酸引发反应。在装入4.756g(46.94mmol,1.82当量)的net
3 7.5h之后淬灭反应。将反应混合物(184.16g澄清橙色溶液)储存在t=-20℃直至进一步处理。步骤4
[0063]
化合物8:通过在ta=55℃/600-100mbar下蒸馏掉5体积来浓缩包含化合物7的淬
灭反应混合物。加入甲苯(4体积),然后加入23.1%nacl溶液(2.5体积)和7.4%nahco3溶液(2.5体积)的混合物。分离各相,并用甲苯(5体积)再萃取水层(ap 1#1,ph 9)。将合并的有机层(op1)的体积确定为198ml。在ta=58℃/200-79mbar下,通过蒸馏掉132ml溶剂,将op1浓缩至4.3体积的浓缩体积。将浓缩物用甲醇(3.5体积)稀释并加入乙酸甲酯(1体积)。加入在meoh中的30%naome(0.60当量),并用甲醇(0.5体积)漂洗加料罐。将反应混合物在ti=20℃下搅拌3h。
[0064]
通过在ti=20℃下历经5分钟加入乙酸(0.60当量)淬灭反应混合物以达到5-6的ph。在ta=56℃/300-260mbar下蒸馏掉5体积的溶剂。加入乙酸乙酯(2.5体积),并在ta 58℃/200mbar下蒸馏掉2.5体积。加入乙酸乙酯(5体积)、23.1%nacl溶液(2.5体积)和水(2.5体积),并在搅拌之后分离各相(-》ap 2#1ph 6,op 2#1)。将水层(ap2#1)用乙酸乙酯(3体积)(-》op 2#2)再萃取。将合并的有机层用23.1%nacl溶液(5体积)洗涤,并且有机层(op3#1)的体积被确定为180ml。
[0065]
在ta=60℃/330-300mbar下,通过蒸馏掉116ml溶剂,将op3#1浓缩至4.0体积的浓缩体积。在tj=60℃下(仍为溶液)加入2-甲基-2-丁醇(5体积)。在tj=67℃/280-195mbar下蒸馏掉2.75体积的溶剂,得到略微浑浊的溶液。
[0066]
历经30min将溶液升温至ti=70℃。然后历经100min使溶液冷却至室温。在ti约33℃开始沉淀。将悬浮液在ti=20℃下搅拌85min。然后在ti=20℃下历经50分钟加入正庚烷(8体积),历经25分钟将悬浮液冷却至ti=10℃,并在该温度下搅拌3小时。过滤悬浮液(2min),用2-甲基-2-丁醇/正庚烷的混合物(0.7体积/1.4体积,在10℃下)洗涤滤饼,最后用冷却至ti=10℃的正庚烷(3体积)洗涤滤饼。在真空/氮气中在吸滤器上干燥产物过夜,并进一步在旋转蒸发仪上在ta=45℃下干燥产物6h,至97.22%的干重含量。17.00g n.校正/16.527g lod校正(y:73.91%)。
[0067]1h nmr(氯仿-d)δ7.23-7.43(m,17h),5.90(ddt,j=17.2,10.4,5.8hz,1h),5.31(dq,j=17.1,1.5hz,1h),5.24(dd,j=10.4,1.3hz,1h),5.10(d,j=3.3hz,1h),4.59-5.01(m,9h),4.53-4.58(m,2h),4.44(d,j=7.9hz,1h),4.00-4.12(m,2h),3.83-3.94(m,2h),3.71-3.82(m,4h),3.68(s,3h),3.32-3.35(m,1h),2.34(tt,j=12.2,3.2hz,1h),2.20(d,j=13.2hz,1h),1.91-2.05(m,2h),1.40-1.60(m,3h),1.16-1.30(m,4h),1.12(d,j=6.6hz,4h),0.92(t,j=7.6hz,1h),0.81(t,j=7.4hz,3h)。ms:c
47h61
no
14
的计算值=863.99;实测值m/z=886.4(m+na
+
)。步骤5
[0068]
化合物9:将化合物8(25.00g)溶解在dcm(6体积)中。在tj=50℃/真空下蒸馏掉溶剂(4体积)。加入dcm(6体积)并蒸馏掉相同体积的溶剂。加入dcm(6体积)并蒸馏掉相同体积
1.69(m,5h),1.28-1.43(m,1h),1.04-1.21(m,5h),0.76-0.99(m,3h)。ms:c
17h21
f3o5s5的计算值=394.41,实测值m/z=417.0(m+na)。
[0075]
化合物12:将化合物9(20.45g,1wt.)、二丁基氧化锡(iv)(0.37wt./1.7当量)、甲醇(4体积)和甲苯(2体积)在tj=82℃下加热回流,并在回流下搅拌2h。经由在tj=65℃/320mbar下蒸馏除去溶剂(3体积)。加入甲苯(3体积),并将溶液在tj=82℃下回流搅拌75min。通过在tj=65℃/400-140mbar下蒸馏除去溶剂(4体积)。加入甲苯(3体积)并经由在tj=65℃/130mbar下蒸馏除去溶剂(3体积)。加入甲苯(3体积)并经由在tj=65℃/105mbar下蒸馏除去溶剂(3体积)。
[0076]
在ti=20℃下将乙腈(5体积)加入到浓缩物中。加入含化合物11的甲苯(2.25当量;ca18-0119)、氟化铯(3.0当量;f17-04152)和甲醇(1.0当量)。制备水(0.5当量)和乙腈(0.5当量)的混合物。将1/4的制备的acn溶液加入到反应混合物中,随后在ti=20℃下搅拌1h。加入第二部分的acn溶液,并将混合物再搅拌一小时。将此再重复两次。在加入最后的acn/水部分之后,将反应混合物在ti=20℃下搅拌180min。
[0077]
通过加入7.4%nahco3水溶液(4体积)淬灭混合物并在ti=20℃下搅拌50min。将双相混合物经硅藻土床(2wt;预先用12体积甲苯调节)过滤。用甲苯(3体积)漂洗滤饼。分离各相并用甲苯(3体积)萃取水层。将合并的有机层用半饱和nahco3水溶液(5体积)洗涤。将有机层经na2so4(2.0wt)干燥,过滤na2so4,并用甲苯(2体积)漂洗滤饼。将4-甲基吗啉(1.0当量;f17-03830)加入到产物溶液中。将溶液在4℃下储存过夜。步骤7
[0078]
化合物13:将包含化合物12的有机相在旋转蒸发仪上在ta=55℃/200-90mbar下浓缩至5体积。装入4-甲基吗啉(20当量)和dcm(8体积)。在ti=20℃下加入乙酸酐(8当量)和乙酸(2当量;f16-04758)。将烧瓶抽空并用氮气吹扫三次。加入三苯基膦(0.05当量)和pd[(c6h5)3p]4(0.05当量),然后进行另一次抽空/氮气吹扫循环。将反应混合物在ti=20℃下搅拌18h。
[0079]
通过在环境温度下历经20min加入水(5体积)来淬灭反应。分离各相,并用柠檬酸15%w/w水溶液(5体积)洗涤有机层。向有机相中加入饱和nahco3(5体积)和甲醇(0.5体积)。将混合物在环境温度下剧烈搅拌45min。分离各相,将有机相用水洗涤两次(每次5体积),并在旋转蒸发仪上在tj=50℃/600mbar下浓缩至7体积。步骤8
[0080]
化合物14:向包含化合物13的浓缩物(140ml)中加入甲醇(0.2体积)和水(0.5体积),并冷却至ti=0-5℃。制备tca(3.0当量)和dcm(1体积)的混合物,并在ti=1-2℃下历经20min将其掺入到浓缩物中。将反应混合物在该温度下搅拌3.5h。
[0081]
在ti=1-3℃下在25分钟内将饱和的nahco3水溶液(5体积)掺入到反应混合物中,并使混合物升温直至室温。分离各相并用dcm(2体积)萃取水相。将合并的有机层用水(5体积)洗涤并经na2so4(1.5wt)干燥。将na2so2过滤并用dcm(2体积)漂洗。
[0082]
纯化:向色谱柱中装入1548g(10wts)硅胶(直径15cm,床高22cm)并用1:1的乙酸乙酯/庚烷调节。将来自步骤6/7/8镜管(telescope)的582g产物溶液(原材料:157.63g)装入柱的顶部并用15ml dcm预洗脱。首先应用60体积(9.5l)的洗脱液1(1:1的乙酸乙酯/庚烷)洗脱柱:在收集1l的洗涤级分之后,收集19种级分1#1至1#19(每种体积0.5l)。之后,将洗脱液更换为洗脱液2(3:1的乙酸乙酯/庚烷),收集另外的级分1#20至1#33(每种体积1.0l)。通过tlc分析级分:汇集物1:汇集级分1#18至1#29并将其浓缩,提供了80.88g固体残余物的化合物14(98.15%a/a)。收集级分1#15至1#17作为第二汇集物ii,提供了9.98g固体残余物的第二批化合物14(67.1%a/a)。
[0083]
替代纯化:将biotage筒(40kg二氧化硅,kp-sil flash 400l型)在夹套中用2-丙醇(10l)径向压缩,然后用庚烷(94l)调节,然后用1:1庚烷/etoac(98l)调节。将含粗化合物14的甲苯/dcm(12.319kg n.校正/3.308kg校正)装入到吸滤器(nutsch)中,并在氮气压力下转移到柱上。用小体积的二氯甲烷(0.5l)漂洗吸滤器,并将漂洗溶液转移到柱上。将柱用264l 1:1的庚烷/etoac洗脱,然后用260l 1:3的庚烷/etoac洗脱。用含另外的12.234kg n.校正化合物14的甲苯/dcm重复纯化步骤。
[0084]
收集含有化合物14的所有级分,合并,并在160l玻璃衬里反应器中在tj=60℃/242-156mbar下浓缩至12体积。将浓缩物转移到加料罐中,并且测量体积为71l。
[0085]
将溶液转移到反应器中并在tj=60℃/176-170mbar下进一步浓缩至5体积。经由加料罐装入2-丙醇(36l)且经由在tj=60℃/185-120mbar下蒸馏除去30l溶剂。加入2-丙醇(24.5l)并经由在tj=60℃/120-93mbar下蒸馏除去20l溶剂。加入2-丙醇(20l)并经由在60℃/98-90mbar下蒸馏除去25l溶剂。
[0086]
将反应混合物在ti=55℃下搅拌约1h,并且随后用结晶化合物14(1g)种晶(可以通过将在色谱法之后获得的化合物14的样品加入到2-丙醇中并且搅拌直到观察到结晶来获得晶种)。在4h内将反应混合物冷却至ti=1.7℃,并在该温度下搅拌8.5h。将所得悬浮液转移到吸滤器上并过滤到ml-鼓(ml-drum)中。用母液(14l)漂洗反应器。
[0087]
向反应器中装入2-丙醇(10l)并冷却至ti=1.7℃。将洗涤液转移到吸滤器上并在
2.5h内过滤到ml-鼓中。将滤饼在真空和氮气流下干燥3天。排出产物。2.246kg n.校正/2.241kg lod校正。(在干质量的基础上的y:70.9%回收步骤)。
[0088]1h nmr(氯仿-d)δ7.20-7.45(m,24h),5.66(d,j=6.8hz,1h),5.14-5.25(m,2h),5.05(d,j=8.4hz,1h),4.69-5.01(m,7h),4.61(d,j=11.4hz,1h),4.35(dd,j=10.6,3.0hz,1h),3.95-4.12(m,3h),3.76-3.87(m,2h),3.59-3.74(m,7h),3.41(t,j=4.7hz,1h),3.29(t,j=9.6hz,1h),3.08-3.21(m,1h),2.66(dd,j=9.5,2.2hz,1h),2.29(tt,j=12.6,3.1hz,1h),2.13(d,j=12.7hz,1h),1.91-2.08(m,5h),1.36-1.81(m,13h),0.99-1.31(m,9h),0.72-0.98(m,5h)。ms:c
61h79
no
15
的计算值=1066.28,实测值m/z=1088.5(m+na)。
[0089]
可以通过将色谱法之后获得的化合物14加入到2-丙醇中并搅拌直到观察到结晶来获得化合物14的晶种。步骤9
[0090]
化合物15:向化合物14(5.03g;1wt;ca18-0480)中加入2-丙醇(15体积)、水(0.5体积)和thf(2.5体积)。将悬浮液升温至ti=30℃以获得溶液。加入pd/c 10%0.2wt;f15-01378)和2-丙醇(3体积),并将混合物在氢气气氛下在大气压下和tj=37℃下搅拌7小时。将脱气的水(1.5体积)加入到反应混合物中,并在tj=37℃/1巴下继续氢化17h。加入脱气的水(2体积),并在上述给定条件下再继续氢化7h。将反应混合物在氢气气氛下在tj=37℃/1巴下搅拌过夜。
[0091]
将氢气气氛更换为氮气并加入固体nahco3(0.05当量)和水(2体积)。将反应混合物在30℃下经0.45μm尼龙膜上过滤,并将滤饼用2-丙醇(3体积)和水(1体积)的混合物漂洗。将合并的滤液在tj=35℃/真空下浓缩至干,得到4.80g固体材料。将固体溶解在水(0.2体积)和thf(3体积)的混合物中,得到澄清溶液。
[0092]
将乙酸异丙酯(25.5体积)冷却至ti=0℃,并在ti=0℃下历经55min经由滴液漏斗加入产物溶液。用水(0.1体积)和thf(0.3体积)的混合物漂洗滴液漏斗。将悬浮液在ti=0℃下搅拌80分钟后过滤。将滤饼用mtbe(3体积)漂洗,并将产物在真空和氮气流下干燥过夜。3.10g n.校正/3.08g lod校正(y lod校正92.66%)。
[0093]1h nmr(400mhz,dmso-d6)δ4.61-4.83(m,2h),4.08-4.26(m,3h),3.98(d,j=8.6hz,1h),3.80(s,1h),3.29-3.57(m,10h),3.19-3.28(m,1h),3.06(t,j=9.5hz,1h),2.34-2.47(m,1h),2.22(d,j=12.7hz,1h),1.91-2.04(m,1h),1.71-1.89(m,5h),1.34-1.69(m,8h),0.68-1.31(m,13h)。ms:c
33h55
no
15
的计算值=705.79,实测值m/z=728.4(m+na)。实施例2:化合物8乙醇溶剂化物的单晶x射线分析
[0094]
已经通过单晶x射线衍射来测定化合物8乙醇溶剂化物的绝对结构。经由以下方法制备晶体:
[0095]
将化合物8(10mg)溶解在2ml透明玻璃小瓶中的乙醇(100μl)中,并加入两滴水(约
20μl)。将该小瓶加盖并在5℃下静置。几天后,注意到非常大的棒状晶体在溶液弯月面下生长,这似乎适于通过单晶x射线衍射进行询问。
[0096]
在agilent technologies(双源)supernova衍射仪上使用单色cu辐射进行sxrd分析。该衍射仪配备有oxford cryosystems低温装置,以使数据收集能够在120(1)k下进行,并且晶体被包裹在paratone油的保护层中。基于作为crysalispro软件包(agilent technologies,2014)的一部分实施的多面晶体模型中的高斯积分来校正所收集的数据的吸收效应。
[0097]
通过直接方法(shelxs97)求解该结构,并通过经由olex2软件包对界面上的f(shelxl97)进行全最小二乘精修来开发。经由olex2完成产生的图像。参见sheldrick,g.m.acta cryst.sect.a 2008,64,112;dolomanov,o.v.,bourhis,l.j.,gildea,r.j.,howard,j.a.k.,puschmann,h.j appl.cryst.2009,42,339-341。
[0098]
在正交空间群p212121中收集、求解和精修数据,并使用platon的addsymm例行程序进行更高度量对称性的搜索,但未能揭示任何更高阶的对称性。参见le page,y.j.appl.cryst.1987,20,264;le page,y.j.appl.cryst.1988,21,983;spek a.l.,acta cryst.2009,d65,148。
[0099]
所有非氢原子位于傅立叶图中,并且在各向异性地描述所有非氢原子的热运动之前精修它们的位置。在该结构内,一个完全占据的乙醇分子旁边的不对称单元内发现了一个完整的结晶学上独立的化合物8式单元。在母体化合物8分子内,在苄基-环c27》c32、c34》c39和c41》c46处注意到无序区域,分别精修为占用率为62:38、68:32和53:47的刚性六边形(afix66)。还发现烯丙氧羰基保护基团的末端乙烯基臂c7》c9是无序的,并且用对于c7-c8具有e.s.d.0.01的的固定键长(dfix)以及对于c8
–
c9具有e.s.d.0.01的的固定键长(dfix)的占用率50:50进行精修。
[0100]
使用具有固定uiso的骑乘模型(riding model)将所有氢原子置于计算位置,对于所有的ch、ch2和nh基团为1.2倍,以及对于所有的ch3和oh基团为1.5倍。
[0101]
发现最高残余傅立叶峰为距c26约的以及发现最深的傅立叶孔为距o8约的
[0102]c49h67
no
15
(m=910.05g/mol)的晶体数据:单斜晶体的空间群i2(编号:5),β=90.35
°
,z=4,t=120(10)k,μ(cukα)=0.765mm-1
,dcalc=1.257g/cm3,439372个测量的反射(7.212
°
≤2θ≤152.404
°
),9977个独特的(r
int
=0.0574,r
sigma
=0.0142),将其用于所有计算中。最终的r1为0.0467(i》2σ(i))以及wr2为0.1279(所有数据)。
[0103]
化合物8乙醇溶剂化物的结构特征。发现所收集的结构的晶胞尺寸如下:空间群:单斜晶体的i2α=90
°
β=90.345(1)
°
γ=90
°
z=4,z`=1发现不对称单元含有一个完整的化合物8式单元和不同的电子密度区域,其明显地精修为一个完全占据的乙醇分子。最终的精修参数如下:r1[i》2σ(i)]=4.67%goof(拟合优度)=1.051wr2(所有数据)=13.20%r
int
=5.74%flack参数=-0.07(4)
[0104]
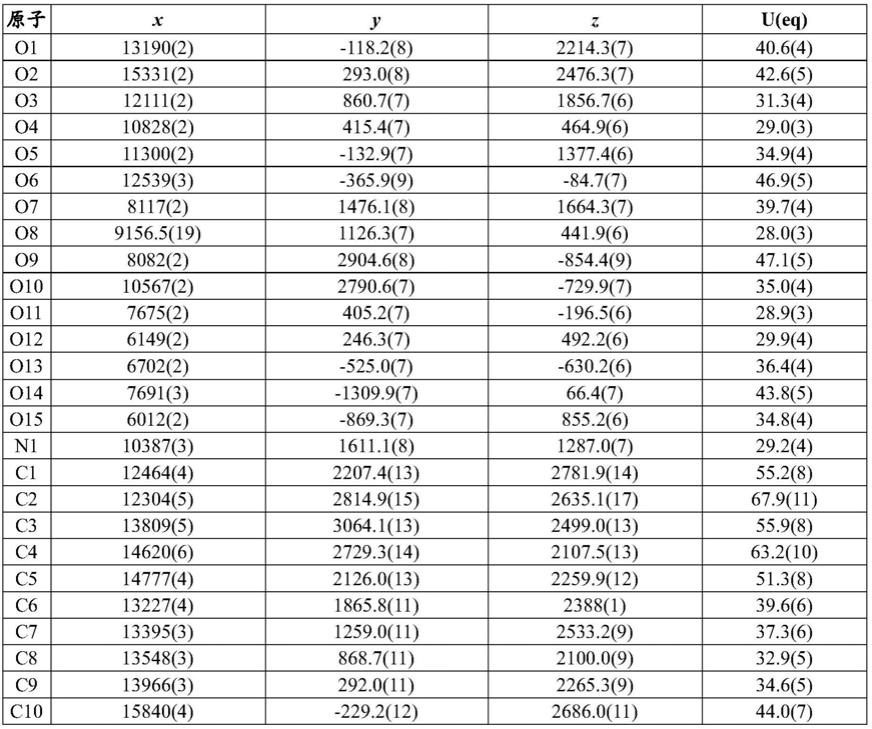
表1说明了结晶化合物8乙醇溶剂化物的分数原子坐标(
×
104)和等效各向同性位移参数u
eq
被定义为正交化u
ij
张量的迹线的1/3。表1
[0105]
表2说明了结晶化合物8乙醇溶剂化物的各向异性位移参数各向异性位移因子指数采用以下形式:-2π2[h2a*2u
11
+2hka*b*u
12
+
…
]。表2
[0106]
表3说明了结晶化合物8乙醇溶剂化物的键长。表3
[0107]
表4说明了结晶化合物8乙醇溶剂化物的键角。表4
[0108]
表5说明了结晶化合物8乙醇溶剂化物的扭转角。表5
[0109]
表6说明了结晶化合物8乙醇溶剂化物的氢原子坐标和各向同性位移参数表6
实施例3:化合物14的热重/差热分析
[0110]
将约5mg结晶化合物14称量到开口铝盘中,装载到同时的热重/差热分析仪(tg/dta)中并保持在室温下。然后以10℃/min的速率将样品从20℃加热至300℃,在此期间记录样品重量的变化以及任何差热事件(dta)。使用氮气作为吹扫气体,流速为300cm3/min。直到熔融时才观察到显著的质量损失。参见图3。实施例4:化合物14的差示扫描量热法
[0111]
将约5mg结晶化合物14称量到铝dsc盘中并用穿孔的铝盖透气地密封。然后将样品盘装入冷却并保持在20℃的seiko dsc6200(配备有冷却器)中。一旦获得稳定的热流响应,以10℃/min的扫描速率将样品和参比加热至190℃并监测所得的热流响应。使用氮气作为吹扫气体,流速为50cm3/min。检测到单一吸热,起始为169.7℃,峰值为171.4℃(82.3mj/mg)。参见图4。实施例5:化合物14的晶体结构表征
[0112]
xrpd分析在panalytical x’pert pro上进行,在3与35
°
2θ之间扫描样品。将结晶化合物14轻轻研磨以释放任何凝聚物并装载到具有kapton或mylar聚合物膜的多孔板上以支撑样品。然后将多孔板放置到衍射仪中,并使用40kv/40ma发电机设置使用以传输模式(步长0.0130
°
2θ)运行的cu k辐射(α1:α2比率=0.5)进行分析。xrpd谱图产生了总结在图2和下表7中的结果。表7
[0113]
本文所述的xrpd峰应理解为反映2θ信号和d-间距信号的
±
0.2的精度。本公开内容还完全并入了美国药典的第941节和来自2014年的国家处方集(usp 37/nf 32,第1卷),其涉及通过xrpd进行的结晶和部分结晶固体的表征。实施例6:化合物14的单晶x射线分析
[0114]
已经通过在环境条件下在己烷缓慢扩散至化合物14的thf溶液中生长的合适晶体的单晶x射线衍射来确定化合物14的绝对结构。
[0115]
在agilent technologies(双源)supernova衍射仪上使用单色辐射进行sxrd分析。该衍射仪配备有oxford cryosystems低温装置,以使数据收集能够在120(1)k下进行,并且晶体被包裹在paratone油的保护层中。基于作为crysalispro软件包(agilent technologies,2014)的一部分实施的多面晶体模型中的高斯积分来校正所收集的数据的吸收效应。
[0116]
通过直接方法(shelxs97)求解该结构,并通过经由olex2软件包对界面上的f(shelxl97)进行全最小二乘精修来开发。经由olex2完成产生的图像。参见sheldrick,
g.m.acta cryst.sect.a 2008,64,112;dolomanov,o.v.,bourhis,l.j.,gildea,r.j.,howard,j.a.k.,puschmann,h.j appl.cryst.2009,42,339-341。
[0117]
在正交空间群p212121中收集、求解和精修数据,并使用platon的addsymm例行程序进行更高度量对称性的搜索,但未能揭示任何更高阶的对称性。参见le page,y.j.appl.cryst.1987,20,264;le page,y.j.appl.cryst.1988,21,983;spek a.l.,acta cryst.2009,d65,148。
[0118]
所有非氢原子位于傅立叶图中,并且在各向异性地描述所有非氢原子的热运动之前精修它们的位置。在该结构内,仅在不对称单元内发现了一个完整的结晶学上独立的化合物14式单元。在最终结构中没有观察到或模拟出无序。
[0119]
使用具有固定uiso的骑乘模型将所有氢原子置于计算位置,对于所有的ch、ch2和nh基团为1.2倍,以及对于所有的ch3和oh基团为1.5倍。
[0120]
发现最高残余傅立叶峰为距c(59)约的以及发现最深的傅立叶孔为距c21约的
[0121]c61h79
no
15
(m=1066.25g/mol)的晶体数据:正交晶系空间群p212121(编号:19),z=4,t=120(1)k,μ(cukα)=0.702mm-1
,dcalc=1.211g/cm3,404815个测量的反射(6.408
°
≤2θ≤153.014
°
),12200个独特的(r
int
=0.1016,r
sigma
=0.0309),将其用于所有计算中。最终的r1为0.0435(i》2σ(i))以及wr2为0.1152(所有数据)。
[0122]
化合物14的结构特征。发现所收集的结构的晶胞尺寸如下:空间群:正交晶系空间群p212121α=90
°
β=90
°
γ=90
°
z=4,z`=2发现不对称单元仅含有一个完整的化合物14式单元。最终的精制参数如下:r1[i》2σ(i)]=4.35%goof(拟合优度)=1.066wr2(所有数据)=11.52%r
int
=10.16%(12200个独立的反射)flack参数=-0.03(5)(100%friedel覆盖率)
[0123]
表8说明了结晶化合物14的分数原子坐标(
×
104)和等效各向同性位移参数u
eq
被定义为正交化u
ij
张量的迹线的1/3。表8
[0124]
表9说明了结晶化合物14的各向异性位移参数各向异性位移因子指数采用以下形式:-2π2[h2a*2u
11
+2hka*b*u
12
+
…
]。表9
[0125]
表10说明了结晶化合物14的键长。表10
[0126]
表11说明了结晶化合物14的键角。表11
[0127]
表12说明了结晶化合物14的扭转角。表12
[0128]
表13说明了结晶化合物14的氢原子坐标和各向同性位移参数表13
实施例7:化合物15乙醇溶剂化物水合物的单晶x-射线分析
[0129]
将化合物15(10mg)溶解在2ml透明玻璃小瓶中的(无水)乙醇(400ul)中并加入水(200ul)。将该小瓶加盖,并在5℃下静置约3周。在三周之后,注意到小的板状晶体在溶液弯月面下生长,这似乎适于通过单晶x射线衍射进行询问。
[0130]
使用agilent supernova双源仪器使用由密封管产生的cu kα辐射进行sxrd分析。该衍射仪配备有oxford cryosystems低温装置,以使数据收集能够在120(1)k下进行,并且晶体被包裹在paratone油的保护层中。收集在手性单斜晶
体的空间群c2中求解和精修的几个数据集。使用球面谐波(scale3 abspack)作为crysalispro软件包(agilent technologies,2014)的一部分的经验校正来校正吸收效应。
[0131]
通过直接方法(shelxs97)求解该结构,并通过经由olex2软件包对界面上的f(shelxl97)进行全最小二乘精修来开发。经由olex2完成产生的图像。参见sheldrick,g.m.acta cryst.sect.a 2008,64,112;dolomanov,o.v.,bourhis,l.j.,gildea,r.j.,howard,j.a.k.,puschmann,h.j appl.cryst.2009,42,339-341。
[0132]
使用platon的addsymm例行程序进行更高度量对称性的搜索,但未能揭示任何更高阶的对称性。参见le page,y.j.appl.cryst.1987,20,264;le page,y.j.appl.cryst.1988,21,983;spek a.l.,acta cryst.2009,d65,148。所有非氢原子位于傅立叶图中,并且在各向异性地描述所有非氢原子的热运动之前精修它们的位置。在该结构内,在电子密度的两个口袋旁边的不对称单元内发现了一个完整的化合物15式单元,所述口袋很好地精修了占用率为0.67的水分子和占用率为0.33的乙醇分子。除了将原子的热运动限制为接近各向同性行为之外,对于c-c长度,乙醇分子内的键长被限制为对于c-o,乙醇分子内的键长被限制为1.44(2)。除了这种溶剂空隙(void)之外,发现母体化合物15分子的甲氧基-醚臂是无序的,因此,在两个具有相同占用率的位置上进行了建模。
[0133]
使用具有固定uiso的骑乘模型将所有氢原子置于计算位置,对于所有的ch、ch2和nh基团为1.2倍,以及对于所有的ch3和oh基团为1.5倍。
[0134]
发现最高残余傅立叶峰为距c(36)约的以及发现最深的傅立叶孔为距o(11)约的
[0135]c33.33h58.33
no
16
(m=729.37g/mol)的晶体数据:单斜晶体的空间群c2(编号:5),α=90
°
,β=95.885(4)
°
,β=90
°
,z=4,t=120(1)k,μ(cukα)=0.860mm-1
,dcalc=1.290g/cm3,114512个测量的反射(6.896
°
≤2θ≤162.986
°
),7536个独特的(r
int
=0.1458,r
sigma
=0.0766),将其用于所有计算中。最终的r1为0.0842(i》2σ(i))以及wr2为0.2463(所有数据)。
[0136]
化合物15乙醇溶剂化物水合物的结构特征。发现所收集的结构的晶胞尺寸如下:空间群:单斜晶体的i2α=90
°
β=95.819(8)
°
γ=90
°
z=4,z`=1发现不对称单元含有一个完整的化合物15式单元,其具有小区域的无序电子密度,等于38个电子/晶胞(9.5个电子/不对称单元),目前精修为水占用率为0.67(以及乙醇占用率为0.33)处部分占用的混合水/乙醇空隙。注意:每个完整的水有10个电子,以及每个完整的乙醇分子有18个电子。最终的精修参数如下:
r1[i》2σ(i)]=8.42%goof(拟合优度)=1.010wr2(所有数据)=24.63%r
int
=14.58%flack参数=0.3(2)
[0137]
表14说明了结晶化合物15乙醇溶剂化物水合物的分数原子坐标(
×
104)和等效各向同性位移参数u
eq
被定义为正交化u
ij
张量的迹线的1/3。表14
[0138]
表15说明了结晶化合物15乙醇溶剂化物水合物的各向异性位移参数各向异性位移因子指数采用以下形式:-2π2[h2a*2u
11
+2hka*b*u
12
+
…
]。表15
[0139]
表16说明了结晶化合物15乙醇溶剂化物水合物的键长。表16
[0140]
表17说明了结晶化合物15乙醇溶剂化物水合物的键角。表17
[0141]
表18说明了结晶化合物15乙醇溶剂化物水合物的氢原子坐标和各向同性位移参数
表18
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1