使用白介素-17(IL-17)拮抗剂治疗扁平苔藓的方法与流程
使用白介素-17(il-17)拮抗剂治疗扁平苔藓的方法
技术领域
1.本披露涉及使用il-17拮抗剂(例如il-17抗体,如苏金单抗)治疗扁平苔藓(lp)和毛发扁平苔藓(lpp)的方法。
背景技术:
2.扁平苔藓(lp)是慢性、炎症性障碍,其可累及皮肤、口腔或生殖器黏膜、结膜和指甲(有时伴随性累及),同时维持一致的组织学表型。该疾病在皮肤上(皮肤扁平苔藓(clp))呈现为多发性丘疹,其可以是局部的或泛发性的,通常非常痒和疼痛。黏膜疾病(黏膜扁平苔藓(mlp))可以由无症状斑块或非常疼痛的糜烂性病变和溃疡组成。毛发扁平苔藓(lpp),一种毛囊形式的扁平苔藓,是罕见的炎症性淋巴细胞介导的障碍,可选择性地累及毛囊。lpp会导致毛囊破坏,并因此导致瘢痕性脱发(assouly等人(2009)semin cutan med surg.[皮肤医学和外科研讨论文集]28:3-10)。clp和mlp亚型之间存在广泛的临床重叠,其中许多患者呈现出重叠的症状和病变。同时,每一个亚型存在于不同的解剖区域,并且具有不同临床特征,例如溃疡可存在于黏膜亚型,但不存在于皮肤亚型,以及毛囊炎症是毛发扁平苔藓的独特特征。
[0003]
lp影响多达5%的全球人口。口腔或生殖器受累发生于60%-70%的患者,并且它可能是20%-30%患者中的唯一疾病表现。病程是不可预测的,典型地持续1-2年,但可能遵循慢性复发性病程。尽管在临床实践中相当频繁地遇到lp并且其预示着对健康相关的生活质量的负面影响,但仍缺乏致力于表征lp的管理和适当治疗的努力。
[0004]
目前使用的疗法大多是对症的,并采用广谱免疫抑制或抗炎局部疗法(例如皮质类固醇)和全身疗法来进行姑息性治疗而不是治愈性治疗。全身性免疫抑制剂(例如糖皮质激素、环孢素、甲氨蝶呤和硫唑嘌呤),以及免疫调节剂(例如阿维a),有助于减轻疾病症状,但在长期治疗后会导致显著的副作用。此外,30%-50%的患者对目前的lp疗法是难治性的,并且由于缺乏临床控制而经历更高的疾病负担,以及显著的心理不适和社会功能缺陷,从而导致生活质量严重受损。
[0005]
鉴于lp的严重性,以及其长期性和对患者生活质量的影响,对于用于治疗lp的安全有效疗法存在高度未满足的医疗需求,特别是对全身性和/或局部疗法的标准护理具有难治性的那些患者。
技术实现要素:
[0006]
苏金单抗(参见例如,wo 2006/013107和wo 2007/117749)是选择性中和人il-17a细胞因子的全人单克隆抗体。它对il-17具有非常高的亲和力,即kd为约100-200pm,并且对于约0.67nm人il-17a的生物学活性的体外中和具有的ic
50
为约0.4nm。因此,苏金单抗以约1:1的摩尔比抑制抗原。这种高结合亲和力使得苏金单抗特别适合用于治疗应用。此外,苏金单抗具有长的半衰期,即约4周,这使得施用之间的时间延长,这是当治疗慢性终生障碍(例如lp)时的特殊特性。
[0007]
几项研究证实,lp患者血清中的il-17a水平升高(pouralibaba,2013)。此外,活检显示由浸润性淋巴细胞产生的il-17a增加。在lpp中,在病变毛囊中检测到il-17ra基因的上调,但在非病变毛囊中未检测到(hobo,2018)。然而,这些研究并未确定il-17a是否是lp的疾病驱动因素,或者il-17a是否仅仅是疾病连带因素(passenger)。事实上,几个病例报告显示用il-17抑制剂苏金单抗治疗后出现苔藓样反应,这表明il-17a可以在预防苔藓样反应中提供保护作用(capusan等人(2018)jaad case reports[jaad病例报告]4:521-3oral lichenoid eruption following secukinumab treatment[苏金单抗治疗后口腔苔藓样疹];doolan等人(2017)j clin exp dermatol[临床与实验皮肤病学杂志]res 9:1cutaneous lichen planus induced by secukinumab[苏金单抗诱导的皮肤扁平苔藓];komori等人(2017)j.derm.[皮肤病学杂志]44:e60-e61oral lichen planus eruption during secukinumab treatment[苏金单抗治疗期间口腔扁平苔藓疹];maglie等人(2018)br.j.derm.[英国皮肤病学杂志]178,296-308oral and cutaneous lichen planus eruption during secukinumab treatment[苏金单抗治疗期间的口腔和皮肤扁平苔藓疹];thompson等人(2016)jaad case reports[jaad病例报告]2:384-6ulcerative,lichenoid mucositis during secukinumab treatment[苏金单抗治疗期间溃疡性苔藓样黏膜炎])。相比之下,solimani等人(2019)front.immunol.[免疫学前沿]10:1808描述了苏金单抗(在第0、1、2、3、4周皮下(s.c.)注射300mg,然后每月治疗)在治疗三名患有急性和慢性顽固性皮肤黏膜lp(即,mlp和clp)的患者中的功效。然而,solimani等人(2019)没有表明对于苏金单抗是否可用于治疗lpp(特别罕见形式的lp)或苏金单抗的其他给药方案是否可以在保持有利的风险/收益特征的同时产生期望的结果。
[0008]
现在,我们已经新设计了新的用il-17拮抗剂,例如il-17抗体或其抗原结合片段(例如苏金单抗)来治疗lp患者(优选地已经对先前用苔藓样疗法的治疗没有充分应答的lp患者),这些治疗是安全、有效的并为患者提供持续应答。
[0009]
在所披露的用途、方法和试剂盒的一些实施例中,该il-17拮抗剂是il-17抗体或其抗原结合片段。在所披露的用途、方法和试剂盒的一些实施例中,该il-17抗体或其抗原结合片段选自由以下组成的组:a)与人il-17的表位结合的il-17抗体或其抗原结合片段,该表位包含leu74、tyr85、his86、met87、asn88、val124、thr125、pro126、ile127、val128、his129;b)与人il-17的表位结合的il-17抗体或其抗原结合片段,该表位包含tyr43、tyr44、arg46、ala79、asp80;c)与具有两条成熟人il-17蛋白质链的il-17同源二聚体的表位结合的il-17抗体或其抗原结合片段,所述表位包含在一条链上的leu74、tyr85、his86、met87、asn88、val124、thr125、pro126、ile127、val128、his129和在另一条链上的tyr43、tyr44、arg46、ala79、asp80;d)与具有两条成熟人il-17蛋白质链的il-17同源二聚体的表位结合的il-17抗体或其抗原结合片段,所述表位包含在一条链上的leu74、tyr85、his86、met87、asn88、val124、thr125、pro126、ile127、val128、his129和在另一条链上的tyr43、tyr44、arg46、ala79、asp80,其中该il-17抗体或其抗原结合片段具有的kd为约100-200pm,并且其中该il-17抗体或其抗原结合片段具有的体内半衰期为约23至约35天;e)与具有两条成熟il-17蛋白质链的il-17同源二聚体的表位结合的il-17抗体,所述表位包含在一条链上的leu74、tyr85、his86、met87、asn88、val124、thr125、pro126、ile127、val128、his129和在另一条链上的tyr43、tyr44、arg46、ala79、asp80,其中如通过生物传感器系统(例如
biacore)所测量的,该il-17抗体具有的kd为约100-200pm,并且其中该il-17抗体具有的体内半衰期为约23至约30天;和f)il-17抗体或其抗原结合片段,该抗体或其抗原结合片段包括:i)包含seq id no:8中所列出的氨基酸序列的免疫球蛋白重链可变结构域(vh);ii)包含seq id no:10中所列出的氨基酸序列的免疫球蛋白轻链可变结构域(v
l
);iii)包含seq id no:8中所列出的氨基酸序列的免疫球蛋白vh结构域以及包含seq id no:10中所列出的氨基酸序列的免疫球蛋白v
l
结构域;iv)包含seq id no:1、seq id no:2和seq id no:3中所列出的高变区的免疫球蛋白vh结构域;v)包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;vi)包含seq id no:11、seq id no:12和seq id no:13中所列出的高变区的免疫球蛋白vh结构域;vii)包含seq id no:1、seq id no:2和seq id no:3中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;viii)包含seq id no:11、seq id no:12和seq id no:13中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;ix)包含seq id no:14中所列出的氨基酸序列的免疫球蛋白轻链;x)包含seq id no:15中所列出的氨基酸序列的免疫球蛋白重链;或xi)包含seq id no:14中所列出的氨基酸序列的免疫球蛋白轻链和包含seq id no:15中所列出的氨基酸序列的免疫球蛋白重链。
[0010]
本文披露了治疗毛发扁平苔藓(lpp)的方法,这些方法包括在第0、1、2、3和4周期间,每周向有需要的患者皮下(sc)施用剂量约150mg-约300mg的白介素(il)-17抗体或其抗原结合片段,并且此后从第8周期间开始,每四周进行施用,其中该il-17抗体或其抗原结合片段包含:
[0011]
i)包含seq id no:8中所列出的氨基酸序列的免疫球蛋白可变重(vh)结构域以及包含seq id no:10中所列出的氨基酸序列的免疫球蛋白可变轻(v
l
)结构域;
[0012]
ii)包含seq id no:1、seq id no:2和seq id no:3中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;或
[0013]
iii)包含seq id no:11、seq id no:12和seq id no:13中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域。
[0014]
本文披露了治疗扁平苔藓(lp)的治疗方法,这些方法包括在第0、1、2、3和4周期间,每周向有需要的患者皮下(sc)施用剂量约150mg-约300mg的白介素(il)-17抗体或其抗原结合片段,并且此后从第6周期间开始每两周进行施用,其中,该il-17抗体或其抗原结合片段包含:
[0015]
i)包含seq id no:8中所列出的氨基酸序列的免疫球蛋白可变重(vh)结构域以及包含seq id no:10中所列出的氨基酸序列的免疫球蛋白可变轻(v
l
)结构域;
[0016]
ii)包含seq id no:1、seq id no:2和seq id no:3中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;或
[0017]
iii)包含seq id no:11、seq id no:12和seq id no:13中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的
免疫球蛋白v
l
结构域。
[0018]
本文披露了治疗扁平苔藓(lp)的治疗方法,这些方法包括在第0周期间向有需要的患者静脉内(iv)施用一次剂量约4mg/kg-约9mg/kg(优选地约6mg/kg)的白介素(il)-17抗体或其抗原结合片段,并且此后从第4周期间开始每四周施用iv剂量约2mg/kg-约4mg/kg(优选地约3mg/kg)的il-17抗体或其抗原结合片段,其中,该il-17抗体或其抗原结合片段包含:
[0019]
i)包含seq id no:8中所列出的氨基酸序列的免疫球蛋白可变重(vh)结构域以及包含seq id no:10中所列出的氨基酸序列的免疫球蛋白可变轻(v
l
)结构域;
[0020]
ii)包含seq id no:1、seq id no:2和seq id no:3中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;或
[0021]
iii)包含seq id no:11、seq id no:12和seq id no:13中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域。
[0022]
在优选的实施例中,以150mg或300mg的剂量皮下(sc)施用il-17拮抗剂(例如,il-17抗体或其抗原结合片段,例如苏金单抗)。在其他优选实施例中,以6mg/kg或3mg/kg的剂量静脉(iv)施用il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗)。
[0023]
在一些实施例中,使用诱导方案,随后是维持方案,施用il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗)。在一些实施例中,诱导方案包括每周施用,并且维持方案包括每两周、每四周(每月)、或每八周(每隔一月)施用。在一些实施例中,诱导方案包括一次施用,并且维持方案包括每四周(每月)施用。在一些实施例中,诱导方案包括每四周(每月)施用,并且维持方案包括每八周(每隔一月)施用。
[0024]
在一些实施例中,在诱导和维持方案期间,以约300mg的剂量sc施用il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗)。在一些实施例中,在诱导和维持方案期间,以约150mg的剂量sc施用il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗)。
[0025]
在一些实施例中,在诱导方案期间,以约6mg/kg的剂量iv施用il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗)。在一些实施例中,在维持方案期间,以约3mg/kg的剂量iv施用il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗)。
[0026]
在所披露的用途、方法和试剂盒的一些实施例中,il-17抗体或其抗原结合片段是人抗体或人源化抗体。在所披露的用途、方法和试剂盒的一些实施例中,il-17抗体或其抗原结合片段是苏金单抗。
[0027]
本文披露了治疗患有毛发扁平苔藓(lpp)的成年患者的治疗方法,该患有毛发扁平苔藓的成年患者用局部皮质类固醇疗法不能充分控制或者局部皮质类固醇疗法对该患者是不可取的,这些方法包括在第0、1、2、3和4周期间向所述患者皮下施用剂量约300mg苏金单抗,然后在此之后每四周进行施用。
[0028]
本文披露了治疗患有扁平苔藓(lp)的成年患者的治疗方法,该患有扁平苔藓的成年患者用局部皮质类固醇疗法不能充分控制或者局部皮质类固醇疗法对该患者是不可取的,这些方法包括在第0、1、2、3和4周期间向所述患者皮下施用剂量约300mg苏金单抗,然后
在此之后每两周进行施用。
[0029]
本文披露了治疗患有扁平苔藓(lp)的成年患者的治疗方法,该患有扁平苔藓的成年患者用局部皮质类固醇疗法不能充分控制或者局部皮质类固醇疗法对该患者是不可取的,这些方法包括在第0周期间,向该患者静脉内(iv)施用一次剂量约6mg/kg的苏金单抗,并且此后从第4周期间开始,每四周施用iv剂量约3mg/kg的苏金单抗。
附图说明
[0030]
图1示出了基于苏金单抗的lp人临床试验的研究设计。入组本试验的患者将有经活检证实形式的lp(lpp、clp或mlp),该lp用局部疗法不能充分控制。在治疗期1中,所有患者在第0、1、2、3和4周每周接受一次盲法研究药物(300mg苏金单抗或安慰剂)的sc注射,然后在此之后每4周接受一次。在从第16周开始的治疗期2中,在治疗期1期间处于安慰剂治疗组的患者将被转换为每2周使用300mg的sc苏金单抗治疗,从初始的常规诱导方案开始(每周五次sc注射300mg),然后维持每2周sc苏金单抗300mg。
[0031]
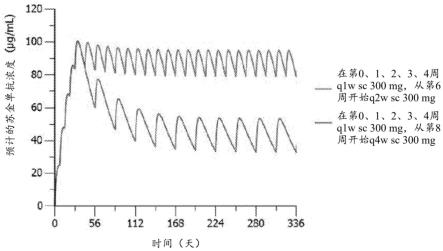
图2示出了在维持方案期间使用每2周和每4周给药间隔预测的300mg苏金单抗的全身性暴露。
具体实施方式
[0032]
如本文所用,il-17是指白介素-17a(il-17a)。
[0033]
术语“包含”涵盖“包括”以及“由
……
组成”,例如,“包含”x的组合物可以仅由x组成或可以包括其他物质,例如x+y。
[0034]
除非另外特别说明或从上下文中显而易见,否则如本文所用,关于数值的术语“约”应理解为在本领域的正常公差内,例如,在平均值的两个标准偏差内。因此,“约”可以在所述值的+/-10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.1%、0.05%或0.01%内,优选地,所述值的+/-10%内。当在数值范围或数字列表前使用时,术语“约”适用于系列中的每个数字,例如,短语“约1-5”应被解释为“约1-约5”,或例如,短语“约1、2、3、4”应被解释为“约1、约2、约3、约4等”。
[0035]
单词“基本上”不排除“完全”,例如,“基本上不含”y的组合物可以完全不含y。必要时,本披露的定义中可以省略单词“基本上”。
[0036]
本文提及的术语“抗体”包括天然存在的和完整的抗体。天然存在的“抗体”是包含由二硫键互相连接的至少两条重(h)链和两条轻(l)链的糖蛋白。每条重链由重链可变区(在本文缩写为vh)和重链恒定区构成。重链恒定区包含三个结构域,即ch1、ch2和ch3。每条轻链由轻链可变区(在本文缩写为v
l
)和轻链恒定区构成。轻链恒定区包含一个结构域,即cl。vh和v
l
区可进一步细分为被称为高变区或互补决定区(cdr)的高变区,它们散布着被称为框架区(fr)的更保守的区域。每个vh和v
l
由从氨基末端排到羧基末端按以下顺序排列的三个cdr和四个fr构成:fr1、cdr1、fr2、cdr2、fr3、cdr3、fr4。重链和轻链的可变区含有与抗原相互作用的结合结构域。抗体的恒定区可以介导免疫球蛋白与宿主组织或因子(包括免疫系统的多种细胞(例如,效应细胞)和经典补体系统的第一成分(c1q))的结合。示例性抗体包括苏金单抗(表1)、抗体xab4(美国专利号9,193,788)、和艾克司单抗(ixekizumab)(美国专利号7,838,638),这些抗体的披露内容通过引用以其全文并入本文。
[0037]
如本文所用,术语抗体的“抗原结合片段”是指保留特异结合抗原(例如,il-17)的能力的抗体的片段。已经显示,全长抗体的片段可以执行抗体的抗原结合功能。涵盖在术语抗体的“抗原结合部分”内的结合片段的实例包括fab片段,一种由v
l
、vh、cl和ch1结构域组成的单价片段;f(ab)2片段,包含在铰链区通过二硫桥连接的两个fab片段的二价片段;fd片段,其由vh和ch1结构域组成;fv片段,其由抗体的单臂的v
l
和vh结构域组成;由vh结构域组成的dab片段(ward等人,1989,nature[自然]341:544-546);和分离的cdr。示例性抗原结合片段包括在seq id no:1-6和11-13(表1)中列出的苏金单抗的cdr,优选重链cdr3。此外,虽然fv片段的两个结构域v
l
和vh是由单独的基因编码的,但是可以使用重组方法将这两个结构域通过能够使它们形成为单条蛋白质链的合成接头来相连,其中v
l
区和vh区配对形成单价分子(被称为单链fv(scfv);参见例如,bird等人,1988science[科学]242:423-426;和huston等人,1988proc.natl.acad.sci.[美国国家科学院院刊]85:5879-5883)。这种单链抗体也旨在涵盖于术语“抗体”的范围内。使用本领域技术人员已知的常规技术获得单链抗体和抗原结合部分。
[0038]
如本文所用,“分离的抗体”是指基本上不含具有不同抗原特异性的其他抗体的抗体(例如,特异性结合il-17的分离的抗体基本上不含特异性结合除il-17以外的抗原的抗体)。如本文所用的术语“单克隆抗体”或“单克隆抗体组合物”是指具有单一分子组成的抗体分子的制剂。如本文所用,术语“人抗体”旨在包括具有可变区的抗体,其中框架区和cdr区二者都源自人来源的序列。“人抗体”无需由人、人组织或人细胞产生。本披露的人抗体可以包括不由人序列编码的氨基酸残基(例如,通过体外随机或位点特异性诱变引入的突变,通过抗体基因重组期间在体内连接处的n-核苷酸添加,或通过体内体细胞突变)。在所披露的程序和组合物的一些实施例中,il-17抗体是人抗体、分离的抗体和/或单克隆抗体。
[0039]
术语“il-17”是指il-17a,先前被称为ctla8,并且包括来自不同物种(例如,人、小鼠、和猴)的野生型il-17a、il-17a的多态变体和il-17a的功能等同物。根据本披露的il-17a的功能等同物与野生型il-17a(例如,人il-17a)优选具有至少约65%、75%、85%、95%、96%、97%、98%、或甚至99%总体序列同一性,并且基本上保留了诱导人真皮成纤维细胞产生il-6的能力。
[0040]
术语“k
d”旨在指特定抗体-抗原相互作用的解离速率。如本文所用,术语“k
d”旨在指由kd与ka的比率(即kd/ka)获得并表达为摩尔浓度(m)的解离常数。可以使用本领域建立的方法确定抗体的kd值。用于确定抗体的kd的优选的方法是通过使用表面等离子体共振,或使用生物传感器系统(例如系统)。在一些实施例中,il-17抗体或其抗原结合片段(例如苏金单抗)结合人il-17,其中kd为约100-250pm。
[0041]
术语“亲和力”是指抗体和抗原在单个抗原位点处的相互作用强度。在每个抗原位点内,抗体“臂”的可变区通过弱非共价力在许多位点处与抗原相互作用;相互作用越多,亲和力越强。用于评估抗体对各种物种的il-17的结合亲和力的标准测定法是本领域已知的,包括例如elisa、蛋白质印迹和ria。抗体的结合动力学(例如,结合亲和力)也可以通过本领域已知的测定法来评估,例如使用分析。
[0042]
根据本领域已知的和本文所述的方法确定的“抑制”一种或多种这些il-17功能特性(例如,生物化学、免疫化学、细胞、生理学或其他生物学活性等)的抗体将被理解为,相对于不存在抗体时(或当存在不相关特异性的对照抗体时)观察到的特定活性,涉及特定活性
在统计学上显著的降低。抑制il-17活性的抗体影响统计学上显著的降低,例如,降低了至少约10%的测量参数,降低了至少50%、80%或90%,并且在所披露的方法和组合物的某些实施例中,使用的il-17抗体可以抑制大于95%、98%或99%的il-17功能活性。
[0043]
如本文所用的“抑制il-6”是指il-17抗体或其抗原结合片段(例如,苏金单抗)降低原代人真皮成纤维细胞产生il-6的能力。原代人(真皮)成纤维细胞中il-6的产生依赖于il-17(hwang等人,(2004)arthritis res ther[关节炎研究与治疗];6:r120-128)。简言之,在不同浓度的il-17结合分子或具有fc部分的人il-17受体的存在下用重组il-17刺激人真皮成纤维细胞。可以将嵌合的抗cd25抗体(巴利昔单抗)方便地用作阴性对照。16h刺激后取上清液并通过elisa测定il-6。当如以上测试时,il-17抗体或其抗原结合片段(例如苏金单抗)典型地具有的抑制il-6产生(在1nm人il-17的存在下)的ic
50
为约50nm或更低(例如,从约0.01至约50nm),即所述抑制活性是对人真皮成纤维细胞中由hu-il-17诱导的il-6产生而测量的。在所披露的方法和组合物的一些实施例中,如以上所定义的,il-17抗体或其抗原结合片段(例如苏金单抗)及其功能衍生物具有的抑制il-6产生的ic
50
为约20nm或更低、更优选地约10nm或更低、更优选地约5nm或更低、更优选地约2nm或更低、更优选地约1nm或更低。
[0044]
除非另有说明,根据本披露,术语“衍生物”用于定义il-17抗体或其抗原结合片段(例如苏金单抗)的例如特定序列(例如,可变结构域)的氨基酸序列变体和共价修饰(例如,聚乙二醇化、脱酰胺作用、羟基化、磷酸化、甲基化等)。“功能衍生物”包括具有与所披露的il-17抗体一样的定性的生物学活性的分子。功能衍生物包括如本文披露的il-17抗体的片段和肽类似物。片段包含根据本披露(例如,指定序列)的多肽序列内的区域。本文披露的il-17抗体的功能衍生物(例如,苏金单抗的功能衍生物)优选地包含与本文披露的il-17抗体和其抗原结合片段的vh和/或v
l
序列(例如,表1的vh和/或v
l
序列)具有至少约65%、75%、85%、95%、96%、97%、98%、或甚至99%总体序列同一性的vh和/或v
l
结构域,并且基本上保留与人il-17结合的能力,或例如抑制il-17诱导的人真皮成纤维细胞的il-6产生。
[0045]
短语“基本上相同”意指与特定参考序列相比,相关氨基酸或核苷酸序列(例如,vh或v
l
结构域)与其相同或具有非实质性差异(例如,通过保守氨基酸取代)。非实质性差异包括微小的氨基酸变化,例如在特定区域(例如,vh或v
l
结构域)的5个氨基酸序列中的1个或2个取代。在抗体的情况下,第二抗体具有相同的特异性并且具有其至少50%的亲和力。与本文披露的序列基本上相同(例如,具有至少约85%序列同一性)的序列也是本技术的一部分。在一些实施例中,相对于所披露的序列,衍生物il-17抗体(例如,苏金单抗的衍生物,例如苏金单抗生物类似抗体)的序列同一性可以是约90%或更高,例如90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高。
[0046]
关于天然多肽与其功能衍生物的“同一性”在本文中定义为,在将序列比对及必要时引入空位以实现最大百分比同一性,且不考虑任何保守性取代为序列同一性部分之后,候选序列中与相应天然多肽的残基相同的氨基酸残基的百分比。n-末端或c-末端延伸与插入均不应解释为降低同一性。用于比对的方法及计算机程序是已知的。百分比同一性可以通过标准比对算法确定,例如altshul等人描述的基于局部比对搜索工具(blast)((1990)j.mol.biol.[分子生物学杂志],215:403 410);needleman等人的算法((1970)j.mol.biol.[分子生物学杂志],48:444453);或者meyers等人的算法((1988)
comput.appl.biosci.[生物科学中的计算机应用],4:11 17)。一组参数可以是具有空位罚分12、空位延伸罚分4、以及移码空位罚分5的blosum 62评分矩阵。也可使用已经整合到align程序(版本2.0)中的e.meyers和w.miller((1989)cabios[生物科学中的计算机应用],4:11-17)的算法,使用pam120权重残基表、空位长度罚分12和空位罚分4确定两个氨基酸或核苷酸序列之间的百分比同一性。
[0047]“一个或多个氨基酸”是指例如所有天然存在的l-α-氨基酸且包括d-氨基酸。短语“氨基酸序列变体”是指当与根据本披露的序列相比时其氨基酸序列具有一些差异的分子。根据本披露的抗体的氨基酸序列变体,例如特定序列的变体仍然具有与人il-17结合的能力或例如抑制il-17诱导的人真皮成纤维细胞的il-6产生的能力。氨基酸序列变体包括取代性变体(去除至少一个氨基酸残基且在根据本披露的多肽中的相同位置插入不同氨基酸的那些变体)、插入性变体(紧邻根据本披露的多肽中的特定位置处的氨基酸插入一个或多个氨基酸的那些变体)以及缺失性变体(在根据本披露的多肽中去除一个或多个氨基酸的那些变体)。
[0048]
术语“药学上可接受的”意指不干扰一种或多种活性成分的生物活性的有效性的无毒性材料。
[0049]
关于化合物(例如,il-17结合分子或另一种试剂)的术语“施用”用于指通过任何途径将所述化合物递送至患者。
[0050]
如本文所用,短语“受影响的位置”是指患者身体上示出lp迹象的任何位置,例如口腔、生殖器、结膜、头发等。
[0051]
如本文所用,短语“活性斑块”是指示出正在经历免疫失调、炎症、肿胀、疼痛、瘙痒等迹象的受影响的位置。
[0052]
如本文所用,“治疗有效量”是指il-17拮抗剂(例如,il-17结合分子(例如,il-17抗体或其抗原结合片段,如苏金单抗)或il-17受体结合分子(例如,il-17抗体或其抗原结合片段))的量,在以单剂量或多剂量向患者(例如,人)施用时,有效地治疗、预防、防止障碍或复发的障碍的发作,治愈、延迟、减少障碍或复发的障碍的严重程度,减轻障碍或复发的障碍的至少一种症状,或延长患者的存活使其超过在没有这种治疗下所预期的存活期。当应用于单独施用的单独活性成分(例如,il-17拮抗剂,例如苏金单抗)时,该术语仅指所述成分。当应用于组合时,该术语是指产生治疗作用的活性成分(无论连续还是同时组合施用)的组合量。
[0053]
术语“治疗(treatment或treat)”在本文中被定义为根据本披露的il-17抗体(例如,苏金单抗或艾克司单抗)或包含所述抗il-17抗体的药物组合物向受试者或向来自受试者的分离的组织或细胞系的应用或施用,其中所述受试者患有特定的疾病(例如lp,如皮肤扁平苔藓(clp)、黏膜扁平苔藓(mlp)、毛发扁平苔藓(lpp)或其组合),与疾病(例如lp,如clp、mlp、lpp或其组合)相关的症状,或具有发展为该疾病(例如lp,如clp、mlp、lpp或其组合)的倾向(如果适用),其中目的是治愈(如果适用)疾病,延迟疾病的发作,降低疾病严重性,减缓、改善疾病的一种或多种症状,改善疾病,减少或改善任何与疾病相关的症状或向疾病发展的倾向。术语“治疗(treatment或treat)”包括治疗怀疑患有疾病的患者以及患病或已诊断患有疾病或医学病症的患者,并且包括遏制临床复发。
[0054]
如本文所用,短语“患者群体”用于意指一组患者。在所披露的方法的一些实施例
中,il-17拮抗剂(例如il-17抗体,例如苏金单抗)用于治疗lp(例如,clp、mlp、lpp或其组合)患者群体。
[0055]
如本文所用,关于患者的“选择(selecting)”和“被选(selected)”用于意指基于(由于)具有预定标准的特定患者,特定患者是从更大的患者组中特别选择的。类似地,“选择性治疗”是指向患有特定疾病的患者提供治疗,其中此患者是基于具有预定标准的特定患者从较大的患者组中特别选择的。类似地,“选择性施用”是指向患者施用药物,该患者是基于(由于)具有预定标准的特定患者从较大的患者组中特别选择的。通过选择、选择性治疗和选择性施用,意味着基于患者的个人病史(例如,先前的治疗干预,例如先前用生物制剂治疗),生物学特征(例如,特定的遗传标记),和/或表现(例如,不满足特定的诊断标准)向患者递送个性化疗法,而不是仅仅基于患者在较大组中的成员资格而递送标准治疗方案。参考如本文所用的治疗方法,选择不是指对具有特定标准的患者的偶然治疗,而是指基于具有特定标准的患者对患者施用治疗的有意选择。因此,选择性治疗/施用不同于标准治疗/施用,标准治疗/施用向患有特定疾病的所有患者递送特定药物,而不考虑这些患者的个人病史、疾病表现和/或生物学特征。在一些实施例中,基于患有lp(例如,clp、mlp、lpp或其组合),选择患者以使用il-17拮抗剂(例如il-17抗体或其抗原结合片段,如苏金单抗)进行治疗。在一些实施例中,基于患有活动性lp(例如,clp、mlp、lpp或其组合),选择患者以使用il-17拮抗剂(例如il-17抗体或其抗原结合片段,如苏金单抗)进行治疗。在一些实施例中,基于患有稳定型皮肤lp(例如,clp、mlp、lpp或其组合),选择患者以使用il-17拮抗剂(例如il-17抗体或其抗原结合片段,如苏金单抗)进行治疗。在一些实施例中,基于先前对在先的苔藓样疗法有不充分的应答,选择患者以使用il-17拮抗剂(例如il-17抗体或其抗原结合片段,如苏金单抗)进行治疗。在一些实施例中,基于对局部皮质类固醇疗法的难治性,选择患者以使用il-17拮抗剂(例如il-17抗体或其抗原结合片段,如苏金单抗)进行治疗。在一些实施例中,基于先前对局部类固醇有不充分的应答,选择患者以使用il-17拮抗剂(例如il-17抗体或其抗原结合片段,如苏金单抗)进行治疗。在一些实施例中,基于患有用局部皮质类固醇疗法不能充分控制的lp(例如lpp)或局部类固醇疗法对于患者是不可取的,选择患者(例如,患有扁平苔藓(lpp)的患者)以使用il-17拮抗剂(例如,il-17抗体或其抗原结合片段,例如,苏金单抗)进行治疗。“皮质类固醇疗法是不可取的”的患者是例如对皮质类固醇疗法过敏、免疫系统减弱、或妨碍使用皮质类固醇进行安全和/或有效治疗的其他副发病变和/或联合用药的患者。
[0056]
il-17拮抗剂
[0057]
各种披露的程序、试剂盒、用途和方法利用il-17拮抗剂,例如il-17结合分子(例如,可溶性il-17受体,il-17抗体或其抗原结合片段,例如苏金单抗)或il-17受体结合分子(例如,il-17受体抗体或其抗原结合片段)。在一些实施例中,il-17拮抗剂是il-17结合分子,优选il-17抗体或其抗原结合片段。
[0058]
在一个实施例中,il-17抗体或其抗原结合片段包含至少一个含有高变区cdr1、cdr2和cdr3的免疫球蛋白重链可变结构域(vh),所述cdr1具有氨基酸序列seq id no:1,所述cdr2具有氨基酸序列seq id no:2,并且所述cdr3具有氨基酸序列seq id no:3。在一个实施例中,il-17抗体或其抗原结合片段包含至少一个含有高变区cdr1’、cdr2’和cdr3’的免疫球蛋白轻链可变结构域(v
l’),所述cdr1’具有氨基酸序列seq id no:4,所述cdr2’具有
氨基酸序列seq id no:5并且所述cdr3’具有氨基酸序列seq id no:6。在一个实施例中,il-17抗体或其抗原结合片段包含至少一个含有高变区cdr1-x、cdr2-x和cdr3-x的免疫球蛋白重链可变结构域(vh),所述cdr1-x具有氨基酸序列seq id no:11,所述cdr2-x具有氨基酸序列seq id no:12,并且所述cdr3-x具有氨基酸序列seq id no:13。
[0059]
在一个实施例中,il-17抗体或其抗原结合片段包含至少一个免疫球蛋白vh结构域和至少一个免疫球蛋白v
l
结构域,其中:a)该免疫球蛋白vh结构域包含(例如依次):i)高变区cdr1、cdr2和cdr3,所述cdr1具有氨基酸序列seq id no:1,所述cdr2具有氨基酸序列seq id no:2,并且所述cdr3具有氨基酸序列seq id no:3;或ii)高变区cdr1-x、cdr2-x和cdr3-x,所述cdr1-x具有氨基酸序列seq id no:11,所述cdr2-x具有氨基酸序列seq id no:12,并且所述cdr3-x具有氨基酸序列seq id no:13;和b)免疫球蛋白v
l
结构域包含(例如依次)高变区cdr1’、cdr2’和cdr3’,所述cdr1’具有氨基酸序列seq id no:4,所述cdr2’具有氨基酸序列seq id no:5,并且所述cdr3’具有氨基酸序列seq id no:6。
[0060]
在一个实施例中,il-17抗体或其抗原结合片段包含:a)包含seq id no:8中所列出的氨基酸序列的免疫球蛋白重链可变结构域(vh);b)包含seq id no:10中所列出的氨基酸序列的免疫球蛋白轻链可变结构域(v
l
);c)包含seq id no:8中所列出的氨基酸序列的免疫球蛋白vh结构域和包含seq id no:10中所列出的氨基酸序列的免疫球蛋白v
l
结构域;d)包含seq id no:1、seq id no:2和seq id no:3中所列出的高变区的免疫球蛋白vh结构域;e)包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;f)包含seq id no:11、seq id no:12和seq id no:13中所列出的高变区的免疫球蛋白vh结构域;g)包含seq id no:1、seq id no:2和seq id no:3中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;或h)包含seq id no:11、seq id no:12和seq id no:13中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域。
[0061]
为便于参考,基于卡巴特(kabat)定义以及如通过x射线分析且使用乔西亚(chothia)和同事们的方法所确定的,在下表1中提供苏金单抗单克隆抗体的高变区的氨基酸序列。
[0062]
[0063][0064]
表1:苏金单抗的高变区的氨基酸序列。
[0065]
根据imgt的苏金单抗cdr如下:轻链cdr1(qsvsssy;seq id no:16)、cdr 2(gas;seq id no:17)、cdr3(qqygsspct;seq id no:18);和重链cdr1(gftfsnyw;seq id no:19)、cdr2(inqdgsek;seq id no:20)、(vrdyydiltdyyihywyfdl;seq id no:21)。
[0066]
在优选的实施例中,恒定区结构域还包含适合的人恒定区结构域,例如,如“sequences of proteins of immunological interest[免疫学目的蛋白质序列]”(kabat e.a.等人,美国卫生及公共服务部(us department of health and human services),公共卫生署(public health service),美国国立卫生研究院(national institute of health))中所述。编码苏金单抗的v
l
的dna列出在seq id no:9中。编码苏金单抗的vh的dna列出在seq id no:7中。
[0067]
在一些实施例中,il-17抗体或其抗原结合片段(例如,苏金单抗)包含seq id no:10的三个cdr。在其他实施例中,il-17抗体或其抗原结合片段包含seq id no:8的三个cdr。在其他实施例中,il-17抗体或其抗原结合片段包含seq id no:10的三个cdr和seq id no:8的三个cdr。根据卡巴特和乔西亚,可以在表1中发现seq id no:8和seq id no:10的cdr。根据imgt,cdr为seq id no:16-18(分别为轻链cdr1、cdr2、cdr3)和seq id no:19-21(分别为轻链cdr1、cdr2、cdr3)中所列出。可以例如在seq id no:6中看到轻链(cysl97)中的游离半胱氨酸。
[0068]
在一些实施例中,il-17抗体或其抗原结合片段包含seq id no:14的轻链。在其他实施例中,il-17抗体或其抗原结合片段包含seq id no:15的重链。在其他实施例中,il-17抗体或其抗原结合片段包含seq id no:14的轻链和seq id no:15的重链结构域。在一些实施例中,il-17抗体或其抗原结合片段包含seq id no:14的三个cdr。在其他实施例中,il-17抗体或其抗原结合片段包含seq id no:15的三个cdr。在其他实施例中,il-17抗体或其抗原结合片段包含seq id no:14的三个cdr和seq id no:15的三个cdr。可以在表1中发现seq id no:14和seq id no:15的cdr。
[0069]
高度可变区可与任意种类的骨架区相连,但优选为人源。适合的框架区描述于
kabat e.a.等人(同上)中。优选的重链框架是人重链框架,例如苏金单抗抗体的框架。该框架依次由例如fr1(seq id no:8的氨基酸1至30)、fr2(seq id no:8的氨基酸36至49)、fr3(seq id no:8的氨基酸67至98)和fr4(seq id no:8的氨基酸117至127)区组成。考虑到由x射线分析确定的苏金单抗的高变区,另一个优选的重链框架依次由fr1-x(seq id no:8的氨基酸1至25)、fr2-x(seq id no:8的氨基酸36至49)、fr3-x(seq id no:8的氨基酸61至95)和fr4(seq id no:8的氨基酸119至127)区组成。以类似的方式,轻链框架依次由fr1’(seq id no:10的氨基酸1至23)、fr2’(seq id no:10的氨基酸36至50)、fr3’(seq id no:10的氨基酸58至89)和fr4’(seq id no:10的氨基酸99至109)区组成。
[0070]
在一个实施例中,il-17抗体或其抗原结合片段(例如,苏金单抗)选自人il-17抗体,该抗体至少包含:a)免疫球蛋白重链或其片段,该免疫球蛋白重链或其片段包含可变结构域以及人重链的恒定部分或其片段,该可变结构域依次包含高变区cdr1、cdr2和cdr3;所述cdr1具有氨基酸序列seq id no:1,所述cdr2具有氨基酸序列seq id no:2,并且所述cdr3具有氨基酸序列seq id no:3;和b)包含可变结构域的免疫球蛋白轻链或其片段,所述可变结构域依次包含高变区cdr1’、cdr2’和cdr3’以及人轻链的恒定部分或其片段,所述cdr1’具有氨基酸序列seq id no:4,所述cdr2’具有氨基酸序列seq id no:5,并且所述cdr3’具有氨基酸序列seq id no:6。
[0071]
在一个实施例中,il-17抗体或其抗原结合片段选自包含抗原结合位点的单链抗体或其抗原结合片段,该抗原结合位点包含:a)依次包含高变区cdr1、cdr2和cdr3的第一结构域,所述cdr1具有氨基酸序列seq id no:1,所述cdr2具有氨基酸序列seq id no:2,并且所述cdr3具有氨基酸序列seq id no:3;和b)依次包含高变区cdr1’、cdr2’和cdr3’的第二结构域,所述cdr1’具有氨基酸序列seq id no:4,所述cdr2’具有氨基酸序列seq id no:5,并且所述cdr3’具有氨基酸序列seq id no:6;以及c)结合第一结构域的n端末端和第二结构域的c端末端或结合第一结构域的c端末端合第二结构域的n端末端的肽接头。
[0072]
可替代地,如在所披露的方法中使用的il-17抗体或其抗原结合片段可以包含通过序列在本文列出的il-17抗体的衍生物(例如,聚乙二醇化变体、糖基化变体、亲和力成熟变体等)。可替代地,在所披露的方法中使用的il-17抗体或其抗原结合片段的vh或v
l
结构域可以具有与本文列出的vh或v
l
结构域(例如,在seq id no:8和10中列出的那些结构域)基本上相同的vh或v
l
结构域。本文披露的人il-17抗体可以包含与seq id no:15中列出的重链基本上相同的重链和/或与seq id no:14中列出的轻链基本上相同的轻链。本文披露的人il-17抗体可以包含:含有seq id no:15的重链和含有seq id no:14的轻链。本文披露的人il-17抗体可以包含:a)一条重链,其包含具有与seq id no:8中所示的氨基酸序列基本上相同的氨基酸序列的可变结构域和人重链的恒定部分;和b)一条轻链,其包含具有与seq id no:10中所示的氨基酸序列基本上相同的氨基酸序列的可变结构域和人轻链的恒定部分。
[0073]
可替代地,在所披露的方法中使用的il-17抗体或其抗原结合片段可以是本文列出的参考il-17抗体的氨基酸序列变体(只要含有cysl97)。本披露还包括il-17抗体或其抗原结合片段(例如,苏金单抗),其中苏金单抗(但不是cysl97)的vh或v
l
结构域的一个或多个氨基酸残基中通常仅几个(例如,1-10个)发生了改变;例如通过突变,例如相应dna序列的定点诱变。在所有此类衍生物和变体的情况中,il-17抗体或其抗原结合片段在所述分子的约50nm或更低、约20nm或更低、约10nm或更低、约5nm或更低、约2nm或更低、或更优选地约
1nm或更低的浓度下,能够将约1nm(=30ng/ml)人il-17的活性抑制50%,如wo 2006/013107的实例1中所述针对人真皮成纤维细胞中由hu-il-17诱导的il-6产生来测量所述抑制活性。
[0074]
在一些实施例中,il-17抗体或其抗原结合片段(例如苏金单抗)与成熟人il-17的表位结合,该表位包含leu74、tyr85、his86、met87、asn88、val124、thr125、pro126、ile127、val128、his129。在一些实施例中,il-17抗体(例如苏金单抗)与成熟人il-17的表位结合,该表位包含tyr43、tyr44、arg46、ala79、asp80。在一些实施例中,il-17抗体(例如苏金单抗)与具有两条成熟人il-17链的il-17同源二聚体的表位结合,所述表位包含在一条链上的leu74、tyr85、his86、met87、asn88、val124、thr125、pro126、ile127、val128、his129和在另一条链上的tyr43、tyr44、arg46、ala79、asp80。用于定义这些表位的残基编号方案基于是成熟蛋白(即,缺少23个氨基酸的n-末端信号肽且以甘氨酸开始的il-17a)的第一个氨基酸的残基。不成熟的il-17a的序列列出在swiss-prot条目q16552中。在一些实施例中,il-17抗体具有kd为约100-200pm(例如,如通过测验确定的)。在一些实施例中,il-17抗体对于约0.67nm人il-17a的生物学活性的体外中和具有约0.4nm的ic
50
。在一些实施例中,皮下(sc)施用的il-17抗体的绝对生物利用度的范围为约60%-约80%,例如约76%。在一些实施例中,il-17抗体(如苏金单抗)具有的消除半衰期为约4周(例如,约23至约35天、约23至约30天,例如约30天)。在一些实施例中,il-17抗体(如苏金单抗)具有的t
max
为约7-8天。
[0075]
在所披露的方法中使用的特别优选的il-17抗体或其抗原结合片段是人抗体,尤其是如在wo 2006/013107的实例1和2中所述的苏金单抗。用于在所披露的方法、试剂盒和方案中使用的其他优选的il-17抗体是以下列出的那些:美国专利号:8,057,794;8,003,099;8,110,191;和7,838,638以及美国公开专利申请号:20120034656和20110027290,将其通过引用以其全文并入本文。
[0076]
治疗方法和il-17拮抗剂的用途
[0077]
所披露的il-17拮抗剂(例如il-17结合分子(例如,il-17抗体或其抗原结合片段,例如苏金单抗)或il-17受体结合分子(例如,il-17受体抗体或其抗原结合片段))可以在体外、离体使用,或掺入药物组合物中并在体内施用来治疗患有lp(例如,clp、mlp、lpp或其组合)的患者(例如,人类患者)。
[0078]
扁平苔藓(lp)是影响皮肤和黏膜皮肤的炎症性自身免疫性疾病。尽管病理生理学尚未完全明确,但lp是展现出th1细胞因子表达增加以及t-细胞对基底膜区域成分的反应性增加的t-细胞介导的障碍。有几种临床类型的lp具有相似的组织病理学特征:皮肤扁平苔藓(clp)(lp发生在皮肤(cutaneous skin)上),黏膜扁平苔藓(mlp)(lp发生在黏膜皮肤上),毛发扁平苔藓(lpp)(lp影响毛囊),指甲扁平苔藓,色素性扁平苔藓,苔藓样药疹。lp的免疫学和组织病理学特征描述于例如arora等人(2014)indian j dermatol.[印度皮肤病杂志]59(3):257-261,和atas等人(2016)postepy dermatol alergol.[皮肤病学和过敏学进展]33(3):188-92。
[0079]
lp典型地通过活检证实,意味着该障碍已被“活检证实”。在优选的实施例中,患者患有经活检证实的lp(mlp、clp、lpp或其组合)。
[0080]
在优选的实施例中,使用所披露的方法、用途、试剂盒等进行治疗的lp患者患有
lpp。在优选的实施例中,使用所披露的方法、用途、试剂盒等进行治疗的lp患者患有mlp。在优选的实施例中,使用所披露的方法、用途、试剂盒等进行治疗的lp患者患有clp。
[0081]
如本文所用,短语“稳定型皮肤lp”是指lp,其中患者:1)具有》3的基线研究者总体评估(iga);并且2)对局部皮质类固醇疗法是难治性的或对局部类固醇具有不充分的应答。在一些实施例中,使用所披露的方法、用途、试剂盒等进行治疗的lp患者患有稳定型皮肤lp。
[0082]
如本文所用,短语“控制不充分”、“不充分的应答”、“没有充分应答”等是指在患者中产生不充分应答或治疗失败的治疗,例如,在用给定药剂治疗后患者仍有该障碍的一种或多种病理症状,例如,在lp的情况下,症状包括瘙痒、脱发斑块、疼痛、灼热、损伤等。在一些实施例中,在施用il-17拮抗剂之前,患者对先前用苔藓样疗法进行治疗有不充分的应答。在一些实施例中,患者对先前用局部类固醇(例如,局部皮质类固醇)进行治疗有不充分的应答。
[0083]
对用苔藓样疗法(例如,皮质类固醇)进行治疗有充分应答但由于副作用而中止的患者被称为“不耐受”。在一些实施例中,患有将使用所披露的方法、用途、试剂盒等治疗的lp(例如,lpp、mlp、clp或其组合)的患者对先前的苔藓样疗法(例如皮质类固醇)不耐受。在一些实施例中,患者对局部皮质类固醇治疗(例如高效皮质类固醇(根据who定义))不耐受。
[0084]
难治性是指特定类型的不充分应答,即“难治性”意指患者已经用至少4周的高效苔藓样疗法(例如皮质类固醇)治疗而没有显著改善。在一些实施例中,根据所披露的方法、用途、试剂盒等治疗的患有lp(例如,lpp、mlp、clp或其组合)的患者对用先前的苔藓样疗法的治疗是难治性的。在一些实施例中,患者对局部皮质类固疗法(例如高效皮质类固醇(根据who定义))是难治性的。
[0085]
如本文所用,“苔藓样疗法”是指采用lp药剂(例如小分子、生物疗法、乳剂、软膏剂等)或采用lp模式(例如光线疗法),包括局部疗法、全身疗法、光线疗法、类视黄醇及其组合的lp治疗。这些包括乳剂、洗剂、喷雾剂或洗发剂形式的局部疗法(例如,中低效皮质类固醇[根据who指南的第iv-vii组,参见bolognia jl、jorizzo jl、schaffer jv.glucocorticosteroids[糖皮质激素]dermatology[皮肤病学]第3版2012.ch 125,2075-88;ference jd,last ar.choosing topical corticosteroids[选择局部皮质类固醇]am fam physician[美国家庭医生].2009年1月15;79(2):135-40]);用于治疗瘙痒和/或疼痛的非处方(otc)润肤剂、洗发剂和润滑剂,例如含有薄荷醇、普莫卡因或抗组胺剂的止痒洗剂;用于口腔疼痛的混合药物(例如,含有苯海拉明、粘性利多卡因、抗酸剂、制霉菌素或皮质类固醇的otc漱口水);局部麻醉剂、全身性药剂(例如,生物制剂(例如tnfα抑制剂,例如阿达木单抗、英夫利昔单抗、赛妥珠单抗和依那西普、阿法西普、布瑞吉努单抗(briakinumab)、依法珠单抗、优特克单抗、艾克司单抗(ixekizumab)、布达鲁单抗(brodalumab)、古塞库单抗(guselkumab)、瑞莎珠单抗(risankizumab)、替拉珠单抗(tildrakizumab)),非生物免疫调节治疗(例如,甲氨蝶呤、阿普斯特、全身性皮质类固醇、环孢素、环磷酰胺、柳氮磺胺吡啶、硫唑嘌呤、吗替麦考酚酯、氨苯砜(dapson)、羟氯喹));类视黄醇(例如顺式视黄酸(alitretinoin));病灶内注射皮质类固醇;光线疗法(例如uvb);光化学疗法(例如补骨脂素和uva(puva));局部钙调磷酸酶抑制剂(环孢霉素、他克莫司、吡美莫司)或局部维生素d类似物;高效-超高效的局部皮质类固醇(根据who的定义,为第i、
ii、iii组);具有已知抗炎特性的抗真菌药物,例如灰黄霉素、伊曲康唑、倍他米松、地塞米松、incb018424、曲安奈德、阿普斯特、姜黄糊剂、硫酸盐葡萄糖胺、醋酸曲安奈德、芝麻油、倍他米松二丙酸酯、丙酸氯倍他索、益生菌(例如动物双歧杆菌乳酸亚种hn019、罗伊氏乳杆菌(lactobacilli reuteri))、ω-3、泼尼松、泼尼松龙、富血小板血浆、orabase糊剂、番茄红素、局部洋甘菊、绿茶、co2激光治疗、polybiotics、光生物调节、甲硝唑、多西环素、米诺环素、雪松蜜、马齿苋、姜黄素类、阿法赛特、六氨基乙酰丙酸酯、羟氯喹、adcortyl、依法珠单抗、氟轻松、辅酶q10粘膜粘附片、罗马洋甘菊(chamaemelum nobile)、西罗莫司、他克莫司、清眩汤(qingxuan decoction)、nsaid局部冲洗、nsaid、槲皮素、navs萘、甲氯乙胺(valchlor)、布比卡因、燕麦片浴。关于苔藓样疗法(包括lp药剂)的进一步信息可以在husein-elahmed(2019)j eur acad dermatol venereol[欧洲皮肤病学和性病学会杂志]doi:10.1111/jdv.15771中找到,将其通过引用以其整体并入本文。
[0086]
优选的中低效力局部皮质类固醇是0.05%去羟米松乳膏、0.025%醋酸氟轻松软膏、0.05%氟氢缩松软膏、0.2%戊酸氢化可的松软膏、0.1%醋酸曲安奈德乳膏、0.02%二丙酸倍他米松洗剂、0.1%戊酸倍他米松乳膏、0.025%醋酸氟轻松乳膏、0.05%氟氢缩松乳膏、0.1%氢化可的松丁酸酯乳膏、0.2%戊酸氢化可的松乳膏、0.1%醋酸曲安奈德洗剂、0.05%戊酸倍他米松洗剂、0.05%地奈德乳膏、0.01%醋酸氟轻松溶液、0.1%地塞米松磷酸钠乳膏、1%醋酸氢化可的松乳膏、0.25%醋酸甲泼尼龙乳膏。
[0087]
如本文所用,“诱导(induction)”是指诱导降低或缓解疾病负担的疗法的一部分。此后,用“维持(maintenance)”方案治疗患者,以使患者维持在无病(或无复发)状态。
[0088]
可以使用各种已知的测量苔藓样疾病的方法和工具来评估lp治疗的有效性。此类测试包括,例如,活检和随后的组织病理、疾病表面积的医师评估(psad)(参见nct00285779)、研究者总体评估(iga)评分(其中0/1评分表示症状清除或几乎清除,以及评分》3代表中度至重度疾病);网状红斑性溃疡(reu)评分(piboonniyom等人(2005)oral surg oral med oral pathol oral radiol endod[口腔外科口腔医学口腔病理学口腔放射学];99(6):696-703);皮肤病生活质量指数(dlqi)(参见例如,finlay(1994)clin exp dermatol.[临床与实验皮肤病学]19(3):210-6,其中0/1评分表明疾病对患者的生活质量没有影响);体表面积(bsa)(医疗保健专业人员据此估计受lp影响的患者体表面积的百分比;根据披露的方法、试剂盒和用途,获得bsa低于1%的患者被认为对治疗有应答);峰值瘙痒数值评定量表(nrs)(参见例如,yosipovitch等人(2019)br j dermatol.[英国皮肤病学杂志]181(4):761-769);lpp活动指数(lppai)(参见例如,chiang等人,(2010)j am acad dermatol[美国皮肤病学会杂志]62:387-92);口腔扁平苔藓症状严重程度测量(olpssm)(参见例如,burke(2019)oral dis.[口腔疾病]9月;25(6):1564-1572);scalpdex(参见例如,chen(2002)arch.dermatol.[皮肤病学文献]138:803-07);总体疾病严重程度的患者评估;扁平苔藓症状量表;epworth嗜睡量表(ess);使用视觉模拟量表(vas)的疼痛(参见例如,chainani-wu等人(2008)oral surg oral med oral pathol oral radiol endod.[口腔外科口腔医学口腔病理学口腔放射学]105(1):51-8;chaudhary s.(2004)aust dent j.[澳大利亚牙科杂志];49(4):192-195);毛发检查评分;改良口腔黏膜炎指数(momi)(参见例如,chainani-wu等人(2008),同上),口腔健康影响程度量表(ohip-14)(参见例如,mary等人(2017)j clin diagn res.[临床和诊断研究杂志]11(8):zc78-zc81),以及患者停止
或减少局部治疗的能力。
[0089]
我们生成了独特的研究者总体评估(iga)评分,可用于评估mlp、clp和lpp的lp严重程度(以及lp患者对治疗的应答)。该iga(表2)提供了统一的5分制分级系统,以评估所有三种lp亚型(mlp、clp和lpp)患者的疾病严重程度。主要亚型定义了患者的iga评分。iga分级仅基于主要亚型。此外,如果存在,还单独收集伴随亚型的iga评分
[0090][0091]
[0092][0093]
表2
‑‑
对扁平苔藓的研究者总体评估(iga)。应主要由病变特征决定分级。例如疼痛或瘙痒的症状可能相关,也可能不相关。
[0094]
如本文所用,术语“基线”等(例如,“基线值”)是指在患者用il-17抗体或其抗原结合片段治疗之前给定的变量的值。
[0095]
在一些实施例中,患者是患有lp(例如,lpp、mlp、clp或其组合)的成年人类患者。在一些实施例中,患者是患有lp(例如,lpp、mlp、clp或其组合)的儿童人类患者。用于限定儿童患者的年龄上限因专家而异,并且可以包括上至21岁的青少年(参见例如berhman re、kliegman r、arvin am、nelson we.nelson textbook of pediatrics[纳尔逊儿科学教材],第15版philadelphia:w.b.saunders company[费城:桑德斯出版公司];1996;
2.rudolph am等人rudolph’s pediatrics[鲁道夫儿科学],第21版new york:mcgraw-hill[纽约:麦格劳-希尔集团];2002;和avery md,first lr.pediatric medicine[儿科医学],第2版baltimore:williams&wilkins[巴尔的摩:威廉姆斯和威尔金斯出版社];1994)。如本文所用,术语“儿童”通常是指十六岁或十六岁以下的人,这是美国食品药品监督管理局(us fda)使用的对儿童的定义。
[0096]
在一些实施例中,不考虑患者的体重,在第0、1、2、3和4周期间,每周向儿童患者施用sc剂量的il-17抗体(例如苏金单抗),然后在此之后以约150mg-约300mg(例如150mg或300mg)的剂量,每两周或四周进行施用。
[0097]
在一些实施例中,在第0、1、2、3、和4周期间,每周向儿童患者施用sc剂量的il-17抗体(例如苏金单抗),然后在此之后在患者体重《25kg的情况下以约75mg的剂量,或在患者体重》25kg的情况下以约150mg的剂量,每两周或每四周进行施用。在一些实施例中,在第0、1、2、3、和4周期间,每周向儿童患者施用sc剂量的il-17抗体(例如苏金单抗),然后在此之后在患者体重《50kg的情况下以约75mg的剂量,或在患者体重》50kg的情况下以约150mg的剂量,每两周或每四周进行施用。
[0098]
在一些实施例中,在第0、1、2、3、和4周期间,每周向儿童患者施用sc剂量的il-17抗体(例如苏金单抗),然后在此之后在患者体重《25kg的情况下以约150mg的剂量,或在患者体重》25kg的情况下以约300mg的剂量,每两周或每四周进行施用。在一些实施例中,在第0、1、2、3、和4周期间,每周向儿童患者施用sc剂量的il-17抗体(例如苏金单抗),然后在此之后在患者体重《50kg的情况下以约150mg的剂量,或在患者体重》50kg的情况下以约300mg的剂量,每两周或每四周进行施用。
[0099]
在一些实施例中,在第0周期间,向儿童患者施用一次iv剂量约4mg/kg-约9mg/kg(优选地约6mg/kg)的il-17抗体(例如苏金单抗),并且此后从第4周期间开始,以约2mg/kg-约4mg/kg(优选地约3mg/kg)的iv剂量每4周(每月)进行施用。
[0100]
当与药学上可接受的载体组合使用时,il-17拮抗剂,例如il-17结合分子(例如,il-17抗体或其抗原结合片段,例如苏金单抗)或il-17受体结合分子(例如,il-17抗体或其抗原结合片段)可以用作药物组合物。除il-17拮抗剂外,这种组合物还可以包含载体、各种稀释剂、填充剂、盐、缓冲剂、稳定剂、增溶剂和本领域已知的其他材料。载体的特征将取决于施用途径。用于在所披露的方法中使用的药物组合物还可以含有用于治疗特定靶向障碍的其他治疗剂。例如,药物组合物还可以包括抗炎剂。此类另外的因子和/或药剂可以包括在药物组合物中与il-17结合分子一起来产生协同效应或使由il-17拮抗剂(例如il-17结合分子(例如,il-17抗体或其抗原结合片段,如苏金单抗)或il-17受体结合分子(例如,il-17抗体或其抗原结合片段))引起的副作用最小化。在优选的实施例中,在所披露的方法中使用的药物组合物包含150mg/ml的苏金单抗。
[0101]
用于在所披露的方法中使用的药物组合物可以按常规方式制备。在一个实施例中,药物组合物以冻干形式提供。为立即施用,将其溶解于合适的水性载体中,例如无菌注射用水或无菌缓冲生理盐水。如果认为需要通过输注而不是单次快速静脉注射来构成更大体积的溶液用于施用,则在配制时将人血清白蛋白或患者自身的肝素化血液掺入盐水中可能是有利的。过量的这种生理惰性蛋白质的存在防止了通过吸附到容器壁和输注溶液使用的管道上而损失抗体。如果使用白蛋白,合适的浓度是按重量计盐水溶液的从0.5%至
4.5%。其他配制品包括即用型液体配制品。
[0102]
抗体,例如il-17的抗体,通常以即用型水性形式配制成用于肠胃外施用,或者配制成冻干物,用于在施用前用适合的稀释剂复水。在所披露的方法和用途的优选的实施例中,il-17拮抗剂(例如il-17抗体,例如苏金单抗)被配制成即用型(即稳定即用型)液体药物配制品。在所披露的方法和用途的一些实施例中,il-17拮抗剂(例如il-17抗体,例如苏金单抗)被配制成冻干物。适合的冻干配制品可以在小的液体体积(例如,2ml或更少,例如2ml、1ml等)中复水以允许皮下施用,并且可以提供具有低水平抗体聚集的溶液。现在抗体作为药物的活性成分被广泛使用,包括产品herceptin
tm
(曲妥珠单抗)、rituxan
tm
(利妥昔单抗)、synagis
tm
(帕利珠单抗)等。用于将抗体纯化为药物级抗体的技术是本领域已知的。当通过静脉内、经皮或皮下注射施用治疗有效量的il-17拮抗剂,例如il-17结合分子(例如,il-17抗体或其抗原结合片段,如苏金单抗)或il-17受体结合分子(例如,il-17抗体或其抗原结合片段)时,该il-17拮抗剂将处于无热原,肠胃外可接受的溶液形式。除il-17拮抗剂外,用于静脉内、经皮或皮下注射的药物组合物可以含有等渗媒介物,例如氯化钠、林格氏溶液、右旋糖、右旋糖和氯化钠、乳酸林格氏溶液或在本领域中已知的其他媒介物。
[0103]
在实施本披露的一些治疗方法或用途时,向患者(例如哺乳动物(例如,人))施用治疗有效量的il-17拮抗剂,例如il-17结合分子(例如,il-17抗体或其抗原结合片段,如苏金单抗)或il-17受体结合分子(例如,il-17抗体或其抗原结合片段)。虽然应理解所披露的方法提供了使用il-17拮抗剂(例如,苏金单抗)治疗lp(例如,clp、lpp、mlp或其组合)患者,但这并不排除如果患者有待最终用il-17拮抗剂治疗,这种il-17拮抗剂疗法必然是单一疗法。实际上,如果患者被选择用il-17拮抗剂进行治疗,那么il-17拮抗剂(例如,苏金单抗)可以根据本披露的方法单独施用或与用于治疗lp(例如,clp、lpp、mlp或其组合)患者的其他药剂和疗法组合(例如与至少一种另外的lp药剂或苔藓样疗法组合)施用。当与一种或多种另外的lp药剂或苔藓样疗法共同施用时,可以与其他药剂同时地或顺序地施用il-17拮抗剂。如果顺序施用,则主治医疗保健专业人员决定将il-17拮抗剂与其他药剂组合施用的适当顺序和用于共同递送的适当剂量。
[0104]
在治疗lp(例如,clp、llp、mlp或其组合)期间,各种苔藓样疗法可以有益地与所披露的il-17抗体(如苏金单抗)组合。非限制性实例包括lp药剂(例如,小分子、生物疗法、乳剂、软膏剂等)和lp模式(例如,光线疗法),例如局部疗法、全身疗法、光线疗法、类视黄醇及其组合。这些包括乳剂、洗剂、喷雾剂或洗发剂形式的局部治疗(例如,低-中效皮质类固醇[根据who指南的iv-vii组]);用于治疗瘙痒和/或疼痛的非处方(otc)润肤剂、洗发剂和润滑剂,例如含有薄荷醇、普莫卡因或抗组胺剂的止痒洗剂;用于口腔疼痛的混合药物(例如,含有苯海拉明、粘性利多卡因、抗酸剂、制霉菌素或皮质类固醇的otc漱口水);局部麻醉剂、全身性药剂(例如,生物制剂(例如tnfα抑制剂,例如阿达木单抗、英夫利昔单抗、赛妥珠单抗和依那西普、阿法西普、布瑞吉努单抗(briakinumab)、依法珠单抗、优特克单抗、艾克司单抗(ixekizumab)、布达鲁单抗(brodalumab)、古塞库单抗(guselkumab)、瑞莎珠单抗(risankizumab)、替拉珠单抗(tildrakizumab)),非生物免疫调节治疗(例如,甲氨蝶呤、阿普斯特、全身性皮质类固醇、环孢素、环磷酰胺、柳氮磺胺吡啶、硫唑嘌呤、吗替麦考酚酯、氨苯砜(dapson)、羟氯喹));类视黄醇(例如顺式视黄酸);病灶内注射皮质类固醇;光线疗法(例如uvb);光化学疗法(例如补骨脂素和uva(puva));局部钙调磷酸酶抑制剂(环孢霉素、
他克莫司、吡美莫司)或局部维生素d类似物;高效-超高效的局部皮质类固醇(根据who的定义,为第i、ii、iii组);具有已知抗炎特性的抗真菌药物,例如灰黄霉素、伊曲康唑、倍他米松、地塞米松、incb018424、曲安奈德、阿普斯特、姜黄糊剂、硫酸盐葡萄糖胺、醋酸曲安奈德、芝麻油、倍他米松二丙酸酯、丙酸氯倍他索、益生菌(例如动物双歧杆菌乳酸亚种hn019、罗伊氏乳杆菌(lactobacilli reuteri))、ω-3、泼尼松、泼尼松龙、富血小板血浆、orabase糊剂、番茄红素、局部洋甘菊、绿茶、co2激光治疗、polybiotics、光生物调节、甲硝唑、多西环素、米诺环素、雪松蜜、马齿苋、姜黄素类、阿法赛特、六氨基乙酰丙酸酯、羟氯喹、adcortyl、依法珠单抗、氟轻松、辅酶q10粘膜粘附片、罗马洋甘菊(chamaemelum nobile)、西罗莫司、他克莫司、清眩汤(qingxuan decoction)、nsaid局部冲洗、nsaid、槲皮素、navs萘、甲氯乙胺(valchlor)、布比卡因和其组合。
[0105]
与il-17结合分子(例如,il-17抗体或其抗原结合片段,例如苏金单抗)或il-17受体结合分子(例如,il-17受体抗体或其抗原结合片段)组合用于在所披露的试剂盒和方法中使用的优选的lp药剂是用于疼痛的非处方润肤剂和润滑剂(包括抗组胺剂)、神奇漱口水、制霉菌素口服剂和中-低效皮质类固醇(根据who定义的iv-vii组)(例如,0.05%去羟米松乳膏、0.025%醋酸氟轻松软膏、0.05%氟氢缩松软膏、0.2%戊酸氢化可的松软膏、0.1%醋酸曲安奈德乳膏、0.02%二丙酸倍他米松洗剂、0.1%戊酸倍他米松乳膏、0.025%醋酸氟轻松乳膏、0.05%氟氢缩松乳膏、0.1%氢化可的松丁酸酯乳膏、0.2%戊酸氢化可的松乳膏、0.1%醋酸曲安奈德洗剂、0.05%戊酸倍他米松洗剂、0.05%地奈德乳膏、0.01%醋酸氟轻松溶液、0.1%地塞米松磷酸钠乳膏、1%醋酸氢化可的松乳膏、0.25%醋酸甲泼尼龙乳膏,以及其组合)。
[0106]
本领域技术人员将能够辨别上述lp药剂的合适剂量,以与所披露的il-17抗体(如苏金单抗)共同递送。
[0107]
il-17拮抗剂,例如il-17结合分子(例如,il-17抗体或其抗原结合片段,如苏金单抗)或il-17受体结合分子(例如,il-17受体抗体或其抗原结合片段)被便利地按胃肠外,例如静脉内(例如,在肘前或其他外周静脉内)、肌内,或皮下施用。使用本披露的药物组合物的静脉内(iv)疗法的持续时间将根据所治疗疾病的严重程度和每个单独患者的病症和个人应答而变化。还考虑使用本披露的药物组合物的皮下(sc)疗法。保健提供者将使用本披露的药物组合物来决定iv或sc疗法的适当持续时间和疗法的施用时间。在优选的实施例中,通过皮下(sc)途径施用il-17拮抗剂(例如苏金单抗)。
[0108]
可以将il-17拮抗剂,例如il-17结合分子(例如,il-17抗体或其抗原结合片段,例如苏金单抗)或il-17受体结合分子(例如,il-17受体抗体或其抗原结合片段)例如在第0、1、2、3和4周期间按约150mg至约300mg(例如,约150mg,约300mg)每周sc向患者(例如患有lpp的患者)施用,并且此后例如在第8周期间开始按约150mg至约300mg(例如,约150mg,约300mg)每月(每4周)sc向患者施用。以此方式,用约150mg-约300mg(例如,约150mg或约300mg)的il-17拮抗剂(例如,苏金单抗)在第0、1、2、3、4、8、12、16、20周等的期间对患者sc给药。
[0109]
可以将il-17拮抗剂,例如il-17结合分子(例如,il-17抗体或其抗原结合片段,例如苏金单抗)或il-17受体结合分子(例如,il-17受体抗体或其抗原结合片段)例如在第0、1、2、3和4周期间按约150mg至约300mg(例如,约150mg,约300mg)每周sc向患者(例如患有
lpp、mlp、clp或其组合的患者)施用,并且此后例如在第6周期间开始按约150mg至约300mg(例如,约150mg,约300mg)每2周sc向患者施用。以此方式,用约150mg-约300mg(例如,约150mg或约300mg)的il-17拮抗剂(例如,苏金单抗)在第0、1、2、3、4、6、8、10、12、14、16、18、20周等的期间对患者sc给药。
[0110]
可替代性地,可以向患者(例如,患有lpp、mlp、clp或其组合的患者)静脉内(iv)施用il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗)。表3中提供了与所披露的il-17拮抗剂一起使用的优选iv方案(剂量和施用方案)以治疗lp。
[0111][0112]
表3:优选的用于在所披露的方法中使用的iv/iv方案,这些方法利用il-17拮抗
剂,例如il-17结合分子(例如,il-17抗体或其抗原结合片段,例如苏金单抗)或il-17受体结合分子(例如,il-17受体抗体或其抗原结合片段)。
[0113]
在一些实施例中,预期可以在第0周期间,以约4mg/kg-约9mg/kg(优选地约6mg/kg)的剂量向患者(例如,患有lpp、mlp、clp或其组合的患者)iv施用一次il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗),并且此后从第4周期间开始每4周(每月)以约2-约4mg/kg(优选地约3mg/kg)的iv剂量进行施用。以此方式,在第0、4、8、12、16、20周等期间,向患者iv给药约4mg/kg-约9mg/kg(例如约6mg/kg)的il-17拮抗剂(例如,苏金单抗)。在优选的实施例中,在第0周期间,以约6mg/kg的剂量向患者iv施用一次il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗),并且此后从第4周期间开始,每4周(每月)以约3mg/kg的iv剂量进行施用。以此方式,在第0周期间,向患者iv给药约6mg/kg的il-17拮抗剂(例如苏金单抗),并且此后在第4、8、12、16、20周等期间,以约3mg/kg的iv剂量进行给药。
[0114]
在一些实施例中,在第0周期间,以约4mg/kg-约9mg/kg(优选地约6mg/kg)的剂量向患者(例如,患有lpp、mlp、clp或其组合的患者)iv施用一次il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗),并且此后从第4周期间开始每8周(每隔一月)以约2.0-约4mg/kg(优选地约3mg/kg)的iv剂量进行施用。
[0115]
在一些实施例中,预期可以以约10mg/kg的剂量每月(每4周)向患者(例如,患有lpp、mlp、clp或其组合的患者)iv施用il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗)。在一些实施例中,预期可以以约10mg/kg的剂量每两个月(每8周)向患者(例如,患有lpp、mlp、clp或其组合的患者)iv施用il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗)。在一些实施例中,预期可以在第0、4、8周期间,以约10mg/kg的剂量每月(每4周)向患者(例如,患有lpp、mlp、clp或其组合的患者)iv施用il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗),并且此后从第16周期间开始每两个月(每8周),以约10mg/kg(例如10mg/kg)的剂量进行施用。
[0116]
可替代地,可以将il-17拮抗剂(例如il-17结合分子(例如,il-17抗体或其抗原结合片段,例如苏金单抗)或il-17受体结合分子(例如,il-17受体抗体或其抗原结合片段))在无负荷方案的情况下向患者(例如,患有lpp、mlp、clp或其组合的患者)施用,例如可以将该拮抗剂以约150mg至约300mg(例如,约150mg、约300mg)每四周向患者sc施用。以此方式,在第0、4、8、12、16、20周等期间,向患者sc给药约150mg-约300mg(例如,约150mg,约300mg)的il-17拮抗剂(例如,苏金单抗)。
[0117]
可替代地,可以将il-17拮抗剂(例如il-17结合分子(例如,il-17抗体或其抗原结合片段,例如苏金单抗)或il-17受体结合分子(例如,il-17受体抗体或其抗原结合片段))在无负荷方案的情况下向患者(例如,患有lpp、mlp、clp或其组合的患者)施用,例如可以将该拮抗剂以约2.5-约4mg/kg(优选地约3mg/kg)每月或以约2.5-约4mg/kg(优选地约3mg/kg)每两个月向患者iv施用。
[0118]
可替代地,也可以将il-17拮抗剂(例如il-17抗体,例如苏金单抗)口服进行递送(例如,使用rani therapeutics公司的技术,例如以下列出的技术递送到肠腔:美国专利号8,734,429、9,492,378、9,456,988、9,415,004、9,6297,99、9,757,548、9,757,514、9,402,806;美国公开申请2017/0189659、2017/0100459)。
[0119]
应当理解,对于某些患者(例如,患有lpp、mlp、clp或其组合的患者)可能需要剂量
递增,该患者在治疗的第10周、第12周、第14周、第16周、第18周、第20周、第22周、第24周、第48周、第52周或第104周对用il-17拮抗剂(例如il-17结合分子(例如il-17抗体或其抗原结合片段,例如苏金单抗)或il-17受体结合分子(例如il-17受体抗体或其抗原结合片段))治疗展现出不充分的应答(例如,随时间的部分应答、无应答或丧失应答,例如,如通过本文披露的任何lp评分系统测量的)。因此,苏金单抗的sc剂量可以大于约150mg-约300mg sc,例如约200mg、约250mg(在原始150mg剂量的情况下)、约350mg、约450mg(在原始300mg剂量的情况下)等;类似地,iv剂量可以大于约2mg/kg-约9mg/kg,例如约2.5mg/kg、约3mg/kg、4mg/kg、约5mg/kg、约6mg/kg(例如在原始2mg/kg剂量的情况下)、约9.5mg/kg、10mg/kg、11mg/kg、12mg/kg、15mg/kg、20mg/kg、25mg/kg、30mg/kg、35mg/kg(在原始9mg/kg剂量的情况下)等。
[0120]
类似地,在以下某些患者中可以使用更频繁的给药(例如在维持方案期间),例如对用il-17抗体或其抗原结合片段(例如苏金单抗)进行治疗具有不充分应答(例如随时间的部分应答、无应答、或丧失应答)的患者。这些患者可能被切换成进行更频繁的施用(而不是增加剂量),例如从每4周(每月;q4w)施用il-17抗体或其抗原结合片段(例如苏金单抗)切换成每两周(q2w)或每周(q1w)施用,或从每2周(q2w)施用切换成每周(q1w)施用。这种切换可以按照被医疗保健专业人员确定是有必要的来进行,例如在治疗的第10周、第12周、第14周、第16周、第18周、第20周、第22周、第24周、第48周、第52周、或第104周。
[0121]
因此,在一些实施例中,如果患者在每四周施用的一段时间后对用il-17抗体或其抗原结合片段(例如苏金单抗)的治疗没有充分应答,那么将il-17抗体或其抗原结合片段(例如苏金单抗)每两周(q2w)向患者施用作为维持方案。在上述实施例中,“每四周施用的时间”由医疗保健专业人员根据患者的应答确定。例如,假设在第0、1、2、3和4周期间进行诱导方案(例如,sc诱导,例如使用150mg或300mg苏金单抗)给药,并且在第8周进行第一次q4w维持剂量给药,医疗保健专业人员可以将患者从q4w转换为q2w维持治疗,其中第一次q2w施用发生在第10周、第14周、第18周、第22周、第26周、第30周、第54周等。作为另一个实例,假设在第0、1、2、3和4周期间每周进行诱导方案(例如,sc诱导,例如,使用150mg或300mg苏金单抗)给药,并且在第8周第一次q4w维持剂量,医疗保健专业人员可以将患者从q4w转换为q2w维持治疗,其中第一次q2w施用发生在第12周、第16周、第20周、第24周、第28周、第52周等。
[0122]
还应理解,剂量减少也可用于某些患者,例如患有lp、mlp、clp或其组合的患者,这些患者展现出特别强的治疗应答,或对用il-17拮抗剂(例如,il-17抗体或其抗原结合片段,例如苏金单抗)进行治疗的不良事件/不良反应。因此,il-17拮抗剂(例如il-17抗体或其抗原结合片段,例如苏金单抗)的剂量可以降低至小于约150mg-约300mg sc,例如约250mg、约200mg、约150mg(在原始300mg剂量的情况下)、约100mg、约50mg(在原始150mg剂量的情况下)等。类似地,iv剂量可以降低至小于约8mg/kg,例如约7mg/kg、5mg/kg、4mg/kg、3mg/kg、2mg/kg、1mg/kg等。在一些实施例中,如通过医疗保健专业人员所确定的,il-17拮抗剂(例如il-17结合分子(例如,il-17抗体或其抗原结合片段,例如苏金单抗)或il-17受体结合分子(例如,il-17受体抗体或其抗原结合片段))可以按初始剂量为300mg或150mg sc递送向患者施用,然后如果需要,将剂量增加至约450mg(在原始300mg剂量的情况下)或约300mg(在原始150mg剂量的情况下)。
[0123]
类似地,在维持方案期间在以下某些患者中可以使用更低频率的给药,例如对用il-17抗体或其抗原结合片段(例如苏金单抗)的治疗具有特别强烈治疗应答或不良事件/不良反应的患者。这些患者可能被切换成更低频率的施用(而不是降低剂量),例如从每4周(每月;q4w)施用il-17抗体或其抗原结合片段(例如苏金单抗)切换成每六周(q6w)或每八周(q8w)施用,或从每2周(每月;q2w)施用il-17抗体或其抗原结合片段(例如苏金单抗)切换成每四周(q4w)或每六周(q6w)施用。这种切换可以按照被医疗保健专业人员确定是有必要的来进行,例如在治疗的第10周、第12周、第14周、第16周、第18周、第20周、第22周、第24周、第48周、第52周、或第104周。
[0124]
因此,在一些实施例中,如果患者在每两周(q2w)施用的一段时间后对il-17抗体或其抗原结合片段(例如苏金单抗)的治疗充分应答,则il-17抗体或其抗原结合片段(例如苏金单抗)每四周(q4w)向患者施用作为维持方案。在上述实施例中,“每四周施用的时间”由医疗保健专业人员根据患者的应答确定。例如,假设在第0、1、2、3和4周期间进行诱导方案(例如,sc诱导,例如使用150mg或300mg苏金单抗)给药,并且在第6周进行第一次q2w维持剂量给药,医疗保健专业人员可以将患者从q2w转换为q4w维持治疗,其中第一次q4w施用发生在第8周、第10周、第12周、第14周、第16周、第18周、第20周、第22周、第24周、第52周等。作为另一个实例,假设在第0、1、2、3和4周期间每周进行诱导方案(例如,sc诱导,例如,使用150mg或300mg苏金单抗)给药,并且在第6周第一次q2w维持剂量,医疗保健专业人员可以将患者从q24w转换为q4w维持治疗,其中第一次q4w施用发生在第8周、第10周、第12周、第14周、第16周、第18周、第20周、第22周、第24周、第52周等。
[0125]
如本文所用,“固定剂量”是指平稳剂量,即不基于患者的特征而改变的剂量。因此,固定剂量与可变剂量,例如基于身体表面积的剂量或基于体重的剂量(典型地给定为mg/kg)不同。在所披露的方法、用途、药物组合物、试剂盒等的一些实施例中,向lp(例如,clp、mlp、lpp或其组合)患者施用固定剂量的il-17抗体,例如固定剂量的苏金单抗,例如固定剂量的约75mg-约450mg苏金单抗,例如约75mg、约150mg、约300mg、约400mg或约450mg苏金单抗。可替代地,在一些实施例中,向lp(例如,clp、mlp、lpp或其组合)患者施用基于体重的剂量,例如基于以kg为单位的患者体重给予以mg为单位的剂量(mg/kg)。
[0126]
给药的时间通常从苏金单抗的首次剂量的当天(也称为“基线”)测量。然而,医疗保健提供者通常使用不同的命名规则来确定给药时间表,如表4所示。
[0127][0128]
表4:用于给药方案的一般命名规则。粗体项是指在此使用的命名规则。
[0129]
值得注意的是,第零周可以被一些医疗保健提供者称为第一周,而第零天可以被一些医疗保健提供者称为第一天。因此,有可能不同医疗保健专业人员将指明剂量例如在第3周/在第21天期间、在第3周/在第22天期间、第4周/在第21天期间、第4周/在第22天期间给予,而指的是相同给药时间表。为了一致性,给药的第一周将在本文中称为第0周,而给药的第一天将被称为第1天。然而,本领域技术人员将理解,此命名规则仅用于一致性并且不
应被解释为限制,即,每周给药是提供每周剂量的il-17抗体,无论医疗保健专业人员是否参考特定的一周为“第1周”或“第2周”。
[0130]
在一个给药方案中,抗体在第0、1、2、3、4、8、12、16、20等期间施用。一些提供者可以将该方案称为每周一次,持续五周,然后在此之后每月一次(或每4周一次),从第8周期间开始,而其他人可以将该方案称为每周一次,持续四周,并然后在此之后每月(或每4周)一次,从第4周期间开始。本领域技术人员应当理解的是在第0、1、2和3周对患者施用注射,随后在第4周开始每月给药一次,与以下情况相同:1)在第0、1、2、3和4周对患者施用注射,随后在第8周开始每月给药一次;2)在第0、1、2、3和4周向患者施用注射,随后每4周进行给药;和3)在第0、1、2、3和4周对患者施用注射,随后每月施用。
[0131]
在一个实施例中,在第0、1、2、3、4、6、8、10、12等期间向lp患者施用抗体。一些提供者可以将该方案称为每周一次,持续五周,然后在此之后每隔一周(或每2周一次),从第6周期间开始,而其他人可以将该方案称为每周一次,持续四周,并然后在此之后每隔一周(或每2周)一次,从第4周期间开始。本领域技术人员应当理解的是在第0、1、2和3周向患者施用注射,随后在第4周开始每隔一周(或每2周)进行施用,与以下情况相同:1)在第0、1、2、3和4周向患者施用注射,随后在第6周开始每隔一周(或每2周)进行给药;2)在第0、1、2、3和4周向患者施用注射,随后每2周进行给药;和3)在第0、1、2、3和4周对患者施用注射,随后每隔一周进行施用。
[0132]
如本文所用,短语“按以允许[施用途径]递送[指定剂量]的剂量配制”用于表示给定的药物组合物可用于通过指定的施用途径(例如,sc或iv)提供所需剂量的il-17拮抗剂,例如il-17抗体,如苏金单抗。作为实例,如果所需的sc剂量是300mg,那么临床医生可能使用具有浓度为150mg/ml的2ml il-17抗体配制品、具有浓度为300mg/ml的1ml il-17抗体配制品、具有浓度为600mg/ml的0.5ml il-17抗体配制品等。在每个这种情况下,这些il-17抗体配制品处于足够高的浓度以允许皮下递送il-17抗体。皮下递送典型地需要递送小于或等于约2ml的体积,优选约1ml或更小的体积。优选的配制品是即用型液体药物组合物,这些组合物包含约25mg/ml至约150mg/ml的苏金单抗、约10mm至约30mm组氨酸(ph 5.8)、约200mm至约225mm海藻糖、约0.02%聚山梨醇酯80、和约2.5mm至约20mm甲硫氨酸。
[0133]
如本文所用,短语“具有足够量的il-17拮抗剂的容器以允许[指定剂量]的递送”用于表示给定容器(例如,小瓶、笔、注射器)已在其中配置可用于提供所需剂量的一定体积的il-17拮抗剂(例如,作为药物组合物的一部分)。作为实例,如果所需剂量是300mg,那么临床医生可能使用来自含有浓度为150mg/ml的il-17抗体配制品的容器中的2ml、来自含有浓度为300mg/ml的il-17抗体配制品的容器中的1ml、来自含有浓度为600mg/ml的il-17抗体配制品的容器中的0.5ml等。在每个这种情况下,这些容器具有足够量的il-17拮抗剂以允许递送所需的300mg的剂量。
[0134]
在所披露的用途、方法、和试剂盒的一些实施例中,il-17抗体(例如苏金单抗)或其抗原结合片段的剂量是约300mg,il-17抗体(例如苏金单抗)或其抗原结合片段按150mg/ml的浓度包含在液体药物配制品中,并且将2ml的药物配制品配置于两个预填充注射器、注射笔、或自动注射器内,每个都具有1ml的药物配制品。在这种情况下,在每次施用期间,对于300mg的总剂量,患者接受每次1ml的两次注射。在一些实施例中,il-17抗体(例如苏金单抗)或其抗原结合片段的剂量是约300mg,il-17抗体(例如苏金单抗)或其抗原结合片段按
150mg/ml的浓度包含在液体药物配制品中,并且将2ml的药物配制品配置于自动注射器或pfs内。在这种情况下,在每次施用期间,对于300mg的总剂量,患者接受2ml的一次注射。在采用2ml的一次注射的方法中(例如,通过单个pfs或自动注射器)(即“单剂量制剂”),药物暴露(auc)和最大浓度(c
max
)与采用1ml的两次注射的方法(例如通过两个pfs或两个ai)(即“多剂量制剂”)等效(类似,即根据us fda标准,在可接受的变化范围内)。
[0135]
本文披露了治疗毛发扁平苔藓(lpp)的方法,这些方法包括在第0、1、2、3和4周期间,每周向有需要的患者皮下(sc)施用剂量约150mg-约300mg的白介素(il)-17抗体或其抗原结合片段,并且此后从第8周期间开始,每四周进行施用,其中该il-17抗体或其抗原结合片段包含:
[0136]
i)包含seq id no:8中所列出的氨基酸序列的免疫球蛋白可变重(vh)结构域以及包含seq id no:10中所列出的氨基酸序列的免疫球蛋白可变轻(v
l
)结构域;
[0137]
ii)包含seq id no:1、seq id no:2和seq id no:3中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;或
[0138]
iii)包含seq id no:11、seq id no:12和seq id no:13中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域。
[0139]
本文还披露了il-17抗体(例如苏金单抗)或其抗原结合片段用于在治疗lpp中使用,在第0、1、2、3和4周期间,以约150mg-约300mg的剂量每周将其皮下(sc)施用至有需要的患者,并且此后从第8周期间开始,每月(每4周)以约150mg-约300mg的剂量进行sc施用。本文还披露了il-17抗体(例如苏金单抗)或其抗原结合片段用于在制造用于治疗lpp的药物中使用,在第0、1、2、3和4周期间,以约150mg-约300mg的剂量每周将其皮下(sc)施用至有需要的患者,并且此后从第8周期间开始,每月(每4周)以约150mg-约300mg的剂量进行sc施用。
[0140]
本文披露了治疗扁平苔藓(lp)的治疗方法,这些方法包括在第0、1、2、3和4周期间,每周向有需要的患者皮下(sc)施用剂量约150mg-约300mg的白介素(il)-17抗体或其抗原结合片段,并且此后从第6周期间开始每两周进行施用,其中,该il-17抗体或其抗原结合片段包含:
[0141]
i)包含seq id no:8中所列出的氨基酸序列的免疫球蛋白可变重(vh)结构域以及包含seq id no:10中所列出的氨基酸序列的免疫球蛋白可变轻(v
l
)结构域;
[0142]
ii)包含seq id no:1、seq id no:2和seq id no:3中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;或
[0143]
iii)包含seq id no:11、seq id no:12和seq id no:13中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域。
[0144]
本文还披露了il-17抗体(例如苏金单抗)或其抗原结合片段用于在治疗lp中使用,在第0、1、2、3和4周期间,以约150mg-约300mg的剂量每周将其皮下(sc)施用至有需要的患者,并且此后从第6周期间开始,每2周以约150mg-约300mg的剂量进行sc施用。本文还披
露了il-17抗体(例如苏金单抗)或其抗原结合片段用于在制造用于治疗lpp的药物中使用,在第0、1、2、3和4周期间,以约150mg-约300mg的剂量每周将其皮下(sc)施用至有需要的患者,并且此后从第6周期间开始,每2周以约150mg-约300mg的剂量进行sc施用。
[0145]
本文披露了治疗扁平苔藓(lp)的治疗方法,这些方法包括在第0周期间向有需要的患者静脉内(iv)施用一次剂量约4mg/kg-约9mg/kg(优选地约6mg/kg)的白介素(il)-17抗体或其抗原结合片段,并且此后从第4周期间开始每四周施用iv剂量约2mg/kg-约4mg/kg(优选地约3mg/kg)的il-17抗体或其抗原结合片段,其中,该il-17抗体或其抗原结合片段包含:
[0146]
i)包含seq id no:8中所列出的氨基酸序列的免疫球蛋白可变重(vh)结构域以及包含seq id no:10中所列出的氨基酸序列的免疫球蛋白可变轻(v
l
)结构域;
[0147]
ii)包含seq id no:1、seq id no:2和seq id no:3中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;或
[0148]
iii)包含seq id no:11、seq id no:12和seq id no:13中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域。
[0149]
本文还披露了il-17抗体(例如苏金单抗)或其抗原结合片段用于在治疗lp中使用,在第0周期间,将其以约4mg/kg至约9mg/kg(优选地约6mg/kg)的剂量向有需要的患者静脉内(iv)施用一次,并且此后从第4周期间开始,每月(每4周)以约2mg/kg至约4mg/kg(优选地约3mg/kg)的剂量进行iv施用。本文还披露了il-17抗体(例如苏金单抗)或其抗原结合片段用于在制造用于治疗lpp的药物中使用,在第0周期间,将其以约4mg/kg至约9mg/kg(优选地约6mg/kg)的剂量向有需要的患者静脉内(iv)施用一次,并且此后从第4周期间开始,每月(每4周)以约2mg/kg至约4mg/kg(优选地约3mg/kg)的剂量进行iv施用。
[0150]
在所披露的方法、用途、组合物、和试剂盒的一些实施例中,il-17抗体或其抗原结合片段与具有两条成熟il-17蛋白质链的il-17同源二聚体的表位结合,所述表位包含在一条链上的leu74、tyr85、his86、met87、asn88、val124、thr125、pro126、ile127、val128、his129和在另一条链上的tyr43、tyr44、arg46、ala79、asp80,其中如通过生物传感器系统(例如biacore)所测量的,该il-17抗体具有的kd为约100-200pm,并且其中该il-17抗体具有的体内半衰期为约23至约30天。
[0151]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,如果患者在每四周使用的一段时间后对用il-17抗体或其抗原结合片段的治疗没有充分应答,则il-17抗体或其抗原结合片段每两周向患者施用作为维持方案。
[0152]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,il-17抗体或其抗原结合片段的剂量是约150mg。
[0153]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,il-17抗体或其抗原结合片段的剂量是约300mg。
[0154]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,在用il-17抗体或其抗原结合片段治疗之前,患者对用苔藓样疗法的治疗没有充分应答,该苔藓样疗法选自由以下组成的组:局部疗法、全身疗法、光线疗法、类视黄醇及其任意组合。
[0155]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,在用il-17抗体或其抗原结合片段治疗之前,患者对局部皮质类固醇疗法是难治性的或患者对用局部类固醇的治疗没有充分应答。
[0156]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,在用il-17抗体或其抗原结合片段治疗期间,向患者伴随施用苔藓样疗法,该苔藓样疗法选自由以下组成的组:局部疗法、全身疗法、光线疗法、类视黄醇及其任意组合。
[0157]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,在用il-17抗体或其抗原结合片段治疗期间,向患者伴随施用至少一种低效至中效的局部固醇。
[0158]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,患者患有经活检证实的皮肤扁平苔藓(clp)、经活检证实的黏膜扁平苔藓(mlp)或经活检证实的毛发扁平苔藓(lpp)。
[0159]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,患者患有clp并且具有≥3%的基线体表面积(bsa)受累,有或没有指甲受累。
[0160]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,患者具有mlp和一个或多个选自口腔、生殖器和结膜的受影响部位。
[0161]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,患者患有lpp并且具有至少三个活动性斑。
[0162]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,患者:
[0163]
a)具有≥3的基线研究者总体评估(iga);并且
[0164]
b)对局部皮质类固醇疗法是难治性的或对局部类固醇具有不充分应答。
[0165]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,在用il-17抗体或其抗原结合片段治疗后,与基线iga评分相比,患者的iga评分得到至少两分的改善。
[0166]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,患者是成年人。
[0167]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,il-17抗体或其抗原结合片段配置于药物配制品中,其中所述药物配制品进一步包含缓冲剂和稳定剂。
[0168]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,药物配制品处于液体形式。
[0169]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,药物配制品处于冻干形式。
[0170]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,将药物配制品配置于至少一个预填充注射器、至少一个小瓶、至少一个注射笔、或至少一个自动注射器内。
[0171]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,将至少一个预填充注射器、至少一个小瓶、至少一个注射笔、或至少一个自动注射器配置于试剂盒内,并且其中所述试剂盒进一步包含使用说明书。
[0172]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,il-17抗体或抗原结合片段的剂量是300mg,按单次皮下施用、以来自包含150mg/ml的il-17抗体或抗原结合片段的配制品的2毫升(ml)的总体积向患者施用该剂量,并且其中患者对于il-17抗体或抗原结合片段的药物暴露等同于患者对于使用两次单独皮下施用的1ml总体积的il-17抗体或抗原结合片段的药物暴露,两次中每次都是相同配制品。
[0173]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,向患者施用的il-17抗体或抗原结合片段剂量是300mg,按两次单独皮下施用、以每次来自包含150mg/ml的il-17抗体或抗原结合片段的配制品的1ml的体积施用该剂量。
[0174]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,il-17抗体或抗原结合片段具有的t
max
为约7-8天。
[0175]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,il-17抗体或抗原结合片段具有的绝对生物利用度为约60%-约80%。
[0176]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,il-17抗体或抗原结合片段是人单克隆抗体。
[0177]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,il-17抗体或抗原结合片段是igg1/κ同种型。
[0178]
在一些实施例中,当该方法用于治疗患者群体时,至少30%的所述患者在治疗16周后达到iga 0/1。
[0179]
在一些实施例中,当该方法用于治疗患者群体时,至少40%的所述患者在治疗16周后达到iga 0/1。
[0180]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,患者患有mlp,并且如通过改良口腔黏膜炎指数(momi)所测量的,用il-17抗体或其抗原结合片段治疗16周后,患者的mlp得到改善。
[0181]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,如通过毛发扁平苔藓活动指数(lppai)所测量的,用il-17抗体或其抗原结合片段治疗16周后,患者的lpp得到改善。
[0182]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,如通过峰值瘙痒数值评定量表(nrs)所测量的,用il-17抗体或其抗原结合片段治疗16周后,患者的瘙痒得到改善。
[0183]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,如通过视觉模拟量表(vas)所测量的,用il-17抗体或其抗原结合片段治疗16周后,患者的疼痛得到改善。
[0184]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,如通过皮肤病生活质量指数(dlqi)0/1所测量的,用il-17抗体或其抗原结合片段治疗16周后,患者的生活质量得到改善。
[0185]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,患者患有mlp,并且如口腔健康影响程度量表(ohip-14)所测量的,用il-17抗体或其抗原结合片段治疗16周后,该患者的mlp得到改善。
[0186]
在所披露的方法、用途、组合物和试剂盒的一些实施例中,患者用il-17抗体或其抗原结合片段治疗持续至少一年。
[0187]
在本披露的优选的实施例中,il-17抗体或其抗原结合片段是单克隆抗体。
[0188]
在本披露的优选的实施例中,il-17抗体或其抗原结合片段是人抗体或人源化抗体。
[0189]
在本披露的优选的实施例中,il-17抗体或其抗原结合片段是人抗体。
[0190]
在所披露的方法、用途和试剂盒的优选的实施例中,il-17抗体或抗原结合片段是人单克隆抗体。
[0191]
在本披露的优选的实施例中,il-17抗体或其抗原结合片段是igg1亚型的人抗体。
[0192]
在优选的实施例中,il-17抗体或其抗原结合片段具有κ轻链。
[0193]
在本披露的优选的实施例中,il-17抗体或其抗原结合片段是igg1κ型的人抗体。
[0194]
在所披露的方法、用途和试剂盒的优选的实施例中,il-17抗体或抗原结合片段具有的t
max
为约7-8天。
[0195]
在所披露的方法、用途和试剂盒的优选的实施例中,il-17抗体或抗原结合片段具有的绝对生物利用度为约60%-约80%。
[0196]
在本披露的优选的实施例中,il-17抗体或其抗原结合片段是苏金单抗。
[0197]
本文披露了治疗患有毛发扁平苔藓(lpp)的成年患者的治疗方法,该患有毛发扁平苔藓的成年患者用局部皮质类固醇疗法不能充分控制或者局部皮质类固醇疗法对该患者是不可取的,这些方法包括在第0、1、2、3和4周期间向所述患者皮下施用剂量约300mg苏金单抗,然后在此之后每四周进行施用。在优选的实施例中,lpp是经活检证实的。
[0198]
本文披露了治疗患有扁平苔藓(lp)的成年患者的治疗方法,该患有扁平苔藓的成年患者用局部皮质类固醇疗法不能充分控制或者局部皮质类固醇疗法对该患者是不可取的,这些方法包括在第0、1、2、3和4周期间向所述患者皮下施用剂量约300mg苏金单抗,然后在此之后每两周进行施用。在优选的实施例中,患者患有皮肤扁平苔藓(clp)、黏膜扁平苔藓(mlp)、毛发扁平苔藓(lpp)或其任意组合。在所披露的方法、用途、组合物和试剂盒的一些实施例中,clp、mlp或lpp是经活检证实的。
[0199]
本文披露了治疗患有扁平苔藓(lp)的成年患者的治疗方法,该患有扁平苔藓的成年患者用局部皮质类固醇疗法不能充分控制或者局部皮质类固醇疗法对该患者是不可取的,这些方法包括在第0周期间,向该患者静脉内(iv)施用一次剂量约6mg/kg的苏金单抗,并且此后从第4周期间开始,每四周施用iv剂量约3mg/kg的苏金单抗。在优选的实施例中,患者患有皮肤扁平苔藓(clp)、黏膜扁平苔藓(mlp)、毛发扁平苔藓(lpp)或其任意组合。在所披露的方法、用途、组合物和试剂盒的一些实施例中,clp、mlp或lpp是经活检证实的。
[0200]
试剂盒
[0201]
本披露还涵盖用于治疗lp的试剂盒。此类试剂盒包含il-17拮抗剂,例如il-17结合分子(例如,il-17抗体或其抗原结合片段,例如苏金单抗)或il-17受体结合分子(例如,il-17抗体或其抗原结合片段)(例如,处于液体或冻干形式)或包含il-17拮抗剂(如上所述)的药物组合物。另外,此类试剂盒可以包含用于施用il-17拮抗剂的工具(例如,自动注射器、注射器和小瓶、预填充注射器、预填充笔)以及使用说明书。这些试剂盒可以含有用于治疗lp(例如,clp、lpp、mlp或其组合)的另外的hs治疗剂(如上所述),例如用于与包含的il-17拮抗剂(例如il-17结合分子,例如il-17抗体,例如苏金单抗)组合递送。此类试剂盒还可以包含用于施用il-17拮抗剂(例如,il-17抗体,例如苏金单抗)以治疗患有lp(例如,clp、lpp、mlp或其组合)的患者的说明书。此类说明书可以提供与包含的il-17拮抗剂(例如il-17结合分子,例如il-17抗体,如苏金单抗)一起使用的剂量(例如,3mg/kg、6mg/kg、300mg、450mg),施用途径(例如,iv、sc),和给药方案(例如,每周、每月、每周,然后每月、每周,然后每隔一周等)。
[0202]
短语“用于施用的工具”用于指示用于向患者全身性地施用药物的任何可用的器具,包括但不限于预填充注射器、小瓶和注射器、注射笔、自动注射器、iv注射槽和注射袋、
泵等。使用此类物品,患者可以自我施用药物(即,在没有医疗保健专业人员的帮助下施用药物)或医生可以施用药物。在一些实施例中,以配置于两个pfs或自动注射器中的2ml的总体积递送300mg的总剂量,每个pfs或自动注射器含有:具有150mg/ml的il-17抗体(例如苏金单抗)的1ml的体积。在这种情况下,患者接受两次1ml注射(多剂量制剂)。在优选的实施例中,以配置于单个pfs或自动注射器中的、具有150mg/ml的il-17抗体(例如苏金单抗)的2ml的总体积递送300mg的总剂量。在这种情况下,患者接受一次2ml注射(单剂量制剂)。
[0203]
本文披露了用于在患有lp(例如,clp、lpp、mlp或其组合)的患者的治疗中使用的试剂盒,这些试剂盒包含il-17拮抗剂(例如il-17结合分子,例如il-17抗体或其抗原结合片段,例如苏金单抗),以及用于将il-17拮抗剂施用至患有lp(例如,clp、lpp、mlp或其组合)的患者的工具。
[0204]
在一些实施例中,该试剂盒进一步包含用于向患者(优选地患有lpp的患者)施用il-17拮抗剂的说明书,其中这些说明书指示在第0、1、2、3和4周期间,以约150mg-约300mg(例如约150mg、约300mg)的剂量每周向患者sc施用il-17拮抗剂(例如il-17结合分子,例如il-17抗体或其抗原结合片段,例如苏金单抗),然后在此之后每四周进行施用。
[0205]
在一些实施例中,该试剂盒进一步包含用于向患有lp(例如,clp、lpp、mlp或其组合)的患者施用il-17拮抗剂的说明书,其中这些说明书指示在第0、1、2、3和4周期间,以约150mg-约300mg(例如约150mg、约300mg)的剂量每周向患者sc施用il-17拮抗剂(例如il-17结合分子,例如il-17抗体或其抗原结合片段,例如苏金单抗),然后在此之后每两周进行施用。
[0206]
在一些实施例中,该试剂盒进一步包括用于向患有lp的患者施用il-17拮抗剂的说明书,其中这些说明书指示在第0周期间,以约4mg/kg-约9mg/kg(优选地约6mg/kg)的剂量向患者iv施用一次il-17拮抗剂(例如il-17结合分子,例如il-17抗体或其抗原结合片段,例如苏金单抗),并且此后从第4周期间开始,每4周(每月)以约2-约4mg/kg(优选地约3mg/kg)的iv剂量进行施用。
[0207]
综述
[0208]
在所披露的用途、方法和试剂盒的优选的实施例中,il-17抗体或其抗原结合片段选自由以下组成的组:a)与人il-17的表位结合的il-17抗体或其抗原结合片段,该表位包含leu74、tyr85、his86、met87、asn88、val124、thr125、pro126、ile127、val128、his129;b)与人il-17的表位结合的il-17抗体或其抗原结合片段,该表位包含tyr43、tyr44、arg46、ala79、asp80;c)与具有两条成熟人il-17蛋白质链的il-17同源二聚体的表位结合的il-17抗体或其抗原结合片段,所述表位包含在一条链上的leu74、tyr85、his86、met87、asn88、val124、thr125、pro126、ile127、val128、his129和在另一条链上的tyr43、tyr44、arg46、ala79、asp80;d)与具有两条成熟人il-17蛋白质链的il-17同源二聚体的表位结合的il-17抗体或其抗原结合片段,所述表位包含在一条链上的leu74、tyr85、his86、met87、asn88、val124、thr125、pro126、ile127、val128、his129和在另一条链上的tyr43、tyr44、arg46、ala79、asp80,其中该il-17抗体或其抗原结合片段具有的kd为约100-200pm,并且其中该il-17抗体或其抗原结合片段具有的体内半衰期为约23至约35天;e)与具有两条成熟il-17蛋白质链的il-17同源二聚体的表位结合的il-17抗体,所述表位包含在一条链上的leu74、tyr85、his86、met87、asn88、val124、thr125、pro126、ile127、val128、his129和在另一条链
上的tyr43、tyr44、arg46、ala79、asp80,其中如通过生物传感器系统(例如)所测量的,该il-17抗体具有的kd为约100-200pm,并且其中该il-17抗体具有的体内半衰期为约23至约30天;和f)il-17抗体或其抗原结合片段,该抗体或其抗原结合片段包括:i)包含seq id no:8中所列出的氨基酸序列的免疫球蛋白重链可变结构域(vh);ii)包含seq id no:10中所列出的氨基酸序列的免疫球蛋白轻链可变结构域(v
l
);iii)包含seq id no:8中所列出的氨基酸序列的免疫球蛋白vh结构域以及包含seq id no:10中所列出的氨基酸序列的免疫球蛋白v
l
结构域;iv)包含seq id no:1、seq id no:2和seq id no:3中所列出的高变区的免疫球蛋白vh结构域;v)包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;vi)包含seq id no:11、seq id no:12和seq id no:13中所列出的高变区的免疫球蛋白vh结构域;vii)包含seq id no:1、seq id no:2和seq id no:3中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;viii)包含seq id no:11、seq id no:12和seq id no:13中所列出的高变区的免疫球蛋白vh结构域以及包含seq id no:4、seq id no:5和seq id no:6中所列出的高变区的免疫球蛋白v
l
结构域;ix)包含seq id no:14中所列出的氨基酸序列的免疫球蛋白轻链;x)包含seq id no:15中所列出的氨基酸序列的免疫球蛋白重链;或xi)包含seq id no:14中所列出的氨基酸序列的免疫球蛋白轻链和包含seq id no:15中所列出的氨基酸序列的免疫球蛋白重链。
[0209]
在所披露的方法、试剂盒或用途的最优选的实施例中,il-17抗体或其抗原结合片段是单克隆抗体,优选地人抗体,优选地人igg1抗体,最优选地苏金单抗。
[0210]
在所披露的方法、试剂盒或用途的最优选的实施例中,il-17抗体或其抗原结合片段(优选地苏金单抗)的剂量大小是平稳的,剂量是150mg或300mg(最优选地300mg),施用途径是sc,并且方案是在第0、1、2、3、4、8、12周等进行施用(在第0、1、2、3和4周期间每周一次,然后在第8周期间开始每四周一次)或在第0、1、2、3、4、6、8、10、12周等进行施用(在第0、1、2、3和4周期间每周一次,然后在第6周期间开始每隔一周一次)。
[0211]
本披露的一个或多个实施例的细节陈述于上文所附的说明书中。现在描述优选方法和材料,但类似或等效于本文所述的任何方法和材料也可以用于本披露的实践或测试。根据说明书并且根据权利要求书,本披露的其他特征、目标和优点将是清楚的。在本说明书和随附权利要求书中,单数形式包括复数指代物,除非上下文另外明确地说明。除非另外定义,否则本文所用的全部技术和科学术语具有与本披露所属领域的普通技术人员通常所理解的相同的意义。在本说明书中引证的所有专利以及出版物均通过引用并入。提供以下实例以便更充分地说明本披露的优选实施例。这些实例决不应被解释为限制如由所附权利要求书限定的披露的主题的范围。
[0212]
实例
[0213]
实例1:临床试验cain457s12201-一项旨在评估苏金单抗300mg在32周内在患有经活检证实形式的、用局部疗法控制不充分的扁平苔藓的成年患者中的功效、安全性和耐受性的概念验证研究
[0214]
设计的目的和基本原理:
[0215]
这项概念验证研究的目的是研究苏金单抗在治疗患有经活检证实的、用局部疗法控制不充分的扁平苔藓的成年患者中的功效,并评估经32周治疗的安全性和耐受性。该试
验的双盲、随机、安慰剂对照设计能够在充分和受控的设置下评估苏金单抗300mg在两种不同给药方案和三种所选亚型的扁平苔藓(mlp、clp、lpp)中的功效和安全性。
[0216]
将患者分配到特定的扁平苔藓亚型并以平行组方式对他们进行监测的基本原理是单独地评估苏金单抗在每个亚型中的功效和安全性。三种所选亚型之间存在广泛的病理生理和临床的重叠,尤其是在clp和mlp亚型之间,其中许多患者呈现出重叠的症状和病变。然而,每个亚型存在于不同的解剖区域,并具有不同的临床特征,例如溃疡可以存在于黏膜亚型,但不存在于皮肤亚型,以及毛囊炎症是毛发扁平苔藓的独特特征。
[0217]
根据患者的主要临床亚型(通过活检证实)将患者分为三个亚组,以便应用亚型特异性评估。通过使用这种设计,该试验还能够收集关于非主要(“伴随”)亚型的数据,例如,纳入黏膜lp为主的亚组的患者的皮肤病变数据。通过允许在一次试验中纳入和评估所有三种亚型,这种“篮式试验”设计利用了亚型之间的重叠,同时通过使用亚型特异性的评估、评分和终点来捕获每个亚型的独特特征。
[0218]
研究设计:
[0219]
这是一项多中心、随机、双盲、安慰剂对照、平行组试验,其评估了两种不同给药方案中苏金单抗300mg在患有经活检证实形式的扁平苔藓患者中的功效和安全性。
[0220]
如图1所示,该研究由三个队列(每个扁平苔藓亚型一个队列:皮肤扁平苔藓(clp)、黏膜扁平苔藓(mlp)和毛发扁平苔藓(lpp))和4个研究期组成。
[0221]
基于患者的主要亚型将患者分配到三个队列中的一个,并在筛选访视时进行活检以确认临床诊断:
[0222]
·
主要是皮肤扁平苔藓
[0223]
·
主要是黏膜扁平苔藓
[0224]
·
毛发扁平苔藓
[0225]
每一个队列在整个4个时期遵循相同的研究设计:
[0226]
·
筛选期:基线前长达4周
[0227]
·
治疗期1:基线至第16周
[0228]
·
治疗期2:第16周至第32周
[0229]
·
随访:在第32周后的8周
[0230]
筛选期:
[0231]
长达4周的筛选期用于评估患者的试验资格并清除/调整禁用药物。筛选期涵盖从签署知情同意/筛选访视(-4周)到随机访视(第0周)的时间。
[0232]
如果患者由于暂时性状况或由于禁用药物清除期不足而未能通过初始筛选,则可以重新筛选患者。受试者只能重新筛选一次,并且在受试者重新同意之前不应执行重新筛选程序。
[0233]
治疗期1:
[0234]
治疗期1是安慰剂对照的,并且涵盖从第0周(随机访视)到第16周的时间。符合所有资格标准的患者以2:1的比例随机分配到其队列内的以下两个治疗组之一:
[0235]
·
每4周苏金单抗300mg组:受试者每周接受诱导治疗,随后每4周接受一次苏金单抗300mg。
[0236]
·
安慰剂持续16周随后每2周苏金单抗300mg组:受试者接受匹配的安慰剂注射。
[0237]
在治疗期1中,所有受试者在第0、1、2、3和4周每周接受皮下注射盲法研究药物(300mg苏金单抗或安慰剂)。此后,所有受试者的盲法研究药物注射频率为每4周一次直至第16周。在治疗期1期间不允许家中施用研究药物。完成治疗期1的受试者在第16周访视时转入至治疗期2。唯一的例外是来自安慰剂持续16周随后每2周苏金单抗300mg组的受试者,其在第16周访视时得到自发缓解。自发缓解定义为第16周时iga为0或1。这些受试者不继续进行治疗期2以避免不必要的治疗。相反,他们在第16周访视后直接进入随访期。
[0238]
治疗期2:
[0239]
治疗期2开始于第16周访视,并且涵盖到第32周访视的时间。
[0240]
根据治疗组,受试者接受以下治疗:
[0241]
·
每4周苏金单抗300mg组:受试者每4周接受一次苏金单抗300mg的持续治疗,加上匹配的安慰剂注射以维持治疗盲法。
[0242]
·
安慰剂持续16周随后每2周苏金单抗300mg组:受试者被转换为每2周用苏金单抗300mg进行积极治疗(包括开始于第16周的诱导),但在第16周时得到缓解的受试者除外。
[0243]
第16周注射是治疗期2的第一次注射。
[0244]
在治疗期2期间治疗保持盲态。这意味着开始于第16周的访视,所有受试者在第16、17、18、19和20周接受由每周盲法研究药物注射(苏金单抗300mg或安慰剂)组成的诱导,然后每2周进行盲法研究药物注射,每2周苏金单抗300mg与安慰剂交替(每4周苏金单抗300mg组)或每2周苏金单抗300mg(安慰剂持续16周随后每2周苏金单抗300mg组)直到第30周。
[0245]
最后一次研究药物注射是在第30周。治疗期2的结束是第32周。第32周后,所有受试者进入随访期。
[0246]
随访:
[0247]
第32周后有8周的随访期。
[0248]
剂量和方案的基本原理
[0249]
本研究将评估两种不同的苏金单抗给药方案:
[0250]
·
每4周苏金单抗300mg s.c.
[0251]
·
每2周苏金单抗300mg s.c.
[0252]
两种给药方案均以常规诱导开始,该常规诱导由在第0、1、2、3、4或16、17、18、19、20周每周注射苏金单抗300mg组成。正如广泛的中度至重度银屑病3期临床开发项目所证明的那样,在第一个月期间每周给药的诱导是安全的,并且能够快速达到有效药物浓度,从而导致快速出现临床应答(langley等人(2014)n engl j med.[新英格兰医学杂志]371(4):326-38)。
[0253]
每4周300mg sc方案的基本原理:
[0254]
苏金单抗300mg皮下施用,初始诱导后每四周的施用(维持)是与苏金单抗3期注册项目一致的,该项目已证明该给药方案在中度至重度斑块型银屑病患者中的功效和安全性(langley,2014)。此外,关于苏金单抗在患有clp和mlp的患者中潜在功效的临床证据来自病例系列,该病例系列示出对用每4周给药方案进行治疗的临床应答(solimani,2019)。在这个病例系列中没有报告相关的安全问题。
[0255]
每2周300mg sc方案的基本原理:
[0256]
除了上文概述的每4周给药方案外,在该2期研究中,还评估了第二种更高剂量方案(每2周300mg)对于患有扁平苔藓的患者的功效和安全性,从而比较两种给药方案并评估剂量反应关系。
[0257]
对于成功治疗中度至重度扁平苔藓,可能需要比斑块型银屑病更高的局部暴露;该患者群体可能对局部治疗具有高度抵抗力,尤其是在溃疡性/糜烂性病变的情况下。顽固患者随后需要全身治疗,包括免疫抑制剂如麦考酚酯或环孢菌素,以得到部分/完全应答(deen(2015)j dermatol.[皮肤病学杂志]42(3):311-4)。关于其他生物制剂在扁平苔藓中使用的报道很少,有一篇报道在clp患者中每周成功使用40mg阿达木单抗(chao(2009)cutis[皮肤]84(6):325-8)。
[0258]
对于苏金单抗,在第一个月期间的相同诱导期(第0、1、2、3和4周期间每周一次)后,可以用缩短的剂量间隔(每2周)取得比4周的间隔可以达到的全身暴露显著更高和更一致的全身暴露(图2)。在已完成的葡萄膜炎和银屑病的临床研究中,每2周苏金单抗300mg s.c.已经在约120名患者中进行了至少24周的测试。已经观察到安全特性与每4周苏金单抗300mg s.c.的安全特性一致。此外,目前正在2项患有化脓性汗腺炎的患者的3期试验(nct03713632、nct03713619)中和体重≥90kg的患有中度至重度银屑病的患者的3期试验(nct03504852)中评估每2周300mg的给药方案。
[0259]
详细的方案总结如下表5:
[0260]
[0261]
[0262]
[0263]
[0264][0265]
[0266]
[0267]
[0268]
[0269]
[0270]
[0271]
[0272]
[0273]
[0274]
[0275]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1