发酵乳杆菌菌株及含有其的用于预防或治疗代谢疾病的组合物的制作方法
文档序号:31694521发布日期:2022-10-01 03:15阅读:119来源:国知局
导航: X技术> 最新专利>有机化合物处理,合成应用技术
1.本公开涉及一种新型发酵乳杆菌(lactobacillus fermentum)菌株和包含该菌株的用于预防或治疗代谢疾病的组合物。
背景技术:
2.随着社会的发展,肥胖已成为一种严重的疾病,世界卫生组织(who)已将肥胖视为一种需要治疗的疾病。最近,在韩国也观察到由于西化饮食而导致的肥胖患病率增加的趋势,并且对治疗和预防肥胖的兴趣与日俱增。肥胖是指由于食物消费和能量消耗之间的不平衡而导致体脂过度积累的状态。此外,肥胖与胰岛素抵抗、糖耐量、高脂血症等密切相关,并可能伴有包括心血管疾病、脂肪肝病、癌症、糖尿病在内的代谢疾病作为并发症。
3.最近,众所周知,肥胖患者的脂肪组织中的炎症反应增加,肥胖有时被认为是一种低度全身性炎症。特别是已报道与脂肪组织的大小成比例增加的炎性巨噬细胞会增加炎症反应,在这种状态下脂肪组织产生和分泌的炎性脂肪因子是代谢疾病(如心血管疾病和糖尿病)的致病因素。因此,使这些分子增加的肥胖可以被视为几乎所有成人疾病的原因。
4.目前处方的肥胖药物有罗氏鲜(xenical)(roche pharmaceuticals.,瑞士)、诺美亭(reductil)(abbott co.,美国)和exolise(arkopharma llc,法国)等。肥胖药物主要分为食欲抑制剂、能量消耗促进剂或脂肪吸收抑制剂,并且大多数肥胖药物为食欲抑制剂,其通过控制与下丘脑相关的神经递质来抑制食欲。然而,常规的肥胖药物存在例如心脏病、呼吸系统疾病和神经系统疾病的副作用,并且具有体内持久性低的问题。因此,需要开发安全有效的肥胖治疗。
5.同时,对使用安全微生物(例如乳酸菌)来预防或治疗肥胖的益生菌已进行了积极研究。特别是,研究表明,乳酸菌具有例如维持正常肠道菌群、改善肠道菌群、抗糖尿病和抗血脂作用、抑制癌变、抑制结肠癌和宿主免疫系统非特异性活性的作用。
6.关于与肥胖预防和治疗效果相关的乳酸菌,韩国专利第10-1494279号公开了对脂肪细胞分化具有抑制作用的植物乳杆菌(lactobacillus plantarum)ky1032菌株(保藏号kccm-10430),韩国专利第10-0996577号公开了具有肥胖抑制作用的弯曲乳杆菌(lactobacillus curvatus)hy7601(保藏号kctc 11456bp),以及韩国专利第10-1394348号公开了对脂肪细胞分化具有抑制作用的植物乳杆菌dsr920菌株(保藏号kccm 11210p),但它们都没有成熟到足以取得商业上的成功。
7.因此,需要继续研究具有优异抗肥胖效果的新菌株。
技术实现要素:
8.技术问题
9.因此,本发明人通过研究开发具有优异抗肥胖效果的新菌株,发现了发酵乳杆菌菌株(保藏号kctc 14106bp)显示出优异的抗肥胖效果,从而完成了本发明。
10.解决方案
11.本发明的一个方面提供了一种发酵乳杆菌菌株(保藏号kctc 14106bp)。
12.本发明的另一方面提供一种用于预防或治疗代谢疾病的药物组合物,该药物组合物包含发酵乳杆菌菌株(保藏号kctc 14106bp)或其培养物作为活性成分。
13.本发明的又一方面提供了一种用于预防或抑制代谢疾病的食品组合物,该食品组合物包含发酵乳杆菌菌株(保藏号kctc 14106bp)或其培养物。
14.本发明的再一方面提供了一种用于预防或抑制代谢疾病的饲料组合物,该饲料组合物包含发酵乳杆菌菌株(保藏号kctc 14106bp)或其培养物。
15.本发明的又再一方面提供了一种预防和治疗代谢疾病的方法,该方法包括向对象施用发酵乳杆菌菌株(保藏号kctc 14106bp)或其培养物。
16.发明效果
17.本公开涉及一种新型发酵乳杆菌(保藏号kctc 14106bp)菌株和包含该菌株的用于预防或治疗代谢疾病的组合物。根据本发明的发酵乳杆菌可以抑制白色脂肪组织中的脂肪堆积并增加抗炎细胞。此外,根据本发明的发酵乳杆菌可以有效抑制棕色脂肪组织和肝组织中的脂肪堆积。发酵乳杆菌菌株可以表现出优异的血糖改善作用,特别是可以降低空腹血糖水平。发酵乳杆菌菌株可通过改善葡萄糖耐量和增加胰岛素敏感性来有效改善胰岛素抵抗。因此,该发酵乳杆菌菌株可有用地用于预防或治疗代谢疾病如肥胖。
附图说明
18.通过以下结合附图的描述,可以更详细地理解示例性实施方式,其中:
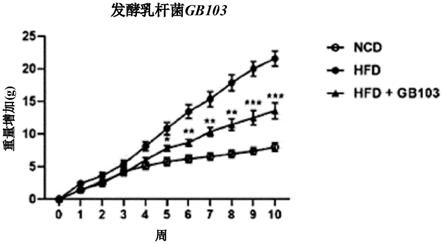
19.图1至图3是示出了分别口服施用16种乳酸菌菌株后的饲喂高脂饮食的小鼠与仅饲喂高脂饮食的小鼠相比的体重的图。
20.图4是比较各来自饲喂正常饲料的小鼠、饲喂高脂饮食的小鼠、饲喂高脂饮食并口服施用普通乳酸菌的小鼠以及饲喂高脂饮食并口服施用发酵乳杆菌(l.fermentum)gb103菌株的小鼠的白色脂肪组织中的脂肪细胞的大小的图。
21.图5是比较饲喂正常饲料的小鼠、饲喂高脂饮食的小鼠、饲喂高脂饮食并口服施用普通乳酸菌的小鼠以及饲喂高脂饮食并口服施用发酵乳杆菌gb103菌株的小鼠的白色脂肪组织中的m1巨噬细胞、m2巨噬细胞和调节性t(treg)细胞的数量的图。
22.图6是比较饲喂正常饲料的小鼠、饲喂高脂饮食的小鼠、饲喂高脂饮食并口服施用普通乳酸菌的小鼠以及饲喂高脂饮食并口服施用发酵乳杆菌gb103菌株的小鼠的棕色脂肪组织中的脂肪细胞的大小的图。
23.图7是比较饲喂正常饲料的小鼠、饲喂高脂饮食的小鼠、饲喂高脂饮食并口服施用普通乳酸菌的小鼠以及饲喂高脂饮食并口服施用发酵乳杆菌gb103菌株的小鼠的肝脏重量的图。
24.图8是比较饲喂正常饲料的小鼠、饲喂高脂饮食的小鼠、饲喂高脂饮食并口服施用普通乳酸菌的小鼠以及饲喂高脂饮食并口服施用发酵乳杆菌gb103菌株的小鼠的肝组织中脂肪堆积程度的图。
25.图9是比较饲喂正常饲料的小鼠、饲喂高脂饮食的小鼠、饲喂高脂饮食并口服施用普通乳酸菌的小鼠以及饲喂高脂饮食并口服施用发酵乳杆菌gb103菌株的小鼠的空腹血糖
水平以确认降低血糖作用的图。
26.图10是比较饲喂正常饲料的小鼠、饲喂高脂饮食的小鼠、饲喂高脂饮食并口服施用普通乳酸菌的小鼠以及饲喂高脂饮食并口服施用发酵乳杆菌gb103菌株的小鼠中施用葡萄糖后随着时间的推移的血糖水平以确认糖耐量改善作用的图;以及
27.图11是比较饲喂正常饲料的小鼠、饲喂高脂饮食的小鼠、饲喂高脂饮食并口服施用普通乳酸菌的小鼠以及饲喂高脂饮食并口服施用发酵乳杆菌gb103菌株的小鼠中施用胰岛素后随着时间的推移的血糖水平以确认胰岛素抵抗改善作用的图。
具体实施方式
28.本发明的一个方面提供了一种发酵乳杆菌菌株(保藏号kctc 14106bp)。
29.乳杆菌(lactobacillus)是一种广泛分布于自然界的需氧或兼性厌氧的革兰氏阳性杆菌。乳杆菌属包括发酵乳杆菌、清酒乳杆菌(l.sakei)等。本发明人选择了一种具有优异的抗肥胖效果的新型发酵乳杆菌菌株,并将其命名为“发酵乳杆菌gb103”。该菌株于2019年9月6日以保藏号sd1342保藏于韩国生命工学研究院韩国典型菌种保藏中心(korea collection for type cultures,korea research institute of bioscience and biotechnology)。相同菌株于2020年1月14日以保藏号kctc 14106bp保藏于韩国生命工学研究院韩国典型菌种保藏中心。此外,该菌株属于益生菌菌株,对人体无害,并且可无副作用使用。
30.如本文所用,术语“发酵乳杆菌(lactobacillus fermentum)gb103”可互换地描述为发酵乳杆菌(l.fermentum)gb103或发酵乳杆菌(lactobacillus fermentum)菌株(保藏号kctc 14106bp)。
31.本发明的另一方面提供一种用于预防或治疗代谢疾病的药物组合物,该药物组合物包含发酵乳杆菌菌株(保藏号kctc 14106bp)或其培养物作为活性成分。
32.发酵乳杆菌菌株(保藏号kctc 14106bp)与上述相同。在这种情况下,菌株可以是活的或死的,并且优选活菌株。另外,菌株的培养物可以含有也可以不含有菌株,优选含有菌株。
33.基于组合物的总重量,所述组合物包括治疗有效量或营养有效浓度的活性成分发酵乳杆菌菌株(保藏号kctc 14106bp)或其培养物,其中包括的含量为104至10
16
cfu/g,优选106至10
12
cfu/g,或包括具有等量活菌株的培养物。一般而言,对于成年患者,可以一次或分几次施用1
×
106cfu/g或更多的活菌株,优选1
×
108至1
×
10
12
cfu/g的活菌株。
34.如本文所用,术语“代谢疾病”,也称为代谢综合征,是被认为由胰岛素抵抗引起的疾病并且是具有胆固醇、血压和血糖水平中的两种或更多种异常的症状。代谢综合征是对各种心血管疾病和2型糖尿病的风险因素一起聚集为一个疾病群的现象的概念化,并且涵盖了胰岛素抵抗以及与胰岛素抵抗相关的所有复杂多样的各种代谢异常和临床特征。具体地,代谢疾病可以是选自由肥胖、高血压、动脉硬化、高脂血症、脂肪肝、非酒精性脂肪肝病、高胰岛素血症、糖尿病和胰岛素抵抗综合征组成的组中的任一种。
35.如本文所用,术语“肥胖”,也称为多脂症,是一种过多体脂异常堆积的疾病。不规律的饮食习惯、摄食过多、缺乏体力活动、内分泌系统疾病、遗传因素、心理因素、服药等都可导致肥胖。此外,肥胖会增加动脉硬化、心血管疾病(中风和缺血性心血管疾病)、高血压、
糖尿病、高脂血症、脂肪肝、胆石症、阻塞性睡眠呼吸暂停、月经不调、多囊卵巢疾病、不孕症、性欲减退、抑郁症、退行性关节炎、痛风等的发病率。肥胖可以是单纯性肥胖、症状性肥胖、儿童肥胖、成人肥胖、细胞增殖性肥胖、细胞肥大性肥胖、上身肥胖、下身肥胖、内脏脂肪肥胖或皮下脂肪肥胖。
36.如本文所用,术语“高血压”是指流经动脉的血流的灌流血压升高的现象。如果收缩压达到140mmhg,舒张压达到90mmhg以上,一般就可以诊断为高血压。高血压没有明显的症状,有不明原因的原发性(或特发性)高血压,以及由肾病、内分泌疾病、妊娠中毒症等引起的继发性高血压。大多数高血压病例(90%至95%)是原发性高血压,其被认为是由遗传原因以及环境因素(例如肥胖、压力、酒精和吸烟)引起的。
37.如本文所用,术语“动脉硬化”定义为由于动脉壁失去弹性、异常组织增殖和脂肪在动脉壁内层内堆积而使动脉壁宽度变窄的现象。动脉硬化是指动脉发生病变的术语,并根据受动脉硬化影响的器官进行命名。例如,动脉硬化包括但不限于由动脉硬化引起的脑梗塞和由冠状动脉硬化引起的心肌梗塞。
38.如本文所用,术语“高脂血症”是由于脂质代谢不能正常进行以致血液中有大量脂质(如甘油三酯和胆固醇)而导致的疾病。具体而言,高脂血症是指血液中脂质成分(如甘油三酯、ldl胆固醇和游离脂肪酸)增加的状态。高脂血症包括但不限于高胆固醇血症或高甘油三酯血症。
39.如本文所用,术语“脂肪肝”是由于脂质代谢紊乱而导致肝细胞中脂肪过度堆积的状态,并且定义为脂肪达到肝脏重量的5%或更多的情况。这引起各种疾病,例如心绞痛、心肌梗塞、中风、动脉硬化、脂肪肝、胰腺炎等。脂肪肝分为由饮酒引起的酒精性脂肪肝和不是由酒精引起的非酒精性脂肪肝病(non-alcoholic fatty liver disease,nafld)。
40.如本文所用,术语“非酒精性脂肪肝病”是指脂肪肝不是由酒精引起的情况,包括一系列肝损害过程,从肝脏的单纯性脂肪变性、非酒精性脂肪性肝炎(non-alcoholic steatohepatitis,nash)到肝硬化。非酒精性脂肪肝病的病因是:诸如抗心律失常剂、抗病毒剂、类固醇、或细胞毒性剂的药物的副作用;过多的诸如碳水化合物的卡路里消耗;肥胖;糖尿病;和一些遗传原因。
41.如本文所用,术语“高胰岛素血症”是血液中存在过量胰岛素的疾病。胰岛素是由胰腺分泌的,是调节血糖水平并促进葡萄糖流入肌肉和其他外周组织的激素。因此,高胰岛素血症可能由于胰岛素分泌器官胰腺的紊乱而发生,最常由胰岛素抵抗引起。
42.如本文所用,术语“糖尿病”是一种慢性疾病,其特点是胰岛素相对或绝对缺乏导致葡萄糖耐受不良。糖尿病包括所有类型的糖尿病,例如可以是1型糖尿病、2型糖尿病和遗传性糖尿病,但不限于此。1型糖尿病是胰岛素依赖型糖尿病,主要由β细胞破坏所致。如本文所用,术语“2型糖尿病”是胰岛素非依赖型糖尿病,其由胰岛素抵抗引起。2型糖尿病是因为在肌肉和脂肪组织中没有检测到胰岛素的增加,或者即使检测到了胰岛素也没有有效地发生作用而引起的。
43.如本文所用,术语“胰岛素抵抗”是指细胞对降低血糖水平的胰岛素没有反应,因此不能有效燃烧葡萄糖的状态。当胰岛素抵抗高时,身体认为需要更多的胰岛素并产生更多的胰岛素。这会导致高胰岛素血症、高血压或血脂异常,以及心脏病和糖尿病。
44.如本文所用,术语“胰岛素抵抗综合征”是由胰岛素抵抗引起的疾病的通用术语。
其特点是细胞对胰岛素作用产生抵抗、高胰岛素血症和极低密度脂蛋白(very low-density lipoprotein,vldl)和甘油三酯升高、以及高密度脂蛋白(high density lipoprotein,hdl)降低、高血压等,其被公认为是心血管疾病和2型糖尿病的风险因素。
45.根据本发明的实施方式,菌株可以抑制白色脂肪组织中的脂肪堆积。具体地,在本发明的实施方式中,将该菌株口服施用至饲喂高脂饮食的小鼠模型导致小鼠模型的白色脂肪组织中脂肪细胞的大小显著减小。同时,当对饲喂高脂饮食的小鼠模型口服施用普通乳酸菌时,小鼠模型白色脂肪组织中脂肪细胞的大小没有减小。基于此,确认该菌株抑制白色脂肪组织中的脂肪堆积(图4)。
46.根据本发明的实施方式,该菌株可以减少白色脂肪组织中的代谢炎症(meta-inflammation)。如本文所用,术语“代谢炎症”是慢性和低度的炎症,是指当提供过量的营养物或代谢物时发生的炎症反应。特别是,已知由肥胖引起的慢性炎症反应在增加胰岛素抵抗和发展代谢异常的过程中起重要作用。
47.在本发明的实施方式中,将该菌株口服施用至饲喂高脂饮食的小鼠模型导致小鼠模型白色脂肪组织中的m1巨噬细胞减少,并且m2巨噬细胞和treg细胞显著增加。同时,当对饲喂高脂饮食的小鼠模型口服施用普通乳酸菌时,小鼠模型的白色脂肪组织中m1巨噬细胞显著减少,但m2和treg细胞没有变化。基于此,确认该菌株抑制白色脂肪组织中的炎症反应(图5)。
48.根据本发明的实施方式,该菌株可以抑制棕色脂肪组织中的脂肪堆积。具体地,在本发明的实施方式中,将该菌株口服施用至饲喂高脂饮食的小鼠模型导致小鼠模型的棕色脂肪组织中脂肪细胞的大小显著减小。同时,当对饲喂高脂饮食的小鼠模型口服施用普通乳酸菌时,小鼠模型棕色脂肪组织中脂肪细胞的大小没有减小。基于此,确认该菌株抑制棕色脂肪组织中的脂肪堆积(图6)。
49.根据本发明的实施方式,该菌株可以减轻肝脏重量并抑制肝组织中的脂肪堆积。具体地,在本发明的实施方式中,将该菌株口服施用至饲喂高脂饮食的小鼠模型导致小鼠模型的肝脏重量和组织中的脂肪堆积减少。同时,当对饲喂高脂饮食的小鼠模型口服施用普通乳酸菌时,小鼠模型的肝组织中堆积了大量脂肪,并且肝脏重量也没有变化。基于此,确认该菌株降低了肝脏重量并抑制了组织中的脂肪堆积(图7和图8)。
50.根据本发明的实施方式,该菌株可以降低血糖水平。优选地,该菌株可以降低空腹血糖水平并改善葡萄糖耐量。具体地,在本发明的实施方式中,将该菌株口服施用至饲喂高脂饮食的小鼠模型导致该小鼠模型的空腹血糖水平和施用葡萄糖后的血糖水平降低。同时,当对饲喂高脂饮食的小鼠模型口服施用普通乳酸菌时,空腹血糖水平和施用葡萄糖后的血糖水平均没有降低。基于此,确认该菌株降低了空腹血糖水平并改善了葡萄糖耐量(图9和图10)。
51.根据本发明的实施方式,该菌株可以改善胰岛素抵抗。具体地,在本发明的实施方式中,当将该菌株口服施用至饲喂高脂饮食的小鼠模型时,施用胰岛素后小鼠模型的血糖水平显著降低。同时,当对饲喂高脂饮食的小鼠模型口服施用普通乳酸菌时,空腹血糖水平和施用胰岛素后的血糖水平均没有降低。基于此,确认该菌株通过增加胰岛素敏感性来改善胰岛素抵抗(图11)。
52.该组合物还可以包含冷冻保护剂或赋形剂。具体地,冷冻保护剂可以是选自由甘
油、海藻糖、麦芽糖糊精、脱脂奶粉和淀粉组成的组中的一种或多种。此外,赋形剂可以是选自由葡萄糖、糊精和脱脂奶粉组成的组中的一种或多种。
53.基于组合物的总重量,组合物可以包含0.01wt%至20wt%或0.01wt%至10wt%的冷冻保护剂,具体地,组合物可以包括5wt%至20wt%%的甘油、2wt%至10wt%的海藻糖、2wt%至10wt%的麦芽糖糊精、0.5wt%至2wt%的脱脂奶粉和0.1wt%至1wt%的淀粉。此外,基于组合物的总重量,组合物可以包含75wt%至95wt%或85wt%至95wt%的赋形剂。
54.本发明的又一方面提供了一种用于预防或抑制代谢疾病的食品组合物,该食品组合物包含发酵乳杆菌菌株(保藏号kctc 14106bp)或其培养物。
55.发酵乳杆菌菌株(保藏号kctc 14106bp)与上述相同。
56.在这种情况下,代谢疾病如上所述,并且特别地,该菌株可以是用于预防或抑制肥胖的食品组合物。
57.食品组合物包括所有形式,例如功能性食品、营养补充剂、保健食品、食品添加剂,并且食品组合物的种类可以按照本领域公知的常规方法制备成各种形式。
58.在将该菌株用作食品添加剂的情况下,该菌株可以照原样添加,或者可以与其他食品或食品成分一起使用,并且可以根据常规方法适当使用。有效成分的混合量可以根据使用目的(预防、保健或治疗性处理)来适当确定。通常,在制备食品或饮料时,活性成分在含有该菌株的原料组合物中的添加量可以为0.0001wt%至1wt%,特别是0.001wt%至0.1wt%。但是,在为了保健和卫生或健康控制目的而长期摄入的情况下,该量可低于上述范围。
59.本发明的再一方面提供了一种用于预防或抑制代谢疾病的饲料组合物,该饲料组合物包含发酵乳杆菌菌株(保藏号kctc 14106bp)或其培养物。
60.发酵乳杆菌菌株(保藏号kctc 14106bp)与上述相同。
61.用于预防或改善代谢疾病的饲料组合物可以根据本领域已知的制备饲料组合物的各种方法,通过添加适当有效浓度范围的发酵乳杆菌菌株(保藏号kctc14106bp)来制备。
62.本发明的又再一方面提供了一种预防和治疗代谢疾病的方法,该方法包括向对象施用发酵乳杆菌菌株(保藏号kctc 14106bp)或其培养物。
63.对象可患有代谢疾病。此外,对象可以是哺乳动物,优选人。在这种情况下,发酵乳杆菌菌株(保藏号kctc 14106bp)与上述相同。此外,菌株或其培养物的施用途径、剂量和施用频率可以根据患者的状况以及副作用存在或不存在以各种方式和量施用至对象,并且最佳的施用方法、剂量和施用频率可以由本领域技术人员在适当的范围内适当地进行选择。另外,代谢疾病的种类如上所述。
64.本发明的再一方面提供了发酵乳杆菌菌株(保藏号kctc 14106bp)或其培养物治疗代谢疾病的用途。
65.在这种情况下,发酵乳杆菌菌株(保藏号kctc 14106bp)与上述相同。另外,代谢疾病的种类如上所述。
66.具体实施方式
67.下文将通过以下实施例更为详细地描述本发明。然而,以下实施例仅用于说明本发明,并且本发明的范围不受以下实施例的限制。
68.实施例1.筛选具有抗肥胖效果的菌株
69.使用小鼠模型从购自mediogen co.,的16种乳酸菌中选择具有抗肥胖功效的乳酸菌。具体来说,用60%高脂饮食(high fat diet,hfd)饲喂,然后口服施用各乳酸菌的c57bl/6小鼠作为实验组。仅用60%高脂饮食饲喂的小鼠作为对照组。在这种情况下,每只小鼠每天以5
×
109cfu口服施用各乳酸菌。根据实验组和对照组的体重差异确定抗肥胖作用。
70.结果,发酵乳杆菌gb103菌株最有效地抑制了体重增加。在这种情况下,有一些发酵乳杆菌乳酸菌没有表现出抗肥胖作用(图1至图3)。基于此,确认了发酵乳杆菌gb103菌株在发酵乳杆菌乳酸菌中表现出抗肥胖作用。
71.实施例2.发酵乳杆菌gb103菌株在白色脂肪组织中的脂肪堆积抑制作用的确认
72.使用小鼠模型来确认发酵乳杆菌gb103(保藏号kctc 14106bp)菌株在白色脂肪组织中的脂肪堆积抑制作用。具体来说,用60%的高脂饮食(hfd)饲喂,然后口服施用发酵乳杆菌gb103菌株的c57bl/6小鼠作为实验组。此外,以仅饲喂60%高脂饮食的小鼠作为阴性对照组,以饲喂60%高脂饮食并口服施用普通乳酸菌(植物乳杆菌mg5120)的小鼠作为阳性对照组。此外,将饲喂正常饲料(normal chow diet,ncd)的小鼠用作正常组。在这种情况下,每只小鼠每天以5
×
109cfu口服施用从mediogen co.,购买的普通乳酸菌,或发酵乳杆菌gb103菌株。
73.各测试物质施用完毕后,通过剖检分离白色脂肪组织。分离的白色脂肪组织用10%中性缓冲福尔马林固定。然后,制备石蜡切片,用苏木精和伊红(h&e)染色,然后观察细胞大小。
74.结果表明,与正常组相比,饲喂高脂饮食的阴性对照组和阳性对照组的脂肪细胞大小增大,而口服施用发酵乳杆菌gb103菌株的实验组的脂肪细胞大小显著减小(图4)。基于此,确认了发酵乳杆菌gb103菌株有效抑制白色脂肪组织中的脂肪堆积。
75.实施例3.发酵乳杆菌gb103菌株在白色脂肪组织中的免疫细胞调节作用的确认
76.使用小鼠模型来确认施用发酵乳杆菌gb103菌株导致白色脂肪组织中免疫细胞变化。具体来说,用60%(hfd)饲喂,然后口服施用发酵乳杆菌gb103菌株的c57bl/6小鼠作为实验组。此外,以仅饲喂60%高脂饮食的小鼠作为阴性对照组,以饲喂60%高脂饮食并口服施用普通乳酸菌(植物乳杆菌mg5120)的小鼠作为阳性对照组。此外,将饲喂正常饲料(ncd)的小鼠用作正常组。在这种情况下,每只小鼠每天以5
×
109cfu口服施用从mediogen co.,购买的普通乳酸菌,或发酵乳杆菌gb103菌株。
77.各测试物质施用完毕后,通过剖检从各组小鼠的附睾白色脂肪细胞组织中分离免疫细胞,用特异性抗体对细胞染色,然后通过流式细胞仪分析。用弯剪将脂肪组织切碎,与2mg/mlⅱ型胶原(worthington)在37℃下孵育45分钟,然后通过离心机分离基质血管组分(svf)。用facs缓冲液洗涤,然后在4℃下封闭10分钟以抑制非特异性结合。将抗mhcⅱ(biolegend,ca,美国)、抗f4/80(biolegend,ca,美国)、抗cd206(biolegend,ca,美国)、抗cd11c(biolegend,ca,美国)和抗cd11b(biolegend,ca,美国)抗体添加到m1/m2巨噬细胞中,并在4℃下反应30分钟,然后用facs缓冲液洗涤。使用抗tcrβ(biolegend,ca,美国)和抗cd4(biolegend,ca,美国)抗体对treg细胞进行与上述相同的程序,然后用ebioscience
tm foxp3/转录因子染色缓冲液进行处理用于固定和增加通透性以用抗foxp3抗体(ebioscience,ca,美国)染色。在mhcii+f4/80+巨噬细胞中,用m2巨噬细胞分析cd11b+
cd206+细胞,用m1巨噬细胞分析cd11b+cd11c+细胞。用tcrβ+cd4+foxp3+分析treg细胞。
78.结果显示,饲喂高脂饮食的阴性和阳性对照组小鼠的炎性m1巨噬细胞数量均高于正常组,而口服施用发酵乳杆菌gb103菌株的实验组小鼠的m1巨噬细胞数量显著低于阴性对照组。还确认了饲喂高脂饮食的阴性和阳性对照组小鼠的抗炎m2巨噬细胞和treg细胞数量均低于正常组,而口服施用发酵乳杆菌gb103菌株的实验组小鼠的m2巨噬细胞和treg细胞数量与阴性对照组相比显著增加。基于此,确认了发酵乳杆菌gb103菌株在白色脂肪组织中的免疫细胞调节作用(图5)。
79.实施例4.发酵乳杆菌gb103菌株在棕色脂肪组织中的脂肪堆积抑制作用的确认
80.使用小鼠模型来确认发酵乳杆菌gb103菌株在棕色脂肪组织中的脂肪堆积抑制作用。具体来说,用60%(hfd)饲喂,然后口服施用发酵乳杆菌gb103菌株的c57bl/6小鼠作为实验组。此外,以仅饲喂60%高脂饮食的小鼠作为阴性对照组,以饲喂60%高脂饮食并口服施用普通乳酸菌(植物乳杆菌mg5120)的小鼠作为阳性对照组。此外,将饲喂正常饲料(ncd)的小鼠用作正常组。在这种情况下,每只小鼠每天以5
×
109cfu口服施用从mediogen co.,购买的普通乳酸菌,或发酵乳杆菌gb103菌株。
81.各测试物质施用完毕后,通过剖检从各组小鼠中分离棕色脂肪组织。分离的棕色脂肪组织用10%中性缓冲福尔马林固定。然后,制备石蜡切片,用h&e染色,然后观察细胞大小。
82.结果表明,与正常组相比,饲喂高脂饮食的阴性对照组和阳性对照组小鼠的脂肪细胞大小增大,而口服施用发酵乳杆菌gb103菌株的实验组的脂肪细胞大小显著减小(图6)。基于此,确认了发酵乳杆菌gb103菌株有效抑制棕色脂肪组织中的脂肪堆积。
83.实施例5.发酵乳杆菌gb103菌株在肝组织中的脂肪堆积抑制作用的确认
84.使用小鼠模型来确认发酵乳杆菌gb103菌株在肝组织中的脂肪堆积抑制作用。具体来说,用60%(hfd)饲喂,然后口服施用发酵乳杆菌gb103菌株的c57bl/6小鼠作为实验组。此外,以仅饲喂60%高脂饮食的小鼠作为阴性对照组,以饲喂60%高脂饮食并口服施用普通乳酸菌(植物乳杆菌mg5120)的小鼠作为阳性对照组。此外,将饲喂正常饲料(ncd)的小鼠用作正常组。在这种情况下,每只小鼠每天以5
×
109cfu口服施用从mediogen co.,购买的普通乳酸菌,或发酵乳杆菌gb103菌株。
85.各测试物质施用完毕后,通过剖检取出肝脏并测量肝脏重量,比较评价各组间的肝脏重量。提取的肝脏用10%缓冲福尔马林固定后,制备石蜡切片,用h&e染色,然后观察细胞大小。
86.结果表明,与正常组相比,饲喂高脂饮食的阴性对照组和阳性对照组小鼠的肝脏重量增加,而口服施用发酵乳杆菌gb103菌株的实验组小鼠的肝脏重量与阴性对照组相比显著减少(图7)。此外,与正常组相比,饲喂高脂饮食的阴性和阳性对照组小鼠的肝组织中的脂肪堆积增加,然而,口服施用发酵乳杆菌gb103菌株的实验组小鼠的肝组织中的脂肪堆积很少,并且脂肪堆积水平与阴性对照组相似(图8)。基于此,确认了发酵乳杆菌gb103菌株有效抑制肝脏重量和肝组织中的脂肪堆积。
87.实施例6.发酵乳杆菌gb103菌株的空腹血糖降低和糖耐量改善作用的确认
88.进行葡萄糖耐量试验(glucose tolerance test,gtt)以确认发酵乳杆菌gb103菌株的葡萄糖耐量改善作用。首先,用60%(hfd)饲喂,然后口服施用发酵乳杆菌gb103菌株的
c57bl/6小鼠作为实验组。此外,以仅饲喂60%高脂饮食的小鼠作为阴性对照组,以饲喂60%高脂饮食并口服施用普通乳酸菌(植物乳杆菌mg5120)的小鼠作为阳性对照组。此外,将饲喂正常饲料(ncd)的小鼠用作正常组。在这种情况下,每只小鼠每天以5
×
109cfu口服施用从mediogen co.,购买的普通乳酸菌,或发酵乳杆菌gb103菌株。
89.为了进行葡萄糖耐量试验,将小鼠禁食16小时或更长时间,然后以1g/kg的剂量腹腔内注射葡萄糖溶液。然后,在0、30、60、90和120分钟后从小鼠的尾静脉采血,并使用血糖仪测量血糖。在这种情况下,0分钟的血糖是指空腹血糖。
90.结果表明,与正常组相比,饲喂高脂饮食的阴性和阳性对照组小鼠的空腹血糖水平显著增加。同时,口服施用发酵乳杆菌gb103菌株的实验组小鼠的空腹血糖水平与阴性对照组相比显著降低(图9)。
91.此外,确认了在施用葡萄糖后,饲喂高脂饮食的阴性和阳性对照组小鼠的血糖水平高于正常组,而口服施用发酵乳杆菌gb103菌株的实验组小鼠的血糖水平与阴性对照组相比显著降低(图10)。基于此,确认发酵乳杆菌gb103菌株表现出空腹血糖降低和葡萄糖耐量改善作用。
92.实施例7.发酵乳杆菌gb103菌株的胰岛素抵抗改善作用的确认
93.进行胰岛素耐量试验(itt)以确认发酵乳杆菌gb103菌株的胰岛素抵抗改善作用。首先,用60%(hfd)饲喂,然后口服施用发酵乳杆菌gb103菌株的c57bl/6小鼠作为实验组。此外,以仅饲喂60%高脂饮食的小鼠作为阴性对照组,以饲喂60%高脂饮食并口服施用普通乳酸菌(植物乳杆菌mg5120)的小鼠作为阳性对照组。此外,将饲喂正常饲料(ncd)的小鼠用作正常组。在这种情况下,每只小鼠每天以5
×
109cfu口服施用从mediogen co.,购买的普通乳酸菌,或发酵乳杆菌gb103菌株。
94.为了进行胰岛素耐量试验,将小鼠禁食4.5小时,然后以1u/kg的剂量腹腔内施用胰岛素溶液。0、30、60、90和120分钟后从小鼠的尾静脉采血,然后使用血糖仪测量血糖。
95.结果确认了在施用胰岛素后,饲喂高脂饮食的阴性和阳性对照组小鼠的血糖水平高于正常组,而口服施用发酵乳杆菌gb103菌株的实验组小鼠的血糖水平与阴性对照组相比显著降低(图11)。基于此,确认了发酵乳杆菌gb103菌株通过增加胰岛素敏感性有效改善胰岛素抵抗。
96.《保藏号》
97.保藏机构名称:韩国生命工学研究院韩国典型菌种保藏中心(kctc)
98.保藏号:kctc14106bp
99.保藏日期:20200114。
100.
- 该技术已申请专利。仅供学习研究,如用于商业用途,请联系技术所有人。
- 技术研发人员:梁甫伎 张明浩 姜昶镐 白南树
- 技术所有人:GI生物群系公司
- 我是此专利的发明人
- 该领域下的技术专家
- 如您需求助技术专家,请点此查看客服电话进行咨询。
- 1、薛老师:1.CRISPR-Cas系统 2.基因编辑 3.基因修复 4.天然产物合成 5.单分子技术开发与应用
- 2、张老师:1.探索新型氧化还原酶结构-功能关系,电催化反应机制 2.酶电催化导向的酶分子改造 3.纳米材料、生物功能多肽对酶-电极体系的影响4. 生物电化学传感和生物电合成体系的设计与应用。
- 3、豆老师:1.环境纳米材料及挥发性有机化合物(VOCs) 2.CO污染物的催化氧化 3.低温等离子体 4.吸脱附等控制技术
- 4、赵老师:1.高分子材料改性及加工技术 2.微孔及过滤材料 3.环境友好高分子材料
- 5、邬老师:1.高分子材料的共混与复合 2.涉及材料功能化及结构与性能的研究; 高分子热稳定剂的研发
- 如您是高校老师,可以点此联系我们加入专家库。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
精彩留言,会给你点赞!
专利分类正在加载中....