IL1-R1衍生的IL-1β抑制剂及其用途的制作方法
il1-r1衍生的il-1
β
抑制剂及其用途
技术领域
1.本发明整体涉及生物制药领域,以及其在炎症异常(如类风湿关节炎、克罗恩病等)、糖尿病、心血管疾病和痛风相关病症中的应用。具体地说,本发明涉及一种异二聚体组成,il1-r1/il-1racp衍生物,其能够抑制细胞因子il-1β。
背景技术:
2.白细胞介素-1(il-1)细胞因子家族包括11种蛋白质(il-1f1到il-1f11),对人和小鼠的11个单个基因编码。il-1型细胞因子是先天免疫反应的主要介质,白细胞介素-1受体拮抗剂(il-1ra)对il-1或il-1β主要成员的阻滞表明il-1在人类一系列自身炎症性疾病中的核心作用。在几种不同类型的细胞中,il-1或il-1β快速上调数百个基因的基质rna表达。il-1和il-1β的强大促炎作用限制在三个主要水平:(i)合成和释放,(ii)膜受体,(iii)细胞间信号传递。该通路包括il-1或il-1β信号的胞外和胞内传导,包括增强或终止il-1反应的正反馈和负反馈机制。磷酸化和泛素化现象对配体与受体结合反应的复杂组合序列导致核kappa-b因子信号通路和丝裂原活化蛋白激酶jnk和p38通路的激活。通过转录和转录后机制共同诱导典型的il-1靶基因(如il-6,il-8,mcp-1,cox-2,ib,il-1,il-1β,mkp-1)的表达。值得注意的是,大多数参与细胞对il-1反应的细胞内成分也介导对其他细胞因子(il-18和il-33)、toll样受体(tlr)和许多形式的细胞毒性应激的反应(见weber a,et al.,sci signal.,2010jan 19;3(105),作者的完整理论计算作为参考资料纳入本文)。
3.il-1和il-1β独立结合普遍表达的il-1i型受体(il-1r1)。第三种特异性配体,il-1受体拮抗剂(il-1ra)以类似的特异性和亲和力与il-1ri结合,但不激活受体或触发进一步的信号传导。il-1受体辅助蛋白(il-1racp)是il-1/il-1ri复合物信号传递所需的辅助受体,也是il-1家族其他成员,特别是il-18和il-33激活il-1r1所必需的辅助受体。ⅱ型il-1受体(il-1r2)与il-1和il-1β结合,但缺乏能够传递信号的胞浆部分,从而充当陷阱受体。固定在il-1r2等离子膜的il-1ra和il-1受体细胞外链的自然“服务”结构域(表示sil-1ri、sil-1rii和sil-1racp,其中“s”表示“soluble”(“可溶解的”)是细胞外间隙il-1信号传导的诱导负调节因子,其过量由转录增强和控制释放共同调节,可限制或停止il-1的作用。
4.在il-1信号转导中的起始阶段是配体引起的il-1ri第一个胞外结构域构象的改变,使il-1racp更容易被吸引。通过被称为toll-和il-1r样(tir)结构域的保守胞浆片段,三维复合体快速组装了两种细胞内信号蛋白,即髓细胞分化原反应基因88(myd88)和白细胞介素1受体激活蛋白激酶(irak)4。缺乏myd88或irak4的小鼠存在明显的il-1信号传导缺陷。同样,irak4基因突变的个体也存在il-1ri和toll样受体(tlr)信号传导缺陷。il-1、il-1ri、il-racp、myd88和irak4形成稳定的il-1诱导的第一信号模块。与此平行的是irak4的(自)磷酸化,irak4随后磷酸化irak1和irak2,然后是肿瘤坏死因子相关因子(traf)6的参与和齐聚。irak1和2作为适配器和蛋白激酶来进一步传递信号。irak1,irak2和traf6复合物与原代受体复合物分离,在缺乏这些蛋白的细胞中,核转录因子kappa-b(nf-kappa-b)和
激活蛋白1(ap-1)的激活被破坏。
5.许多炎症性疾病的原因是过度产生il-1。特别是,il-1过量与糖尿病、心血管疾病、痛风、某些类型的关节炎(例如类风湿关节炎(ra))以及一些不太常见的自身免疫性疾病有关,例如家族性地中海热(fmf)、白塞病等。(ozen s,bilginer y.“a clinical guide to autoinflammatory diseases:familial mediterranean fever and next-of-kin”,nat.rev.rheumatol.2014mar;10(3):135-47).
6.rilonacept是一种il-1拮抗剂,包括il-1特异性融合蛋白,该蛋白由人il-1racp胞外结构域il-1结合部分、人il-1ri胞外结构域il-1结合部分和多聚组分组成。这种il-1特异性融合蛋白在美国专利第6,472,179号,美国专利第2003/0143697号,2003年7月31日发布,美国专利第7361,350号和美国专利第2005/0197293号,2005年9月8日发布中都有描述(所有这些都通过连接完全包含在本文中)。rilonacept商品名arcalyst,已被美国食品药品监督管理局(fda)注册,用于治疗冷卟啉(cryopyrin)相关周期性综合征(caps),包括12岁及以上成人和儿童的家族性寒冷性自身炎症综合征(fcas)和muckle-wells syndrome(mws)食管贲门粘膜撕裂综合征。目前,正在进行关于rilonacept的进一步临床研究,例如在痛风方面的研究。
技术实现要素:
7.本说明以简化的形式介绍了一些概念,这些概念将在详细说明中进一步阐述。
8.本说明无意确定本发明的基本属性或必要属性,也无意用于确定所申报的本发明的范围。
9.在某些方面,本发明提出能够结合人il-1β的异二聚体蛋白组成(genbank:aah08678.1)。蛋白质组成由第一多肽组成,该多肽包括含有人il1-r1氨基酸18到333的第一氨基酸序列(genbank:aam88423.1)和第二氨基酸序列,其中包含人类免疫球蛋白γ-1fc片段的第一个fc突变(genbank:j00228.1)。蛋白质组成包括第二多肽,其中包括另一个第一氨基酸序列,包含21到358的人il1-racp氨基酸(genbank:baa25421.1)和另一个第二氨基酸序列,其中包括人免疫球蛋白γ-1fc片段的第二突变。选择蛋白质组成中的第一和第二突变,以促进第一和第二突变之间的异二聚体组装,而不是任何同源聚体组装。蛋白质组成可能具有人il-1β/il-1f2结合活性,kd值不超过约10-11
摩尔/升。蛋白质组成的第一个多肽可能包含seq id no.1的氨基酸序列,第二多肽可能包含具有seq idno.2的氨基酸序列。
10.在某些方面,本发明是包含第一多肽的异二聚体蛋白组成,该多肽包括seq id no.8的氨基酸序列,以及第二多肽,包括具有seq id no.9的氨基酸序列。
11.在某些方面,本发明提供一种治疗组合物,其包含包括seq id no.8的氨基酸序列的第一多肽的异二聚体蛋白组合物,以及包括具有seq id no.9的氨基酸序列的第二多肽。治疗组合物同时可包括约6%(质量/体积)蔗糖,约3%(质量/体积)的平均分子量为3350da的聚乙二醇,约50毫摩尔/升氯化钠和约20毫摩尔/升l-组氨酸,ph值约4.5至约7.0。ph值约6.5。
12.在某些方面,本发明提供一种治疗组合物。该治疗组合物包括一种能结合人il-1β的异二聚体蛋白组成。蛋白质组成由第一多肽组成,该多肽包括含有人il1-r1氨基酸18至333的第一氨基酸序列和含有人免疫球蛋白γ-1片段fc的第一突变fc的第二氨基酸序列。
蛋白质组成包括第二多肽,该多肽包括含有人il1-racp氨基酸21至358的另一个第一氨基酸序列,以及包括人免疫球蛋白γ-1fc片段的第二fc突变的另一个第二氨基酸序列。选择蛋白质组合物中的第一和第二突变,以促进第一和第二突变之间的异二聚体组装,而不是任何同源聚体组装。
13.蛋白质组成可能具有人il-1β/il-1f2结合活性,kd值不超过约10-11
摩尔/升。该治疗组合物可通过人fc elisa的测定,在小鼠皮下注射了5毫克/千克的剂量之后,在体循环中至少具有约97小时的异源二聚体蛋白质半衰期。
14.该治疗组合物可通过人fc elisa的测定,在食蟹猕猴皮下注射10毫克/千克后,在体循环中具有至少约3天的异二聚体蛋白半衰期。该治疗组合物可包括由含有seq id no.1氨基酸序列的第一多肽,以及包含seq id no.2的氨基酸序列的第二多肽组成的异二聚体蛋白。治疗组合物同时可包括约6%(质量/体积)蔗糖,约3%(质量/体积)的平均分子量为3350da的聚乙二醇,约50毫摩尔/升氯化钠和约20毫摩尔/升l-组氨酸,ph值约6.5。
15.在某些方面,本发明提供一种治疗组合物,其包含包括seq id no.8氨基酸序列的第一多肽的异二聚体蛋白组合物,以及包括具有seq id no.9的氨基酸序列的第二多肽的异二聚体蛋白。治疗组合物同时可包括约6%(质量/体积)蔗糖,约3%(质量/体积)的平均分子量为3350da的聚乙二醇,约50毫摩尔/升氯化钠和约20毫摩尔/升l-组氨酸,ph值约4.5至约7.0。ph值约6.5。
16.在某些方面,本发明提供了一种含有包括seq id no.8多肽和seq id no9的另一种多肽的组合异二聚体蛋白的物质或组合物,用于治疗某些与il-1β调节有关的紊乱或疾病,包括,不局限于列出的,关节炎,痛风,类风湿关节炎,冷卟啉相关周期性综合征(caps),硬皮病,糖尿病,动脉粥样硬化,干眼症,眼部过敏反应,葡萄膜炎,复发性心包炎,家族性地中海热(fmf),st段抬高的心肌梗塞(stemi)、急性呼吸窘迫综合征/细胞因子风暴(arsd/crs)、schnitzler综合征、术后切口疼痛、慢性肾病(ckd)、pfapa(周期性发热、口疮性口炎、咽炎和腺炎)综合征、噬血细胞性淋巴组织细胞增生症(hlh)、巨噬细胞激活综合征(mas)、坏疽性脓皮病、川崎病、寻常痤疮、特应性皮炎、白塞病、乳腺癌、非小细胞肺癌或中风。
17.在某些方面,本发明所介绍的构思是一种治疗或预防与人类il-1β活性调节有关的疾病或状态的方法。该方法包括在需要治疗或预防与人类il-1β活性调节有关的疾病的患者中使用治疗有效量的药物组合物,该药物组合物包括由具有seq id no.8的氨基酸序列的第一多肽和具有seq id no.9的氨基酸序列的第二多肽组成的异二聚体蛋白。与il-1β调节有关的疾病,包括:不局限于列出的,关节炎,痛风,类风湿关节炎,冷卟啉相关周期性综合征(caps),硬皮病,糖尿病,动脉粥样硬化,干眼症,眼部过敏反应,葡萄膜炎,复发性心包炎,家族性地中海热(fmf),st段抬高的心肌梗塞(stemi)、急性呼吸窘迫综合征/细胞因子风暴(arsd/crs)、schnitzler综合征、术后切口疼痛、慢性肾病(ckd)、pfapa(周期性发热、口疮性口炎、咽炎和腺炎)综合征、噬血细胞性淋巴组织细胞增生症(hlh)、巨噬细胞激活综合征(mas)、坏疽性脓皮病、川崎病、寻常痤疮、特应性皮炎、白塞病、乳腺癌、非小细胞肺癌或中风。
18.附图简要说明
19.为帮助更好的了解本发明,提供了以下附图和说明:
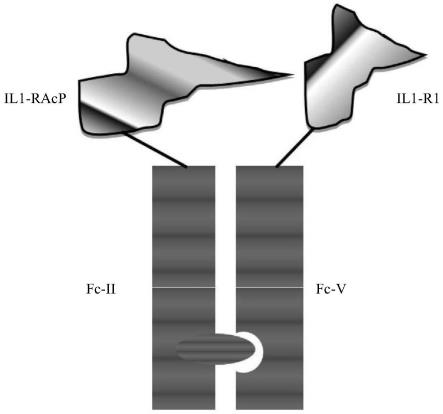
20.图1中说明了根据本发明思路的异二聚体蛋白组合,包括通过柔性连接器连接到
igg-fc结构域(fc-ii)的il1-r1胞外部分和通过另一柔性连接器连接到igg-fc结构域(fc-v)的il1-racp胞外部分;
21.图2中显示了不同il-1β/il-1f2浓度下有代表性的缓冲正常感测图系列,最低曲线显示il-1β/il-1f2浓度为0.919nmol/l,其后各曲线分别显示浓度为1.838、3.676、7.35、14.7和29.4nmol/l;
22.图3显示了具有代表性的il1结合数据;相对反应是通过减去“仅针对缓冲”背景值计算的;误差条显示了bioacoret200评价软件包计算的标准偏差值;
23.图4显示了具有代表性的浓度响应曲线,x轴显示摩尔单位il-1β/il-1f2浓度,y轴显示单位响应的响应(当量响应);
24.图5显示了一次皮下注射10mg/kg药物后,初级组3只食蟹猕猴血清中异二聚体illr-fcv-racp-fcii(以纳克/毫升为单位)的浓度(垂直线表示不同时间点的标准差值);
25.图6显示了对照组三只食蟹猕猴在一次皮下注射10mg/kg药物后血清中il1r-fcv-racp-fcii异二聚体的浓度(以纳克/毫升为单位),三条曲线上显示了代码为f1290、f1269和f1254的三只个体动物的测量情况;
26.图7显示了小鼠il-1b/il-1f2在小鼠胚胎成纤维细胞中诱导小鼠分泌il6的异二聚体il1r-fcv-racp-fcii滴定曲线;插页表格显示了采用4个参数算法进行曲线代入和曲线插值以确定ic50值的结果;
27.图8显示了人il-1b/il-1f2在mrc5细胞诱导的分泌人il6的异二聚体il1r-fcv-racp-fcii的滴定曲线,插页表格显示了采用4个参数算法进行曲线代入和曲线插值以确定ic50值的结果;和
28.图9显示了il-1b/il-1f2诱导恒河猴分泌人il6在mrc5细胞中的异二聚体il1r-fcv-racp-fcii滴定曲线,插页表格显示了采用4个参数算法进行曲线代入和曲线插值以确定ic50值的结果。
29.发明详述
30.公开的发明思想部分地基于能够与人il-1β结合并削弱其功能的异二聚体蛋白的结构工程。根据本发明的思想的异二聚体蛋白结构包括il1-r1的胞外部分(genbank:aam88423.1)和il-1racp(genbank:baa25421.1)或其功能碎片。它们中的每一个,il-r1部分和il-1racp部分,都与人igγ-1fc片段的一个单独突变结合在一起(genbank:j00228.1)。将异二聚体蛋白结构中的两个单独的fc突变组成,以促进在两个fc突变之间形成异二聚体,而不是任何同质结构。为了可以重组产生异二聚体蛋白结构,根据本发明的思路,构建了异二聚体蛋白表达系统中异二聚体蛋白结构过量产生的dna表达载体,制备了异二聚体蛋白结构稳定高表达的哺乳动物细胞。开发了一种蛋白质纯化程序,该程序可以根据本发明的思想获得具有生理意义且实际上是纯度的异二聚体蛋白质结构制剂。因此,纯化蛋白分子在使用人il-1βin vitro酶联免疫吸附试验(elisa)中表现出高度的特异性活性(genbank:aah08678.1)。该蛋白分子在动物皮下给药时具有可接受的药代动力学概况,而不会导致任何体重减轻或不良的临床事件。2014年3月6日发布的国际专利申请编号wo/2014/035361和2013年2月15日发布的国际专利申请编号pct/us/2013/026349部分地公开了本发明思想的设计、准备和主题构成的初步描述,本文引用了这两份文件。
31.说明书中使用的术语通常具有一定的含义,作为在本发明的上下文中,以及在使
用该术语的特定上下文中为本技术领域的标准。下面或说明书中的其他地方讨论某些术语,以便在描述本发明的成分和方法以及如何获得和使用这些成分方和方法时,为技术人员提供进一步的解释。该术语的任何使用的范围或含义将根据使用该术语的具体上下文来理解。“大约”和“大致”这两个术语一般指的是专业人员根据测量的性质或精确度对测量数量的允许误差。通常,允许的误差范围在给定值或值范围的20%(%)以内,10%以内,最好在5%以内。或者,特别是在生物系统中,术语“大约”和“大致”可以表示在数量级内的值,最好是在给定值的5倍范围内,最好是在给定值的2倍范围内。这里给出的定量值是近似值,除非另有说明,也就是说,除非给出精确值,否则可以使用术语“大约”或“大致”。
32.本发明的方法可以包括相互一致的比较步骤,包括野生型序列与一个或多个突变(测序变体)的比较。这种比较通常包括聚合序列的比较,例如使用在本领域中众所周知的序列比较程序和/或算法(例如,blast、fasta和megalign等)。该技术领域的技术人员清楚地知道,在这种比较中,如果突变包含残余嵌入物或缺损,在序列比较是将在不包含嵌入物或残余缺损的聚合物序列中出现“空白”(通常用连字符或“a”表示)。
33.本发明的方法可以包括统计计算,例如,确定ic50或ec50的值等。该领域的专业技术人员可以清楚地理解,它们可以使用市场上的一系列软件产品来执行,例如prism(美国加利福尼亚州拉霍亚的graphpad software inc.)或类似产品。
[0034]“同源”一词在其所有语法形式和拼写形式中,都是指具有“共同进化起源”的两种蛋白质之间的联系,包括来自同一物种生物超家族的蛋白质,以及来自不同物种生物的同源蛋白质。类似的蛋白质(以及编码它们的核酸)具有序列同源性,这反映在它们的序列在同一性百分比或具有特定残基或基序和保留位置的相似性上。然而,在这种情况下,通常使用“同源”一词,使用副词修饰,如“高”,可能指序列的相似性,可能表示,也可能不表示共同的进化起源。
[0035]
术语“序列相似性”,在其所有语法形式中,都是指核酸或氨基酸序列之间具有或不具有共同进化起源的同一性或一致性的程度。
[0036]
术语“蛋白质”和“多肽”交替使用。这里描述的多肽可以包括一个以上连续的氨基酸链,从而形成二聚体或其他低聚体结构。一般而言,根据本发明的构想用于哺乳动物的多肽在允许适当的转译后修饰的哺乳动物细胞中表达,例如在cho或hek293细胞系中,尽管预计其他表达的哺乳动物细胞系也可以使用。由此,根据本发明思路的多肽可以转译后被修饰而不会显著影响其生物功能。
[0037]
在某些方面,根据本发明构思,异二聚体蛋白结构的功能变体包括具有至少人il1-r1或il-1racp的生物活性部分或其功能片段的融合蛋白,以及一个或多个融合结构域。类似融合结构域的已知例子,包括,但不限于聚组氨酸、谷氨酰胺谷氨酰胺、谷胱甘肽s-转移酶(gst)、硫氧还蛋白、蛋白a、蛋白g、免疫球蛋白重链恒定区(如fc)、麦芽糖结合蛋白(mbp)或人血清白蛋白。可以选择合并域,使其具有所需的属性。例如,多肽il1-r1或il-1racp位点可以连接到稳定多肽il1-r1或il-1racpin vivo的结构域(“稳定”域),例如,使用合适的肽连接器。术语“稳定”是指增加多肽从体循环中的半衰期的任何影响,无论是由于衰变减少、清除减少还是其他药代动力学影响。已知,与免疫球蛋白fc片段的融合赋予某些蛋白质所需的药代动力学特性。同样,与人血清白蛋白的融合也可能具有预期的特性。可以选择其他类型的融合域,包括多聚(例如二聚、四聚)域和赋予额外生物功能的功能域,例
如促进目标区域的积累或in vivo作用。
[0038]
在某些方面,根据本发明思想,异二聚体蛋白结构包括连接到igg-fc结构域的il1-r1胞外部分或其功能片段,和连接到另一个igg-fc结构域的il-1racp胞外部分或其功能片段。选择igg-fc结构域和另一个igg-fc结构域,为促进蛋白质异二聚体结构的形成,而不是蛋白质的任何同源结构。细胞外il1-r1位点可以利用柔性连接器连接到igg-fc结构域,其中il-1racp或其功能片段可以利用相同氨基酸序列的柔性连接器或通过不同的柔性连接器连接到igg-fc构域。
[0039]
在图1举例说明实施方法中,il1-r1细胞外位点通过柔性连接器连接到igg-fc(fc-ii)结构域,该结构域可能包括符合seq id no.1的氨基酸序列,其中il-1racp通过柔性连接器连接到另一个igg-fc构域(fc-v),该结构域可能包括具有seq id no.2的氨基酸序列。
[0040]
多肽hil1-r1-higg1-fc(seq id no.1)
[0041][0042]
多肽hil-1racp-higg1-fc(seq id no.2)
[0043][0044][0045]
在某些方面,本发明的思想包括带开放式多肽编码读取框的重组dna分子,包括使用柔性连接器连接到igg-fc结构域(fc-ii)的前333个il-r1氨基酸,以及另一个带有开放式多肽编码读取框的重组dna分子,该多肽包括使用柔性连接器连接到另一个igg-fc结构域(fc-v)的前358个人il-1racp氨基酸。
[0046]
在实施方法中,包含人类il1-r1的前333个氨基酸的多肽通过包括seq id no.3的氨基酸序列的柔性连接器连接到igg-fc结构域(fc-ii)。据此,dna分子可以包括具有seq id no.4的核苷酸序列。另一种多肽包括人il-1racp的前358个氨基酸,通过柔性连接器连接到另一个igg-fc结构域(fc-v),该连接器可能包含具有seq id no.5的氨基酸序列。据此,dna分子可以包括具有seq id no.6的核苷酸序列。
[0047]
多肽hil1-r1-higg1-fc(seq id no.3)
[0048][0049]
dna hil1-r1-higg1-fc(seq id no.4)
[0050][0051][0052]
多肽hil-1racp-higg1-fc(seq id no.5)
[0053][0054]
dna hil-1racp-higg1-fc(seq id no.6)
[0055][0056]
在某些方面,本发明包括用于多肽高表达的重组哺乳动物表达质粒,该多肽包括使用柔性连接器连接到igg-fc结构域(fc-ii)的前333个il-r1氨基酸,以及另一个带有开放式多肽编码读取框的重组dna分子,该多肽包括使用柔性连接器连接到另一个igg-fc结构域(fc-v)的前358个人il-1racp氨基酸。该质粒包括两个巨细胞病毒(cmv)催化剂,用于提供编码指定多肽和指定第二多肽的两个基因的转译,在各自之后有一个转译结束序列和一个聚腺苷化序列。质粒还含有一个复制起始点和一个氨苄西林抗药性基因,以支持质粒在细菌中的繁殖和选择。质粒中还含有谷氨酰胺合成酶基因,这是一种被广泛用于建立稳定的chok1和nso细胞系的标记。
[0057]
在实施方法中,根据本发明思想,哺乳动物表达质粒包括具有seq id no.7的核苷酸序列。
[0058]
表达质粒hil1-r1-higg1-fc-ii/il-1racp-higg1-fc-v(seq id no.7)
[0059]
[0060]
[0061]
[0062]
[0063][0064]
在某些方面,本发明的思想包括用于产生异二聚体蛋白结构的哺乳动物表达系统,该结构包括含有通过柔性连接器连接到igg-fc结构域(fc-ii)的人il-1r1氨基酸残基18至333的多肽,以及含有通过柔性连接器连接到另一个igg-fc结构域(fc-v)的人il-1racp氨基酸残基21至358的另一多肽。
[0065]
在实施例中,根据本发明思想,哺乳动物表达系统包括携带包含具有seq id no.7的核苷酸序列的质粒的中国仓鼠卵巢细胞(cho-k1)。
[0066]
在某些方面,根据本发明思想,哺乳动物表达系统产生含有seq id no.8多肽和含有seq id no.9的另一种多肽的异二聚体蛋白结构。
[0067]
多肽hil1-r1-higg1-fc(seq id no.8)
[0068][0069]
多肽hil-1racp-higg1-fc(seq id no.9)
[0070][0071]
在某些方面,本发明提供了一种含有包括seq id no.8多肽和另一种seq id no.9多肽的组合异二聚体蛋白的物质或组合物,用于治疗某些与il-1β调节有关的紊乱或疾病,包括,不局限于列出的,关节炎,痛风,类风湿关节炎,冷卟啉相关周期性综合征(caps),硬皮病,糖尿病,动脉粥样硬化,干眼症,眼部过敏反应,葡萄膜炎,复发性心包炎,家族性地中海热(fmf),st段抬高的心肌梗塞(stemi)、急性呼吸窘迫综合征/细胞因子风暴(arsd/crs)、schnitzler综合征、术后切口疼痛、慢性肾病(ckd)、pfapa(周期性发热、口疮性口炎、咽炎和腺炎)综合征、噬血细胞性淋巴组织细胞增生症(hlh)、巨噬细胞激活综合征(mas)、坏疽性脓皮病、川崎病、寻常痤疮、特应性皮炎、白塞病、乳腺癌、非小细胞肺癌或中风。
[0072]
在某些方面,本发明所介绍的构思是一种治疗或预防与人类il-1β活性调节有关的疾病或状态的方法。该方法包括在需要治疗或预防与人类il-1β活性调节有关的疾病的患者中使用治疗有效量的药物组合物,该药物组合物包括由具有seq id no.8的氨基酸序列的第一多肽和具有seq id no.9的另一种多肽的异二聚体蛋白结构。与il-1β调节有关的疾病,包括:不局限于列出的,关节炎,痛风,类风湿关节炎,冷卟啉相关周期性综合征(caps),硬皮病,糖尿病,动脉粥样硬化,干眼症,眼部过敏反应,葡萄膜炎,复发性心包炎,家族性地中海热(fmf),st段抬高的心肌梗塞(stemi)、急性呼吸窘迫综合征/细胞因子风暴(arsd/crs)、schnitzler综合征、术后切口疼痛、慢性肾病(ckd)、pfapa(周期性发热、口疮性口炎、咽炎和腺炎)综合征、噬血细胞性淋巴组织细胞增生症(hlh)、巨噬细胞激活综合征(mas)、坏疽性脓皮病、川崎病、寻常痤疮、特应性皮炎、白塞病、乳腺癌、非小细胞肺癌或中风。
实施例
[0073]
以下示例说明了本发明思想的上述观点和其他观点。这些示例并不全面,其目的是向本领域的技术人员提供关于如何获得和评估这里所述化合物、制剂、物品、物品和/或方法的实施例示例。示例仅用于说明这里所公开的发明,并不限制发明者视为发明的范围。已尽一切努力确保定量值(如数量、温度等)的准确性,但应考虑到某些误差和偏差的可能性。
[0074]
实施例1:本发明多肽的制备。
[0075]
多肽hil1-r1-higg1-fc含seq id no.1,和多肽hil-1racp-higg1-fc含seq id no.2使用本领域已知的分子生物学、细胞培养和蛋白质生物化学技术在cho-k1中共表达,并在pct出版物wo/2014/035361和pct申请,系列编号pct/us/2013/026349中进行了描述。重点是,表达多肽的cho-k1细胞使用详细描述的方案进行收集和裂解。细胞裂解液纯化后,首先将含有表达多肽的上清液引入蛋白a亲和层析柱中,经ph修正后的蛋白a亲和层析柱洗脱液用q-蔗糖树脂经阴离子交换层析(aiex)进一步纯化。采用排阻hplc(sec-hplc)、sds-page等可接受的分析技术对aiex的流动组成进行了分析。
[0076]
为后续研究,获得了含多肽hil1-r1-higg1-fc和hil-1racp-higg1-fc的治疗组合物,多肽含量为40mg/ml,6%(质量/体积)蔗糖,3%(质量/体积)聚乙二醇(peg)3350、50mmol/l氯化钠和20mmol/l l-组氨酸,ph值约4.5至约7.0,建议约6.5。
[0077]
成品中所含多肽序列已按以下示例所述进行了分析。成品中的多肽主要含有具有seq id no.8的hil1-r1-higg1-fc多肽和具有seq id no.9的hil-1racp-higg1-fc多肽。
[0078]
实施例2:本发明的多肽作图和多肽描述。
[0079]
实际上按照上面的例子所述制备的三个产物样品已经按照下面所述进行了分析。首先,采用液相色谱-质谱法(lc-ms)测定了各样品所含两种完整多肽的分子量。通过液相色谱-串联质谱(lc-ms/ms)完成肽图谱。最后,完成末端肽测序。
[0080]
为通过lc/ms确定完整肽的质量,蛋白质样品根据本领域众所周知的协议进行了还原和去糖基化。
[0081]
肽作图实际上是按照以下方式进行的:
[0082]
样品通过赖氨酸c、胰蛋白酶和糜蛋白酶消化。每个样品用lc-ms/ms进行分析。
[0083]
1)根据一项已知的协议(vs280,promega公司,麦迪逊,威斯康星州)对40微克样品通过胰蛋白酶进行变性、还原和分解。
[0084]
2)根据一项已知的协议(va1170,promega公司,麦迪逊,威斯康星州),对40微克样品通过赖氨酸c进行变性、还原和分解。
[0085]
3)根据已知的程序(va106a,promega公司,麦迪逊,威斯康星州)对40微克样品通过糜蛋白酶进行变性、还原和分解。
[0086]
4)使用agilent 1900高效液相色谱系统(加利福尼亚州,圣克拉拉,agilent technologies)按照以下方式,进行了高效液相色谱分析:
[0087]
分析柱——waters acquity uplc beh c18,1.7μm,2.1
×
150mm
[0088]
柱温:45℃
[0089]
样品体积:10微升
[0090]
溶剂a:h2o与0.1%甲酸
[0091]
溶剂b:乙腈(acn)加0.1%甲酸
[0092]
流量:300微升/分钟(min)
[0093]
试验条件:98%a,2%b;0(初始状态)
[0094]
70%的a,30%的b;0-35分钟(线性梯度)
[0095]
5%a,95%b;35-46分钟(线性梯度)
[0096]
95%a,2%b;46-50分钟(线性梯度)
[0097]
98%a,2%b;50-60分钟(平衡)
[0098]
数据系统:pc控制的数据采集系统
[0099]
5)串联质谱分析-使用qtof 6550质谱仪(加利福尼亚州圣克拉拉,agilent technologies,)获得光谱。在正离子记录模式下进行光谱仪的工作。在m/z 350-2000范围内获得质谱,分辨率为20000(m/z1521),依赖数据记录时,选择了10种最常见的源离子进行cid破碎串联质谱分析,绝缘宽度为4.0da,碰撞能量公式为:(斜率)*(m/z)/100+缩进。采用动态排除法降低ms/ms重复获得,提高多肽鉴定。
[0100]
6)数据分析-提取原始数据,使用spectrum millz 5.01和hunter(agilent technologies)进行搜索。对获得的ms和ms/ms光谱进行了比较蛋白质数据库和诱捕受体序列数据库的分析。酶参数受到限制,胰蛋白酶的最大不规则裂解为2,赖氨酸c为2,糜蛋白酶为5。对n末端肽进行了额外的非酶搜索。所有其他搜索参数都是spectrum mill系统的默认设置(半胱氨酸尿素甲基化,初始离子为+/-20ppm,碎片离子为+/-50ppm,估计峰值强度的最低相应百分比(spi%)为50%)。形成了连接的正反向数据库,用于in situ计算假阳性率(fdr)。动态地分配每个数据集的阈值,以保持在肽水平上的假阳性率小于0.1%。同时,使用手动检查每个分析样本中的每个单独确定的蛋白质。
[0101]
在完整的质量分析中,确定了两个分辨率较好的主峰(各频率大于98%),第一个对应分子量=61,505.9
±
0.1da,第二个对应分子量=64,753.3
±
0.1da。第一个峰值对应于seq id no.8(理论分子量61,495da),第二个对应于seq id no.9(理论分子量64,743da)。分子量的差异(~11da)最有可能是由于天冬氨酸残基在脱糖基化后的脱氨所致。
[0102]
多肽作图和c末端序列分析进一步验证了序列数据,具有较高的置信度。
[0103]
实施例3:利用表面等离子共振(spr)定量分析来评估根据本发明思路的多肽与rankl的结合的亲和性。
[0104]
用专门设计的表面等离子共振(spr)定量分析方法测定了所得il1r-fcv-racp-fcii异二聚体多肽与il-1β/il-1f2(登记号ncbi np_000567)的结合亲和性。定量分析采用捕获方法,将人蛋白igg与触感芯片表面交叉交联,捕获il1r-fcv-racp-fcii异二聚体对其igg片段(fc)。用一系列不同浓度的il-1β/il-1f2计算离解常数(kd)。
[0105]
试剂和设备:
[0106]
设备:
[0107]
biacoret200,设备编号12108,ge healthcare,配备biacore t200管理和评估软件包。
[0108]
试剂:
[0109]
异二聚体il1r-fcv-racp-fcii母液,20mg/ml多肽,6%(质量/体积)蔗糖,3%
[0110]
(质量/体积)peg3350,50mmol/l氯化钠和20mmol/l l-组氨酸,ph6.5。来源于
e.coli的人、重组il-1β/il-1f2,ala117-ser269,注册号np_000567,r&d systems,目录号201-lb,批号ad1412111
[0111]
cm5触控芯片,s系列,ge healthcare,br-1005-30,批号10189577
[0112]
人源抗体捕捉试剂盒,ge healthcare,目录编号br-1008-39,批次编号10202616;
[0113]
hbs-ep+10倍移动缓冲液,ge healthcare,目录编号br-1006-69;
[0114]
程序:
[0115]
igg与人蛋白的接合:
[0116]
igg与人蛋白(fc)的接合过程根据制造商的协议,使用以下条件完成。
[0117]
1.cm5触控芯片放置在机器中,充满biacore移动缓冲液,1x hbs-ep,以10μl/min的速度持续6分钟,重复两次。所有步骤都在25℃的温度下完成。实验用1、2通道;3、4通道作备用;
[0118]
2.人蛋白igg,0.5mg/ml放入0.15mol/l nacl中,在固定化缓冲液(10mmol/l醋酸钠,ph5.0)中稀释20倍,至最终浓度25μg/ml;
[0119]
3.固定化试剂按如下方式制备:edc(1-乙基-3-(3-二甲基氨基丙基)碳化二亚胺)-0.4mol/l milli-q水;nhs(n-羟基琥珀酰亚胺)-0.1mol/l milli-q水;盐酸乙醇胺1mol/l,milli-q水中ph8.5;
[0120]
4.对表面活化和固定化采用了标准方案;
[0121]
5.激活:将edc和nhs按1:1的比例混合,以10μl/min的速度注入芯片7分钟;
[0122]
6.固定化:将人蛋白iggk以10μl/min的速度注入芯片5分钟;
[0123]
7.失活:用1mol/l盐酸乙醇胺以10μl/min的速率注入7分钟,阻断无反应活性基团;
[0124]
8.抗体接合后,用1x hbs-ep以10μl/min的速度冲洗芯片2次,持续6分钟,然后进行两次“干”作业循环,不添加任何蛋白成分。工作循环包括配体基负载阶段(异二聚体il1r-fcv-racp-fcii)1分钟,洗涤阶段3分钟,样品负载阶段(il-1)1分钟,洗涤阶段16.7分钟,芯片再生阶段1分钟,3mol/l mgcl2。所有步骤均以10微升/分钟的速度进行,样品加载阶段除外,该阶段以30微升/分钟的速度进行。
[0125]
实验数据:
[0126]
评估异二聚体il1r-fcv-racp-fcii与il-1β/il-1f2相互作用的亲和性。
[0127]
本实验的目的是测定异二聚体il1r-fcv-racp-fcii和il-1β/il-1f2的组合恒量。将人蛋白igg共价固定在cm5触控芯片上,然后进行异二聚体il1r-fcv-racp-fcii负载,再应用不同浓度的人il-1β/il-1f2。获得一系列感测图,用于计算kd值。
[0128]
实验条件:
[0129]
1.初步系列实验制备了几种不同浓度的异二聚体il1r-fcv-racp-fcii(1、10和100μg/ml),并对其进行了固定化igg与人蛋白的结合分析。结果发现,在1微克/毫升的浓度下,il1r-fcv-racp-fcii异二聚体在~100回应单位范围内产生了足够的信号,所有定量分析均采用该浓度;
[0130]
2.在一些试点运行中优化了结合/分解循环参数,并在表1中列出;
[0131]
3.人il-1β/il-1f2的浓度如表2所示,其中对3.676nmol/l的浓度进行了两次独立的运行,作为仪器的内部重复性检查;
[0132]
4.获得了一系列对应于不同浓度il-1β/il-1f2的感测图。通过扣除“仅用于缓冲”的感测图对数据进行了梳理。缓冲正规感测图如图2所示,相应的数据如表2所示。
[0133]
表1 biacore循环参数。
[0134]
过程时间,s流速,μl/min异二聚体负载12010il1负载12030离解100030再生2030
[0135]
实验数据分析
[0136]
对实验条件进行了优化,使曲线代入算法能够准确使用。如感测图所示(图2),所有测试的il-1β/il-1f2浓度均呈现剂量相关的关联曲线。由于异二聚体il1r-fcv-racp-fcii与il-1β/il-1f2相互作用的亲和性非常高,因此没有观察到在1000s范围内的解离。因此,不可能使用动力学模型准确计算kd值。
[0137]
使用langmuir 1:1结合模型分析平衡态数据作为计算kd的替代方法。根据该方法,根据一系列不同浓度的阳极电解液在平衡状态下的结合水平图(等量回应)计算kd。数据见表2。
[0138]
实验数据见表3,如图3所示。应用了4个参数曲线代换算法,得到的浓度响应关系曲线,如图4所示。用描述给定曲线的方程计算kd,形成评估biacore t200的软件。
[0139]
表2根据平衡态模型计算的异二聚体il1r-fcv-racp-fcii和人il-1β/il-1f2的kd值。
[0140][0141]
表3il-1β/il-1f2的浓度和结合(相对回应)。采用biacore t200评估软件计算标准差值,%,然后通过乘以rmax*标准误差值%转换为标准差值。标准误差值在图3中显示为误差条。
[0142][0143]
实施例4:小鼠皮下注射il1r-fcv-racp-fcii异二聚体后的药代动力学(pk)。
[0144]
异二聚体多肽il1r-fcv-racp-fcii(seq id no.1和seq id no.2)实际上如上文示例中所述,已共表达和纯化。在动物体内给药时,多肽在以下缓冲液中溶解:1%质量/体积蔗糖,100mmol/l氯化钠,20mmol/l盐酸l-精氨酸,25mmol/l碳酸氢钠,ph6.3。给药用多肽母体浓度为0.5mg/ml。
[0145]
14只dba/1雄性小鼠按体重随机分为7组,每组2只,研究第0天。在6组小鼠第0天皮下(背部)注射单剂量il1r-fcv-racp-fcii异二聚体(5mg/kg至10ml/kg)。其余组小鼠不给药,在研究第0天通过心脏穿刺制备血浆获得血液样本。对施药组小鼠进行处死时,在研究期间在给定时间点从眶窦或通过心脏穿刺获得血液样本制备血浆。所有动物在给药当天(第0天)记录体重,然后每组每周3次,包括处死日当天。在给药后0h和36h内取样的各组未测出体重变化。用药后96h至21d期间的各组0天至处死日的平均体重下降幅度最小。没有一只老鼠的体重下降超过道德标准。经过生活期的研究,血浆样品用酶联免疫吸附试验(elisa)对hu-fc蛋白进行分析。以elisa法定量测定小鼠血浆样品中hu-fc作为il1r-fcv-racp-fcii异二聚体循环水平的输出数据。对研究中所有小鼠的样本进行了定量分析。
[0146]
在给药后所有时间点的动物血浆中测定多肽(定义为人fc蛋白)。之后,利用prism5.0c(graphpad software inc,美国加州拉霍亚graphpad软件公司)中的单相衰变模型方程,测定hu-fc elisa测定多肽的药代动力学。测定hu-fc峰值循环水平(cmax)为1.284ug/ml,达到峰值循环水平(tmax)的时间为给药后24小时。半衰期(t1/2)为97小时31分钟,速率常数(k)为0.0071h-1。未用药动物血浆中hu-fc低于测定水平。研究结果见表4。
[0147]
表4注入后每个时间点的人蛋白fc
±
平均标准错误的平均浓度(微克/毫升)
[0148][0149]
*0.040-该数量分析测定临界值
[0150]
利用prism软件根据三倍样品的平均光密度测定人fc蛋白浓度。
[0151]
^经眶窦采集血样
[0152]
#通过心脏穿刺采集血样
[0153]
实施例5:灵长目动物皮下注射il1r-fcv-racp-fcii异二聚体后的药代动力学(pk)。
[0154]
为了本研究的目的,最初使用了三只以前没有接受过药物的雄性食蟹猕猴。动物年龄约2-4岁,体重约2公斤。给动物注射一剂过表达和纯化的异二聚体il1r-fcv-racp-fcii(seq id no.1和seq id no.2)含与上文示例1中的成分基本相同的组合物,皮下注射,剂量水平10毫克/千克,研究日第1天。三只动物的初级组生物测试结果如图5所示。为了进一步实现研究目标,在第1天给另外3只雄性食蟹猕猴皮下注射一次剂量的il1r-fcv-racp-fcii异二聚体,剂量水平为10毫克/千克,在第21天之前的指定时间点采集血样。3只动物对照组的生物测试结果如图5所示。所有动物每天观察一次,以检测研究期间对该药物的任何反应。在给药前,测量并记录体重。用于药物动力学分析的血液样品在给定的时间点获取。用于生物分析的血清样品保存在-80℃环境中。血浆多肽浓度的测定采用elisa法。
[0155]
在研究过程中没有观察到临床特征。体重情况令人满意。对药代动力学数据的初步分析结果显示,单次皮下注射10mg/kg后的cmax和tmax为约24~48h。另外3只动物的药代动力学分析结果表明,il1r-fcv-racp-fcii异二聚体在3只动物中有2只至少在第10天的血浆中数量测定,1只在第14天前数量测定。采用winnonlin 6.3软件包中的非食谱模型测定了三只猴子对照观察组的药代动力学参数,见表5。
[0156]
表5食蟹猕猴单次皮下注射试验中药代动力学参数总结(括号内为cv%平均值)
[0157][0158]1平均调和值
[0159]2中值[最小-最大]
[0160]
*计算值,因为曲线下方面积
额外
》20%
[0161]
所有动物均观察到广泛水平的异二聚体il1r-fcv-racp-fcii。观察到的个体间变异相对较高,cv%为约60%。后者是由于在动物f1290(图6)中检测到的最低药物水平,其异二聚体il1r-fcv-racp-fcii水平至少比其余两只动物低5倍。在第1天至第2天之间达到最大浓度(cmax)。t1/2的计算值为约4天。
[0162]
实施例6:异二聚体il1r-fcv-racp-fcii的中间比活性。
[0163]
il1r-fcv-racp-fcii是由人il-1r和il-1racp的可溶性部分组成的异二聚体,每个部分都与igg1独特的fc片段相连。将人il-1r的333个氨基酸位点序列与几个动物物种的相应位点进行比较,显示与啮齿动物(小鼠、大鼠)的il-1r位点序列只有中等程度的一致性(~64%)。然而,人il-1r与其他灵长类动物的序列之间存在明显更高的序列一致性(例如,马莫西猴为91%)。下文进一步介绍了构成异二聚体分子il1r-fcv-racp-fcii部分的358个氨基酸人il-1racp位点与某些动物物种中相应位点的蛋白质二元序列匹配。该异二聚体il1r-fcv-racp-fcii位点的种间序列同一性略高。在比较人il-1racp的358个氨基酸位点与macaca mulatta(92%)其同源基因序列时,不同于与mus musculus(85%)的同源基因序列比较,观察到更高的序列一致性。
[0164]
为了比较性评估il1r-fcv-racp-fcii(seq id no.1和seq id no.2)新型潜在异二聚体试剂功能(抑制)进行了以下研究。用人、恒河猴和小鼠的il-1βil-1f2同源基因序列进行定量分析。在小鼠胚胎成纤维细胞中比较人与小鼠il-1β/il-1f2。在人肺成纤维细胞mrc5中比较人与恒河猴il-1βil-1f2。使用之前描述的小鼠抗人il-1βil-1f2单克隆抗体和山羊抗小鼠il-1βil-1f2多克隆抗体作为功能比较药物。使用通过mrc5或mef细胞产生il-6的诱导il-1βil-1f2定量,来测定对所有三个同源基因序列的抑制特性(ic50值)。
[0165]
材料和反应物
[0166]
细胞
[0167]
mrc5细胞,人肺成纤维细胞,atcc目录编号ccl-171,批次编号59474707。
[0168]
实验使用小鼠胚胎成纤维细胞。
[0169]
介质
[0170]
dmem,dulbecco改良针培养基,高葡萄糖(4.5g/l),invitrogen,目录编号11995-065,批号1237317,添加l-谷氨酰胺和1x青霉素/链霉素,以及10%的标准胎牛血清,gemini bioproducts,目录编号100-106,批号a78d00e。
[0171]
试剂
[0172]
异二聚体il1r-fcv-racp-fcii,制剂浓度1.5mg/ml。
[0173]
来源于e.coli的人、重组il-1βil-1f2,ala117-ser269,注册号np_000567,r&dsystems,目录号201-lb,批号ad1412111
[0174]
来源于e.coli的恒河猴、重组il-1βil-1f2,ala117-ser269,注册号p48090,r&dsystems,目录号1318-rl,批号gug0110111
[0175]
来源于e.coli的鼠、重组il-1β/il-1f2,vla118-ser269,注册号np_032387,r&dsystems,目录号401-ml-005,批号bn0713032
[0176]
鼠抗人il-1βil-1f2单克隆抗体,克隆号no8516,r&d systems,目录编号mab201,批号awe1011081
[0177]
山羊抗小鼠il-1β/il-1f2多克隆抗体,克隆号no8516,r&d systems,目录号af-401-na,批号np2812121
[0178]
免疫测定il-6quantakine,r&d systems,目录编号d6050,批次编号308916
[0179]
小鼠il-6quantakine免疫测定,r&d systems,目录编号m6000b,批号309487
[0180]
程序
[0181]
细胞维持
[0182]
上清液在300x g条件下离心10分钟,收集纯化上清液,根据中间试实验的需要直接(小鼠胚胎成纤维细胞)或1/5稀释(mrc5)用于elisa。
[0183]
elisa
[0184]
本定量分析采用了酶免疫定量分析夹心法。将il-6特异性单克隆抗体预涂于微量滴定板上。用移液管将标准品和样品放入孔中,用固定化抗体结合已有的il-6。将任何不结合的物质冲洗后,将il-6特有的与酶结合的多克隆抗体加入孔中。冲洗去除任何未结合的抗体和酶试剂后,将培养基溶液加入孔中,在孔中形成染色,染色强度与初始阶段结合的il-6成正比。停止染色,并测量其强度。
[0185]
实验数据
[0186]
三个系列实验的目的是确定一个合适的细胞系,用于测定人和小鼠同源基因序列il-1β/il-1f2给药时的il6分泌量。进行了若干初步的中间实验,以确定小鼠细胞对il-1β/il-1f2处理的il6稳定分泌反应。根据初步实验数据,选择小鼠胚胎成纤维细胞作为模型细胞系,进行il1r-fcv-racp-fcii异二聚体滴定实验il1r-fcv-racp-fcii异二聚体滴定曲线在小鼠胚胎成纤维细胞中对小鼠il-1β/il-1f2诱导小鼠il6分泌的结果如图7所示。il6产生数据根据图9所示的校准曲线计算。插页上的表格显示了采用4个参数算法进行曲线置换和曲线插值确定ic50值的结果;小鼠il-1b/il-1f2的il1r-fcv-racp-fcii异二聚体的ic50计算值为》210ng/ml。
[0187]
实验数据显示,异二聚体il1r-fcv-racp-fcii是人il-1β/il-1f2信号通路的有效抑制剂,但不是小鼠il-1b/il-1f2的有效抑制剂:il1r-fcv-racp-fcii异二聚体对人il-1b/il-1f2的ic50值为0.19ng/ml,对小鼠il-1b/il-1f2的ic50值》200ng/ml(分别为0.95pmol/l和》1000pmol/l,假设il1r-fcv-racp-fcii异二聚体的分子量为200kda)。通过人il-1b/il-1f2在mrc5细胞中诱导的分泌人il6的异二聚体il1r-fcv-racp-fcii的滴定曲线,如图8所示。异二聚体il1r-fcv-racp-fcii对人il-1b/il-1f2的ic50计算值(曲线插值表中的x列)为0.22ng/ml。通过恒河猴il-1b/il-1f2在mrc5细胞中诱导的分泌人il6的异二聚体il1r-fcv-racp-fcii的滴定曲线,如图9所示。异二聚体il1r-fcv-racp-fcii对人il-1β/il-1f2的ic50计算值为0.38ng/ml。最终浓度200纳克/毫升的异二聚体il1r-fcv-racp-fcii制剂的il-6分泌物为95%。异二聚体il1r-fcv-racp-fcii是人和恒河猴il-1b/il-1f2信号通路的有效抑制剂:异二聚体il1r-fcv-racp-fcii对人il-1b/il-1f2的ic50值为0.19ng/ml,对il-1b/il-1f2的ic50值为0.38ng/ml(分别为1.1pmol/l和1.9pmol/l)。最终浓度200纳克/毫升的异二聚体il1r-fcv-racp-fcii制剂的il-6分泌物为92%。
[0188]
因此,在处理小鼠或人细胞il-1b/il-1f2过程中刺激il-6的产生,作为il1r-fcv-racp-fcii异二聚体新候选制剂对人、小鼠和恒河猴il-1b/il-1f2同源基因序列抑制特性的功能分析。
[0189]
对三个同源基因序列均确定了合适的细胞系,并对实验条件进行了优化,包括细胞密度、处理持续时间和il6测定的线性范围。数据见表6。
[0190]
表6在人、小鼠和恒河猴的il-1b/il-1f2同源基因序列方面的il1r-fcv-racp-fcii异二聚体的ic50值。
[0191][0192]
此处提及的所有出版物和专利都以链接的方式完整地呈现在本文中,也通过链接囊括了单独提及的每个出版物和专利。
[0193]
虽然已经考虑了本发明主题的具体实施例,但上述说明书仅限作为例证,并非详尽无遗。在审核本说明书和下面的权利要求时,对于本领域的专业技术人员来说,各种方案
都清楚易懂。本发明的全部范围必须参照权利要求,以及类似物和说明书的完整范围,与指定的方案一起来确定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1