一种SGLT2抑制剂中间体的合成方法与流程
一种sglt2抑制剂中间体的合成方法
技术领域
1.本发明涉及药物合成技术领域,具体涉及一种sglt2抑制剂中间体的合成方法。
背景技术:
2.钠依赖性葡萄糖转运子2(sodium
‑
dependent glucose transporter 2,sglt2)是近年来发现的具有全新作用机制的糖尿病治疗靶点。sglt2主要位于肾近端小管s1段的上皮细胞上,能够将血液流经肾小球时被滤出的葡萄糖重新吸收回血液中。sglt2抑制剂能够减少sglt2对原尿中葡萄糖的重吸收,增加尿糖排出,从而达到降低血糖的目的。sglt2抑制剂具有非胰岛素依赖性以及无低血糖风险等特点,是目前最有前景的糖尿病治疗药物之一。
3.相关技术中sglt2抑制剂的合成路线主要有以下三种。第一种合成路线以达格列净为起始原料采用六步法合成泰格列净,得到的泰格列净原料药的成本高,不具备市场竞争力。
[0004][0005]
第二种合成路线以n
‑
1为起始原料经过7步反应合成
ⅴ
,总收率18%,成本较高。过程需要使用危险的化合物钠氢,最后一步氧化使用dmso作为氧化剂,其副产物二甲硫醚具有非常不愉快的气味,过程还需要使用比较危险的钯碳氢化的合成方法及钯碳这类昂贵的试剂,导致实用性较差。
[0006][0007]
第三种合成路线为以化合物m
‑
1为起始原料,第一步为将化合物m
‑
1脱碘得到化合物m
‑
2,第二步为将化合物m
‑
2酸性水解脱去甲基,得到化合物m
‑
3,第三步为将化合物m
‑
3氧化,得到化合物m
‑
4。
[0008][0009]
由于起始原料m
‑
1无法大量采购得到,选择这一合成路线,则需要自己进行m
‑
1的合成,而m
‑
1的合成需要上述第二种合成路线中部分试剂及条件。整个合成的路线总共需要7步反应,路线较长,总收率较低。
[0010]
因此,需要一种全新的简便、廉价的通用合成路线,来实现sglt2抑制剂中间体的
合成。
技术实现要素:
[0011]
本发明要解决的技术问题是:提供一种sglt2抑制剂中间体的合成方法;该方法成本低且收率好。
[0012]
为解决上述技术问题,本发明提供的技术方案为,一种sglt2抑制剂中间体的合成方法,包括以下步骤:
[0013][0014]
s1、氧化:将化合物ⅰ添加至氧化体系后,液液分离,收集有机相a得到化合物ⅱ;
[0015]
s2、脱烷基:将化合物ⅱ添加至脱烷基体系后,得反应液,液液分离,得到化合物ⅲ;
[0016]
s3、碘代:将化合物ⅲ添加至碘代体系后,液液分离,收集有机相b得到化合物ⅳ;
[0017]
s4、还原:将化合物ⅳ溶解后,添加还原体系,液液分离,收集有机相c得到目标产物
ⅴ
,即为sglt2抑制剂中间体;
[0018]
其中,所述tempo为2,2,6,6
‑
四甲基哌啶氧化物;bn表示苄基;ac表示乙酰基。
[0019]
根据本发明的一些实施方式,所述步骤s1中溶剂选用二氯甲烷、碳酸氢盐和水的混合溶液。
[0020]
根据本发明的一些实施方式,所述碳酸氢盐为碳酸氢钠和碳酸氢钾中的至少一种。
[0021]
根据本发明的一些实施方式,所述碳酸氢盐中碳酸氢根与化合物ⅰ的物质的量之比2.0~5.0:1;优选地,所述碳酸盐中碳酸氢根与化合物ⅰ的物质的量之比2.0~3.0:1。
[0022]
根据本发明的一些实施方式,所述二氯甲烷与化合物ⅰ的体积比为2~10:1;优选地,所述二氯甲烷与化合物ⅰ的体积比为2~3:1。
[0023]
根据本发明的一些实施方式,所述水与化合物ⅰ的体积比为3~10:1;优选地,所述水与化合物ⅰ的体积比为9~10:1。
[0024]
根据本发明的一些实施方式,所述氧化体系为tempo氧化体系。
[0025]
根据本发明的一些实施方式,所述tempo氧化体系由tempo、溴化物和次氯酸盐组成。
[0026]
根据本发明的一些实施方式,所述tempo与化合物ⅰ的物质的量之比为0.05~0.5:1;优选地,所述tempo与化合物ⅰ的物质的量之比为0.10~0.15:1。
[0027]
根据本发明的一些实施方式,所述溴化物为溴化钠、溴化锂和溴化钾中的至少一种。
[0028]
根据本发明的一些实施方式,所述溴化物中溴离子与化合物ⅰ的物质的量之比为0.05~0.5:1;优选地,所述溴化物中溴离子与化合物ⅰ的物质的量之比为0.10~0.20:1。
[0029]
根据本发明的一些实施方式,所述次氯酸盐中次氯酸根与化合物ⅰ的物质的量之比为2~3:1;优选地,所述次氯酸盐中次氯酸根与化合物ⅰ的物质的量之比2.4~2.6:1。
[0030]
根据本发明的一些实施方式,所述步骤s1中反应过程中温度为
‑
10~30℃;优选地,所述步骤s1中反应过程中温度为
‑
5~5℃。
[0031]
根据本发明的一些实施方式,所述脱烷基体系为乙酸酐体系。
[0032]
根据本发明的一些实施方式,所述乙酸酐体系由乙酸酐和酸组成。
[0033]
根据本发明的一些实施方式,所述乙酸酐与化合物ⅱ的体积比为1~5:1;优选地,所述乙酸酐与化合物ⅱ的体积比为1.5~2:1。
[0034]
根据本发明的一些实施方式,所述酸为硫酸、甲基磺酸和对甲苯磺酸中的至少一种。
[0035]
根据本发明的一些实施方式,所述酸中硫原子与化合物ⅱ的物质的量之比为0.05~2:1;优选地,所述酸中硫原子与化合物ⅱ的物质的量之比为0.1~0.15:1。
[0036]
根据本发明的一些实施方式,所述乙酸酐体系的温度为
‑
10~10℃;优选地,所述乙酸酐体系的温度为
‑
5~5℃。
[0037]
根据本发明的一些实施方式,所述脱烷基步骤中液液分离操作包含以下过程:
[0038]
1)将反应液加入水中,加热,搅拌30~40min,用乙酸乙酯萃取后,收集有机相d;
[0039]
2)将有机相d减压浓缩后,加入乙醇和水,控制温度为
‑
5~5℃,得混合物e;
[0040]
3)将氢氧化钠添加至混合物e中,控制温度为25~35℃,反应3~4h得混合物f;
[0041]
4)将10%盐酸添加至混合物f中,将ph值调节至2~3,得混合物g;
[0042]
5)将甲苯添加至混合物g中,萃取,收集有机相h;
[0043]
6)将有机相h进行减压浓缩。
[0044]
根据本发明的一些实施方式,所述加热温度为20~50℃;优选地,所述加热温度为25~35℃。
[0045]
根据本发明的一些实施方式,所述碘代体系由三苯基磷、碘、咪唑和四氢呋喃组成。
[0046]
根据本发明的一些实施方式,所述三苯基膦与化合物ⅲ的物质的量之比为1~2:1;优选地,所述三苯基膦与化合物ⅲ的物质的量之比为1.05~1.2:1。
[0047]
根据本发明的一些实施方式,所述咪唑与化合物ⅲ的物质的量之比为1~2:1;优选地,所述咪唑与化合物ⅲ的物质的量之比为1.05~1.2:1。
[0048]
根据本发明的一些实施方式,所述碘单质与化合物ⅲ的物质的量之比为1~2:1;优选地,所述碘单质与化合物ⅲ的物质的量之比为1.05~1.2:1。
[0049]
根据本发明的一些实施方式,所述四氢呋喃与化合物ⅲ的体积之比为2~10:1;优选地,所述四氢呋喃与化合物ⅲ的物质的量之比为2~3:1。
[0050]
根据本发明的一些实施方式,所述步骤s3中反应过程中温度为20~70℃;优选地,所述步骤s3中反应过程中温度为55~65℃。
[0051]
根据本发明的一些实施方式,所述化合物ⅳ溶解选用叔丁醇、碳酸氢盐和水的混合溶液。
[0052]
根据本发明的一些实施方式,所述碳酸氢盐为碳酸氢钠和碳酸氢钾中的至少一种。
[0053]
根据本发明的一些实施方式,所述碳酸氢盐与化合物ⅳ的物质的量之比为1.5~5.0:1;优选地,所述碳酸氢盐与化合物ⅳ的物质的量之比为2.0~2.5:1。
[0054]
根据本发明的一些实施方式,所述叔丁醇与化合物ⅳ的体积比为2~10:1;优选地,所述碳酸氢盐与化合物ⅳ的物质的量之比为2.0~2.5:1。
[0055]
根据本发明的一些实施方式,所述水与化合物ⅳ的体积比为2~10:1;优选地,所述水与化合物ⅳ的物质的量之比为2.0~2.5:1。
[0056]
根据本发明的一些实施方式,所述还原体系为亚磷酸盐体系。
[0057]
根据本发明的一些实施方式,所述亚磷酸盐体系为亚磷酸钙。
[0058]
根据本发明的一些实施方式,所述亚磷酸盐与化合物ⅳ的物质的量之比为1.0~2.0;优选地,所述亚磷酸盐与化合物ⅳ的物质的量之比1.2~1.4。
[0059]
根据本发明实施方式的sglt2抑制剂中间体的合成方法,至少具有如下有益效果:本发明的合成方法合成步骤少,工艺简单易操作;合成过程未使用到昂贵及危险的化合物,没有安全风险;总收率达到60%以上;该方法使用市购的起始物料,成本低,确保了合成路线重现性好,是适用于大规模工业生产的工艺。
附图说明
[0060]
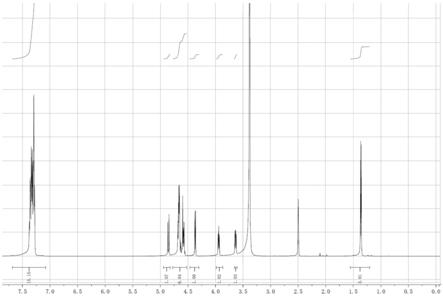
图1为本发明实施例制得的化合物
ⅴ
对应的核磁共振图谱。
具体实施方式
[0061]
为详细说明本发明的技术内容、所实现目的及效果,以下结合实施方式并配合附图予以说明。实施例中所使用的试验方法如无特殊说明,均为常规方法;所使用的材料、试剂等,如无特殊说明,均可从商业途径得到的试剂和材料。
[0062]
本发明的实施例为:一种sglt2抑制剂中间体的合成方法,包括以下步骤:
[0063]
s1、化合物ⅱ的合成:
[0064]
向三口瓶中加入二氯甲烷(500ml)、化合物ⅰ(100.0g),碳酸氢钠(93.2g)和水(1000.0g)溶液,控制温度为2℃,加入溴化钾(13.2g)和2,2,6,6
‑
四甲基哌啶氧化物(3.5g),搅拌5分钟后加入次氯酸钠水溶液(有效氯10%,200g),加料结束后开始计时,反应0.5h后开始hplc监控,待化合物ⅰ含量≤1.5%时反应结束。反应结束后,静置15min,分液,保留有机相;水洗10min,静置15min,分液,收集下层有机相;将有机相进行减压浓缩至无明显馏分,得到化合物ⅱ(105.0g)。
[0065]
s2、化合物ⅲ的合成:
[0066]
向反应釜中加入化合物ⅱ(100.0g),乙酸酐(500g)和硫酸(1.0g),控制温度为0℃,反应0.5h后开始hplc监控,待化合物ⅱ含量≤1.0%时反应结束。反应结束后将反应液缓慢的加入水中,控制温度为30℃,搅拌30min,用乙酸乙酯萃取一次,将有机相进行减压浓缩至无明显馏分,加入乙醇(100g)和水(100g),降温至0℃,加入氢氧化钠(20g),升温至30℃,搅拌3h;再用10%盐酸将ph值调至2;用甲苯萃取一次,收集有机相;将有机相进行减压浓缩至无明显馏分,得到化合物ⅲ(93.0g)。
[0067]
s3、化合物ⅳ的合成:
[0068]
向三口瓶中加入四氢呋喃(500ml)、化合物ⅲ(93.0g),咪唑(18.8g)和三苯基膦(53.4g),控制温度为60℃下,加入碘(51.6g)和thf(300ml)的溶液,加料结束后,搅拌4小时开始hplc监控,待化合物ⅲ含量≤1.0%时反应结束。反应结束后,降温至室温,用水(300g)洗涤一次,收集有机相;将有机相用无水硫酸钠干燥后,再将有机相进行减压浓缩至无明显馏分,得到化合物ⅳ(115.0g)。
[0069]
s4、化合物
ⅴ
的合成:
[0070]
向三口瓶中加入叔丁醇(500ml)、化合物ⅳ(115.0g),碳酸氢钠(38.8g)和水(500g),控温20℃下,分批加入亚磷酸钙(30.0g),加料结束后,搅拌1小时开始hplc监控,待化合物ⅳ含量≤1.0%时反应结束。反应结束后静置15min,分液,保留有机相;水洗10min,静置15min,分液,收集有机相,将有机相进行减压浓缩至无明显馏分;将正庚烷添加至馏分中,打浆得到粗品;粗品使用乙酸乙酯和正庚烷混合溶剂体系(乙酸乙酯和正庚烷的体积比1:5)结晶,得到化合物
ⅴ
。
[0071]
本实施例所得化合物
ⅴ
的质量为49.0g,总收率为61.2%,纯度为98.5%。
[0072]
本发明的实施例制得的化合物
ⅴ
的核磁共振谱图见图1。相应峰位置如下:
[0073]1h nmr(500mhz,dmso
‑
d6)δ7.40
–
7.26(m,15h),4.85(d,j=11.5hz,1h),4.70
–
4.62(m,4h),4.62
–
4.53(m,2h),4.36(d,j=6.0hz,1h),3.94(dd,j=6.1,4.9hz,1h),3.63(dd,j=7.3,4.8hz,1h),1.36(d,j=6.5hz,3h).
[0074]
综上所述,本发明提供的合成方法合成步骤少,工艺简单易操作;合成过程未使用到昂贵及危险的化合物,没有安全风险;总收率达到60%以上;该方法使用市购的起始物料,成本低,确保了合成路线重现性好,是适用于大规模工业生产的工艺。
[0075]
以上所述仅为本发明的实施例,并非因此限制本发明的专利范围,凡是利用本发明说明书及附图内容所作的等同变换,或直接或间接运用在相关的技术领域,均同理包括在本发明的专利保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1