多发性骨髓瘤诊断生物标志物及其应用
1.本发明涉及骨髓瘤诊断的生物标志物及其应用,尤其涉及多发性骨髓瘤诊断的生物标志物及该生物标志物在诊断试剂、诊断装置上的应用,属于生物医学领域。
背景技术:
2.多发性骨髓瘤是一种以恶性浆细胞异常增生伴有单克隆免疫球蛋白过度生成的恶性肿瘤,发病率居血液恶性浆细胞疾病的第二位。绝大部分病例存在单克隆免疫球蛋白或其片段(m 蛋白)的分泌,导致相关器官或组织损伤。常见临床表现为骨痛、贫血、肾功能损害、血钙增高和感染等。随着我国老龄人口的逐年增加,其发病率也逐年升高,现已达到2/10万左右, 低于西方国家(约5/10万)。此病多发于中、老年人,男性多于女性,虽然新型药物及造血干细胞移植使得患者生存时间延长,但多发性骨髓瘤至今仍无法治愈。
3.incrna是一类长度大于200核苷酸的转录本,在转录、转录后和染色体修饰等多个层面,调控胚胎发育、细胞增殖、转移和分化等各种生命活动,其异常表达与多种疾病的发生发展密切相关。lncrnas有组织特异性与时空特异性,不同组织之间的lncrnas表达量不同,同一组织或器官在不同生长阶段,其中的lncrnas表达量也会变化,lncrnas可从染色质重塑、转录调控及转录后加工等多种层面实现对基因表达的调控。研究发现incrna的失调与癌症的发生和发展之间存在着联系,某些incrna的失调与多发性骨髓瘤有关,但其作用及其临床意义尚不完全清楚。因此针对多发性骨髓瘤,研发合适的特异性lncrnas作为疾病诊断标志物等方面具有重要的研究和临床意义。
技术实现要素:
4.本发明所要解决的技术问题是确定一种能够诊断多发性骨髓瘤的标志物。
5.为了解决上述技术问题,本方案的多发性骨髓瘤诊断生物标志物,所述生物标志物为 lnc
‑
rna,所述lnc
‑
rna为linc00475;所述生物标志物利用血液作为生物样品。
6.本方案的检测lnc
‑
rna表达的试剂在制备诊断多发性骨髓瘤的产品中的应用,所述 lnc
‑
rna为linc00475。
7.本方案的检测lnc
‑
rna表达的试剂在制备诊断多发性骨髓瘤的产品中的应用,所述试剂包括通过反转录pcr、实时定量pcr、免疫检测、原位杂交或芯片技术等检测linc00475表达水平用的试剂。
8.上述方案中,所述试剂包括与linc00475或其dna序列结合的核酸。所述核酸包括探针、分子信标、双杂交探针、或复合探针检测linc00475表达量时使用的引物和/或探针。
9.上述方案中,所述核酸包括针对linc00475的引物。
10.上述方案中,所述引物序列为seq id no:1,具体为18s,正向:5
’‑
gtaacc cgttgaaccccatt 和:5
’‑
ccatccaatcggtagtagcg
‑3’
;linc00475正向:5
’‑
ttgatagtctgattcatctgctg
‑3’
,反向:5
’‑
:atgggctaacgttttgggc
‑3’
。
11.上述方案中,所述产品是芯片、试剂盒、试纸或高通量测序平台。
12.本方案中,诊断包括判断受试者是否已经患病、是否存在患病的风险、判断患者是否已经复发、对药物治疗的反应性、或预后情况。
13.本方案中,lncrnas相对表达量分析采用graphpad prism 5软件,采用软件中单样本t 检验和独立样本t检验,p<0.05时,认为结果在统计学上具有显著性差异,p<0.01时,结果在统计学上具有极显著性差异。研究发现,相对健康人样本,多发性骨髓瘤病人linc00475 的表达量发生了显著性的上调表达,在统计学上具有极显著性差异,可以说明linc00475可以作为多发性骨髓瘤特异性标志物用于诊断。
附图说明
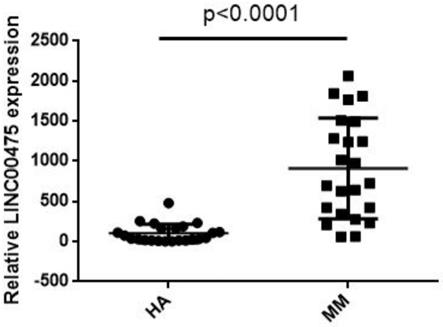
14.图1为linc00475在多发性骨髓瘤病人和正常健康人之间的差异表达图。
具体实施方式
15.下面结合附图和具体实施例对本方案进行详细说明。实施例中未注明具体条件的试验方法按照常规条件进行处理。本方案中总rna提取试剂盒购自bioteke公司;逆转录试剂盒购自thermoscientific公司;taq dna聚合酶/pfu dna聚合酶购自广州锐博公司;sybr greeni mix购自德国罗氏公司。
16.本方案中linc00475序列为seq id no:2。
17.实施例一,多发性骨髓瘤linc00475的表达量发生了显著性的上调表达的验证。
18.a1:收集20例临床确诊的多发性骨髓瘤患者和20例健康对照者。所有参加者血样为晨起空腹抽取,采集外周血3ml置于真空edta抗凝采血管中,颠倒混匀;3000rpm离心10分钟,收集上清液,然后12000rpm离心10分钟,离心后将上层血清分装于无rna酶的2mlep 管中,置于
‑
80℃冰箱保存。
19.a2:将骨髓瘤患者和健康对照者的血清样本于
‑
80℃中取出,待4℃自然溶解;按bioteke 公司的试剂盒说明书提取血清总rna。
20.取骨髓瘤患者和健康对照者总rna样本1.0μl,用紫外分光光度计检测提取的rna浓度和纯度,取吸光度(a260/280nm)在1.8
‑
2.0的样本用于后续试验。另取10μlrna样本,按照逆转录试剂盒说明书操作将rna逆转录为cdna,样本均置-20℃保存。
21.a3:设计lncrnas rt
‑
qpcr引物对
22.用标准曲线测定rt
‑
qpcr引物对表达水平,所有读数均在标准曲线范围内。为了确认pcr 产物的特异性,采用熔融曲线分析和随后的pcr产物克隆和测序。所有反应一式三份。所用引物序列如下:18s,正向:5
’‑
gtaacc cgttgaaccccatt和:5
’‑
ccatccaatcggtagtagcg
‑3’
; linc00475正向:5
’‑
ttgatagtctgattcatctgctg
‑3’
,反向:5
’‑
:atgggctaacgttttgggc
‑3’
。
23.a4:实时荧光定量pcr检测
24.pcr反应体系为20μl,包括sybr greenⅰmix 10μl,10μmol/l上、下游引物各 0.8μl,cdna模板3μl,rnase
‑
free h2o 5.4μl。样品的初始扩增周期为95℃10min,然后进行40个循环,扩增时间分别为95℃15s,60℃30s,然后,72℃30s。在60~95℃时用7500softwarev2.0.1软件分析熔解曲线。每个样本做3个复孔,结果取其均值并计算。以18s作为内参照进行pcr扩增。采用2
‑‑△△
ct
法计算linc00475的相对表达量。公式:
△
ct =ct
(linc00475)-ct(18s),
△△
ct=
△
ct(mm患者组)-
△
ct(对照组),rq=2
‑‑△△
ct
。rq代表相对变化表达量。
25.a5:统计学分析
26.用spss 26.0和graphpad prism5软件进行统计分析及绘图。定量资料如果呈正态分布,则用平均值
±
标准误表示,如果呈非正态分布,则采用中位数(四分位数)[m(p25,p75)] 表示。p<0.05时,认为结果在统计学上具有显著性差异。
[0027]
分别在20例mm病人和20例正常健康人中检测linc00475的表达量,结果显示在m病人中lncrnas发生了显著性的上调表达,见图1,表达差异在2倍以上,p<0.01。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1