一种瑞德西韦磷酸中间体尾链动态动力学拆分方法与流程
1.本发明涉及一种rna聚合酶抑制剂的药物中间体,具体的说,涉及瑞德西韦磷酸的中间体及其制备方法。
背景技术:
2.瑞德西韦,也称为gs
‑
5374,是由美国吉利德科学公司研发,是一种核苷类似物前药,其机理是能够抑制依赖rna的rna抑制酶(rdrp),该药主要作为mers 病毒的试验药物进行研究,目前已经完成iii期临床试验。被认为可以有效抑制呼吸道上皮细胞中sars病毒和mers病毒的复制,这些病毒跟2019
‑
ncov结构相似,瑞德西韦结构式如下:
[0003][0004]
瑞德西韦尚未在任何国家获得批准上市,目前并不是商业化可以直接使用的药品,其疗效和副作用还有待更多的临床实验数据的支持和确认。但从目前的报道来看,瑞德西韦是最近特效药的候选药物。
[0005]
瑞德西韦的化合物专利cn103052631公开了一代合成方法:
[0006][0007]
首先是化合物15在丁基锂的作用下与内酯14进行糖苷化反应。化合物16 接着进行氰基化反应,紧接着进行脱苄基保护得到化合物4。化合物4再与化合物19反应得到消旋的最终化合物,最终进行sfc拆分得到手性化合物。该路线缺点是化合物19的合成收率只有21%,化合物19和化合物4的反应合成化合物 4a的收率仅有23%。化合物4a需要经过手性拆分,很难大规模制备。
[0008]
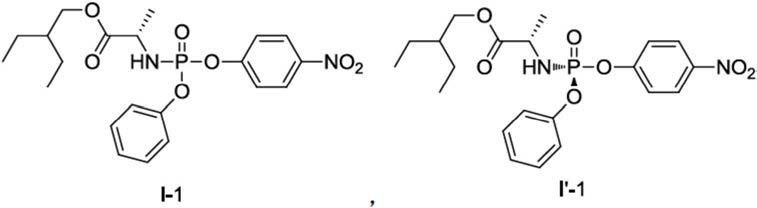
travis k.warren等人2016年发表的nature 531,381
‑
385(2016).公开了瑞德西韦二代合成方法,使用手性磷酸侧链(i
’‑
1),避免了手性拆分的情况。并且公开了化合物式(i
‑
1)在异丙醚作为溶剂重结晶得到中间体式(i
’‑
1)工艺。
[0009]
鉴于已有的路线存在的一些缺陷,有必要进一步开发对环境友好,适用于商业化生产的瑞德西韦磷酸酯尾链的路线。
技术实现要素:
[0010]
本发明提供了一种瑞德西韦磷酸酯尾链动态学拆分方法,该方法简单易行,绿色环保,降低了成本,方便实施工业化生产。
[0011]
为了实现本发明的目的,本发明提供了如下技术方案:
[0012]
第一方面,一种化合物式(i)拆分得到瑞德西韦中间体式为(i’)的制备方法,包含以下步骤:1)化合物式(i)在催化剂、碱条件下进行结晶诱导的差向异构化;2)分离得到式单一构型的i’化合物。
[0013][0014]
其中,r1,r2,r4,r5为h或卤素,r3为卤素或硝基。
[0015]
所述化合物式(i)为差向异构体混合物。
[0016]
所述碱选自1,4
‑
2氮杂二环[2,2,2]辛烷、1
‑
氮杂二环[2,2,2]辛烷、吡啶、 4
‑
二甲胺基吡啶、咪唑、n,n
‑
二甲基苯胺;
[0017]
所述碱的用量为0.01~10当量;
[0018]
所述溶剂选自乙酸乙酯、乙酸甲酯、乙酸异丙酯、乙腈、四氢呋喃、2
‑
甲基四氢呋喃、乙醚、异丙醚、甲基叔丁基醚、异丁醚、异戊醚、二氧六环、乙二醇二甲醚、乙二醇二乙醚、二氯甲烷、氯仿、甲苯、氯苯、环己烷、正己烷、正庚烷以及上述溶剂的不同组合;
[0019]
所述催化剂为对硝基苯酚、五氟苯酚;
[0020]
所述催化剂的用量为0.01~1当量;
[0021]
所述反应温度为
‑
20℃~120℃;
[0022]
所述反应时间为0.01~100h;
[0023]
第二方面,本发明提供了一种(s)
‑2‑
乙基丁基2
‑
(((4
‑
硝基苯氧基)(酚羟基)磷酰)氨基)丙酸酯式(i
‑
1)混合物拆分得到瑞德西韦中间体式为(i
’ꢀ‑
1)的制备方法,包含以下步骤:1)(s)
‑2‑
乙基丁基2
‑
(((4
‑
硝基苯氧基)(酚羟基)磷酰)氨基)丙酸酯(i
‑
1)在催化剂、碱条件下进行结晶诱导的差向异构化;2)分离得到式单一构型的i’化合物。
[0024][0025]
所述化合物式(i
‑
1)为差向异构混合物;
[0026]
所述碱选自1,4
‑
二氮杂二环[2,2,2]辛烷、1
‑
氮杂二环[2,2,2]辛烷、吡啶、 4
‑
二甲胺基吡啶、咪唑、n,n
‑
二甲基苯胺;
[0027]
所述碱的用量为0.01~10当量;
[0028]
所述溶剂选自乙酸乙酯、乙酸甲酯、乙酸异丙酯、乙腈、四氢呋喃、2
‑
甲基四氢呋喃、乙醚、异丙醚、甲基叔丁基醚、异丁醚、异戊醚、二氧六环、乙二醇二甲醚、乙二醇二乙醚、二氯甲烷、氯仿、甲苯、氯苯、环己烷、正己烷、正庚烷以及上述溶剂的不同组合;
[0029]
所述催化剂为对硝基苯酚;
[0030]
所述催化剂的用量为0.01~1当量
[0031]
所述反应温度为
‑
20℃~120℃;
[0032]
所述反应时间为0.01~100h;
[0033]
第三方面,本发明提供了一种(s)
‑2‑
乙基丁基2
‑
(((全氟苯氧基)(酚羟基)磷酰)氨基)丙酸酯式(i
‑
2)混合物拆分得到瑞德西韦中间体式为(i
’‑
2) 的制备方法,包含以下步骤:1)(s)
‑2‑
乙基丁基2
‑
(((全氟苯氧基)(酚羟基) 磷酰)氨基)丙酸酯(i
‑
2)在催化剂、碱条件下进行结晶诱导的差向异构化;2) 分离得到式单一构型的i
’‑
2化合物。
[0034][0035]
所述化合物式(i
‑
2)为差向异构混合物;
[0036]
所述碱选自1,4
‑
二氮杂二环[2,2,2]辛烷、1
‑
氮杂二环[2,2,2]辛烷、吡啶、 4
‑
二甲胺基吡啶、咪唑、n,n
‑
二甲基苯胺;
[0037]
所述碱的用量为0.01~10当量;
[0038]
所述溶剂选自乙酸乙酯、乙酸甲酯、乙酸异丙酯、乙腈、四氢呋喃、2
‑
甲基四氢呋喃、乙醚、异丙醚、甲基叔丁基醚、异丁醚、异戊醚、二氧六环、乙二醇二甲醚、乙二醇二乙醚、二氯甲烷、氯仿、甲苯、氯苯、环己烷、正己烷、正庚烷以及上述溶剂的不同组合;
[0039]
所述催化剂为五氟苯酚;
[0040]
所述催化剂的用量为0.01~1当量
[0041]
所述反应温度为
‑
20℃~120℃;
[0042]
所述反应时间为0.01~100h;
[0043]
本发明的有益效果在于:化合物式(i)差向异构混合物,在动态动力学拆分条件下,经过结晶诱导的差向异构化,最终转化为单一构型的i’化合物。提高了反应的总收率,提高了原材料的利用率,工艺更加绿色高效。
具体实施方式
[0044]
在以下实例中进一步定义本发明。应理解,这些实例虽然指示本发明的优选实施例,但是仅以说明方式给出,并不限制本发明的权利要求。
[0045]
实施例1
[0046]
取(s)
‑2‑
乙基丁基2
‑
(((4
‑
硝基苯氧基)(酚羟基)磷酰)氨基)丙酸酯式(i
‑
1)(s
p
∶r
p
≈71∶29)25g,加入乙酸异丙酯(25ml)搅拌溶清,加入正庚烷(100ml),加入1,4
‑
二氮杂二环[2,2,2]辛烷(0.63g),加入对硝基苯酚(0.78 g),控温至10~15℃,保温搅拌12~14h。降
温至0~5℃,过滤、漂洗,收集滤液进行下一次循环操作。湿品真空干燥得到白色固体16.7g,收率67%。
[0047]
实施例2
[0048]
取(s)
‑2‑
乙基丁基2
‑
(((4
‑
硝基苯氧基)(酚羟基)磷酰)氨基)丙酸酯式(i
‑
1)(s
p
∶r
p
≈49∶51)25g,加入乙酸异丙酯(25ml)搅拌溶清,加入正庚烷(100ml),加入咪唑(0.38g),加入对硝基苯酚(0.78g),滴加正庚烷(100 ml),控温至0~5℃,保温搅拌40~48h。过滤、漂洗,收集滤液进行下一次循环操作。湿品真空干燥得到白色固体21.2g,收率85%。
[0049]
实施例3
[0050]
取(s)
‑2‑
乙基丁基2
‑
(((全氟苯氧基)(酚羟基)磷酰)氨基)丙酸酯式 (i
‑
2)(s
p
∶r
p
≈70∶30)30g,加入异丙醚(300ml),搅拌溶清,加入咪唑(0.41 g),加入五氟苯酚(1.11g),升温至0~5℃,保温搅拌40~48h。降温至0~ 5℃,过滤、漂洗,收集滤液进行下一次循环操作。湿品真空干燥得到白色固体 24.6g,收率82%。
[0051]
实施例4
[0052]
取(s)
‑2‑
乙基丁基2
‑
(((全氟苯氧基)(酚羟基)磷酰)氨基)丙酸酯式 (i
‑
2)(s
p
∶r
p
≈49∶51)30g,加入异丙醚(300ml),搅拌溶清,加入咪唑(0.41 g),加入五氟苯酚(1.11g),升温至0~5℃,保温搅拌40~48h。降温至0~ 5℃,过滤、漂洗,收集滤液进行下一次循环操作。湿品真空干燥得到白色固体 26.1g,收率87%。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1