可结合SARS-CoV-2的纳米抗体及其应用的制作方法
本发明涉及生物医药领域。更特别地,涉及一种可结合sars-cov-2的多肽,以及上述多肽在治疗、预防和检测sars-cov-2中的应用。
背景技术:
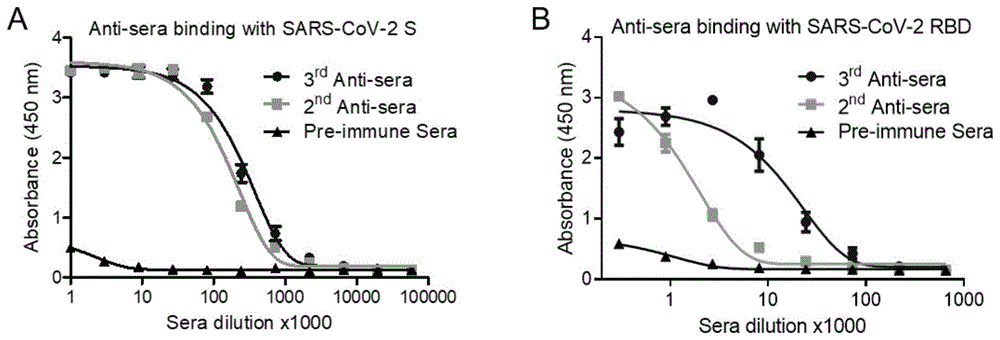
:2019年12月,一种新型冠状病毒(sars-cov-2)出现,导致人类爆发严重甚至致命的肺炎。该病毒进入细胞依赖于病毒刺突蛋白(s蛋白)的受体结构域(rbd)与靶细胞受体血管紧张素转换酶2(ace2)之间的结合,这表明,破坏rbd-ace2相互作用将阻止sars-cov-2进入细胞。因此,以rbd为靶点,筛选与rbd有结合活性的抗体从而抑制rbd和ace2的结合将是对抗sars-cov-2行之有效的方法。1993年,一种来源于骆驼科的新型天然抗体被发现。该抗体天然缺失轻链而只由重链组成,其重链包含两个恒定区(ch2和ch3)、一个铰链区和一个重链可变区(variableheavychaindomain,vhh,即抗原结合位点),该重链可变区的相对分子质量约为13kda,仅为常规抗体的1/10,且分子高度和直径均在纳米级别,是目前可获得的最小的功能性抗体片段,因此又被称为纳米单抗(nanobody,nb)。因纳米单抗稳定性高(90℃条件下仍不会降解)、亲和力高、与人源抗体同源性超过80%、毒性和免疫原性均较低等特点,最近纳米单抗被广泛用于免疫诊断试剂盒研发、影像学研发以及针对肿瘤、炎症、传染病和神经系统疾病等领域的抗体药物研发。有研究报道,sars-cov-2的rbd-ace2结合机制与sars-cov的几乎相同,且利用rbd蛋白免疫动物可以产生强有效的针对sars-cov的多克隆抗体,从而抑制病毒侵入。根据这些研究推断,抗rbd抗体也可以有效地阻止sars-cov-2的进入。因此我们期望通过新的技术手段,获得可检测sars-cov-2的特异性检测抗体,以及高效稳定的、低ic50的sars-cov-2特异性中和抗体。技术实现要素:本发明通过用抗原免疫羊驼,获取羊驼源纳米单抗及其vhh,用于治疗sars-cov-2感染的病人。基于这些研究,本发明提供了一种可结合sars-cov-2的多肽,包括3个互补决定区cdr1-3,cdr1序列为或包括seqidno:1-9所示序列之一,cdr2序列为或包括seqidno:10-20所示序列之一,cdr3序列为或包括seqidno:21-38所示序列之一。在一个具体实施方案中,所述多肽还包括4个框架区fr1-4,所述fr1-4与所述cdr1-3交错排列。例如,可将fr1-4序列设计为如seqidno:39-42所示,但本发明的范围不限于此。抗体的特异性识别和结合能力主要由cdr区序列决定,fr序列影响不大,可根据物种来设计,这是本领域公知的。例如,可设计人源、鼠源或骆驼源的fr区序列来连接上述cdr,从而一个可结合sars-cov-2的多肽或结构域。例如,人源的fr1-4的序列可设计为43-46。在一个优选实施方案中,所述多肽为单克隆抗体。在一个优选实施方案中,所述多肽为vhh。在一个优选实施方案中,所述多肽为骆驼源的vhh或人源化的vhh。在一个具体实施方案中,所述多肽的cdr序列如下:i)cdr1的序列为fsissxdt,其中,第6位的x表示异亮氨酸或缬氨酸;并且ii)cdr2的序列为seqidno:10并且cdr2的序列为seqidno:21;或者cdr1的序列为seqidno:11并且cdr2的序列为seqidno:22。优选地,cdr1的序列为seqidno:1,cdr2的序列为seqidno:10,并且cdr3的序列为seqidno:21;或cdr1的序列为seqidno:2,cdr2的序列为seqidno:11,并且cdr3的序列为seqidno:22。在一个具体实施方案中,所述多肽的cdr序列如下:i)cd1的序列为seqidno:6ii)cd2的序列选自seqidno:15-17;并且iii)cd3的序列选自seqidno:26-35。优选地,cd1的序列为seqidno:6,cdr2的序列为seqidno:15,并且cd3的序列选自seqidno:26-33和35;或者cd1的序列为seqidno:6,cdr2的序列为seqidno:16,并且cd3的序列为seqidno:27;或者cd1的序列为seqidno:6,cdr2的序列为seqidno:17,并且cd3的序列为seqidno:34。在一个具体实施方案中,所述多肽的cdr序列如下:cd1的序列为seqidno:3,cdr2的序列为seqidno:12,并且cd3的序列为seqidno:23;或者cd1的序列为seqidno:4,cdr2的序列为seqidno:13,并且cd3的序列为seqidno:24;或者cd1的序列为seqidno:5,cdr2的序列为seqidno:14,并且cd3的序列为seqidno:25;或者cd1的序列为seqidno:7,cdr2的序列为seqidno:18,并且cd3的序列为seqidno:36;或者cd1的序列为seqidno:8,cdr2的序列为seqidno:19,并且cd3的序列为seqidno:37;或者cd1的序列为seqidno:9,cdr2的序列为seqidno:20,并且cd3的序列为seqidno:38。本发明还提供了上述多肽在制备sars-cov-2感染治疗剂中的应用。在一个优选实施方案中,上述多肽的cdr序列如下:cd1的序列为seqidno:3,cdr2的序列为seqidno:12,并且cd3的序列为seqidno:23;或者cd1的序列为seqidno:6,cdr2的序列为seqidno:16,并且cd3的序列为seqidno:27;或者cd1的序列为seqidno:6,cdr2的序列为seqidno:17,并且cd3的序列为seqidno:34。本发明还提供了上述多肽在在制备sars-cov-2检测剂中的应用。在一个优选实施方案中,上述多肽的cdr序列如下:cd1的序列为seqidno:3,cdr2的序列为seqidno:12,并且cd3的序列为seqidno:23;或者cd1的序列为seqidno:6,cdr2的序列为seqidno:16,并且cd3的序列为seqidno:27;或者cd1的序列为seqidno:6,cdr2的序列为seqidno:17,并且cd3的序列为seqidno:34。本发明还提供了编码上述多肽的核酸。本发明还提供了上述核酸在制备sars-cov-2治疗和预防药物中的应用。在一个具体实施方案中,所述核酸为dna或rna。在一个具体实施方案中,所述核酸存在于基因表达框中。本发明还提供了包含上述核酸的表达框的表达载体。在一个优选实施方案中,所述表达载体为类病毒表达载体。在一个优选实施方案中,所述表达载体为腺相关病毒表达载体(aav载体)。本发明针对sars-cov-2进行纳米抗体药物开发,通过免疫羊驼、利用噬菌体库展示纳米单抗的平台技术等,筛选到特异性结合sars-cov-2s蛋白上受体结构域(rbd)的纳米抗体vhh,鉴定了其cdr序列,并构建了人源化的vhh-hufc1(c9nb);利用病毒中和实验评估c9nb在治疗sars-cov-2感染的疗效;同时,利用aav载体装载了编码c9nb的表达序列。本发明为sars-cov-2的临床预防、治疗和检测提供了潜在的纳米抗体新药。附图说明图1为sars-cov-s蛋白第2和3次免疫羊驼一周后分别针对s蛋白(a)和rbd蛋白(b)的抗血清效价,以免疫前的血清为对照;图2为sars-cov-s-vhh噬菌体抗体文库为模板扩增的pcr产物的电泳图;图3为sars-cov-s-vhh噬菌体抗体文库的淘选鉴定,其中,a为噬菌体文库针对s蛋白淘选后elisa检测统计图;b为从第二轮(2nd)和第三轮(3rd)淘选后的噬菌体抗体文库各挑选96个克隆,针对rbd蛋白进行噬菌体elisa检测统计图;图4为真核表达的vhh抗体的elisa检测统计图,每个点代表一个克隆,纵坐标为针对rbd的od450/空白对照的od450,比值大于5.0定义为阳性;图5为真核表达的vhh抗体的spr检测统计图;图6为elisa检测不同纯化浓度的阳性vhh抗体与rbd蛋白结合的od450统计图;图7为阳性vhh抗体中和sars-cov-2病毒感染实验统计图,其中,a为阳性抗体中和假病毒感染实验统计图;b为阳性抗体中和真病毒感染实验统计图。具体实施方式1.羊驼免疫与抗血清的获得用250μgsars-cov-2的s蛋白与250μl弗氏完全佐剂的乳化混合物对羊驼进行初免,在第14天、28天用125μgs蛋白与250μl弗氏不完全佐剂加强免疫2次,第2次免疫1周后,采血检测抗血清滴度;第3次免疫1周后,采血200ml用于噬菌体抗体库的构建。抗血清效价通过elisa检测,分别用浓度为0.5μg/ml的s蛋白和rbd蛋白包被检测板,每孔加入梯度稀释的抗血清(对照为免疫前羊驼血清),37℃孵育1.5h,洗涤2次,每孔加入1:10000稀释的辣根过氧化物酶标记的goatanti-llammaigg(h+l)二抗,37℃孵育1h,洗涤4-6次后,加100μltmb底物,37℃孵育10min,50μl0.2m的h2so4中止反应,测定od450nm。elisa检测血清效价规定为在od450是空白对照的2.1倍以上并且大于0.2的最高稀释倍数。结果如图1所示,2免和3免的抗血清针对s蛋白效价分别为2.19×106和6.56×106针对rbd蛋白效价分别为2.43×104和2.19×105。由此可见,该抗原可诱导骆驼产生特异性针对s蛋白上rbd区域的高滴度抗血清。2.vhh噬菌体库构建及淘选收集200ml免疫后骆驼的外周血,利用淋巴细胞分离液(geficoll-paqueplus)分离获得骆驼的pbmc,根据trizol操作手册,提取rna,并利用oligo(dt)反转为cdna,通过引物扩增,以及分子克隆等技术,将骆驼的vhh基因克隆至phagemid质粒,转化tg1细菌,得到vhh噬菌体库。为了进一步鉴定cov-vhh噬菌体库是否构建成功,通过pcr扩增免疫s蛋白羊驼的vhh目的基因,可以看出目的条带为500bp,大小符合预期(图2),说明该cov-vhh噬菌体抗体文库里含有vhh基因。挑选50个克隆进行测序,测序结果显示,所测序列没有完全一致的重复序列;比对结果显示,差异序列大多在cdr结合区。经检测,该实验构建了一个cov-vhh噬菌体抗体文库,库容为2.0×109,阳性率为100%,序列多样性(diversity)为100%,有效插入率(inframerate)大于95%。在m13ko7辅助噬菌体的帮助下,用vhh-phagemid转化的细菌,进行噬菌体抗体库的复苏,并用peg/nacl进行沉淀。将包被有50μg/ml的s-his蛋白进行三次富集噬菌体抗体库。将富集的噬菌体,洗脱、转化、涂板、挑取单克隆进行噬菌体分别与s蛋白和rbd蛋白elisa的结合鉴定,将结合读值>1.0的克隆进行测序,并克隆至表达载体pvax1,转染293f细胞表达生产纳米单抗。淘选后的文库与s蛋白进行结合检测。噬菌体elisa结果显示,没有富集前的cov-vhh噬菌体文库与s蛋白的结合读值为0.79,经过一轮、二轮、三轮富集后的噬菌体文库读值分别为1.58、2.43、2.78(图3a)。为了进一步验证富集后的文库中结合cov-vhh蛋白的阳性噬菌体率,从第2轮和第3轮富集后的文库里各挑选了94个克隆进行单个噬菌体elisa检测。结果显示,第2轮文库里,36.1%的单个噬菌体克隆与s蛋白结合,其中52.9%的单个噬菌体克隆同时与rbd结合,第3轮文库里31.9%的噬菌体克隆克隆与rbd结合,而且结合读值/空白对照组读值大于5(图3b),通过s蛋白淘选成功的富集了高结合力的cov-vhh噬菌体文库。3.vhh-hufc(c9nb)真核表达通过分子克隆技术,将上述经序列分析得到的21个不同序列的纳米单抗vhh基因融合人的fc基因并插入在pcdna3.4建形成nb-hufc-pcdna3.4表达质粒。将构建好的nb-hufc-pcdna3.4,转染293tt细胞,表达生产nb-hufc(c9nb),并利用proteing纯化。收集纯化的vhh-hufc1(c9nb)进行elisa测定,部分抗体有很好的结合能力(图4)。构建的人源化抗体相应的序列号如表1所示。表1人源化抗体snb对应的原抗体编号及cdr序列对上述elisa检测的全部克隆进行抗体与rbd蛋白的亲和力测定试验。应用fortebio生物分子相互作用平台检测亲和力。将待测抗体vhh-hfc1固化至anti-humaniggfccapturebiosensors(ahc)探头上,固化时间400s,再结合抗原rbd-his蛋白,结合时间180s,解离时间180s,观察抗体-抗原的结合解离情况,由仪器拟合曲线,导出数据。亲和力测定结果如表2所示,大部分的抗体的亲和力(kd)能达到10-8至10-9m(nm级别),部分抗体的结合解离曲线如图5所示。可见,我们获得的这些c9nb纳米抗体具有较高的亲和力,能够特异性地识别和结合sars-cov-2病毒s蛋白上的rbd结构域。其中,抗体c9nb15,c9nb22和c9nb31获得稳态时响应值较高,说明这三个抗体的结合能力较强,针对这三个抗体进行进一步研究。表2c9nb亲和力的总结。cloneidka(1/ms)kd(1/s)kd(m)response(nm)c9nb016.48e+042.97e-034.59e-080.0156c9nb026.85e+051.69e-022.47e-080.0302c9nb044.40e+056.30e-031.43e-080.1824c9nb057.62e+051.11e-031.46e-090.0195c9nb071.84e+052.40e-021.30e-070.0166c9nb095.16e+054.67e-039.04e-090.1254c9nb123.79e+054.70e-031.24e-080.2218c9nb133.04e+052.49e-048.19e-100.0203c9nb145.76e+04<1.0e-07<1.0e-120.0159c9nb156.94e+054.22e-036.09e-090.2314c9nb193.48e+051.31e-023.76e-080.0366c9nb224.92e+052.94e-035.99e-090.2322c9nb248.30e+053.53e-034.25e-090.1684c9nb253.12e+051.92e-036.14e-090.0168c9nb272.46e+055.61e-032.28e-080.016c9nb282.04e+035.82e-022.86e-050.0068c9nb291.34e+055.95e-044.45e-090.0169c9nb305.46e+051.16e-022.12e-080.0469c9nb316.37e+056.64e-031.04e-080.246c9nb334.34e+051.95e-034.51e-090.1328注:ka为结合常数,kd为解离常数,kd为亲和力,response为获得稳态时的响应值。4.抗体梯度稀释elisa用0.5μg/ml的rbd蛋白包被检测板,每孔100μl,37℃孵育2h,洗涤2-4次,4%牛血清封闭,每孔250μl,37℃孵育1h,洗涤2-4次,每孔加入梯度稀释的纯化抗体100μl,37℃孵育1.5h,洗涤2次,每孔加入1:10000稀释的辣根过氧化物酶标记的anti-human抗体100μl,37℃孵育1h,洗涤4-6次后,加100μltmb底物,37℃孵育10min,50μl0.2m的h2so4中止反应,测定od450nm。结果显示(图6),当抗体c9nb15,c9nb22,c9nb31浓度分别低至0.001526,0.000763,0.000763ug/ml,其与rbd蛋白结合的od450/空白对照的od450,比值仍大于2。5.c9nb中和sars-cov-2假病毒通过将表达萤火虫荧光素酶(pnl43r-e-luciferase)和pcdna3.1(invitrogen)表达载体共转染到293t细胞(atcc)中,分别生成了sars-cov-2、sars-cov和mers–cov假病毒。48h后收集病毒上清。病毒滴度通过相对光单位的荧光素酶活性测定(bright-glo荧光素酶检测载体系统,promegabiosciences)。对照单克隆抗体为抗sfts抗体snb02(1mg/ml)。选取vhh-hufc1中的c9nb15,c9nb22和c9nb31进行体外中和实验。将抗体梯度稀释为不同的浓度,与sars-cov-2、sars-cov和mers-cov假病毒一起,于5%co237℃下共孵育1个小时,添加1.5x104个huh7细胞,5%co237℃温箱培养48小时后,通过检测荧光素酶活性测定评估单克隆抗体的半最大抑制浓度(ic50)结果如图7a所示,c9nb15,c9nb22和c9nb31具有很好的中和活性,当抗体浓度分别在0.00395,0.00794和0.02029μg/ml时,抑制率能达到90%。6.c9nb中和sars-cov-2真病毒sars-cov-2聚焦还原中和试验(frnt)是在一个生物安全三级认证实验室进行的。使用先前从一名感染患者的鼻咽拭子中获得的临床分离物(beta/shenzhen/szth-003/2020,epi_isl_406594atgisaid),对活的sars-cov-2进行中和试验。连续稀释检测抗体,与75μl的sars-cov-2(8×103聚焦形成单位/ml,ffu/ml)在96孔微波板中混合,37℃孵育1小时。然后将混合物转移到96孔板中,接种veroe6细胞,在37℃条件下吸收1小时。然后去除接种菌,加入覆盖培养基(100μl含1.6%的羟甲基纤维素,cmc)。然后在37℃下孵育24小时。4%多聚甲醛溶液固定细胞30分钟,去除覆盖层。用0.2%tritonx-100使细胞通透,并与交叉反应兔抗sars-cov-nigg(sinobiological,inc)在室温下孵化1小时,然后加入hrp标记的山羊抗兔igg(h+l)抗体(jacksonimmunoresearch)。细胞在室温下进一步孵育。该反应是用kpltrueblue过氧化物酶底物(seracare生命科学公司)进行的。使用elispot分析仪(cellulartechnologyltd.)计算sars-cov-2病灶的数量。结果如图7b所示,c9nb15,c9nb22和c9nb31具有很好的中和活性,当抗体浓度分别在0.0308,0.1716和0.0411μg/ml时,抑制率能达到90%。10、aav病毒载体装载的vvh腺相关病毒载体(aav)源于非致病的野生型腺相关病毒,由于其安全性好、宿主细胞范围广(分裂和非分裂细胞)、免疫源性低,在体内表达外源基因时间长等特点,被视为最有前途的基因转移载体之一,在世界范围内的基因治疗和疫苗研究中得到广泛应用。aavhelper-free病毒包装系统购于cellbiolabs,sandiegousa。将上述vhh的dna编码序列通过分子克隆技术插入到paav-mcs质粒;通过测序证明构建成功后,将构建好的质粒paav-ab与phelper和paav-dj质粒按照质量比1:1:1的方式使用pei转染试剂共转染aav-293t细胞。转染后分别于48、72、96和120小时收集上清,并用5xpeg8000(sigma)进行浓缩,最后用1.37g/ml氯化铯进行纯化。纯化的aav溶解于pbs里,进行鉴定和分装后保存于-80℃。由于上述抗体可特异性识别并结合sars-cov-2的s蛋白,并且c9nb15,c9nb22和c9nb31具有良好的中和活性,因此,装载vhh的aav载体导入到人体后,可使人体表达具有中和活性的抗体,从而使人体可预防sars-cov-2感染,也可治疗感染了sars-cov-2的患者。以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。序列表<110>南京拓峰生物科技有限公司<120>可结合sars-cov-2的纳米抗体及其应用<160>46<170>siposequencelisting1.0<210>1<211>8<212>prt<213>人工序列(artificialsequence)<400>1pheserileserserileaspthr15<210>2<211>8<212>prt<213>人工序列(artificialsequence)<400>2pheserileserservalaspthr15<210>3<211>8<212>prt<213>人工序列(artificialsequence)<400>3glyphethrleuasptyrtyrala15<210>4<211>8<212>prt<213>人工序列(artificialsequence)<400>4glyphethrseraspargtyrthr15<210>5<211>8<212>prt<213>人工序列(artificialsequence)<400>5glyphethrtrpasntyrhisala15<210>6<211>8<212>prt<213>人工序列(artificialsequence)<400>6glyglythrleualaserpheala15<210>7<211>8<212>prt<213>人工序列(artificialsequence)<400>7glyasnilepheseriletyrthr15<210>8<211>8<212>prt<213>人工序列(artificialsequence)<400>8lysileileleuserphetyrasp15<210>9<211>8<212>prt<213>人工序列(artificialsequence)<400>9argasnilepheseriletyrthr15<210>10<211>7<212>prt<213>人工序列(artificialsequence)<400>10ilethrserargargaspthr15<210>11<211>7<212>prt<213>人工序列(artificialsequence)<400>11ileserserargserphethr15<210>12<211>7<212>prt<213>人工序列(artificialsequence)<400>12ileserserserglyserthr15<210>13<211>8<212>prt<213>人工序列(artificialsequence)<400>13ileserserserglyglyserthr15<210>14<211>8<212>prt<213>人工序列(artificialsequence)<400>14ileserserserglyserthrthr15<210>15<211>7<212>prt<213>人工序列(artificialsequence)<400>15ileasnileileasnargthr15<210>16<211>7<212>prt<213>人工序列(artificialsequence)<400>16ileaspvalileasnargala15<210>17<211>7<212>prt<213>人工序列(artificialsequence)<400>17ileasnileileasnargpro15<210>18<211>7<212>prt<213>人工序列(artificialsequence)<400>18valthrserglyglyserthr15<210>19<211>7<212>prt<213>人工序列(artificialsequence)<400>19ilethrasnserglyserthr15<210>20<211>7<212>prt<213>人工序列(artificialsequence)<400>20ilethrserglyglyserthr15<210>21<211>10<212>prt<213>人工序列(artificialsequence)<400>21tyrglyglnaspvalleuglyglniletyr1510<210>22<211>10<212>prt<213>人工序列(artificialsequence)<400>22tyrglyglnaspileleuglyglniletyr1510<210>23<211>15<212>prt<213>人工序列(artificialsequence)<400>23alaglyvalvalhisaspvalglnalametcysvalmetasnpro151015<210>24<211>22<212>prt<213>人工序列(artificialsequence)<400>24thralaargproserleutrpalavalvalalaglycysproleuasp151015glnasnthrtyrpheser20<210>25<211>20<212>prt<213>人工序列(artificialsequence)<400>25alaalaprohisserglyservalcysproargtrpalaglutyrtyr151015glyvalasphis20<210>26<211>22<212>prt<213>人工序列(artificialsequence)<400>26alaalahisphevalproproglyserargleuargaspcysleuval151015asngluleutyrasntyr20<210>27<211>22<212>prt<213>人工序列(artificialsequence)<400>27alaalahisphevalproproglyserargleuargglycysleuval151015asngluleutyrasntyr20<210>28<211>22<212>prt<213>人工序列(artificialsequence)<400>28alaalahisphevalproproglyserargleuargglycysleuval151015asnglualatyrasntyr20<210>29<211>22<212>prt<213>人工序列(artificialsequence)<400>29alaalahisphevalproproglyglyargleuargglycysleuval151015asnaspleutyrasntyr20<210>30<211>22<212>prt<213>人工序列(artificialsequence)<400>30alaalahisphevalproproglyserargleuargglycysleuval151015asnaspleutyrasntyr20<210>31<211>22<212>prt<213>人工序列(artificialsequence)<400>31alaalahisphevalproproglyserargleuargglycysleuval151015asnaspvaltyrasntyr20<210>32<211>22<212>prt<213>人工序列(artificialsequence)<400>32alaalahisphevalproprogluserargleuargglycysleuval151015asngluleutyrasntyr20<210>33<211>22<212>prt<213>人工序列(artificialsequence)<400>33alaalahisphevalproprogluserargleuargglycysleuval151015asnglualatyrasntyr20<210>34<211>22<212>prt<213>人工序列(artificialsequence)<400>34alaalahisphevalproproglyserargleuglyglycysleuval151015asngluleutyrasntyr20<210>35<211>22<212>prt<213>人工序列(artificialsequence)<400>35alaalahisphevalproproglyserargpheargglycysserval151015asngluleutyrasntyr20<210>36<211>9<212>prt<213>人工序列(artificialsequence)<400>36asnalaargleupheaspproglytyr15<210>37<211>5<212>prt<213>人工序列(artificialsequence)<400>37asnthrphehistyr15<210>38<211>10<212>prt<213>人工序列(artificialsequence)<400>38thrthralaglysertrpglnglyasptyr1510<210>39<211>25<212>prt<213>人工序列(artificialsequence)<400>39gluvalglnleuvalgluserglyglyglyleuvalglnproglygly151015serleuargleusercysalaalapro2025<210>40<211>17<212>prt<213>人工序列(artificialsequence)<400>40metglytrptyrhisglnalaproglylysglnarggluleuvalala151015ala<210>41<211>38<212>prt<213>人工序列(artificialsequence)<400>41asntyralaaspservallysglyargphethrileserargaspasn151015alalysasnthrvaltyrleuglnmetasnserleulysprogluasp202530thralavaltyrtyrcys35<210>42<211>20<212>prt<213>人工序列(artificialsequence)<400>42trpglyglnglythrglnvalthrvalsersergluprolysthrpro151015lysproglnpro20<210>43<211>25<212>prt<213>人工序列(artificialsequence)<400>43glnvalargleuvalgluserglyglyglyservalglnalaglyglu151015thrleuargleusercysthralaser2025<210>44<211>17<212>prt<213>人工序列(artificialsequence)<400>44metglytrptyrargglnglyproglyasnglucysglumetvalala151015tyr<210>45<211>36<212>prt<213>人工序列(artificialsequence)<400>45alaaspserthrlysglyargphethrileserglnaspasnalalys151015histhrleutyrleuglnmetasnserleulysprogluaspthrgly202530valtyrtyrcys35<210>46<211>10<212>prt<213>人工序列(artificialsequence)<400>46glyglnglythrargvalthrvalserser1510当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1