水稻根分泌多肽PEP1及其编码基因和应用
水稻根分泌多肽pep1及其编码基因和应用
技术领域
1.本发明涉及生物技术领域,特别涉及一种植物根分泌多肽及其编码基因在调控植物根生长与发育中的应用。
背景技术:
2.根是植物重要的地下器官,其不仅可以固定植株,而且还可以从土壤中吸收营养、水分等物质供植物的生长发育。此外,植物的根系还可以监测土壤环境中的各种信号分子,比如土壤中的水分含量,营养物质的水平以及一些植物激素及信号等,以提高植物对其生长环境的适应性(meng et al.2019)。植物根系主要分为两大类,分别为直根系和须根系。水稻是单子叶模式植物,其根系为须根系,主要由种子根和不定根及种子根和不定根上的侧根和根毛组成(rebouillat et al.2009;coudert et al.2010)。研究表明根冠比高,发达的根系有助于提高水稻的抗旱能力及产量(fukai et al.1995;gowda et al.2011)。之前研究表明,水稻根系的生长发育受到外源信号与内源遗传程序的严格调控(benfey et al.2012;orman
‑
ligeza et al.2013)。
3.之前的研究解结果表明,多肽可以作为外源的信号分子调控拟南芥的根系发育(oh et al.,2018)。外源施加人工合成的多肽根茎生长因子1(rgf1)可以回复tpst
‑
1突变体中根尖分生区缺陷的表型,表明rgf1是维持根尖干细胞所必需的(matsuzaki et al.2010)。进一步的突变分析表明,rgf/glv通过转录后调控机制控制根分生组织中生长素外排载体pinformed2的丰度和运输动力学进而调控植物根尖分生区的大小(whitford et al.2012)。植物根分生组织的大小也受多肽cle(clavata3(clv3)/embryo surfrounding region(esr)
‑
related)家族的调控。拟南芥中有32个cle多肽编码基因,其编码的多肽可分为两组:a型cle和b型cle。a型cle多肽在根分生组织发育中起作用,而b型cle多肽与根维管束发育有关(cock and mccormick 2001;whitford et al.2008)。例如a型cle多肽cle40是柱状细胞分化所必需的,功能丧失的突变体cle40由于柱状细胞的延迟分化而表现出具有不规则形状的根尖,从而表现为短根表型(stahl et al.2009)。其他另一些的cle多肽(cle26,cle40,cle45)通过调节维管束发育过程中原上皮形成来控制主根的生长(depuydt et al.2013;rodriguez
‑
villalon et al.2014;rodriguez
‑
villalon et al.2015;hazak et al.2017)。此外,酪氨酸硫酸化肽psk与psy1可通过调节伸长区/分分生区中的细胞扩增来促进主根生长(amano et al.2007;kwezi et al.2011;hartmannet et al.2014;ladwiget et al.2015)。凯氏带完整性因子1(cif1)多肽对于凯氏带的形成是必不可少的,因为cif1功能丧失的突变体在高铁浓度下表现出严重的生长发育迟缓,但是通过使用外源施加cif1多肽处理后,可以完回复这些缺陷(nakayama et al.2017)
4.与拟南芥相比,多肽调控水稻根系生长发育的机制尚不清楚。所以分离鉴定水稻根系生长发育相关的多肽,确定这些多肽的编码基因对进一步全面了解水稻及其他单子叶植物根系发生发育的机理,获得优良基因以培育新的水稻品种是十分重要的和必要的。
5.参考文献:
6.amano y,tsubouchi h,shinohara h et al(2007)tyrosine
‑
sulfated glycopeptide involved in cellular proliferation and expansion in arabidopsis.proc.natl.acad.sci.u.s.a.104,18333
‑
18338(amano y,tsubouchi h,shinohara h等(2017)酪氨酸硫酸化糖肽参与拟南芥中的细胞增殖和扩增。美国科学院院刊104,18333
‑
18338)。
7.benfey pn(2012)toward a systems analysis of the root.cold spring harbor symposia on quantitative biology,77,91(benfey pn(2012)植物根系系统分析指南。冷泉港定量生物学座谈会77,91)。
8.cock j and mccormick s(2001)a large family of genes that share homology with clavata3.plant physiol.126,939
‑
942(cock j and mccormick s(2001)clavata3同源基因家族分析研究。植物生理126,939
‑
942)。
9.coudert y,b
è
s m,le tv et al(2011)transcript profiling of crown rootless1 mutant stem base reveals new elements associated with crown root development in rice.bmc genomics 12,1
‑
12(coudert y,b
è
s m,le tv等(2011)水稻根发育分子遗传学。bmc基因组学12,1
‑
12)。
10.coudert y,perin c,courtois b et al(2010)genetic control of root development in rice,the model cereal.trends plant sci 15,219
‑
226(coudert y,perin c,courtois b等(2010)谷物模式植物水稻根系发育的遗传控制。植物科学进展15,219
‑
226)。
11.depuydt s,rodriguez
‑
villalon a,santuari l et al(2013)suppression of arabidopsis protophloem differentiation and root meristem growth by cle45 requires the receptor
‑
like kinase bam3.proc.natl.acad.sci.u.s.a.110,7074
‑
7079(depuydt s,rodriguez
‑
villalon a,santuari l等(2013)cle45抑制拟南芥原位生物分化和根分生组织生长需要类受体激酶bam3。美国科学院院刊110,7074
‑
7079)。
12.fukai s,cooper m(1995)development of drought resistant cultivars using physio
‑
morphological traits in rice.field crops res 40,67
‑
87(fukai s,cooper m(1995)利用水稻生理形态性状开发抗旱品种。田间作物研究40,67
‑
87)。
13.hartmann j,fischer c,dietrich p et al(2014)kinase activity and calmodulin binding are essential for growth signaling by the phytosulfokine receptor pskr1.plant j.78,192
‑
202(hartmann j,fischer c,dietrich p等(2014)激酶活性和钙调蛋白结合对于植物硫代素受体pskr1的生长信号传递至关重要。植物期刊78,192
‑
202)。
14.hazak o,brandt b,cattaneo p et al(2017)perception of root
‑
active cle peptides requires coryne function in the phloem vasculature.embo rep.18,1367
‑
1381(hazak o,brandt b,cattaneo p等(2017)cle肽的根部感知活性需要在韧皮部脉管系统中发挥coryne功能。水稻根发育分子遗传学。embo简报18,1367
‑
1381)。
15.kwezi l,ruzvidzo o,wheeler ji et al(2011)the phytosulfokine(psk)receptor is capable of guanylate cyclase activity and enabling cyclicgmp
‑
dependent signaling in plants.j.biol.chem.286,22580
‑
22588(kwezi l,ruzvidzo o,
wheeler ji等(2011)植物硫代因子(psk)受体具有鸟苷酸环化酶活性,并能够在植物中实现依赖环gmp的信号传导。生物化学期刊286,22580
‑
22588 2,15
‑
34)。
16.ladwig f,dahlke ri,st
ü
hrwohldt n et al(2015)phytosulfokine regulates growth in arabidopsis through a response module at the plasma membrane that includes cyclic nucleotide
‑
gated channel17,h+
‑
atpase,and bak1.plant cell 27,1718
‑
1729(ladwig f,dahlke ri,st
ü
hrwohldt n等(2015)植物硫代因子(psk)通过质膜上的响应模块调节拟南芥的生长,质膜包括环核苷酸门控通道17,h
+
‑
atp酶和bak1。植物细胞27,1718
‑
1729)。
17.lv,q.,zhong,y.,wang,y.,et al(2014)spx4 negatively regulates phosphate signaling and homeostasis through its interaction with phr2 in rice.plant cell,26,1586
–
1597(lv q,zhong y,wang y,等(2014)spx4通过与水稻中的phr2相互作用来负调控磷酸信号和稳态。植物细胞26,1586
‑
1597)。
18.matsuzaki y,ogawa
‑
ohnishi m,mori a et al(2010)secreted peptide signals required for maintenance of root stem cell niche in arabidopsis.science 329,1065
‑
1067(matsuzaki y,ogawa
‑
ohnishi m,mori a(2009)分泌多肽信号对于维持拟南芥根干细胞是必需的。科学329,1065
‑
1067)。
19.meng f,xiang d,zhu j et al(2019)molecular mechanisms of root development in rice.rice12,1(meng f,xiang d,zhu j等(2019)水稻根发育的分子机制。水稻12,1)。
20.nakayama t,shinohara h,tanaka m et al(2017)a peptide hormone required for casparian strip diffusion barrier formation in arabidopsis roots.science 355,284
‑
286(nakayama t,shinohara h,tanaka m等(2017)拟南芥根中凯氏带扩散屏障的形成所必需的一种多肽激素。科学355,284
‑
286)。
21.orman
‑
ligeza b,parizot b,gantet pp et al(2013)post
‑
embryonic root organogenesis in cereals:branching out from model plants.trends plant sci.18,459
‑
467(orman
‑
ligeza b,parizot b,gantet pp等(2013)谷物的胚后根器官发生:从模型植物中分支出来。植物科学进展18,459
‑
467)。
22.rebouillat j,dievart a,verdeil jl et al(2009)molecular genetics of rice root development.rice 2,15
‑
34(rebouillat j,dievart a,verdeil jl等(2009)水稻根发育分子遗传学。水稻2,15
‑
34)。
23.rodriguez
‑
villalon a,gujas b,kang yh et al(2014)molecular genetic framework for protophloem formation.proc.natl.acad.sci.u.s.a.111,11551
‑
11556(rodriguez
‑
villalon a,gujas b,kang yh等(2014)初生韧皮部形成的分子遗传框架。美国科学院院刊111,11551
‑
11556)。
24.rodriguez
‑
villalon a,gujas b,van wijk r et al(2015)primary root protophloem differentiation requires balanced phosphatidylinositol
‑
4,5
‑
biphosphate levels and systemically affects root branching.development 142,1437
‑
1446(rodriguez
‑
villalon a,gujas b,van wijk r等(2015)初生根初生韧皮部的分化需要磷脂酰肌醇
‑
4,5
‑
双磷酸的水平与系统地影响根的分支之间的平衡。发育142,1437
‑
1446)。
25.stahl y,wink rh,ingram gc et al(2009)a signaling module controlling the stem cell niche in arabidopsis root meristems.curr.biol.19,909
‑
914(stahl y,wink rh,ingram gc等(2009)控制拟南芥根分生组织中干细胞龛的信号传导模块。现代生物学19,909
‑
914)。
26.wang wj,li cy,and li ms(2019)construction of an expression vector of gpc
‑
3ctl epitope.journal of southern medical university,29,1548
‑
1550.(wang wj,li cy,和li ms(2019)gpc
‑
3ctl表位的表达载体的构建。南方医科大学学报29,1548
‑
1550)。
27.whitford r,fernandez a,de groodt r et al(2008)plant cle peptides from two distinct functional classes synergistically induce division of vascular cells.proc.natl.acad.sci.u.s.a.105,18625
‑
18630(whitford r,fernandez a,de groodt等(2008)来自两个不同功能类别的植物cle肽协同诱导维管束细胞分裂。美国科学院院刊105,18625
‑
18630)。
28.whitford r,fernandez a,tejos r et al.(2012)golven secretory peptides regulate auxin carrier turnover during plant gravitropic responses.dev.cell.22,678
‑
685(whitford r,fernandez a,tejos r等(2012)golven分泌肽在植物重力响应过程中调控植物生长素载体的转化。发育细胞22,678
‑
685)。
技术实现要素:
29.本发明要解决的技术问题是提供一种调控植物根发育相关多肽及其编码基因和应用。
30.为了解决上述技术问题,本发明提供一种调控植物根发育多肽的用途:用于处理植物,所述处理后植物的根长度变短或者变长;
31.所述多肽为以下任一:
32.氨基酸序列如seq id no:1(序列表no:1)所示;
33.seq id no:1所示所示氨基酸序列组成的多肽经过一个或几个氨基酸残基的取代和/或缺失和/或添加且与植物根发育相关的由其衍生的多肽。
34.作为本发明的调控植物根发育多肽的用途的改进:
35.多肽的前体蛋白的氨基酸序列如seq id no:2所示;
36.或者,将seq id no:2所示的蛋白质经过一个或几个氨基酸残基的取代和/或缺失和/或添加且与植物发育相关的由其衍生的蛋白质;
37.本发明提供另一种调控植物根发育基因的用途:用于构建转基因植物,所述转基因植物的根长度变短或者变长;
38.所述基因为以下任一:
39.基因编码区的核苷酸序列如seq id no:3所示;
40.或者,将seq id no:3所示的基因经过一个或几个核苷酸的取代和/或缺失和/或添加且与植物发育相关的由其衍生的基因。
41.作为本发明的调控植物根发育基因的用途的改进:
42.所述植物为水稻。
43.作为本发明基因用途的改进:
44.使用不同浓度的多肽处理植物,得到长度变短或者变长的植物;
45.作为本发明基因用途的进一步改进:
46.将重组表达载体ⅰ导入目的植物中,得到长度变短的转基因植物;
47.将seq id no:3所示dna分子插入质粒pcambia1300的多克隆位点得到的重组表达载体ⅰ—ospep1过表达载体。
48.作为本发明基因用途的进一步改进:
49.将重组表达载体ⅱ导入目的植物中,得到长度变短的转基因植物;
50.将seq id no:3所示基因dna片段通过正向与反向连接到过渡载体pbssk
‑
in后插入质粒pcambia1300得到的重组表达载体
ⅱ‑‑‑
ospep1抑制表达载体。
51.本发明技术方案具体如下:
52.本发明提供的多肽(pep1),其前体蛋白,以及编码基因来自粳稻秀水134(oryza sativa l.ssp.japonica cv.xiushui134),是如下(a)或(b)的多肽,其前体蛋白,或者编码基因,是如下(a),(b),(c),(d),(e)或(f)的多肽,蛋白,或者编码基因:
53.(a)由序列表1所示氨基酸序列组成的多肽;
54.(b)将序列表1所示氨基酸序列组成的多肽经过一个或几个氨基酸残基的取代和/或缺失和/或添加且与植物根发育相关的由其衍生的多肽;
55.(c)由序列表中序列2所示的氨基酸序列组成的蛋白质;
56.(d)将序列表中序列2的蛋白质经过一个或几个氨基酸残基的取代和/或缺失和/或添加且与植物发育相关的由其衍生的蛋白质;
57.(e)由序列表中序列3所示的核苷酸序列组成的基因;
58.(f)将序列表中序列3的基因经过一个或几个核苷酸的取代和/或缺失和/或添加且与植物发育相关的由其衍生的基因;
59.所述植物发育体现在植株根长性状上。
60.为了使(a)中的pep1便于纯化,可在由序列表中序列1所示的氨基酸基酸序列组成的蛋白质的氨基末端或羧基末端连接上包括但不限于如表1所示的标签。
61.表1、标签的序列。
[0062][0063]
上述(a)中的pep1可人工合成,也可先合成其编码基因,再进行生物表达得到。上
述(a)中的pep1的编码基因可通过将序列表中序列3所示的dna序列中缺失一个或几个氨基酸残基的密码子,和/或进行一个或几个碱基对的错义突变,和/或在其5'端和/或3'端连上表1所示的标签的编码序列得到。
[0064]
所述蛋白的编码基因也属于本发明的保护范围。
[0065]
所述蛋白的编码基因(ospep1)可为如下1)或2)或3)或4)的dna分子:
[0066]
1)、其编码序列是序列表中序列3所示的dna分子,即基因的编码区的核苷酸序列如序列3所示;
[0067]
2)、在严格条件下与1)限定的dna序列杂交且编码相同功能蛋白质的dna分子;
[0068]
3)、与1)或2)限定的dna序列具有90%以上同源性,且编码相同功能蛋白质的dna分子。
[0069]
含有所述基因或其反义基因的重组表达载体、表达盒、转基因细胞系或重组菌均属于本发明的保护范围。
[0070]
可用现有的植物表达载体构建含有ospep1基因的重组表达载体。
[0071]
所述植物表达载体包括但不限于如双元农杆菌载体和可用于植物微弹轰击的载体等。所述植物表达载体还可包含外源基因的3'端非翻译区域,即包含聚腺苷酸信号和任何其它参与mrna加工或基因表达的dna片段。所述聚腺苷酸信号可引导聚腺苷酸加入到mrna前体的3'端,如包括但不限于农杆菌冠瘿瘤诱导(ti)质粒基因(如胭脂合成酶nos基因)、植物基因(如大豆贮藏蛋白基因)3'端转录的非翻译区均具有类似功能。
[0072]
使用ospep1构建重组植物表达载体时,在其转录起始核苷酸前可加上任何一种增强型启动子或组成型启动子,包括但不限于如花椰菜花叶病毒(camv)35s启动子、玉米的泛素启动子(ubiquitin),它们可单独使用或与其它植物启动子结合使用;此外,使用本发明的基因构建植物表达载体时,还可使用增强子,包括翻译增强子或转录增强子,这些增强子区域可以是atg起始密码子或邻接区域起始密码子等,但必需与编码序列的阅读框相同,以保证整个序列的正确翻译。所述翻译控制信号和起始密码子的来源是广泛的,可以是天然的,也可以是合成的。翻译起始区域可以来白转录起始区域或结构基因。
[0073]
为了便于对转基因植物细胞或植物进行鉴定及筛选,可对所用植物表达载体进行加工,如加入包括但不限于可在植物中表达的编码可产生颜色变化的酶或发光化合物的基因(gus基因、荧光素酶基因等)、具有抗性的抗生素标记物(庆大霉素标记物、卡那霉素标记物等)或是抗化学试剂标记基因(如抗除草剂基因)等。从转基因植物的安全性考虑,可不加任何选择性标记基因,直接以逆境筛选转化植株。
[0074]
所述重组表达载体具体可为如下(i)或(ii):
[0075]
(i)将序列表的序列3所示dna分子插入质粒pcambia1300
‑
的多克隆位点得到的含有上述基因的重组表达载体;
[0076]
(ii)将序列表的序列3所示基因dna片段通过正向与反向连接到过渡载体pbssk
‑
in后插入质粒pcambia1300得到的重组表达载体;
[0077]
(i)或(ii)中的所述质粒pcambia1300与pbssk
‑
in都是改造得到的(已公开)。
[0078]
本发明还保护一种培育转基因植物的方法,是将所述基因或基因的片段通过正反向连接到过渡载体pbssk
‑
in后导入目的植物中,所述转基因植物为与目的植物相比根长度改变的转基因植物。
[0079]
利用任何一种可以引导外源基因在植物中表达的载体,将本发明所提供的ospep1基因或基因的片段通过正反向连接到过渡载体pbssk
‑
in后导入植物细胞,可获得根长改变的转基因细胞系及转基因植株。携带有ospep1基因或其部分基因正反向连接的表达载体可通过使用ti质粒、ri质粒、植物病毒载体、直接dna转化、显微注射、电导、农杆菌介导等常规生物学方法转化植物细胞或组织,并将转化的植物组织培育成植株。被转化的植物宿主可为禾本科植物,如水稻(如秀水134)。
[0080]
当培育根长大于目的植物的转基因植物时;所述方法是将(i)所述重组表达载体导入目的植物中,得到根变长的转基因植物。当培育根长小于目的植物的转基因植物时;所述方法是将(ii)所述重组表达载体导入目的植物中,得到根变短的转基因植物。
[0081]
本发明发现了一个新的水稻根分泌多肽pep1及其编码基因ospep1,并获得了含有该编码基因或该基因的部分片段通过正向与反向连接到过渡载体pbssk
‑
in的重组表达载体,用重组载体转化目的植物,可以得到根长改变的转基因植物。因此ospep1可以作为一种潜在的分子育种工具,通过改良植物的根长来提高植物产量。
[0082]
综上所述,本发明分离、鉴定了一个控制水稻根生长的多肽pep1,并确定了其编码基因ospep1(loc_os11g09560)以及前体蛋白ospep1。即,本发明分离鉴定了一个调控植物根发育的多肽pep1及其编码基因ospep1。外源施加pep1处理植物,可抑制植物的根发育。并获得了含有该编码基因或该基因部分dna的重组表达载体,用重组表达载体转化的植物,可以得到根生长发育改变的转基因植物。因此该多肽可作植物生长调节剂,其编码基因以及前体蛋白可以作为一个潜在的分子育种靶运用于作物的改良,通过调控作物根生长发育来提高作物产量。
附图说明
[0083]
下面结合附图对本发明的具体实施方式作进一步详细说明。
[0084]
图1为实施例1中基因ospep1(loc_os11g09560)编码一个含有五个氨基酸(sdfdr)的蛋白;
[0085]
a为基因ospep1编码蛋白的氨基酸序列,5个氨基酸残基的多肽pep1用下划线标出;
[0086]
b为lc
‑
ms分析野生型水稻植株根系分泌多肽物质;
[0087]
c为lc
‑
ms/ms鉴定得到的滞留时间为12.25分钟的野生型水稻植株根系分泌多肽物质ser
‑
asp
‑
pro
‑
asp
‑
arg(pep1);
[0088]
d为lc
‑
ms分析loc_os11g09560过量表达转基因水稻植株根系分泌多肽物质;
[0089]
e为lc
‑
ms/ms鉴定得到的滞留时间为12.26分钟的loc_os11g09560过量表达转基因水稻植株根系分泌多肽物质ser
‑
asp
‑
pro
‑
asp
‑
arg(pep1)。
[0090]
图2为实施例1中根分泌多肽pep1的功能分析;
[0091]
a为不同pep1浓度处理7天后野生型植株的表型,标尺为5厘米;
[0092]
b为不同pep1浓度处理7天后野生型植株主根长度统计;误差用
±
sd表示(测量样本数量≥15);不同的字母表示0.01水平的显著性差异(单因素方差分析,lsd方法);
[0093]
c为野生型植株未使用pep1(
‑
pep1)处理的根尖伸长区(左上)与分生区(左下)或者使用10
‑6m pep1处理(+pep1)2天后的根尖伸长区(右上)与分生区(右下)的纵切表型,标
尺为100微米;
[0094]
d为c图中的分生区长度的统计结果;误差用
±
sd表示(测量样本数量≥15)。***p<0.001(t检验);
[0095]
e为c图中伸长区细胞长度的统计结果。误差用
±
sd表示(测量样本数量≥15)。***p<0.001(t检验)。
[0096]
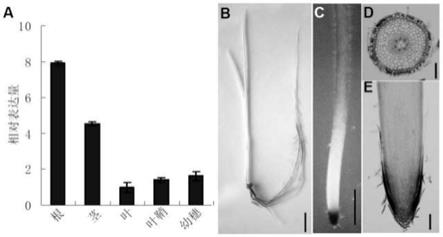
图3为实施例2中基因ospep1的表达谱;
[0097]
a为qrt
‑
pcr检测基因ospep1在水稻根、茎、叶、以及幼穗中的表达量,根、茎、叶、叶鞘样品取自7天苗龄水稻苗;
[0098]
b为7天苗龄的proospep1::gus转基因植株的gus染色结果,标尺为1厘米;
[0099]
c为2天苗龄的proospep1::gus转基因植株主根的gus染色,标尺为0.1厘米;
[0100]
d为c图中主根伸长区的横切gus染色图,标尺为100μm;
[0101]
e为c图中主根分生区区的纵切gus染色图。标尺为100μm。
[0102]
图4为实施例2中ospep1过表达转基因植株的表型分析;
[0103]
a为7天苗龄的wt与ospep1过表达猪基因株系oe1、oe2和oe3植株表型(标尺为5厘米);
[0104]
b为a图中相应株系的根长统计,误差用sd用表示(统计的个体数目大于30),***p<0.001(t检验);
[0105]
c为qrt
‑
pcr检测a图中相应植株中基因ospep1的表达量,误差用
±
sd表示(三次生物学重复);
[0106]
d为野生型wt与ospep1过量表达转基因植株oe2在10
‑6m pep1浓度处理2天的根尖伸长区(上)与分生区(下)与的纵切表型,标尺为100微米;
[0107]
e为d图中的根尖分生区长度的统计结果,误差用
±
sd表示(测量样本数量≥15)。不同的字母表示0.01水平的显著性差异(单因素方差分析,lsd方法);
[0108]
f为d图中伸长区细胞长度的统计结果,误差用
±
sd表示(测量样本数量≥15);不同的字母表示0.01水平的显著性差异(单因素方差分析,lsd方法)。
[0109]
图5为实施例2中ospep1抑制表达转基因植株的表型分析;
[0110]
a为7天苗龄的wt与ospep1过表达猪基因株系ri1、ri2和ri3植株表型(标尺为5厘米);
[0111]
b为a图中相应株系的根长统计,误差用sd用表示(统计的个体数目大于30),***p<0.001(t检验);
[0112]
c为qrt
‑
pcr检测a图中相应植株中基因ospep1的表达量,误差用
±
sd表示(三次生物学重复);
[0113]
d为野生型wt与ospep1过量表达转基因植株ri2在10
‑6m pep1浓度处理2天的根尖伸长区(上)与分生区(下)与的纵切表型,标尺为100微米;
[0114]
e为d图中的根尖分生区长度的统计结果,误差用
±
sd表示(测量样本数量≥15),不同的字母表示0.01水平的显著性差异(单因素方差分析,lsd方法);
[0115]
f为d图中伸长区细胞长度的统计结果。误差用
±
sd表示(测量样本数量≥15),不同的字母表示0.01水平的显著性差异(单因素方差分析,lsd方法)。
具体实施方式
[0116]
下面结合具体实施例对本发明进行进一步描述,但本发明的保护范围并不仅限于此:
[0117]
水培培养基的成分如下
[0118][0119][0120]
以下实施例中的基因表达量检测结果,如无特殊说明,均是以野生型植株秀水134的目的基因表达量为1,其它植株的目的基因表达量与野生型植株的目的基因表达量进行比较。
[0121]
实施例1、水稻多肽pep1的获得及其功能研究
[0122]
一、水稻多肽pep1及其编码基因的获得
[0123]
1、水稻根部分泌多肽的获得:
[0124]
选取30粒左右饱满的野生型水稻(秀水134)种子,用0.5%稀硝酸进行破休眠处理16
‑
22小时后,用自来水清洗2
‑
3次,加适量自来水浸泡种子于37℃的培养箱中催芽约两天至露白。在这期间每天早晚各换水一次。最后将露白的种子播于浮在营养液(水培培养基)上的尼龙网纱上,并置于人工气候室中培养。人工气候室的培养条件:光照为14小时,平均昼夜温度为30℃/22℃,光照强度保持在200μmol/m2s1,湿度为60%。培养10天后,收集培养基用于后续根分泌物质的浓缩、提取以及沉淀。具体方法为:首先使用旋转蒸发仪将上一步
获得的培养液(500ml)浓缩20倍。然后加入含有1%nem(n
‑
ethylmorpholine,n
‑
乙基吗啉)的20ml的氯酚室温振荡1分钟后,10000g离心10分钟,收集有机相,加入20倍体积丙酮室温过夜沉淀。然后10000g离心10分钟,收集沉淀,使用丙酮清洗3
‑
4次,再使用真空干燥至粉末。最后将粉末送往公司(中科新生命)使用液相色谱串联质谱(lp
‑
ms/ms)方法鉴定得到234个水稻根分泌多肽。
[0125]
2、水稻分泌型多肽编码候选基因的获得。
[0126]
之前的研究结果表明,拟南芥中一些小信号多肽(psk,psy1,clv3/cle)编码基因的产物大都为长度在70
‑
110氨基酸,且不富含半胱氨酸的蛋白质。所以本发明推测如果水稻中的某些基因编码的蛋白具这些类特点,那么该基因有可能是类似多肽的候选编码基因。基于这种猜测,本发明从水稻基因组注释数据库(http://rice.plantbiology.msu.edu/index.shtml,2017年3月)中一共下载得到了66343个蛋白编码基因,然后利用microsoft word 2003与excel 2003得到了12678个长度在50
‑
150氨基酸的蛋白编码基因。分泌型的多肽在其n端有一段信号肽序列,本发明使用hmm网页中的signalp 4.1服务器筛选得到704个n末端具有信号肽蛋白编码基因(p≥0.75)。最后本发明使用excel 2003去除了含有6或者更多半胱氨酸的蛋白编码基因,得到416个潜在的水稻多肽编码候选基因。
[0127]
3、水稻根分泌多肽pep1及其编码基因的确定。
[0128]
通过比对上述方法1获得的234个根分泌多肽和方法2获得的416个假想的水稻多肽编码基因,本发明发现得到了一个新的多肽(ser
‑
asp
‑
pro
‑
asp
‑
arg)以及确定了其编码基因(loc_os11g09560)(图1a),为了进一步地确认loc_os11g09560是该多肽的编码基因,本发明使用lp
‑
ms/ms检测了该基因过表达转基因植株根系的分泌物分,结果发现,与野生型的根系分泌物质中的该多肽的峰值相比,该过量表达转基因植株的根系分泌物质中该多肽峰值明显增强(图1b
‑
e)。这些结果表明,基因loc_os11g09560确实是该多肽的编码基因,此后将该多肽(ser
‑
asp
‑
pro
‑
asp
‑
arg)命名为pep1,其编码基因(loc_os11g09560)命名为ospep1。
[0129]
二、水稻多肽pep1的功能研究
[0130]
本发明使用不同浓度人工合成的pep1处理水稻幼苗(浓度如图2a所述,处理方式为播种后开始处理,处理时间为7天),结果发现外源施加pep1可以显著抑制水稻主根的伸长(图2a和b)。为了明确pep1抑制水稻根伸长的细胞学基础,本发明观察了这些水稻根尖的切片结构,结果发现pep1处理后,水稻根尖的分生区长度与伸长区细胞的长度显著缩短,但是其静止中心区域没有显著变化(根尖的分生区切片所示,如图2c
‑
e)。
[0131]
实施例2、水稻多肽pep1编码基因ospep1的表达谱研究
[0132]
一、qrt
‑
pcr检测基因ospep1在水稻不同组织的表达
[0133]
以野生型秀水134水稻为材料,在正常营养液(水培培养基)中培养7天,取其根、茎、叶及叶鞘,然后待植株将要抽穗时候,取其幼穗。所有样品于液氮中速冻并研磨,分别抽提总rna并进行逆转录获得相应的cdna。用qrt
‑
pcr方法检测ospep1在各组织中的表达。结果表明,ospep1基因在本发明所检测的不同组织中都有表达,在根中表达量较高(图3a)。检测引物序列如下:
[0134]
5'
‑
ggcgtggatgacgggagact
‑
3';
[0135]
5'
‑
tacatcctcattcctcgttg
‑
3',
[0136]
其反应体系与程序如下
[0137]2×
master:2.5μl
[0138]
cdna模板:0.1μl
[0139]
primer
‑
f(10μm):0.1μl
[0140]
primer
‑
r(10μm):0.1μl
[0141]
h2o:2.2μl
[0142]
total:5μl;
[0143]
pcr程序如下:
[0144]
起始:95℃1分钟
[0145]
扩增:95℃10秒
[0146]
58℃10秒
[0147]
72℃20秒45循环
[0148]
溶解曲线:95℃5秒
[0149]
65℃1分钟
[0150]
97℃降温处理,直到65℃
[0151]
冷却:40℃30秒;
[0152]
二、gus染色检测ospep1在水稻不同组织的表达
[0153]
提取秀水134水稻的dna,以此dna为模板进行pcr扩增制备基因ospep1启动子前2kb核苷酸序列。pcr扩增的引物如下:
[0154]
5'
‑
gcatgcctgcaggtcgacgtttctcagctacgcccctg
‑
3';
[0155]
5'
‑
ccatggtaccgtggatccccggagcgcagccgtcgtct
‑
3',
[0156]
将获得pcr产物利用重组克隆的方法插入到本实验室改造的载体pbi101.3
‑
gusplus的sali和bamhi酶切位点之间(lv et al.,2014),得到proospep1::gus载体。载体经过测序检验正确。将构建的过表达载体转入农杆菌eha105,用于转化野生型植株,参照常规步骤,具体如下:
[0157]
(1)取培养好的菌液500μl于1.5ml离心管中,室温,4000rmp,离心2分钟,去上清。用含200μmol/l乙酰丁香酮的30ml aam感菌液制成悬浮液,菌液终浓度od600为0.01;将长到一定大小(约为1立方厘米)的80~120个水稻愈伤组织挑出,放入农杆菌悬浮液,在水平摇床上摇晃5分钟;
[0158]
(2)将愈伤组织取出,置于无菌的滤纸上沥干30到40分钟;
[0159]
(3)将愈伤组织置于有一张无菌滤纸的共培养基上,25℃暗培养3天;
[0160]
(4)上述的愈伤组织取出,再用无菌水清洗5到6次,其间需不停的振荡。用含300mg/l羧苄青霉素钠(carb)的无菌水清洗2遍,每次在水平摇床上摇晃30分钟。最后置于无菌滤纸上沥干2小时;
[0161]
(5)将晾干的愈伤转入含300mg/l羧苄青霉素钠和相应筛选压力的选择培养基上进行第一轮选择,28℃,光照培养14天;
[0162]
(6)将长有抗性愈伤的初始愈伤转到含300mg/l羧苄青霉素钠和相应筛选压力的培养基上进行第二轮选择,28℃,光照培养,直到颗粒性的抗性愈伤组织长出(约14天左
右);
[0163]
(7)挑取从不同愈伤来的颜色鲜黄的抗性愈伤3到5颗,移入装有分化培养基的塑料广口瓶中,用封口膜封好,放入恒温(25℃)培养室中(光周期:16小时光照),等待分化成苗(约40天);
[0164]
(8)待苗长至3厘米左右,用剪刀从苗基部剪去老根和愈伤组织,放入生根培养基中壮苗(约1周)。将根部和茎叶分化得较完好的苗从试管挑出(苗长至试管顶部,就要及时开盖),打开封口膜,加入适量蒸馏水或无菌水(防止培养基长菌),炼苗2到3天,然后洗去琼脂,移栽到温室的水培条件中生长。利用抗赤霉素基因的引物检测转基因植物,引物序列如下:
[0165]
5'
‑
atgaaaaagcctgaactcacc
‑
3';
[0166]
5'
‑
ctattcctttgccctcggacg
‑
3',
[0167]
在得到的t2代转移基因水稻中,选择代表性株系(gus染色阳性的转基因植株)进行gus染色研究ospep1在水稻不同组织中的表达情况。结果表明基因ospep1主要在水稻根部表达,尤其是根尖的根冠区域、以及分生区和成熟区的外表皮(图3b
‑
e)。
[0168]
实施例3、水稻多肽pep1编码基因ospep1的功能研究
[0169]
一、ospep1过表达重组载体的构建
[0170]
提取秀水134水稻的mrna并逆转录为cdna,以此cdna为模板进行pcr扩增制备ospep1序列(seq id no:3所示dna)。pcr扩增的引物如下:
[0171]
5'
‑
acgggggacgagctcatgggagagaaggagcggag
‑
3';
[0172]
5'
‑
gactctagaggatcccaactgatgtttacatcctca
‑
3',
[0173]
将获得pcr产物利用重组克隆的方法插入到本实验室改造的载体pcambia1300(lv et al.,2014)的saci与psti酶切位点之间,得到ospep1过表达载体。ospep1过表达载体经过测序检验正确。
[0174]
二、ospep1过表达水稻的获得
[0175]
将上述步骤一构建的ospep1过表达载体转入农杆菌eha105,用于转化水稻秀水134,得到32株阳性转基因植株,具体步骤等同于实施例2的步骤二。
[0176]
在得到的t2代转移基因水稻中,挑选三个代表性转基因株系(ospep1过量表达的独立转基因植系)(oe1,oe2,oe3)进行表型分析。结果表明,与野生型相比,转基因株系的株高其根长度显著缩短(见图4a和b)。用实时定量pcr的方法对水稻秀水134与ospep1过表达转基因植株中(oe1,oe2,oe3)中内源ospep1相对表达量进行分析(引物为:ggcgtggatgacgggagact;tacatcctcattcctcgttg),结果表明,ospep1的过表达转基因株系的主根长度与ospep1表达量正相关(见图4c)。此外本发明观察了这些ospep1过表达转基因水稻根尖的切片结构,与对照植株秀水134(wt)相比,ospep1过表达转基因水稻根尖的分生区长度与伸长区细胞的长度显著缩短,外源的pep处理不能恢复ospep1过表达转基因水稻根尖缺陷表型至野生型水平(见图4d
‑
f)。
[0177]
三、ospep1抑制表达重组载体的构建
[0178]
提取水稻秀水134的mrna并逆转录为cdna,以此长cdna为模板进行pcr扩增制备ospep1的部分dna序列:
[0179]
actcgggagagagggagcgcagattgtgcgtgaggaaacggatgggaagcagcgatttcgatcgagggg
cgcgatttgggggcgtggatgacgggagactgggagaggggacgaagcggtgtgaggagatggtgggagcgatttggg
[0180]
pcr扩增的引物如下:
[0181]
5'
‑
actcgggagagagggagcgc
‑
3';
[0182]
5'
‑
cccaaatcgctcccaccatc
‑
3',
[0183]
将克隆到的pcr产物与t载体(购自takara公司)连接,连接好的质粒分别用psti、bamh i以及pst i、sal i酶切得到两片段;两片段一同连入pbssk
‑
in载体(wang et al.2019),分两步进行。pbssk
‑
in先用pst i、bamh i酶切,连上一个片段后,再nsi i、sal i酶切,连另一片段。最后用sac i、sal i将两片段以及intron切下,连入相同酶切的植物双元载体pcambia1300中(lv et al.,2014),得到ospep1抑制表达载体。ospep1抑制表达载体经过测序检验正确。
[0184]
四、ospep1抑制表达水稻的获得
[0185]
将上述步骤三构建的ospep1抑制表达载体转入农杆菌eha105,用于转化水稻秀水134,得到53株阳性转基因植株。具体步骤等同于实施例2的步骤二。
[0186]
在得到的t2代转移基因水稻中,挑选三个代表性株系(ospep1抑制表达的独立转基因植株)(ri1,ri2,ri3)进行表型分析。结果表明,与野生型相比其根长度显著缩短(见图5a和b)。用实时定量pcr的方法对秀水134与ospep1抑制表达转基因植株(ri1,ri2,ri3)中内源ospep1相对表达量进行分析(引物为:ggcgtggatgacgggagact;tacatcctcattcctcgttg),结果表明,基因ospep1的抑制表达转基因株系的主根长度与ospep1表达量正相关(见图5c);此外本发明观察了这些ospep1抑制表达转基因水稻根尖的切片结构,与对照秀水134(wt)相比,ospep1抑制表达转基因水稻根尖的分生区长度与伸长区细胞的长度显著缩短,外源的pep处理可以恢复ospep1抑制表达转基因水稻根尖缺陷表型至野生型水平(见图5d
‑
f)。
[0187]
综合以上的结果,本发明将通过lc
‑
ms/ms鉴定得到的234个水稻根系分泌多肽和416个水稻分泌型多肽候选编码基因的对比研究,并结合遗传学实验,找到了一个调控水稻主根发育的根分泌多肽pep1(ser
‑
asp
‑
pro
‑
asp
‑
arg)并确定了其编码基因ospep1(loc_os11g09560)。本发明的生理实验结果表明外源施加pep1抑制水稻根伸长,本发明的遗传学实验表明,过量表达或抑制表达均会抑制水稻根伸长。这些结果表明,水稻根分泌多肽可能作为一个信号分子在水稻根发育中起着重要作用,可以通过调控ospep1的表达量控制水稻根的生长发育。
[0188]
最后,还需要注意的是,以上列举的仅是本发明的若干个具体实施例。显然,本发明不限于以上实施例,还可以有许多变形。本领域的技术人员能从本发明公开的内容直接导出或联想到的所有变形,均应认为是本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1