具有光交联活性的氨基酸类化合物的制备方法与流程
本发明涉及生物医药技术领域,更具体地说,涉及一种具有光交联活性的氨基酸类化合物的制备方法。
背景技术:
光交联剂是化学生物学研究的重要工具,通常包含光反应活性基团和响应基团,在紫外光照射下,光反应活性基团活化介导蛋白质和配体之间的不可逆连接。小分子连接光交联剂可以促进与蛋白质靶标的不可逆结合,若小分子是氨基酸类分子,便可促进氨基酸小分子与特定位点的蛋白质靶标结合,生成化学稳定的、交联的蛋白质-探针复合物,可用于各种下游的生物活性测试和分析。
氨基酸是构成蛋白质的基本单位,基于氨基酸类分子与蛋白质结构的特殊构效关系,制备具有光交联活性的氨基酸类化合物对该领域的研究具有重要的应用意义,可以有效地探究氨基酸类化合物在细胞内蛋白质上的作用情况。现阶段研究人员已经发现并能够制备出多种含有光交联活性的基团,例如,苯基叠氮类、二苯甲酮类等,但是这些基团的光交联活性并不高,且目前对于具有光交联活性的氨基酸类化合物的研究尚少,其制备过程繁琐,还需要额外合成一些中间试剂。
技术实现要素:
本发明的目的在于提供一种具有光交联活性的氨基酸类化合物的制备方法,该制备过程简单,不需要再额外合成一些中间试剂,得到的氨基酸类化合物中含有光交联活性较高的双吖丙啶基团,使得氨基酸类化合物在后续研究使用中灵敏度更高。本发明提供的诸多技术方案中的优选技术方案所能产生的诸多技术效果详见下文阐述。
为实现上述目的,本发明提供了以下技术方案:
本发明提供了一种具有光交联活性的氨基酸类化合物的制备方法,包括以下步骤:
1)在丙酮-干冰浴的条件下,将1-羟基-3-酮庚炔和无水氨混合,35-40℃的温度下搅拌反应5h,冷却混合溶液,并在30min内向混合溶液内加入羟胺-o-磺酸的无水甲醇溶液,回流搅拌1h,蒸发剩余的氨,过滤得到悬浮液,蒸发溶剂,再用二氯甲烷溶解、三乙胺处理,缓慢加入碘的二氯甲烷溶液,直到出现持久的橙棕色,经过柱层析法分离得到化合物1;
2)冰浴条件下,将咪唑和三苯基膦加入二氯甲烷中充分搅拌溶解,再向混合物中加入碘以及化合物1的二氯甲烷溶液,在避光条件下搅拌反应4h,通过na2s2o3的水溶液淬灭,再用乙酸乙酯萃取水层,得到的混合有机层用饱和食盐水洗涤、无水硫酸钠干燥,真空去除溶剂得到化合物2;
3)将化合物2溶解在dmf(n,n-二甲基甲酰胺)中,向溶液中添加氰化钾,加热条件下搅拌反应,然后用水淬灭、乙酸乙酯萃取,得到的有机层用饱和食盐水洗涤、无水硫酸钠干燥,除去溶剂后采用柱层析法分离得到化合物3;
4)向氢氧化钠的水溶液中加入化合物3,再加入乙醚,分离水层并用盐酸的水溶液酸化,将水层用乙酸乙酯萃取、无水硫酸钠干燥,过滤、减压蒸发,得到化合物4;
5)将化合物4和n-羟基丁二酰亚胺溶于dmf中,在氮气氛围、冰浴条件下加入1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐,逐渐升至室温条件反应,经洗涤分离得到化合物5;
6)体积比为1:1的水和1,4-二氧六环混合作为溶剂,加入碳酸氢钠使溶剂呈碱性,将化合物5和组氨酸或异亮氨酸加入碱性溶剂中反应生成(3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酰基)组氨酸(x1)或(3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酰基)异亮氨酸(x2);在乙腈溶剂中加入三乙胺处理,再加入化合物5和半胱氨酸反应生成(3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酰基)半胱氨酸(x3)。
优选地,步骤4)中化合物3和氢氧化钠的水溶液混合后需要进行回流,回流的时间为7h。
优选地,步骤5)中所述洗涤分离的具体步骤为:向反应所得的混合物中加入乙酸乙酯溶解,依次经过水洗、盐酸水溶液洗、饱和食盐水洗,再用无水硫酸钠干燥后旋除溶剂,采用柱层析法分离得到化合物5。
本发明提供的技术方案中,具有光交联活性的氨基酸类化合物的制备方法包括将1-羟基-3-酮庚炔和无水氨混合,加入羟胺-o-磺酸反应,得到的产物经三乙胺处理,再加入碘反应生成化合物1,将咪唑和三苯基膦加入二氯甲烷中,再与碘和化合物1的二氯甲烷溶液反应生成化合物2,化合物2与氰化钾反应生成化合物3,将氢氧化钠的水溶液加入化合物3中得到化合物4,化合物4和n-羟基丁二酰亚胺溶于dmf中,加入1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐反应生成化合物5,化合物5分别与组氨酸或异亮氨酸或半胱氨酸反应得到相应的具有光交联活性的氨基酸类化合物。如此设置,该制备过程较为简单,不需要再额外合成一些中间试剂,得到的氨基酸类化合物中含有光交联活性较高的双吖丙啶基团,使得氨基酸类化合物在后续研究使用中灵敏度更高。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
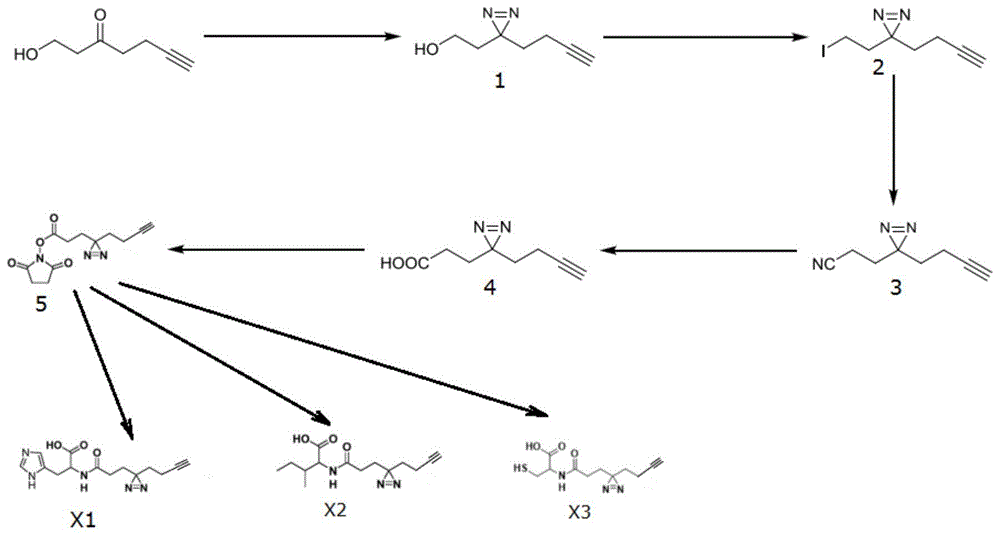
图1是本发明实施例中具有光交联活性的氨基酸类化合物的合成路线图。
图中:化合物1为3-(3-丁炔-1-基)-3h-双吖丙啶-3-乙醇,化合物2为3-(3-炔-1-丁基)-3-(2-碘乙基)-3h-双吖丙啶,化合物3为3-(3-(丁-3-炔基)-3h-双吖丙啶-3-基)丙腈,化合物4为3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酸,化合物5为2,5-二氧代吡咯烷-1-基3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酸酯,x1为(3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酰基)组氨酸,x2为(3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酰基)异亮氨酸,x3为(3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酰基)半胱氨酸。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚,下面将对本发明的技术方案进行详细的描述。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所得到的所有其它实施方式,都属于本发明所保护的范围。
本具体实施方式的目的在于提供一种具有光交联活性的氨基酸类化合物的制备方法,解决目前其制备过程繁琐,还需要额外合成一些中间试剂,含有的光亲和基团的光交联活性不高的问题。
以下,参照附图对实施例进行说明。此外,下面所示的实施例不对权利要求所记载的发明内容起任何限定作用。另外,下面实施例所表示的构成的全部内容不限于作为权利要求所记载的发明的解决方案所必需的。
请参阅图1,具有光交联活性的氨基酸类化合物的制备方法包括以下的制备步骤。
将1-羟基-3-酮庚炔(2.52g,20mmol)加入圆底烧瓶中,在丙酮-干冰浴的条件下,将无水氨(20ml)冷凝在圆底烧瓶里。将混合物置于35-40℃的温度下搅拌5小时,用干冰冷却该溶液,并在30分钟内加入羟胺-o-磺酸(2.59g,23mmol)的无水甲醇(6ml)溶液,将混合物在35℃下回流搅拌1小时。然后,蒸发一夜以除去剩余的氨气,过滤得到悬浮液,过滤时用甲醇多次洗涤滤饼。将悬浮液真空蒸发掉溶剂,再将其溶解在二氯甲烷(10ml)中并用三乙胺(3.5ml)处理,一边搅拌一边缓慢加入碘(3.7g,28.8mmol)的二氯甲烷(10ml)溶液,直到出现持久的橙棕色。将得到的混合物在硅胶柱上通过二氯甲烷-己烷(体积比为4:1)洗脱液进行色谱分离,再用含5%乙醚的二氯甲烷相继续洗涤硅胶柱后,得到化合物1。其中,1-羟基-3-酮庚炔的结构式为:
在冰浴条件下(0℃),将咪唑(359mg,5.27mmol)和三苯基膦(509mg,1.94mmol)充分溶解在二氯甲烷(15ml)中,向混合溶剂中加入碘(536mg,2.11mmol)。将溶液搅拌5分钟,缓慢加入化合物1(242mg,1.76mmol)的二氯甲烷溶液。将混合物在避光条件下搅拌反应4小时。加入na2s2o3的水溶液(10ml)淬灭,用乙酸乙酯对水层进行萃取。得到的混合有机层用饱和食盐水洗涤,并用无水硫酸钠干燥。真空除去溶剂得到粗产物。粗产物经快速柱色谱法纯化(己烷∶乙酸乙酯=20∶1),得到呈无色油状的化合物2。化合物2为3-(3-炔-1-丁基)-3-(2-碘乙基)-3h-双吖丙啶,其结构式为:
将化合物2(1.23g,5.0mmol)溶解在dmf中,向溶液中添加氰化钾(0.64g,0.01mol),将混合物在70℃的条件下搅拌反应10小时,然后用水淬灭。随后,将混合物用乙酸乙酯萃取出有机相,用饱和食盐水洗涤,并用无水硫酸钠干燥。去除溶剂得到粗产物,将粗产物通过快速柱色谱法纯化(己烷∶乙酸乙酯=5∶1),得到呈无色油状的化合物3。化合物3为3-(3-(丁-3-炔基)-3h-双吖丙啶-3-基)丙腈,其结构式为:
将naoh溶液(10ml,10%)加入到化合物3(0.88g,6.0mmol)中,化合物3与氢氧化钠混合后需要对混合物进行回流,回流时间设定为7小时,然后向混合物中加入乙醚。分离得到水层,并用盐酸溶液酸化。将水层用乙酸乙酯萃取,得到的混合有机相通过无水硫酸钠干燥,过滤,并在减压下蒸干,得到化合物4。化合物4为3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酸,其结构式为:
将化合物4和n-羟基丁二酰亚胺溶于dmf中,在氮气作保护气、冰浴条件(0℃)下,向混合物中加入1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐,逐渐升至室温条件进行反应,反应时间为16小时。经过洗涤分离过程得到化合物5。化合物5为2,5-二氧代吡咯烷-1-基3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酸酯,其结构式为:
将组氨酸溶解在水和1,4-二氧六环的混合溶剂中,水和1,4-二氧六环的体积比为1:1,加入碳酸氢钠使溶液呈碱性,然后加入化合物5,室温条件下搅拌反应至少12小时。真空旋除溶剂,过滤,用甲醇冲洗多次。收集滤液,真空旋干,用高效液相色谱法纯化,得到(3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酰基)组氨酸,其结构式为:
将异亮氨酸溶解在水和1,4-二氧六环的混合溶剂中,水和1,4-二氧六环的体积比为1:1,加入碳酸氢钠使溶液呈碱性,然后加入化合物5,室温条件下搅拌反应至少12小时。真空旋除溶剂,用水和乙酸乙酯萃取,保留有机相,旋干溶剂,用高效液相色谱法纯化,得到(3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酰基)异亮氨酸,其结构式为:
将半胱氨酸、三乙胺和化合物5溶解在5ml乙腈溶剂中,室温条件下搅拌反应至少12小时。真空旋除溶剂,过滤,用甲醇冲洗多次。收集滤液,真空旋干,用高效液相色谱法纯化,得到(3-(3-(丁-3-炔-1-基)-3h-双吖丙啶-3-基)丙酰基)半胱氨酸,其结构式为:
经过以上制备过程得到了三种具有光交联活性的氨基酸类化合物,当然,将氨基酸变成与本发明中具有相同的反应基团的其它氨基酸,可以得到另外的氨基酸类化合物。该制备方法简单,不需要额外合成其它的中间反应物,得到的具有光交联活性的氨基酸类化合物均含有双吖丙啶基团,其光反应活性更高。
可以理解的是,上述各实施例中相同或相似部分可以相互参考,在一些实施例中未详细说明的内容可以参见其他实施例中相同或相似的内容。本发明提供的多个方案包含本身的基本方案,相互独立,并不互相制约,但是其也可以在不冲突的情况下相互结合,达到多个效果共同实现。
以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到变化或替换,都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应以所述权利要求的保护范围为准。
- 还没有人留言评论。精彩留言会获得点赞!