一类抗真菌化合物、其制备方法及其用途与流程
1.本公开属于医药领域,具体涉及一种抗真菌化合物及其制备方法。
背景技术:
2.抗真菌治疗方案的开发已经是当今社会面临的一个持续性挑战。目前用于治疗真菌感染的可利用的药物包括两性霉素b,一种与真菌膜甾醇相互作用的大环内酯多烯:氟胞嘧啶,一种与真菌蛋白和dna生物合成相互作用的氟嘧啶,和多种抑制真菌膜
‑
甾醇生物合成的唑类抗真菌药物(例如酮康唑,伊曲康唑,和氟康唑)(alexander et al.,drugs,1997,54,657.)。即使两性霉素b具有宽的活性范围并被视为抗真菌疗法的“金标准”,其应用因输注相关的反应和肾毒性而受到限制(warnock,j.antimicrob.chemother.,1998,41,95.)。由于耐药性微生物的发展及其窄的活性谱,氟胞嘧啶的使用也受到限制。唑类抗真菌药的广泛使用正引起假丝酵母菌种(candida spp)的临床耐药株的出现。
3.抗真菌药物比其它抗细菌药物的发展较缓慢,其主要原因是许多真菌具有真核细胞的某些特征,给选择用药带来了困难,随着免疫功能受损害的病人中真菌感染发病率和死亡率的不断增加,寻找一种敏感,广谱,安全的抗真菌药物显得极为迫切,近年来,随着分子真菌学的发展,发现了一系列作用机制新颖的抗真菌化合物。
4.烯丙胺(allyamine)是从杂环螺旋萘(heteroeylic spironaphene)衍生而来的一类高效,低毒抗真菌药。其抗真菌谱包括曲霉菌,念珠菌和申克孢子菌丝。自从发现萘替芬具有较高的广谱抗真菌活性以来,该类化合物的抗真菌研究进展很快,至今已发展为一类具有高度活性的抗真菌新型结构化合物(bioorganic&medicinal chemistry 2000,8,2487
‑
2499.;j.med.chem.1993,36,2810
‑
2816.;j.med.chem.1995,38,1831
‑
1836.)。烯丙胺类抗真菌药物通过抑制真菌的角鲨烯环氧化酶(se)阻断真菌细胞麦角固醇的合成,进而破坏其细胞膜的生成。真菌与哺乳动物中se的氨基酸序列的差异可能是烯丙胺类抗真菌药物选择性的分子基础。此类药物结构的侧链部分和se的亲脂性位点结合,致se构象改变而失活,由此引起角鲨烯的积累和麦角固醇的缺乏。由于角鲨烯积累使细胞膜渗透性增加,导致真菌细胞死亡。目前已上市或正研究的化合物有萘替芬,特比萘芬,布替萘芬,托萘酯等,其中萘替芬,特比萘芬,布替萘芬已在国内外相继上市,随着该类化合物研究的不断深入,将会有更多的烯丙胺衍生物抗真菌药不断用于临床。
技术实现要素:
5.本公开提供一种式(i)所示的化合物或其可药用盐,或其异构体,
[0006][0007]
其中,
[0008]
r1和r2各自独立地选自烷基,羟基,氰基,烷氧基,
‑
nr
a1
r
a2
,环烷基,杂环基,芳基,杂芳基,所述的烷基,烷氧基,环烷基,杂环基,芳基,杂芳基任选被选自氘,卤素,氰基,羟基,氨基,硝基,烷基,卤代烷基,烷氧基,
‑
nr
a1
r
a2
,
‑
cor
a2
,
‑
sr
a1
,
‑
so2r
a2
,
‑
so2or
a2
,
‑
so2nr
a1
r
a2
,环烷基,杂环基,芳基,杂芳基的取代基取代;或者
[0009]
r1和r2与其共同连接的氮原子形成如式(a)所示的杂环,其中式(a)所示的杂
[0010][0011]
环为包含至少一个氮原子的杂环基,杂芳基,螺杂环,桥杂环;所述的杂环基,杂芳基,螺杂环,桥杂环任选被选自卤素,羟基,氨基,氰基,硝基,
‑
sh,烷基,卤代烷基,烷氧基,
‑
nr
a1
r
a2
的取代基取代;
[0012]
环a选自芳基,杂芳基;
[0013]
每个a任选选被r
a
取代,r
a
独立地选自卤素,氰基,羟基,叠氮基,硝基,烷基,烷氧基,氧代,=nr
a1
,
‑
sr
a1
,
‑
or
a1
,
‑
nr
a1
r
a2
,
‑
cor
a2
,
‑
conr
a1
r
a2
,
‑
coor
a2
,
‑
n(r
a2
)
‑
c(o)r
a2
,
‑
n(r
a2
)
‑
c(o)or
a2
,
‑
n(r
a2
)
‑
c(o)
‑
nr
a2
r
a2
,
‑
n(r
a2
)
‑
so2r
a2
,
‑
so2r
a2
,
‑
so2or
a2
,
‑
so2nr
a1
r
a2
,
‑
o
‑
so2‑
nr
a1
r
a2
,
‑
o(co)
‑
nr
a1
r
a2
,环烷基,杂环基,芳基,杂芳基;
[0014]
其中r
a
的烷基、环烷基,杂环基,芳基,杂芳基,各自独立地任选被选自卤素,氰基,羟基,烷基,环烷基,杂环基,芳基,杂芳基,卤代烷基,烷氧基和羟烷基的基团取代;
[0015]
其中a和r
a
的杂芳基包含独立地选自s,n和o的杂原子;
[0016]
r3和r4各自独立地选自氢,氘,卤素,烷基,卤代烷基,烷氧基,环烷基;
[0017]
v选自其中r5选自烷基,烷氧基,环烷基,杂环基,硅烷基,亚烯基,亚炔基;或者
[0018]
v选自所述r6选自芳基,杂芳基,所述芳基,杂芳基任选被任选自卤素,氰基,羟基,叠氮基,氨基,硝基,烷基,卤代烷基,烷氧基,
‑
nr
a1
r
a2
的取代基取代;
[0019]
r
a1
选自氢,烷基,卤代烷基,羟烷基,
‑
—ch2‑
coor
a2
,和
‑
c(o)
‑
nh2,
[0020]
r
a2
选自氢,烷基,羟烷基,环烷基,杂环基,芳基和杂芳基;其中所述烷基,卤代烷基,羟烷基,环烷基,杂环基,芳基,杂芳基独立地被任选自卤素,氰基,羟基,
‑
coor
a3
,烷基,卤代烷基,羟烷基和烷氧基的取代基取代;
[0021]
其中r
a3
选自氢,烷基和卤代烷基;
[0022]
n选自1,2,3,4,5,6,7,8,9,10。
[0023]
可选的实施方案中,r1和r2各自独立地选自c1‑6烷基,羟基,氰基,c1‑6烷氧基,
‑
nr
a1
r
a2
,c3‑8环烷基,3
‑
8元杂环基,c6‑
10
芳基,5
‑
10元杂芳基,所述的c1‑6烷基,c1‑6烷氧基,c3‑8环烷基,3
‑
8元杂环基,c6‑
10
芳基,5
‑
10元杂芳基任选被1,2,3,4,5,6个选自氘,卤素,氰基,羟基,氨基,硝基,c1‑6烷基,c1‑6卤代烷基,c1‑6烷氧基,
‑
nr
a1
r
a2
,
‑
cor
a2
,
‑
sr
a1
,
‑
so2r
a2
,
‑
so2or
a2
,
‑
so2nr
a1
r
a2
,c3‑8环烷基,3
‑
8元杂环基,c6‑
10
芳基,5
‑
10元杂芳基的取代基取代;或者
[0024]
r1和r2与其共同连接的氮原子形成如式(a)所示的杂环,其中式(a)所示的杂
[0025][0026]
环为包含至少一个氮原子的3
‑
12元杂环基,5
‑
10元杂芳基,3
‑
12元的螺杂环,3
‑
12元的桥杂环;所述的3
‑
12元杂环基,5
‑
10元杂芳基,3
‑
12元的螺杂环,3
‑
12元的桥杂环任选被1
‑
3个选自卤素,羟基,氨基,氰基,硝基,
‑
sh,c1‑6烷基,c1‑6卤代烷基,c1‑6烷氧基,
‑
nr
a1
r
a2
的取代基取代;
[0027]
环a选自c6‑
10
芳基,5
‑
10元杂芳基;
[0028]
每个a任选被0,1,2,3,4,5,6,7个r
a
取代,r
a
独立地选自卤素,氰基,羟基,叠氮基,硝基,c1‑6烷基,c1‑6烷氧基,氧代,=nr
a1
,
‑
sr
a1
,
‑
or
a1
,
‑
nr
a1
r
a2
,
‑
cor
a2
,
‑
conr
a1
r
a2
,
‑
coor
a2
,
‑
n(r
a2
)
‑
c(o)r
a2
,
‑
n(r
a2
)
‑
c(o)or
a2
,
‑
n(r
a2
)
‑
c(o)
‑
nr
a2
r
a2
,
‑
n(r
a2
)
‑
so2r
a2
,
‑
so2r
a2
,
‑
so2or
a2
,
‑
so2nr
a1
r
a2
,
‑
o
‑
so2‑
nr
a1
r
a2
,
‑
o(co)
‑
nr
a1
r
a2
,c3‑8环烷基,3
‑
8元杂环基,c6‑
10
芳基,5
‑
10元杂芳基;
[0029]
其中r
a
的c1‑6烷基、c3‑8环烷基,3
‑
8元杂环基,c6‑
10
芳基,5
‑
10元杂芳基,各自独立地任选被1,2,3个选自卤素,氰基,羟基,c1‑6烷基,c3‑8环烷基,3
‑
8元杂环基,c6‑
10
芳基,5
‑
10元杂芳基,c1‑6卤代烷基,c1‑6烷氧基和羟烷基的基团取代;
[0030]
其中a和r
a
的杂芳基包含独立地选自1,2,3,4,5个选自s,n和o的杂原子;
[0031]
r3和r4各自独立地选自氢,氘,卤素,c1‑6烷基,c1‑6卤代烷基,c1‑6烷氧基,c3‑8环烷基;
[0032]
v选自其中r5选自c1‑6烷基,c1‑6烷氧基,c3‑8环烷基,3
‑
8元杂环基,c1‑6硅烷基,c1‑6亚烯基,c1‑6亚炔基;或者
[0033]
v选自所述r6选自c6‑
10
芳基,5
‑
10元杂芳基,所述c6‑
10
芳基,5
‑
10元杂芳基任选被1,2,3,4,5,6个任选自卤素,氰基,羟基,叠氮基,氨基,硝基,c1‑6烷基,c1‑6卤代烷基,c1‑6烷氧基,
‑
nr
a1
r
a2
的取代基取代;
[0034]
r
a1
选自氢,c1‑6烷基,c1‑6卤代烷基,羟烷基,
‑
ch2‑
coor
a2
,和
‑
c(o)
‑
nh2,
[0035]
r
a2
选自氢,c1‑6烷基,羟烷基,c 3
‑8环烷基,3
‑
8元杂环基,c6‑
10
芳基和5
‑
10元杂芳基;其中所述c1‑6烷基,羟烷基,c 3
‑8环烷基,3
‑
8元杂环基,c6‑
10
芳基和5
‑
10元杂芳基独立地任选被1,2,3个选自卤素,氰基,羟基,
‑
coor
a3
,c1‑6烷基,c1‑6卤代烷基,羟烷基,和c1‑6烷氧基的取代基取代;
[0036]
其中r
a3
选自氢,c1‑6烷基和c1‑6卤代烷基。
[0037]
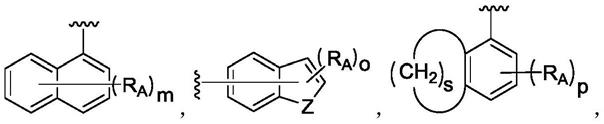
可选的实施方案中环a选自
[0038]
优选
[0039]
m选自0,1,2,3,4,5,6,7;
[0040]
o选自0,1,2,3,4,5,6;
[0041]
p选自0,1,2,3;
[0042]
s选自3,4,5;
[0043]
z选自o,s或nh;
[0044]
其中r
a
如上所述。
[0045]
可选的实施方案中,其中环a选自
[0046][0047]
m选自0,1,2,3,4,5,6,7;
[0048]
o选自0,1,2,3,4,5;
[0049]
p选自0,1,2,3;
[0050]
其中r
a
如上所述;
[0051]
r1,r2各自独立的选自c1‑6烷基,c3‑
12
环烷基,所述c1‑6烷基,c3‑
12
环烷基被芳基,杂芳基取代;所述芳基优选c6‑
10
芳基,所述杂芳基优选5
‑
10元杂芳基。
[0052]
可选的实施方案中,v为其中r5选自c1‑6烷基,c3‑8环烷基。
[0053]
可选的实施方案中,v为其中r5选自c1‑6烷基。
[0054]
可选的实施方案中可选的实施方案中,r3和r4各自独立地选自氢。
[0055]
可选的实施方案中,n为1。
[0056]
可选的实施方案中,环a选自
[0057][0058]
其中r3和r4各自独立地选自氢;
[0059]
v为其中r5选自c1‑6烷基,c3‑8环烷基,优选c1‑6烷基;
[0060]
其中n为1;
[0061]
m选自0,1,2,3,4;
[0062]
r
a
如上所述。
[0063]
可选的实施方案中,环a选自
[0064][0065]
可选的实施方案中,所述的式i所示的化合物或其可药用盐,或其异构体,其为式(ii)所示化合物,
[0066][0067]
其中r1,r2各自独立的选自c1‑6烷基,c3‑
12
环烷基,所述c1‑6烷基,c3‑
12
环烷基被芳基,杂芳基取代;所述芳基优选c6‑
10
芳基,所述杂芳基优选5
‑
10元杂芳基;或者
[0068]
r1,r2与其连接的氮原子组成3
‑
12元杂环基;
[0069]
r5选自c1‑6烷基。
[0070]
可选的实施方案中,式(ii)所示化合物,其中r1,r2各自独立的选自c1‑6烷基,c3‑
12
环烷基;或者
[0071]
r1,r2与其连接的氮原子组成3
‑
12元杂环基;
[0072]
r5选自c1‑6烷基。
[0073]
可选的实施方案中,式(ii)所示化合物,其中r1,r2各自独立的选自甲基,乙基,正丙基,异丙基,正丁基,叔丁基,环丙基,环丁基,环戊基,环己基;或者
[0074]
r1,r2与其连接的原子组成三元杂环基,四元杂环基,五元杂环基,六元杂环基,七元杂环基,八元杂环基;
[0075]
r5为叔丁基。
[0076]
可选的实施方案中,式(ii)所示化合物r1为甲基或环丙基,r2为甲基,乙基,正丙基,异丙基,正丁基,叔丁基,环丙基,环丁基,环戊基,环己基;或者r1,r2与其连接的原子组成三元杂环基,四元杂环基,五元杂环基,六元杂环基;
[0077]
r5为叔丁基。
[0078]
本公开提供的式(i)所示的化合物或其可药用盐,或其异构体,其为
[0079][0080]
本公开中,可药用盐的酸根部分具体可选自卤素,甲酸根,醋酸根,苯甲酸根,苯磺酸根,樟脑磺酸根,柠檬酸根,乙二磺酸根,富马酸根,葡庚糖酸根,葡糖酸根,葡萄糖醛酸根,羟乙磺酸根,乳酸根,乳糖醛酸根,十二烷基硫酸根,苹果酸根,马来酸根,甲磺酸根,萘甲酸根,萘磺酸根,硝酸根,硬脂酸根,油酸根,草酸根,双羟萘酸根,磷酸根,磷酸氢根,磷酸二氢根,聚半乳糖醛酸根,琥珀酸根,硫酸根,磺基水杨酸根,酒石酸根,对甲苯磺酸根,三氟乙酸根,优选自卤素,醋酸根,甲磺酸根或对甲苯磺酸根,最优选氯离子,溴离子,碘离子,醋酸根,甲磺酸根,苯磺酸根或对甲苯磺酸根。
[0081]
本公开中,根据实际可药用盐的酸根部分离子价数,一价酸根部分可选择与一个式(i)所示的化合物成盐,二价酸根可选自与一个式(i)所示的化合物成盐或者与两个式(i)所示的化合物成盐,三价酸根可选自与一个式(i)所示的化合物成盐,或者与两个式(i)所示的化合物成盐,或者与三个式(i)所示的化合物成盐。
[0082]
可选的实施方案中,所述式(i)所示的化合物或其可药用盐,或其异构体,其为
[0083][0084]
本公开给出的任何式或结构也意图代表化合物的未标记形式以及同位素标记形式。同位素标记的化合物具有本文给出的式所描述的结构,不同之处在于一个或多个原子被具有选定原子质量或质量数的原子取代。可掺入本公开化合物中的同位素的实例包括氢,碳,氮,氧,磷,氟和氯的同位素,包括但不限于2h(氘,d),3h(tri),
11
c,
13
c,
14
c,
15
n,
18
f,
31
p,
32
p,
35
s,
36
cl和
125
i。本公开内容的各种同位素标记的化合物,例如其中掺入有放射性同
位素如3h,
13
c和
14
c的那些,此类同位素标记的化合物可用于代谢研究,反应动力学研究,检测或成像技术。
[0085]
本公开提供一种之制备式(i)所示的化合物或其可药用盐,或其异构体的方法,
[0086][0087]
式(i
‑
a)所示化合物与r2‑
x1在溶剂中反应形成式(i
‑
b)所示化合物,式(i
‑
b)所示化合物经酸根交换得到式(i)所示的化合物,其中r2如上所定义,x1为可离去基团,x为可药用盐的酸根部分。
[0088]
本公开提供一种制备式(i)所示的化合物或其可药用盐,或其异构体的方法,
[0089][0090]
式(i
‑
f)所示化合物与式(i
‑
e)所示化合物在溶剂中反应形成式(i
‑
d)所示化合物,式(i
‑
d)所示化合物经酸根交换得到式(i)所示的化合物,其中q选自1,2,3,4,5,6,7,8,9,10,x1为可离去基团,x为可药用盐的酸根部分。
[0091]
本公开中所述的x1为可离去基团,具体可选基于磺酸基的离去基团,例如ots(对甲苯磺酸根),oms(甲磺酸根),otf(三氟甲磺酸根);或者卤素离子,具体可选自碘离子、氯离子或者溴离子。
[0092]
可选的实施方案中,制备式(i)所示的化合物或其可药用盐,或其异构体的方法,其中q选自1,2,3,4。
[0093]
可选的实施方案中,制备式(i)所示的化合物或其可药用盐,或其异构体的方法,其中药用盐的酸根部分优选氯离子,溴离子,碘离子,醋酸根,苯磺酸根,甲磺酸根或对甲苯磺酸根。
[0094]
本公开中提供的制备式(i)所示的化合物或其可药用盐,或其异构体的方法,所述溶剂选自甲苯、二氧六环、四氢呋喃、邻二甲苯、叔丁基醚、叔丁醇、叔戊醇、乙二醇二甲醚、乙二醇单甲醚、异丙醚、n,n
‑
二甲基乙酰胺、n,n
‑
二甲基甲酰胺、二甲基亚砜、n
‑
甲基吡咯烷酮、乙酸乙酯、乙酸异丙酯、乙酸丁酯、乙腈、异丙醇、乙醇、丙酮的至少一种溶剂中进行。
[0095]
可选的实施方案中,制备式(i)所示的化合物或其可药用盐,或其异构体的方法,所述反应溶剂为乙腈。
[0096]
本公开还提供了一种药物组合物,包括至少一种前述化合物或其可药用盐,或其异构体,以及药学上可接受的载体、稀释剂或赋形剂。
[0097]
在某些实施方式中,所述的药物组合物的单位剂量为0.001mg
‑
1000mg。
[0098]
在某些实施方式中,基于组合物的总重量,所述的药物组合物含有0.01%
‑
99.99%的前述化合物。
[0099]
在某些实施方式中,所述的药物组合物含有0.1%
‑
99.9%的前述化合物。
[0100]
在某些实施方式中,所述的药物组合物含有0.5%
‑
99.5%的前述化合物。
[0101]
在某些实施方式中,所述的药物组合物含有1%
‑
99%的前述化合物。
[0102]
在某些实施方式中,所述的药物组合物含有2%
‑
98%的前述化合物。
[0103]
在某些实施方式中,基于组合物的总重量,所述的药物组合物含有0.01%
‑
99.99%的药学上可接受的载体、稀释剂或赋形剂。
[0104]
在某些实施方式中,所述的药物组合物含有0.1%
‑
99.9%的药学上可接受的载体、稀释剂或赋形剂。
[0105]
在某些实施方式中,所述的药物组合物含有0.5%
‑
99.5%的药学上可接受的载体、稀释剂或赋形剂。
[0106]
在某些实施方式中,所述的药物组合物含有1%
‑
99%的药学上可接受的载体、稀释剂或赋形剂。
[0107]
在某些实施方式中,所述的药物组合物含有2%
‑
98%的药学上可接受的载体、稀释剂或赋形剂。
[0108]
本公开中还涉及式(i)所示的化合物或其可药用盐,或其异构体,或含有式i所示的化合物或其可药用盐,或其异构体的药物组合物在制备用于治疗真菌引起的疾病或感染的药物中的用途。
[0109]
本公开中所述真菌为皮肤癣菌,丝状真菌,双相真菌,暗色孢属真菌,毛癣菌,狗小孢子菌,絮状表皮癣菌,红色毛发癣菌,须癣毛癣菌,皮炎芽生菌,荚膜组织胞浆菌,申克孢子丝菌,白色念珠菌,近平滑念珠菌,卵圆糠秕孢子菌或酵母菌。
[0110]
本公开中所述的真菌引起的疾病选自手癣、足癣、体癣、股癣、花斑癣及皮肤念珠菌病。
[0111]
本公开提供一种治疗由真菌引起的疾病或感染的方法,给与患者有效量的式(i)所示的化合物或其可药用盐,或其异构体。
[0112]
除非有相反陈述,在说明书和权利要求书中使用的术语具有下述含义。
[0113]
术语“烷基”指饱和脂肪族烃基团,其为包含1至20个碳原子的直链或支链基团,优选含有1至12个碳原子的烷基。非限制性实例包括甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、仲丁基、正戊基、1,1
‑
二甲基丙基、1,2
‑
二甲基丙基、2,2
‑
二甲基丙基、1
‑
乙基丙基、2
‑
甲基丁基、3
‑
甲基丁基、正己基、1
‑
乙基
‑2‑
甲基丙基、1,1,2
‑
三甲基丙基、1,1
‑
二甲基丁基、1,2
‑
二甲基丁基、2,2
‑
二甲基丁基、1,3
‑
二甲基丁基、2
‑
乙基丁基、2
‑
甲基戊基、3
‑
甲基戊基、4
‑
甲基戊基、2,3
‑
二甲基丁基、正庚基、2
‑
甲基己基、3
‑
甲基己基、4
‑
甲基己基、5
‑
甲基己基、2,3
‑
二甲基戊基、2,4
‑
二甲基戊基、2,2
‑
二甲基戊基、3,3
‑
二甲基戊基、2
‑
乙基戊基、3
‑
乙基戊基、正辛基、2,3
‑
二甲基己基、2,4
‑
二甲基己基、2,5
‑
二甲基己基、2,2
‑
二甲基己基、3,3
‑
二甲基己基、4,4
‑
二甲基己基、2
‑
乙基己基、3
‑
乙基己基、4
‑
乙基己基、2
‑
甲基
‑2‑
乙基戊基、2
‑
甲基
‑3‑
乙基戊基、正壬基、2
‑
甲基
‑2‑
乙基己基、2
‑
甲基
‑3‑
乙基己基、2,2
‑
二乙基戊基、正癸基、3,3
‑
二乙基己基、2,2
‑
二乙基己基,及其各种支链异构体等。更优选的是含有1至6个碳原子的低级烷基,非限制性实施例包括甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、仲丁基、正戊基、1,1
‑
二甲基丙基、1,2
‑
二甲基丙基、2,2
‑
二甲基丙基、1
‑
乙基丙基、2
‑
甲基丁基、3
‑
甲基丁基、正己基、1
‑
乙基
‑2‑
甲基丙基、1,1,2
‑
三甲基丙基、1,1
‑
二甲基丁基、1,2
‑
二甲基丁基、2,2
‑
二甲基丁基、1,3
‑
二甲基丁基、2
‑
乙基丁基、2
‑
甲基戊基、3
‑
甲基戊基、4
‑
甲基戊基、2,3
‑
二甲基丁基等。烷基可以是取代的或非取代的,当被取代时,
取代基可以在任何可使用的连接点上被取代,所述取代基优选为一个或多个以下基团,其独立地选自烷基、烯基、炔基、烷氧基、烷硫基、烷基氨基、卤素、巯基、羟基、硝基、氰基、环烷基、杂环烷基、芳基、杂芳基、环烷氧基、杂环烷氧基、环烷硫基、杂环烷硫基、氧代基、羧基或羧酸酯基。
[0114]
术语“亚烷基”指饱和的直链或支链脂肪族烃基,其具有2个从母体烷的相同碳原子或两个不同的碳原子上除去两个氢原子所衍生的残基,其为包含1至20个碳原子的直链或支链基团,优选含有1至12个碳原子,更优选含有1至6个碳原子的亚烷基。亚烷基的非限制性实例包括但不限于亚甲基(
‑
ch2‑
)、1,1
‑
亚乙基(
‑
ch(ch3)
‑
)、1,2
‑
亚乙基(
‑
ch2ch2)
‑
、1,1
‑
亚丙基(
‑
ch(ch2ch3)
‑
)、1,2
‑
亚丙基(
‑
ch2ch(ch3)
‑
)、1,3
‑
亚丙基(
‑
ch2ch2ch2‑
)、1,4
‑
亚丁基(
‑
ch2ch2ch2ch2‑
)等。亚烷基可以是取代的或非取代的,当被取代时,取代基可以在任何可使用的连接点上被取代。
[0115]
术语“环烷基”指饱和或部分不饱和单环或多环环状烃取代基,环烷基环包含3至20个碳原子,优选包含3至12个碳原子,更优选包含3至6个碳原子。单环环烷基的非限制性实例包括环丙基、环丁基、环戊基、环戊烯基、环己基、环己烯基、环己二烯基、环庚基、环庚三烯基、环辛基等;多环环烷基包括螺环、稠环和桥环的环烷基。
[0116]
术语“螺环烷基”指5至20元的单环之间共用一个碳原子(称螺原子)的多环基团,其可以含有一个或多个双键,但没有一个环具有完全共轭的π电子系统。优选为6至14元,更优选为7至10元。根据环与环之间共用螺原子的数目将螺环烷基分为单螺环烷基、双螺环烷基或多螺环烷基,优选为单螺环烷基和双螺环烷基。更优选为4元/4元、4元/5元、4元/6元、5元/5元或5元/6元单螺环烷基。
[0117]
螺环烷基的非限制性实例包括:
[0118][0119]
术语“稠环烷基”指5至20元,系统中的每个环与体系中的其他环共享毗邻的一对碳原子的全碳多环基团,其中一个或多个环可以含有一个或多个双键,但没有一个环具有完全共轭的π电子系统。优选为6至14元,更优选为7至10元。根据组成环的数目可以分为双环、三环、四环或多环稠环烷基,优选为双环或三环,更优选为5元/5元或5元/6元双环烷基。稠环烷基的非限制性实例包括:
[0120][0121]
术语“桥环烷基”指5至20元,任意两个环共用两个不直接连接的碳原子的全碳多环基团,其可以含有一个或多个双键,但没有一个环具有完全共轭的π电子系统。优选为6至14元,更优选为7至10元。根据组成环的数目可以分为双环、三环、四环或多环桥环烷基,优选为双环、三环或四环,更有选为双环或三环。桥环烷基的非限制性实例包括:
[0122][0123]
所述环烷基环可以稠合于芳基、杂芳基或杂环烷基环上,其中与母体结构连接在一起的环为环烷基,非限制性实例包括茚满基、四氢萘基、苯并环庚烷基等。环烷基可以是任选取代的或非取代的,当被取代时,取代基优选为一个或多个以下基团,其独立地选自烷基、烯基、炔基、烷氧基、烷硫基、烷基氨基、卤素、巯基、羟基、硝基、氰基、环烷基、杂环烷基、芳基、杂芳基、环烷氧基、杂环烷氧基、环烷硫基、杂环烷硫基、氧代基、羧基或羧酸酯基。
[0124]
术语“杂环基”指饱和或部分不饱和单环或多环环状烃取代基,其包含3至20个环原子,其中一个或多个环原子为选自氮、氧或s(o)
m
(其中m是整数0至2)的杂原子,但不包括
‑
o
‑
o
‑
、
‑
o
‑
s
‑
或
‑
s
‑
s
‑
的环部分,其余环原子为碳。优选包含3至12个环原子,其中1~4个是杂原子;更优选包含3至6个环原子。单环杂环基的非限制性实例包括吡咯烷基、咪唑烷基、四氢呋喃基、四氢噻吩基、二氢咪唑基、二氢呋喃基、二氢吡唑基、二氢吡咯基、哌啶基、哌嗪基、吗啉基、硫代吗啉基、高哌嗪基等,优选哌啶基、吡咯烷基。多环杂环基包括螺环、稠环和桥环的杂环基。
[0125]
术语“螺杂环基”指5至20元的单环之间共用一个原子(称螺原子)的多环杂环基团,其中一个或多个环原子为选自氮、氧或s(o)
m
(其中m是整数0至2)的杂原子,其余环原子为碳。其可以含有一个或多个双键,但没有一个环具有完全共轭的π电子系统。优选为6至14元,更优选为7至10元。根据环与环之间共用螺原子的数目将螺杂环基分为单螺杂环基、双螺杂环基或多螺杂环基,优选为单螺杂环基和双螺杂环基。更优选为4元/4元、4元/5元、4元/6元、5元/5元或5元/6元单螺杂环基。螺杂环基的非限制性实例包括:
[0126][0127]
术语“稠杂环基”指5至20元,系统中的每个环与体系中的其他环共享毗邻的一对原子的多环杂环基团,一个或多个环可以含有一个或多个双键,但没有一个环具有完全共轭的π电子系统,其中一个或多个环原子为选自氮、氧或s(o)
m
(其中m是整数0至2)的杂原子,其余环原子为碳。优选为6至14元,更优选为7至10元。根据组成环的数目可以分为双环、三环、四环或多环稠杂环基,优选为双环或三环,更优选为5元/5元或5元/6元双环稠杂环基。稠杂环基的非限制性实例包括:
[0128][0129]
术语“桥杂环基”指5至14元,任意两个环共用两个不直接连接的原子的多环杂环基团,其可以含有一个或多个双键,但没有一个环具有完全共轭的π电子系统,其中一个或多个环原子为选自氮、氧或s(o)
m
(其中m是整数0至2)的杂原子,其余环原子为碳。优选为6至14元,更优选为7至10元。根据组成环的数目可以分为双环、三环、四环或多环桥杂环基,优选为双环、三环或四环,更有选为双环或三环。桥杂环基的非限制性实例包括:
[0130][0131]
所述杂环基环可以稠合于芳基、杂芳基或环烷基环上,其中与母体结构连接在一起的环为杂环基,其非限制性实例包括:
[0132]
等。
[0133]
杂环基可以是任选取代的或非取代的,当被取代时,取代基优选为一个或多个以下基团,其独立地选自烷基、烯基、炔基、烷氧基、烷硫基、烷基氨基、卤素、巯基、羟基、硝基、氰基、环烷基、杂环烷基、芳基、杂芳基、环烷氧基、杂环烷氧基、环烷硫基、杂环烷硫基、氧代基、羧基或羧酸酯基。
[0134]
术语“芳基”指具有共轭的π电子体系的6至14元全碳单环或稠合多环(也就是共享毗邻碳原子对的环)基团,优选为6至10元,例如苯基和萘基。所述芳基环可以稠合于杂芳基、杂环基或环烷基环上,其中与母体结构连接在一起的环为芳基环,其非限制性实例包括:
[0135][0136]
芳基可以是取代的或非取代的,当被取代时,取代基优选为一个或多个以下基团,其独立地选自烷基、烯基、炔基、烷氧基、烷硫基、烷基氨基、卤素、巯基、羟基、硝基、氰基、环烷基、杂环烷基、芳基、杂芳基、环烷氧基、杂环烷氧基、环烷硫基、杂环烷硫基、羧基或羧酸酯基,优选苯基。
[0137]
术语“稠环芳基”可以是含有8
‑
14个环原子由两个或两个以上环状结构彼此共用两个相邻的原子连接起来形成的不饱和的具有芳香性的稠环结构,环原子优选8
‑
12个。例如包括全部不饱和稠环芳基,例如萘、菲等,还包括部分饱和稠环芳基,例如苯并3
‑
8元饱和单环环烷基、苯并3
‑
8元部分饱和单环环烷基,具体实例如2,3
‑
二氢
‑
1h
‑
茚基、ih
‑
茚基、1,2,3,4
‑
四氢萘基、1,4
‑
二氢萘基等。
[0138]
术语“杂芳基”指包含1至4个杂原子、5至14个环原子的杂芳族体系,其中杂原子选自氧、硫和氮。杂芳基优选为5至12元,例如咪唑基、呋喃基、噻吩基、噻唑基、吡唑基、噁唑基、吡咯基、四唑基、吡啶基、嘧啶基、噻二唑、吡嗪基等,优选为咪唑基、吡唑基、嘧啶基或噻唑基;更优选为吡唑基或噻唑基。所述杂芳基环可以稠合于芳基、杂环基或环烷基环上,其中与母体结构连接在一起的环为杂芳基环,其非限制性实例包括:
[0139][0140]
杂芳基可以是任选取代的或非取代的,当被取代时,取代基优选为一个或多个以下基团,其独立地选自烷基、烯基、炔基、烷氧基、烷硫基、烷基氨基、卤素、巯基、羟基、硝基、氰基、环烷基、杂环烷基、芳基、杂芳基、环烷氧基、杂环烷氧基、环烷硫基、杂环烷硫基、羧基或羧酸酯基。
[0141]
术语“稠杂芳基”可以是含有5
‑
14个环原子(其中至少含有一个杂原子)由两个或两个以上环状结构彼此共用两个相邻的原子连接起来形成的不饱和的具有芳香性的稠环结构,同时包括碳原子、氮原子和硫原子可以被氧代,优选"5
‑
12元稠杂芳基"、"7
‑
12元稠杂
芳基"、"9
‑
12元稠杂芳基"等,例如苯并呋喃基、苯并异呋喃基、苯并噻吩基、吲哚基、异吲哚、苯并噁唑基、苯并咪唑基、吲唑基、苯并三唑基、喹啉基、2
‑
喹啉酮、4
‑
喹啉酮、1
‑
异喹啉酮、异喹啉基、吖啶基、菲啶基、苯并哒嗪基、酞嗪基、喹唑啉基、喹喔啉基、酚嗪基、喋啶基、嘌呤基、萘啶基、吩嗪、吩噻嗪等。
[0142]
稠杂芳基可以是任选取代的或非取代的,当被取代时,取代基优选为一个或多个以下基团,其独立地选自烷基、烯基、炔基、烷氧基、烷硫基、烷基氨基、卤素、巯基、羟基、硝基、氰基、环烷基、杂环烷基、芳基、杂芳基、环烷氧基、杂环烷氧基、环烷硫基、杂环烷硫基、羧基或羧酸酯基。
[0143]
术语“烷氧基”指
‑
o
‑
(烷基)和
‑
o
‑
(非取代的环烷基),其中烷基的定义如上所述。烷氧基的非限制性实例包括:甲氧基、乙氧基、丙氧基、丁氧基、环丙氧基、环丁氧基、环戊氧基、环己氧基。烷氧基可以是任选取代的或非取代的,当被取代时,取代基优选为一个或多个以下基团,其独立地选自烷基、烯基、炔基、烷氧基、烷硫基、烷基氨基、卤素、巯基、羟基、硝基、氰基、环烷基、杂环烷基、芳基、杂芳基、环烷氧基、杂环烷氧基、环烷硫基、杂环烷硫基、羧基或羧酸酯基。
[0144]
术语“烷硫基”指
‑
s
‑
(烷基)和
‑
s
‑
(非取代的环烷基),其中烷基的定义如上所述。烷硫基的非限制性实例包括:甲硫基、乙硫基、丙硫基、丁硫基、环丙硫基、环丁硫基、环戊硫基、环己硫基。烷硫基可以是任选取代的或非取代的,当被取代时,取代基优选为一个或多个以下基团,其独立地选自烷基、烯基、炔基、烷氧基、烷硫基、烷基氨基、卤素、巯基、羟基、硝基、氰基、环烷基、杂环烷基、芳基、杂芳基、环烷氧基、杂环烷氧基、环烷硫基、杂环烷硫基中的一个或多个取代基所取代。
[0145]
术语“羟烷基”指被羟基取代的烷基,其中烷基如上所定义。
[0146]
术语“卤代烷基”指被卤素取代的烷基,其中烷基如上所定义。
[0147]
术语“氘代烷基”指被氘原子取代的烷基,其中烷基如上所定义。
[0148]
术语“羟基”指
‑
oh基团。
[0149]
术语“氧基”指=o基团。例如,碳原子与氧原子通过双键连接,其中形成酮或醛基。
[0150]
术语“卤素”指氟、氯、溴或碘。
[0151]
术语“氨基”指
‑
nh2。
[0152]
术语“氰基”指
‑
cn。
[0153]
术语“硝基”指
‑
no2。
[0154]
术语“羧基”指
‑
c(o)oh。
[0155]
术语“醛基”指
‑
cho。
[0156]
术语“羧酸酯基”指
‑
c(o)o(烷基)或
‑
c(o)o(环烷基),其中烷基、环烷基如上所定义。
[0157]
术语“酰卤”指含有
‑
c(o)
‑
卤素的基团的化合物。
[0158]“任选”或“任选地”意味着随后所描述的事件或环境可以但不必发生,该说明包括该事件或环境发生或不发生的场合。例如,“任选被烷基取代的杂环基团”意味着烷基可以但不必须存在,该说明包括杂环基团被烷基取代的情形和杂环基团不被烷基取代的情形。
[0159]“取代的”指基团中的一个或多个氢原子,优选为最多5个,更优选为1~3个氢原子彼此独立地被相应数目的取代基取代。不言而喻,取代基仅处在它们的可能的化学位置,本
领域技术人员能够在不付出过多努力的情况下确定(通过实验或理论)可能或不可能的取代。例如,具有游离氢的氨基或羟基与具有不饱和(如烯属)键的碳原子结合时可能是不稳定的。
具体实施方式
[0160]
以下结合实施例进一步描述本公开所述的化合物,可药用盐的制备,但这些实施例并非限制本公开中的范围。
[0161]
本公开中实施例中未注明具体条件的实验方法,通常按照常规条件,或按照原料或商品制造厂商所建议的条件。未注明具体来源的试剂,为市场购买的常规试剂。
[0162]
化合物的结构是通过核磁共振(nmr)或/和质谱(ms)来确定的。nmr位移(δ)以10
‑6(ppm)的单位给出。nmr的测定是用bruker avance
‑
400核磁仪,测定溶剂为氘代二甲基亚砜(dmso
‑
d6)、氘代氯仿(cdcl3)、氘代甲醇(cd3od),内标为四甲基硅烷(tms)。
[0163]
ms的测定用agilent 1200/1290 dad
‑
6110/6120 quadrupole ms液质联用仪(生产商:agilent,ms型号:6110/6120 quadrupole ms)。
[0164]
高效液相色谱法(hplc)分析使用agilent hplc 1200dad、agilent hplc 1200vwd和waters hplc e2695
‑
2489高压液相色谱仪。
[0165]
实施例1
[0166]
(e)
‑
n,n,n,6,6
‑
四甲基
‑
n
‑
(萘
‑1‑
基甲基)庚
‑2‑
烯
‑4‑
炔基
‑1‑
碘化铵
[0167][0168]
冰水浴下,将1
‑
a(10g,34.4mmol)溶解到60ml乙腈中,接着加入碘甲烷(9.75g,68.8mmol),然后在室温下搅拌约18小时,抽滤,得到11.5g化合物1,纯度>99%,lcms(esi):306.1[m+]。
[0169]1hnmr(cdcl3,400mhz):8.63(d,j=8.8hz,1h),7.94
‑
7.84(m,3h),7.69(t,j=7.6hz,1h),7.55
‑
7.45(m,2h),6.41(d,j=15.6hz,1h),6.10
‑
6.02(m,1h),5.56(s,2h),4.84(d,j=7.6hz,2h),3.19(s,6h),1.22(s,9h)。
[0170]
实施例2
[0171]
(e)
‑
n,n,n,6,6
‑
四甲基
‑
n
‑
(萘
‑1‑
基甲基)庚
‑2‑
烯
‑4‑
炔基
‑1‑
对甲苯磺酸铵
[0172][0173]
冰水浴下,将1
‑
a(10g,34.4mmol)溶解到35ml乙腈中,接着加入对甲苯磺酸甲酯(8.36g,44.7mmol),然后在室温下搅拌约18小时,抽滤,得到10.2g化合物2,纯度>99%,lc
‑
ms(esi):306.1[m+]。
[0174]1hnmr(cdcl3,400mhz):8.49(d,j=7.2hz,1h);7.91
‑
7.77(m,5h);7.48
‑
7.39(m,3h);7.19(d,j=7.6hz,2h);6.23(d,j=15.6hz,1h);6.01
–
5.93(m,1h);5.40(s,2h);4.61(d,j=7.6hz,2h);3.08(s,6h);2.36(s,3h);1.21(s,9h)。
[0175]
实施例3
[0176]
(e)
‑
n,n,n,6,6
‑
四甲基
‑
n
‑
(萘
‑1‑
基甲基)庚
‑2‑
烯
‑4‑
炔基
‑1‑
醋酸铵
[0177][0178]
将化合物2(1.0g,2.09mmol)溶解到少量乙腈中,以6%的乙酸铵
‑
醋酸
‑
乙腈为流动相,经c18反相硅胶柱进行阴离子交换处理,收集所需淋洗液,浓缩干有机溶剂,水相冻干后得600mg产物,lc
‑
ms(esi):306.1[m
+
]。
[0179]1hnmr(cdcl3,400mhz):8.35(d,j=7.6hz,1h);7.95(d,j=7.6hz,1h);7.88(d,j=7.6hz,1h);7.77(d,j=6.8hz,1h);7.65
‑
7.61(m,1h);7.55
‑
7.50(m,2h);6.18(d,j=15.6hz,1h);6.09
–
6.02(m,1h);5.27(s,2h);4.44(d,j=6.8hz,2h);3.06(s,6h);2.05(s,3h);1.24(s,9h)。
[0180]
实施例4
[0181]
(e)
‑
n,n,n,6,6
‑
四甲基
‑
n
‑
(萘
‑1‑
基甲基)庚
‑2‑
烯
‑4‑
炔基
‑1‑
甲磺酸铵
[0182][0183]
室温下,将1
‑
a(1.0g,3.4mmol)溶解到10ml乙腈中,接着加入甲磺酸甲酯(0.75g,6.8mmol),然后升温至50℃,搅拌约18小时,将反应液浓缩,经c18反相柱纯化得到0.9g化合物4,纯度98.5%,lc
‑
ms(esi):306.1[m
+
]。
[0184]1hnmr(cdcl3,400mhz):8.47(d,j=8.4hz,1h);7.92(d,j=8.0hz,1h);7.88
‑
7.83(m,2h);7.69
‑
7.65(m,1h);7.55
‑
7.46(m,2h);6.30(d,j=15.2hz,1h);6.08
–
5.99(m,1h);5.33(s,2h);4.55(d,j=7.6hz,2h);3.08(s,6h);2.89(s,3h);1.22(s,9h)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1